Составить уравнение кальций с хлором
Реакция взаимодействия кальция и хлора.










Уравнение реакции взаимодействия кальция и хлора:
Кальций взаимодействует с хлором .
Реакция кальция и хлора протекает при условии: при температуре 200-400 °C.
В результате реакции происходит образование хлорида кальция .










- ← Реакция калия и хлора
- Реакция цинка с гидроксидом натрия →
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (105 893)
- Экономика Второй индустриализации России (101 447)
- Программа искусственного интеллекта ЭЛИС (22 637)
- Метан, получение, свойства, химические реакции (15 899)
- Мотор-колесо Дуюнова (15 110)
- Гидротаран – самодействующий энергонезависимый водяной насос (14 466)
- Природный газ, свойства, химический состав, добыча и применение (13 936)
- Крахмал, свойства, получение и применение (13 509)
- Прямоугольный треугольник, свойства, признаки и формулы (13 061)
- Целлюлоза, свойства, получение и применение (11 910)
- Пропилен (пропен), получение, свойства, химические реакции (11 652)
- Этилен (этен), получение, свойства, химические реакции (11 171)
- Бутан, получение, свойства, химические реакции (9 847)
- Оксид алюминия, свойства, получение, химические реакции (9 364)
- Оксид железа (III), свойства, получение, химические реакции (9 140)
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Кальций — элемент 4-го периода и ПА-группы Периодической системы, порядковый номер 20. Электронная формула атома [18Ar]4s 2 , степени окисления +2 и 0. Относится к щелочноземельным металлам. Имеет низкую электроотрицательность (1,04), проявляет металлические (основные) свойства. Образует (как катион) многочисленные соли и бинарные соединения. Многие соли кальция малорастворимы в воде. В природе — шестой по химической распространенности элемент (третий среди металлов), находится в связанном виде. Жизненно важный элемент для всех организмов.Недостаток кальция в почве восполняется внесением известковых удобрений (СаС03, СаО, цианамид кальция CaCN2 и др.). Кальций, катион кальция и его соединения окрашивают пламя газовой горелки в темно-оранжевый цвет (качественное обнаружение).
Серебристо-белый металл, мягкий, пластичный. Во влажном воздухе тускнеет и покрывается пленкой из СаО и Са(ОН)2.Весьма реакционноспособный; воспламеняется при нагревании на воздухе, реагирует с водородом, хлором, серой и графитом:

Восстанавливает другие металлы из их оксидов (промышленно важный метод — кальцийтермия):

Получение кальция в промышленности:

Кальций применяется для удаления примесей неметаллов из металлических сплавов, как компонент легких и антифрикционных сплавов, для выделения редких металлов из их оксидов.
Основный оксид. Техническое название негашёная известь. Белый, весьма гигроскопичный. Имеет ионное строение Ca 2+ O 2- . Тугоплавкий, термически устойчивый, летучий при прокаливании. Поглощает влагу и углекислый газ из воздуха. Энергично реагирует с водой (с высоким экзо-эффектом), образует сильно щелочной раствор (возможен осадок гидроксида), процесс называется гашение извести. Реагирует с кислотами, оксидами металлов и неметаллов. Применяется для синтеза других соединений кальция, в производстве Са(ОН)2, СаС2 и минеральных удобрений, как флюс в металлургии, катализатор в органическом синтезе, компонент вяжущих материалов в строительстве.
Уравнения важнейших реакций:

Получение СаО в промышленности — обжиг известняка (900-1200 °С):
СаСО3 = СаО + СО2
Уравнения важнейших реакций:

Получение Са(ОН)2 в промышленности — гашение извести СаО (см. выше).
Хлорид кальция, характеристика, свойства и получение, химические реакции.
Хлорид кальция – неорганическое вещество, имеет химическую формулу CaCl2.
Краткая характеристика хлорида кальция:
Хлорид кальция – неорганическое вещество белого цвета.
Химическая формула хлорида кальция CaCl2.
Хлорид кальция – неорганическое химическое соединение, соль соляной кислоты и кальция.
Хорошо растворяется в воде, метаноле, этаноле, пропаноле. Практически не растворим в ацетоне. Не растворим в жидком аммиаке.
Растворяясь в воде? выделяет значительное количество тепла. Водные растворы хлорида кальция замерзают при низких температурах (20%-ный – при −18,57 °C, 30%-ный – при −48 °C).
С водой хлорид кальция образует кристаллогидраты с общей формулой CaCl2·nH2O, где n может быть 1, 2, 4 или 6: гидрат хлорида кальция CaCl2·H2O, дигидрат хлорида кальция CaCl2·2H2O, тетрагидрат хлорида кальция CaCl2·4H2O, гексагидрат хлорида кальция CaCl2·6H2O.
Гексагидрат CaCl2·6H2O устойчив до 29,8 °C, при более высоких температурах из насыщенного раствора выпадают кристаллогидраты с 4, 2 и 1 молекулами H2O.
Обладает высокой гигроскопичностью.
Пищевой хлорид кальция нетоксичен. Технический хлористый кальций по степени воздействия на организм относится к умеренно опасным веществам (3-й класс опасности по ГОСТ 12.1.005). Хлорид кальция относительно безвреден для растений и почвы.
Негорюч, пожаро- и взрывобезопасен.
Хлорид кальция является пищевой добавкой Е509.
В природе хлорид кальция встречается в виде минерала антарктицита (CaCl2•6H2O).
Физические свойства хлорида кальция:
| Наименование параметра: | Значение: |
| Химическая формула | CaCl2 |
| Синонимы и названия иностранном языке | calcium chloride (англ.) |
кальций хлористый (рус.)
Получение хлорида кальция:
В промышленности технический хлорид кальция получают из известняка в качестве побочного продукта при производстве кальцинированной соды (процесс Сольвея), а также как побочный продукт в процессе рекуперации аммиака в этом же процессе.
Пищевой хлорид кальция получают взаимодействием соляной кислоты и гидроксида кальция (в виде известкового молока).
Хлорид кальция получают в результате следующих химических реакций:
- 1. взаимодействия карбоната кальция и хлорида натрия:
Основная химическая реакция процесса Сольвея.
- 2. взаимодействия карбоната кальция и хлорида аммония:
Реакция протекает при кипении. Реакция рекуперации аммиака. Используется в процессе Сольвея.
- 3. взаимодействия гидроксида кальция и хлорида аммония:
Реакция рекуперации аммиака. Используется в процессе Сольвея.
- 4. взаимодействия оксида кальция и хлорида аммония:
Реакция рекуперации аммиака. Используется в процессе Сольвея.
- 5. взаимодействия гидроксида кальция и хлора:
- 6. взаимодействия гидроксида кальция и хлорида магния:
Химические свойства хлорида кальция. Химические реакции хлорида кальция:
Химические свойства хлорида кальция аналогичны свойствам хлоридов других металлов . Поэтому для него характерны следующие химические реакции:
1. реакция взаимодействия хлорида кальция и алюминия:
3CaCl2 + 2Al → 3Ca + 2AlCl3 (t = 600-700°C).
В результате реакции образуются кальций и хлорид алюминия.
2. реакция взаимодействия хлорида кальция и гидроксида натрия :
В результате реакции образуются хлорид натрия и гидроксид кальция . В ходе реакции используется концентрированный раствор гидроксида натрия.
3. реакция взаимодействия хлорида кальция и ортофосфата лития:
В результате реакции образуются хлорид лития и ортофосфат кальция . В ходе реакции хлорид кальция используется в виде концентрированного раствора.
4. реакция взаимодействия хлорида кальция и ортофосфата калия :
В результате реакции образуются ортофосфат кальция и хлорид калия.
5. реакция взаимодействия хлорида кальция и ортофосфата натрия :
В результате реакции образуются ортофосфат кальция и хлорид натрия.
6. реакция взаимодействия хлорида кальция и хромата натрия:
В результате реакции образуются хромат кальция и хлорид натрия. В ходе реакции хлорид кальция и хромат натрия используется в виде насыщенных растворов.
7. реакция взаимодействия хлорида кальция и карбоната натрия :
В результате реакции образуются карбонат кальция и хлорид натрия.
8. реакция взаимодействия хлорида кальция и карбоната аммония:
В результате реакции образуются карбонат кальция и хлорид аммония.
9. реакция взаимодействия хлорида кальция и нитрата серебра:
В результате реакции образуются нитрат кальция и хлорид серебра.
10. реакция взаимодействия хлорида кальция и сульфата калия:
В результате реакции образуются сульфат кальция и хлорид калия.
11. реакция взаимодействия хлорида кальция и силиката натрия:
В результате реакции образуются силикат кальция и хлорид натрия.
12. реакция взаимодействия хлорида кальция и сульфида бария:
В результате реакции образуются сульфид кальция и хлорид бария. В ходе реакции используются насыщенные растворы сульфида бария и хлорида кальция.
13. реакция электролиза хлорида кальция:
В результате реакции образуются кальций и хлор .
14. реакция термического разложения гексагидрата хлорида кальция:
В результате реакции образуются хлорид кальция и вода .
Применение и использование хлорида кальция:
Хлорид кальция используется во множестве отраслей промышленности и для бытовых нужд:
– в дорожном хозяйстве для обеспыливания гравийных дорог, а также как противогололёдное средство;
– в цветной металлургии для получения металлического натрия , титана ;
– для осушки газов;
– в строительстве как компонент бетонных смесей для ускорения схватываемости цемента ;
– при производстве пластмасс и керамики как добавка;
– в производстве удобрений для сельского хозяйства;
– при нефтедобыче в составе буровых растворов;
– в пищевой промышленности в качестве пищевой добавки Е509 как загуститель, отвердитель, желирующий агент.




хлорид кальция реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие хлорида кальция
реакции
Подробно решение уравнений окислительно-восстановительных реакций (ОВР) методом электронного баланса разобраны на странице "Метод электронного баланса".
Ниже приведены примеры решения уравнений окислительно-восстановительных реакций соединений хлора:
Если в окислительно-восстановительной реакции принимают участие простые вещества, молекулы которых состоят из двух или более атомов элементов, то в электронном балансе кол-во отданных и полученных электронов определяют с учётом кол-ва атомов в молекуле: H2 0 -2e - → 2H +1 .
Уравнения окислительно-восстановительных реакций соединений хлора
1. Уравнение реакции соляной кислоты с кислородом (HCl+O2):
2. Уравнение реакции соляной кислоты с перманганатом калия (HCl+KMnO4):
Следует обратить внимание, что часть хлорид-ионов соляной кислоты окисляется до хлора, а другая часть переходит в состав молекул хлорида калия и хлорида магния без изменения своей степени окисления, поэтому, коэффициенты в первую очередь ставятся перед Cl2, KCl, MnCl2 и только потом, перед HCl.
3. Уравнение реакции соляной кислоты с хромом на воздухе (HCl+Cr):
4. Уравнение реакции соляной кислоты с манганатом калия (HCl+K2MnO4):
5. Уравнение реакции разбавленной соляной кислоты с кальцием (HCl+Ca):
6. Уравнение реакции разбавленной соляной кислоты с гидридом кальция с образованием хлорида кальция и водорода:
7. Уравнение реакции хлорида кальция с водородом с образованием гидрида кальция и соляной кислоты:
8. Уравнение реакции хлорида железа (II) с водородом с образованием железа и соляной кислоты:
9. Уравнение реакции хлорида железа с хлором в нейтральной среде с образованием метагидроксида железа и соляной кислоты:
10. Уравнение реакции окисления на воздухе хлорида железа (III):
11. Уравнение реакции хлорида железа (III) с водородом с образованием хлорида железа (II) и соляной кислоты:
12. Уравнение реакции хлорида меди с алюминием с образованием хлорида алюминия и меди:
13. Уравнение реакции хлорида аммония с нитратом калия с образованием оксида азота, хлорида калия и воды:
14. Уравнение реакции хлорида аммония с магнием с образованием хлорида магния, аммиака и водорода:
15. Уравнение реакции разложения гипохлорита натрия с образованием хлората и хлорида натрия:
16. Уравнение реакции разложения хлората калия с образованием хлорида калия и кислорода:
17. Уравнение реакции хлората калия с алюминием:
18. Уравнение реакции хлората калия с концентрированной соляной кислотой:
19. Уравнение реакции хлората калия с концентрированной серной кислотой:
20. Уравнение реакции хлората калия с серой:
21. Уравнение реакции хлората калия с красным фосфором:
22. Уравнение реакции хлората калия с гидридом кальция:
23. Уравнение реакции разложения хлорной кислоты:
24. Уравнение реакции разложения перхлората калия:
25. Уравнение реакции разложения хлорита натрия:
26. Уравнение реакции гипохлорита кальция с пероксидом водорода:
27. Уравнение реакции хлорноватистой кислоты с иодоводородом:
28. Уравнение реакции разложения оксида хлора (I):
29. Уравнение реакции разложения диоксида хлора при нагревании (сопровождается большим выделением тепла - взрывом):
30. Уравнение реакции диоксида хлора с гидроксидом калия:
31. Уравнение реакции диоксида хлора с озоном:
32. Уравнение реакции диоксида хлора с пероксидом водорода:
33. Уравнение реакции дихлоргексаоксида с гидроксидом калия:
34. Уравнение реакции разложения оксида хлора (VII):
Если вам понравился сайт, будем благодарны за его популяризацию :) Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:

Щелочные металлы
Щелочные металлы — это элементы главной подгруппы I группы Периодической системы химических элементов Менделеева (ПСМ) (кроме водорода).
Задание 9.1. Назовите все щелочные металлы. Составьте схемы строения атомов натрия и калия. Укажите распределение их валентных электронов.
На внешнем уровне у атомов таких металлов находится по 1 электрону, но расстояние до ядра, а значит, и притяжение к нему, у этих электронов различно.
Вопрос. У какого элемента (натрия или калия) внешние электроны дальше от ядра?
Чем дальше электроны от ядра, тем слабее они притягиваются к нему, тем легче данный атом отдаёт электроны. А это означает, что металлические свойства выражены тем ярче, чем дальше валентные электроны от ядра (при прочих равных условиях). Поэтому сверху вниз в каждой главной подгруппе увеличивается число энергетических уровней в атомах, растёт металлическая активность элементов, т. е. способность их атомов отдавать электроны.
Вопрос. Какой металл более активный: натрий или калий?
Таким образом, активность щелочных металлов возрастает
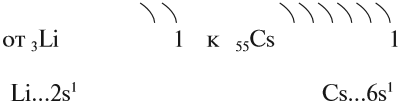
Но поскольку на внешнем уровне любого щелочного металла находится один электрон, в любой химической реакции щелочные металлы могут отдать только один электрон. Значит, они имеют постоянную валентность I и образуют оксиды состава
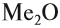
Этот оксид растворяется в воде, реагирует с нею:
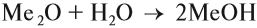
Полученное основание — щёлочь.
Вопрос. Что такое щёлочь? (См. урок 2.3.)
В подгруппе сверху вниз увеличивается и сила оснований, т. е. способность диссоциировать в водных растворах на ионы. Самой сильной щёлочью является CsOH.
Рассмотрим свойства щелочных металлов на примере натрия. При этом будем придерживаться схемы, изложенной начале второй части.
Строение атома Nа изображается схемой:
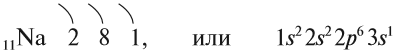
Имея один валентный электрон (…3s 1 ), натрий является активным металлом с постоянной валентностью I:
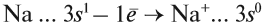

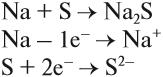
Вопрос. Почему атом серы присоединил 2 электрона?
Задание 9.2. Составьте уравнения реакций натрия с хлором Cl2, азотом N2 и водой (при затруднениях см. пояснения в уроке 7).
Даже небольшие кусочки натрия (величиной с горошину) при попадании в воду вызывают оглушительный взрыв — это взрывается водород (см. урок 12). Тот же эффект будет, если натрий опустить в раствор кислоты или соли. Кроме того, здесь возможны более сложные побочные процессы. Поэтому составлять уравнения реакций для щелочных металлов в качестве примеров процессов
- металл + раствор кислоты →
- металл + раствор соли →
Натрий образует основный оксид Nа2O, который реагирует с водой, с кислотами и кислотными оксидами (см. урок 2.1), например:
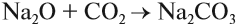
Задание 9.3. Составьте уравнения реакций оксида натрия с водой и с серной кислотой.
Гидроксид натрия NaOH (едкий натр, каустическая сода) проявляет все свойства щелочей: реагирует с кислотными оксидами, кислотами, растворами солей (см. урок 2.3), например:
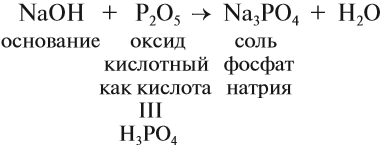
Все соединения натрия окрашивают пламя в жёлтый цвет. Это качественная реакция на соединения натрия.
Задание 9.4. Составьте уравнения реакций гидроксида натрия с хлоридом железа III, фосфорной кислотой, оксидом серы IV. (При затруднениях см. урок 2.3.)
Задание 9.5. Опишите по разобранной схеме свойства калия и его соединений.

Щелочноземельные металлы
Металлы главной подгруппы II группы в отличие от щелочных металлов имеют довольно разные свойства.
- Сколько электронов на внешнем уровне атомов этих металлов?
- Какой металл более активен: натрий или магний? Почему?
Вопрос. Как изменяется активность металлов в подгруппе сверху вниз? Почему?
В этой подгруппе, как и у щелочных металлов, сверху вниз увеличивается сила оснований, т. е. способность диссоциировать в водных растворах на ионы. Кроме того, увеличивается заряд иона, а значит, усиливается притяжение группы ОН в гидроксиде металла: ионы Na + и OH – притягиваются слабее, чем Са 2+ и ОН – .
Поэтому первые два элемента этой подгруппы не образуют щелочей:
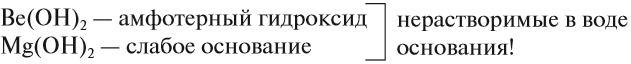
Кальций уже образует сильное основание — щёлочь, а стронцию и барию соответствуют ещё более сильные основания.
Запомните: Ca, Sr, Ba — щелочноземельные* металлы, так как их оксиды проявляют щелочные свойства.
Несмотря на эти различия, перечисленные элементы имеют много сходного в свойствах.
Вопрос. Какую валентность проявляют эти химические элементы в соединениях?
Главное сходство химических элементов главной подгруппы II группы заключается в том, что они проявляют в соединениях постоянную валентность II, так как на внешнем уровне имеют по два электрона, а на предвнешнем уровне нет незавершённых подуровней.
Рассмотрим свойства химических элементов главной подгруппы II группы на примере кальция. Строение атома кальция изображается схемой:
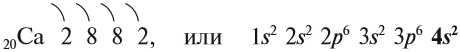
Имея два валентных электрона: …4s 2 , кальций является активным металлом, поскольку оба электрона расположены на внешнем уровне. Его постоянная валентность равна двум:
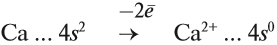
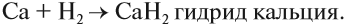
Рассмотрим как происходит взаимодействие кальция с азотом:
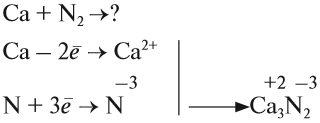
Вопрос. Почему атом азота присоединяет три электрона?
Задание 9.6. Составьте уравнения реакций кальция с кислородом, хлором (Cl2), серой, водой, соляной кислотой.
Оксид кальция CaO (негашёная известь) очень активно реагирует с водой с выделением такого большого количества теплоты, что вода закипает:
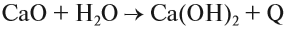
Вопрос. С какими ещё веществами может реагировать оксид кальция?
Как основный оксид CaO реагирует с кислотными оксидами и с кислотами:
- CaO + SO2 → СаSO3
- CaO + НNO3 → … (закончить уравнение этой реакции).
Гидроксид кальция Са(ОН)2 (гашёная известь) проявляет все свойства щелочей.
Вопрос. С какими веществами могут реагировать щелочи? (При затруднении см. урок 2.3.)
Задание 9.7. Составить уравнения реакций:
Прозрачный раствор гидроксида кальция в воде называется известковой водой. Она мутнеет при пропускании через неё углекислого газа:
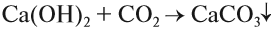
Этот эффект реакции считают качественным признаком того, что в данном растворе присутствуют ионы кальция. Убедиться в этом поможет также реакция с пламенем: все соединения кальция окрашивают пламя в кирпично-красный цвет.
Задание 9.8. Опишите по предложенной схеме свойства магния и его соединений.
Многие соединения кальция играют заметную роль в нашей жизни. Достаточно сказать, что фосфат кальция, карбонат кальция составляют основу костей, зубов. Без ионов кальция не может свертываться кровь. Без соединений кальция невозможно построить дом, так как известь (гашёная и негашёная) обеспечивает скрепление строительных блоков друг с другом:
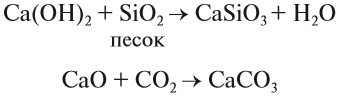
Образование в результате этих реакций прочных нерастворимых карбонатов и силикатов кальция надёжно скрепляет стены. Аналогичные реакции происходят при схватывании цемента.
Оксид кальция в больших количествах получают обжигом известняка:
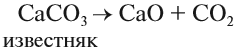
Карбонат кальция СаСО3 составляет основу мела, мрамора, известняка. Из него состоят целые горы и пласты земной коры. Под действием воды и углекислого газа из воздуха карбонат кальция переходит в водорастворимое состояние — гидрокарбонат кальция:
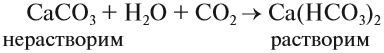
Аналогичные процессы происходят и с карбонатами магния. В результате этих и других процессов в природной воде появляются ионы кальция и магния.
Вода, содержащая ионы кальция и магния, называется ЖЁСТКОЙ.
Этот термин возник из-за того, что некоторые овощи и плоды под действием такой воды становятся жёсткими: ионы кальция и магния вступают в реакцию с органическими компонентами плодов и овощей.
Чаще всего жёсткая вода приносит неприятности: долго развариваются продукты, плохо моет мыло (см. урок 24.4), на стенках котлов и труб появляется слой накипи, что может привести к авариям:
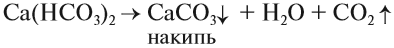
Накипь, конечно, можно растворить при помощи соляной кислоты:
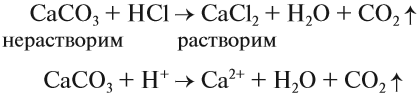
Задание 9.10. Можно ли растворить накипь при помощи серной, азотной, фосфорной кислот? Ответ подтвердите ионно-молекулярными уравнениями реакций.
Но лучше всего в случаях, когда жёсткость воды повышена, а это нежелательно, умягчать воду. Для этого ионы кальция и магния нужно перевести в нерастворимое состояние.
Вопрос. Умягчается ли вода при кипячении?
Частично вода умягчается при кипячении, так как при этом растворимые гидрокарбонаты переходят в нерастворимые карбонаты. Но некоторые соли кальция и магния (сульфаты, хлориды) при нагревании не изменяются. В этом случае в воду добавляют вещества, образующие с ионами кальция и магния осадки.
Задание 9.11. Какие из солей: кальцинированная сода, фосфат натрия, поваренная соль — устраняют жёсткость воды? Ответ подтвердить ионными уравнениями реакций, считая, что в состав воды входит сульфат кальция.
Чаще всего для умягчения воды используют кальцинированную соду Na2CO3:
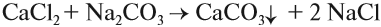
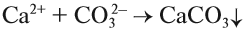

Выводы
Щелочные металлы — это простые вещества, которые образованы элементами главной подгруппы первой группы. Это очень активные металлы, которые образуют с водой сильные растворимые основания — щёлочи.
Щелочноземельные металлы — это простые вещества, которые образованы некоторыми элементами главной подгруппы второй группы Ca, Sr, Ba. Это очень активные металлы, которые образуют с водой щёлочи. Ионы кальция и магния делают воду жёсткой.
Читайте также:

