Саркома костей клинические рекомендации
СМОТРЕТЬ ДРУГИЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
Год утверждения 2020
Профессиональные ассоциации
- Общероссийский национальный союз "Ассоциация онкологов России"
- Автономная некоммерческая организация "Восточно-Европейская группа по изучению сарком"
- Общероссийская общественная организация "Российское общество клинической онкологии"
Одобрено Научно-практическим Советом Минздрава РФ
Оглавление
1. Краткая информация
- опухоль неэпителиального происхождения;
- развивается из клеток производных мезодермы.
- лучевая терапия,
- иммунодефицит,
- болезнь Педжета,
- болезнь Олье,
- доброкачественные опухоли кости.
У большинства пациентов этиологические факторы не выявляются.
Первичные ЗНО костей 0,001 % от всех впервые выявленных ЗНО.
В РФ заболеваемость 1,03 случая на 100 тыс. населения, как в других странах.
Злокачественное новообразование костей и суставных хрящей (C40):
C40.0 – лопатки и длинных костей верхней конечности;
C40.1 – коротких костей верхней конечности;
C40.2 – длинных костей нижней конечности;
C40.3 – коротких костей нижней конечности;
C40.8 – поражение костей и суставных хрящей конечностей, выходящее за пределы одной и более вышеуказанных локализаций;
C40.9 – костей и суставных хрящей конечности неуточненной локализации.
Злокачественное новообразование костей и суставных хрящей других и неуточненных локализаций (C41):
C41.0 – костей черепа и лица;
C41.1 – нижней челюсти;
C41.2 – позвоночного столба;
C41.3 – ребер, грудины и ключицы;
C41.4 – костей таза, крестца и копчика;
C41.8 – поражение костей и суставных хрящей, выходящее за пределы одной и более вышеуказанных локализаций;
C41.9 – костей и суставных хрящей неуточненное.
Стадирование
По TNM AJCC/UICC 7-го пересмотра (2010 г.) (TNM AJCC/UICC 8-го пересмотра (2019 г.)
Клиника определенной стадийности и зависит от локализации опухоли.
Первый симптом - боль.
Возможна субфебрильная температура.
Быстрая прогрессия - через 2–3 месяца припухлость и гиперемия кожи.
Нарушение функции при локализации вблизи сустава.
Без лечения через 5–7 месяцев - выраженная прогрессирующая интоксикация:
- слабость,
- резкое похудание,
- повышение температуры тела,
- лейкоцитоз,
- увеличенная СОЭ.
2. Диагностика
- доброкачественные опухоли,
- метастатические опухоли костей,
- остеомиелит,
- артрит,
- дегенеративно-дистрофические изменения суставов.
Критерии установления диагноза:
- анализ жалоб пациента,
- осмотр,
- данные инструментальных и лабораторных исследований,
- морфологическая верификация.
Сбор анамнеза, в том числе наследственного и онкологического.
У пациентов старше 40 лет необходимо исключить метастатическое поражение костей.
- начало развития заболевания,
- наличие болевого синдрома,
- изменения функции.
Оценить влияние клиники на качество жизни пациента.
- Оценить состояние области пораженной кости.
- Проверить функцию сустава.
- Исключить риск патологического перелома.
- Пальпация периферических лимфоузлов.
- общий̆ (клинический) мочи,
- общий̆ (клинический) крови,
- общетерапевтический биохимический крови,
- коагулограмма.
Рентгенография пораженной области и близлежащего сустава в двух проекциях с линейкой.
МРТ пораженного отдела скелета.
КТ органов грудной клетки.
При подозрении на диссеминацию:
- сцинтиграфия с 99Tc,
- УЗИ брюшной полости, забрюшинного пространства, периферических лимфоузлов.
При саркоме Юинга - биопсия костного мозга с миелограммой.
Для верификации - биопсия опухоли.
Стандарты биопсии опухоли:
1. Под контролем сертифицированного онкоортопеда или радиолога.
2. Морфологическая верификация проводится в крупных онкологических ЛПУ.
3. Предпочтительна толстоигольная биопсия.
4. Открытый доступ возможен:
1) при анатомически трудной локализации;
2) при отрицательной трепанобиопсии, скудности и малой информативности материала.
5. При открытом доступе выбирается стандартный оперативный̆ доступ.
6. Тактика разрабатывается совместно с хирургом-онкоортопедом, химиотерапевтом и, при необходимости, лучевым терапевтом.
7. Неправильный выбор места биопсии или нарушение техники ограничивает выбор способа мышечной пластики, повышает риск рецидива.
- биопсийного материала с целью верификации;
- операционного материала с целью оценки краев резекции, лечебного патоморфоза.
3. Лечение
1. Паростальная (юкстакортикальная) остеосаркома – только радикальное хирургическое лечение.
2. Периостальная остеосаркома:
- радикальное хирургическое лечение,
- консервативного лечения для перевода в резектабельное состояние.
3. Остеосаркома высокой степени злокачественности – комбинированное лечение:
- блок неоадъювантной терапии,
- радикальное хирургическое лечение,
- блок адъювантной терапии.
Органосохранные операции:
- при возможности отступа не менее 3–5 см,
- при условии отсутствия опухоли в костномозговом канале оставшейся части кости.
Главное условие операбельности - радикальность и абластичность удаления опухоли.
Ампутация или экзартикуляция конечности:
- обширное первично-множественное распространение,
- вовлечение магистрального сосудисто-нервного пучка, исключающее реконструктивно -пластический этап,
- прогрессирование на фоне предоперационной̆ терапии,
- отказ пациента от органосохранной операции,
- жизненные показания к экстренной хирургии – распад, кровотечение.
Использование модульных систем эндопротезирования.
Виды реконструктивных операций в объеме эндопротезирования:
1) стандартные первичные операции у взрослых;
2) стандартные первичные операции у детей̆ и подростков;
3) эндопротезирование редких анатомических зон;
4) ревизионное эндопротезирование.
Требования к эндопротезу для взрослых:
1) модульность конструкции;
2) максимальная надежность и ремонтопригодность;
3) универсальность компонентов;
4) максимальный срок службы;
5) стабильная фиксация;
6) хороший̆ функциональный̆ результат;
7) короткий̆ срок изготовления.
Особенности эндопротеза для детей̆ и подростков:
1) бесцементный способ фиксации;
2) раздвижной̆ механизм (инвазивный̆ и неинвазивный).
Реэндопротезирование проводят в медорганизациях с подготовленной командой онкологов, травматологов-ортопедов и хирургов с практическим опытом.
Индивидуальные системы протезирования, персонализированный инструментарий, прототипы операций при опухоли:
- костей таза,
- позвоночника,
- других сложных анатомических локализаций.
При использовании онкологических эндопротезов применяют длительные режимы профилактической антибиотикотерапии:
1) цефалоспорины 3 поколения + клиндомицин или ванкомицин 10 - 14 дней в стационаре,
2) пероральные в последующие 4 недели.
Факторы риска инфицирования:
- высокая злокачественность,
- глубокое расположение опухоли,
- иммунносупрессия от неоадъювантной ХТ,
- предшествующая ЛТ,
- неадекватная антибиотикопрофилактика,
- прием кортикостероидов,
- большая раневая поверхность,
- продолжительная операция (более 3 часов),
- кровопотеря более 0,5 объема циркулирующей крови,
- вторичное заживление раны,
- некрозы кожи,
- дополнительные хирургические манипуляции,
- сопутствующие заболевания (анемия, сахарный диабет и т.д.)
Калечащие операции (ампутации, экзартикуляции и др.):
- при технической невозможности радикальности R0 (R1),
- по витальным показаниям.
Хирургическая тактика не имеет принципиальных различий.
Комбинированное лечение при локализованной форме:
- предоперационная ХТ,
- операция,
- послеоперационная ХТ.
Предоперационная ХТ:
- улучшает результаты лечения;
- позволяет оценку in vivoактивности химиопрепаратов;
- облегчает выполнение операции;
- 3–4 цикла;
- при некрозе опухоли от 90% вероятность увеличения безрецидивной и общей̆ выживаемости.
При локализованной опухоли - 4 цикла AP:
- Доксорубицин 90 мг/м2 в/в, 96-часовая инфузия;
- Цисплатин 120 мг/м 2 в/в или в/а инфузия 1 день каждые 4 недели.
Послеоперационная ХТ - режим определяется по степени лекарственного патоморфоза:
- при III–IV степени - повторение АР, также 4 цикла,
- при меньшей степени некроза - 12 месяцев альтернирующих схем:
- 4 цикла HDI: ифосфамид 2 г/м 2 (с месной) в/в инфузия 1–7 дни, через 3 недели, КСФ 8–16 дни;
- через 3 недели – HD MTX: метотрексат 12 г/м 2 в/в (с кальция фолинатом), 4 введения с интервалом в 14 дней только для молодых пациентов.
- при явной низкой эффективности 2 курсов - смена на 2 курса высокодозного ифосфамида или высокие дозы метотрексата с кальция фолинатом;
- при крайне низкой степени лечебного патоморфоза возможны 2 курса гемцитабин 900мг/м 2 в 1, 8 дни + доцетаксел 100мг/м 2 8 день, филграстим 5 мкг/кг п/к 9-19 дни.
При нерезектабельной остеосаркоме 2-я и последующие линии ХТ:
- GemTax - Гемцитабин 900мг/м 2 в 1, 8 дни + Доцетаксел 100мг/м 2 в/в 8 день + филграстим 5мкг/кг п/к 9-19 дни, 2 цикла
- Сорафениб 400 мг х 2 раза в день, 3 месяца
Протонная терапия:
- самостоятельный метод при саркомах костей черепа, позвоночника, орбиты,
- после хирургического лечения при R1 и R2 краях резекции.
- не отличается от общепринятой̆ классификации для первичных опухолей̆ костей̆,
- при внекостной форме - как опухоли мягких тканей̆.
Радикальная операция - наилучший локальный контроль.
Локальное лечение из-за высокой̆ частоты метастазирования в кости и костный̆ мозг дополняется комбинированной̆ ХТ:
- 4 - 6 циклов индукционной̆ ХТ за 12–24 недель,
- после локального лечения 12 месяцев 6-10 циклов ХТ с 3-недельным интервалом.
Комбинация из 4-6 наиболее активных цитостатиков:
- доксорубицин,
- циклофосфамид,
- ифосфамид,
- винкристин,
- дактиномицин,
- этопозид.
Лучевая терапия:
- при невозможности радикального оперативного вмешательства,
- при недостаточном лечебном патоморфозе (более 10 % жизнеспособных клеток).
- СОД 40–45 Гр при микроскопических остаточных опухолях,
- СОД 50–60 Гр при макроскопических изменениях,
- дистанционная 3-D и интенсивно модулированная (IMRT) РОД = 2–2,5 Гр, СОД = 60 Гр с ХТ при отказе или нерадикальной операции,
- при метастазах в легкие – крупнопольная РОД = 2 Гр, СОД = 20 Гр.
ХТ - чередование режимов IE и VAC каждые 3–4 недели:
- IE:
- этопозид 100 мг/м 2 в/в 1–5 дни;
- ифосфамид 1,8 г/м 2 в/в инфузия 1–5 дни с месной.
- VAC:
- винкристин 2 мг/м 2 в/в 1 день;
- доксорубицин 75 мг/м 2 в/в 1 день;
- циклофосфамид 1200 мг/м 2 в/в 1 день.
При раннем прогрессировании - менее 1 года после завершения комбинированного лечения ХТ:
- циклофосфамид 250 мг/м 2 в/в 1–5 дни; топотекан 0,75 мг/м 2 в/в 1–5 дни; каждые 3–4 недели;
- этопозид 100 мг/м 2 в/в 1–5 дни; топотекан 0,75 мг/м 2 в/в 1–5 дни; каждые 3–4 недели;
- иринотекан 250 мг/м 2 в/в 6 день; темозоломид 150 мг/м 2 внутрь или в/в 1–5 дни; каждые 4 недели;
- GemTax: гемцитабин 900 мг/м 2 1, 8 дни 90-минутная инфузия; доцетаксел 100 мг/м 2 8день; КСФ п/к 9–19 дни.
Рекомендуется комбинированная ХТ в сочетании с возможным оперативным лечением.
Выбор 2-й линии ХТ зависит от первичного лечения:
- высокие дозы метотрексата, ифосфамид,
- не доказана эффективность этопозида,
- при метастазах через 6 месяцев после лечения, возможно повторение режима химиотерапии.
При метастатическом поражении легких возможно оперативное вмешательство с ХТ:
- метастазэктомия,
- повторная торакотомия.
ХТ при метастазах в легких:
- те же режимы в такой же последовательности, как при лечении первичной опухоли,
- 3-я и более линий терапии - сорафениб (нексавар) 400 мг 2 раза в сутки ежедневно.
При рецидиве саркомы Юинга - паллиативная терапия, за исключением ограниченного рецидива после длительного свободного периода.
Единственный прогностический фактор при рецидиве - время его возникновения, лучшие результаты при свободном периоде больше 2 лет.
- такая же стандартизированная ХТ, как при локализованной саркоме,
- остеогенной саркомы в легкие повышение выживаемости после резекции остаточных метастазов только после эффективной̆ ХТ и тотальной ЛТ легкого,
- в кости или костный̆ мозг 5-летняя выживаемость менее 20%,
- в кости показана ЛТ,
- интенсивные и высокодозные режимы ХТ с аутотрансплантацией костного мозга оправданы у отдельных пациентов,
- при местно-распространенной и/или метастатической гигантоклеточной опухоли кости таргетная терапия деносумабом 120мг п/к 1, 8, 15 и 28 дни, далее через 28 дней.
ЖКТ – желудочно-кишечный тракт
КТ – компьютерная томография
МРТ – магнитно-резонансная томография
ПНЭТ (PNET) – примитивная нейроэктодермальная опухоль
ПЭТ – позитронно-эмиссионная томография
СМТ – саркомы мягких тканей
УЗИ – ультразвуковое исследование
IMRT – intensity-modulated radiation therapy
КСФ-поддержка – применение колониестимулирующих факторов (АТХ - L03AA)
1. 2020 Клинические рекомендации "Саркомы костей" (Общероссийский национальный союз "Ассоциация онкологов России"; Автономная некоммерческая организация "Восточно-Европейская группа по изучению сарком"; Общероссийская общественная организация "Российское общество клинической онкологии").
Определение
Саркома кости – опухоль неэпителиального происхождения. Развивается из клеток производных мезодермы, в частности мезенхимы (первичной соединительной ткани).
Терминология
Безрецидивная выживаемость – от момента наступления ремиссии до момента возникновения рецидива.
Бессобытийная выживаемость – от начала лечения до момента прекращения ремиссии независимо от причины, приведшей к ней.
Общая выживаемость – от начала лечения до окончания исследования или смерти пациента.
Критерии качества
Уровень убедительности рекомендаций
Уровень достоверности рекомендаций
Выполнение УЗИ органов брюшной полости (комплексное) и забрюшинного пространства
Получение полного патолого-анатомического заключения до начала системной терапии
Выполнение предоперационной терапии (химиотерапия, лучевая терапия) в соответствии с рекомендациями
Выполнение хирургического пособия согласно клиническим рекомендациям с обязательным указанием объем удаленных тканей, маркировки краев, отступов, удаленных жизненно важных структур, метода закрытия раны
УДД
Расшифровка
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
Несравнительные исследования, описание клинического случая
Имеется лишь обоснование механизма действия или мнение экспертов
УУР
Расшифровка
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Остеосаркома (или остеогенная саркома), которую еще иногда не совсем правильно называют раком кости, — самая распространенная злокачественная опухоль костной системы.
Некоторые цифры и факты:
- В большинстве случаев остеосаркому диагностируют в молодом возрасте — от 10 до 30 лет.
- Наиболее высока распространенность заболевания среди подростков, но это не означает, что не могут заболеть люди другого возраста.
- Каждый десятый случай остеогенной саркомы встречается у людей старше 60 лет.
- Среди прочих онкологических заболеваний остеосаркома встречается редко. У детей она составляет 2% от всех видов рака, у взрослых — еще меньше.
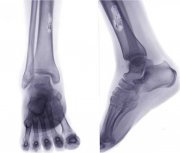
Чаще всего остеосаркома встречается там, где находятся зоны роста — ближе к концам длинных трубчатых костей. Излюбленные места локализации опухоли: область колена (нижний конец бедренной и верхний конец большеберцовой кости), верхняя часть плечевой кости. Намного реже встречаются поражения других костей: таза, челюстей и др. Редкие локализации в большинстве случаев обнаруживают у людей старшего возраста.
Почему возникает остеосаркома?
Точные причины возникновения опухоли не известны. Но существуют некоторые факторы риска:
- Возраст. В группе максимально высокого риска подростки и молодые люди, у которых кости интенсивно растут.
- Рост. Обычно люди, у которых возникает саркома, имеют рост выше среднего.
- Облучение костей. Риски повышены у людей, которые перенесли курс лучевой терапии высокими дозами, особенно если это было в детстве. Влияние рентгенографии и компьютерной томографии не доказано.
- Некоторые заболевания костей: болезнь Педжета, множественная наследственная остеохондрома.
- Некоторые наследственные патологии: наследственная ретинобластома, синдром Ли-Фраумени, синдром Ротмунда-Томсона, синдром Блума, синдром Вернера.
Среди факторов риска для многих онкозаболеваний большое значение имеют особенности образа жизни: масса тела, вредные привычки, характер питания, физическая активность. Можно сказать, что остеосаркома — в данном случае исключение. Для того чтобы образ жизни внёс свою лепту в возникновение злокачественной опухоли, должны пройти десятилетия, а рак костей, как мы уже знаем, наиболее распространен среди молодых людей.
Симптомы остеосаркомы
Чаще всего встречается остеогенная саркома бедренной и большой берцовой кости — в области коленного сустава. Типичный симптом заболевания — упорные боли в суставе, кости. Иногда они постоянные, а иногда то стихают, то нарастают. Болевые ощущения могут усиливаться по ночам, во время физической активности (при ходьбе, беге, занятиях спортом). Если поражена нога, человек начинает хромать.
Дети, особенно маленькие, физически активны, они часто падают, ударяются, поэтому у них первые симптомы остеосаркомы легко спутать с травмой. У взрослого человека, особенно если он не занимается спортом и тяжелым физическим трудом, подобные проявления сразу должны насторожить и стать причиной для визита к врачу.
Какие выделяют стадии остеосаркомы?
Существуют разные классификации, чаще всего врачи определяют стадию остеосаркомы в соответствии с системой MSTS. Учитывают три показателя:
- G — степень озлокачествления. Может быть низкой (G1), когда ткань опухоли похожа на нормальную, и более агрессивной высокой (G2), в которой клетки практически полностью утратили первоначальные черты.
- T — степень распространения опухоли. Она может находиться в пределах кости (T1) или прорастать в соседние ткани (T2).
- M — наличие метастазов. M0 — метастазов нет, M1 — есть.
Другая классификация — AJCC, она учитывает распространение первичной опухоли (T), метастазы в ближайших лимфатических узлах (N), метастазы в других частях тела (M) и степень озлокачествления (G).
Методы диагностики
По симптомам можно только заподозрить рак кости или другое заболевание. Для того чтобы получить точный диагноз, врач назначит обследование, которое может включать:
- Рентгенографию. Быстрый и простой метод диагностики, в некоторых случаях помогает сразу констатировать опухоль. Если есть подозрение на метастазы в легких, проводят рентген грудной клетки.
- Магнитно-резонансная томография (МРТ) и компьютерная томография (КТ) помогают более детально рассмотреть опухоль, обнаружить прорастание в соседние ткани.
- Позитронно-эмиссионная томография. В организм вводят слабое радиоактивное вещество в безопасных дозах, которое сильнее всего накапливается в опухолевых клетках. Затем делают снимки. Это позволяет не только рассмотреть основную опухоль, но и обнаружить метастазы в разных частях тела.
- Общий и биохимический анализы крови. Применяют как дополнительный метод диагностики, чтобы оценить общее состояние человека. Также они могут косвенно указывать на степень агрессивности опухоли.
- Биопсия. Самый точный метод диагностики. Её применяют всегда, даже если другие исследования уже убедительно показывают, что у пациента есть рак кости. Биопсия помогает установить окончательный диагноз, отличить остеосаркому от других опухолей, определить степень озлокачествления. Врач может взять образец ткани при помощи иглы или через разрез.

Как проводят лечение остеосаркомы?
Лечение остеосаркомы состоит из трех этапов.
Начинают с курса предоперационной, или неоадъювантной, химиотерапии. В среднем он продолжается 10 недель. Назначают комбинацию нескольких препаратов — это помогает усилить эффект. Задачи неоадъювантной химиотерапии: уменьшить размер остеосаркомы и уничтожить метастазы. Благодаря предоперационной химиотерапии и современным химиопрепаратам, выживаемость при остеосаркоме в последние годы значительно улучшилась.
Затем следует хирургическое лечение. В прошлом единственным выходом была ампутация пораженной руки или ноги. Современные хирурги чаще всего могут обойтись удалением части кости или сустава. Их можно заменить на специальный протез и практически полностью восстановить функцию конечности. Операции при остеосаркоме стали более щадящими.
Послеоперационный курс химиотерапии (адъювантная) нужен для того, чтобы удалить раковые клетки, которые могли остаться в организме после хирургического вмешательства. В среднем он продолжается 18 недель, иногда дольше.
Как лечить рецидив остеогенной саркомы? В целом схема лечения примерно та же — операция, курс химиотерапии. После рецидива прогноз намного хуже, но все еще есть шанс на выздоровление.
Прогноз при остеосаркоме
Прогнозы для онкобольных выстраивают на основе особого показателя — пятилетней выживаемости. Он обозначает процент пациентов, которые остались живы в течение пяти лет с момента установления диагноза. Конечно, многие живут и дольше. Пять лет — условный рубеж, после которого можно с достаточно высокой вероятностью предполагать, что человек выздоровел.

Наиболее благоприятен прогноз в случаях, когда опухоль локализованная — то есть не успела распространиться по организму и может быть полностью удалена во время операции. Пятилетняя выживаемость составляет 60–80%, а если опухоль чувствительна к современным таргетным препаратам — до 90%.
Если есть метастазы остеосаркомы, прогноз сильно ухудшается. Пятилетняя выживаемость падает до 15–30%. Но она может быть выше, в пределах 40%, если:
- рак успел распространиться только в легкие;
- все метастазы можно обнаружить и удалить.
Метастазы остеосаркомы чаще всего обнаруживают в легких, реже в костях, головном мозге и других местах.
Зачастую прогноз ухудшается из-за того, что человек не обратил внимания на первые симптомы и не посетил вовремя врача. Если есть хотя бы малейшее подозрение на рак, если возникли любые необычные симптомы — лучше сразу перестраховаться и пройти обследование. Иногда от этого зависит жизнь. Запишитесь на прием к врачу-онкологу, звоните:
Вам поставили диагноз: саркома костей?
Очень часто пациенты чувствуют себя безгранично одинокими вначале пути. Но вы должны понимать - вы не одни. Мы поможем вам справиться с болезнью и будем идти с Вами рука об руку через все этапы вашего лечения.
Что такое саркома костей?
Филиалы и отделения, где лечат саркомы костей
Хирургическое отделение онкологической ортопедии
Контакты: (495) 150 11 22
Отделение комбинированного лечения опухолей костей, мягких тканей и кожи
Заведующий отделения: Александр Александрович Курильчик
Контакты: 8 (484) 399 31 30
Введение
Опухоли костей – это обобщающее понятие, которое включает в себя все доброкачественные и злокачественные новообразования, поражающие скелет человека.
Скелет - совокупность костей человеческого организма. Служит опорой мягким тканям, точкой приложения мышц, вместилищем и защитой внутренних органов. Скелет взрослого человека состоит из 205—207 костей. Почти все они объединяются в единое целое с помощью суставов, связок и других соединений.


Статистика саркомы костей (эпидемиология)
Первичные злокачественные опухоли костей составляют 0,001% от всех впервые выявленных злокачественных новообразований. В России заболеваемость первичными злокачественными опухолями костей составляет 1,03 случая на 100 тыс. населения, что соответствует данным по заболеваемости в других странах.
Морфологическая классификация опухолей костей:
- Доброкачественные опухоли костей
- Остеома
- Остеоид — остеома
- Остеохондрома
- Хондрома.
- 2. Злокачественные опухоли костей
- Злокачественная фиброзная гистиоцитома
- Остеосаркома
- Саркома Юинга;
- Хондросаркома.
- Метастазы в кости опухолей различных локализаций
- Пограничные опухоли костей – Гигантоклеточная опухоль.
Стадии и симптоматика саркомы костей
Клиническая классификация TNM
Т - первичная опухоль
Тх - оценка первичной опухоли невозможна.
Т0 - первичная опухоль не обнаружена.
Т1 - опухоль размером до 8 см в наибольшем измерении.
Т2 - опухоль размером более 8 см в наибольшем измерении.
Т3 - множественные опухоли в кости первичного очага.
N - регионарные лимфатические узлы
Nx - состояние регионарных лимфатических узлов оценить невозможно.
N0 - метастазов в регионарных лимфатических узлах нет.
N1 - метастазы в регионарных лимфатических узлах имеются.
М - отдаленные метастазы
Мх - наличие отдаленных метастазов оценить невозможно.
М0 - отдаленных метастазов нет.
M1 - наличие отдаленных метастазов:
М1а - метастазы в легкие;
M1b - метастазы иной локализации.
G - гистопатологическая дифференцировка
Gх - степень дифференцировки не может быть установлена.
G1 - высокая степень дифференцировки.
G2 - средняя степень дифференцировки.
G3 - низкая степень дифференцировки.
G4 - недифференцированные опухоли.

Боль – самый ранний признак. Для начала болезни характерна тупая, ноющая боль без четкой локализации в кости. Дальнейшее развитие заболевания приводит к появлению невыносимо сильной боли, пик приходится на ночное время, не купируется обычными анальгетиками. У более чем половины пациентов на месте роста опухоли пальпируется припухлость по плотности мягче костной ткани. Пораженная конечность отекшая, может быть покраснение кожи.
Причины возникновения саркомы костей и факторы риска
К факторам риска развития сарком костей можно отнести предшествующую лучевую терапию, состояние иммунодефицита, болезнь Педжета, болезнь Олье, доброкачественные опухолевые поражения кости так же могут приводить к злокачественной трансформации. Однако, у большинства пациентов специфических этиологических факторов не выявляется.
Диагностика саркомы костей
·Для верификации онкопроцесса поразившего кость и определения дальнейшей тактики лечения, необходимо определить гистологический тип опухоли. “Золотым стандартом” - является выполнение трепан-биопсии либо открытой биопсии.
·Компьютерная томография легких. Наиболее часто саркомы костей метастазируют в легкие, а разряжающая возможность флюорографии и рентгеновского исследования невелика, поэтому пациентам с саркомами костей необходимо выполнение компьютерной томографии органов грудной клетки.
·Компьютерная томография или магнитно-резонансная томография первичного очага опухоли. Эти исследования позволяют адекватно оценить распространенность опухолевого процесса, прилежание опухоли к магистральным сосудисто-нервным структурам, степень вовлечения прилежащих мягких тканей.
·Ультразвуковое исследование брюшной полости, печени, прилежащих зон регионарного лимфооттока. Саркомы костей редко метастазируют в печень и регионарные лимфотические коллекторы (3-5%) и наличие метастазов в них является неблагоприятным прогностическим фактором, однако проводить исследование этих областей так же необходимо.
·Сцинтиграфия костей. Второй по частоте развития метастазов сарком костей точкой являются кости, поэтому проведение сцинтиграфии для таких пациентов обязательно.
·Так же необходимо диагностировать и вовремя назначить коррегириующую терапию сопутствующих хронических либо впервые выявленных заболеваний – сахарный диабет, различные кардиальные патологии, нарушения дыхания, нарушения работы почек и прочие.
Лечение саркомы костей
В первую очередь следует рассматривать возможность выполнения органосохранных операций. Главным условием операбельности пациентов является радикальность и абластичность удаления опухоли, что гарантирует отсутствие местного рецидива.
· Эндопротезирование онкологическим эндопротезом плечевого сустава.
· Эндопротезирование онкологическим эндопротезом тазобедренного сустава.
· Эндопротезирование онкологическим эндопротезом коленного сустава.
· Тотальное эндопротезирование бедренной кости.
· Модульное эндопротезирование вертлужной впадины после удаления опухолей костей таза.
· Эндопротезирование тел позвонков на всех уровнях позвоночного столба.
· Эндопротезирование онкологическим эндопротезом лучезапястного сустава.
· Эндопротезирование онкологическим эндопротезом локтового сустава.
· Реконструкция удаленных фрагментов костей при помощи ауто/аллопластики.
· Резекция костей плечевого пояса (лопатка, ключица).
· Резекции ребер и грудной стенки.
· Использование собственной кости пациента для замещения дефекта после операции.
· Онкологическое эндопротезирование, металлолстеосинтез.
· Расширенные операции при массивных опухолях плечевого пояса (межлопаточно-грудная ампутация).
При невозможности выполнения органосохранных операций необходимо выполнение калечащих операций в радикальном объеме. Ампутация или экзартикуляция конечности выполняются в следующих случаях:
- обширное первично-множественное распространение опухоли;
- вовлечение в опухолевый процесс магистрального сосудисто-нервного пучка.
- технически исключающий проведение реконструктивно-пластического этапа операции;
- прогрессирование на фоне предоперационной химиотерапии;
- отказ пациента от органосохранной операции;
- жизненные показания к экстренной хирургии – распад опухоли, кровотечения.
Так же в клинической практике лечения злокачественных поражений костей применятся лучевая и химиотерапия.
Осложнения противоопухолевого лечения саркомы костей и их коррекция
Одним из главных типов осложнений после выполненных операций являются инфекционные и механические. Данные проблемы являются актуальными не только, для онкоортопедии но и для классической травматологии - ортопедии. Разработаны и внедрены алгоритмы по борьбе с данными типами осложнений.
Особенности реабилитации после лечения саркомы костей
Реабилитация пациентов, которым было проведено хирургическое лечение по поводу опухолевого поражения костей в нашем отделении – является одной из приоритетных задач для врачей нашего центра. Этот процесс включает себя большое количество специалистов: онкологов, врачей ЛФК, неврологов и даже психологов. Хорошее психоэмоциональное состояние пациента, является одним из главных факторов для более быстрой реабилитации больного. Для каждого пациента подбирается индивидуальный план реабилитационных мероприятий. Как правило на 2-3 сутки после операции пациент встает на ноги и начинает получать минимальные нагрузки. C каждым днем нагрузка увеличивается, под чутким контролем врачей. В большинстве случаев пациент, получивший у нас лечение, покидает нас на своих ногах и с огромной мотивацией на быстрое выздоровление.
Прогноз заболевания саркомы костей
Важно понимать, что течение болезни индивидуально и не всегда возможно предугадать его течение. Оно может благоприятным или неблагоприятным, но бывают исключения из правил, как их плохих, так и из хороших. Неблагоприятными факторами, которые могут влиять на выживаемость являются: высокая степень злокачественности, размеры первичной опухоли, локализация опухоли в костях таза и позвоночнике, слабая реакция опухоли не проводимую химиотерапию, выраженная сопутствующая патология. При проведении правильного лечения общая пятилетняя выживаемость больных с высокозлокачественными саркомами костей составляет до 75%. При опухолях низкой степени злокачественности она выше и может достигать 90%.
Филиалы и отделения, в которых лечат саркомы костей
Контакты: (495) 150 11 22
Заведующий отделения: Александр Александрович Курильчик
Контакты: 8 (484) 399 31 30
- Вакансии
- Нормативные документы
- Работа с обращением граждан
- Перечень лекарственных препаратов
- Контролирующие организации
- Политика конфиденциальности
- Виды медицинской помощи
- Как записаться на прием / обследование
- Платные услуги
- Порядок и условия получения медицинской помощи
- О правилах госпитализации
- Дневной стационар
- Психологическая помощь
- Страховые организации
- О предоставлении платных медицинских услуг
- Права пациента
ФГБУ "НМИЦ радиологии"
МНИОИ им. П.А. Герцена
тел.:+7 (495) 150-11-22
НИИ урологии и интервенционной
радиологии им. Н.А. Лопаткина
тел.:+7 (499) 110-40-67
Читайте также:

