С наибольшей скоростью водород реагирует с бромом йодом фтором или хлором












Последнее обновление
4 апреля 2020г.
1. От увеличения площади поверхности соприкосновения реагентов не зависит скорость реакции между
1) серой и железом 2) кремнием и кислородом
3) водородом и кислородом 4) цинком и соляной кислотой
2. На скорость химической реакции 2NH3(г) = N2(г) + 3Н2(г) НЕ влияет изменение
1) концентрации аммиака 2) давления 3) концентрации водорода 4) температуры
3. С наименьшей скоростью происходит реакция между водородом и
1) фтором 2) бромом 3) иодом 4) хлором
4. Для увеличения скорости химической реакции Fe(тв) + 2Н + = Fe 2+ + Н2(г) ↑ необходимо
1) увеличить концентрацию ионов железа 2) уменьшить температуру
3) добавить несколько кусочков железа 4) увеличить концентрацию кислоты
5. С наибольшей скоростью происходит реакция между водородом и
1) бромом 2) иодом 3) фтором 4) хлором
6. При комнатной температуре водород наиболее активно реагирует с
1) серой 2) азотом 3) фтором 4) бромом
7. Скорость реакции между железом и раствором серной кислоты будет уменьшаться при
1) повышении температуры 2) разбавлении кислоты
3) увеличении концентрации кислоты 4) размельчении железа
8. Для увеличения скорости реакции гидролиза этилацетата необходимо
1) добавить уксусную кислоту 2) добавить этанол
3) нагреть раствор 4) увеличить давление
9. С наибольшей скоростью при обычных условиях происходит взаимодействие воды с
1) оксидом кальция 2) железом 3) оксидом кремния (IV) 4) алюминием
10. Скорость химической реакции CaO(тв) + 3C(тв) = CaC2(тв) + CO(г)↑ увеличивается при
1) повышении концентрации СО 2) понижении температуры
3) повышении давления 4) повышении температуры
11. Увеличение концентрации азота увеличивает скорость реакции
12. Скорость реакции цинка с соляной кислотой НЕ зависит от
1) концентрации кислоты 2) температуры 3) давления 4) площади поверхности соприкосновения реагентов
13. С наименьшей скоростью при комнатной температуре протекает реакция между
1) Na и O2 2) CO и O2 3) CaO и H2O 4) NH3 и HCl
14. Скорость химической реакции Р4(тв) + 5О2(г) = Р4О10 увеличивается при
1) добавлении фосфора 2) увеличении концентрации кислорода
3) увеличении концентрации оксида фосфора (V) 4) уменьшении давления
15. Увеличению скорости химической реакции Fe + S = FeS способствует
1) повышение давления 2) охлаждение реакционной смеси
3) добавление серы 4) повышение температуры
16. С наибольшей скоростью протекает реакция между
1) AgNO3(р-р) и NaCl(р-р) 2) CaCO3 и HCl(р-р) 3) Zn и H2SO4 4) Mg и O2
17. С наибольшей скоростью при комнатной температуре протекает реакция
1) CH3COOH(р-р) с NaOH(р-р) 2) C2H5OH(ж) с Na 3) CH3Cl(г) с Na 4) C6H5OH(тв) с NaOH(р-р)
18. Для увеличения скорость химической реакции Cr(тв) + 2H + (р-р) = Сr 2+ + H2(г) необходимо
1) увеличить количество хрома 2) увеличить концентрацию ионов водорода
3) уменьшить температуру 4) увеличить концентрацию водорода
19. С наибольшей скоростью соляная кислота взаимодействует с
1) металлическим цинком 2) раствором гидроксида натрия
3) металлическим железом 4) твердым карбонатом железа (II)
20. Скорость химической реакции Mg(тв) + 2HCl(р-р) = MgCl2 + H2↑ НЕ зависит от
1) концентрации хлороводородной кислоты 2) температуры
3) концентрации водорода 4) степени измельчения магния
21. Какое утверждение правильно характеризует роль катализатора в химической реакции?
1) Катализатор вступает в реакцию с исходными веществами и расходуется в результате реакции.
2) Катализатор увеличивает тепловой эффект реакции.
3) Катализатор ускоряет как прямую, так и обратную реакции.
4) Катализатор смещает равновесие в сторону реагентов.
22. Скорость реакции оксида углерода (II) с кислородом уменьшается при
1) нагревании 2) пропускании газов над нагретой платиной
3) добавлении углекислого газа 4) увеличении объема реакционного сосуда
23. Скорость химической реакции Р4(тв) + 5О2(г) = Р4О10 зависит от
1) количества взятого фосфора 2) температуры
3) концентрации оксида фосфора (V) 4) объема взятого кислорода
24. Скорость реакции азота с водородом увеличится при
1) пропускании смеси над нагретым железом 2) добавлении аммиака
3) охлаждении смеси 4) увеличении объема реакционного сосуда
25. Скорость реакции азота с водородом НЕ зависит от
1) температуры 2) катализатора 3) давления 4) количества продукта реакции
26. Увеличение скорости химической реакции 2Fe + 3Cl2(г) = 2FeCl3 способствует:
1) понижение давления 2) уменьшение концентрации хлора
3) охлаждение системы 4) повышение температуры
27. Скорость реакции между цинком и раствором соляной кислоты уменьшится, если
1) нагреть реакционную смесь 2) разбавить кислоту
3) пропустить через реакционную смесь хлороводород 4) использовать цинковый порошок
28. При комнатной температуре с наибольшей скоростью с водой реагирует
1) калий 2) кальций 3) магний 4) алюминий
29. Для увеличения скорости реакции гидролиза 1-бромпропана необходимо
1) добавить кислоту 2) понизить концентрацию 1-бромпропана
3) повысить температуру 4) повысить концентрацию пропанола
30. Скорость реакции между магнием и раствором медного купороса НЕ зависит от
1) площади поверхности соприкосновения реагентов 2) температуры
3) объема реакционного сосуда 4) концентрации соли
Химические свойства водорода
Атом водорода имеет электронную формулу внешнего (и единственного) электронного уровня 1s 1 . С одной стороны, по наличию одного электрона на внешнем электронном уровне атом водорода похож на атомы щелочных металлов. Однако, ему, так же как и галогенам не хватает до заполнения внешнего электронного уровня всего одного электрона, поскольку на первом электронном уровне может располагаться не более 2-х электронов. Выходит, что водород можно поместить одновременно как в первую, так и в предпоследнюю (седьмую) группу таблицы Менделеева, что иногда и делается в различных вариантах периодической системы:
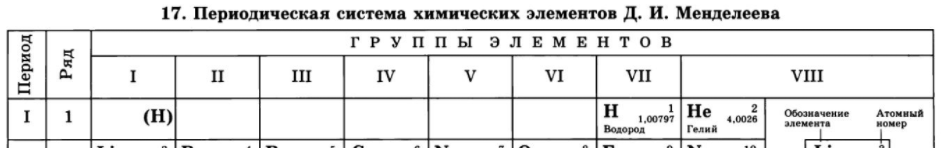
С точки зрения свойств водорода как простого вещества, он, все-таки, имеет больше общего с галогенами. Водород, также как и галогены, является неметаллом и образует аналогично им двухатомные молекулы (H2).
В обычных условиях водород представляет собой газообразное, малоактивное вещество. Невысокая активность водорода объясняется высокой прочностью связи между атомами водорода в молекуле, для разрыва которой требуется либо сильное нагревание, либо применение катализаторов, либо и то и другое одновременно.
Из металлов водород реагирует только с щелочными и щелочноземельными! К щелочным металлам относятся металлы главной подгруппы I-й группы (Li, Na, K, Rb, Cs, Fr), а к щелочно-земельным — металлы главной подгруппы II-й группы, кроме бериллия и магния (Ca, Sr, Ba, Ra)
При взаимодействии с активными металлами водород проявляет окислительные свойства, т.е. понижает свою степень окисления. При этом образуются гидриды щелочных и щелочноземельных металлов, которые имеют ионное строение. Реакция протекает при нагревании:
Следует отметить, что взаимодействие с активными металлами является единственным случаем, когда молекулярный водород Н2 является окислителем.
Из неметаллов водород реагирует только c углеродом, азотом, кислородом, серой, селеном и галогенами!
Под углеродом следует понимать графит или аморфный углерод, поскольку алмаз — крайне инертная аллотропная модификация углерода.
При взаимодействии с неметаллами водород может выполнять только функцию восстановителя, то есть только повышать свою степень окисления:
Водород не реагирует с оксидами металлов, находящихся в ряду активности металлов до алюминия (включительно), однако, способен восстанавливать многие оксиды металлов правее алюминия при нагревании:
Из оксидов неметаллов водород реагирует при нагревании с оксидами азота, галогенов и углерода. Из всех взаимодействий водорода с оксидами неметаллов особенно следует отметить его реакцию с угарным газом CO.
С неорганическими кислотами водород не реагирует!
Из органических кислот водород реагирует только с непредельными, а также с кислотами, содержащими функциональные группы способные к восстановлению водородом, в частности альдегидные, кето- или нитрогруппы.
В случае водных растворов солей их взаимодействие с водородом не протекает. Однако при пропускании водорода над твердыми солями некоторых металлов средней и низкой активности возможно их частичное или полное восстановление, например:
Химические свойства галогенов
Галогенами называют химические элементы VIIA группы (F, Cl, Br, I, At), а также образуемые ими простые вещества. Здесь и далее по тексту, если не сказано иное, под галогенами будут пониматься именно простые вещества.
Все галогены имеют молекулярное строение, что обусловливает низкие температуры плавления и кипения данных веществ. Молекулы галогенов двухатомны, т.е. их формулу можно записать в общем виде как Hal2.
Следует отметить такое специфическое физическое свойство йода, как его способность к сублимации или, иначе говоря, возгонке. Возгонкой, называют явление, при котором вещество, находящееся в твердом состоянии, при нагревании не плавится, а, минуя жидкую фазу, сразу же переходит в газообразное состояние.
Электронное строение внешнего энергетического уровня атома любого галогена имеет вид ns 2 np 5 , где n – номер периода таблицы Менделеева, в котором расположен галоген. Как можно заметить, до восьмиэлектронной внешней оболочки атомам галогенов не хватает всего одного электрона. Из этого логично предположить преимущественно окисляющие свойства свободных галогенов, что подтверждается и на практике. Как известно, электроотрицательность неметаллов при движении вниз по подгруппе снижается, в связи с чем активность галогенов уменьшается в ряду:
Все галогены являются высокоактивными веществами и реагируют с большинством простых веществ. Однако, следует отметить, что фтор из-за своей чрезвычайно высокой реакционной способности может реагировать даже с теми простыми веществами, с которыми не могут реагировать остальные галогены. К таким простым веществам относятся кислород, углерод (алмаз), азот, платина, золото и некоторые благородные газы (ксенон и криптон). Т.е. фактически, фтор не реагирует лишь с некоторыми благородными газами.
Остальные галогены, т.е. хлор, бром и йод, также являются активными веществами, однако менее активными, чем фтор. Они реагируют практически со всеми простыми веществами, кроме кислорода, азота, углерода в виде алмаза, платины, золота и благородных газов.
При взаимодействии всех галогенов с водородом образуются галогеноводороды с общей формулой HHal. При этом, реакция фтора с водородом начинается самопроизвольно даже в темноте и протекает со взрывом в соответствии с уравнением:
Реакция хлора с водородом может быть инициирована интенсивным ультрафиолетовым облучением или нагреванием. Также протекает со взрывом:
Бром и йод реагируют с водородом только при нагревании и при этом, реакция с йодом является обратимой:
Взаимодействие фтора с фосфором приводит к окислению фосфора до высшей степени окисления (+5). При этом происходит образование пентафторида фосфора:
При взаимодействии хлора и брома с фосфором возможно получение галогенидов фосфора как в степени окисления + 3, так и в степени окисления +5, что зависит от пропорций реагирующих веществ:
При этом в случае белого фосфора в атмосфере фтора, хлора или жидком броме реакция начинается самопроизвольно.
Взаимодействие же фосфора с йодом может привести к образованию только триодида фосфора из-за существенно меньшей, чем у остальных галогенов окисляющей способности:
Фтор окисляет серу до высшей степени окисления +6, образуя гексафторид серы:
Хлор и бром реагируют с серой, образуя соединения, содержащие серу в крайне не свойственных ей степенях окисления +1 и +2. Данные взаимодействия являются весьма специфичными, и для сдачи ЕГЭ по химии умение записывать уравнения этих взаимодействий не обязательно. Поэтому три нижеследующих уравнения даны скорее для ознакомления:
Как уже было сказано выше, фтор способен реагировать со всеми металлами, даже такими малоактивными как платина и золото:
Остальные галогены реагируют со всеми металлами кроме платины и золота:
Более активные галогены, т.е. химические элементы которых расположены выше в таблице Менделеева, способны вытеснять менее активные галогены из образуемых ими галогеноводородных кислот и галогенидов металлов:
Аналогичным образом, бром вытесняет серу из растворов сульфидов и сероводорода:
Хлор является более сильным окислителем и окисляет сероводород в его водном растворе не до серы, а до серной кислоты:
Вода горит во фторе синим пламенем в соответствии с уравнением реакции:
Бром и хлор реагируют с водой иначе, чем фтор. Если фтор выступал в роли окислителя, то хлор и бром диспропорционируют в воде, образуя смесь кислот. При этом реакции обратимы:
Взаимодействие йода с водой протекает в настолько ничтожно малой степени, что им можно пренебречь и считать, что реакция не протекает вовсе.
Фтор при взаимодействии с водным раствором щелочи опять же выступает в роли окислителя:
Умение записывать данное уравнение не требуется для сдачи ЕГЭ. Достаточно знать факт о возможности такого взаимодействия и окислительной роли фтора в этой реакции.
а при нагревании:
Йод реагирует с щелочами исключительно по второму варианту, т.е. с образованием йодата, т.к. гипоиодит не устойчив не только при нагревании, но также при обычной температуре и даже на холоду:
Фтор – газ светло-зеленого цвета (tпл = — 220 о С tкип = — 188 о С). По поводу истинного цвета фтора возникало немало разногласий: из-за необычайно высокой реакционной способности редко кто осмеливался получать его в достаточном количестве в прозрачном сосуде. Но последующие исследования подтвердили окраску фтора, о которой сообщал ещё Муассан.

Фтор в запаянной ампуле
Фтор взаимодействует почти со всеми простыми веществами, включая тяжелые инертные газы (Kr, Xe). В его атмосфере загорается даже стекловата (SiO2 + 2F2 = 4HF + O2) и вода (2H2O + 2F2 = 4HF + O2). При этом наряду с кислородом в продуктах реакции присутствуют фториды кислорода OF2, O2F2 и озон O3.
Фтор используют для получения некоторых ценных фторпроизводных углеводородов, обладающих уникальными свойствами, как, например, смазочных веществ, выдерживающих высокую температуру, пластической массы, стойкой к химическим реагентам (тефлон), жидкостей для холодильников (фреонов).
В организме человека фтор содержится в виде нерастворимых фторидов, главным образом фторапатита, и входит в состав костной ткани и зубной эмали. Для укрепления эмали рекомендуют использовать специальные фторсодержащие зубные пасты. С этой же целью фторируют питьевую воду, доводя концентрацию фторид-ионов примерно до 1 мг/л. Однако следует помнить, что в больших количествах растворимые в воде фториды ядовиты.
Фториды – соли слабой плавиковой кислоты HF, представляющей собой водный раствор фтороводорода. Молекулы HF в плавиковой кислоте связаны друг с другом настолько прочными водородными связями, что ее состав правильнее было бы передать формулой (HF)n. Поскольку эта кислота (наряду с газообразным фтороводородом) обладает уникальной способностью разъедать стекло, её хранят в полиэтиленовой, свинцовой или парафиновой посуде.
Применение фтористого водорода довольно разнообразно. Безводный HF используют, главным образом, при органических синтезах, а плавиковую кислоту – при получении фторидов, травления стекла, удалении песка с металлических отливок, при анализах минералов и т.д.
Физические свойства
При обычных условиях хлор – газ жёлто-зеленого цвета с резким запахом. Он в 2,5 раза тяжелее воздуха, ядовит. Вдыхание даже небольших количеств хлора вызывает раздражение дыхательных путей и кашель. В одном объёме воды при 20 о С растворяется 2,5 объема хлора. Раствор хлора в воде называется хлорной водой.
Нахождение в природе
Хлор в природе в свободном состоянии практически не встречается. Широко распространены его соединения: каменная соль NaCl, сильвинит KCl ∙ NaCl и карналлит KCl ∙ MgCl2. Большое количество хлоридов содержится в морской воде. Хлор входит в состав зеленого вещества растений – хлорофилла.

Минерал сильвинит
Получение
В промышленности хлор получают электролизом водного раствора или расплава хлорида натрия:
В лаборатории хлор можно получить действием концентрированной соляной кислоты (при нагревании) на различные окислители, такие как оксид марганца (IV) MnO2, перманганат калия KMnO4, бертолетова соль KClO3 и др.:
Химические свойства
Хлор – химически активное вещество, взаимодействует с простыми и сложными веществами.
Взаимодействие с простыми веществами
Как сильный окислитель хлор реагирует:
в) с некоторыми менее электроотрицательными неметаллами:
С кислородом и азотом хлор непосредственно не взаимодействует.
Взаимодействие со сложными веществами
а) Реакция взаимодействия хлора с водой идет в две стадии. На первой стадии процесса образуются две кислоты – соляная HCl и хлорноватистая HClO:
Затем происходит процесс разложения хлорноватистой кислоты:
HClO = HCl + [O]→ атомарный кислород
Образованием атомарного кислорода объясняется окисляющее и отбеливающее действие хлора в воде. В хлорной воде погибают микроорганизмы. Органические красители, помещенные в хлорную воду, обесцвечиваются.
б) Обратите внимание, что с кислотами хлор не реагирует.
в) Взаимодействие хлора с растворами щелочей происходит по-разному в зависимости от условий протекания реакции:
на холоде: Cl2 + 2NaOH = NaCl + NaClO + H2O
при нагревании: 3Cl2 + 6KOH = 5KCl + KClO3 + 3H2O
г) Хлор взаимодействует с бромидами и йодидами металлов:
С фторидами металлов хлор не реагирует, так как его окислительная способность ниже окислительной способности фтора:
д) Хлор легко взаимодействует со многими органическими веществами, например с метаном, бензолом и др.:
Хлороводород и соляная кислота
Хлороводород HCl – бесцветный газ с резким запахом, в воде хорошо растворяется, при 0 о С в 1 л воды растворяется около 400 л HCl. Раствор хлороводорода в воде имеет кислую реакцию и называется хлороводородной, или соляной кислотой. Соляная кислота является сильной кислотой, обладает всеми общими свойствами кислот.
Соляная кислота – активный химический реагент, она взаимодействует:
HCl + NaOH = NaCl + H2O

Реакция соляной кислоты с цинком
- с металлами, которые находятся в ряду напряжений до водорода:
Последняя реакция является качественной реакцией на хлорид-ион.
Хлороводород можно получать:
а) прямым синтезом водорода и хлора;
б) действием концентрированной серной кислоты на твердые хлориды, например:
(Отметим, что аналогичным способом можно получать HF, но нельзя получить HBr и HI, так как они являются сильными восстановителями и окисляются серной кислотой до свободных брома и йода).
Применение хлора и хлороводорода. Физиологическая роль соляной кислоты в организме человека
Хлор используется для отбеливания бумаги и тканей, в производстве пластмасс, для дезинфекции питьевой воды. Хлор является исходным веществом при получении таких важнейших продуктов, как хлорная известь, фосген, хлороформ, определенные виды моющих средств, ядохимикатов, каучуков и т.д. Огромное количество хлора используется для синтеза хлороводорода, растворением которого в воде получают соляную кислоту.
В организме человека соляная кислота вырабатывается клетками слизистой желудка. Она играет важную физиологическую роль, так как способствует перевариванию белков и убивает различные болезнетворные бактерии.
Скачать рефераты по другим темам можно здесь
*на изображении записи фотография сильвинитовой шахты
Галогены (греч. hals - соль + genes - рождающий) - химические элементы VIIa группы: F, Cl, Br, I, At. Реагируют с большинством других элементов и органических соединений.
Галогены широко распространены в природе. Их химическая активность падает от фтора к астату.

От F к At (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Все галогены относятся к неметаллам, являются сильными окислителями.
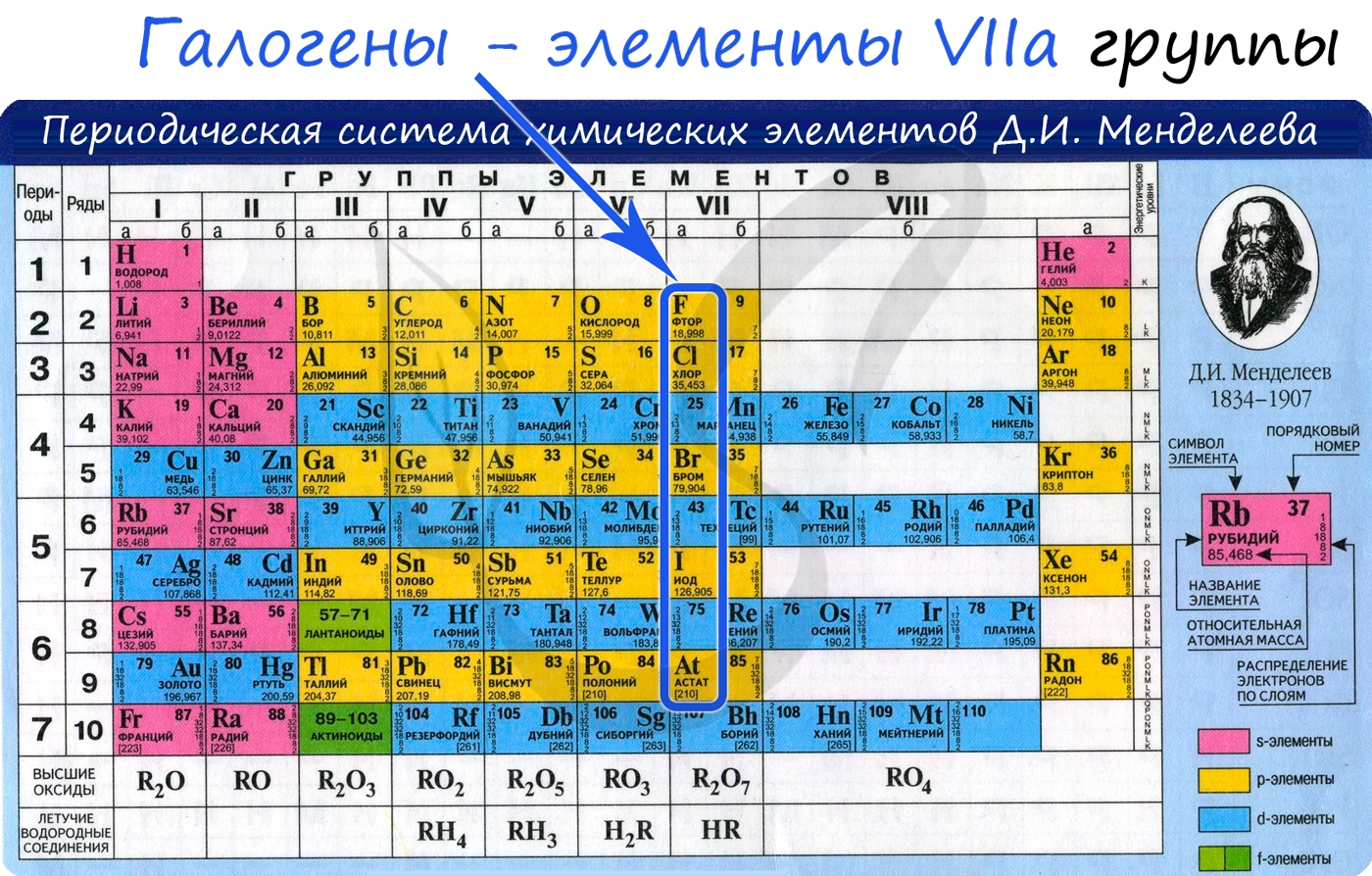
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 np 5 :
- F - 2s 2 2p 5
- Cl - 3s 2 3p 5
- Br - 4s 2 4p 5
- I - 5s 2 5p 5
- At - 6s 2 6p 5
Для галогенов характерны нечетные степени окисления: -1, +1, +3, +5, +7. Это связано с электронной конфигурацией атомов в возбужденном состоянии.

- NaCl - галит (каменная соль)
- CaF2 - флюорит, плавиковый шпат
- NaCl*KCl - сильвинит
- 3Ca3(PO4)2*CaF2 - фторапатит
- MgCl2*6H2O - бишофит
- KCl*MgCl2*6H2O - карналлит

Галогены в чистом виде можно получить путем электролиза водных растворов и расплавов их солей. Например, хлор в промышленности получают электролизом водного раствора хлорида натрия.
Электролизом расплава гидрофторида калия KHF2 в безводной плавиковой кислоте - HF - был впервые получен фтор.
Более активные галогены способны вытеснять менее активные. Активность галогенов убывает: F → Cl → Br → I.

В лабораторных условиях галогены могут быть получены следующими реакциями.
-
Реакции с металлами
Для галогенов характерна высокая реакционная способность. Фтор реагирует со всеми металлами без исключения, некоторые из них в атмосфере фтора самовоспламеняются.
Реакции с неметаллами
Хлор, как и фтор, химически весьма активен. Не реагирует только с кислородом, азотом и благородными газами.

F2 + H2 → HF (в темноте со взрывом)
Галогены вступают в реакцию друг с другом. Чтобы определить степени окисления в получающихся соединениях, вспомните электроотрицательность ;)
Br2 + F2 → BrF (фтор более электроотрицателен, чем бром - F - )
Br2 + I2 → IBr3 (бром более электроотрицателен, чем йод - Br - )
Реакции с водой
Реакция фтора с водой протекает очень энергично, носит взрывной характер.
Хлор реагирует с водой обратимо, образуя хлорную воду - смесь хлорноватистой и соляной кислоты. Бром вступает в те же реакции, что и хлор.

Замечу, что активность йода существенно ниже, чем у остальных галогенов. С неметаллами йод почти не реагирует, а с металлами - только при нагревании.
Реакции с щелочами
Cl2 + NaOH → NaCl + NaClO + H2O
Галогены способны вытеснять друг друга из солей. Более активные вытесняют менее активные.
KBr + I2 ⇸ (реакция не идет, так как йод менее активен, чем бром)
Соединения, образованные из галогенов и водорода. К галогеноводородам относятся следующие вещества:
- HF - фтороводород (газ), фтороводородная (плавиковая) кислота (жидкость)
- HCl - хлороводород (газ), соляная кислота (жидкость)
- HBr - бромоводород, бромоводородная кислота
- HI - йодоводород, йодоводородная кислота
- HAt - астатоводород, астатоводородная кислота
При н.у. HCl, HBr, HI - газы, хорошо растворимые в воде.
В промышленности применяют получение прямым методом: реакцией водорода с галогенами.
В лабораторных условиях галогеноводороды можно получить в реакциях обмена между галогенсодержащими солями и сильными кислотами.
HF - является слабой кислотой, HCl, HBr, HI - сильные кислоты. Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.

Галогеноводороды реагируют с основными, амфотерными оксидами и основаниями с образованием соответствующих солей.
KOH + HCl → KCl + H2O (реакция нейтрализации)

Реакции протекают в тех случаях, если в результате выпадает осадок, выделяется газ или образуется слабый электролит (вода).
В некоторых реакциях проявляют себя как сильные восстановители, особенно HI.

В целом взаимодействие галогеноводородов с оксидами неметаллов нехарактерно. В этой связи важно выделить реакцию SiO2 с плавиковой кислотой.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Читайте также:

