Роста новых сосудов при раке
По сосудам поступает питание для всех органов и тканей организма. Ангиогенез опухоли – это способность рака обеспечивать собственное кровоснабжение за счет формирования новой сосудистой сети: без питательных веществ и кислорода раковые клетки погибнут, поэтому создание опухолью новых артерий – необходимое и обязательное условие роста злокачественного новообразования.
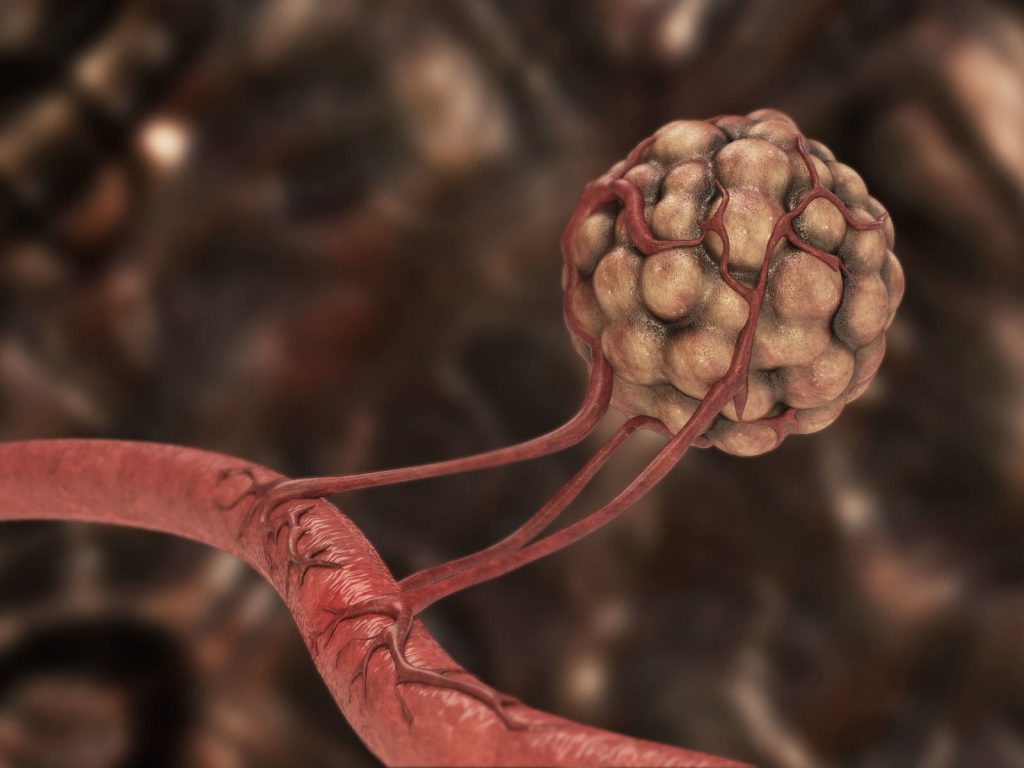
Кровоснабжение ракового очага
Ангиогенез опухоли – что это такое
У здорового взрослого человека новые сосуды не образуются – в сформировавшемся организме в этом нет никакой необходимости. В норме появление и рост новых артерий и вен происходит в следующих ситуациях:
- В период эмбриогенеза, при беременности у плода и в первые месяцы жизни ребенка;
- При регенерации тканей на фоне травмы или после операции.
Ангиогенез опухоли – это патологический вариант возникновения новой сосудистой сети, возможный за счет стимулирующего действия злокачественного новообразования на имеющиеся мелкие капилляры и артерии. На первом этапе формирования ракового очага злокачественные клетки получают питание и кислород из окружающих тканей, но этот бессосудистый механизм опухолевого роста возможен только до величины узла в 1-2 мм. Затем, если нет собственных сосудов, в опухоли происходят следующие события:
- некроз всей или локального участка новообразования;
- апоптоз раковых клеток;
- переход в дремлющее состояние.
Механизм формирования сосудов в опухоли
Любой кровеносный сосуд состоит из клеток эндотелия. Это самые стабильные и долгоживущие клетки в живом организме, которые не обновляются длительное время (в кишечнике в каждый момент времени происходит обновление 14% клеток кишечной стенки, а в сосудах – 0.01%). Состояние покоя определяет стабильность системы: без определенного стимулирующего влияния никаких новых капилляров и артерий не будет. Ангиогенез опухоли – это прямое и выраженное воздействие раковой опухоли на эндотелий сосудов, которые находятся рядом с новообразованием. Включение механизма формирования капилляров в опухоли происходит при создании определенных условий и при обязательной величине новообразования в 1-2 мм. Основные этапы ангиогенеза:
- Активация эндотелия стимуляторами злокачественного новообразования;
- Пролиферация эндотелиальных клеток;
- Миграция эндотелия (перемещение) в опухоль;
- Появление и рост кровеносного сосуда.
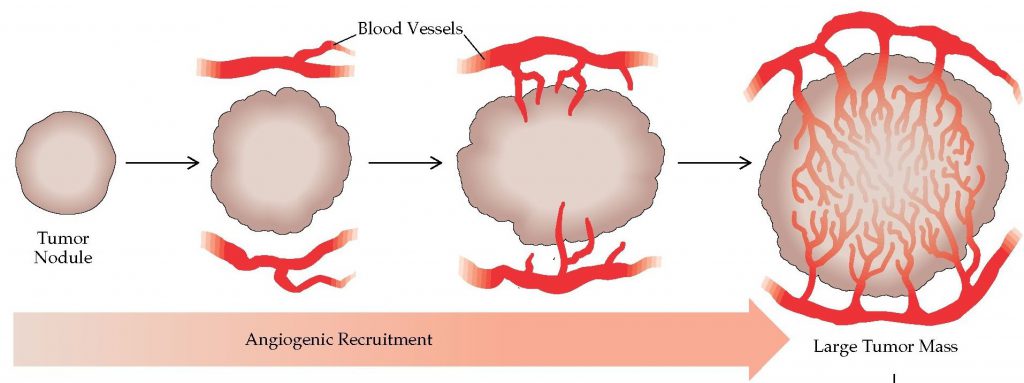
Механизм ангиогенеза опухолевого очага
Прогностическое значение ангиогенеза для рака
Необходимо понимать – ангиогенез опухоли является важнейшим фактором опухолевого роста: если в очаге рака стали формироваться новые капилляры, то можно ожидать в ближайшее время появление первых признаков заболевания с быстрым увеличением размеров злокачественного новообразования. И что самое худшее – появление новых артерий открывает ворота для метастазирования: раковые клетки из первичного очага могут устремиться в путешествие по организму, захватывая новые территории, расселяясь по органам и тканям, что резко снижает вероятность благоприятного прогноза для выздоровления.
Доктор медицинских наук В. ПРОЗОРОВСКИЙ.
Хотя post factum многое представляется само собой разумеющимся, но прошло немало лет, прежде чем медики догадались, что для интенсивного размножения опухолевых клеток нужны кислород и питательные вещества, поэтому быстрорастущая злокачественная опухоль требует крови больше, чем, скажем, липома, доброкачественная опухоль из жировой ткани. А значит, по мере развития раковая опухоль должна прорастать новыми кровеносными сосудами.
В 1971 году появилась статья американского хирурга Джуды Фолкмана, в которой впервые было высказано предположение, что рост опухолей, превышающих в диаметре несколько миллиметров, возможен только в случае формирования и прорастания в них мелких капилляров. В 1982 году американские ученые Ваупель, Каллиновски и Окуниефф показали, что во всех злокачественных опухолях действительно идет интенсивное новообразование сосудов. Верно и обратное — если образование новых сосудов прекращается, то дальнейший рост опухоли становится невозможен.
Открытие Фолкмана послужило началом целой череды научных достижений, в результате которых на свет явилась стройная теория ангиогенеза. Согласно ей образование сосудов в раковой опухоли, так же как и в любой поврежденной ткани, протекает в несколько стадий. Что же побуждает организм образовывать новые капилляры?
АКТИВАТОРЫ РОСТА НОВЫХ СОСУДОВ
Факторы роста совершенно необходимы здоровому организму для восстановления кровотока при различных повреждениях, но их избыток может стать роковым для онкологического больного. Повышение синтеза ФРЭС стимулирует метастазирование опухолей — под воздействием этого вещества раковые клетки выходят в кровяное русло и распространяются по всему организму. С другой стороны, ФРЭС играет и положительную роль — прорастающие в опухоли сосуды формируют в ней своеобразный мягкий скелет, который удерживает клетки на месте, не давая им метастазировать.
Кстати, при недостатке кислорода выработка ФРЭС и других факторов роста усиливается — ведь организму нужно скомпенсировать гипоксию увеличением кровотока. Отсюда можно сделать вывод об увеличении риска онкологических заболеваний при снижении концентрации кислорода в воздухе из-за уничтожения зеленых насаждений, загрязнения окружающей среды и т.д. Также доказано, что молекулы, вырабатывающиеся в организме человека при стрессе, одновременно стимулируют синтез ФРЭС. Этот факт наводит на мысли о пагубной роли нер-вного напряжения в возникновении раковых опухолей.
ВЕЩЕСТВА, ПРЕПЯТСТВУЮЩИЕ РОСТУ НОВЫХ СОСУДОВ
По счастью, помимо молекул, способствующих прорастанию опухоли сосудами, в организме синтезируются и собственные факторы, препятствующие росту сосудов (ингибиторы). В здоровом организме существует баланс между активаторами и ингибиторами роста новых кровеносных сосудов. При многих серьезных заболеваниях организм как бы теряет контроль над поддержанием этого равновесия. Смещение равновесия в сторону избыточного формирования новых сосудов происходит при онкологических заболеваниях, диабете, ревматоидном артрите и т.д. При таких опасных недугах, как заболевания коронарных артерий, инсульт, напротив, скорость роста новых сосудов явно ниже нормы.
Первым известным природным веществом, тормозящим рост новых сосудов, стал гликопротеин тромбоспондин, вырабатываемый различными клетками, в том числе и клетками стенок кровеносных сосудов. Тромбоспондин тормозит размножение и прикрепляемость эндотелиальных клеток, сдерживая таким путем рост капилляров.
В 1997 году тот же О’Рейли при исследовании культуры клеток злокачественной опухоли гемангиоэндотелиомы выделил еще один мощный блокатор формирования кровеносных сосудов — эндостатин. Это вещество является частью молекулы полипептида коллагена. Эндостатин активирует программируемую гибель эндотелиальных клеток и, вероятно, тормозит процесс их активации, размножения и миграции.
Помимо тромбоспондина, ангиостатина и эндостатина в органах и тканях животных исследователи обнаружили множество веществ, которые подавляют рост капилляров. К таким веществам относятся некоторые гормоны, фрагменты гепарина и др. Из известных природных ингибиторов можно назвать интерфероны, которые, кстати, борются и с вирусами. Однако как названные вещества, так и многие другие свойственные организму продукты обмена веществ обладают многофункциональным действием и из-за побочных эффектов не могут быть использованы в качестве лекарственных препаратов. Тем не менее интерес ученых к этой группе соединений не ослабевает.
"СОСУДИСТЫЙ" ПОДХОД К ЛЕЧЕНИЮ РАКА
Долгое время противораковая терапия была направлена лишь на подавление роста опухолевых клеток и усиление иммунного ответа. Сейчас уже ясно, что без формирования новых сосудов не может быть роста злокачественных опухолей. Лишенные возможности стимулировать образование новых капилляров, первичные и метастатические опухоли перестают расти. Поэтому появился новый класс ангиостатиков, то есть лекарств, тормозящих прорастание новых кровеносных сосудов. Такие соединения очень перспективны для борьбы со злокачественными опухолями на любой стадии их развития. Более того, существующие сейчас препараты эффективны по отношению к определенным опухолям, а блокаторы роста сосудов могут стать универсальным средством противораковой терапии, причем тем более эффективными, чем злокачественнее опухоль.
По противоопухолевой активности другой природный ингибитор — эндостатин сильнее, чем ангиостатин. Уже в малых дозах он предотвращает метастазирование крупных опухолей, а в больших — оказывает мощное тормозящее действие на рост первичных опухолей, таких, как карциномы, саркомы и меланома, вызывая в некоторых случаях их полную гибель. Очевидно, после разработки методов получения ангиостатина и эндостатина в промышленных масштабах эти препараты получат широкое клиническое применение, поскольку существенных побочных реакций при их использовании даже в больших дозах пока не выявлено.
Первый класс веществ, которые сейчас испытываются в качестве противоопухолевых препаратов, — соединения, непосредственно блокирующие рост эндотелиальных клеток. К этой категории веществ относится уже упомянутый природный белок эндостатин. Его синтетический аналог комбрестатин А4 — химическая модификация соединения, содержащегося в древесине южноафриканского дерева Combretum caffrum, — проходит клинические испытания. Препарат также проявляет способность подавлять размножение клеток сосудов, стимулируя клеточный апоптоз. В настоящее время большое внимание уделяется созданию веществ, блокирующих размножение уже активированных клеток эндотелия. Из них наиболее удачным по активности и малой токсичности является синтетический препарат TNP-470, прошедший клинические испытания при раке почек, шейки матки и саркоме Капоши.
Ко второй группе препаратов, тормозящих рост сосудов, относятся природные или синтетические вещества, так или иначе блокирующие передачу сигнала на рецепторы факторов роста. Как уже было сказано, ФРЭС взаимодействует с эндотелиальными клетками посредством специальных белковых структур — рецепторов. Клетки здорового организма к этим веществам — блокаторам рецепторов нечувствительны. Клинические испытания проходят препараты антител к ФРЭС, которые эффективно блокируют рецепторы ФРЭС, не давая молекуле фактора роста запустить биохимический каскад, приводящий к прорастанию новых сосудов. Уже понятно, что лекарственные препараты на основе антител замедляют опухолевый рост и продлевают жизнь пациентам. Фактически антитела к ФРЭС — пока единственное антиангиогенное лекарство, уже появившееся на мировом фармацевтическом рынке. Ученые также синтезировали несколько молекул — аналогов ФРЭС, блокирующих рецепторы. Эти вещества тестируются в онкологических клиниках.
На стадии клинических испытаний находится и печально известный препарат талидомид. Почти полвека тому назад он применялся в качестве снотворного, но вызывал уродства плода у беременных женщин. Как случайно выяснилось впоследствии, это было связано с нарушением образования необходимых для роста плода сосудов, хотя механизм действия соединения так и остался до конца не выясненным. Талидомид оказался эффективным при лечении больных миеломой, раком простаты и легких, саркомой и ганглиобластомой.
К третьей группе веществ, подавляющих прорастание сосудов, а следовательно, и рост опухоли, относятся блокаторы (ингибиторы) активности опухолевых ферментов — металлопротеаз, которые разрушают внеклеточный матрикс и оболочку сосуда, давая клеткам эндотелия возможность мигрировать в сторону опухоли. В недавнее время созданы вещества, которые блокируют ионы металлов, входящих в активный центр ферментов, выводя ферменты опухоли из строя и тем лишая ее способности расти. Разработка препаратов такого типа действия — приномастата, маримастата и СOL-3 — находится на стадии клинических испытаний.

В 1628 году английский врач Уильям Гарвей открыл кровообращение, а спустя некоторое время, в 1661 году, итальянский медик Марчелло Мальпиги — мельчайшие сосудики, капилляры, соединяющие артерии и вены у животных и человека. Сегодня наука о сердечно-сосудистой системе, ее функциях, заболеваниях — одна из ключевых в медицине, однако лишь недавно, в конце ХХ века, ученым пришло в голову, что кровеносные сосуды играют важную роль и в опухолевом росте. Теперь уже никто из медиков не сомневается, что раковая опухоль не может расти без постоянно образующихся вокруг нее новых сосудов.
Хотя post factum многое представляется само собой разумеющимся, но прошло немало лет, прежде чем медики догадались, что для интенсивного размножения опухолевых клеток нужны кислород и питательные вещества, поэтому быстрорастущая злокачественная опухоль требует крови больше, чем, скажем, липома, доброкачественная опухоль из жировой ткани. А значит, по мере развития раковая опухоль должна прорастать новыми кровеносными сосудами .
В 1971 году появилась статья американского хирурга Джуды Фолкмана, в которой впервые было высказано предположение, что рост опухолей, превышающих в диаметре несколько миллиметров, возможен только в случае формирования и прорастания в них мелких капилляров. В 1982 году американские ученые Ваупель, Каллиновски и Окуниефф показали, что во всех злокачественных опухолях действительно идет интенсивное новообразование сосудов. Верно и обратное — если образование новых сосудов прекращается, то дальнейший рост опухоли становится невозможен.
Открытие Фолкмана послужило началом целой череды научных достижений, в результате которых на свет явилась стройная теория ангиогенеза. Согласно ей образование сосудов в раковой опухоли, так же как и в любой поврежденной ткани, протекает в несколько стадий. Что же побуждает организм образовывать новые капилляры?

Американский хирург Джуда Фолкман более 30 лет назад впервые высказал гипотезу о том, что если каким-либо способом прекратить рост сосудов, питающих опухоль, то ее дальнейшее развитие и метастазирование прекратятся.
АКТИВАТОРЫ РОСТА НОВЫХ СОСУДОВ
Факторы роста совершенно необходимы здоровому организму для восстановления кровотока при различных повреждениях, но их избыток может стать роковым для онкологического больного. Повышение синтеза ФРЭС стимулирует метастазирование опухолей — под воздействием этого вещества раковые клетки выходят в кровяное русло и распространяются по всему организму. С другой стороны, ФРЭС играет и положительную роль — прорастающие в опухоли сосуды формируют в ней своеобразный мягкий скелет, который удерживает клетки на месте, не давая им метастазировать .
Кстати, при недостатке кислорода выработка ФРЭС и других факторов роста усиливается — ведь организму нужно скомпенсировать гипоксию увеличением кровотока. Отсюда можно сделать вывод об увеличении риска онкологических заболеваний при снижении концентрации кислорода в воздухе из-за уничтожения зеленых насаждений, загрязнения окружающей среды и т.д. Также доказано, что молекулы, вырабатывающиеся в организме человека при стрессе, одновременно стимулируют синтез ФРЭС. Этот факт наводит на мысли о пагубной роли нервного напряжения в возникновении раковых опухолей .

ВЕЩЕСТВА, ПРЕПЯТСТВУЮЩИЕ РОСТУ НОВЫХ СОСУДОВ
По счастью, помимо молекул, способствующих прорастанию опухоли сосудами, в организме синтезируются и собственные факторы, препятствующие росту сосудов (ингибиторы). В здоровом организме существует баланс между активаторами и ингибиторами роста новых кровеносных сосудов. При многих серьезных заболеваниях организм как бы теряет контроль над поддержанием этого равновесия. Смещение равновесия в сторону избыточного формирования новых сосудов происходит при онкологических заболеваниях, диабете, ревматоидном артрите и т.д. При таких опасных недугах, как заболевания коронарных артерий, инсульт, напротив, скорость роста новых сосудов явно ниже нормы.
Первым известным природным веществом, тормозящим рост новых сосудов, стал гликопротеин тромбоспондин, вырабатываемый различными клетками, в том числе и клетками стенок кровеносных сосудов. Тромбоспондин тормозит размножение и прикрепляемость эндотелиальных клеток, сдерживая таким путем рост капилляров.
В 1997 году тот же О’Рейли при исследовании культуры клеток злокачественной опухоли гемангиоэндотелиомы выделил еще один мощный блокатор формирования кровеносных сосудов — эндостатин. Это вещество является частью молекулы полипептида коллагена. Эндостатин активирует программируемую гибель эндотелиальных клеток и, вероятно, тормозит процесс их активации, размножения и миграции.
Помимо тромбоспондина, ангиостатина и эндостатина в органах и тканях животных исследователи обнаружили множество веществ, которые подавляют рост капилляров. К таким веществам относятся некоторые гормоны, фрагменты гепарина и др. Из известных природных ингибиторов можно назвать интерфероны, которые, кстати, борются и с вирусами. Однако как названные вещества, так и многие другие свойственные организму продукты обмена веществ обладают многофункциональным действием и из-за побочных эффектов не могут быть использованы в качестве лекарственных препаратов. Тем не менее интерес ученых к этой группе соединений не ослабевает.
"СОСУДИСТЫЙ" ПОДХОД К ЛЕЧЕНИЮ РАКА
Долгое время противораковая терапия была направлена лишь на подавление роста опухолевых клеток и усиление иммунного ответа. Сейчас уже ясно, что без формирования новых сосудов не может быть роста злокачественных опухолей. Лишенные возможности стимулировать образование новых капилляров, первичные и метастатические опухоли перестают расти. Поэтому появился новый класс ангиостатиков, то есть лекарств, тормозящих прорастание новых кровеносных сосудов. Такие соединения очень перспективны для борьбы со злокачественными опухолями на любой стадии их развития. Более того, существующие сейчас препараты эффективны по отношению к определенным опухолям, а блокаторы роста сосудов могут стать универсальным средством противораковой терапии, причем тем более эффективными, чем злокачественнее опухоль.
По противоопухолевой активности другой природный ингибитор — эндостатин сильнее, чем ангиостатин. Уже в малых дозах он предотвращает метастазирование крупных опухолей, а в больших — оказывает мощное тормозящее действие на рост первичных опухолей, таких, как карциномы, саркомы и меланома, вызывая в некоторых случаях их полную гибель. Очевидно, после разработки методов получения ангиостатина и эндостатина в промышленных масштабах эти препараты получат широкое клиническое применение, поскольку существенных побочных реакций при их использовании даже в больших дозах пока не выявлено.
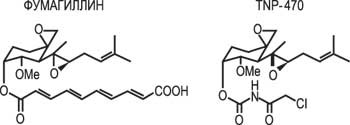
Первый класс веществ, которые сейчас испытываются в качестве противоопухолевых препаратов, — соединения, непосредственно блокирующие рост эндотелиальных клеток. К этой категории веществ относится уже упомянутый природный белок эндостатин. Его синтетический аналог комбрестатин А4 — химическая модификация соединения, содержащегося в древесине южноафриканского дерева Combretum caffrum, — проходит клинические испытания. Препарат также проявляет способность подавлять размножение клеток сосудов, стимулируя клеточный апоптоз. В настоящее время большое внимание уделяется созданию веществ, блокирующих размножение уже активированных клеток эндотелия. Из них наиболее удачным по активности и малой токсичности является синтетический препарат TNP-470, прошедший клинические испытания при раке почек, шейки матки и саркоме Капоши.
Ко второй группе препаратов, тормозящих рост сосудов, относятся природные или синтетические вещества, так или иначе блокирующие передачу сигнала на рецепторы факторов роста. Как уже было сказано, ФРЭС взаимодействует с эндотелиальными клетками посредством специальных белковых структур — рецепторов. Клетки здорового организма к этим веществам — блокаторам рецепторов нечувствительны. Клинические испытания проходят препараты антител к ФРЭС, которые эффективно блокируют рецепторы ФРЭС, не давая молекуле фактора роста запустить биохимический каскад, приводящий к прорастанию новых сосудов. Уже понятно, что лекарственные препараты на основе антител замедляют опухолевый рост и продлевают жизнь пациентам. Фактически антитела к ФРЭС — пока единственное антиангиогенное лекарство, уже появившееся на мировом фармацевтическом рынке. Ученые также синтезировали несколько молекул — аналогов ФРЭС, блокирующих рецепторы. Эти вещества тестируются в онкологических клиниках.
На стадии клинических испытаний находится и печально известный препарат талидомид. Почти полвека тому назад он применялся в качестве снотворного, но вызывал уродства плода у беременных женщин. Как случайно выяснилось впоследствии, это было связано с нарушением образования необходимых для роста плода сосудов, хотя механизм действия соединения так и остался до конца не выясненным. Талидомид оказался эффективным при лечении больных миеломой, раком простаты и легких, саркомой и ганглиобластомой.
К третьей группе веществ, подавляющих прорастание сосудов, а следовательно, и рост опухоли, относятся блокаторы (ингибиторы) активности опухолевых ферментов — металлопротеаз, которые разрушают внеклеточный матрикс и оболочку сосуда, давая клеткам эндотелия возможность мигрировать в сторону опухоли. В недавнее время созданы вещества, которые блокируют ионы металлов, входящих в активный центр ферментов, выводя ферменты опухоли из строя и тем лишая ее способности расти. Разработка препаратов такого типа действия — приномастата, маримастата и СOL-3 — находится на стадии клинических испытаний.
Автор статьи: Доктор медицинских наук В. ПРОЗОРОВСКИЙ
Подпишитесь на НОВОСТИ и получайте эксклюзивную информацию о самых последних исследованиях по противостоянию раку. Информация доступна только подписчикам.

В 1628 году английский врач Уильям Гарвей открыл кровообращение, а спустя некоторое время, в 1661 году, итальянский медик Марчелло Мальпиги – мельчайшие сосудики, капилляры, соединяющие артерии и вены у животных и человека. Сегодня наука о сердечно-сосудистой системе, ее функциях, заболеваниях – одна из ключевых в медицине, однако лишь недавно, в конце ХХ века, ученым пришло в голову, что кровеносные сосуды играют важную роль и в опухолевом росте. Теперь уже никто из медиков не сомневается, что раковая опухоль не может расти без постоянно образующихся вокруг нее новых сосудов.

Хотя post factum многое представляется само собой разумеющимся, но прошло немало лет, прежде чем медики догадались, что для интенсивного размножения опухолевых клеток нужны кислород и питательные вещества, поэтому быстрорастущая злокачественная опухоль требует крови больше, чем, скажем, липома, доброкачественная опухоль из жировой ткани. А значит, по мере развития раковая опухоль должна прорастать новыми кровеносными сосудами.
В 1971 году появилась статья американского хирурга Джуды Фолкмана, в которой впервые было высказано предположение, что рост опухолей, превышающих в диаметре несколько миллиметров, возможен только в случае формирования и прорастания в них мелких капилляров. В 1982 году американские ученые Ваупель, Каллиновски и Окуниефф показали, что во всех злокачественных опухолях действительно идет интенсивное новообразование сосудов. Верно и обратное – если образование новых сосудов прекращается, то дальнейший рост опухоли становится невозможен.
Открытие Фолкмана послужило началом целой череды научных достижений, в результате которых на свет явилась стройная теория ангиогенеза. Согласно ей, образование сосудов в раковой опухоли, так же как и в любой поврежденной ткани, протекает в несколько стадий. Что же побуждает организм образовывать новые капилляры?
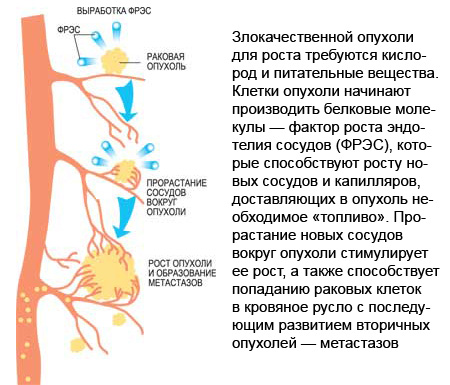


Факторы роста совершенно необходимы здоровому организму для восстановления кровотока при различных повреждениях, но их избыток может стать роковым для онкологического больного. Повышение синтеза ФРЭС стимулирует метастазирование опухолей – под воздействием этого вещества раковые клетки выходят в кровяное русло и распространяются по всему организму. С другой стороны, ФРЭС играет и положительную роль – прорастающие в опухоли сосуды формируют в ней своеобразный мягкий скелет, который удерживает клетки на месте, не давая им метастазировать.
Кстати, при недостатке кислорода выработка ФРЭС и других факторов роста усиливается – ведь организму нужно скомпенсировать гипоксию увеличением кровотока. Отсюда можно сделать вывод об увеличении риска онкологических заболеваний при снижении концентрации кислорода в воздухе из-за уничтожения зеленых насаждений, загрязнения окружающей среды и т.д. Также доказано, что молекулы, вырабатывающиеся в организме человека при стрессе, одновременно стимулируют синтез ФРЭС. Этот факт наводит на мысли о пагубной роли нервного напряжения в возникновении раковых опухолей.
По счастью, помимо молекул, способствующих прорастанию опухоли сосудами, в организме синтезируются и собственные факторы, препятствующие росту сосудов (ингибиторы). В здоровом организме существует баланс между активаторами и ингибиторами роста новых кровеносных сосудов. При многих серьезных заболеваниях организм как бы теряет контроль над поддержанием этого равновесия. Смещение равновесия в сторону избыточного формирования новых сосудов происходит при онкологических заболеваниях, диабете, ревматоидном артрите и т.д. При таких опасных недугах, как заболевания коронарных артерий, инсульт, напротив, скорость роста новых сосудов явно ниже нормы.

Первым известным природным веществом, тормозящим рост новых сосудов, стал гликопротеин тромбоспондин, вырабатываемый различными клетками, в том числе и клетками стенок кровеносных сосудов. Тромбоспондин тормозит размножение и прикрепляемость эндотелиальных клеток, сдерживая таким путем рост капилляров.
В 1997 году тот же О’Рейли при исследовании культуры клеток злокачественной опухоли гемангиоэндотелиомы выделил еще один мощный блокатор формирования кровеносных сосудов – эндостатин. Это вещество является частью молекулы полипептида коллагена. Эндостатин активирует программируемую гибель эндотелиальных клеток и, вероятно, тормозит процесс их активации, размножения и миграции.
Помимо тромбоспондина, ангиостатина и эндостатина в органах и тканях животных исследователи обнаружили множество веществ, которые подавляют рост капилляров. К таким веществам относятся некоторые гормоны, фрагменты гепарина и др. Из известных природных ингибиторов можно назвать интерфероны, которые, кстати, борются и с вирусами. Однако как названные вещества, так и многие другие свойственные организму продукты обмена веществ обладают многофункциональным действием и из-за побочных эффектов не могут быть использованы в качестве лекарственных препаратов. Тем не менее интерес ученых к этой группе соединений не ослабевает.

Долгое время противораковая терапия была направлена лишь на подавление роста опухолевых клеток и усиление иммунного ответа. Сейчас уже ясно, что без формирования новых сосудов не может быть роста злокачественных опухолей. Лишенные возможности стимулировать образование новых капилляров, первичные и метастатические опухоли перестают расти. Поэтому появился новый класс ангиостатиков, то есть лекарств, тормозящих прорастание новых кровеносных сосудов. Такие соединения очень перспективны для борьбы со злокачественными опухолями на любой стадии их развития. Более того, существующие сейчас препараты эффективны по отношению к определенным опухолям, а блокаторы роста сосудов могут стать универсальным средством противораковой терапии, причем тем более эффективными, чем злокачественнее опухоль.
По противоопухолевой активности другой природный ингибитор – эндостатин – сильнее, чем ангиостатин. Уже в малых дозах он предотвращает метастазирование крупных опухолей, а в больших – оказывает мощное тормозящее действие на рост первичных опухолей, таких, как карциномы, саркомы и меланома, вызывая в некоторых случаях их полную гибель. Очевидно, после разработки методов получения ангиостатина и эндостатина в промышленных масштабах эти препараты получат широкое клиническое применение, поскольку существенных побочных реакций при их использовании даже в больших дозах пока не выявлено.

Первый класс веществ, которые сейчас испытываются в качестве противоопухолевых препаратов, – соединения, непосредственно блокирующие рост эндотелиальных клеток. К этой категории веществ относится уже упомянутый природный белок эндостатин. Его синтетический аналог комбрестатин А4 – химическая модификация соединения, содержащегося в древесине южноафриканского дерева Combretum caffrum, – проходит клинические испытания. Препарат также проявляет способность подавлять размножение клеток сосудов, стимулируя клеточный апоптоз. В настоящее время большое внимание уделяется созданию веществ, блокирующих размножение уже активированных клеток эндотелия. Из них наиболее удачным по активности и малой токсичности является синтетический препарат TNP-470, прошедший клинические испытания при раке почек, шейки матки и саркоме Капоши.
Ко второй группе препаратов, тормозящих рост сосудов, относятся природные или синтетические вещества, так или иначе блокирующие передачу сигнала на рецепторы факторов роста. Как уже было сказано, ФРЭС взаимодействует с эндотелиальными клетками посредством специальных белковых структур – рецепторов. Клетки здорового организма к этим веществам – блокаторам рецепторов нечувствительны. Клинические испытания проходят препараты антител к ФРЭС, которые эффективно блокируют рецепторы ФРЭС, не давая молекуле фактора роста запустить биохимический каскад, приводящий к прорастанию новых сосудов. Уже понятно, что лекарственные препараты на основе антител замедляют опухолевый рост и продлевают жизнь пациентам. Фактически антитела к ФРЭС – пока единственное антиангиогенное лекарство, уже появившееся на мировом фармацевтическом рынке. Ученые также синтезировали несколько молекул – аналогов ФРЭС, блокирующих рецепторы. Эти вещества тестируются в онкологических клиниках.
На стадии клинических испытаний находится и печально известный препарат талидомид. Почти полвека тому назад он применялся в качестве снотворного, но вызывал уродства плода у беременных женщин. Как случайно выяснилось впоследствии, это было связано с нарушением образования необходимых для роста плода сосудов, хотя механизм действия соединения так и остался до конца не выясненным. Талидомид оказался эффективным при лечении больных миеломой, раком простаты и легких, саркомой и ганглиобластомой.


К третьей группе веществ, подавляющих прорастание сосудов, а следовательно, и рост опухоли, относятся блокаторы (ингибиторы) активности опухолевых ферментов – металлопротеаз, которые разрушают внеклеточный матрикс и оболочку сосуда, давая клеткам эндотелия возможность мигрировать в сторону опухоли. В недавнее время созданы вещества, которые блокируют ионы металлов, входящих в активный центр ферментов, выводя ферменты опухоли из строя и тем лишая ее способности расти. Разработка препаратов такого типа действия – приномастата, маримастата и СOL-3 – находится на стадии клинических испытаний.
Читайте также:

