Ревизия брюшной полости при раке яичников
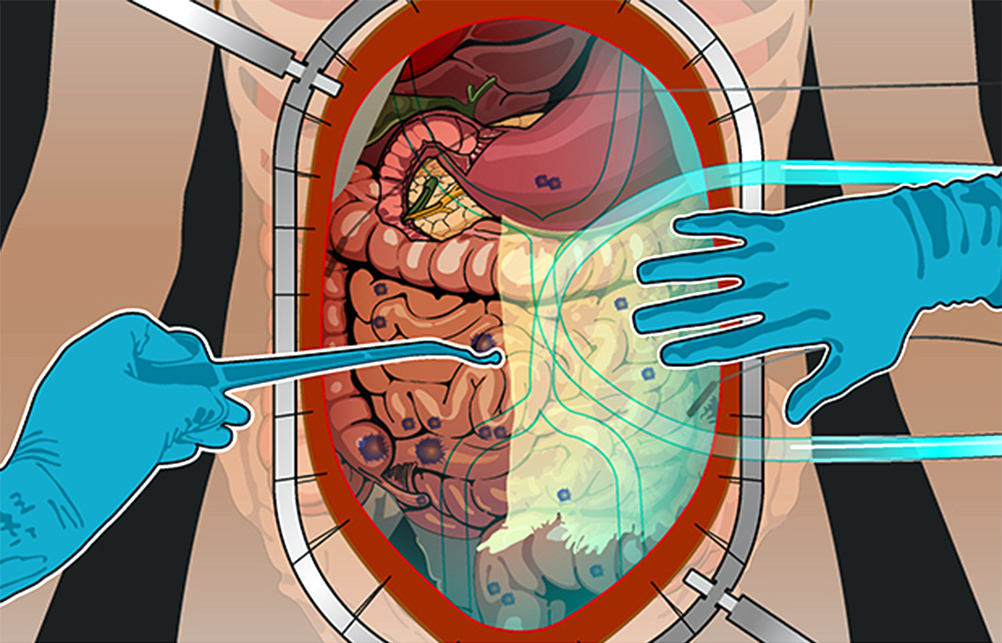
Средняя продолжительность жизни при карциноматозе брюшины без лечения – от 1,5 до 6 месяцев. Лечить же таких больных еще совсем недавно было нечем. Ни хирургия, ни химиотерапия не справлялись. Пациентов признавали инкурабельными (неизлечимыми). Показатель 5-летней выживаемости в начале 90-х был практически равен 0.
Но последние 20 лет активно развивается методика лечения перитонеального канцероматоза с применением HIPEC (англ. hyperthermic intraperitoneal chemotherapy) – гипертермической интраперитонеальной (внутрибрюшинной) химиотерапии. Методика дает отличные результаты: увеличивает 5-летнюю выживаемость до 40-50%, а иногда дает полное излечение.
Самое плохое – даже многие врачи не знают, что при канцероматозе существует способ продлить жизнь. Поэтому сегодня мы расскажем про HIPEC подробно: кому это поможет, какие дает результаты и сколько стоит.
Цель – уничтожить максимум опухолевых клеток, которые неизбежно останутся даже после самого тщательного хирургического удаления очагов и спровоцируют рецидив.
Свойства, которые делают HIPEC действительно уникальной методикой, мы разъясним чуть ниже, а сначала определимся, при каких диагнозах она может помочь и почему она иногда оказывается единственным способом продлить жизнь человеку на последних стадиях рака.
При каких опухолях образуется канцероматоз брюшины, и почему он так опасен
В брюшную полость распространяются многие из часто встречающихся видов рака.
- рак яичников – в 60-70% случаев приводит к канцероматозу;
- рак желудка – канцероматоз в 40-50% случаев;
- рак поджелудочной железы – в 30-40% случаев;
- рак толстой и прямой кишки (колоректальный рак) – в 10-15% случаев;
- рак печени;
- рак шейки матки;
- рак червеобразного отростка (аппендикса);
- редкие первичные опухоли брюшины (мезотелиома и псевдомиксома).
Все эти злокачественные новообразования распространяют раковые клетки либо когда первичная опухоль физически прорастает в брюшную полость, либо вместе с током крови и лимфы – иногда это происходит во время хирургических операций по поводу первичных опухолей.
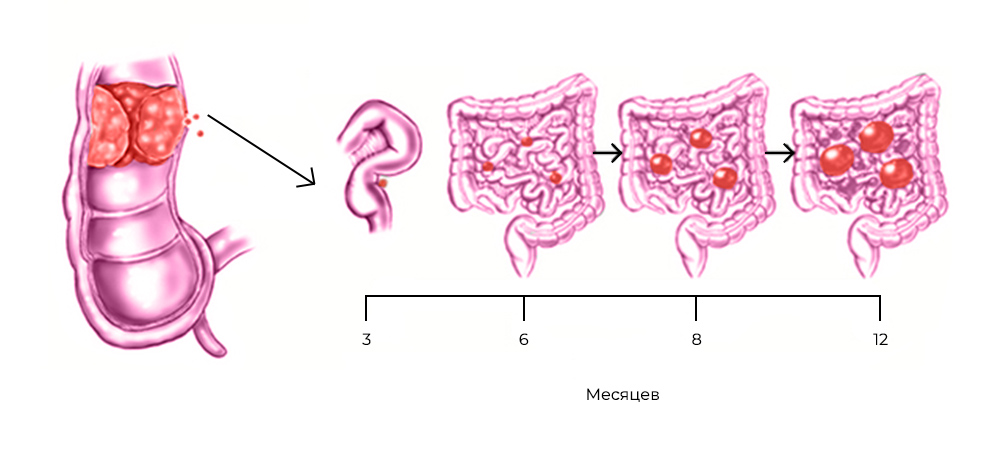
Развитие канцероматоза при колоректальном раке: из прямой кишки в брюшную полость
Стоит раковым клеткам попасть в полость, ограниченную брюшиной – они, скорее всего, дадут начало вторичным опухолям, метастазам. Перитонеальная ткань – богатый источник факторов роста и комфортная среда для их развития. Микроскопические метастазы распространяются по поверхности брюшины, поражают внутренние органы.
Метастазы нарушают кровоток и лимфоток, лишают внутренние органы питания и пространства, зачастую становятся причиной непроходимостей (например, кишечной, или сдавливают мочеточники). Кроме того, это провоцирует асцит – выпот и скопление жидкости в брюшной полости – наиболее распространенный симптом при канцероматозе.
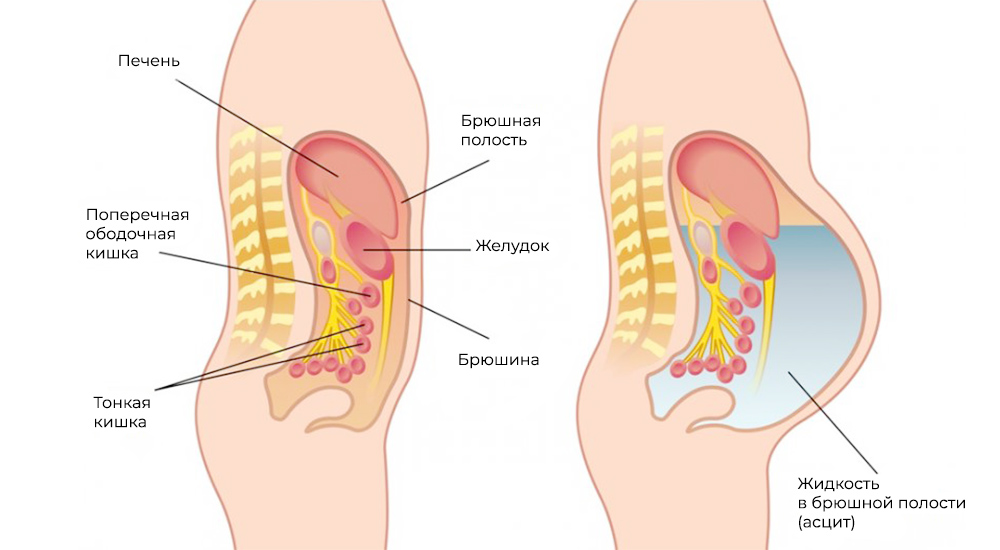
Асцит – скопление жидкости в брюшной полости
Застой крови и лимфы, интоксикация, сдавление внутренних органов метастазами и/или скопившейся жидкостью при асците – это причины, почему пациенты с канцероматозом без лечения не проживают и года.
На протяжении почти всей истории онкологии считалось, что перитонеальный карциноматоз и опухоли брюшины не поддаются никакому из существующих видов лечения.
Лучевая терапия в лечении канцероматоза не применяется, поскольку высокие дозы облучения такой обширной области живота опасны для пациента еще более серьезными осложнениями.
Хирургическое лечение малоэффективно, т.к. метастазы на поверхности брюшины могут быть микроскопического размера, либо расположены в недоступных местах, и врач не видит их во время операции. А для быстрого рецидива канцероматоза достаточно и единичных раковых клеток, оставшихся в полости брюшины.
Системная химиотерапия почти не дает чувствительного воздействия на опухоли брюшины –опухолевые очаги размером до 3 мм (таких при канцероматозе большинство) практически не развивают систему собственных кровеносных сосудов – и поэтому слабо доступны для системной внутривенной химиотерапии.
Вводить химиотерапию в более высоких дозах, чтобы повысить концентрацию препаратов в перитонеальной области – невозможно, т.к. это может необратимо навредить остальным органам и тканям, до которых доберется перенасыщенный химиопрепаратом кровоток.
Во второй половине 20 века появились первые работы, рассказывающие о возможностях применения внутрибрюшинной химиотерапии. Последние 20 лет это направление активно развивается, а создал его еще в 80-х годах XX века американский хирург-онколог Пол Шугабейкер – он первым придумал совместить циторедуктивную операцию с горячей химиотерапией, вводимой непосредственно в брюшную полость. И это дало результат
Гипертермия – это повышение температуры.
- Высокая температура сама по себе способна вызывать повреждение и гибель опухолевых клеток. К тому же, делает их более уязвимыми для действия химиопрепаратов: усиливает проницаемость клеточных мембран.
- Причем чувствительность увеличивается избирательно – опухолевые клетки начинают гибнуть при температуре 40 °C, а здоровые – сохраняются до 44°C. В условиях гипертермии особенности опухолевых тканей (иное кровоснабжение, степень оксигенации, особенности репарации ДНК) становятся для них не преимуществом, а слабым местом.
- Кроме того, повышение температуры обычно вызывает иммунную реакцию: растет количество лимфоцитов – клеток иммунитета, способных уничтожать опухолевые клетки. В плазме крове увеличивается уровень интерлейкинов, интерферонов, факторов некроза опухоли и т.д. Все они имеют собственную противоопухолевую активность, и дополнительно способны усиливать эффект некоторых химиопрепаратов.
- Еще один важный плюс гипертермии – она способствует более активному проникновению препарата в ткани – на глубину до 3 мм – этого хватит, чтобы охватить большинство микро-метастазов, которые останутся после хирургической операции.
Внутри брюшины – химиотерапия работает лучше. Для HIPEC используются стандартные химиопрепараты, но их локальное применение при перитонеальном карциноматозе – куда эффективнее.
Процедура HIPEC – это, строго говоря, вторая половина целого комплекса мероприятий. Без циторедуктивной хирургической операции HIPEC может проводиться в считанном количестве случаев по особым показаниям. Обычно процедура – продолжение хирургической операции, которое дает серьезное улучшение прогноза выживаемости.
Вместе с удалением опухолевых очагов, все вмешательство занимает от 6 до 18 часов. Процесс можно разделить на 4 этапа.
1) Ревизия брюшной полости. Проводится она для того, чтобы понять, показано ли лечение с помощью HIPEC для этого пациента, принесет ли оно увеличение продолжительности жизни и улучшение ее качества. Во время ревизии хирург внимательно осматривает брюшную полость и определяет перитонеальный индекс рака (peritoneal cancer index – PCI).
Чтобы его рассчитать, брюшную полость и тонкую кишку условно делят на 13 областей-квадрантов, в каждом из них оценивают самый крупный опухолевый очаг по шкале от 0 до 3:
- очагов не обнаружено — 0 баллов;
- очаги размером менее 0,5 см — 1 балл;
- очаги размером менее 0,5–5 см — 2 балла;
- очаг более 5 см или несколько узлов меньшего размера— 3 балла.
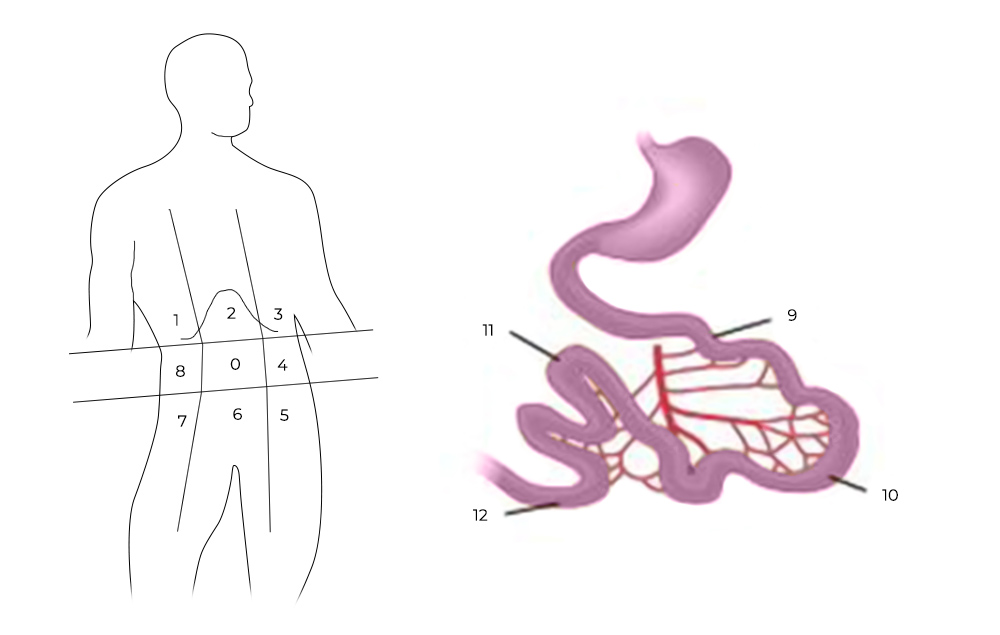
Разделение брюшной полости на участки для определения PCI
Баллы суммируются по всем квадрантам – это и есть значение PCI. Чем больше баллов – тем хуже прогноз. Если PCI выше критического (принимая во внимание тип опухоли и состояние пациента) – то и операцию, и процедуру HIPEC могут признать нецелесообразными.
Проводят ревизию интраоперационно – т.е. непосредственно перед проведением основной операции. В некоторых случаях ее можно провести в виде отдельной диагностической лапароскопической операции – малотравматичной, через небольшие проколы в стенке живота.
2) Циторедуктивная операция. Если по результатам ревизии PCI оценен как удовлетворительный, то хирург приступает к удалению всех видимых и пальпируемых (те, что чувствуются наощупь) опухолевых узлов.
Удаляют отдельные участки брюшины, орган, в котором находится первичная опухоль, соседние внутренние органы или их части, если они тоже поражены метастазами. Часто это участки кишечника, селезенка, желчный пузырь.
3) Гипертермическая интраперитонеальная химиотерапия. Собственно, HIPEC. В брюшную полость вводят катетеры и температурные датчики, соединенные со специальным аппаратом и емкостью с раствором химиопрепарата. Эта перфузионная система (под контролем врачей, конечно) поддерживает заданную температуру и давление циркулирующей жидкости. Раствор химиопрепарата в течение 60–90 минут циркулирует в брюшной полости пациента.
После процедуры препарат удаляют из брюшной полости, промывают ее физраствором, удаляют датчики и катетеры.
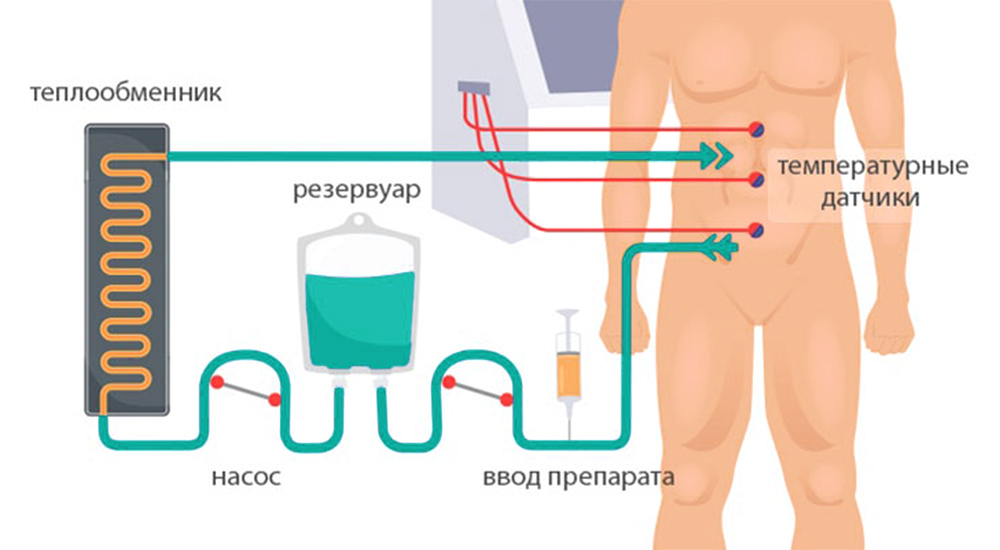
Схема проведения HIPEC
4) Реконструктивная операция. Если удалены части кишечника, хирург восстанавливает непрерывность кишки – формирует анастомоз, выводит верхний конец толстой/тонкой/слепой кишки на поверхность живота для отхождения каловых масс.
В среднем, в клинике пациент проводит 2-4 недели. Через 2-3 недели после операции проводится контрольное обследование. Его необходимо повторять через 3 месяца, и постепенно частоту проверок снижают до 1 раза в год.
В этом видео наши коллеги проводят процедуру HIPEC пациентке с раком яичников.
Как любое лечение, HIPEC имеет риски и противопоказания
Послеоперационный период стоит отдельным этапом, но он не менее важен. Мы всегда понимаем, насколько сложным для наших пациентов (а многие попадают к нам в крайне тяжелом состоянии) может быть период восстановления после такого длительного и достаточно агрессивного вмешательства, как циторедуктивная операция + HIPEC. Поэтому сразу после операции мы переводим пациента в отделение интенсивной терапии, под круглосуточное наблюдение.
Осложнения могут быть те же, что и после любого хирургического вмешательства на брюшной полости, поэтому за пациентом внимательно следят на случай появления признаков кровотечения или воспаления послеоперационной раны – и готовы в любую минуту оказать помощь.
Побочные действия от химиотерапевтического препарата при внутрибрюшной гипертермической химиотерапии даже менее выражены, чем при внутривенном введении – при том, что дозировки, а значит, и противоопухолевое действие, при HIPEC в десятки раз выше.
К сожалению, при всем нашем желании и мастерстве наших хирургов, есть пациенты, для которых полезный эффект вмешательства не оправдает сложностей послеоперационного восстановления.
Чтобы циторедуктивная операция с последующей процедурой HIPEC была эффективной, нужно соблюдение нескольких условий:
- Пациент должен быть в состоянии перенести и хирургическую операцию, и химиотерапию одновременно. Возраст или показатели здоровья не должны этому препятствовать – например, не должно быть почечной или печеночной недостаточности. Перед процедурой мы обязательно всесторонне обследуем пациента.
- Процесс распространения метастазов должен быть ограничен только брюшной полостью. Если есть метастазы в других органах, которые нельзя удалить – они будут распространяться дальше, и сведут эффект HIPEC на нет.
- Метастазы размером более 2,5 мм не должны покрывать всю поверхность брюшины – удалить их все будет невозможно.
Мы провели ей циторедуктивную операцию и процедуру HIPEC, и после этого она уже 10 месяцев живет без прогрессирования заболевания.
В некоторых случаях HIPEC приводит к устойчивому излечению. Например, коллеги из США сообщали о женщине с мезотелиомой брюшины. С помощью HIPEC она преодолела болезнь, уже 3 года живет без признаков рака и смогла родить ребенка.

Jessica Blackford-Cleeton, которой HIPEC позволила выжить и стать мамой.
К сожалению, HIPEC пока применяется в считанном количестве клиник. Причин этому несколько, и они характерны для всех новых технологичных способов лечения.
- Методика все еще считается инновационной, не все врачи имеют нужный опыт работы. К тому же, для проведения процедуры нужен не 1 и не 2, а целая бригада медиков самой высокой квалификации – это длительная, сложная и напряженная операция.
- Оборудование дорогое, не все страны и не все клиники могут потратиться на перфузионную систему и расходные материалы.
- Врачи бывают довольно консервативны. Кто-то считает, что процедура требует более подробного изучения. А кто-то из них не любит участвовать в проведении гипертермической химиотерапией, потому что опасается за собственное здоровье – испарения химиопрепаратов во время HIPEC могут быть вредными для медиков, которые при этом присутствуют. Хотя, в целом, испарения из закрытого контура минимальны, негативные последствия, даже если есть – не являются необратимыми, врачу нужно лишь более внимательно следить за состоянием почек и печени.
Однако более 70 ведущих хирургов-онкологов из 55 онкоцентров в 14 странах мира, включая США (где и родилась эта процедура), Канаду, Францию и Великобританию, пришли к выводу о том, что HIPEC может существенно повысить ожидаемую продолжительность жизни у пациентов, страдающих канцероматозом, особенно при колоректальном раке.
Клинические исследования из разных стран показывали результаты, когда пациенты после лечения канцероматоза брюшины с применением HIPEC жили 7 лет при опухолях аппендикса, более 5 лет при мезотелиоме брюшины, 5 лет при колоректальном раке, 2 года при раке яичников – тогда как при стандартном лечении их выживаемость колебалась от 2 до 14 месяцев.
Мы в свою очередь убедились в эффективности HIPEC на собственном обширном клиническом опыте. Мы надеемся, что через несколько лет HIPEC будет внедряться в стандарты лечения по ОМС и станет доступна по всей стране. А пока – мы даем пациентам возможность не искать подобную помощь за рубежом, а получить ее в Москве.
Одним из осложнений онкологических заболеваний является асцит – скопление жидкости в брюшной полости. Выделяемый экссудат является отфильтрованной плазмой крови, которая по ряду причин выделилась в брюшную полость. В Юсуповской больнице созданы все условия для лечения пациентов, страдающих онкологическими заболеваниями:
- пациенты находятся в комфортных палатах, оснащённых притяжно-вытяжной вентиляцией и кондиционерами;
- медицинский персонал внимательно относится к пожеланиям онкобольных и их родственников;
- пациенты обеспечены диетическим питанием и индивидуальными средствами личной гигиены;
- для диагностики онкологических заболеваний врачи используют аппаратуру ведущих производителей Европы, Японии, США и применяют инновационные методики лабораторных исследований;
- онкологи применяют современные схемы лечения безопасными лекарственными препаратами, зарегистрированными в РФ.
В клинике онкологии работают кандидаты и доктора медицинских наук. Все тяжёлые случаи онкологических заболеваний обсуждаются на заседании экспертного совета с их участием. Врачи коллегиально вырабатывают тактику лечения пациента.

Причины образования асцита у онкологических больных
Опухолевый асцит развивается при следующих заболеваниях брюшной полости:
- раке яичников и эндометрия;
- злокачественных новообразованиях лёгких;
- опухолях желудочно-кишечного тракта и поджелудочной железы;
- раке молочной железы.
При оседании опухолевых клеток на брюшине возникает механическое препятствие для оттока лимфы. Если опухоль развивается в воротах печени, нарушается отток венозной крови и повышается гидростатическое давление в органе. В брюшной полости скапливается жидкость и развивается асцит. Лимфома брюшной полости сопровождается хилёзным асцитом (скоплением лимфы, богатой жировыми клетками).
Асцит брюшной полости при онкологии яичников
Рак яичников – злокачественная опухоль придатков матки. Заболевание имеет 4 стадии развития. На третьей и четвёртой стадии рака яичников развивается злокачественный асцит. При раке яичников появление асцита связанно с нарушением процесса выделения и всасывания экссудата. Если все системы организма функционируют нормально, в полости брюшины находится незначительное количество экссудата, который там циркулирует. Он препятствует слипанию внутренних органов. Во время перистальтики кишечника не возникает трения петель кишок между собой. Экссудат всасывается там же, где и вырабатывается. Здоровый организм самостоятельно контролирует этот процесс.
При раке яичников нарушается функционирование листков брюшной полости. Страдают барьерная, резорбтивная и секреторная функция брюшины. В результате экссудата может вырабатываться или слишком много, или процесс его обратного всасывания значительно нарушается. Итогом этого патологического процесса является скопление большого количества жидкости в области брюшной полости.
При прогрессировании рака яичников на листках брюшины, покрывающей брюшную полость и внутренние органы, оседают раковые клетки. Нарушается резорбтивная функция брюшины. Лимфатические сосуды оказываются закупоренными метастазами злокачественной опухоли. Нарушается лимфодренаж, что приводит к развитию асцита.
На появление асцита при раке яичников влияют ещё несколько факторов:
- быстрое распространение атипичных клеток на соседние ткани из-за близкого расположения брюшных складок;
- большое количество кровеносных и лимфатических сосудов в брюшной полости;
- попадание в брюшину раковых клеток при проведении полостных операций;
- метастазирование рака яичников на стенки брюшной полости;
- раковая интоксикация на четвёртой стадии развития злокачественного процесса.
Также развивается асцит после химиотерапии. Если патологическим процессом затронута венозная система, асцит при раке яичника протекает тяжело и стремительно. Канцероматоз брюшины – это осложнение рака яичников, для которого характерны множественные метастазы злокачественной опухоли на различных участках брюшины. Характерным признаком канцероматоза является асцит. В правой доли печени также могут образоваться метастазы рака яичников.
Симптомы асцита при раке яичников
При постоянном увеличении количества жидкости передняя стенка живота становится напряжённой. На ней натягиваются кожные покровы. Это производит впечатление очень тонкой и сглаженной кожи, появляются стрии (растяжки). Пупок выворачивается наружу.
В зависимости от объёма скопившегося в брюшной полости экссудата выделяют 3 стадии асцита при раке яичников. Если количество жидкости не превышает 400 мл, наблюдается только вздутие живота и симптомы основного заболевания. При умеренном асцит количество жидкости в брюшной полости не превышает 5 л. У пациентки, кроме вздутия живота, отмечаются следующие симптомы:
У пациенток появляется болезненность в животе. При затяжном течении заболевания развивается перитонит, сердечная и дыхательная недостаточность.
Если асцит при раке яичников сформировался, наблюдается отёчность низа живота, области наружных половых органов, нижних конечностей. У некоторых пациенток могут возникать боли с правой стороны живота (симптом ложного аппендицита). Пациентки интересуются, сколько живут при раке яичников 3-4 стадии с асцитом. Если развился асцит брюшной полости при онкологии, прогноз пессимистичный.
Диагностика асцита
Для того чтобы выявить или подтвердить асцит при раке яичников, врачи применяют следующие диагностические методы:
- визуальный осмотр и пальпация области живота;
- гинекологический осмотр,
- инструментальные методы исследования.
При осмотре выявляют увеличение объёма живота. Методом пальпации определяют флюктуацию (наличие жидкости). При перкуссии области живота определяют притупленный звук над всей поверхностью брюшной стенки. При повороте пациентки на бок он смещается вниз.
К инструментальным методам диагностики относят:
- трансвагинальное ультразвуковое исследование (выявление новообразования в яичниках, распространённость патологического процесса на расположенные поблизости органы, наличие экссудата);
- компьютерную томографию органов малого таза, грудной и брюшной полости;
- лапароскопию с и цитологическим исследованием полученной жидкости;
- рентгеноскопию органов грудной клетки (позволяет выявить высокое положение диафрагмы, обнаружить жидкость в плевральной полости).
Если появляется жидкость в брюшной полости при онкологии, прогноз малоутешительный. Поскольку асцит появляется на 3-4 стадии рака яичников, при появлении первых подозрений на возникновение этого патологического процесса женщине следует немедленно обратиться к гинекологу. Это может стать залогом успешного лечения рака яичников и благоприятного прогноза на выздоровление.
Лечение пациентов с асцитом при онкологии
При выборе методики лечения пациентов с асцитом, развившимся при онкологических заболеваниях, опираются на результаты, врачи ориентируются на результаты диагностических исследований. Онкологи учитывают количество патологического экссудата, возраст пациентки, наличие метастазов, возраст пациентки. Лечебный процесс назначают в течение первых двух недель после постановки диагноза.
К основным способам лечения онкологических больных с асцитом относят:
- консервативную терапию (количество жидкости в брюшной полости пытаются уменьшить с помощью диуретических средств);
- установка дренажа для своевременного удаления накопившейся жидкости;
- полноценная хирургическая операция на яичниках;
- внутриполостная химиотерапия (введение лекарственных средств непосредственно в брюшную полость).
Для поддерживающей терапии назначают мочегонные средства. При применении мочегонных препаратов для нормализации водно-электролитного обмена обязательно назначают препараты калия. Откачать жидкость из брюшной полости при онкологии можно с помощью малоинвазивной операции лапароцентеза. Проведение лапароцентеза с установлением дренажа значительно облегчает состояние пациентки. За одну процедуру удаляют до 10 литра экссудата.
Внутрибрюшная химиотерапия подавляет рост злокачественных клеток непосредственно в очаге поражения, способствует уменьшению объёма скопившейся жидкости и улучшению процессов обратного всасывания экссудата. Дополнительные методы лечения включают в себя:
- инфузионную терапию (при удалении большого количества экссудата резко снижается уровень альбумина в сыворотке крови);
- иммунотерапию;
- радиотерапию.
Диета при асците при онкологии позволяет улучшить состояние пациентов. Правильно подобранный рацион питания способствует снижению уровня жидкости в брюшной полости. Для уменьшения количества экссудата рекомендуется ограничить питьевой режим и употреблять в пищу как можно меньше соли.
Звоните по телефону Юсуповской больницы, где специалисты контакт-центра ответят на все ваши вопросы. Клиника работает круглосуточно и без выходных.
Эффективный подход в лечении рака яичников. Интервальная химиотерапия и лапароскопия. Профессор Пучков К.В.
Мой опыт лапароскопических оперативных вмешательств по поводу кист, опухолей и рака яичников составляет более 800 операций, который обобщен в многочисленных научных работах и монографиях. Регулярно по этой теме мной проводится мастер-классы для гинекологов и онкологов.
Выбор тактики лечения пациенток с раком яичников осуществляется тремя специалистами — врачом- хирургом, онкологом и химиотерапевтом, с обязательным участием грамотного морфолога.
Я придерживаюсь определенной стратегии в лечении этой категории больных. Она позволяет быстро поставить правильный диагноз. Обойтись малоинвазивными методами операций и в большинстве случаев сохранить возможность женщины к беременности и родам.
Суть стратегии, которой я придерживаюсь в лечении этой категории больных
- Следует напомнить о важности индивидуального подхода, так как в каждом конкретном случае решается не только судьба пациентки и ее семьи, но и судьба будущих детей.
- Необходимо тщательное обследование на предоперационном этапе для более точного понимания стадии болезни.
- Важным этапом в диагностике и лечении является выполнение лапароскопии, цели и задачи которой совершенно различны в каждом конкретном случае. Лапароскопия это малоинвазивная процедура, которая позволяет оценить характер и объем поражения, взять неограниченное количество разного материала патологических тканей и жидкостей из брюшной полости и малого таза для морфологического исследования, удалить первичную опухоль и при необходимости выполнить полный онкологический объем (пангистерэктомия с экстирпацией большого сальника и парааортальной лимфаденэктомией).
К. В. Пучков: "Онкологическое заболевание - не приговор"
Техника лапароскопической операции при опухоли яичника

Пучков К.В., Политова А.К. Лапароскопические операции в гинекологии: монография.- М.: МЕДПРАКТИКА, 2005. - 212 с.

Пучков К.В., Баков В.С., Иванов В.В. Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии: Монография.- М.: ИД МЕДПРАКТИКА – М.- 2005.- 168 с. 
Пучков К.В., Иванов В.В.. Технология дозированного лигирующего электротермического воздействия на этапах лапароскопических операций: монография.- М.: ИД МЕДПРАКТИКА, 2005.- 176 с.
Лапароскопическая пангистерэктомия с субтотальной резекцией большого сальника и лимфаденэктомией.
После пангистерэктомии, извлечение макропрепаратов сальника, лимфоузлов и матки из брюшной полости осуществляется в пластиковом контейнере трансвагинальным доступом.
Затем я обязательно тщательно послойно ушиваю стенки влагалища и связки тазового дна эндоскопическим способом, используя рассасывающиеся нити Монокрил 0 на атравматичной игле. Этот этап очень важен для профилактики опущения стенок влагалища и мочевого пузыря в послеоперационном периоде.
Следует отметить, что по данным литературы последних лет, мнение ученых о значимости интраоперационного нарушения целостности опухоли изменилось. E.Surwit (1994), W.Parker и J.Berek (1993) не отметили ухудшения прогноза из-за ятрогенного разрыва интактной капсулы злокачественной опухоли яичника. Авторы полагают, что частота рецидивов определяется лишь наличием плотных спаек, дифференцировкой опухоли и большим количеством асцитической жидкости. F.Y.Ahmed (1996), S.Kodama и K.Tanaka (1997) указывают, что наличие асцита, спаек, дооперационный разрыв капсулы опухоли и уровень СА-125 влияют на прогноз заболевания, в то время как нарушение целостности новообразования или пункция опухоли во время проведения хирургического вмешательства оказываются прогностически незначимыми.
Несмотря на представленные литературные данные, все манипуляции с кистой и опухолью, я выполняю в специальном контейнере (20х20 см). Поэтому в случае случайной перфорация стенки, это происходит в контейнере без контаминации брюшной полости, то есть в условиях полной абластики.
Всем пациенткам после удаления препарата необходимо выполнять гистологическое исследование для стадирования онкологического процесса.
Исходя из моего длительного опыта (22 года) и многочисленных данных литературы, лапароскопический доступ имеет ряд преимуществ в сравнении с традиционным, сохраняя при этом основные онкологические принципы выполнения оперативных вмешательств. При лапароскопии отмечается лучшая визуализация операционного поля за счет достаточного освещения и оптического увеличения, более тщательная диссекция сосудистых структур, более тщательный гемостаз, уменьшение болевого синдрома в послеоперационном периоде, полное отсутствие лимфореи, сокращение сроков реабилитации. Эти преимущества позволяют в случае постановки диагноза рака яичника своевременно начать химиотерапию, что существенно сказывается на результатах лечения этой категории больных.
Высокая квалификация хирурга, четкое понимание стоящих перед ним задач при первичном выявлении злокачественной опухоли любой локализации и новообразований яичников в частности, позволяет выполнить адекватный объем оперативного вмешательства, тщательную ревизию брюшной полости и правильное стадирование онкологического процесса, что помогает избавить пациентку от нередко существенно отсроченной по времени повторной операции. В связи с этим чрезвычайно актуальным остается вопрос определения адекватной тактики хирурга во время операции, так как от грамотности его действий зависит прогноз дальнейшего лечения и судьба больной.
Средняя длительность оперативного вмешательства составляет 1-1,5 часа. На следующий день пациентки встают с постели и принимают жидкую пищу. Выписываются на 2-3 сутки. На 7 сутки проходят контрольный осмотр на кресле, при необходимости выполняется Узи органов малого таза и брюшной полости.
Обязательно данные гистологического исследования обсуждаются с врачами смежных специальностей (онколог, химиотерапевт, радиолог) для определения оптимальной тактики дальнейшего лечения.
При необходимости, по желанию пациента, курсы химиотерапии могут быть проведены в Швейцарской университетской клиники под контролем опытных онкологов.

Профессор, д.м.н. Пучков К.В.
Сертифицирован по специальностям: хирургия, гинекология, урология, проктология, онкология.
Стаж: 32 года

«Когда вы пишете письмо, знайте: оно попадает мне на мою личную электронную почту. На все ваши письма я отвечаю всегда только сам. Я помню, что вы доверяете мне самое ценное - свое здоровье, свою судьбу, свою семью, своих близких и делаю все возможное, чтобы оправдать ваше доверие.
Каждый день я по нескольку часов отвечаю на ваши письма.
Направляя мне письмо с вопросом, вы можете быть уверены, что я внимательно изучу вашу ситуацию, при необходимости запрошу дополнительные медицинские документы.
Огромный клинический опыт и десятки тысяч успешных операций помогут мне разобраться в вашей проблеме даже на расстоянии. Многим пациентам требуется не хирургическая помощь, а правильно подобранное консервативное лечение, в то время как другие нуждаются в срочной операции. И в том, и в другом случае я намечаю тактику действий и при необходимости порекомендую прохождение дополнительных обследований или неотложную госпитализацию. Важно помнить, что некоторым больным для успешной операции требуется предварительное лечение сопутствующих заболеваний и правильная предоперационная подготовка.
В письме обязательно (!) укажите возраст, основные жалобы, место проживания, контактный телефон и адрес электронной почты для прямой связи.
Чтобы я мог детально ответить на все ваши вопросы, прошу высылать вместе с вашим запросом сканированные заключения УЗИ, КТ, МРТ и консультаций других специалистов. После изучения вашего случая, я направлю вам либо подробный ответ, либо письмо с дополнительными вопросами. В любом случае я постараюсь вам помочь и оправдать ваше доверие, которое является для меня наивысшей ценностью.
Читайте также:

