Распространение опухоли в организме
Доброкачественные и злокачественные опухоли
С клинической точки зрения опухоли не равнозначные. В зависимости от степени дифференциации, скорости и характера роста, склонности к метастазированию и рецидивам, вторичным изменениям в опухолях, влияния их на организм, их разделяют на доброкачественные, злокачественные и с местным деструктивным ростом.
Доброкачественные (зрелые) - опухоли построены из клеток, по структуре которых всегда можно определить, из какой ткани они растут. Если они не размещены около жизненно важных центров, то проявляются местными изменениями и незначительно влияют на организм. Однако, такие опухоли могут переходить в злокачественные - малигнизироваться.
Злокачественные (незрелые) - опухоли построены из мало- или недифференцированных клеток, которые теряют структурное подобие клеток, из которых они происходят. В отличие от доброкачественных опухолей, они дают метастазы, рецидивируют, проявляются местными изменениями и влияют на весь организм, не переходя в дифференцированные формы.
Опухоли с местным деструктивным ростом - занимают промежуточное положение между доброкачественными и злокачественными. Они имеют признак инфильтративного роста, но не метастазируют. Такими является кавернозная гемангиома, десмоид.
Основные дифференциальные признаки доброкачественных и злокачественных опухолей поданы в таблице 6.
| Доброкачественные опухоли | Злокачественные опухоли |
| Имеют незначительные отклонения вот материнской ткани | Выраженный атипизм |
| Экспансивный рост | Инфильтративный рост |
| Растут медленно | Растут быстро |
| Достигают больших размеров | Редко достигают больших размеров |
| Редко поддаются язву ванню | Часто поддаются язву ванню |
| Не дают метастазов | Дают метастазы |
| Рецидивирование не характерно | Часто рецидивируют |
| Мало нарушают общее положение больного | Имеют значительное влияние на весь организм |
В зависимости вот степени дифференциации, различают экспансивную, оппозиционную и инфильтративную (инвазивную) формы роста опухолей. Первая форма присуща доброкачественным опухолям, вторая и третья - злокачественным.
Опухоль, которая растет экспансивно, увеличивается в виде узла, отодвигая окружающие ткани. Клетки, которые окружают ее, атрофируются, а строма поддается коллапсу, который предопределяет образования псевдокапсулы и четкость пределов опухоли.
Оппозиционный рост - промежуточный между экспансивным и инфильтративным. Опухоль растет из множественных точек роста - очаговых пролифератов, которые представляют "опухолевое поле". Опухолевая трансформация (малигнизация) осуществляется последовательно с центра к периферии и завершается слиянием очагов малигнизации в единственный узел.
Инфильтративный рост характеризуется тем, что опухолевые элементы распространяются в направлениях наименьшего сопротивления и врастают в окружающие ткани, разрушая их. Пределы опухоли в таком случае не четки, стерты.
Относительно полости органа выделяют эндофитный и екзофитный рост. Как своеобразную форму рассматривают прединвазивный, или интраепителиальный, рак. Гистологически выявляют дисплазию эпителия, атипизм, исчезает нормальная его форма, но базальная мембрана не повреждается.
Опухоли, которые растут экспансивно, не распространяются за пределы органа. В случае инфильтративного роста опухоль распространяется не только в органе, но и за его пределами. Различают непрерывное контактное распространение опухоли и метастазирование.
Непрерывное распространение - это прорастание опухоли в соседние органы. При инфильтративном росте опухолевые клетки могут достигать серозной оболочки, где возникает реактивное воспаление, а организация экссудата завершается образованием соединений с соседними органами. По соединениям опухоль прорастает в эти органы (например, рак желудка прорастает в печенку или поджелудочную железу). Когда сращиваются полые органы, то в результате непрерывного распространения и некроза возможно образование фистул. Фистула толстой кишки, например, наблюдается при раке желудка или желчного пузыря.
Метастазирование - это перенесение опухолевых клеток из первичного очага в отдаленные участки с дальнейшим приживлением их и образованием вторичных очагов. Существует несколько путей метастазирования: гематогенный, лимфогенный, периневральный, имплантационный, смешанный.
Гематогенные метастазы - возникают тогда, когда клетки злокачественной опухоли попадают в кровеносное русло и двигаются за током венозной или артериальной крови. Распространение по венам - путь метастазирования, который встречается чаще всего. При этом существуют два возможных направления: первый - по системе полой вены, когда опухолевые клетки из первичного очага (матки, почки, костей скелета) переносятся в легкие; второй - по системе портальной вены, когда опухоли желудка, кишечника, поджелудочной железы метастазируют в печенку. Иногда возможны парадоксальные и ретроградные метастазы. Артериальный путь метастазирования касается, в первую очередь, первичного очага, локализованного в легких. При этом возникают метастазы в головной мозг, костный мозг, печенку и другие органы. Гематогенный путь метастазирования наиболее присущ саркомам.
Лимфогенное метастазирование - это перенесение опухолевых клеток в регионарные, а позже - в отдаленные лимфатические узлы. Впоследствии опухолевые клетки через грудной лимфатический проток проникают в кровеносную систему.
Перемещение раковых клеток в отдаленные места организма – безусловный признак злокачественности процесса. Метастазирование рака указывает на запущенную форму болезни: распространение опухоли начинается при достаточном увеличении массы опухолевой ткани. Около 30% всех впервые выявленных злокачественных новообразований имеют метастазы, что связано со скрытым течением болезни, несвоевременным обращением к врачу и несовершенством медицинской диагностики.
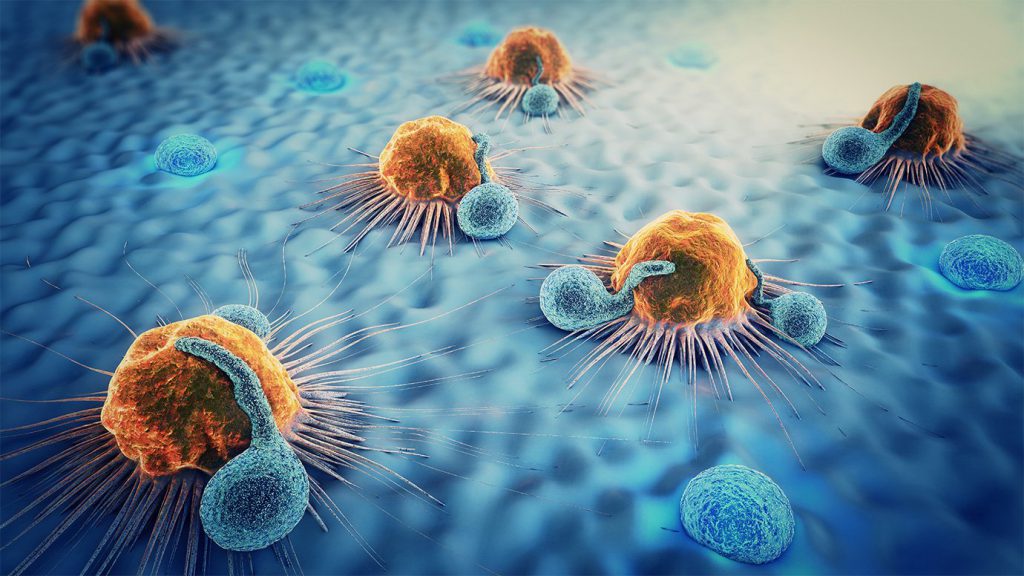
Метастатические клетки могут проникать в любые места организма
Метастазирование рака – что это
Любое злокачественное новообразование всегда имеет первичную локализацию. Метастазирование рака (от греческого metastasis – перемещение, перенос, смена места) – это распространение опухолевых клеток по организму, когда из первичного очага различными способами рак перемещается в ткани и органы, став причиной быстрого ухудшения состояния здоровья. По сути, опухоль-паразит отправляет в автономное путешествие по организму хозяина своих агентов: не все приживутся в новых местах, но многие станут основой для формирования вторичного очага злокачественного новообразования. Метастазирование рака – это абсолютный признак злокачественности (наличие метастазов относит опухоль к запущенным стадиям болезни).
Основные пути распространения опухоли
Выделяют несколько путей распространения опухолевых агентов. К наиболее частым относятся:
- лимфогенное метастазирование рака (раковые клетки отправляются в путь по лимфатическим сосудам, застревая в первых барьерах – регионарных лимфоузлах);
- гематогенное (через кровеносные сосуды, где функции барьеров выполняют органы, поэтому метастазы задерживаются в печени, костном мозге, легких, почках и головном мозге);
- имплантационное (при соприкосновении внутренних серозных оболочек, что характерно для опухолей в брюшной полости);
- прививочное (проявление метастазов в послеоперационных рубцах, куда клетки опухоли попадают во время хирургического вмешательства);
- периневральное (редкий вариант распространения опухолевых агентов вдоль нервных стволов характерно для некоторых видов онкологии – при раке простаты, опухоли прямой кишки).
В подавляющем большинстве случаев перемещение рака происходит лимфогенным и гематогенным путем: микроэмболы опухоли способны достигать любых участков тела, чаще задерживаясь в типичных местах с формированием стандартных симптомов осложненного течения злокачественного новообразования.
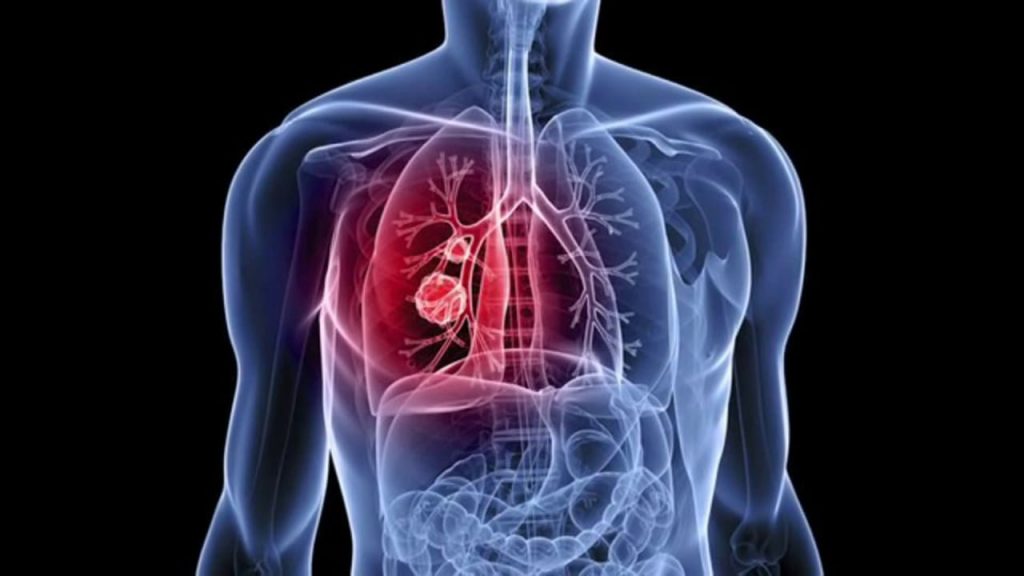
Метастазы при раке легкого проникают в головной мозг, кости и надпочечники
Особенности метастазирования
К важным особенностям переноса опухолевых клеток по организму относятся:
- Временной фактор (метастазирование рака начинается при достижении критической массы новообразования, когда накапливается определенное количество опухолевых структур);
- Наличие излюбленных мест для каждого вида рака (в частности, при раке легкого надо искать метастазы в головном мозге, костях и надпочечниках);
- Возрастной фактор (чем моложе пациент, тем раньше и агрессивнее процесс метастазирования);
- Гистологическая структура (низкодифференцированные новообразования значительно раньше дают метастазы);
- Травматический фактор (любое случайное или намеренное повреждение опухолевой ткани может стать причиной для начала процесса перемещения метастатических очагов);
- Стрессовое воздействие (острая стрессовая ситуация может запустить метастазирование рака, что объясняется снижением противоопухолевой иммунной защиты).
Опухоль-паразит не ограничивается одним очагом первичной локализации: при появлении возможности для распространения по организму карцинома незамедлительно отправит своих агентов для захвата новых территорий. Метастататический рак – это крайне неблагоприятный прогностический фактор, указывающий на высокий риск для жизни больного человека (даже при хирургическом удалении первичного очага, сложно, а порой невозможно, убрать все вторичные очаги и микрометастазы, обеспечив пациенту реальный шанс для выздоровления).
Организм человека состоит из многих миллионов клеток. Большинство из них в процессе роста периодически подвергается делению. В здоровом организме эти процессы строго контролируются, в том числе, и на генном уровне. Однако при онкологических заболеваниях ограничения роста и деления клеток в определенном органе или ткани утрачиваются, указанные процессы становятся неконтролируемыми, что и является причиной возникновения опухоли. Раздел медицины, который занимается изучением опухолей, называется онкологией, а специалисты в этой области — онкологами. Онкологи проводят лечение больных, которые страдают как злокачественными, так и доброкачественными опухолями.
Что происходит в организме человека в результате роста опухоли?
В чем заключается опасность опухоли?
В результате неконтролируемого роста опухоль постепенно проникает в здоровые органы и ткани, вызывая их повреждение. При этом опухоль может распространяться и на соседние органы, находящиеся от нее на значительном отдалении. Например, опухоль молочной железы может вызвать поражение костей путем образования в них вторичных опухолей. Такие вторичные опухоли, возникающие в отдаленных от первичной опухоли органах, называют метастазами. Именно метастазы представляют собой главную опасность, связанную с прогрессирующим характером онкологического заболевания.
Каковы причины возникновения опухоли у конкретного человека и в определенном органе?
В каких органах чаще всего возникают злокачественные опухоли?
В экономически развитых странах, в том числе в России, наиболее часто возникают опухоли легких. Кроме того, в общей структуре опухолей значительное место занимают опухоли желудка, толстого кишечника, молочной железы, женских половых органов, кожи. У мужчин опухоли развиваются чаще, чем у женщин.
Обязательно ли опухоль становится причиной смерти?
Многие опухоли, при условии их своевременного лечения, не становятся причиной смерти онкологических больных. В некоторых случаях опухоль все же является причиной смерти. Все зависит от конкретного типа опухоли у данного больного, а таких типов известно более 200. В ряде случаев течение онкологического заболевания может быть длительным, а наличие опухоли не оказывает существенного влияния на образ жизни пациента на протяжении многих лет. Многие опухоли растут настолько медленно, что их лечение может быть нецелесообразным (например, это относится к некоторым опухолям предстательной железы).
Вам следует спросить у врача, как обстоит дело в вашем конкретном случае.
Можно ли излечиться от опухоли полностью?
В чем заключается цель лечения опухоли?
Практически в каждом случае лечение опухоли может продлить жизнь больного и улучшить ее качество. При большинстве типов опухолей врачи, исходя из своего опыта, довольно хорошо знают, какую часть больных можно излечить. В настоящее время в лечении опухолей достигнуты определенные успехи, и методы такого лечения, в том числе и химиотерапия, постоянно совершенствуются. Спросите у лечащего врача, каковы перспективы лечения в вашем случае.
Лечение опухоли может увеличить продолжительность жизни и улучшить ее качество.
Обязательно ли вы будете страдать от боли?
На этот вопрос можно дать отрицательный ответ. Многие опухоли не сопровождаются болевыми ощущениями. Кроме того, даже в тех случаях, когда вызванная опухолью боль все-таки возникает, ее можно преодолеть с помощью современных обезболивающих средств. В настоящее время в распоряжении врачей имеются многочисленные методы борьбы даже с очень сильной болью, поэтому, в случае необходимости, лечащий врач назначит вам соответствующие таблетки или инъекции. Некоторые больные сознательно отказываются от приема обезболивающих средств. Если и у вас имеется такое предубеждение, то посоветуйтесь с врачом.
Какой может быть ваша реакция на диагноз опухоли?
Первоначальной реакцией может быть шок или отчаяние. Однако в дальнейшем, как правило, наступает осознание необходимости получить такое лечение, которое позволило бы активно противостоять заболеванию.
Не допускайте того, чтобы ваши психологические реакции стали преградой, мешающей проведению эффективного лечения.
Всегда помните о том, что вы не одиноки. Обратитесь за советом и помощью к своим близким и друзьям. Постарайтесь больше общаться с лечащим врачом. Попросите, чтобы он объяснил все, что вас интересует. Если что-то осталось непонятным, то спросите его еще раз.
Онкологический больной особенно нуждается в психологической поддержке.
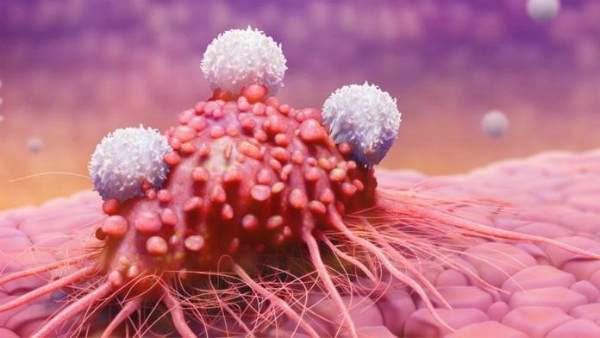
Рак – грозное и опасное онкологическое заболевание. Коварство его заключается в том, что злокачественная опухоль может давать метастазы, распространяясь по всему организму, поражая другие органы и ткани.
Что такое рак?
Раковая опухоль развивается под влиянием различных факторов – внешних (радиация, курение, стрессы, неправильное питание и др.) и внутренних (наследственность). В какой-то момент нормальная клетка мутирует – превращается в атипичную и начинает усиленно делиться, образуя опухоль, сначала очень маленькую. Затем опухоль начинает расти, она выделяет так называемый протеин раковой клетки – токсин, который и вызывает симптомы рака: слабость, отсутствие аппетита, снижение гемоглобина и лейкоцитов.
Такие мутированные клетки постоянно образуются в организме всех людей. Однако иммунная система обнаруживает и уничтожает их до того, как они начинают бесконтрольно размножаться. Но иногда происходит сбой, и клетка не уничтожается, тогда и возникает рак.
Как появляются метастазы
Атипичные раковые клетки отрываются от первичной опухоли и разносятся по организму, образуя в разных местах вторичные очаги – метастазы. Распространяются оторвавшиеся клетки по сосудам: кровеносным и лимфатическим. Попав в орган, некоторое время раковые клетки остаются неизмененными, а затем по неизвестным пока причинам начинают усиленно делиться, образуя новый очаг. Вокруг нового очага образуется сеть кровеносных сосудов, подпитывающих опухоль и способствующих ее росту.
Метастазы гораздо опаснее, чем основная опухоль. Именно они ответственны за те боли, которые испытывает больной, и они чаще всего являются причиной летального исхода.
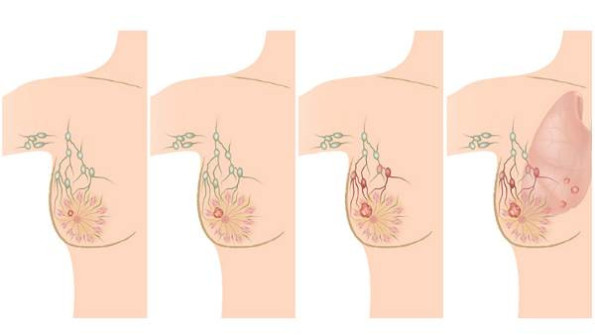
Какие опухоли дают метастазы
Метастазирование у женщин и мужчин имеет некоторые отличия.
У женщин метастазы чаще всего развиваются при раке груди, опухолях почек и щитовидной железы.
У мужчин источником метастазов являются первичные опухоли простаты, легкого и почек.
Чаще всего метастазы затрагивают костную систему, реже всего – кожу.
Как быстро метастазируют опухоли?
Это зависит от многих причин.
Степень дифференцировки. Это условное деление опухолей основано на внешних отличиях раковых клеток от нормальных: при высокодифференцированной опухоли ее клетки внешне схожи с обычными, в случае низкодифференцированного рака его клетки значительно видоизменены. Высокодифференцированный рак метастазирует медленно; низкодифференцированный – намного агрессивнее и распространяется очень быстро.
Возраст больного. У людей молодого возраста метастазы формируются значительно быстрее, чем у пожилых. Очевидно, дело в том, что в молодом организме все процессы, в том числе и рост злокачественных опухолей, происходят быстрее.
Состояние иммунной системы. Крепкая иммунная система может достаточно долго сдерживать рост вторичных очагов, не давая новым образованиям разрастаться.
Психологический настрой. Если человек не верит в успех лечения, у него опустились руки и он не хочет больше бороться с болезнью, то исход заболевания вряд ли будет положительным.
При всех злокачественных опухолях применяются универсальные принципы стадирования, но при каждом типе рака они имеют определенные нюансы. Правильное определение стадии опухоли — одна из первостепенных задач, которая стоит перед онкологом на этапе обследования пациента.
Для чего нужно определять стадию рака?
Определение стадии злокачественной опухоли помогает решать важные задачи:
Стадии злокачественных опухолей TNM
TNM — основная система классификации стадий раковых заболеваний, она была разработана еще в середине прошлого столетия. Последняя, седьмая редакция Классификации TNM была принята в 2009 году. Она останется неизменной до тех пор, пока не накопятся новые технологии диагностики и лечения рака, из-за которых ее придется пересмотреть.
В классификации TNM учитываются три основные характеристики злокачественных опухолей, они соответствуют буквам аббревиатуры:
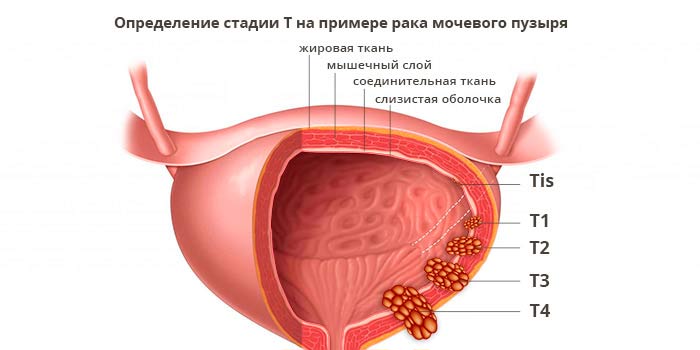
- T — tumor — характеристики первичной опухоли.
- N — nodus — распространение опухолевых клеток в регионарные лимфатические узлы.
- M — metastasis — наличие отдаленных метастазов.
В зависимости от характеристик конкретной злокачественной опухоли, при определении стадии к каждой букве приписывают цифру или специальное обозначение:
Характеристики первичной опухоли (T)
Если нужно уточнить стадию, к цифре дополнительно добавляют букву. Например, M1a при немелкоклеточном раке легкого означает, что опухолевые клетки распространились во второе легкое, либо присутствуют в плевральном выпоте (жидкости вокруг легких), либо в перикардиальном выпоте (жидкости вокруг сердца).
Иногда перед аббревиатурой TNM ставят букву, которая обозначает, каким образом был установлен диагноз:
- p — стадия рака была диагностирована патологоанатомами, после того как опухоль была удалена и оценена под микроскопом;
- c — клинический диагноз, установленный до проведения биопсии по данным обследования.
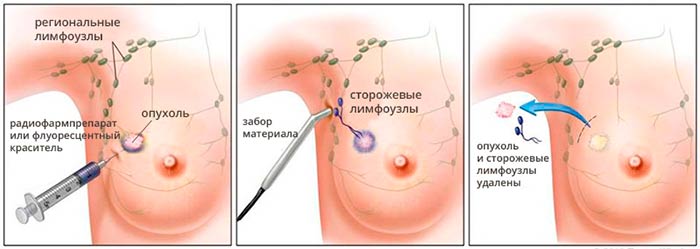
Оценивая результаты сентинель-биопсии, врачи применяют следующие обозначения:
- pNX(sn) — сторожевой лимфоузел не удалось оценить;
- pN0(sn) — в сторожевом лимфоузле не обнаружено метастазов;
- pN1(sn) — в сторожевом лимфоузле обнаружен метастаз.
Другие системы определений стадий опухолевого процесса
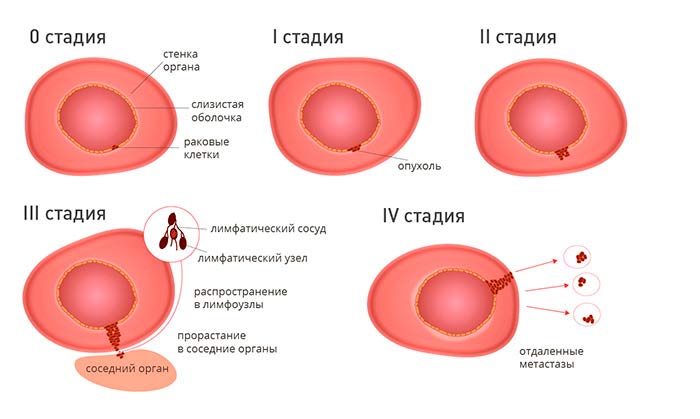
Врачи-онкологи часто используют упрощенную классификацию по стадиям злокачественных опухолевых образований. Она опирается на систему TNM, но в ней выделяют всего пять стадий, которые обозначаются римскими цифрами:
Под микроскопом раковые клетки отличаются от нормальных, и степень этого различия говорит о том, насколько агрессивно они себя ведут. В свою очередь, от этого зависит успешность лечения, вероятность рецидива, прогноз для пациента. Поэтому, наряду с общепринятой классификацией по стадиям, выделяют степени злокачественности рака. Их обозначают буквой G, к которой приписывают соответствующие индексы:
- GX — степень злокачественности онкологического заболевания не удалось оценить.
- G1 — высокодифференцированные опухоли. Опухолевая ткань сильно похожа на нормальную. Такой рак ведет себя наименее агрессивно, редко метастазирует. Прогноз для пациента наиболее благоприятный.
- G2 — умеренно дифференцированная опухоль. Раковые клетки уже довольно сильно отличаются от нормальных и ведут себя более агрессивно.
- G3 и G4 — низкодифференцированные и недифференцированные опухоли. Они отличаются наибольшей степенью злокачественности, ведут себя очень агрессивно, плохо реагируют на лечение.
Для того чтобы оценить, насколько успешно прошло хирургическое лечение рака, иногда онкологи используют специальную постоперационную классификацию:
- RX — сложно проверить, осталась ли опухолевая ткань в организме пациента после хирургического лечения.
- R0 — опухоль в организме пациента после операции отсутствует.
- R1 — обнаружена остаточная опухоль по данным микроскопического исследования.
- R2 — оставшаяся опухоль настолько большая, что обнаруживается при осмотре, без микроскопии.
Некоторые онкологические заболевания не укладываются в рамки общепринятой системы TNM:
- Опухоли у детей — это отдельная категория онкологических заболеваний. Они сильно отличаются от злокачественных опухолей, которые обнаруживаются у взрослых. Для них разработаны специальные системы классификаций, мы не будем их рассматривать в этой статье.
- Рак крови. Такие онкологические заболевания, как лимфома, лейкемия, множественная миелома не могут быть описаны системой TNM, потому что при них чаще всего нет солидной (плотной) опухоли с определенной локализацией. В каждом случае применяется своя специфическая классификация по стадиям.
- Опухоли нервной системы обычно не распространяются за пределы головного и спинного мозга. В настоящее время для них нет единой общепринятой классификации. Чаще всего, определяя стадию при таких онкологических заболеваниях, врачи используют только букву T.
Как определяют стадию онкологического заболевания?
В онкологии применяется много разных методов диагностики. Они обладают разной информативностью, позволяют установить диагноз с разной степенью точности. Соответственно, определить стадию можно тоже разными способами, с разной степенью достоверности. Для этого применяют специальные обозначения:
- C1 — стадия рака определена с помощью стандартных диагностических процедур — осмотра пациента врачом, рентгенографии, эндоскопического исследования. Это наименее точный метод.
- C2 — диагноз установлен на основании специальных, более точных методов диагностики: компьютерной томографии, МРТ, ПЭТ-сканирования, специальных разновидностей рентгенографии, эндосонографии, биопсии и др.
- C3 — выполнено диагностическое хирургическое вмешательство, получен фрагмент патологически измененной ткани, проведено цитологическое и гистологическое исследование.
- C4 — стадия опухоли установлена после полноценного хирургического вмешательства и исследования удаленной опухоли.
Важно понимать: стадия рака не меняется в процессе лечения
Стадию заболевания при раке устанавливают на момент первичного обследования — то есть сразу после того, как диагностировано онкологическое заболевание. Даже если в будущем опухоль уменьшится или, напротив, будет прогрессировать, стадия не изменится. Это важно понимать. Выживаемость и прогноз рассчитываются именно по стадии, которая диагностирована изначально.
Как быстро развивается рак?
За сколько времени рак переходит в 4 стадию? Здесь сроки тоже сильно различаются. Это зависит от агрессивности опухоли, от того, насколько рано больной обратился к врачу, какое проводилось лечение. Например, есть меланома, которая метастазирует очень быстро, а есть базальноклеточный рак кожи — он очень редко дает метастазы.
В онкологии есть такой показатель — время удвоения объема опухоли. Исследования показали, что масса быстрорастущих опухолей легких увеличивается вдвое примерно за 223 дня, а медленнорастущих — за 545 дней. Для аденокарцином этот срок составляет в среднем 303 дня, для плоскоклеточного рака — 77 дней, мелкоклеточного рака легких — 70.
Для того чтобы узнать, за какое время опухоль достигнет объема 1 см3, нужно время удвоения объема умножить на 30. Нехитрые расчеты показывают, что зачастую на это уходят годы.
На какой стадии можно излечиться от рака?
Вероятность ремиссии наиболее высока при стадиях рака 0 и I. Пятилетняя выживаемость таких пациентов приближается к 100%. При II стадии прогноз серьезнее, но у многих пациентов все еще можно добиться ремиссии. При III стадии некоторых больных все еще можно вылечить, остальным показано паллиативное лечение, которое помогает затормозить прогрессирование рака, справиться с мучительными симптомами, продлить жизнь. На IV стадии ремиссия возможна лишь в крайне редких случаях, ее вероятность ничтожно мала. У таких пациентов в основном проводится паллиативное лечение.
Конечно же, это очень обобщенные данные. Всегда нужно говорить не о раке в целом, а о его конкретных типах. Потому что рак бывает разным.
Естественное развитие большинства злокачественных новообразований проходит через четыре главные фазы: малигнизацию (трансформацию) клеток-мишеней, рост малигнизированных клеток, местную инвазию и развитие дистантных метастазов.
Относительная автономность роста опухолей
Одним из кардинальных свойств опухолей является автономность роста — относительная независимость опухоли от воздействия регуляторных систем организма опухоленосителя и приобретение ею способности к самоуправлению.
При аутокринном механизме клетки опухоли могут одновременно секретировать сигналы для пролиферации и рецепторы для них, что позволяет делящимся клеткам неоплазмы не реагировать на внешние регуляторные влияния организма и быть независимыми от них.
Паракринный механизм связан с секрецией факторов роста опухолевыми клетками и действием их на соседние клетки. Более того, в опухолевых клетках может осуществляться синтез цитокинов и факторов роста и воспринимающих их рецепторов, не характерных для нормальных гистогенетических предшественников.
В то же время автономность роста опухоли относительна. Опухолевые клетки для своей жизнедеятельности должны получать из кровотока питательные вещества и кислород, что делает невозможным их существование вне связи с организмом.
Кроме того, они испытывают постоянное влияние со стороны окружающих нормальных клеток, элементов экстрацеллюлярного матрикса стромы. иммунной, эндокринной и нервной систем. Известно также, что на прогрессирование заболевания влияет пол и возраст больного, У молодых рост и развитие опухопи происходит намного быстрее, чем у пожилых; по частоте заболеваемости рак желудка преобладает у мужчин, а меланома кожи — у женщин и т.д.
Кинетика опухолевых клеток
Скорость роста каждой конкретной опухоли индивидуальна и определяется тремя основными параметрами: продолжительностью клеточного цикла, величиной пролиферативного пула (т.е. числом способных делиться кпеток в опухоли) и уровнем преобладания воспроизведения клеток над их потерей.
Размножение клеток в норме осуществляется путем деления. Время, за которое происходит удвоение клетки и осуществляется полноценная передача генетической информации, называют клеточным циклом (циклом деления), или кинетикой клетки.
Клеточный цикл состоит из двух этапов. Более продолжительный из них — интерфаза. Она занимает до 99% всего времени цикла деления клетки и состоит из трех периодов: G1, G2 и S. Во время интерфазы клетка обладает высокой синтетической активностью и занята воспроизведением своих компонентов.
Затем следует короткий период — митоз (М), во время которого завершается процесс разделения на две дочерние клетки. Клетки, возникающие в результате митотических делений и образующие живой организм, называют соматическими. Основные периоды клеточного цикла показаны на рисунке 6.1.

Рис. 6.1. Схема фаз нормального клеточного цикла [по Вольпе П., 1979 с изменениями].
Первая фаза цикла деления — пресинтетический период или G1-период, наступает поспе митоза и составляет около половины всего жизненного цикла клетки. В этот период происходит интенсивное увеличение цитоплазмы клетки, синтезируются и накапливаются вещества, необходимые для репликации (самовоспроизведения) ДНК. В позднем G1-периоде часть клеток могут выходить из клеточного цикла, дифференцироваться и переходить к выполнению своих функций.
Эти клетки, выполнив свою функцию, в конечном счете погибают. Однако как исключение существуют ткани, в которых специализированные клетки могут возвращаться в клеточный цикл, например клетки печени. Такой клеточный цикл называется продленным.
Опухолевые клетки также способны выходить из клеточного цикла, находиться в фазе покоя и вновь возвращаться в клеточный цикл, сохраняя способность к дальнейшему делению.
Вторая фаза — S-период или синтетический, составляет до 30% продолжительности цикла и характеризуется удвоением числа хромосом, в результате чего плоидность клетки возрастает до четырех. При входе в эту фазу клетка всегда проходит и все последующие стадии цикла деления.
Третья фаза — постсинтетический период или G2-период, когда клетка готовится к митозу. В ней происходит интенсивный синтез цитоплазматических белков и белков, связанных с ДНК. G2-период занимает около 19-20% продолжительности всего цикла.
Митоз, или фаза М, — самый короткий по продолжительности период, занимающий примерно 1% времени всего цикла.
В этой фазе в тетраплоидной клетке (общее число хромосом 4n) каждая хромосома разделяется вдоль по длине, образуя две копии (сестринские хроматиды), ядро раздваивается, а цитоплазма делится пополам, и в результате образуются две дочерние клетки. Каждая дочерняя клетка после митоза содержит по две копии каждой хромосомы. Эти копии называются гомологичными хромосомами.
Общее число хромосом в клетке, известное как диплоидный набор, обозначают 2n. Митотическое деление гарантирует постоянство набора хромосом в соматических клетках. Что касается продолжитепьности клеточного цикла, то в норме она варьирует в разных клетках. По классическим представлениям фазы цикла относительно стабильны по продолжительности (в среднем, G1 — 8 ч; S — 6 ч: G2 — 4 ч; М — до 2 ч), а весь цикл занимает у клеток млекопитающих, в среднем, около 20 ч (рис 6.1).
Следует сказать, что одним из ведущих механизмов действия современных противоопухолевых химиопрепаратов является избирательное воздействие на определенные структуры клетки в разные фазы клеточного цикла. Фазовозависимость цитостатиков обязательно учитывается при проведении химиотерапии.
В опухолевых клетках имеются те же фазы, что и в нормальных. Иногда при злокачественном росте встречается прямое деление — амитоз, когда клетка делится без разрушения ядра и ядрышек.
Кишки большинства опухолей обладают такой же и даже большей продолжительностью клеточного цикла, чем клетки нормальных, быстро обновляющихся тканей. Об этом убедительно говорят авторадиографические исследования. Не существует ни одной опухоли, клетки которой достигали бы скорости размножения нормальных костно-мозговых клеток или клеток покровного эпителия кишечника.
Здесь следует отметить, что, к сожалению, более высокий уровень пролиферации клеток в нормальных тканях, чем в некоторых опухолях, является существенным препятствием для их успешного химиолучевого лечения.
Изучение опухолей показало, что их клональный характер не означает одинаковости всех их клеток, особенно — в отношении клеточного цикла. Клеточный состав опухоли обычно представлен необратимо постмитотическими клетками (составляют от 30 до 70% всех клеток опухоли), т.е. не способными делится, вплоть до момента гибели; покоящимися клетками (законсервированы в фазе G0), способными снова войти в митотический цикл (стволовые опухолевые клетки) и клетками с различной продолжительностью фазы G1, составляющие пролиферирующий пул опухолевых клеток и относящиеся к фракции роста (рис. 6.2).

Рис. 6.2. Клеточный состав типичной опухоли [Cajano А. и соавт., 1972].
I — необратимо посмитотические клетки;
II — покоящиеся клетки (способны снова войти в митотический цикл);
Ill — клетки в митотическом цикле с различной продолжительностью фазы G1
Темп роста новообразования и определяется в основном величиной фракции роста. На ранних, субмикроскопических стадиях опухолевого роста подавляющее большинство злокачественных клеток находится в цикле, составляя пролиферативный пул или фракцию роста.
По мере роста опухоли клетки во все более увеличивающемся количестве покидают этот пул вследствие потерь или возвращения в фазу G0. Поэтому ко времени клинического обнаружения опухоли большинство ее клеток не находится в репликационном пуле.
В тоже время многие опухоли, например рак толстой кишки или молочной железы, имеют небольшие фракции роста. Наилучшим, хоть и грубым морфологическим выражением темпа роста опухоли (пролиферативной активности) является частота митозов или митотический индекс (доля митозов в исследуемой популяции клеток).
Их можно оценить просто по количеству фигур митоза в единице площади гистологического среза опухолевой ткани, с помощью проточной цитометрии или методом авторадиографии с меченым предшественником ДНК — Н-тимидином.
Общеизвестно, что от величины фракции роста опухолевых клеток зависит чувствительность новообразования к химиотерапии. Поскольку большинство цитостатиков действуют на клетки, активно синтезирующие ДНК, нетрудно понять, почему опухоли, содержащие, скажем, 5% своих клеток в репликационном пуле, являются медленно растущими, но относительно устойчивыми к химиотерапии.
И напротив, агрессивные, быстро растущие опухоли (лимфомы и др.), имеющие большой пуп делящихся клеток, подчас буквально тают на глазах под влиянием химиотерапии, и лечение может оказаться эффективным.
Среди опухолевых клеток особого внимания заслуживают сравнительно небольшая часть клеток, которые можно охарактеризовать, как опухолевые стволовые клетки (tumor stem cells). Они способны длительное время существовать в организме вне митотического цикла, в периоде относительного покоя и называются еще покоящиеся (G0), клоногенные клетки.
Однако, под влиянием каких-либо стимулов, эти клетки могут выходить из стагнированного состояния, вступать в клеточный цикл и неограниченно делиться, пополняя пуп пролиферирующих клеток, потомство которых расселяется и колонизирует новые участки тканей.
Уровень воспроизведения опухолевых клеток и клеточные потери. Во взрослом организме количество клеток постоянно, так как количество новообразованных и утратившихся тонко и надежно сбалансировано. При развитии опухолей происходит нарушение этого баланса.
Однако по мере увеличения размеров опухоли темп роста снижается, клеточная пролиферация замедляется, клеточные потери увеличиваются вследствие иммунного воздействия и недостаточного кровоснабжения. При этом доминирующий фактор клеточных потерь — ишемический некроз.
Основными причинами возникновения очагов некроза являются уменьшение по мере роста функционирующей сосудистой сети на единицу объема опухоли и сосудистый стаз. Поэтому доля некротизированных клеток по мере увеличения размеров опухоли всегда увеличивается.
Таким образом, темп роста злокачественных новообразований определяется в основном величиной фракции роста (пулом пропиферирующих клеток) и показателем преобладания воспроизведения клеток над их потерей. В некоторых случаях, особенно с относительно большой фракцией роста, это преобладание велико и приводит к быстрому увеличению массы опухоли, а в других случаях оно весьма незначительно.
Так, в карциномах желудочно-кишечного тракта воспроизведение клеток превышает их потерю примерно лишь на 10% и они имеют тенденцию к гораздо более медленному росту.
Инфильтративный рост опухолей
Инфильтративный (инвазивный) рост (от лат. infiltratio — проникновение) заключается в прямом проникновении (прорастании) опухолевых клеток в окружающие ткани и является одним из основных свойств злокачественности.
В отличие от злокачественных, для доброкачественных опухолей характерен экспансивный рост, т.е. при росте они сдавливают и раздвигают (отодвигают) окружающие нормальные ткани.
При этом сдавленные опухолью элементы окружающей ткани атрофируются, но их количество нарастает и образует вокруг опухоли подобие капсулы (псевдокапсула), В тоже время и некоторые злокачественные опухоли (рак почки, околощитовидной железы, фибросаркома) также растут экспансивно.
Артерии обычно не подвергаются инфильтрирующему росту, так как имеющиеся в их стенке эластин и коллагеновые волокна оказывают значительное сопротивление опухолевым клеткам. Высказывается предположение, что резистентности артерий способствует и высокое внутрисосудистое давление.
Понятно, что вследствие инвазивного роста опухоли прорастают в окружающие анатомические структуры и органы и вызывают нарушения соответствующих функций. Именно эти патогенетические особенности злокачественного роста лежат в основе развития вторичных симптомов и клинических феноменов новообразований.
Кроме того, инвазивный рост является обязательным компонентом метастатического каскада: диссеминации опухолевых клеток по организму предшествует их инвазия из первичного очага в окружающие ткани.
Макроскопические формы рака зависят от того, в каком направлении происходит распространение опухолевой массы: в толщу органа (эндофитная) или за его пределы в виде выбухающего узла (экзофитная) (рис. 6.3).

Рис. 6.3. Основные клинико-морфологические формы роста опухолей.
Экзофитная форма — новообразование имеет вид узла, который выступает в просвет полого органа, или распространяется в толще паренхиматозного, или выступает над поверхностью тела и довольно четко отграничен от здоровых тканей. При этом граница опухоли от видимого ее края составляет около 1 см. Независимо от формы роста раковая опухоль характеризуется склонностью к распаду и изъязвлению, что объясняется особенностями ее кровоснабжения.
Экзофитные опухопи при распаде приобретают вид блюдца — язвы с выступающими, подрытыми в виде валика краями. Такие опухоли называют блюдцеобразными. Экзофитные опухоли в паренхиматозных органах представляют собой округлые узлы, при наружном осмотре они обычно не видны.
При длительном росте из-за особенностей кровоснабжения в центре опухолей происходит распад. Такие формы экзофитных опухолей паренхиматозных органов получили название полостных. По характеру происходящих процессов они аналогичны блюдцеобразным ракам полых органов, но по внешнему виду довольно далеки от них.
Эндофитная форма — раковые клетки распространяются преимущественно в пределах стенки органа. В этих случаях стенка или сам орган становятся толще и плотнее, границы опухоли четко не определяются, а микроскопически от видимого края опухоли распространяется приблизительно на 6 см.
Такой характер роста называют инфильтративным, а опухоль — эндофитным, или инфильтративным раком. Инфильтративный рост новообразования в паренхиматозных органах встречается редко и такая форма опухоли называется диффузной.
Обычно такие опухоли выделяют в качестве особых разновидностей, например в легком — перибронхиальная разветвленная и пневмониелодобная формы, в молочной железе — инфильтративно-отечная, маститоподобная и рожистоподобная формы, в печени — инфильтративная, рак-цирроз и т.д.
Инфильтративно рак протекает более злокачественно, отличается быстрым течением, ранним и бурным метастазированием и плохим прогнозом. При распаде эндофитного рака валикообразные края вокруг изъязвления не образуются, а такие опухоли называются язвенно-инфильтративными. Когда наблюдается сочетание экзо- и эндофитного компонентов опухоли, говорят смешанной форме опухолевого роста.
Делению на основные четыре формы рака (экзофитная, блюдцеобразная, инфильтративная и язвенно-инфильтративная) в наибольшей степени соответствуют новообразования желудочно-кишечного тракта. Рак наружных локализаций обычно имеет вид экзофитной или изъязвленной (соответствует блюдцеобразной) опухоли.
Кроме того, вышеназванным формам роста опухолей часто сопутствует так называемый оппозиционный или вовлекающий рост. Он характерен для воспаления, которое часто сопутствует опухолевому процессу, увеличивая объем и размеры опухоли.
Возможность наличия оппозиционного роста необходимо учитывать при планировании специального лечения, а подготовка к операции или лучевой терапии должна включать противовоспалительную и антибактериальную составляющую.
Формирование опухолевого узла из клональных потомков трансформированной клетки — это сложный процесс роста новообразования, на который влияет множество факторов. Среди них ведущими являются: кинетика (динамика) роста опухолевых клеток, опухолевая прогрессия и гетерогенность, а также ангиогенез в опухоли.
Угляница К.Н., Луд Н.Г., Угляница Н.К.
Читайте также:

