Раковые эмболы в сосудах что это

Эмболизация — малоинвазивная процедура, которая может дополнять хирургическое лечение или использоваться самостоятельно. Хирург через прокол в бедренной артерии проводит специальный катетер в артерии, непосредственно питающие опухоль и через него закрывает их специальными частицами — эмболами, которые перекрывают кровоток. В ряде случаев используют эмболы, способные выделять химиопрепарат в ткань опухоли — такое вмешательство называется химиоэмболизация.
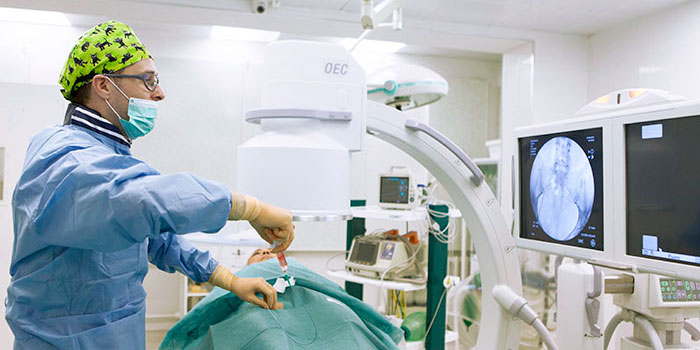
Эмболизация применяется для лечения многих заболеваний. С начала XXI века эта процедура получает все более широкое применение и в онкологии, в первую очередь из-за своей эффективности и малоинвазивности — эмболизации безболезненны, не требуют наркоза, инструмент вводится через пункцию артерии, т. е. нет никакой операционной раны.
Эмболизация у онкологических пациентов
Эмболизация артерий для лечения опухолей и их метастазов помогает решить следующие задачи:
- в качестве самостоятельного метода лечения — эмболизация (чаще всего в варианте химиоэмболизации) может приводить к ишемии ткани опухоли и ее гибели. Для некоторых заболеваний, например, ряд опухолей печени, этот лечения может приводить к полной ремиссии без хирургического лечения.
- в сочетании с хирургическим лечением эмболизация используется как вспомогательная технология — чаще всего для уменьшения кровотечения во время операции за счет деваскуляризации (обескровливания) новообразования;
- в ряде случаев эмболизация, выполненная перед операцией, дает возможность проведения более радикальной операции за счет предварительного уменьшения опухоли;
- эмболизация также может применяться для борьбы с симптомами и осложнениями онкологических заболеваний — это в первую очередь остановка опасных кровотечений, которые угрожают жизни пациента, кроме того — облегчение боли, вызванной злокачественным новообразованием; еще одним эффектом является уменьшение объема и замедление роста опухоли.
Виды эмболизации артерий у онкологических больных:
- предоперационная — выполняется в качестве первого этапа хирургического вмешательства;
- в качестве самостоятельного метода лечения — чаще всего при опухолях печени, почек и ряде других опухолей
- в качестве паллиативного метода лечения — для остановки кровотечений, уменьшения болевого синдрома, уменьшения объемов и темпа роста опухоли.
Как проводится эмболизация артерий?
Эмболизация выполняется врачами-рентгенохирургами в специально оборудованной ангиографической операционной. Перед эмболизацией всегда проводят ангиографию. В сосуды вводят рентгенконтрастное вещество, в ходе чего записывают рентгеновское изображение в цифровом видеоформате. Это помогает врачу оценить расположение и анатомию сосудов, определить, из каких артерий осуществляется кровоснабжение опухоли.
Чаще всего эмболизацию выполняют под местной анестезией. В редких случаях приходится использовать общую анестезию (наркоз). За 4–5 часов до процедуры пациента просят ограничить прием пищи, иногда дают успокоительные препараты.
В большинстве случаев доступ к нужному сосуду получают через бедренную артерию, это самый типичный доступ для всех ангиографических исследований и вмешательств, но могут использовать и другие артерии в других местах (лучевую на запястье, плечевую в области локтевого сгиба и т. п.). Врач обрабатывает кожу антисептиком и делает небольшой прокол, вводит в артерию специальный катетер размером не более 1,5 мм и продвигает его до тех пор, пока не достигнет нужного сосуда. Через катетер в сосуд вводят эмболы, которые перекрывают его просвет.
Существуют разные виды эмболов:
- Поливинилалкоголь (PVA) представляет собой частицы размером от 50 до 1000 мкм. Это относительно недорогой и простой в применении препарат, однако, в настоящее время он считается устаревшим. Сейчас чаще всего применяют сферические эмболы, например, Bead Block и Embozene.
- Спирали из платины и нержавеющей стали. После установки в просвете сосуда на них быстро образуется тромб, который перекрывает кровоток. Иногда такие спирали применяют вместе с желатиновыми губками: сначала устанавливают спираль, а затем через катетер вводят губку — ее частички оседают между витками. Их применяют только для остановки кровотечений, обусловленных опухолями.
- Химиоэмболизация — введение в просвет сосуда эмболов, содержащих химиопрепарат. Таким образом, с одной стороны происходит закупорка сосудов, кровоснабжающих опухоль, а с другой химиопрепарат поступает непосредственно в ткань опухоли и не оказывает побочные эффекты, которые возникают при его введении в вену. При этом в самой опухоли создаются очень высокие концентрации препарата, невозможные при обычном введении. Мы применяем самые современные препараты для химиоэмболизации: DC Beads (Terumo, Япония) и Hepaspheres (Merit Medical, США)., которые высвобождают химиопрепарат в течение длительного времени, в стабильной дозировке.
- Радиоэмболизация — введение эмболов, содержащих радиоактивные изотопы. Эта процедура еще называется внутренней лучевой терапией, так как в опухоль изнутри вводят дозу радиации, разрушающей ее клетки. Для этого обычно используют изотоп Иттрий-90.
К эмболизации артерий наиболее часто прибегают при следующих онкологических заболеваниях:
- В качестве самостоятельного метода лечения: Первичные и метастатические опухоли печени, почек, легких и других локализаций.
- В комбинации с хирургическими методами: Первичные и метастатические опухоли печени, почек, легких, костей, позвоночника, матки, простаты, мочевого пузыря и т. д.
- Для остановки кровотечений при опухолях: малого таза, легких, прямой кишки, толстой кишки, печени, матки, простаты, опухолях головы и шеи. Т. е. практически при любой локализации с целью прекращения кровотечения.
Эмболизация также широко применяется для лечения заболеваний, не связанных с онкологией:
- Миома матки. Эмболизация маточных артерий — наименее травматичный способ лечения миомы матки, обладающий высокой эффективностью — около 98,5% женщин, перенесших эту процедуру, не нуждаются в дополнительном лечении.
- Аденома простаты. Эмболизация - эффективный, малоинвазивный способ лечения аденомы предстательной железы, который сегодня становится все более распространен в развитых странах.
- Варикоцеле — наименее инвазивная альтернатива хирургическому лечению, выполняется амбулаторно за 20–30 минут.
- Сосудистые мальформации различной локализации.
- Аневризмы — в первую очередь аневризмы головного мозга, способные вызвать геморрагический инсульт.
Насколько безопасна эмболизация?
Цель эмболизации в онкологии — не только прекратить приток крови к патологическому очагу, но и сохранить при этом кровообращение в соседних здоровых тканях. Современная техника эмболизации с использованием микрокатетеров позволяет обеспечить необходимую точность эмболизации.
Для того чтобы обеспечить точность в ходе эмболизации всегда проводят ангиографию. Врач внимательно изучает сосудистую сеть, кровоснабжение опухоли и определяет, в какой сосуд должны быть введены эмболы. Эмболы вводятся только после детального изучения сосудистой анатомии опухоли в ходе вмешательства. Перед эмболизацией вам также могут назначить УЗИ, КТ, МРТ и другие исследования.
Существует ряд противопоказаний к проведению эмболизации, но все они являются относительными, то есть процедура, как правило, все же может быть проведена при соблюдении некоторых условий. Например, у пациента с нарушением функции почек должно быть нормализовано артериальное давление, водно-солевой баланс, а во время ангиографии нужно использовать минимальное количество контрастного вещества.
В Европейской клинике с каждым пациентом работают индивидуально. Врач оценивает общее состояние больного, учитывает сопутствующие заболевания, размеры и расположение опухоли, особенности ее кровоснабжения.
Врачи-специалисты Европейской клиники имеют огромный опыт проведения эмболизации артерий при различных видах опухолей. Мы используем значительный собственный и опыт коллег из ведущих зарубежных клиник. Некоторые процедуры, которые мы предлагаем пациентам в Европейской клинике (например, эмболизация при аденоме простаты), даже в Европе, США и Израиле являются прерогативой крупных университетских клиник из-за необходимости иметь хирургов самого высокого уровня.
Нашими врачами были выполнены первые в России эмболизации миомы матки, артерий простаты, мы первыми стали работать с самыми современными препаратами для эмболизации — Bead Block, Embozene, DC Bead и др.
Общеизвестно, что дистантное распространение по лимфатическим и кровеносным сосудам (метастазирование) — это высшее выражение автономности опухоли, главный отличительный признак злокачественного процесса и наиболее частая причина смерти больных.
Способность к метастазированию позволяет опухолевым клеткам покидать первичную опухоль и колонизировать новые территории, где, по крайней мере, вначале нутриенты и пространство для роста не ограничены.
Важным и необходимым условием метастазирования является способность опухоли формировать собственную сосудистую сеть. Образование сосудов в опухоли, а следовательно, и процесс метастазирования может начаться, когда количество неоппастических клеток составит более 10 3 (1-2 мм).
Однако на практике опухоли разного гистогенеза имеют различную критическую массу, необходимую для метастазирования. В целом, считается, что более крупные и менее дифференцированные опухоли обладают большим инвазивно-метастатическим потенциалом, хотя это и не абсолютная закономерность.
Довольно часто при очень больших размерах, глубокой инвазии опухоли и даже при наличии карцинемии как отдаленные, так и регионарные метастазы могут и не выявляться.
Данный факт объясняется отсутствием гено- и фенотипических свойств инвазивности опухолевых клеток и соответствующей протйвомтастатической сопротивляемостью организма. Не вся опухоль а лишь субклон(ы) клеток внутри нее в ходе опухолевой профессии приобретают способностью к метастазированию и для этого должно пройти достаточное время.
Метастазирование (греч. metastasis — перемена места, перемещение, перенос) — это перенос по сосудам (лимфатическим, кровеносным) неоппастических клеток за пределы первичной опухоли в различные органы и ткани с образованием вторичных опухолевых узлов той же гистологической структуры. Понятно, что интравазальное распространение или обсеменение клетками естественных полостей имеет большое прогностическое значение.
Метастазирование — это сложный биологический процесс, результат взаимодействия опухоли и организма и абсолютный признак злокачественности, его мопекулярно-генетические механизмы изложены ранее. В данном разделе представлены клинические аспекты данной проблемы.
Феномен метастазирования опухолей впервые описал Жан Клод Рекамье (1829) на примере метастаза рака молочной железы в головной мозг; он же впервые ввел терминологию, которой мы пользуемся до настоящего времени.
Приблизительно 30% впервые выявленных злокачественных опухолей уже имеют метастазы. Такое развитие событий выражается в многократном увеличении негативного клинического эффекта, оказываемого первичным узлом, сильно ограничивает возможности лечения и нередко, в гораздо большей мере, способствует наступлению смерти, чем существование первичной опухоли.
По сути, метастаз — это спонтанный аутотрансплантат опухоли в виде опухолевых эмболов, которые не всегда могут быть источником метастазов и часто погибают от недостатка питания или под действием иммунной системы.
Вновь сформированные метастазы появляются как симбиоз опухолевых и поддерживающих клеток из нормальных тканей. Пути распространения злокачественных клеток из первичного очага могут быть различными. Чаще всего они распространяются по лимфатической системе.
Лимфогенное метастазирование
После осуществления метастатического каскада злокачественные клетки могут проникать в лимфатический сосуд и с током лимфы попадают в первые (регионарные и/или нерегионарные) на их пути лимфатические узлы (органные и/или внеорганные). В норме узлы выполняют две антиметастатические функции. Первая (кратковременная) — механическая, барьерная — заключается в чисто механическом ограничении диссеминации опухолевых клеток.
Вторая — иммунологическая — обусловлена усиленной продукцией иммунокомпетентных клеток, способных лизироватъ поступающие в узел опухолевые клетки, что, однако, далеко не всегда служит препятствием к их росту.
В случае преодоления этих барьеров и прогрессирующего размножения злокачественных клеток, в лимфатических узлах формируются типичные лимфогенные метастазы. Такой механизм их формирования называется классическим, ортоградным. Однако в лимфатических сосудах опухолевые клетки могут перемещаться в разных направлениях.
В частности, при поражении всех лимфатических путей органа происходит блокада лимфооттока на уровне лимфатических сосудов и регионарных узлов При этом в зависимости от градиента давления лимфы и в связи с отсутствием клапанов внутри капилляров возможно распространение опухолевых клеток по лимфатическим сосудам в обратном направлении (ретроградные метастазы), что свидетельствует о плохом прогнозе.
Наконец, опухолевая блокада типичных путей лимфооттока может сопровождаться возникновением парадоксальных направлений лимфогенного метастазирования и поражением лимфатических узлов, не регионарных для органа, где находится первичная опухоль.
Например, появление метастазов рака грудного отдела пищевода в кардиальные лимфоузлы объясняется не ретроградной циркуляцией, а эмболией раковых клеток книзу по лимфатическим капиллярам стенки пищевода.
Лимфогенное метастазирование типично дпя рака и меланомы. Саркомы хотя и могут давать лимфогенные метастазы, но используют этот путь реже и позже и в тоже время — это прогностически крайне неблагоприятно. Возможность образования, а тем более наличие в регионарных лимфоузлах метастазов, обосновывает необходимость их удаления при радикальных операциях для достижения абластичности оперирования.
Гематогенное метастазирование называют еще отдаленным и связано оно с проникновением опухолевых клеток в кровеносные сосуды, где они формируют микротромбоэмболы.
Вирховские законы эмболии, в целом, действуют и при эмболии опухолевой. Так, колоректальные раки метастазируют ортоградно (по току крови) по системе воротной вены в печень. Однако, не только пассивный перенос опухолевых клеток важен при эмболии. Метастатические очаги могут возникать из эмболов, минующих малый круг (например, в мозге) через анастомозы и позвоночные сосуды (при раке легкого).
Избирательность метастазирования не всегда связана с анатомией его сосудистых путей. Например, многие карциномы (легкого, простаты, почек, щитовидной и молочной железы) часто метастазируют в кости. Установлена возможность ретроградного распространения по сосудам злокачественных клеток, связанная с их активной локомоцией и блоком венозных путей оттока.
Доказано, что количество метастазов коррелирует со степенью развития кровеносной системы опухоли. Так, меланома, не выходящая за пределы базальной мембраны эпидермиса и не васкуляризированная, не проявляет склонности к метастазированию.
В целом, для злокачественных новообразований характерна последовательность распространения злокачественных клеток — вначале лимфогенного, затем гематогенного. Объясняется это рядом морфологических обстоятельств.
Во-первых, общеизвестно, что многие карциномы возникают в органах, изначально богатых лимфатическими сосудами (легкие, молочная железа, кишечник и др.), и поэтому они метастазируют в первую очередь лимфогенным путем, а в органах, бедных такими сосудами (печень, почки) — сразу же гематогенно.
В тоже время, необходимо отметить, что органы и ткани, которые исключительно редко затрагиваются метастатическим процессом, — единичны. К ним относятся, например, селезенка (но не при лимфомах и лейкемиях), скелетная мускулатура, а также миокард.
В-четвертых, в последовательности метастазирования играют определенную роль и биохимические различия лимфы и крови, определяющие циркуляцию, адгезию и другие процессы.
Имплантационное метастазирование
Имплантационное метастазирование происходит в случае, если опухоль прорастает в плевральную, перикардиальную, перитонеальную полость или субарахноидальное пространство. Так возникает карциноматоз брюшины, плевры и т.д. (типичный пример — метастаз Шницлера в брюшину дугласова пространства при раке желудка). Более редко наблюдаются другие формы метастазирования злокачественных опухолей.
Прививочные метастазы — возникновение опухоли в послеоперационных рубцах после удаления злокачественного новообразования. Наиболее частой причиной таких метастазов является нарушение правил абластики и антибпастики во время операции.
Метастазирование по продолжению (per contituitatem). Примером такого метастазирования является периневральное распространение опухолевых клеток при раке предстательной железы, прямой кишки и т.д. Для данного вида метастазирования характерны постоянные, сильные и трудно купируемые боли.
Вместе с тем они способны возвращаться в клеточный цикл в любое время и, таким образом, давать начало выявляемым клинически метастазам, иногда через весьма продолжительное время после обнаружения и/или удаления первичной опухоли.
Таким образом, в настоящее время достаточно полно изучены механизмы и маршруты метастазирования, локализация регионарных и отдаленных метастазов (которые в значительной мере определяются особенностями лимфо- и гемодинамики пораженного опухолью органа); время возникновения (хронология метастазирования); частота.
Эти сведения необходимо учитывать при диагностике, классификации по стадиям и по системе TNM, планировании и осуществлении специального лечения, определении индивидуального прогноза. Значительно меньше изучен вопрос, какие причины обусловливают развитие метастазов.
Клинические особенности метастазирования
1. Не вызывает сомнения, что метастазирование — это функция времени. Считается, что карцинемия является основным признаком и условием метастазирования опухопи. В 80-90% случаев опухолевые клетки можно обнаружить в крови даже в ранние сроки опухолевого процесса.
Однако большинство опухолевых клеток до определенного времени вследствие воздействия противоопухолевых механизмов защиты организма погибает. Поэтому нахождение опухолевых эмболов в кровеносных сосудах стромы опухоли имеет существенно более неблагоприятное прогностическое значение, чем карцинемия.
Полагают, что избирательность метастазирования связана с рядом факторов: анатомические особенности кровоснабжения опухоли; общность антигенных свойств опухоли и органа, где развился метастаз; способность раковых клеток реагировать на характерные для того или иного органа местные цитокины, обеспечивающие соответствующую направленную миграцию и успешное приживление метастаза; особенности метаболизма и местного иммунитета в органах, что определяет их противоопухолевые свойства.
Из особенностей кровоснабжения необходимо, например, указать на возможность быстрого метастазирования дифференцированного рака щитовидной железы вследствие отрицательного давления в системе вен и лимфатических сосудов железы в норме.
Установлено, что избирательная локализация метастазов рака молочной железы в легком обусловлена способностью раковых клеток железы отвечать пролиферацией на цитокины легочного происхождения.
С другой стороны, хотя главными в инвазии представляются все же свойства самих опухолевых клеток, не все нормальные ткани подвержены опухолевой инвазии в одинаковой степени. Например, капсулы печени и почки, периост часто ограничивают распространение опухолей при непосредственном контакте с ними. Существенным барьером на пути опухолевой инвазии является хрящ, стенка артерий, фиброзная ткань.
3. Более раннее и обширное метастазирование чаще наблюдается у лиц молодого возраста.
4. Склонность злокачественных опухолей метастазировать определяется их морфологией: недифференцированные обычно метастазируют чаще, чем высокодифференцированные. Однако из этого правила имеются исключения. Так, независимо от степени дифференцировки. базалиомы, тимомы, хондросаркомы и глиомы метастазируют редко, в то же время как высокодифференцированные опухоли щитовидной железы и надпочечников метастазы дают часто.
5. Метастазирование учащается по мере роста опухоли. Чем больше размеры опухоли, тем выше вероятность отделения и миграции отдельных клеток или их комплексов.
Существуют, однако, и многочисленные исключения из этого правила: широкая лимфогенная и гематогенная диссеминация небольших по объему опухолей (Т1) и отсутствие метастазов при далеко зашедшем раке (Т4). Более того, у некоторых больных вначале клинически проявляются метастазы и лишь спустя несколько лет — первичная опухоль (оккультные формы рака).
6. Часто метастазы выявляются после травмы опухоли или ее удаления. При этом распространение клеток из первичной опухоли через лимфатические пути осуществляется в течение нескольких секунд. Вероятно, различные манипуляции могут способствовать поступлению (выталкиванию) опухолевых клеток в лимфатические пути.
7. Общей закономерностью является преобладание лимфогенного, лимфогематогенного и имплантационного путей метастазирования злокачественных эпителиальных опухолей (раки) и гематогенного — злокачественных неэпителиальных опухолей (саркомы).
Лишь саркомы матки, имеющей развитую лимфатическую сеть, могут вначале распространяться лимфогенным, а затем гематогенным путем. При одинаковой инвазирующей активности в отношении лимфатических структур саркоматозных и раковых клеток, преимущественно гематогенное метастазирование при саркомах пока не имеет убедительного объяснения.
Отчасти это можно объяснить различиями в строении поверхностных мембран опухолевых клеток. Предполагается также, что саркомы обычно возникают в органах, бедных лимфатической сетью (кости, мышцы и др.). и именно поэтому им характерны почти исключительно гематогенные метастазы.
8. Стресс и метастазирование. В последние годы большое внимание в механизмах противометастатической сопротивляемости организма уделяется стрессу, как реакции организма на злокачественную опухоль.
В общем виде постулируется, что к усилению метастазирования приводит повышение активности гипоталамо-гипофизарного комплекса и коры надпочечников. Нормальная функция эпифиза, вилочковой железы и лимфоидной ткани препятствует метастазированию.
Угляница К.Н., Луд Н.Г., Угляница Н.К.
Эмболизация при раке
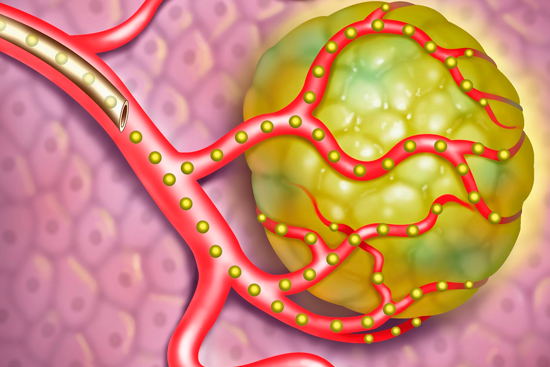
Эмболизация при раке относится к малоинвазивным методикам лечения онкозаболевания, применяется при многих видах раковой опухоли, но в большинстве случаев – при злокачественных новообразованиях печени. Цель процедуры – закупорить (перекрыть) кровеносные сосуды, питающие онкоочаг. Без кровообращения атипичные клетки прекращают распространение, что ведет к уменьшению, разрушению и гибели опухоли.
Эмболизация при раке — это современный прогрессивный метод борьбы с метастазами в труднодоступных местах, когда оперативное удаление опухоли представляет определенные трудности. Методика активно используется при крупных онкообразованиях, во время подготовки к оперативному вмешательству.
Эмболизация при раке осуществляется тремя способами:
- Артериальная или трансартериальная (ТАЭ) эмболизация – применяется при опухолях печени и матки. В артерию вводится катетер, через который подается эмболизирующий агент, приводящий к обструкции сосуда.
- Химиоэмболизация – комбинация ТАЭ и химиотерапии проводится одним из двух вариантов. Первый – цитостатики предварительно покрывают частицами эмболизирующего вещества. Второй – через катетер в артерию вводят химиопрепарат, затем просвет сосуда закупоривают.
- Радиоэмболизация – комбинация эмболизации и облучения заключается в доставке микросфер (радиоактивные частицы) в артерию, которые оседают рядом с онкоочагом, выделяя радиоактивное излучение на протяжении нескольких часов или дней.
Эмболизация при раке используется в трех вариантах:
- Основной самостоятельный метод лечения.
- Паллиативная помощь – на последних стадиях онкопроцесса для устранения болевого синдрома, купирования кровотечения, уменьшения побочных эффектов и осложнений болезни.
- Предоперационная эмболизация – используется при больших объемах опухоли для уменьшения ее размеров и улучшения операционного доступа, а также для снижения кровопотери во время операции.
Ее применяют как отдельный метод, так и в составе комплексного лечения, сочетая с лучевой или химиотерапией
Эмболизация при раке является перспективной альтернативой хирургическому вмешательству в онкологии благодаря своим преимуществам:
- Малотравматичная технология, не оставляющая рубцов, как после операции.
- Минимальный риск инфицирования и других осложнений.
- Отсутствие кровотечения после процедуры.
- Нет особой необходимости в применении общей анестезии. Это особенно актуально для лиц с непереносимостью медикаментозных средств.
- Восстановление в кратчайший период.
- Высокая эффективность.
- Сохранение целостности тканей.
- Возможность применения при неоперабельных формах онкозаболеваний.
- Минимальное токсическое воздействие.
- Возможность подбора доз эмболизирующего агента индивидуально, в зависимости от вида новообразования, локализации, стадии.
- Вероятность развития побочных эффектов сведена к минимуму.
- Не требуется длительная госпитализация.
- Возможность проведения манипуляции несколько раз до получения терапевтического эффекта без вреда для других органов и организма в целом.
Недостатки эмболизации немногочисленны. Назначается процедура индивидуально и подходит не для всех случаев. Проводить манипуляцию должен высококвалифицированный опытный специалист. При неопытности хирурга эмбол может проникнуть в здоровые ткани, и привести к осложнениям.
Химиоэмболизация при раке печени эффективна благодаря анатомическим особенностям. Ветви печеночной артерии кровоснабжают новообразования печени. Трансартериальная эмболизация закупоривает ветви, при этом не нарушая работу здоровых тканей, которые кровоснабжаются другим источником (ветвями воротной вены). При некоторых видах опухолей печени можно рассчитывать на полное выздоровление благодаря ТАЭ.
Эмболизация при раке шейки матки чаще сочетается с химиотерапией и лучевой терапией, включает три этапа. Первый этап – проведение двух курсов химиотерапии. Второй этап – двухсторонняя эмболизация маточных артерий при раке шейки матки, проводится через день—два после второго курса химиотерапии в рентген операционной. Третий этап – через неделю после ТАЭ выполняется облучение. Недостаток данного метода – системное воздействие цитостатика на организм.
Эмболизация при раке легких показана, когда у больного наблюдается кровохарканье, либо имеются противопоказания к операции или облучению. Для механической окклюзии используются в основном микроскопические волокна тефлонового велюра. Для химической – гипертонический раствор или этиловый спирт. Эмболизацию бронхиальных артерий проводят с гемостатической целью и с целью введения химиопрепаратов в зону опухоли. Улучшение наблюдается у 90% пациентов.
Эмболизация при раке почки показана при невозможности проведения полноценного оперативного вмешательства по тем или иным причинам. Через катетер, подведенный к сосудам пораженной почки, вводят эмбол (желатинообразный, пластиковый шарик), который закупоривает сосуд. Развитие опухоли замедляется или полностью останавливается. Когда состояние больного позволяет проводят нефрэктомию. В некоторых случаях методику используют перед оперативным вмешательством для снижения уровня кровопотери.
Эмболизация используется в различных областях медицины, например, в сосудистой хирургии вен нижних конечностей, в гинекологии при миоме матки, но в онкологии эту методику считают экспериментальной. Еще нет достаточных исследований, долгосрочных прогнозов, поэтому возможность проведения этой малоинвазивной операции рассматривают у каждого больного в отдельности.
Ограничения к выполнению процедуры связаны с конкретным диагнозом. Противопоказания в основном относительные:
- Гепатит, цирроз.
- Декомпенсированная почечная, печеночная, сердечная, дыхательная недостаточность.
- Асцит.
- Венозное кровотечение при варикозной болезни.
- Бронхолегочная эмболия.
- Объемные полости распада в онкоочаге.
- Невозможность надежной фиксации катетера.
- Генерализованный онкопроцесс.
- Непереносимость рентгеноконтрастного вещества.
- Аномалии артерий.
- Острый инфекционный процесс.
- Беременность.
- Болезни, связанные с нарушением свертываемости крови.
- Операбельный рак матки.
Вопрос о целесообразности эмболизации решается в каждом конкретном случае и зависит от состояния пациента.
Эмболизация при раке осуществляется в основном амбулаторно. Предварительно проводится диагностика. Главный метод обследования – ангиография с контрастированием, позволяющая оценить состояние сосудов, выявить источники кровоснабжения ракового очага.
Особой подготовки не требуется, но больной не должен есть и пить за 4–5 часов до операции. Для выполнения манипуляции общий наркоз используется редко, чаще – местное обезболивание. После обезболивания прокалывают артерию в нужном месте, вводят микрокатетер, через который запускается эмбол. В качестве эмболизирующих материалов используются:
- Жидкие вещества – удобны тем, что свободно проникают через сосудистые разветвления.
- Клееподобные вещества – превращаются в полимер после реакции с ионами.
- Вязкие материалы – применяются в качестве химиоэмболизации преимущественно при онкозаболеваниях печени.
- Склерозирующие – уплотняют эндотелий, используются для эмболизации некрупных сосудов.
- Микрочастицы – нужны для окклюзии мелких сосудов.
- Желатиновая губка или гель-пена – вызывает временную закупорку.
- Акриловые микросферы – вызывают постоянную окклюзию.
- Спирали – приводят к мгновенному тромбообразованию.
Для предупреждения осложнений после эмболизации ее проводят на фоне антибиотикотерапии.
По данным исследований и наблюдений, если процедура прошла успешно, и удалось закупорить сосуд, по которому происходит кровообращение опухоли, то пациент начинает чувствовать себя лучше, отмечается уменьшение болевого синдрома. У некоторых больных боли проходят довольно быстро, если удается полностью закупорить все сосуды, питающие опухоль. В некоторых случаях, если образование получает кровоснабжение из нескольких ветвей или хорошо развиты коллатерали, манипуляция оказывается неэффективной.
Эффективность эмболизации оценивается по следующим критериям:
- Регрессия полная – исчезновение проявлений заболевания, выздоровление.
- Регрессия частичная – уменьшение размеров онкоочага на 50% и более, отсутствие других очагов поражения.
- Стабилизация – объем пораженного органа уменьшается менее, чем наполовину, отсутствие новых очагов.
- Прогрессирование – увеличение объемов пораженного органа на 25% и более, появление новых онкоочагов.
Неэффективность эмболизации может быть связана с анатомическими особенностями, формой раковой опухоли, отсутствием опыта у врача. Некоторые виды опухолей при метастазировании могут трансформироваться в быстрорастущую форму, поэтому перед процедурой следует провести тщательное обследование больного.
Метод эмболизации исследуется и апробируется врачами-исследователями разных стран. Специалисты считают, что в скором времени с развитием микроэндоскопической техники, его можно будет использовать для лечения рака разных локализаций. Уже сейчас в ведущих онкологических центрах для визуализации кровеносного русла используют новейшую аппаратуру, работающую по принципу МРТ в режиме реального времени. Это облегчает проведение и улучшает эффективность процедуры.
Читайте также:

