Рак вульвы и беременность
Вульва — это наружная часть женских половых органов, которая представлена преддверием влагалища, большими и малыми половыми губами, клитором. В этой области могут возникать злокачественные опухоли. Чаще всего они поражают клитор, внутреннюю поверхность больших половых губ и малые половые губы.
Причины и факторы риска рака вульвы
В настоящее время ученым известно два механизма возникновения рака вульвы. У молодых женщин (особенно у курящих) чаще всего встречаются опухоли, связанные с инфицированием вирусом папилломы человека. Вероятно, проникая в клетку, возбудитель может вызывать изменения в генах, которые приводят к производству аномальных белков и, как следствие, бесконтрольному размножению клеток.
У женщин старше 55 лет чаще всего нет инфекции ВПЧ, но у них обнаруживается мутация в гене p53, который играет важную роль в предотвращении онкологических заболеваний.
Помимо папилломавирусной инфекции, известны и другие факторы риска рака вульвы:
- Возраст. На женщин младше 50 лет приходится менее 20% случаев, а на женщин старше 70 лет — более 50%.
- Курение. Традиционно воздействие табачного дыма принято связывать с повышенным риском рака легких. Но на самом деле курение повышает риск многих онкологических заболеваний.
- ВИЧ-инфекция. Вирус иммунодефицита ослабляет защитные силы организма и повышает риск инфицирования ВПЧ.
- Интраэпителиальная неоплазия вульвы. Является предраковым заболеванием. В области вульвы появляются аномальные клетки, поначалу они находятся в поверхностных слоях кожи, но со временем могут трансформироваться в рак.
- Диагностированный рак шейки матки. При этом имеется повышенный риск рака вульвы.
Классификация рака вульвы
Наиболее распространенный тип рака вульвы — плоскоклеточная ороговевающая карцинома. Как правило, она развивается у пожилых женщин (старше 55 лет). Реже встречаются бородавчатые и базалоидные (как правило, у молодых женщин), поверхностные плоскоклеточные карциномы.

В 8% случаев злокачественные опухоли вульвы представлены аденокарциномами, которые происходят из железистых клеток. Как правило, они развиваются в бартолиновых железах. Эти железы расположены в толще больших половых губ, они увлажняют влагалище во время половых актов. Нередко опухоли бартолиновых желез ошибочно принимают за кисты. Иногда аденокарциномы развиваются из клеток потовых желез, которые находятся в области наружных женских половых органов.
В редких случаях в области вульвы встречаются базальноклеточные карциномы (разновидность рака кожи).
В 6% случаев в области вульвы встречаются меланомы — злокачественные опухоли, которые происходят из клеток, продуцирующих пигмент меланин. Такая локализация для меланомы не совсем характерна, чаще она возникает на открытых участках кожи, на которые воздействуют солнечные лучи.
Классификация рака вульвы по стадиям:
- 1 стадия: при 1 стадии опухоль, которая растет в пределах вульвы и не поражает соседние органы, лимфатические узлы.
- 2 стадия: при 2 стадии опухоль, которая проросла в соседние структуры, такие как мочеиспускательный канал, влагалище, анус.
- 3 стадия: на 3 стадии опухоль, при которой раковые клетки распространились в лимфатические узлы.
- 4 стадия: при 4 стадии рака вульвы поражение лимфатических узлов более выраженное по сравнению с 3 стадией, наблюдается прорастание опухоли в верхнюю часть мочеиспускательного канала, влагалища, в мочевой пузырь, прямую кишку, кости таза, наличие отдаленных метастазов.
Стадия опухоли определяет подходы к лечению и дальнейший прогноз.
Как кодируется рак вульвы в МКБ 10?
В Международной Классификации Болезней для рака вульвы предусмотрены следующие коды:
Симптомы рака вульвы
Предраковые изменения и ранние стадии рака вульвы могут не иметь симптомов. Когда опухоль прорастает глубже, и раковые клетки начинают распространяться в лимфатические узлы, практически у всех женщин возникают некоторые проявления:
- Участок кожи в области вульвы, который отличается от окружающей здоровой ткани: он может быть светлее или темнее, иметь красноватый или розовый цвет.
- На коже появляется уплотнение, бляшка, бородавка, язвочка.
- Возникает зуд, жжение, боли.
- Многих женщин беспокоят кровотечения из влагалища вне месячных.
Чаще всего эти симптомы вызваны не онкологическим заболеванием. Но всегда есть небольшая вероятность того, что это рак.
Аденокарцинома, которая развивается из бартолиновой железы, выглядит как образование в области половых губ, которое можно прощупать. Аналогичными симптомами проявляется киста.
Диагностика рака вульвы
Основной метод диагностики рака вульвы — биопсия. Изучение образца тканей под микроскопом помогает с высокой точностью отличить доброкачественное образование от злокачественного. Для того чтобы понять, из какого места брать ткани, врач осматривает вульву с помощью кольпоскопа, обрабатывает кожу раствором уксусной кислоты или толуидинового синего: в результате патологические очаги становятся более заметны.
По показаниям (если опухоль большая, и есть подозрение, что она распространилась за пределы вульвы) назначают другие методы диагностики:
- Эндоскопическое исследование мочевого пузыря и прямой кишки.
- КТ и МРТ помогают обнаружить очаги опухолевого роста в лимфатических узлах, различных органах.
- Рентгенографию грудной клетки проводят для поиска метастазов в грудной клетке.
- ПЭТ-сканирование — эффективный метод поиска отдаленных метастазов.

Лечение рака вульвы
При раке вульвы прибегают к классической триаде лечения в онкологии: хирургии, химиотерапии и лучевой терапии. Основным фактором, определяющим лечебную тактику, является тип и стадия опухоли. При облучении рака вульвы врач принимает во внимание возраст женщины, ее общее состояние здоровья и сопутствующие заболевания.
Хирургическое лечение рака вульвы
Хирургия — основной метод лечения рака вульвы. Во время операции врач старается полностью удалить опухолевую ткань, при этом сохранив эстетичный внешний вид половых органов, нормальную эвакуацию мочи и стула (это особенно важно, когда опухоль находится близко к мочеиспускательному каналу и анусу). В зависимости от стадии, прибегают к одному из следующих вариантов хирургических вмешательств:
- Локальное иссечение опухоли. Возможно на ранних стадиях. Хирург иссекает опухоль и примерно 1,3 см окружающих тканей, подкожной жировой клетчатки. Удаленную ткань отправляют в лабораторию для микроскопии. На краях разреза не должно быть обнаружено опухолевых клеток (отрицательный край резекции) — это будет говорить о том, что опухоль удалена полностью, и в организме, скорее всего, больше не осталось раковых клеток.
- Вульвэктомия. Хирург удаляет всю вульву или ее большую часть. Существуют разные варианты вульвэктомии. В одних случаях после операции удается сохранить нормальный внешний вид половых органов, у некоторых женщин впоследствии приходится прибегать к реконструктивно-пластической хирургии.
- Эвисцерация (экзентерация) таза — наиболее сложная и травматичная операция, ее проводят, если рак распространился на тазовые органы. Удаляют мочевой пузырь, нижнюю часть толстой и прямую кишку, матку вместе с шейкой и влагалищем. Объем вмешательства зависит от того, куда успела прорасти опухоль.
- Удаление лимфатических узлов. Раньше оно проводилось всегда — на всякий случай, так как хирург не мог точно знать, распространились ли опухолевые клетки в ближайшие лимфатические узлы. В настоящее время есть возможность проводить сентинель-биопсию — исследование лимфатического узла, который находится первым на пути оттока лимфы от опухоли. Если в нем нет раковых клеток, то не имеет смысла удалять остальные лимфоузлы.
Иногда, если после операции высок риск рецидива, хирургическое лечение сочетают с курсом лучевой терапии и химиотерапии.
Химиотерапия при раке вульвы
В настоящее время не существует четких однозначных схем химиотерапии при раке вульвы. Тем не менее, противоопухолевые препараты могут принести пользу в следующих случаях:
- До операции химиотерапию применяют в сочетании с лучевой терапией. Вместе они помогают уменьшить опухоль и облегчить ее удаление.
- Химиопрепараты назначают при рецидивах рака вульвы после хирургического лечения.
Лучевая терапия при раке вульвы
Лучевую терапию применяют при раке вульвы в следующих случаях:
- До операции в сочетании с химиотерапией. Это помогает уменьшить опухоль, перевести неоперабельный рак в операбельный.
- После операции для профилактики рецидива.
- Лучевую терапию можно использовать в качестве единственного метода лечения при поражении паховых и тазовых лимфоузлов.
- Ее применяют отдельно или в сочетании с химиотерапией для лечения женщин, которым противопоказано хирургическое вмешательство.
Прогноз при раке вульвы
Сколько живут при раке вульвы? Даже если лечение проведено успешно, и наступила ремиссия, в будущем у женщины сохраняется риск рецидива рака. Поэтому все пациентки нуждаются в длительном, в течение нескольких лет, наблюдении. Прогноз оценивают по пятилетней выживаемости — показателю, который демонстрирует процент выживших женщин в течение 5 лет после того, как был установлен диагноз. Этот показатель зависит от стадии рака и от того, насколько он распространился за пределы вульвы:
- При местном раке, который находится в пределах вульвы (соответствует стадии I и II), 5-летняя выживаемость составляет 86%.
- При региональном раке, когда опухолевые клетки распространились в лимфоузлы и соседние органы (соответствует стадиям III и IVA) — 54%.
- При распространенном раке, когда имеются отдаленные метастазы (соответствует стадии IVB) — 16%.
Можно ли предотвратить рак вульвы?
Основные меры профилактики рака вульвы сводятся к предотвращению инфицирования вирусом папилломы человека. Нужно ограничить количество половых партнеров (в идеале он должен быть один), пользоваться презервативами. От опасных штаммов ВПЧ эффективно защищает вакцина.
Так как рак вульвы чаще встречается среди курящих женщин, эффективной мерой профилактики является отказ от вредной привычки.
Цены на лечение рака вульвы в Европейской онкологической клинике
Стоимость лечения рака вульвы зависит от стадии опухоли, объема хирургического вмешательства, от того, нужно ли его дополнить химиотерапией, лучевой терапией, другими видами лечения. В Европейской онкологической клинике можно получить помощь на уровне ведущих западных онкологических центров, но по более низкой цене.
Прием онколога-гинеколога — 5 700 р.
Фотодинамическая терапия — от 170 т.р (рассчитывается в зависимости от веса пациента).
В литературе можно найти менее 50 случаев рака вульвы у беременных. Lutz и соавт. предполагают, что риск рака вульвы составляет 1 случай па 8000 беременных. По современным данным, он равен 1 случаю на 20 000 беременных. Рак вульвы — одна из наиболее злокачественных эпидермальных опухолей, после меланомы, саркомы и аденокистозного рака.
В последние годы появлялись сообщения о рецидиве рака вульвы у беременных, метастатической меланоме вульвы, быстро прогрессирующей лейомиосаркоме вульвы и первичной хориокарциноме вульвы. Средний возраст больных 25—35 лет; самой младшей пациентке было 17 лет. В связи с увеличением случаев диагностирования преинвазивного рака вульвы его все чаще обнаруживают у беременных.
Терапию дисплазии вульвы проводят после родов. Необходимо проводить биопсию всех подозрительных областей, чтобы исключить инвазию. При наличии интраэпителиальной неоплазии роды можно проводить через естественные родовые пути, но необходимо тщательное кольпоскопическое исследование нижних отделов полового тракта, чтобы исключить наличие преинвазивных или инвазивных очагов.
Gitsch и соавт. составили краткий список методов терапии и их результатов у беременных с раком вульвы, но надо отметить, что список был неоднородным. Barclay провел ретроспективное исследование у 31 беременной с раком вульвы. Во время беременности терапия была проведена 12 женщинам; двое получили лечение после родов.
В 1974 г. Barclay представил сведения о 9 больных, одна из которых подверглась ЛТ во время беременности. Хирургическое вмешательство во время беременности было выполнено 5 больным, после родов 3 женщины подверглись вульвэктомии. В дальнейшем у 9 больных развился рецидив. У женщины, получавшей ЛТ во время беременности, обнаружили РШМ. Lutz и соавт. сообщали о 3 больных, которым диагноз был поставлен во время беременности.
Лечение проводили после родов. Все женщины погибли. Сведения относительно стадии, лечения и продолжительности жизни не представлены.

Беременным при диагностике инвазивных злокачественных новообразований вульвы после 18-й недели беременности проводят стандартное лечение, такое же как и небеременным. При Т1 стадии и глубине инвазии более 1 мм проводят радикальное широкое иссечение с односторонней лимфодиссекцией паховых лимфоузлов. При более крупных опухолях и/или с большей глубиной инвазии выполняют радикальную вульвэктомию и двустороннюю пахово-бедренную лимфаденэктомию.
Больным с пальпируемыми лимфоузлами пахово-бедренной области на ранних сроках беременности рекомендуют обширную диссекцию, т. к. велика вероятность кожного метастазирования. Проведение ЛТ откладывают. Если диагноз поставлен после 36-й недели беременности, обширное локальное иссечение выполняют после родов, т. к. на поздних сроках беременности и в ранний послеродовой период кровоснабжение вульвы увеличивается. По-видимому, отсрочка в лечении не оказывает отрицательного влияния.
Женщины, которым лечение проводилось во время беременности, можно рожать через естественные родовые пути только в том случае, если раны хорошо зажили и нет необходимости в дополнительной терапии. Больным с высоким риском осложнений, при наличии показаний к адъюваптной ЛТ проводят кесарево сечение сразу же после созревания плода.
После рождения ребенка яичники перемещают к латеральным каналам брюшной полости и проводят облучение органов таза и паховой области. Поскольку злокачественные новообразования вульвы распространены у социально не обеспеченных лиц, которые часто не соблюдают гигиену беременных, их диагностируют только во время родов или позднее. У этой группы больных терапию следует начинать через неделю после родов. По-видимому, беременность не имеет значительного влияния на течение злокачественных новообразований.
Продолжительность жизни беременных и небеременных больных по каждой стадии сходна.
Bakour и соавт. не выявили противопоказаний к последующим беременностям у женщин со злокачественными новообразованиями вульвы. Полагают, что молодые женщины в случае беременности после обширного хирургического вмешательства восстанавливают свое психологическое состояние. Существует несколько сообщений о том, что женщины после радикальной вульвэктомии и двусторонней паховой лимфаденэктомии имели детей.
Вид родоразрешения определяется акушером в зависимости от состояния вульвы. В большинстве случаев вульва мягкая и не мешает родам через естественные родовые пути. Иногда развивается выраженный вагинальный стеноз или другой вид фиброза, в этих случаях проводят кесарево сечение.
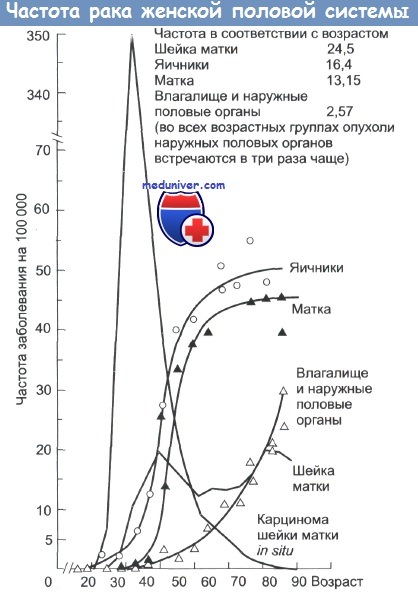
Частота раковых заболеваний женской половой системы в зависимости от возраста.
Широкое рапространение карциномы шейки матки после 40 лет связано с увеличением случаев диагностики опухоли in situ.
Похожие темы научных работ по клинической медицине , автор научной работы — Ключаров И. В., Хасанов А. А.
УДК 618. 1 - 006. 6 : 618. 3 - 06
ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ ГЕНИТАЛИИ И БЕРЕМЕННОСТЬ: ТАКТИКА ВЕДЕНИЯ БЕРЕМЕННОСТИ И РОДОВ
И.В. Ключаров, А.А. Хасанов
Кафедра акушерства и гинекологии № 1 (зав. - докт. мед. наук А.А. Хасанов) Казанского государственного медицинского университета
Рак является второй причиной смерти среди женщин репродуктивного возраста, осложняя от 0,02 до 01% случаев всех беременностей [10]. Диагностированный во время беременности рак представляет собой сложную проблему, возникающую перед врачом, женщиной и ее семьей. На исход заболевания и беременность оказывают влияние как взаимосвязанные этические, религиозные взгляды, эмоциональные убеждения пациентов, так и медицинские этические проблемы. Преимущества и негативные последствия диагностических, химиотерапевтических, лучевых и хирургических процедур должны быть тщательно взвешены во избежание их неблагоприятного влияния на внутриутробный плод. Именно здесь чаще всего скрывается конфликт интересов матери и плода.
Согласно предложенному А.Ф. Урманчеевой [5] определению опухоли органов репродуктивной системы, новообразования, обнаруженные во время беременности или в течение 6 месяцев после ее прерывания и через 12-18 месяцев после родов, относят к ассоциированным с беременностью, так как клинические и морфологические проявления опухоли присутствуют уже во время беременности.
Эпидемиологические данные о сочетании рака и беременности показывают, что заболеваемость раком гениталий во время беременности невысока и варьирует от 0, 02 до 0,1% среди всех злокачественных опухолей [3, 4, 9, 10, 13]. По данным Американской коллегии акушеров и гинекологов (ЛСОО, 1995), в США ежегодно осложняется онкозаболеваниями 3500 беременностей. Частота такого сочетания имеет тенденцию к возрастанию в связи с увеличением возраста беременных [2, 3, 9, 10, 13].
Сведения, представленные отечественными авторами [2, 3, 4], свидетельствуют о стимулирующем влиянии беременности на рост и развитие опухолей. Это связывается, с одной стороны, с подавлением клеточного иммунитета, а с другой - стимулирующим опухоль воздействием гормонов матери и фе-топлацентарного комплекса. В большинстве публикаций [6, 8-10 13-15] приводятся сведения о том, что беременность не только не ухудшает, а в ряде случаев улучшает результаты лечения и прогноз для матери. Это отчетливо заметно в структуре рака шейки матки при беременности В результате цитологического скрининга беременных более 70% случаев заболевания представлено стадией не более 1а, что соответственно определяет лучший прогноз для матери. При раке эндометрия опухоль представлена чаще всего высокодифференцированной аденокар-циномой с поверхностной инвазией в миометрий и соответственно эти пациентки имеют благоприятный прогноз при проведении радикального или органо-сохраняющего лечения [2, 9].
Возникновение, рост и распространение опухолевого заболевания связаны с многообразными метаболическими и иммунологическими нарушениями, которые могут оказать влияние на течение беремен-
ности, приводя к тем или иным осложнениям [2]. Так, феохромоцитома надпочечников вызывает гипертонические кризы, отеки, острое нарушение мозгового кровообращения, шок. Рак печени и острый лейкоз могут приводить к обильным внутренним и наружным кровотечениям. Возможны осложнения, связанные с интоксикацией и инфекцией.
Определенный риск для беременности и плода связан с проводимыми диагностическими и терапевтическими процедурами [5, 7, 9-11, 13]. Необходимо помнить, что для плода прогноз более благоприятен при выявлении опухоли в III триместре, а для матери - в I [2].
Эпидемиологические данные свидетельствуют о потенциальной возможности вызывать лейкемию и солидные опухоли у детей и взрослых. Риск возникновения этих заболеваний при облучении во время беременности повышается в 2-3 раза [11].
N.A. Pavlidis [12] рекомендует ограничить проведение стадирующих рентгенопроцедур беременным с онкозаболеваниями - рентгенография живота, радиоизотопное сканирование и компьютерная томография должны быть исключены. Рекомендованы УЗ-исследование, рентгенография органов грудной клетки и головы, а также магнитно-резонансное исследование головного мозга при стадировании опухолей, поскольку в этих ситуациях избегается прямое воздействие радиации на плод.
Результатом негативного воздействия облучения в периоде имплантации (первые 10 дней) может явиться гибель эмбриона [9, 10], в периоде органогенеза (10 дней - 12 нед) - задержка внутриутробного развития плода, врожденные пороки развития, в плодовом периоде (8 нед - до срока родов) - задержка внутриутробного развития плода, продолжающаяся после рождения, врожденные пороки развития, микроцефалия, задержка интеллектуального развития.
Следует указать, что пороговая доза облучения находится в пределах 5 - 25 сантиГр, в то время как большинство диагностических исследований вызывает облучение значительно меньше указанного даже при отсутствии защиты области живота [10]. Степень воздействия только нескольких таких процедур, как в/в пиелограмма, компьютерная томография области живота, бариевые клизмы, очень близка к нижней границе пороговой дозы [9, 10].
У беременных с аномальным Пап мазком диагноз может быть установлен с помощью кольпоско-пии и биопсии, проводимой прицельно под кольпо-скопическим контролем. Проведение эндоцервикаль-ного кюретажа при беременности противопоказано [12]. Конизация шейки матки имеет ограниченное значение, так как связана с возможностью нарушения беременности. Только в тех ситуациях, когда имеется высокая вероятность опухолевого поражения и зона стыка не может быть исследована коль-поскопическим путем или опухоль распространяется в цервикальный канал, может быть произведена
конизация. Однако E.R.Novak [12] рекомендует перед этим провести кольпоскопическое исследование опытным кольпоскопистом и при возможности ограничиться клиновидной или петлевой биопсией одного участка, чтобы избежать конизации. N.A.Pav-lidis [13] приводит данные об относительной безопасности биопсии в объеме конизации, осложняющейся прерыванием беременности в 17% случаев (в I триместре частота прерывания достигает 33%).
Цитостатические препараты во время беременности оказывают вредное воздействие на плод, новорожденного и мать. Для плода и новорожденного эти повреждающие эффекты включают мутации, тератогенез, которые проявляются врожденными пороками развития (ВПР), токсическим воздействием на органы и замедленным развитием, а для матери в первую очередь самопроизвольным прерыванием беременности и бесплодием.
С учетом проникновения химиотерапевтических препаратов через плаценту особое значение имеет время назначение препаратов. В большинстве случаев токсические эффекты были зафиксированы после терапии в 1 триместре, в периоде эмбриогенеза и реже во II и III триместрах. Доля ассоциированных с химиотерапией ВПР составляет 12,7-17%, а небольшой массы тела плода при рождении -до 40%. Уровень ВПР в популяции варьирует от 1 до 3% [7, 9, 10, 13].
Наиболее часто ВПР зафиксированы при применении антиметаболитов (аминопептин, метотрек-сат, 5-ФУ, арабинозил цитозин) и алкилирующих агентов (бусульфан, циклофосфамид, хлорамбуцил). D.C. Doll et al. [7], изучив 139 случаев полихимиотерапии, проводившихся в I триместре, обнаружили ВПР в 25% случаев, что несколько выше, чем при монохимиотерапии (17%). Панцитопения развилась у 33% новорожденных, подвергшихся воздействию химиотерапии во внутриутробном периоде.
Принципиальное решение вопроса о пролонгировании беременности, проведении диагностических и лечебных процедур, откладывании сроков начала терапии или прерывании беременности, а также объеме терапии принимает лечащий врач при участии беременной, ее семьи и других необходимых специалистов [3-5, 9, 10, 13]. Необходимость выбора лечить или отложить лечение больной раком возникает в следующих случаях: 1) беременность нежелательна; 2) срок беременности менее 24 нед; 3) онкозаболевание диагностировано после достижения плодом зрелости; 4) рак имеет распространенный характер или отсрочка не изменит прогноза для матери. Такие ситуации нетрудно разрешить. Сложности же в выборе обусловлены такими случаями, когда беременность является желанной, а плод -незрелым [9].
В I и II триместрах на первое место должно быть поставлено сохранение здоровья женщины, на второе - обеспечение донашивания беременности и рождения жизнеспособного ребенка [2]. Определение стадии опухоли осуществляется на основе классификаций FIGO и ТNМ с учетом данных гинекологического и дополнительных лучевых методов исследования.
В процессе лечения следует обеспечить [13] улучшение состояния беременной, адекватный объем лечения онкозаболевания, защиту матери и плода на фоне терапии, сохранение репродуктивной функции женщины.
Медицинский аборт в I триместре рекомендуется при местнораспространенном раке шейки матки,
распространенном раке молочной железы, требующем системной терапии, III и IV стадиях агрессивной ходжкинской и неходжкинской лимфомы и острой лейкемии [13].
Несмотря на противоречивые данные о влиянии беременности на возникновение, течение и метаста-зирование опухолей, в ряде случаев допустима отсрочка начала лечения онкобольной до достижения плодом зрелости и жизнеспособности [5, 8, 9, 14].
Рак шейки матки в сочетании с беременностью является одной из наиболее часто встречающихся опухолей и выявляется в 1-13 случаях на 10 тысяч беременностей и в одном случае на 1000-2500 родов [5]. Среди больных частота сочетания рака шейки матки с беременностью составляет 1-3%. Средний возраст таких пациенток - 30 лет [4]. Частота выявления сапсег in situ среди беременных варьирует от 0,025 до 0,13%, что соответствует частоте опухоли в популяции [12]. Распространенность рака шейки матки в последнее время снизилась вследствие улучшения скрининговых исследований, основной целью которых является исключение инвазив-ного рака шейки матки. Диагностика данной опухоли во время беременности может быть затруднена, если кровотечение рассматривать как симптом нарушения беременности. Тем не менее, по данным литературы [5, 10], во время беременности имеется в 3,5 раза более высокий шанс обнаружить рак шейки матки в I стадии из-за частого акушерского обследования. При подозрении на рак шейки матки необходимо провести онкоцитологическое обследование, кольпоскопию, а также петлевую и клиновидную биопсию шейки матки [12]. Эндоцервикальный кюретаж противопоказан. N.A.Pavlidis [13] приводит данные о прерывании беременности в 17% случаев, а в I триместре - до 33% при диатермокониза-ции шейки матки.
Поскольку большинство случаев рака шейки матки диагностируется на ранних стадиях заболевания, в ряде эпизодов онкозаболевания можно отложить основной этап лечения до достижения плодом зрелости и жизнеспособности. Такому решению способствует высокий уровень неонатологической помощи, при котором значительно снизились перинатальная заболеваемость и смертность [5, 10].
При инвазии опухоли до 3 мм и отсутствии вовлечения в процесс лимфатических и кровеносных сосудов беременность может быть пролонгирована до срока доношенности с родоразрешением через естественные родовые пути. При инвазии 3-5 мм и наличии раковых эмболов в сосудах также возможно пролонгирование беременности с последующим родоразрешением кесаревым сечением, за которым следует расширенная экстирпация матки по Верт-гейму с тазовой лимфаденэктомией. При инвазии опухоли более 5 мм ее необходимо лечить как инва-зивную карциному с учетом срока беременности и желания родителей [8-10, 13, 14].
Рекомендации по лечению пациенток с Ib стадией рака шейки матки противоречивы. Так, Т. Germann et al. [8] на основании анализа 9 случаев сделали вывод, что лечение больной с опухолью размером менее 2 см без метастазов в лимфоузлы (стадия IB) может быть отложено до достижения плодом желаемой зрелости и жизнеспособности. Анализ 49 случаев рака шейки матки стадии IB, проведенный L. Sadler et al. [14], показал, что отсрочка по меньшей мере на 6 недель от момента диагноза до проведения лечения в 47 случаях не проявилась прогрес-сированием или рецидивом рака; в 2 случаях женщины погибли.
При II стадии рака шейки матки основным методом лечения является лучевая терапия. При жизнеспособном плоде перед облучением необходимо родоразрешение путем кесарева сечения.
По мнению N.A. Pavlidis [13], рак шейки матки не оказывает негативного влияния на беременность. Несколько ретроспективных исследований [8-10, 14] показали отсутствие разницы в степени дифферен-цировки опухоли или 5-летней выживаемости беременных и небеременных пациенток.
В настоящее время отсутствуют данные о существенной разнице исходов рака шейки матки для пациенток, родивших через естественные родовые пути, в сравнении с кесаревым сечением. Однако кесарево сечение может быть предпочтительнее вследствие возможности избежать имплантационные метастазы в область промежности [9, 10, 14].
Заболеваемость раком яичников, ассоциированным с беременностью, составляет 1:800-20000 [9, 15]. Доля злокачественных опухолей среди всех новообразований яичников, сочетающихся с беременностью, варьирует от 2 до 6% [9]. У молодых женщин чаще встречаются герминогенные опухоли, с возрастом - эпителиальные, несколько реже - опухоли стромы полового тяжа.
Необходима дифференциальная диагностика этих опухолей и доброкачественных опухолей яичников (желтое тело беременности, лютеиновые и фолликулярные кисты, пролиферация гранулезных клеток, липомы яичника), внематочной беременностью и субсерозном миоматозном узле на ножке.
В большинстве случаев рак яичников при беременности протекает бессимптомно и является случайной находкой при УЗИ или во время кесарева сечения. Иногда могут возникать боли в животе из-за разрыва кисты или перекрута ее ножки, увеличения объема живота, препятствия продвижению плода во время родов [9, 15].
Целесообразно динамическое наблюдение с повторным УЗИ на сроке от 14 до 16 нед беременности при наличии односторонней, жидкостной, подвижной и бессимптомной кисты диаметром Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
5. Урманчеева АФ.//Практич. онкол. - 2002. -№ 3. - С. 183-193.
6. Batra S, Singh M., Wynn J.S. //Int J. Gynecol. Cancer. - 2006. - Vol.16 (1). - P. 365-368.
7. Doll D.C., Scott Ringenberg Q., Yarbo J.W. // Semin. Oncol. - 1989. - Vol.16. - P. 337-346.
8. Germann N., Haic-Meder C., Morice P. et al.// Ann Oncol. - 2005. - Vol.16 (3). - P. 397-402.
9. Greer B.E., Goff B.A., Koh W.J. et al. Cancer in pregnant patient./ from: Principle and practice of gynecologic oncology. Li ppincott-Raven Publishers. - 1997.- P. 463-485.
10. Lishner M.// Ann Oncol. - 2005. - Vol.14 (3). -P. 31-36.
11. Male R.H.// Br. J. Cancer. - 1990. - Vol.62. -P. 152-168.
12. Novak E.R. Novak's textbook of gynecology. -1988. - P. 674-675.
13. Pavlidis N .A.// Ann Oncol. - 2000. -Vol. 11(3). - P. 247-255.
14. Sadler L., Sykes P.//Ann Oncol. - 2005. -16 (3). - P. 341-343.
Читайте также:

