Рак предстательной железы патологическая анатомия
Рак предстательной железы развивается в железистых элементах паренхимы и прилежащих к ней терминальных канальцах периферической зоны железы. В процессе старения организма в периферической зоне нарастает количество очагов атипичной гиперплазии, отличающейся от железистой гиперплазии, связанной с развитием аденомы предстательной железы, дезорганизацией железистых структур. Атипичная гиперплазия развивается в зонах с сохранившейся секреторной активностью эпи гелия, подвергающихся в последующем диффузной железистой гиперплазии, что отражает биологическую взаимосвязь между этими процессами и возникновением гистологической картины рака. Эволюция рака предстательной железы включает продолжительное предраковое состояние, при котором повышенная чувствительность нормального эпителия к андрогенной стимуляции и последующая утрата гормональной зависимости являются ключевыми факторами в стимуляции злокачественного роста. Возникающая при этом атипичность клеток отражает потерю их андрогенозависимости.
В начальной стадии развития рака предстательной железы определяется микроскопический очаг малигнизации, включающий область значительного или слабовыраженного атипичного разрастания эпителия. Большинство таких очагов локализуются в периферической части железы и имеют размеры 0,2 —2,1 мм. Гистологически они относятся к светлоклеточному канальцево-альвеолярному или темноклеточному канальцевому раку. При развитии злокачественного процесса многочисленные микроскопические инфильтраты распространяются среди нормальной железистой ткани. При этом участок малигнизации часто оказывается мультицентрическим с разрастанием соединительной ткани. Постепенно происходит конденсация патологического фокуса в раковый узел, пальпируемый при ректальном исследовании. При гистологическом исследовании обнаруживаются области атипичных микроацинусов, занимающих несколько участков в задненижних отделах железы, внутри капсулы. В последующем размеры узла увеличиваются и он занимает значительную часть железы, но не распространяется за ее пределы. Это сопровождается значительной деформацией поверхности долей или доли железы при отсутствии вовлечения в процесс латеральных бороздок и семенных пузырьков. В дальнейшем происходит диффузная инфильтрация ткани железы с распространением злокачественного процесса на ее капсулу, семенные пузырьки и окружающую железу богатую сеть лимфатических и венозных сплетений. Инвазия прямой кишки и перипростатической клетчатки является результатом пенетрации капсулы железы. В дальнейшем в процесс вовлекаются шейка мочевого пузыря, предстательная и мембранозная части мочеиспускательного канала.
Большая часть рака предстательной железы с явными клиническими проявлениями заболевания относится к аденокарциномам, составляющим около 90% всех гистологических форм злокачественных новообразований предстательной железы. Основными признаками аденокарциномы являются нарушения дифференциации желез и анаплазия ядер. Общая патологическая характеристика рака предстательной железы включает расположение простатических ацинусов бок о бок, отсутствие базальных клеток в однослойном эпителии, выстилающем ацинусы, клетки располагаются в виде гроздьев, клеточные границы неотчетливы, в клетках обнаруживаются большие эозинофильные ядрышки, железки приобретают вид линейных инфильтратов в фиброзно-мышечной строме, выраженность ядерного гиперхроматизма, периневральная инфильтрация. Аденокарциномы предстательной железы классифицируются на дифференцированные (образующие при своем росте железистые структуры) и недифференцированные (с отсутствием желез). По степени дифференциации различают высоко-, умеренно- и низкодифференцированные формы рака предстательной железы. По характеру строения желез аденокарциномы дифференцированного типа разделяются на крибриформные, папиллярные и смешанного крибриформно-папиллярного строения.
Важным показателем доброкачественных и злокачественных изменений в простатических железках может служить выстилающий их эпителий, однослойный в случае злокачественной биотрансформации ацинусов с отсутствием базального слоя, и двухслойный в железках аденомы предстательной железы. В высокодифференцированных аденокарциномах отмечается морфологическая однородность эпителия, железистые структуры представлены маленькими прилежащими друг к другу ацинусами. Эпителиальные клетки цилиндрической формы с бледной, субгранулированной цитоплазмой, в нижней трети которой располагаются гиперхроматичные ядра.
Умеренно дифференцированная аденокарцинома характеризуется меньшей выраженностью регулярности желез, отдельные ацинусы слабо демаркированы, в них прослеживается вариабельность просветов. Железы выстланы низким цилиндрическим или кубическим эпителием с недостаточно четкими клеточными границами, гиперхроматичными ядрами и редкими митозами.
Низкодифференцированная аденокарцинома состоит из маленьких, нерегулярных, плотно сжатых ацинусов со слабо определяемыми просветами, выстланными кубическим или многослойным эпителием со скудной цитоплазмой и темными маленькими ядрами. В недифференцированном раке предстательной железы наблюдается полная утрата железистых структур, эпителиальные клетки расположены кучкообразно и в виде тяжей или струн, массивно инфильтрирующих строму, выражены митозы. При развитии рака предстательной железы проявляется выраженная анаплазия ядер. Ядра эпителиальных клеток характеризуются полиморфизмом, изменяются в размере и форме.
Гистологическая картина латентной карциномы характеризуется одиночными очагами пролиферации железистого эпителия. Развитие злокачественного процесса ограничено небольшим участком ткани с отсутствием тенденции к эксцентрическому росту. В противоположность клинически явной карциноме латентная форма редко включает многочисленные зоны крибриформно-папиллярных структур или недифференцированных желез, выявление которых не дает оснований расценивать рак простаты как скрытопротекающее заболевание. Очаги латентного рака предстательной железы обнаруживаются случайно на аутопсии или в ткани удаленных аденоматозных узлов. Для повышения вероятности выявления микроочагов рака предстательной железы в ткани удаленной аденомы целесообразно делать срезы, ориентированные к заднему краю энуклеации аденоматозных узлов, прилежащему к истинной предстательной железе — месту развития рака. При этом число срезов, произведенных у заднего края энуклеации аденомы по отношению к ткани, расположенной кпереди от мочеиспускательного канала, должно находиться в соотношении 3:1. Этот метод позволяет повысить частоту выявления латентной карциномы в ткани удаленных аденоматозных узлов с 6—10% до 20 — 28%. Гистологическая картина оккультного рака предстательной железы в большинстве случаев включает крибриформно-папиллярные структуры. При оккультной форме метастазы проявляются до выявления первичного очага опухоли.
Доброкачественная гиперплазия предстательной железы - дис-гормональное заболевание периуретральной части простаты, приводящее к обструкции выходного отдела мочевого пузыря. Возникает у мужчин с 40 лет, однако в возрасте 70 лет и старше страдают 75 % мужчин.
Точная причина заболевания не установлена. Считается, что гиперпластические узлы – продукт нарушения стромально-эпителиальных взаимоотношений. На гормональную этиологию заболевания указывают следующие факты:
увеличение уровня дегидротестостерона в строме гиперплазированной простаты;
использование препаратов, блокирующих синтез тестостерона к уменьшению размеров гиперплазированной железы;
заболевание не встречается у мужчин, кастрированных до периода полового созревания.
Первоначально гиперплазия обнаруживается в подслизистой оболочке переходной части уретры. Растущие узлы сдавливают просвет уретры и ткань простаты.
Макроскопически характерно увеличение простаты, появление узлов разной величины (при диффузном увеличении железа имеет округлую форму и гладккую повверхность, при узловом – неправильную бугристую). Особенно резко увеличена средняя доля, выдающаяся в просвет мочеиспускательного канала и шейки мочевого пузыря. На разрезе в предстательной железе обнаруживаются разделенные волокнистой псевдокапсулой с четкими границами. В больших узлах встречаются очаги кровоизлияний, инфарктов. Иногда в расширенных гиперплазированных ацинусах выявляются камни. Консистенция увеличенной в объеме и весе простаты чаще остается мягко-эластичной. Однако при разрастании в ней гладко-мышечных клеток и соединительной ткани она приобретает значительную плотность.
Микроскопически в зависимости от пролиферации того или иного клеточного типа простаты различают три гистологические формы узловой гиперплазии предстательной железы: 1) железистая (аденоматозная), 2) фиброзно-мышечная, 3) смешанная.
Аденоматозная гиперплазия (встречается наиболее часто, имеет диффузный характер) сопровождается увеличением железистых элементов, нарушается их расположение (количество, форма и величина долек варьируют). Сами дольки увеличиваются в объеме, границы между ними как бы стираются. Эпителий секреторных отделов и выводных протоков или остается без видимых изменений, или атрофичен, или (чаще) находится в стадии пролиферации.
Смешанная форма (встречается так же часто, как и аденоматозная, имеет узловой характер) характеризуется разнообразной гистологической картиной. В одних участках наблюдается увеличение железистых элементов, в других - стромы, появляется большое количество гладкомышечных клеток, железистые элементы атрофичны, окружены разрастаниями фиброзной и мышечной тканей, нарушена дольчатость железы. Характерна папиллярная гиперплазия железистого эпителия и наличие различной величины кистозных образований. Часто в узлах обнаруживаются клетки хронического воспаления.
Фиброзно-мышечная форма (встречается редко) отличается тем, что простата на большем протяжении состоит из гладко-мышечных клеток и соединительной ткани, среди которых встречаются островки атрофированных железистых элементов. Дольчатость железы нарушена. Прогноз благоприятный, при своевременном лечении.
Осложнения: сдавление и деформация мочеиспускательного канала и шейки мочевого пузыря, затруднение оттока мочи. Прогрессирующая обструкция мочеиспускательного канала сопровождается развитием гидроуретры (растяжение мочеточника), гидронефроза, почечной недостаточности. Стенка мочевого пузыря подвергается компенсаторной гипертрофии, часто недостаточной, наблюдается накопление избытка мочи в пузыре, вторичное инфицирование, развиваются цистит, пиелит, восходящий пиелонефрит и уросепсис.
Аденокарцинома - рак простаты из мелких желез, инфильтрирующих строму. Аденокарцинома в 98 % выявляется как первичный рак простаты и занимает второе место среди онкологических заболеваний у мужчин пожилого возраста
Диспластические пролиферативные нарушения.
Диагноз аденокарциномы во многих случаях ставится после гистологического изучения биопсийного материала, полученного при трансуретральной резекции по поводу гипеплазии простаты, или материала пункционной биопсии, полученной под контролем компьютерного томографа. В крови больных повышается уровень простато-специфического антигена. При ректальном исследовании выявляется диффузное или узловое уплотнение ткани простаты.
Макроскопически характерны множественные желто-белого цвета плотные узлы, локализуюшиеся по периферии железы, под капсулой. Микроскопически выявляется железистый рак (аденокарцинома). В дифференцированной опухолевой ткани наблюдаются однообразные мелкие и средние железы, прорастающие в строму железы.
Развитие аденокарциномы простаты делят на четыре стадии: А – опухолевая ткань обнаруживается случайно (А1 – опухоль локализована, А2 – опухоль занимает большую часть ткани простаты); стадия В – клинически обнаруживаются узлы (В1 – локальное поражение, В2 – узлы выявляются более чем в одной доле простаты); стадия С – опухоль прорастает через капсулу железы без метастазирования; стадия D – опухоль дает метастазы (D1 – метастазирование в региональные лимфатические узлы таза, D2 – отдаленные метастазы).
Метастазирование. Ранние метастазы обнаруживаются в запирательных лимфатических узлах, далее поражаются подвздошные и околоаортальные лимфатические узлы. Почти у всех больных, умерших от аденокарциномы простаты, опухоль давала метастазы в позвоночник, ребра, кости таза.
22) Грипп: острое высококонтагиозное эпидемическое заболевание, возникающее обычно в холодное время года и вызываемое РНК-вирусом, тропным к эпителию дыхательных путей. Выделяют 3 серологических типа вируса гриппа:
Вирус А – представляет наибольшую эпидемическую опасность.
Вирус В - вызывает локальные вспышки и эпидемии.
Вирус С – приводит к спорадическим случаям.
Патогенез. Вирус обуславливает 3 стадии заболевания:
1 стадия – внедрение и репродукция вируса. Продолжительность этой стадии соответствует инкубационному периоду (от нескольких часов до 2-4 дней).
2 стадия – вирусемия, сопровождается продромальными явлениями.
3 стадия – вторичная репродукция вируса в эпителии дыхательных путей, которая приводит к генерализации инфекции и разгару болезни – повышается температура, появляется головная боль, кашель, катаральный ринит, суставные и мышечные боли.
Все возникающие изменения в организме обусловлены действием вируса:
Цитопатическое действие вируса – дистрофия, некроз, слущивание эпителия дыхательных путей.
Вазопатическое действие вируса – гиперемия, стаз, плазматическое пропитывание, отек, кровоизлияния.
Нейропатическое действие - создается высокая концентрация токсинов в нейрогуморальных центрах продолговатого мозга и гипоталамуса. При этом еще больше увеличиваются сосудистые реакции, понижается тонус бронхиальных мышц и подавляется дренажная функция дыхательных путей.
Иммунодепрессивное действие вируса – снижение фагоцитарной активности лейкоцитов и макрофагов. Развитие вторичной инфекции.
Патологическая анатомия.
Морфологическая картина обусловлена сочетанием местных и общих изменений. Местные изменения связаны с цитопатическим и вазопатическим действием вируса на эпителий дыхательных путей. Общие изменения вызваны вирусемией и интоксикацией. В зависи-мости от выраженности местных и общих изменений выделяют формы заболевания:
Легкая форма гриппа – развивается катаральный (серозный, слизис-тый, десквамативный) риноларингит и реже трахеобронхит. Макроскопически: слизистые оболочки носа, гортани, трахеи и бронхов набухшие, полнокровные, иногда с точечнымим кровоиз-лияниями, покрыты слизью. Микроскопически: в эпителиоцитах гидропическая дистрофия, некроз, слущивание, повышение секреторной активности бокаловидных клеток. В мазках – отпечатках слизистой оболочки видны вирусные включения в виде базофильных
или фуксинофильных телец.
Базофильные тельца – это скопления вируса.
Фуксинофильные тельца – это разрушенные органеллы под воздействием вируса.
Заболевание обычно заканчивается выздоровлением через 5-6 дней.
Грипп средней тяжести – к вышеназванным изменениям при лег-ком течении гриппа присоединяются более значительные поражения:
кроме слизистой трахеи и бронхов поражаются альвеолы.,
меняется характер воспаления – оно становится серозно-гемор-рагическим и фибринозно-геморрагическим,
значительная лимфо-макрофагальная инфильтрация,
некроз и слущивание эпителия наблюдаются на обширных участках слизистой,
повреждается альвеолярный эпителий, в связи с чем снижается выработка суфрактанта,
в легких возникают ателектазы, развитие которых обеспечивается: снижением выработки суфрактанта и закупоркой просвета бронхов слущенным эпителием и густыми слизистыми пробками.
Легкое увеличено в размерах с очагами уплотнения серо-красного цвета, кусочки из этих очагов тонут в воде. Между очагами уплот-нения участки перифокальной эмфиземы. Участки уплотнения могут быть ателектазами или очагами пневмонии.
Микроскопические изменения в легких: кроме описанных выше изменений в слизистых бронхов, ателектазов и эмфиземы в легких развивается межуточная и очаговая пневмония. При межуточной пневмонии межальвеолярные перегородки утолщены, полнокровны, инфильтрированы лимфацитами и гистиоцитами. При очаговых пневмониях в просвете альвеол содержится геморрагический экссу-дат. Выздоровление происходит через 3-4 недели. Однако возможны бронхо-легочные осложнения.
Тяжелый грипп протекает в двух вариантах:
с легочными осложнениями.
Токсический грипп характеризуется тяжелыми общими изменениями, которые присоединяются к бронхо-легочным поражениям.
Общие изменения: геморрагический отек легкого, геморрагический синдром (кровоизляния в мозг, слизистые, серозные оболочки, кожу, внутренние органы), серозно-геморрагический менингит, отек голов-ного мозга, токсический миокардит, гиперплазия лимфоидных орга-нов. Смерть больных при токсической форме гриппа может насту-пить на 4-5 день заболевания.
Грипп с легочными осложнениями возникает при присоединении вторичной бактериальной инфекции (стрепто-, стафило-, пневмокок-ковой, синегнойной) – развивается тяжелая очагово-сливная гнойно-геморрагическая бронхопневмония с гнойным деструктивным пан-бронхитом.
выбухающие плотные очаги пневмонии серо-красного или зелено-красного цвета,
западающие очаги ателектазов синеватого цвета,
вздутые очаги эмфиземы светло-пепельного цвета,
абсцессы грязно-серого цвета,
кровоизлияния темно-красного цвета.
Легочные осложнения гриппозной пневмонии часто приводят к развитию бронхоэктазов, пневмосклерозу, обструктивной эмфиземы, фибринозно-гнойному плевриту с эмпиемой, к гнойному медиастениту.
Кроме легочных осложнений при гриппе могут возникать внелегочные осложнения:
серозный менингит, арахноидит, энцефаломиенит, невриты,
катарально-гнойные отит, гайморит, фронтит.
У детей нередким осложнением является асфиксия вследствие развития истинного крупа или ложного крупа (фибринозное воспаление).
23) Парагрипп (риновирусные инфекции) по свеему течению напоминает легкий грипп (отсюда название болезни). Эти инфекции составляют до 20-50% ОРВИ. Вызывается парагрипп пневмотропным РНК-вирусом. Инкубационный период 3-6 дней, инфекция продолжается 1 неделю. Клин чески проявляется повышенной утомляемостью, сильным насморком с выраженной секрецией слизи, чиханием, болями в горле, субфибтильной температурой, охриплостью, кашлем.
Патологическая анатомия.
Поражаются преимущественно верхние дыхательные пути, развивается серозно-слизистый ларингит, трахеит, бронхит. Выражен отек слизистой, с большим количеством слизи, полнокровием. Микроскопически в эпителии наблюдаются дистрофические и пролиферативные изменения, а также инфильрация лимфоцитами, плазмоцитами и макрофагами. Проли-ферация эпителия, особенно в мелких бронхах и бронхиолах ведет к образованию подушкообразных разрастаний из полиморфных клеток. Интоксикация при парагриппе выражена слабо. Прогноз заболевания в целом благоприятный, однако при нем может возникнуть тяжелое осложнение – ложный круп, особенно часто у детей раннего возраста.
В случаях присоединения вторичной инфекции может возник-нуть бронхопневмония, ангина, отит, синусит.
Аденовирусная инфекция вызывается пневмотропным ДНК-содержащим вирусом у людей любого возраста, но наиболее часто у детей первых лет жизни (до 50% всех заболеваний).
Особенность пути передачи – не только воздушно-капельным, но и контактным путем. Вирус проникает в эпителий дыхательных путей, конъюктивы и кишечника. Инкубационный период 4-5 суток. Патологическая анатомия зависит от тяжести заболевания.
При легкой форме течения отмечается
катаральный риноляринготрахеобронхит и фарингит,
острый катаральный конъюктивит,
регионарный лимфаденит с увеличнием лимфоузлов и селезенки.
Слизистая оболочка отечна, гиперемирована с точечными крово-излияниями, наблюдается выраженная десквамация эпителия. В эпителии обнаруживаются характерные аденовирусные клетки – крупные клетки с увеличенными, неравномерно окрашенными, урод-ливыми ядрами, которые содержат базофильные скопления вируса.
У грудных детей часто развивается серозная аденовирусная брорнхо-пневмония. В серозный экссудат при этой пневмонии входят еще и слущенные альвеоциты, эритроциты, макрофаги. Клетки экссудата подвергаются мелкоглыбчатому распаду с образованием базофильных округлых телец. Часто образуются очаги ателектазов и эмфиземы. А в ряде случаев образуются гиалиновые мембраны.
Тяжерая форма аденовирусной инфекции, которая развивается, как правило, у детей 1-го года жизни, связана с двумя факторами:
с генеразизацией и вторичной репродукцией вируса в эпителии кишечника, печени, почек, поджелудочной железы, а также в ганглиозных клетках головного мозга – наблюдаются дистрофические изменения, аденовирусные клетки, межуточное воспаление,
с присоединением вторичной инфекции и развитием гнойно-некротического воспаления в бронхиальном дереве и легких.
Смерть больных детей наступает прежде всего от легочных осложнений, далее от менингоэнцефалита.
Респираторно-синцитиальная инфекция. Доля этих инфекций в группе ОРВИ составляет 5-20%. Вызывается РНК-содержащим вирусом, который обладает высоким цитопатическим и иммуно-депрессивным действием с развитием иммунодефицита и аутоиммунных реакций. Инкубационный период 3-6 дней. Преимущественно поражаются дети 1-го года жизни, мальчики в 2 раза чаще. У детей старшего возраста и у взрослых течение заболевания легкое или бессиптомное.
Патологическая анатомия.
Отличительной особенностью заболевания является преиму-щественное поражение не начальных, а дистальных отделов дыхательных путей, где возникают более выраженные изменения. В начальных отделах дыхательных путей развивается катаральный ларинготрахеобронхит – отек слизистой, гиперемия.. В мелких бронхах и бронхиолах сочетание десквамации клеток поврежденного эпителия и очаговой пролиферации эпителия в виде сосочков (симпластов). Сосочки образованы крупными клетками со светлыми ядрами. В этих клетках обнаруживаются вирусы. Просвет альвеол заполнен серозным экссудатом с примесью макрофагов, нейтрофилов и единичных гигантских клеток. Часто присоединяется интерстици-альная пневмония с утолщением межальвеолярных перегородок, в которых отмечается выраженная лимфогистоцитарная инфильтрация. В связи с закрытием просвета бронхов и бронхиол развиваются очаги ателектазов и острой эмфиземы.
Осложнения возникают при присоединении вторичной инфекции: пневмонии, менингоэнцефалит.
Клинико-морфологические проявления воздушно-капельных вирусных инфекций зависят от тропности вируса к клеткам слизистых дыхательных путей, альвеол и определенных свойств вирусных токсинов. Все эти инфекции по степени тяжести варьируют от легкого недомогания до тяжелейших форм с пневмониями и другими однотипными осложнениями, угрожающими жизни. Все эти обстоятельства требуют целевой профилактической направленности в предупреждении возникновения ОРВИ, особенно у детей младшего возраста.
Рак предстательной железы чаще развивается под капсулой в каудальной части, хотя может возникнуть в любом другом отделе органа в виде множественных очагов, сливающихся по мере роста в одну опухоль, что легко выявляется при ТРУЗИ простаты (В. В. Бялик и В. Г. Пинчук). В разных участках железы может отмечаться различное строение опухоли. Степень дифференциации новообразования определяет продолжительность жизни больного (Scott с соавт.).
Gottinger и Schmiedt подчеркивают, что для прогноза рака предстательной железы степень морфологической дифференциации опухоли имеет решающее значение. Высокодифференцированные раки предстательной железы редко выходят за пределы капсулы, малодифференцированные в 90 % случаев прорастают капсулу и дают метастазы.
Vrubel и соавторы выделяют следующие типы рака предстательной железы: высокодифференцированный; слабодифференцированный; недифференцированный рак и анапластическую темно- и светлоклеточную аденокарциному. Встречаются и смешанные типы.
Мы пользуемся классификацией, предложенной В. В. Бяликом и В. Л. Бяликом. В ней учтены особенности морфологического строения опухоли, степень ее дифференциации и гистогенез. Это дает возможность определить прогноз заболевания.
К дифференцированным формам авторы относят крупноячеистую аденокарциному, светлоклеточный тубулоальвеолярный рак, темноклеточный тубулярный рак, криброзный рак, слизепродуцирующую аденокарциному, переходноклеточный и плоскоклеточный рак. Малодифференцированными формами считают анапластическую аденокарциному, солидный и скиррозный рак. Недифференцированными являются мелкоклеточный и полиморфноклеточный рак. Есть еще и неклассифицируемые формы.
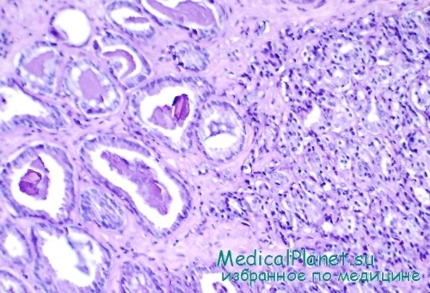
У 343 наблюдаемых нами больных диагноз рака предстательной железы подтвержден морфологически. У 209 пациентов ткань опухоли для гистологического исследования получена путем инструментальной биопсии. При открытой биопсии, выполненной во время эпицистостомии, рак диагностирован у 23 больных. У 27 пациентов рак предстательной железы обнаружен в аденоме при исследовании операционного материала.
Ю. А. Виненцов биопсийный и операционный материал рака предстательной железы подверг гистологическому и гистохимическому исследованию. У 58,7 % больных имели место высокодифференцированные формы рака предстательной железы, у 34,8 % — малодифференцированные, у 6,5 % — недифференцированные.
Крупноячеистая аденокарцинома была у 24,3 % больных и часто сочеталась с аденоматозной гиперплазией предстательной железы. Опухоль состояла из крупных альвеолярной формы желез, выстланных кубическим (реже цилиндрическим) эпителием в один ряд с единичными митозами в них, со слабо выраженным полиморфизмом, с невысокой активностью кислой фосфатазы. Многие железы имели собственную мембрану. Тонкие аргирофильные волокна окружали комплексы эпителиальных клеток. Опухоль бедна стромой, сосуды дифференцированные. В строме и стенке сосудов преобладали нейтральные гликозамингликаны. В. эндотелии сосудов, строме хорошо выражена активность щелочной фосфатазы.
Светлоклеточный тубулоальвеолярный рак отмечен у 13,2 % больных. Развивался на фоне как аденоматозной гиперплазии предстательной железы, так и здоровых тканей. Опухоль железистого строения со слабо выраженным морфологическим атипизмом, единичными митозами. Опухолевые железы мелкие, с сохранившимся просветом. Одни из них имеют альвеолярное строение, другие — тубулярное. Кубический или призматический эпителий, выстилающий железы, крупный со светлой цитоплазмой, крупным округлой формы гиперхромным ядром. В цитоплазме опухолевых клеток невысокая активность кислой фосфатазы. При окраске по Ван-Гизону выявляется фуксинофильная собственная мембрана желез, в препаратах, обработанных серебром,— аргирофильный каркас. Опухоль бедна стромой, волокна ее богаты нейтральными гликозамингликанами, хорошо выражена активность щелочной фосфатазы.
Темноклеточный тубулярный рак выявлен у 9,9 % больных. Развивается чаще на фоне здоровой ткани предстательной железы. Опухоль железистого строения с более выраженным морфологическим атипизмом. Опухолевые клетки группируются в небольшие трубочки или тяжи. Не всегда сохраняется просвет, базальная мембрана отсутствует. Клетки кубической формы с интенсивно окрашенной гомогенной цитоплазмой, крупным глыбчатым гиперхромным ядром. В цитоплазме эпителия выражена активность кислой фосфатазы. Строма неравномерно выражена, богата пикринофильными волокнами. Аргирофильные волокна, окружающие эпителиальные комплексы, интенсивно импрегнированы, с нечеткими контурами. В стенках сосудов, строме выявляются кислые гликозамингликаны, уменьшается активность щелочной фосфатазы.
Криброзный рак предстательной железы (8,7 %) напоминает одноименную опухоль молочной железы. Часто криброзные структуры сочетаются с другими гистологическими формами рака. Опухоль представлена крупными железами находящимися на большом расстоянии друг от Друга. Железы имеют четкие мембраны. Соединительнотканные волокна ее окрашиваются фуксинофильно. Просвет желез выполнен незрелым кубическим эпителием, образующим тяжи, мостики, псевдожелезы и солидные поля. В клетках единичные митозы, в их цитоплазме — умеренная активность кислой фосфатазы. Опухоль богата стромой. В ней преобладают нейтральные гликозамингликаны. В эндотелии мелких сосудов, строме слабо выражена активность щелочной фосфатазы.
Переходноклеточный рак встретился у 1,3 % пациентов. Опухоль растет эндофитно по отношению к протокам предстательной железы и имеет сосочковое строение. Сосочек имеет вид небольшого соединительнотканного выроста, покрытого атипичным переходным эпителием. В цитоплазме клеток хорошая активность кислой фосфатазы. Строма практически отсутствует. Опухоль богата клеточными элементами.
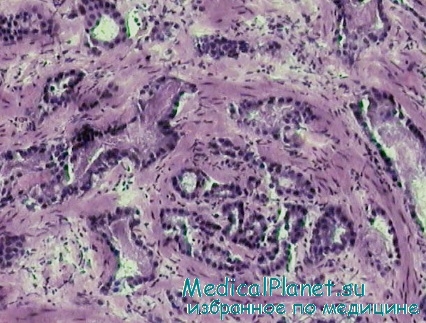
Плоскоклеточный рак предстательной железы выявлен у 1,3% больных. Опухоль с хорошо выраженным морфологическим атипизмом. Полиморфные опухолевые клетки образуют так называемые раковые ячейки различных размеров, окруженные аргирофильными волокнами. Часто встречаются митозы. В ядре и цитоплазме опухолевых клеток хорошая активность кислой фосфатазы. Опухоль имеет четкое органоидное строение, богата волокнистой соединительной стромой, в которой преобладают нейтральные гликозамингликаны. Активность щелочной фосфатазы снижена.
Анапластическая аденокарцинома отмечена у 28,9 % больных. Для этой опухоли характерен выраженный тканевой и клеточный атипизм с пролиферацией и анаплазией. Опухоль представлена железистыми структурами без определенной формы, без собственной мембраны. Эпителий незрелый с резко выраженным нарушением соотношения цитоплазмы и ядра. Ядра круглые, гиперхромные. Цитоплазма интенсивно окрашена, с высокой активностью кислой фосфатазы. Строма неравномерно выражена; рыхлая соединительная ткань местами переходит в соединительную ткань, богатую коллагеновыми волокнами. В строме в одинаковом количестве выявляются кислые и нейтральные гликозамингликаны. Активность щелочной фосфатазы резко снижена.
Солидный рак (3,9 %) развивался на фоне аденоматозной гиперплазии и среди нормальных тканей железы с выраженной морфологической атипией. Паренхима опухоли представлена комплексами атипичного железистого эпителия, утратившего способность оборазовывать железы. В опухолевых клетках частые митозы, высокая активность кислой фосфатазы. В одних опухолях строма слабо выражена, представлена рыхлой соединительной тканью с большим количеством кислых гликозамингликанов и резким снижением активности щелочной фосфатазы, в других — строма хорошо выражена, богата волокнистыми структурами, бедна клеточными элементами, содержит в основном нейтральные гликозамингликаны. Активность щелочной фосфатазы выражена.
Скиррозный рак предстательной железы был у 2 % больных.
Мелкоклеточный рак мы наблюдали у 2,6 % больных, полиморфноклеточный — у 3,9 %. Опухоль развивается на фоне нормальной предстательной железы, не достигает больших размеров. Характеризуется резким тканевым и клеточным атипизмом с выраженным полиморфизмом и анаплазией, содержит большое количество патологических митозов. Паренхима опухоли состоит из недифференцированных клеток с крупным гиперхромным ядром, с маленьким ободком цитоплазмы, высокой активностью кислой фосфатазы.
Для предстательной железы характерны диморфные формы рака. Мы их отметили у 21,2 % наблюдаемых нами больных.
Вопрос о взаимосвязи аденомы и рака предстательной железы освещен в литературе по-разному. Одни авторы относят аденому предстательной железы к предраковым состояниям. Другие полностью отвергают возможность развития рака предстательной железы из ее аденомы и считают оба процесса независимыми друг от друга. Третьи авторы полностью не отвергают возможность малигнизации аденомы.
В. В. Бялик и В. Г. Пинчук установили, что рак из аденомы, развивается реже, чем из неизмененной предстательной железы. Мы же отметили малигнизацию аденомы у 1,4 % больных, перенесших аденомэктомию.
В настоящее время отмечается значительный интерес к иммунологии новообразований (А. К. Агеев, В. И. Говалло и др.).
Изучение морфологии иммунных реакций организма при различной степени зрелости рака предстательной железы поможет в определении прогноза и выборе метода лечения опухоли. Ю. А. Виненцовым проведен количественный морфометрический анализ иммунокомпетентных клеток в 87 наблюдениях рака предстательной железы. Плотность клеточных инфильтратов была максимальной при дифференцированном раке предстательной железы. Среди иммунокомпетентных клеток преобладали лимфоциты, образующие во многих препаратах отдельные скопления. Относительная плотность их равнялась 0,602. Значительной была относительная плотность плазматических клеток, лейкоцитов, ретикулоцитов.
При малодифференцированном раке отмечалось уменьшение клеточных инфильтратов в строме опухоли. Особенно это касалось лимфоцитов. Относительная плотность их снизилась до 0,230. Уменьшилась относительная плотность плазмоцитов, ретикулоцитов, а лейкоцитов оставалась большой.
При недифференцированном раке предстательной железы иммунная клеточная реакция, отсутствовала.
Прогрессировало опухоли сопровождается снижением иммунной клеточной реакции в ее строме. Это дает возможность судить о степени зрелости опухоли и выбирать более эффективные методы лечения.
- Вернуться в оглавление раздела "хирургические болезни"
Читайте также:

