Рак предстательной железы научные
— Идет бурное развитие средств и методов диагностики: того же ПСА и других. На смену УЗИ приходит МРТ, позволяющая достичь гораздо более высокого разрешения. Более современные методы биопсии также выполняются под контролем МРТ-аппарата, а не УЗИ, как прежде.
Совершенствуются и препараты. Пациенты со множественными метастазами в кости благодаря современной химиотерапии живут годами. Там, где мы не можем оперировать, на выручку приходят фармакологи и химиотерапевты, обеспечивая им достаточно долгую продолжительность жизни.
Также развивается лучевая терапия, которая сегодня предлагает таргетные методики — когда мы воздействуем на опухоль прицельно, не затрагивая окружающие ткани.
Если говорить о будущем, то мы, конечно, ждем работ, связанных с генетикой. Медицина будущего позволит не ждать, когда произойдет какая-то поломка в хромосоме, а находить ее предпосылку в геноме и предотвращать болезнь, произведя генетическую коррекцию. Работы в этом направлении уже ведутся.
— Идет бурное развитие средств и методов диагностики: того же ПСА и других. На смену УЗИ приходит МРТ, позволяющая достичь гораздо более высокого разрешения. Более современные методы биопсии также выполняются под контролем МРТ-аппарата, а не УЗИ, как прежде.
Совершенствуются и препараты. Пациенты со множественными метастазами в кости благодаря современной химиотерапии живут годами. Там, где мы не можем оперировать, на выручку приходят фармакологи и химиотерапевты, обеспечивая им достаточно долгую продолжительность жизни.
Также развивается лучевая терапия, которая сегодня предлагает таргетные методики — когда мы воздействуем на опухоль прицельно, не затрагивая окружающие ткани.
Если говорить о будущем, то мы, конечно, ждем работ, связанных с генетикой. Медицина будущего позволит не ждать, когда произойдет какая-то поломка в хромосоме, а находить ее предпосылку в геноме и предотвращать болезнь, произведя генетическую коррекцию. Работы в этом направлении уже ведутся.
Мнение о том, что любая злокачественная опухоль – это приговор, безнадежно устарело. Благодаря достижениям медицины в России уже около 53 % онкологических пациентов, заболевших впервые, успешно вылечиваются. А на ранних стадиях в зависимости от вида рака можно вообще вылечить до 90 % злокачественных опухолей.
Своевременная диагностика и профилактические обследования — это проявление ответственного отношения к своему здоровью.
Специалисты МЕДСИ разработали специальные программы обследования – онкоскрининги. Практика показывает, что они не только позволяют выявить большинство наиболее распространенных онкологических заболеваний, но и являются первым шагом к диагностированию других болезней обследуемых органов и систем.
Если вы хотите пройти профилактическое обследование или наблюдаете тревожные симптомы, запишитесь на скрининг, который даст ответы на беспокоящие вас вопросы.
Мнение о том, что любая злокачественная опухоль – это приговор, безнадежно устарело. Благодаря достижениям медицины в России уже около 53 % онкологических пациентов , заболевших впервые, успешно вылечиваются. А на ранних стадиях в зависимости от вида рака можно вообще вылечить до 90 % злокачественных опухолей.
Своевременная диагностика и профилактические обследования — это проявление ответственного отношения к своему здоровью.
Специалисты МЕДСИ разработали специальные программы обследования – онкоскрининги. Практика показывает, что они не только позволяют выявить большинство наиболее распространенных онкологических заболеваний, но и являются первым шагом к диагностированию других болезней обследуемых органов и систем.
Если вы хотите пройти профилактическое обследование или наблюдаете тревожные симптомы, запишитесь на скрининг, который даст ответы на беспокоящие вас вопросы.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
В настоящее время в России и во многих других странах наметилась стойкая тенденция к увеличению числа больных раком простаты. Популяризация знаний об этом заболевании и современные возможности ранней диагностики позволили значительно увеличить выявляемость рака простаты на ранних стадиях, когда лечение может быть максимально эффективным.
При подробном анализе распространенности РПЖ в России выясняется, что почти у половины больных заболевание впервые выявляется на 3–4 стадии, что значительно затрудняет лечение и снижает его эффективность.
Столь широкое распространение РПЖ ставит его в ряд наиболее важных социальных проблем современности. Болезнь исключительно редко развивается раньше 40 лет и становится все более частым явлением с каждым последующим десятилетием жизни. По данным американских источников, никак себя не проявляющие очаги злокачественного перерождения предстательной железы выявляются у 15–30% мужчин старше 50 лет и у 80% мужчин старше 80 лет. Известно, что при наличии РПЖ у кровного родственника риск заболеть повышается в 2–3 раза.
Как и рак молочных желез у женщин, это заболевание на ранних стадиях практически всегда является случайной находкой или результатом специализированного скринингового обследования, поскольку длительное время не имеет никаких специфичных клинических проявлений, маскируясь за симптомами расстройства мочеиспускания, характерными для аденомы простаты, а иногда вовсе не причиняя пациенту никакого беспокойства.
Факторы окружающей среды, особенно различия в диете также играют важную роль в развитии рака простаты. Высокий уровень содержания в пище жиров животного происхождения является доказанным отрицательным фактором прогноза. В то же время было доказано, что азиатская диета, богатая соей, морепродуктами, рисом, грибами шиитаке, рыбой и зеленым чаем, оказывает некоторый защитный эффект и предотвращает развитие РПЖ.
Как было сказано выше, на начальной стадии РПЖ не имеет выраженной клинической симптоматики, что существенно затрудняет его диагностику. Признаки нарушения оттока мочи одновременно из обеих почек с развитием почечной недостаточности или появление болей в костях могут свидетельствовать о распространенности процесса.
Обнаружение простатоспецифического антигена (ПСА) в 1980-е гг. привело к революции в ранней диагностике РПЖ. ПСА – это белок, который выделяется предстательной железой и может определяться в крови в различных концентрациях. Условной границей нормы считается 4 нг/мл, но многие ведущие урологические клиники мира в последние годы склонны снижать норму этого показателя до 2,5 нг/мл, вводя дополнительные понижающие коэффициенты для более молодых мужчин. Тревожным может являться не только высокое абсолютное значение ПСА, но и высокие темпы его годового прироста (более 0,75 нг/мл). Повышение уровня ПСА – не всегда доказательство наличия рака простаты. Чувствительность этого онкомаркера составляет более 95%, а специфичность – около 75%. То есть в 25% случаев повышение уровня ПСА связано с другими причинами: наличием аденомы простаты, хроническим воспалением в предстательной железе и т. д. Так, уровень сывороточного ПСА может увеличиваться при различных манипуляциях с предстательной железой (массаж, биопсия), даже после эякуляции накануне исследования, а также при наличии инфекции.
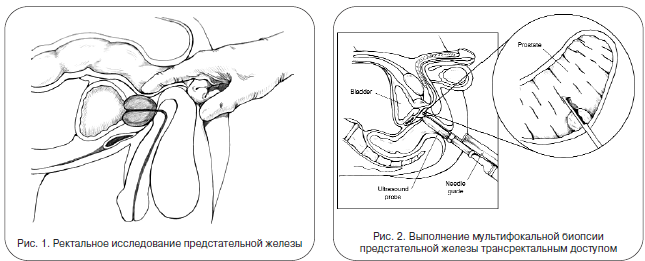
Выбор тактики зависит от возраста больного, сопутствующих заболеваний, клинической стадии болезни, распространения опухоли и ее гистологических характеристик. Очень важно составить прогноз течения заболевания, что возможно на основании накопленного во всем мире многолетнего опыта наблюдения и лечения больных раком простаты. Хотя диагноз РПЖ на сегодняшний день ставится довольно часто, известно, что только у 25% больных непосредственной причиной смерти будет являться это заболевание.
Возраст больного – один из ключевых показателей при выборе оптимальной тактики лечения. Так, 75% больных младше 65 лет умирают от РПЖ при отсутствии надлежащего лечения. Также было установлено, что 50% пациентов с локализованным высокодифференцированным РПЖ живут более 15 лет от момента установления диагноза, даже если активного лечения не проводится.
Подход к лечению больных РПЖ должен быть сугубо индивидуальным. Максимально радикальное лечение – хирургическое (радикальная простатэктомия) подразумевает полное удаление простаты без вскрытия ее фасции единым блоком с семенными пузырьками. Если эта операция выполнена вовремя, с соблюдением всех онкологических принципов и по показаниям, то она позволяет полностью избавить больного от злокачественной опухоли и обеспечивает хороший прогноз для жизни.
Независимо от выбранной методики идея операции остается неизменной – выделение простаты без повреждения капсулы, отсечение ее от мочевого пузыря и мочеиспускательного канала и наложение соустья между пузырем и мочеиспускательным каналом. При необходимости выполняется удаление регионарных лимфатических узлов. Такая операция может быть рекомендована относительно молодым больным с ожидаемой продолжительностью жизни не менее 10–15 лет без тяжелых сопутствующих заболеваний. Несмотря на сопоставимые онкологические результаты, темпы восстановления после операции, сроки медицинской и социальной реабилитации больных во многом зависят именно от выбранной оперативной методики.
Несмотря на хорошие результаты радикальной операции, как и любое другое хирургическое вмешательство, она имеет ряд осложнений, наиболее характерными из которых являются недержание мочи и эректильная дисфункция. Частота осложнений меньше ассоциирована с методикой выполнения операции, но определенно зависит от опыта хирурга и индивидуальных особенностей пациента. Несомненно, существуют способы борьбы с подобными осложнениями, но лучше проводить профилактику их возникновения. Основополагающим ее элементом является определение показаний к операции. Второй по значимости фактор – соблюдение техники выполнения операции, имеющей много тонкостей и особенностей. Так, в зависимости от стадии процесса, локализации опухоли в простате и исходного уровня сексуальной активности у части больных операция может быть выполнена с сохранением нервов, ответственных за эректильную функцию.
Гормональная и химиотерапия в настоящее время большинством экспертов не одобрены для лечения локализованного рака простаты и должны быть резервированы для пациентов с распространенным онкологическим поражением. В таких случаях хороший результат может дать сочетанное лечение – комбинация медикаментозной и дистанционной лучевой терапии. Известно, что лучевая терапия уже десятилетия используется для лечения онкологических заболеваний. За счет поражающего радиоактивного излучения опухолевые клетки теряют свою репродуктивную активность. Радиоактивное излучение проникает глубоко в ткани. Обычно подбирается индивидуальная доза облучения – в зависимости от клинической стадии болезни. Гормональная терапия – один из стандартов нехирургического лечения распространенного РПЖ. Простата – гормоночувствительный орган, биохимические процессы в котором зависят от уровня тестостерона. Устранение его влияния на ткань простаты позволяет добиться гибели гормоночувствительных клеток, присутствующих в раковой опухоли.
Наряду с дистанционным лучевым воздействием в лечении локализованного РПЖ используется интерстициальная лучевая терапия, или брахитерапия. Источники излучения, введенные непосредственно в опухоль, обеспечивают более локальное воздействие. Опыт подобного лечения в отдельных странах насчитывает более 20 лет. Она применима у пациентов с относительно небольшими размерами простаты и невысокими значениями ПСА и обеспечивает хорошие результаты лечения.
Криотерапия представляет собой аблацию ткани путем локального воздействия очень низкой температуры и также показана пациентам с локализованным РПЖ. В 1996 г. Американская ассоциация урологов признала криоаблацию предстательной железы методом терапии локализованного РПЖ и перестала считать данную методику экспериментальной. В настоящее время криоаблация простаты представляет собой минимально инвазивный высокоэффективный способ лечения РПЖ. Посредством введения в простату 12–20 криоигл можно добиться локального снижения температуры тканей ниже 40°С. При этой температуре целостность клеток нарушается, и опухоль разрушается. В дальнейшем на этом месте происходит процесс рубцевания. Ограничения при выборе пациентов для криоаблации простаты сравнимы с таковыми при брахитерапии – большой объем простаты и выход опухоли за границы простаты. Неоспоримые преимущества криоаблации и брахитерапии – малая травматичность операции, низкий процент осложнений и меньшее количество ограничений в связи с возрастом и общим терапевтическим статусом пациента.
Высокоинтенсивный сфокусированный ультразвук, также относящийся к малотравматичным методам лечения, пока не одобрен мировой урологической общественностью ввиду малой продолжительности наблюдений и остается экспериментальным методом лечения РПЖ.
Важно помнить, что вопрос принятия решения о тактике лечения во многом зависит от выбора самого пациента и является результатом подробной беседы со специалистом, включающей тщательный анализ преимуществ и рисков того или иного метода лечения.
В этой статье мы не преследовали цель дать исчерпывающие знания о принципах диагностики и лечения рака простаты – проблемы сложной и многогранной. Мы лишь пытались создать представление о современных возможностях лечения этого грозного заболевания. Рак простаты хорошо поддается лечению и давно перестал быть приговором.
Для того, чтобы понять, чем чреват для представителя мужского пола рак простаты, целесообразно для начала изучить сам орган и его функции.
Простата или, иначе, предстательная железа, располагается в нижней части таза, ниже мочевого пузыря. Она окружает мочеиспускательный канал, поэтому увеличение размеров при раке простаты почти всегда сказывается на качестве мочеиспускания.
В норме железа имеет округлую форму и размер порядка 3-4 см. В простате выделяют три доли – правую, левую и среднюю.
В мужском организме предстательная железа участвует в продуцировании сперматозоидов и поддерживает их жизнеспособность, помогает выводить сперму, доводит консистенцию эякулята до нужной консистенции за счет собственного секрета, блокирует выход из мочевого пузыря при эрекции.
К сожалению, с возрастом ткань этого органа может качественно меняться. При некоторых сопутствующих обстоятельствах возникает риск развития рака простаты.
Рак предстательной железы
Согласно статистике, рак простаты является одной из наиболее распространенных мужских онкологических патологий. Он находится на четвертом месте после злокачественных новообразований в легких, желудке и на коже.
Подвержены данному заболеванию преимущественно представители негроидной расы. За ними идут европеоиды. А вот азиаты болеют раком простаты намного реже – они в статистике находятся на последнем месте.
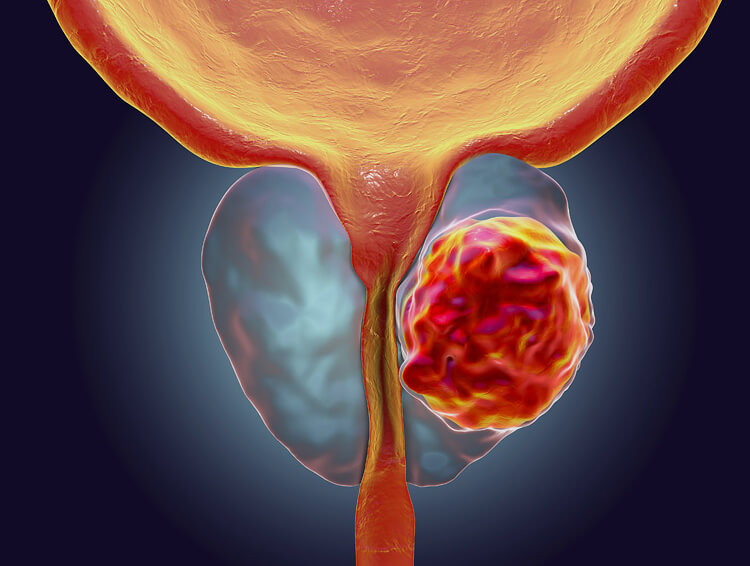
Чаще всего опухоль простаты встречается среди пациентов пожилого возраста – старше 60 лет. В этом возрасте болезнь обнаруживается у каждого сотого представителя мужского пола. Нередко заболевание диагностируют у мужчин в возрасте от 40 до 60 лет – примерно у 1 из 10 тысяч. Результаты обследований пациентов младше 40 лет не выявляют значительного количества заболевших в этой возрастной категории. А вот среди мужчин старше 75 лет рак простаты находят у каждого восьмого.
В международном классификаторе болезней МКБ-10 рак предстательной железы кодируется как С61.
Как возникает рак предстательной железы? В норме жизнеспособные клетки растут и по мере необходимости делятся, образуя дочерние. Постепенно они отживают свое и отмирают. Новые подросшие клетки заменяют старые изношенные. Такой процесс проходит в организме непрерывно, обеспечивая безотказное выполнение органом возложенных на него функций. Процесс отмирания и распада называют апоптозом.
Иногда клетки, из которых состоит ткань простаты, начинают размножаться бесконтрольно и при этом утрачивают способность к апоптозу. Постепенно они могут проникать в другие органы и ткани, нарушая процессы жизнедеятельности организма. При обнаружении этого состояния у пациента можно говорить о раке предстательной железы, конечно, после проведения тщательной диагностики и исключения других заболеваний, обладающих сходной симптоматикой.
Поскольку рак простаты является злокачественным новообразованием, прогнозы и последствия в отношении этой патологии схожи с прогнозами и последствиями для других онкологических процессов. Это, в частности:
- ухудшение качества жизни пациента;
- вероятность рецидива – повторного роста опухоли простаты после ее удаления;
- проникновение клеток в соседние органы и ткани, а также в кровеносную и лимфатическую системы. Такой процесс называется метастазированием;
- риск летального исхода. Хотя онкология простаты считается медленно растущей и не всегда бывает агрессивной, рано или поздно она может привести к смерти больного.
На сегодняшний день причины возникновения рака простаты достоверно не известны. По результатам научных исследований можно выделить лишь определенные факторы риска. При неблагоприятном стечении обстоятельств заболевание с большей вероятностью возникнет у пациентов с такими факторами, нежели у представителей сильного пола, не обремененных ими.
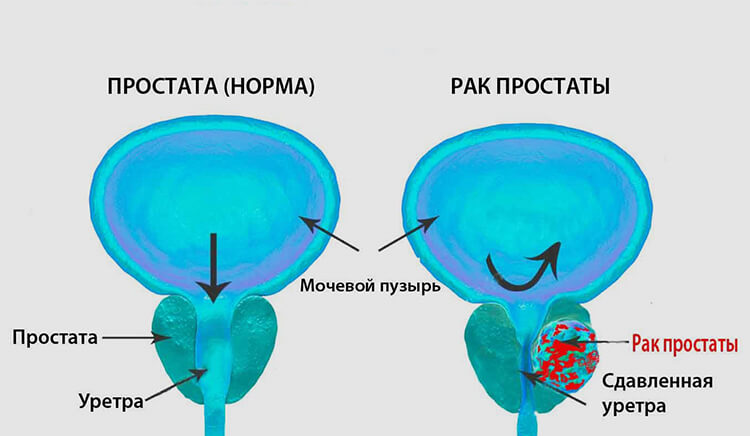
Итак, условными причинами рака простаты у мужчин считаются:
- возраст. Как уже было сказано ранее, вероятность онкологии простаты возрастает по мере увеличение возраста;
- наследственность. Отмечена некоторая взаимосвязь в этом направлении. Если в семейном анамнезе у близких родственников (отца, деда, брата) подобный диагноз присутствовал, мужчине следует быть особенно внимательным к состоянию своей предстательной железы;
- рацион питания. Отмечено, что рак простаты чаще возникает у пациентов, предпочитающий животные жиры и красное мясо, нежели у тех, кто значительную долю своего меню оставляет под фрукты, овощи, цельные крупы и жиры растительного происхождения;
- эндокринное происхождение рака предстательной железы, связанное с физиологическим возрастным снижением интенсивности синтеза мужских половых гормонов, поддерживается рядом специалистов;
- нерегулярная половая жизнь. Она провоцирует застойные явления в тазовой области и может со временем привести к возникновению неконтролируемого клеточного процесса, а значит, и рака простаты. К подобным последствиям приводит и многолетний малоподвижный образ жизни;
- некоторые инфекции. Ретровирус, цитомегаловирус, герпес второго типа могут спровоцировать развитие онкологического процесса в предстательной железе.
Кроме того, хоть и не являются непосредственными причинами рака простаты у мужчин, но относятся к факторам риска: инфекции, передающиеся половым путем, курение и злоупотребление алкоголем, интоксикация кадмием на вредных производствах, стрессы и хронические патологические процессы в организме, приводящие к снижению иммунитета, а также простатит и аденома простаты, особенно, не леченные должным образом.
Чтобы определить форму опухоли простаты, при диагностике специалисты часто пользуются гистологической классификацией В. Л. Бялика. Согласно этой классификации, рак простаты подразделяют на:
- полиморфноклеточное озлокачествление, при котором обнаруживается значительное количество делящихся клеток разных форм и размеров;
- анапластическую аденокарценому – при таком раке простаты меняется внутриклеточная структура, а сами клетки приобретают атипичные формы;
- солидный рак – характеризуется наличием целых пластов видоизмененных клеток. Эти пласты разделяются между собой тонкими прослойками соединительной ткани;
- скиррозную форму, при которой в опухоли присутствует больше соединительной ткани, нежели злокачественных клеток, что обуславливает ее фиброзную консистенцию;
- аденокарционму – рак предстательной железы, сформировавшийся из железистого эпителия. Аденокарцинома является наиболее часто встречающейся онкопатологией простаты – до 95% всех диагностированных случаев;
- плоскоклеточный рак, развивающийся из плоского эпителия;
- тубулярный – стартовавший из узких каналов;
- альвеолярный – образовавшийся в концевых отделах желез.
Чаще всего рак простаты у мужчин возникает в периферических долях предстательной железы. На среднюю долю приходится не более 10% всех выявленных случаев.
Дабы грамотно выстроить эффективную стратегию лечения, важно во время обследования правильно определить стадию рака простаты пациента. При ее установлении учитываются размер новообразования, наличие и степень распространенности на другие органы и ткани, а также уровень простат-специфического антигена (ПСА) в крови больного.
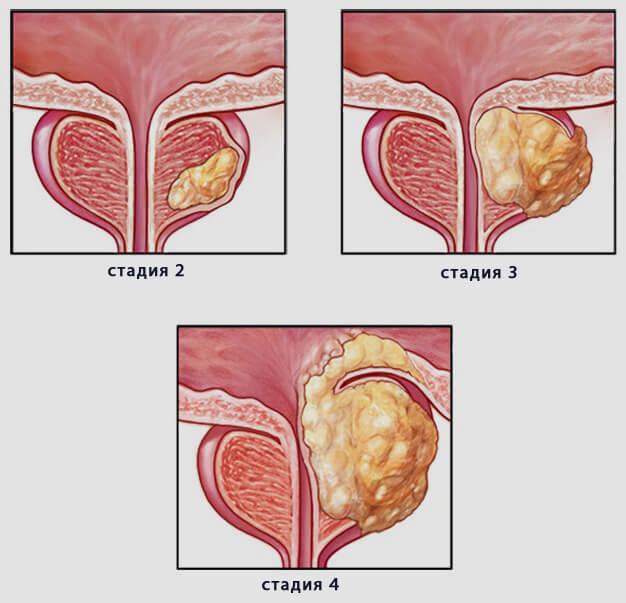
Исходя из вышесказанного, выделяют следующие стадии рака предстательной железы:
- стадия I. Опухоль небольшого размера, сложно прощупывается при ректальном исследовании, локализована исключительно в пределах простаты. Уровень ПСА – менее 10 нг/мг;
- стадия II. Образование более крупное, его можно выявить в процессе ректального исследования. На этом этапе опухоль простаты все еще не выходит за пределы предстательной железы. Уровень ПСА в крови превышает 10 нг/мг, но не достигает 20 нг/мг;
- стадия III. Рак простаты распространяется на соседние доли железы и за его пределы, на ближайшие органы – мочевой пузырь, прямую кишку, семенные пузырьки. Уровень ПСА на этой стадии – более 20 нг/мг. Верхнего предела не существует;
- стадия IV. Опухоль простаты затрагивает лимфоузлы, может распространиться на отдаленные органы, кровеносную и костную системы. Эта стадия характеризуется неконтролируемым уровнем ПСА. Кроме того, именно на четвертой стадии пациент начинает ощущать выраженную симптоматику заболевания.
Первые две стадии рака простаты относят к ранним, третью и четвертую – к поздним. С учетом этого разработается и тактика дальнейших действий. Для ранних стадий она, в зависимости от обстоятельств, может быть выжидательной либо лояльной. Поздние же стадии рака предстательной железы требуют интенсивной терапии, а иногда – и оперативного вмешательства.
Существует и другая система стадирования заболевания – более подробная. При определении стадии рака простаты классификация ТНМ предлагает ориентироваться на три фактора, отраженные в аббревиатуре названия.
Т – tumor: опухоль, новообразование, его размер по отношению к предстательной железе, месторасположение и степень распространения.
N – nodus: лимфатические узлы и их уровень поражения раком простаты.
M — metastasis – метастазы: отсутствие, наличие, количество и месторасположение метастаз в органах и тканях.
Для максимально точной диагностики рака предстательной железы рекомендуется использовать одновременно несколько методик.

Классификация рака простаты
Рак предстательной железы является самой актуальной проблемой современной онкоурологии. Тщательное лабораторно-инструментальное исследование злокачественного образования позволяет определить стадию и степень дифференцировки патологического очага. Эти характеристики влияют на прогноз заболевания, на тактику лечения и его эффективность. Центр урологии в Москве обладает широкими диагностическими возможностями, которые помогают определить стадию и степень дифференцировки опухолевого очага в кратчайшие сроки.

Гистологические формы рака простаты представлены в 90% аденокарциномой (опухоль из железистой ткани), гораздо реже – плоскоклеточными и переходноклеточными формами. Стадий канцерогенеза насчитывается 4, а степеней дифференцировки существует 5. В клинической практике для постановки диагноза учитываются все данные, что позволяет повысить эффективность лечения.
Стадии опухолевого процесса
Еще в прошлом веке медицина пришла к выводу, что успех лечения во многом зависит от степени разрастания опухоли. Любой опухолевый очаг имеет две клинически значимые формы: локальную и распространенную. При локальной форме опухолевый узел находится только в предстательной железе и не выходит за ее пределы. Распространенная форма имеет очаги метастазирования в органах малого таза или в других системах органов. В институте урологии в Москве высококвалифицированные онкоурологи определяют дальнейшую терапевтическую тактику, используя две классификации стадийности онкопроцесса: клиническую и международную.
В клинической практике десятки лет используется следующее описание стадий канцерогенеза:
I стадия – опухоль не выявляется при ректальном осмотре, обнаружить ее можно только при помощи гистологического исследования;
II стадия – злокачественное новообразование можно обнаружить при пальцевом исследовании и при помощи УЗИ-диагностики, но очаг не выходит за пределы органа;
III стадия – опухоль выявляется любыми диагностическими методами и выходит за пределы предстательной железы, поражая жировую клетчатку и анатомические образования органов малого таза;
IV стадия – наличие отдаленных метастазов в других системах органов (печень, костная система, головной мозг, легкие). 4 стадия выставляется при обнаружении метастаза в любом другом органе, даже если сам опухолевый очаг имеет маленькие размеры.
Для унификации и стандартизации описания опухолей была создана специальная международная TNM-классификация. TNM – это аббревиатура, состоящая из трех латинских слов: Tumor (опухоль), Nodus (лимфоузел) и Metastasis (метастаз). Эта классификация учитывает множество показателей: размер опухоли, анатомическую локализацию, метастазирование, поражение лимфатической системы.
Т – описание опухолевого узла, его размеров и распространенности:
N – опухолевое поражение регионарных (тазовых) лимфоузлов
Nх– невозможно оценить состояние регионарных лимфоузлов из-за недостатка данных.
N0– отсутствие метастазирования в тазовые узлы;
N1– найдены метастазы в регионарных лимфатических узлах.
М – отдаленное метастазирование опухолевых клеток:
Мх– недостаточно данных, чтобы выявить отдаленные очаги метастазирования;
М0– нет метастазирования в другие органы;
М1– найдены отдаленные очаги метастазирования: М1а – в любых других лимфатических узлах, кроме тазовых, М1b – в костную систему, M1c – метастатическое поражение других органов.
Каждому пациенту, посетившему клинику урологии в Москве, после получения данных диагностического исследования, разъясняются полученные результаты. Во время беседы лечащий врач расскажет об оптимальной терапевтической или хирургической тактике лечения с учетом индивидуальных особенностей пациента.
Степени дифференцировки раковых клеток
Этот показатель позволяет судить об агрессивности опухолевого узла, скорости его роста и распространения. Степень дифференцировки показывает насколько найденные опухолевые клетки похожи на нормальные клетки предстательной железы. Чем больше гистологическая схожесть, тем больше степень дифференцировки опухоли и благоприятнее прогноз. Гистологическая верификация осуществляется опытными врачами-гистологами нашего центра урологии в Москве, что исключает вероятность постановки неправильного диагноза.
Для оценки гистологической картины предварительно проводится биопсия из нескольких участков простаты (их должно быть не менее шести), а затем врач под микроскопом изучает строение клеток. Для объективности оценки канадским патоморфологом Глисоном была предложена особая шкала, которая впоследствии получила его имя. 1 степень дифференцировки говорит о минимальной атипии клеток, а последняя – о сильных различиях между опухолевыми и нормальными клетками.
По шкале Глисона различают следующие степени рака:
1 – клетки высокодифференцированы, но имеют небольшие структурные отличия от нормальных, железистая ткань представленная неоднородными слоями железистых клеток.
2 – в железистой ткани увеличивается количество стромального (соединительнотканного) компонента;
3 – появление структурно измененных клеток и инфильтрация ими предстательной железы, особенно по краям долей:
4 – значительное уменьшение массы железистой ткани, замещение ее атипичными клетками;
5 – выявленные клетки кардинально отличаются от нормальных клеток простаты: железистые клетки полностью отсутствуют в поле зрения.
Для более точной и безошибочной постановки диагноза врачами клиники урологии в Москве оценивается гистологический результат в нескольких биоптатах предстательной железы. Кроме того, учитывается дифференцировка не только преобладающих клеток опухоли, но и вторых по распространенности. Этот показатель носит название суммы Глисона.
Диагностика, лечение и прогнозы рака в зависимости от стадии
Диагностический поиск направлен в первую очередь на идентификацию опухолевого очага, определение его расположения в толще органа и выявление гистологической формы. Во всех странах мира идет активная политика, направленная на раннее выявление и лечение заболевания. Для этого на уровне Министерств здравоохранения созданы специальные скриннинговые программы, включающие в себя:
при посещении врача любой специальности обязательно проводится пальцевое ректальное исследование всех пациентов старше 45 лет на предмет выявления новообразования;
при подозрении на злокачественное новообразование следует сдать венозную кровь на простатический специфический антиген (PSA);
при пальпируемом образовании предстательной железы или наличии клинической симптоматики проводится трансректальное УЗ-исследование.
Для определения стадии и степени рака предстательной железы также используются следующие методы: прицельная биопсия тканей простаты под ультразвуковым контролем, КТ и МРТ для детализации информации об опухолевом очаге и выявления очагов метастазирования.
После постановки диагноза врач сообщает пациенту о методах лечения, которые наиболее оптимальны и эффективны в его случае. Решение высококвалифицированных онкоурологов основывается не только на многолетнем опыте работы и клинических знаниях, но и на результатах доказательной медицины. Современной медициной доказано, что радикальная простатэктомия на ранних стадиях процесса снижает летальность на 90-95 процентов, а риск рецидива возникает не более, чем в 10% случаев. На поздних стадиях канцерогенеза хирургическое лечение помогает в 50-60% случаев, и чтобы увеличить эффективность терапии дополнительно назначают лучевые и химиотерапевтические методы. Даже в запущенных случаях нередко удается достигнуть высоких показателей десятилетней выживаемости пациентов. Этого можно добиться только при индивидуально подобранной терапевтической тактике с учетом клинических рекомендаций международного уровня.
В институте урологии в Москве пациент находится под тщательным динамическим наблюдением лечащих врачей, что позволяет свести до минимума осложнения от терапии. Лечение опухолей предстательной железы проводится хирургическими, лучевыми и химиотерапевтическими методами с учетом состояния пациента, что дает возможность повысить отдаленные положительные онкологические результаты.
Читайте также:

