Рак почки с инвазией в паранефральную клетчатку
Найдено вопросов: 51
- Вопрос: #78671
- Спрашивает: Светлана ( г. Благовещенск )
- 10.08.2017
- 08:08

- Вопрос: #78641
- Спрашивает: Ольга ( г. Ленинск-Кузнецкий, Кемеровская обл. )
- 28.07.2017
- 20:07

- Вопрос: #78587
- Спрашивает: людмила ( г. санк петербург )
- 11.07.2017
- 18:07

- Вопрос: #78568
- Спрашивает: Наталья ( г. Киев )
- 05.07.2017
- 17:07

- Вопрос: #78566
- Спрашивает: Наталья ( г. Киев )
- 05.07.2017
- 15:07

- Вопрос: #78557
- Спрашивает: Лили ( г. Киев, Украина )
- 03.07.2017
- 13:07

- Вопрос: #78550
- Спрашивает: Светлана ( г. Амурская область, Г. Благовещенск )
- 28.06.2017
- 00:06

- Вопрос: #78497
- Спрашивает: Ярослава ( г. Украина, Киев )
- 08.06.2017
- 10:06

- Вопрос: #78485
- Спрашивает: Людмила ( г. краснодар )
- 04.06.2017
- 22:06

- Вопрос: #78431
- Спрашивает: Андрей ( г. Судак, Россия. )
- 22.05.2017
- 18:05

197136 , г. Санкт-Петербург
ул. Ленина, д. 34
+7 (812) 235-14-87
+7 (812) 235-69-88
+7 (812) 235-67-88
Высокая степень диффе-
Таким образом, при локализованном новообразовании пациенты более молодого возраста чаще выявляются случайно при профилактическом УЗИ, при этом у них меньше размеры новообразования и более часто высокая степень дифференцировки раковых клеток по сравнению с местнораспространенной опухолью. Наибольшие изменения тактика лечения претерпела при раке почки, ограниченном пределами фиброзной капсулы. У этой группы пациентов пересмотрено положение об облигатности радикальной нефрэктомии. Новые методы диагностики, включая МСКТ и МРТ, позволили почти полностью отказаться от ангиографии и экскреторной урографии у этих пациентов при планировании органосохраняющей операции. Обсуждение тактики лечения особенно актуально для данной группы пациентов, у которых приходится делать выбор: нефрэктомия или резекция? Выбор органосохраняющего или органоуносящего оперативного пособия является тактической задачей при раке почки, ограниченном паранефральной клетчаткой, когда нет метастатического распространения опухоли, т.е. при стадиях Т1—3аN0М0. При Т2 стадии опухоль также ограничена фиброзной капсулой почки, но ее размеры превышают 7 см, т.е. новообразование замещает большую часть почки и выполнение органосохраняющей операции невозможно по техническим причинам. Число больных раком почки Т2 стадии, которым выполнена резекция почки, было крайне незначительным, в связи с чем они исключены из анализа.
Обсуждение правильности выбора лечебной тактики на основании анализа отдаленных результатов актуально для больных раком почки стадии Т1аN0М0, Т1бN0М0 и Т3аN0М0. Как известно, стадия Т1а отличается от Т1б только размерами новообразования (до 4 см и от 4 до 7 см), а Т3а — прорастанием опухоли в паранефрий вне зависимости от размеров новообразования. При размерах опухоли более 7 см в ряде наблюдений возможно выполнение резекции почки, если опухоль распространяется преимущественно экстраренально, но для этого должны быть абсолютные показания к органосохраняющей операции. Следовательно, при размере опухоли более 7 см выбор лечебной тактики не зависит от предпочтений хирурга-уролога. При этом функция как ипси- так и контралатеральной почки должна быть сохранна или снижена незначительно, чтобы исключить влияние этих факторов на тактику лечения. Соматический статус больного, а также наличие и выраженность интеркуррентных заболеваний зачастую заставляют планировать операцию в минимальном объеме и согласовывать тактику с анестезиологом. Для объективизации выбора нефрэктомии или резекции мы исключили из анализа пациентов пожилого и старческого возраста с выраженными интеркуррентными заболеваниями.
В последнее время появился термин "элективные", или избирательные показания к органосохраняющей операции, когда лечебная тактика зависит от предпочтений врача при информированном согласии пациента. Для объективизации правомочности выбора лечебной тактики необходимо сравнить отдаленные результаты в двух однородных по полу, возрасту, стадии заболевания группах больных.
Врач осуществляет выбор органосохраняющей или органоуносящей операции при информированном согласии пациента в следующих случаях:
- удовлетворительное состояние пациента при отсутствии выраженных интеркуррентных заболеваний;
- сохранная функция как ипси-, так и контралатеральной почки;
- отсутствие заболеваний (выраженные артериальная гипертензия, сахарный диабет,
- мочекаменная болезнь, нарушения пуринового обмена в анамнезе), которые могут привести к нарушению почечной функции в будущем;
- размеры новообразования 4 см целесообразнее органоуносящее пособие.
Отдаленные результаты лечения больных раком почки рТ1а, рТ1б и рТ3а стадии при размерах опухоли 4 см предпочтительнее радикальная нефрэктомия. Мы согласны с мнением Н.А. Лопаткина и соавт., что "при технической возможности, достаточной функциональной значимости оставшейся части паренхимы и эффективной чашечно-лоханочной системы целесообразно выполнение резекции почки даже при интактной контралатеральной почке. Данное вмешательство является не менее радикальным, чем нефрэктомия".
Внастоящее время выбор лечебной тактики в подавляющем числе наблюдений осуществляется на основании из данных УЗИ и МСКТ, которые не позволяют достоверно дифференцировать Т1 и Т3а стадию. В то же время дифференциальная диагностика Т1 и Т3а стадии важна при размерах новообразования > 4 см. Применение этих двух методов для выбора нефрэктомии или резекции почки правомочно, так как они позволяют установить, возможна ли резекция почки в пределах здоровых тканей. Такая возможность определяется исходя из характеристик опухолевого процесса. Считаем, что после выявления объемного новообразования почки при УЗИ целесообразно выполнение МСКТ почек с контрастированием и трехмерной реконструкцией почечных сосудов и чашечно-лоханочной системы (при наличии технической возможности). В подавляющем большинстве наблюдений получаемой информации достаточно для определения лечебной тактики. Томографические методики дают представление о характеристиках опухолевого процесса и позволяют выбрать тактику лечения. Производится сравнение и дополнение данных УЗИ результатами томографии. Какова же точность используемых методов характеристики опухолевого процесса? Чтобы ответить на этот вопрос, мы оценили истинно-положительные и истинно-отрицательные результаты исследований. Точность УЗИ определена у 300 больных опухолью почки, МСКТ — у 250 и МРТ — у 90 (табл. 5).
Таблица 5. Точность (%) УЗИ, МСКТ и МРТ при характеристике опухолевого процесса
Можно отметить, что несмотря на широкое внедрение современных методов исследования, включая МСКТ и МРТ, имеются наблюдения (5—8%), когда характеристики опухолевого процесса по данным томографической методики были определены неточно. Полученные данные свидетельствуют о том, что информативность МСКТ и МРТ в отношении характеристик опухолевого процесса примерно одинакова (95%) и выше, чем УЗИ (89%). В то же время у ряда больных возможность осуществления органосохраняющей операции в пределах здоровых тканей окончательно может быть определена только интраоперационно. Мы считаем, что онкологическая операция должна быть радикальной, а лимфаденэктомия — обязательный компонент операции по поводу рака почки, какой бы характер (органосохраняющий или органоуносящий) она не носила. Из 493 больных раком почки, оперированных в нашей клинике за последние 10 лет, у 49 (10%) выявлены лимфогенные метастазы. Лишь у 19 (38%) больных до операции были данные о том, что лимфатические узлы увеличены и что данную клиническую ситуацию следует рассматривать, как распространенный рак почки. Таким образом, до операции у 474 больных раком почки лимфатические узлы не были увеличены.
Поясним, почему мы считаем лимфаденэктомию обязательной при неизмененных лимфатических узлах:
- метастатическое поражение регионарных лимфатических узлов выявлено у 30 (6,3%) из 474 больных раком почки, которые оперированы при неизмененных лимфатических узлах:
- что у 30 (61,2%) из 49 больных лимфогенные метастазы были микроскопическими, свидетельствует о целесообразности лимфаденэктомии даже при внешне нормальных лимфатических узлах;
- удаление воротных и превазальных (преаортных или прекавальных в зависимости от стороны поражения) лимфатических узлов в ходе мобилизации магистральных сосудов почки обеспечивает надежный контроль почечных сосудов, что делает оперативное пособие более безопасным;
- ни один из методов дооперационного обследования, в том числе УЗИ, МСКТ и МРТ, не позволяет исключить поражение лимфатических узлов микрометастазами;
- лимфаденэктомия не увеличивает количество осложнений, а также послеоперационную летальность;
- удаление возможных лимфогенных метастазов (в том числе микроскопических) значительно уменьшает вероятность возникновения регионарного рецидива.
Вероятность наличия микрометастазов во внешне неизмененных лимфатических узлах — один из основных аргументов в пользу лимфаденэктомии.
Таким образом, можно сделать следующие выводы:
- При рТ1а, рТ1б и рТ3а стадии и размерах новообразования 4 см целесообразнее проведение нефрэктомии.
- Окончательно возможность осуществления органосохраняющей операции в некоторых наблюдениях может быть установлена только интраоперационно после проведения УЗИ.
- Планирование органоуносящей или органосохраняющей операции при локализованном или местно-распространенном раке почки базируется на анализе размеров, локализации, стадии процесса. Даже при кажущейся большой возможности для выполнения резекции почки интраоперационно могут возникнуть такие ситуации, при которых потребуется нефрэктомия. Поэтому "информированное" согласие пациента означает его осведомленность о возможных вариантах как самой операции, так и прогноза.
- При локализованном и местно-распространенном раке почки, какой бы характер не носила операция (органосохраняющий или органоуносящий), целесообразно осуществление систематической лимфаденэктомии.
Авторы: Ю.Г. Аляев, А.А. Крапивин
Урологическая клиника ММА им. И.М. Сеченова
Материал взят из журнала "Онкоурология", №1, 2005
Почечно-клеточный рак – серьёзное поражение тела, которое часто заканчивается смертельным исходом. Это обусловлено бессимптомным течением начальных стадий патологического процесса. Данные статистики тревожат: согласно отчётам, частота встречаемости недуга ежегодно растёт.
Группу риска по болезни составляют мужчины 50-70 лет. У женщин и молодежи эта карцинома встречается, но реже. При отсутствии своевременного обращения за медицинской помощью этот вид онкологии представляет серьёзную опасность для жизни человека.
Понятие почечно-клеточной онкологии
Почечно-клеточный рак – онкология в мочеполовой системе. Клетки опухоли имеют округлый вид, по размеру образование способно занимать половину брюшной полости. Очаг поражения – эпителий почки и ткани почечных лоханок. Болезнь носит непредсказуемый стремительный характер развития. Наиболее часто при почечно-клеточной онкологии метастазы идут в ткани лёгких и печени, в костную ткань, в отделы головного мозга.
Признаки почечно-клеточной опухоли
Начало болезни почки бессимптомно. Первостепенные признаки патологического процесса в органе:
- в моче присутствуют нитевидные кровяные образования;
- дискомфорт внизу спины;
- уплотнение в почках, обнаруживается при пальпации.
Если из вышеперечисленных обнаружен хотя бы единственный симптом, стоит незамедлительно обратиться к врачу. Если отложить визит в медицинское учреждение, к указанным симптомам вскоре добавляется постоянная ноющая боль внизу спины, беспричинная лихорадка, недомогание, усталость, потеря массы тела.
Причины почечно-клеточного злокачественного процесса
Списка точных причин, гарантированно приводящих к онкологии, нет. Однако учёными определены факторы, помогающие развитию заболевания:
- табакокурение и алкоголизм;
- чрезмерное употребление красного мяса;
- избыточная масса тела;
- гормональные сбои в организме;
- сахарный диабет;
- заболевание мочеполовой системы воспалительного характера;
- артериальная гипертензия;
- бесконтрольное употребление в качестве обезболивающего средства фенацетина;
- воздействие радиоактивных лучей;
- поликистоз почек в результате гемодиализной терапии;
- генетическая предрасположенность;
- травмы почек;
- работа на вредном производстве, связанная с воздействием на организм асбеста, рентгеноконтрастных и кожедубильных веществ.
Этапы развития болезни и её разновидности
Почечно-клеточная карцинома проходит 4 стадии развития. Система TNM представляет описание онкологии: буква Т обозначает факт новообразования. N – отражает вовлеченность в метастазирование лимфоузлов. М – характеризует метастазирование. Течение почечно-клеточной онкологии распределяется по стадиям:
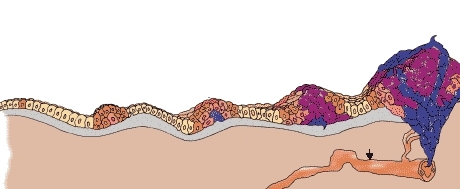
Стадия 0 – размер опухоли маленький, обнаружить её с помощью средств лабораторной диагностики невозможно. Иначе стадия называется g1 – клетки опухоли мало отличаются от здоровых.
Стадия 1 – онкологический процесс начинает прогрессировать. Опухолевое образование в диаметре до 7 см. Это стадия g2, степень патологического процесса средняя.
Стадия 2 – размер опухоли от 7 до 10 см. Новообразование размещается в тканях почки. Метастазов нет. Это стадия g3, онкоклетки специфически выглядят.
Стадия 3 – опухоль разрастается, но не выходит за пределы почечной капсулы. Это стадия g4, при которой онкоклетки резко отличаются от здоровых тканей.
Стадия 4 – рак распространяется метастазами в лимфоузлы, нарушая контуры капсулы почки. Это последний шаг развития недуга. Это стадия gх, онкоклеток уже больше, чем здоровых.
Почечно-клеточный рак классифицируют и по другому критерию:
- Онкология со светлыми клетками. Светлоклеточный вариант рака появляется в результате начала патологического процесса в клетках паренхимы.
- Папиллярный вариант рака. Образуется в тканях почечной лоханки. Онкоклетки этого заболевания называются сосочковыми. Патология встречается редко, но хорошо лечится.
- Хромофобная опухоль. Поражает каналец внутри почек и его корковый слой. Этот вид онкологии представляет интерес для исследователей: сейчас наука располагает ограниченной информацией об указанной разновидности опухоли.
- Онкоцитарная опухоль – заболевание редкое, отличается стремительным развитием, но незначительными метастазами.
- Протоковая онкология – рак трубочек. Этот вид карциномы появляется в центре почки и агрессивно метастазирует. Самый редкий злокачественный тип опухоли.

Диагностика рака опирается на результаты гистологических лабораторных исследований. Благодаря уровню развития современной медицины врачам всё чаще удаётся выявить наличие признаков злокачественного процесса на его начальных стадиях. Это определяет увеличение числа случаев успешного исцеления.
Диагностика почечно-клеточного рака
Как правило, заболевание обнаруживается на поздних стадиях. Для определения типа и этапа развития онкологии применяются специальные процедуры:
- Урография и общий анализ мочи. Процедуры помогают оценить дисфункцию почек в результате онкопоражения. Результат анализа свидетельствует о повышенном СОЭ.
- Ангиография почек – вариант рентген-диагностики. При этой процедуре диагностируются сосуды в почках с помощью рентген-аппарата.
- Рентген-исследование грудной клетки. Посредством исследования врачи делают выводы о метастазах в область лёгких через костную ткань.
- Результат анализа крови свидетельствует о повышенном уровне эритроцитов, креатинина, кальция, СОЭ. Показатели гемоглобина при раке низкие, что связано с анемией.
- УЗИ почек. Эта диагностика позволяет установить локализацию новообразования, оценить его размер и наличие метастазирования в соседние ткани и органы.
- УЗИ с использованием доплера. Данная процедура позволяет изучить состояние кровоснабжения почек и установить наличие поражения онкологией кровеносных сосудов.
- МРТ и КТ. Эти компьютерные исследования призваны подтвердить и уточнить данные, полученные с помощью УЗИ.
- Гистологический анализ. Для анализа берётся образец онкоткани, по которому определяется стадия болезни и разновидность.
Людям, занятым на вредном производстве, рекомендуется систематически проходить обследование на выявление онкологии, так как работа в таких условиях считается одним из факторов риска возникновения рака.
Лечение почечно-клеточного рака
Этот вид рака обнаруживает специфические особенности в лечении:
- Устойчивость поражённых клеток к воздействию консервативных способов терапии, в частности – к лучевой терапии и препаратам, применяемым в химиотерапии.
- Иногда размер опухоли сокращается, а течение болезни замедляется без медицинского вмешательства.
Основное лечение почечно-клеточного рака – операция.
Если размер новообразования не превышает 4 см в диаметре, врач может принять решение о проведении органосберегающего вида хирургического вмешательства: в ходе операции удаляется только сама опухоль с минимальным количеством здоровых тканей почки. В качестве сопутствующей медикаментозной терапии будет назначен микропрепарат.
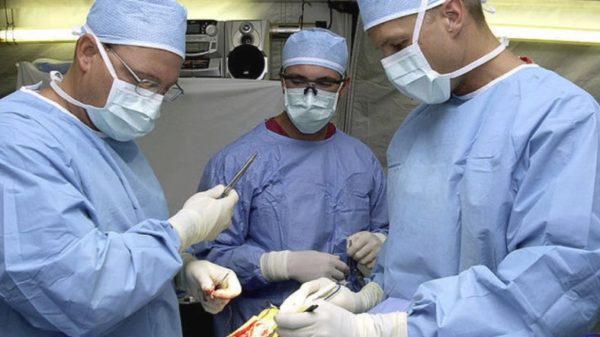
Если опухоль к моменту назначения операции разрослась, врач принимает решение о проведении полного удаления органа мочеполовой системы. В этом случае помимо почки удаляются и близлежащие лимфоузлы и жировые ткани, чтобы избежать вторичного развития онкологии. После кардинального оперативного вмешательства назначают определённый макропрепарат, оказывающий противоонкологическое действие для купирования начального распространения метастазов.
Вспомогательным методом лечения рака после операции является иммунотерапия, цель которой – искусственное формирование иммунитета и защитных сил организма. Эффективны препараты с интерферонами.
Учёными-медиками ведутся разработки новых противораковых препаратов, способные гарантировать выздоровление. К инновационным средствам лечения относится радиочастотная абляция, микроволновая абляция, криодеструкция.
Прогноз при онкологии мочеполовой системы зависит от степени прогрессирования онкологии и её вида. Если рак находится на 4 стадии, лишь 10% больных проживают 5 лет после операции. Соблюдение медицинских рекомендаций и иммунотерапия чуть-чуть продлевают жизнь человека. Если же пациент обратился за медицинской помощью на начальных стадиях болезни, то с вероятностью в 80% прогноз будет благоприятный: соблюдение клинических рекомендаций будет препятствовать повторному развитию рака и способствовать долголетней жизни человека.
Многие патологии возможно предотвратить. Для снижения риска возникновения рака мочеполовых органов рекомендуется:
- Бросить курить и по возможности отказаться от употребления крепких алкогольных напитков. Характерная особенность этой болезни – небольшие дозы алкоголя служат профилактическим и лечебным средством в борьбе с раком.
- Если выявлена воспалительная патанатомия различной локализации, стоит обращаться в медицинское учреждение за назначением лечения. Людям, у которых диагностированы заболевания мочеполовой системы, рекомендуется 1-2 раза в год прописать курс Канефрона, заваривать чай с брусничным листом, пить морсы.
- При гормональных сбоях в организме, о которых свидетельствуют задержки менструации у женщин или изменение характера влагалищных выделений, а также ухудшение качества волос, ногтей, кожи, рекомендуется обратиться за консультацией к гинекологу-эндокринологу для назначения гормональных препаратов для стабилизации уровня гормонов в организме.
- При первых тревожных симптомах со стороны почек незамедлительно проходить обследование, чтобы скорее вскрылась патологическая анатомия органа.
Классификация
Общепринятой системой стадирования почечно-клеточного рака (ПКР) служит классификация TNM, рекомендованная для использования в клинической и научной работе.
Эта классификация периодически претерпевает изменения с учетом накапливаемых знаний.
Последние изменения были внесены в 2009 г. (табл. 2-4).
Таблица 2-4. Классификация почечно-клеточного рака по системе TNM

Выделение подстадии pT1 более не является предметом дискуссий. Деление опухолей стадии Т2 по размерам было недавно включено в классификацию TNM (2009).
Опухоли с инвазией в клетчатку почечного синуса ранее относили к стадии рТ1. Однако с учетом накопленных данных можно предположить, что при инвазии опухоли в почечный синус прогноз хуже, чем при инвазии в паранефральную жировую клетчатку, следовательно, такие опухоли не нужно включать в группу стадирования рТ1.
Известно, что инвазия опухоли в надпочечник — крайне плохой прогностический признак, такие формы рака почки следует классифицировать как опухоли стадии Т4. В предыдущих версиях классификации TNM в ipynny рТ3b включали опухоли с инвазией как в почечную, так и в нижнюю полую вену.
В результате проведения многочисленных исследований прогностическою значения инвазии в нижнюю полую вену по сравнению с инвазией в почечную вену эти две ipyniibi в последнюю версию классификации TNM включены по отдельности. Точность разделения на N1 и N2 обсуждается. Для определения категории М у больных раком почки необходимо выполнять тщательное дооперационное инструментальное обследование, на сегодня включающее компьютерной томографии (КТ) грудной и брюшной полостей.
Прогностические факторы
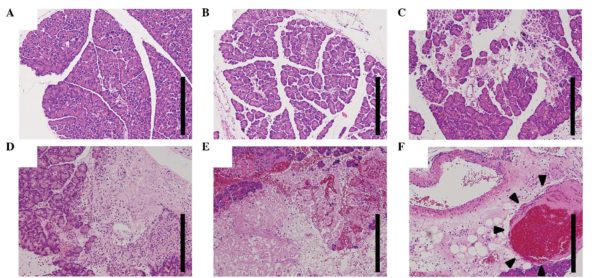
К гистологическим факторам относятся степень ядерной дифференцировки по Фурману, подтип ПКР, признаки саркоматоидного характера, инвазия в мелкие сосуды, некроз опухоли и инвазия в собирательную систему. Степень дифференцировки по Фурману является общепринятой системой гистологической классификации в случае рака почки, которая служит независимым прогностическим фактором.
Выделяют три основных гистологических подтипа почечно-клеточного рака: свелоклеточный — 80-90%, папиллярный — 10-15%, хромофобный — 4-5% случаев. Более благоприятный прогноз течения заболевания отмечают у пациентов с хромофобным раком по сравнению с таковым у больных папиллярным или светлоклеточным раком ночки. Однако прогностическое значение различий в гистологическом строении нивелируется при учете стадии опухолевого процесса.
Среди больных папиллярным раком было выделено две прогностически различные труппы: тип I — опухоль с низким злокачественным потенциалом, клетки с хромофильной цитоплазмой, благоприятный прогноз; тип II — опухоль высокого злокачественного потенциала, клетки с эозинофильной цитоплазмой, высокая предрасположенность к метастазированию.
В последние годы были разработаны послеоперационные прогностические системы и номограммы, включающие комбинации независимых прогностических факторов. Наиболее распространенные прогностические системы приведены в табл. 2-5.
Таблица 2-5. Наиболее распространенные прогностические модели для локализованного и метастатического рака почки

Динамическое наблюдение после нефрэктомии, резекции почки или аблятивной терапии почечно-клеточного рака
Динамическое наблюдение, проводимое после хирургического лечения, позволяет оценить функции почек, выявить наличие послеоперационных осложнений, местных рецидивов, развившихся после резекции почки или аблятивного лечения, рецидивов в контралатеральной почке, а также проанализировать возможность появления отдаленных метастазов.
Методам и срокам проведения контрольных обследований посвящено множество публикаций. В настоящее время нет единого мнения о необходимости динамического наблюдения за пациентами после лечения по поводу рака почки, и практически отсутствуют данные о том, что раннее выявление рецидива способствует улучшению выживаемости по сравнению с поздним его обнаружением. Однако послеоперационное наблюдение и контроль важны для того, чтобы увеличить объем знаний о ПКР. и урологи должны проводить его и указывать время, прошедшее с момента окончания лечения до наступления рецидива или развития метастазов.
Оценку послеоперационных осложнений и выделительной функции почек проводят на основании анамнеза, физикального обследования, определения концентрации сывороточного креатинина и EGFR. Осуществление регулярного контроля уровня EGFR в течение длительного времени позволяет увидеть, ухудшились функции почек после оперативного вмешательства или еще до операции.
Функционирование почек и выживаемость без признаков рака можно оптимизировать путем выполнения (по возможности) органосохраняющих операций в случае наличия опухолей стадий Т1 и Т2. Частота развития местных рецидивов невысока и составляет 2,9%, однако важно выявлять их на ранних стадиях, поскольку наиболее эффективным методом лечения в этом случае бывает выполнение циторедуктивных операций. Рецидив в контралатеральной почке также встречается редко (1,2%), риск его развития повышается при наличии опухолевой ткани по краю резекции, мультифокальном росте и высокой степе пи клеточной анаплазии.
Основная цель динамического наблюдения — раннее выявление метастазов. В частности, это важно при проведении абляционной терапии, такой как криотерапия или радиочастотная абляция. Даже несмотря на то что частота возникновения местных рецидивов в данном случае выше, чем при обычном хирургическом вмешательстве, больного все же можно вылечить путем повторной аблативной терапии или нефрэктомии.
Большее распространение опухоли при метастатическом течении заболевания может ограничить возможности хирургического лечения, которое служит стандартом при обнаружении резектабельных, особенно солитарных, метастазов. К тому же осуществление ранней диагностики рецидива, когда масса опухолевой ткани еще невелика, может способствовать повышению эффективности системной терапии, в том числе в рамках клинических исследований.
Интенсивное лучевое обследование не считают необходимым для всех пациентов, К примеру, при выполнении операций по поводу опухолей стадии Т1а и новообразований низких стадий почти всегда достигают хороших результатов. В связи с этим в зависимости от риска рецидивирования и метастазирования целесообразно осуществлять дифференцированный режим наблюдения. Данных рандомизированных исследований пока не существует, но результаты исследований прогностических факторов с большим сроком наблюдения больных уже позволяют сделать некоторые выводы.
При низкой вероятности развития рецидива может быть достаточно выполнения рентгенографии грудной клетки и ультразвукового исследования (УЗИ). Однако рентгенография малочувствительна к небольшим метастазам, а диагностическая ценность УЗИ имеет ограничения.
При наличии среднего или высокого риска возникновения рецидива методом выбора становится КТ органов грудной клетки и брюшной полости, хотя при этом следует учитывать побочное действие облучения, возникающее при проведении повторных КТ-исследований.
В зависимости от наличия новых эффективных методов лечения может потребоваться применение более жестких схем послеоперационного контроля и наблюдения, в частности при известном более высоком риске развития местного рецидива после проведения криотерапии или радиочастотной абляции. Проблемой является определение оптимального срока наблюдения за больным.
Существует мнение, что проведение наблюдения при помощи методов визуализации после 5 лег выживаемости уже нецелесообразно. Однако возникновение поздних метастазов возможно, хотя они с большей вероятностью будут одиночными и для их излечения понадобится более агрессивное лечение. Кроме того, пациенты, у которых опухоль дает рецидив в контралатеральную почку, могут быть излечены посредством выполнения органосохраняющей операции, если обнаруженная опухоль имеет небольшие размеры. Более того, для опухолей диаметром менее 4 см в ходе послеоперационного наблюдения не выявлено разницы в частоте возникновения рецидивов после осуществления нефрэктомии или резекции почки.
Некоторые авторы, в частности, M.W. Kattan, J.S. Lam, B.C. Liebovich и P.l. Karakiewicz, разработали системы баллов и номограммы для количественного определения вероятности возникновения рецидива, метастазов и последующей смерти пациента. Эти системы сравнивались и проходили валидацию. Было предложено несколько режимов осуществления динамического наблюдения в зависимости от стадии заболевания с использованием прогностических переменных, но ни один из них не включал применение абляционных методов лечения.
Разработаны послеоперационные номограммы, позволяющие оценить вероятность достижения безрецидивной 5-летней выживаемости. Совсем недавно была опубликована и прошла валидацию дооперационная прогностическая модель, основанная на возрасте, симптомах и стадировании по TNM. Соответственно для осуществления мониторинга больных почечно-клеточным раком необходимо использование алгоритма динамического наблюдения, в котором учитывался бы не только риск развития рецидива или появления метастазов, но также и эффективность проведенного лечения (табл. 2-7).
Таблица 2-7. Алгоритм динамического наблюдения с учетом профиля риска прогрессирования

Примечание: НЭ — нефрэктомия; РП — резекция почки; РГК — рентгенография грудной клетки; крио — криоабляция; РА — радиочастотная абляция.
Динамическое наблюдение, осуществляемое за пациентами после лечения по поводу рака почки, должно быть основано па факторах риска, выявленных для данного пациента, и типа полученного им лечения. Цель такого наблюдения — обнаружение местного рецидива или метастазирования на той стадии, когда больного еще можно излечить путем выполнения оперативного вмешательства.
Читайте также:

