Рак печени и рак груди
Сравнительно часто, прогностически не всегда благоприятно. Метастазы в печень при раке молочной железы надо лечить индивидуально, используя хирургическую операцию и химиотерапевтические препараты.
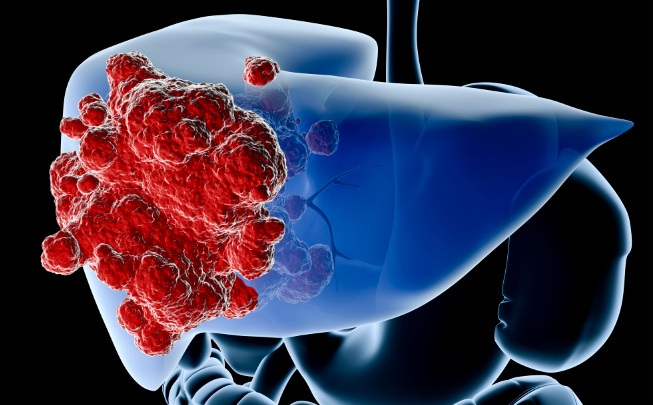
Множественные mts – крайне неблагоприятная ситуация
Метастазы в печень при раке молочной железы
Злокачественное новообразование в груди может отправить раковые клетки через кровь в отдаленные органы очень рано, даже на первых стадиях болезни. Метастазы в печень при раке молочной железы при жизни выявляются почти у 30% пациенток (патологоанатом находит печеночные метастатические очаги у 50%). Хорошо, если очаг одиночный, но такой вариант возникает лишь у каждой десятой: чаще в печеночной ткани обнаруживают несколько метастатический очагов. И нельзя исключить возможность формирования первичного рака печени на фоне опухоли в груди.
Проявления метастатического поражения печени
Крайне редко бессимптомно. Метастазы в печень при раке молочной железы проявляются следующими признаками:
- Тупые или давящие болевые ощущения в животе, чаще в области подреберья справа;
- Изменение цвета кожных покровов и слизистых оболочек (желтуха);
- Накопление жидкости в животе (асцит).
По сути, метастатическое поражение печени – это 4 стадия онкологии, для которой характерны симптомы общей интоксикации:
- Слабость, вялость, апатия;
- Отсутствие аппетита;
- Похудение.
Необходимо быть внимательным к собственному здоровью – каждой пациентке надо сразу обращаться к врачу при возникновении проблем, связанных с органами пищеварения. На первом этапе обследования надо сделать ультразвуковое сканирование органов брюшной полости, но более информативным будет томография (КТ или МРТ с контрастом).
Лечебная тактика
Всегда индивидуально, потому что нюансов много – у каждой пациентки свои особенности. Успешно лечить можно даже множественные mts в печень при раке молочной железы. Для терапии крайне важны следующие факторы:
- Возраст пациентки;
- Стадия онкологии;
- Количество очагов в печеночной ткани;
- Иммуногистохимические особенности первичной опухоли.
Оптимальный вариант – одиночный очаг небольших размеров, который можно удалить хирургически или с помощью радиочастотной аблации. При множественном поражении, когда хирургическое вмешательство выполнить невозможно, используется системная химиотерапия. Лекарственные препараты подбираются с учетом исходного гистотипа и особенностей первичной опухоли. Современные методики эндоваскулярной хирургии позволяют прицельно бить по метастатической опухоли: метод химиоэмболизации основной артерии печени – подведение лекарственного средства прямо к очагу вторичного рака – позволяет значительно увеличить выживаемость при метастатическом раке груди.
Метастазы в печень при раке молочной железы: каков прогноз?
Любое отдаленное метастазирование – это 4 стадия онкологии в груди, при которой все прогнозы рассчитываются в месяцах. При гормоночувствительной карциноме и хорошей реакции на лечение можно рассчитывать на 24-30 месяцев. При высокой степени злокачественности и низкодифференцированных формах рака с множественными очагами в печени – 6-12-18 месяцев. Но – это средние цифры: у каждой пациентки есть шансы изменить статистику в свою пользу.
Рак груди с метастазами в печень
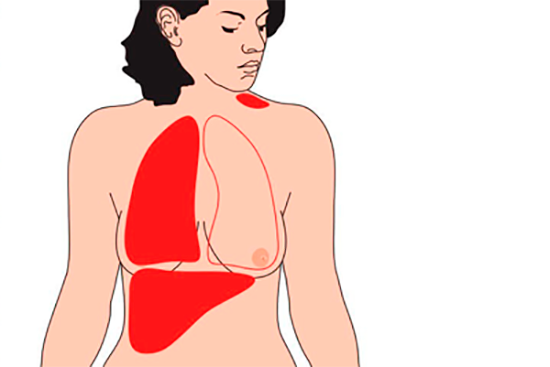
Рак груди возникает, когда атипичные клетки начинают делиться в дольках или протоках молочной железы. Рак груди с метастазами в печень сопровождается наличием раковых клеток не только в молочной железе, но и в печени. Метастазы – отдаленные очаги опухоли, которые формируются из оторвавшихся клеток первичной опухоли. Перемещаться по организму они могут вместе с током крови или лимфы.
Метастазы в печень дают многие опухоли. Печень – один из наиболее крупных органов в организме. В ней происходит очищение крови от токсинов, продуцируются белки и ферменты, откладываются запасы гликогена – источника энергии.
Печень пропускает через себя значительный объем крови – около 1,5 л в минуту. Внутри органа есть особые капилляры, в которых происходит смешение венозной и артериальной крови. Там же происходит замедление кровотока. Особенности системы кровотока создают предрасположенность к распространению атипичных клеток. Первое время раковые клетки неактивны. Позже, под воздействием неустановленных на данный момент факторов, происходит их стремительный рост.
На начальной стадии без специальной диагностики метастазы выявить невозможно. Однако по мере разрастания очага опухоли отмечается ухудшение кровотока, отток желчи. В результате нарушения работы печени наблюдается следующая симптоматика:
- общая слабость, быстрая утомляемость, пониженная работоспособность;
- потеря веса (может быть очень значительной, вплоть до истощения);
- снижение аппетита;
- рвота;
- изменение цвета кожного покрова на желтушный или землистый;
- боли тупого характера, локализованные в правом подреберье, которые сопровождаются ощущением тяжести, распирания;
- увеличение в размерах живота – является следствием асцита;
- расширение вен, расположенных на животе;
- возникновение сосудистых звездочек на кожном покрове;
- тахикардия;
- повышение температуры тела;
- зуд кожи;
- дисфункции кишечника;
- кровотечения пищевода;
- гинекомастия.
Многие из перечисленных признаков могут наблюдаться не только при поражении печени раковыми клетками. Не стоит впадать в панику, если присутствуют отдельные симптомы, например, усталость или вздутие живота. Однако при продолжительной рвоте, рвоте с кровью, черном стуле, желтухе следует сразу обратиться за медицинской помощью.
Пациентов разделяют на 2 категории:
- С единичной опухолью – у которых присутствует 1 или 2 метастаза. Их состояние характеризуется симптоматикой, свойственной первичному поражению печени раковыми клетками.
- С множественными образованиями – наблюдается 3 и более отдаленных опухолевых очагов. В таких случаях симптоматика более выражена.
Процессу метастазирования может способствовать снижение иммунитета. Когда организм не может уничтожить раковую клетку, она начинает ускоренно делиться, образуя опухоль.
Поэтому необходимо обратить внимание на укрепление организма, отказаться от вредных привычек, перейти на правильное питание.
Немаловажным моментом является экологический фактор. Если есть возможность проводить больше времени на свежем воздухе, это следует обязательно делать. По некоторым данным, раковые клетки разрушаются под воздействием кислорода. Известны случаи, когда люди избавлялись от страшной болезни, уехав в деревню, где отсутствуют источники опасных излучений.
Рак груди с метастазами в печень предполагает проведение функциональных печеночных тестов. Однако нельзя рассматривать данный метод диагностики как специфический.
Даже при значительном увеличении печени орган может сохранить свои функции. Компрессия протоков не всегда приводит к возникновению желтушности кожного покрова. На нарушение проходимости крупных протоков в печени будет указывать повышение уровня билирубина выше 34 мкммоль/л.
Анализ крови выявляет нейтрофильный лейкоцитоз, иногда – признаки анемии легкой формы.
Проведение биопсии рекомендуется совмещать с УЗИ, компьютерной томографией или перитонеоскопией. Ткани опухоли имеют белый цвет и рыхлую структуру. Одним из наиболее простых и широко используемых методов является УЗИ, однако он не всегда является информативным в достаточной степени.
Рентгенография позволяет обнаружить увеличение размеров органа. Может отмечаться приподнятость диафрагмы и неровные контуры.
Проведение сканирования дает возможность обнаружить метастазы, размер которых превышает 2 см. Необходимо определить количество имеющихся метастазов, их размеры, место расположения. Эти данные дают возможность проанализировать возможность проведения резекции печени.
Ангиографическое исследование – диагностика проводится после введения в сосуды контрастного вещества. Метод эффективен не только для обнаружения отдаленных очагов, но и для оценки их размеров, локализации, характера роста.
При выборе стратегии лечения обращают внимание на следующие факторы:
- число отдаленных очагов;
- степень поражения;
- выраженность нарушений.
При единичных метастазах показано проведение хирургического вмешательства.
Также могут быть использовать радиочастотная терапия и химиотерапия.
Рак груди с метастазами в печень подразумевает работу с пациентом в нескольких направлениях:
- местное воздействие с целью уничтожения метастазов;
- общая терапия, предназначенная для воздействия на клетки, расположенные за пределами метастазов;
- обезболивающие лекарства.
Общая терапия предполагает использование гормональной и химиотерапии. Эти методы должны использоваться в сочетании с радиотерапией, так как их воздействие проявляется не сразу, а воздействие на раковые клетки должно быть максимально быстрым.
Местное лечение подразумевает применение лучевой терапии, стероидов, проведение операции. Лучевая терапия помогает убрать боли, однако не может увеличить продолжительность жизни пациента.
Также назначается прием обезболивающих препаратов.
Нужно отметить, что раньше рак груди с метастазами в печень рассматривался как абсолютно бесперспективный диагноз. Однако при раннем выявлении можно добиться устранения метастазов и частичного сохранения функций печени, что позволяет продлить жизнь пациента на несколько лет.
К современным методам лечения относится РЧА – чрезкожная чрезпеченочная радиочастотная аблация печени. Процедура заключается во введении в раковую клетку специальной иглы, через которую подается радиоволна. Благодаря воздействию можно добиться некроза атипичных клеток без негативного воздействия на здоровые ткани. Метод позволяет увеличить выживаемость и снизить риск рецидива.
Метод хорош и потому, что при необходимости его можно применять повторно. Рак груди с метастазами в печень имеет свои сложности в лечении. Клетки, образующие метастаз, часто не реагируют на те лекарственные препараты, которые эффективно воздействовали на первичный очаг.
Химиотерапевтическое лечение позволяет притормозить рост вторичного очага, уменьшить число метастазов, убрать болезненную симптоматику. При раннем выявлении первичной опухоли проведение курса химии позволяет снизить вероятность метастазирования.
Также может быть использована таргетная терапия – метод, который предусматривает применение препаратов, которые воздействуют именно на раковую клетку. При метастазах в печени используют препарат сорафениб.
Эмболизация – процедура, которая заключается во ведении в сосуд, который питает опухоль, особого препарата, нарушающего приток крови. Одним из вариантов является химиоэмболизация, заключающаяся во введении особых микросфер, выделяющих химические вещества. Данный метод позволяет обеспечить одновременно воздействие в двух направлениях: перекрывается питание раковых клеток и обеспечивается разрушение клеток за счет действия химических веществ.
Развитие метастаза в печени может привести к компрессии воротной вены, нижней полой вены, желчных протоков. При нарушении оттока желчи происходит проникновение токсичного билирубина в кровь, следствием этого становится механическая желтуха. Билирубин оказывает негативное воздействие на состояние головного мозга. Значительное повышение его уровня приведет к летальному исходу. Для восстановления нормального оттока желчи используют хирургическое вмешательство.
Нельзя однозначно говорить о прогнозе, когда выявлен рак груди с метастазами в печень. Как правило, при вторичных очагах опухоли, обнаруженных в печени, продолжительность жизни составляет от полугода до 1,5 лет. Прогноз ухудшается, если метастазы развились и в других органах.
Интересным фактом является то, что у пациентов с циррозом печени метастазы в этом органе обнаруживаются крайне редко. Это связано с тем, что структура печени повреждена, она имеет рубцы, поэтому раковые клетки не могут закрепиться.
К профилактическим методам относится регулярное посещение врача для осмотра. Рак молочной железы сам по себе опасен, однако при начале лечения на ранней стадии его можно победить. При возникновении первых симптомов следует сразу обратиться к врачу. Регулярные профилактические осмотры позволят исключить вероятность развития метастазов в печень и другие органы.
Чтобы снизить риски, необходимо придерживаться здорового образа жизни и исключать воздействие негативных факторов на организм. Крепкий иммунитет помогает справиться с любым заболеванием, в том числе и таким опасным как рак.

- Как возникает рак молочной железы?
- Типы рака молочной железы
- Причины и факторы риска
- Симптомы рака молочной железы
- Самостоятельная диагностика рака груди
- Диагностика
- Стадии рака молочной железы
- Лечение рака молочной железы
- Прогноз при раке молочной железы
Как возникает рак молочной железы?
Рак груди развивается так же, как и любая другая злокачественная опухоль в организме. Одна или несколько клеток железистой ткани в результате произошедшей в них мутации начинают аномально быстро делиться. Из них образуется опухоль, способная прорастать в соседние ткани и создавать вторичные опухолевые очаги — метастазы.
Мутации, которые приводят к РМЖ, бывают наследственными и приобретенными .
Распространенными наследственными генетическими причинами рака молочной железы становятся мутации в генах BRCA1 и BRCA2. Носительницы мутации BRCA1 имеют риск заболеть раком молочной железы 55–65%, а носительницы BRCA2 — 45%. Такие генетические дефекты передаются по наследству от родителей детям, они становятся причиной рака молочной железы примерно в 15% случаев.
Намного чаще опухоль возникает из-за приобретенных мутаций: они возникают в клетках молочной железы и не передаются по наследству. Например, в 20% случаев увеличено количество копий гена, кодирующего HER2 — белок-рецептор, который находится на поверхности клеток и стимулирует их размножение.
Типы рака молочной железы
Злокачественные опухоли груди делятся на два типа: протоковые и железистые. Протоковый рак молочной железы встречается чаще. Он может быть внутриэпителиальным (in situ) и инвазивным. У внутриклеточного протокового рака молочной железы более благоприятный прогноз, он редко дает метастазы и излечивается в 98% случаев. Инвазивный же вариант опухоли склонен к бесконтрольному росту и генерализации процесса.
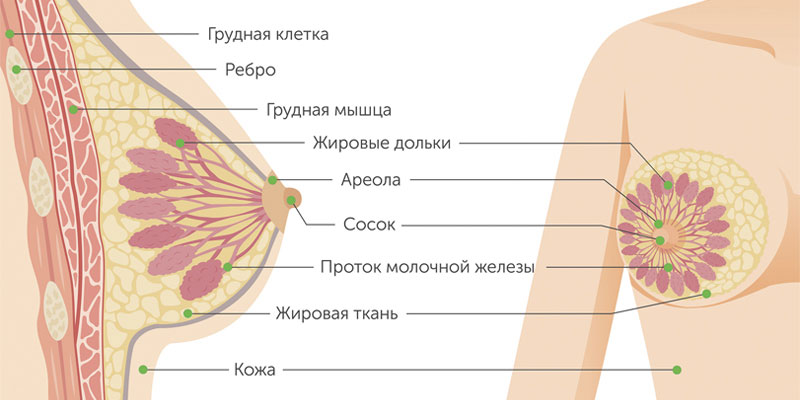
Железистый рак молочной железы может быть дольковым (инвазивная лобулярная карцинома) или произрастать из других клеток железистой ткани. Для долькового рака нередко характерен мультицентричный рост. Скорость увеличения в размерах и сроки метастазирования форм узлового рака груди зависят от степени дифференцировки опухоли.
Причины и факторы риска
К сожалению, полной информации о причинах возникновения рака молочной железы у ученых пока нет. Существует список факторов риска, влияющих на вероятность появления опухоли, однако у некоторых болезнь диагностируют при отсутствии этих факторов, другие же остаются здоровыми при наличии сразу многих из них. Тем не менее, ученые все же связывают развитие рака груди с определенными обстоятельствами, наиболее часто предваряющими его появление. К ним относятся:
- Возраст. Большинство случаев РМЖ приходятся на женщин в возрасте 55 лет и старше.
- Наследственность. Если РМЖ диагностирован у кого-то из близких родственников, риск повышается вдвое.
- Рак молочной железы в анамнезе.
- Повышенная плотность ткани молочной железы по результатам маммографии.
- Некоторые доброкачественные новообразования в молочной железе.
- Раннее начало менструаций — до 12 лет.
- Поздняя менопауза — после 55 лет.
- Отсутствие детей или поздние (после 35 лет) первые роды.
- Воздействие радиации, например, в ходе лучевой терапии, проводимой для лечения другого типа рака.
- Курение и злоупотребление алкоголем. Если женщина ежедневно потребляет 28–42 г этилового спирта, ее риски повышаются на 20%.
- Лишний вес и низкая физическая активность.
- Использование гормональных препаратов: оральные контрацептивы, заместительная гормональная терапия в постменопаузе.
- Травмы молочных желез.
- Сахарный диабет.
- Работа по графику с ночными сменами.
Симптомы рака молочной железы
На ранних стадиях рак молочной железы, как правило, никак клинически не проявляется. Чаще всего опухоль обнаруживается самими больными или выявляется случайно при проведении профилактических исследований.
Пациентки обычно жалуются на наличие пальпируемого образования, выделения из соска. Боль является редким симптомом рака грудной железы, однако болевой синдром может выйти на первый план на этапе генерализации процесса, в особенности при распространении метастазов в кости.
Довольно часто выявляются такие признаки рака груди, как появление асимметрии вследствие изменения размеров пораженной железы. Уменьшение, смещение кверху, деформация и сморщивание молочной железы может наблюдаться при скиррозной (фиброзной) форме опухоли. Напротив, увеличивается грудь на стороне поражения при быстром росте образования или из-за отека, который формируется по причине нарушенного оттока лимфы.
При распространении новообразования в подкожную клетчатку могут наблюдаться изменения кожи. При этом выявляются следующие симптомы рака молочной железы:
Иногда, при распространении опухоли на поверхность кожи могут наблюдаться такие признаки рака груди, как покраснение и изъязвление. Наличие этих симптомов говорит о запущенности процесса.
Изменения соска тоже могут определяться, но только на поздних стадиях. При этом имеют место такие симптомы рака грудной железы, как:
- Симптом Форга — на стороне поражения сосок находится выше, чем на здоровой стороне.
- Симптом Краузе — сосок утолщен, складки ареолы заметно выражены.
Такой признак рака молочной железы, как патологические выделения, является довольно редким, но в ряде случаев может быть единственным симптомом, который выявляется при осмотре. Часто выделения носят кровянистый характер, реже встречаются серозные и гнойные.
Также были выделены особые формы рака груди, которые проявляются типичной симптоматикой. К ним относятся:
- Отечно-инфильтративная форма, для которой характерно увеличение и отечность железы, мраморный цвет кожи, выраженная гиперемия.
- Маститоподобная. Данный вид рака груди проявляется уплотнением пораженной груди, повышением температуры тела.
- Рожистоподобная форма, при которой на коже выявляются очаги (иногда появляются изъязвления), которые внешне напоминают рожистое воспаление.
- Панцирная форма характеризуется наличием множественных узлов, за счет которых происходит сморщивание и деформация железы.
- Рак Педжета — поражает сосок и ареолу. При данной разновидности наблюдают утолщение соска, изменение кожи в виде покраснения и уплотнения, образование корок и чешуек.
Иногда люди, интересуясь по каким признакам можно распознать наличие опухоли молочной железы, по ошибке ищут симптомы рака грудины. Данное название является неверным, так как грудина является центральной плоской костью грудной клетки и даже при метастазировании злокачественного образования груди практически никогда не поражается.
Самостоятельная диагностика рака груди
Самостоятельно проверять грудь на наличие узелков или каких-либо других изменений стоит раз в месяц после менструации. Домашнюю диагностику удобнее всего проводить, принимая ванну или находясь под душем. О любых изменениях, которые удалось обнаружить, стоит как можно быстрее рассказать врачу.
Порядок проведения самообследования молочных желез:
- Разденьтесь выше пояса и встаньте перед зеркалом.
- Поднимите руки вверх и заведите их за голову. Внимательно осмотрите грудь. Повернитесь правым, левым боком.
- Ощупайте молочные железы в положении стоя сложенными указательным, средним и безымянным пальцем. Начинайте с верхней наружной части груди и двигайтесь по часовой стрелке.
- Сожмите сосок двумя пальцами. Проверьте, выделяется ли из него что-нибудь.
- Снова ощупайте молочные железы — теперь в положении лежа.
70% случаев рака молочной железы выявляются пациентами самостоятельно в результате самообследования груди.
Диагностика
Диагностика рака молочной железы начинается с беседы. На этом этапе для врача важно оценить жалобы женщины и выяснить, встречались ли случаи рака молочной железы в её семье, если да — насколько часто. Это помогает заподозрить наследственную форму рака, связанную с мутациями в генах BRCA1, BRCA2, NBS1, CHECK, TP53.
Далее врач осматривает, ощупывает молочные железы, проверяет, нет ли в них узлов и уплотнений, не увеличены ли лимфатические узлы в подмышечной, надключичной и подключичной областях.
После осмотра врач может направить женщину на маммографию — рентгенографию молочной железы. Показаниями к этому исследованию являются: уплотнения в молочной железе, изменения со стороны кожи, выделение крови из соска, а также любые другие симптомы, которые могут указывать на злокачественную опухоль. Также для диагностики рака молочной железы назначают ультразвуковое исследование. Маммография и УЗИ являются взаимодополняющими методами, каждый из них имеет свои преимущества:
Маммография
УЗИ молочных желез
Позволяет обнаружить патологические изменения за 1,5–2 года до появления симптомов.
При кровянистых выделениях из соска можно провести дуктографию — рентгенографию с контрастированием молочных протоков. Это помогает получить дополнительную полезную информацию.
Высокая чувствительность — точная диагностика до 90% случаев рака.
Возможность обнаружить микрокальцинаты до 0,5 мм.
Безопасность — нет воздействия на организм рентгеновскими лучами.
Хорошо подходит при высокой плотности ткани молочной железы, у молодых женщин (до 35–45 лет).
Позволяет отличать кисты (полости с жидкостью) от плотных опухолей.
Позволяет оценить состояние регионарных лимфатических узлов.
Хорошо подходит для контроля положения иглы во время биопсии.
Магнитно-резонансная томография — высокоинформативный метод диагностики злокачественных опухолей молочной железы. Ее применяют при лобулярном раке, когда неинформативны маммография и УЗИ, а также для оценки размеров и расположения опухоли, что помогает определиться с тактикой хирургического лечения. МРТ может применяться для скрининга у женщин-носительниц аномальных генов, связанных с повышенным риском рака молочной железы, при отягощенном семейном анамнезе.
О роли биопсии в диагностике рака молочной железы рассказывает врач Европейской клиники Портной С.М.:

В лаборатории проводят цитологическое и гистологическое исследование, то есть оценивают строение отдельных клеток и ткани. В настоящее время доступны молекулярно-генетические исследования: они помогают выявить мутации, за счет которых произошло злокачественное перерождение, и подобрать оптимальную противоопухолевую терапию.
Биопсия позволяет выяснить, является ли опухоль злокачественной, а также определить ее тип и стадию. Кроме того, исследование биопсийного материала дает ответ на вопрос, является ли опухоль гормонозависимой , что также влияет на схему лечения.
После того как рак диагностирован, важно определить его стадию и понять, насколько сильно он распространился в организме. Для этого применяют следующие исследования:

Стадии рака молочной железы
Стадирование при раке молочной железы опирается на общепринятую систему TNM. Буква T в этой аббревиатуре обозначает размер первичной опухоли:
Буквой N обозначают наличие метастазов в регионарных лимфатических узлах. N0 — очаги в лимфатических узлах отсутствуют. N1, N2 и N3 — поражение разного количества лимфатических узлов.
Буква M обозначает наличие отдаленных метастазов. Рядом с ней может быть указана одна из двух цифр: M0 — нет отдаленных метастазов, M1 — отдаленные метастазы имеются.
В зависимости от значений T, N и M, выделяют пять основных стадий рака молочной железы (внутри некоторых из них есть подстадии):
- Стадия 0: рак на месте.
- Стадия I: опухоль в молочной железе диаметром до 2 см.
- Стадия II: опухоль в молочной железе диаметром до 5 см и более, могут быть метастазы в подмышечных лимфоузлах на стороне поражения.
- Стадия III: опухоль в молочной железе до 5 см и более, может прорастать в грудную стенку или в кожу, имеются очаги в регионарных лимфатических узлах.
- Стадия IV: опухоль может быть любых размеров, не имеет значения, поражены ли регионарные лимфоузлы. Если обнаруживают отдаленные метастазы, всегда диагностируют рак четвертой стадии.
Лечение рака молочной железы
Стратегия лечения рака молочной железы должна подбираться индивидуально для каждой пациентки с учетом таких факторов, как тип опухоли, стадия, чувствительность новообразования к гормональной терапии. Берется во внимание и общее состояние больной. Если опухоль обнаружена на ранних стадиях и выбрана правильная тактика ведения пациентки, то шанс полностью вылечить рак груди является весьма высоким.
Выберите врача-онколога и запишитесь на приём:

Пластический хирург, онколог-маммолог, доктор медицинских наук
Метастазы печени встречаются у 6-25% пациентов с метастатическим раком молочной железы (Tampellini et al, 1997). Большинство авторов цитируют медианную выживаемость 1-14 месяцев (Jaffe et al, 1968; Zinser et al., 1987; Patanaphan et al., 1988; O’Reilly et al., 1990; Hoe et al., 1991), которая неблагоприятно сравнивается с метастазами при другие сайты; изолированные метастазы в мягких тканях имеют среднюю выживаемость 50 месяцев (Tampellini et al, 1997), кость 33-48 месяцев (Sherry et al, 1986) и плевральная болезнь 6-15 месяцев (Johnson et al, 1998). Только церебральные метастазы дают худший прогноз с медианной выживаемостью всего 4 месяца (Johnson et al, 1998). Выживание может быть пролонгировано химиотерапией или эндокринной терапией, и небольшая часть пациентов может выжить в течение 5 лет (3%) или даже 10 лет (1%) при этих методах лечения (Sledge and Miller, 1999). Текущие рекомендации заключаются в том, что пациенты с бессимптомными, эстроген-рецепторными (ER) положительными метастазами в печени могут лечиться эндокринной терапией (Buzdar, 2001). Те, у кого с симптоматическими метастазами или ER-негативными опухолями, лечится комбинированная химиотерапия, такая как FEC (5-фторурацил, эпирубицин и циклофосфамид) или CMF (циклофосфамид, метотрексат, 5-фторурацил) (Fossati et al, 1998; Sledge and Miller, 1999). Такан-химиотерапия может использоваться при антрациклинорезистентном заболевании (Hortobagyi et al, 2000). В сочетании с таксановой химиотерапией часто используются новые методы лечения моноклональными антителами, такими как трастузумаб (для раковых опухолей молочной железы с-erb-B2 / Her-2) (Fournier et al, 2000). Химиотерапия даст ответ у 50-80% пациентов, и выживаемость может быть увеличена (Hortobagyi, 2000). Однако побочные эффекты этих агентов могут быть серьезными и иногда приводят к смертельным осложнениям.
Было проведено несколько исследований хирургического лечения метастазов в печени от рака молочной железы, либо для попытки лечения или дебуляции. Несколько исследований показывают, что небольшая подгруппа пациентов может получить преимущество от выживаемости от операции, и есть сообщения о редких выживших в долгосрочной перспективе (Pocard et al., 2000; Selzner et al., 2000).
Целью этого исследования было выявить факторы, которые позволяют предсказать, что эти пациенты вряд ли выживут в течение длительных периодов времени, для которых химиотерапия может не принести пользы и ухудшить их оставшееся качество жизни.
Метастазы печени могут проявляться бессимптомно во время метастатического скрининга или могут присутствовать с верхней абдоминальной полнотой, массой, асцитом, желтухой или потерей веса (O’Reilly et al, 1990). Ультразвук или КТ обычно подтверждают диагноз. Тесты функции печени нарушаются у 92% пациентов при представлении гамма-глутамилтрансферазы (ГГТ) и щелочной фосфатазы, являющейся наиболее часто повышенными ферментами. Острая желтуха встречается реже (13%) (O’Reilly et al, 1990).
К факторам, отрицательно влияющим на прогноз, относятся: желтуха (Hoe et al, 1991), нарушения функции печени (Zinser et al., 1987; O’Reilly et al., 1990), асцит, осязаемая гепатомегалия (O’Reilly et al, 1990), бедные (Zinser et al., 1987; Hoe et al., 1991). Интервал между первичным представлением и метастатическим заболеванием является важным предиктором выживания в костных метастазах (Sherry et al, 1986), но может не иметь значения в метастазах в печени (O’Reilly et al, 1990). Опухольный маркер CA15-3 часто выше у пациентов, которые плохо себя чувствуют, но не сообщается, что они являются независимым предиктором выживания (Tampellini et al, 1997). Карциноэмбриональный антиген (СЕА) ранее не изучался в этом отношении, хотя он признан полезным для мониторинга прогрессирования заболевания (Cheung et al, 2000).
Влияние картины болезни, как вне печени, так и внутри печени, мало привлекало внимание. Два исследования показывают, что внепеченочная болезнь может нарушать выживаемость (Zinser et al., 1987; Hoe et al., 1991), но нет данных о прогностическом значении распределения болезни в печени.
В этом исследовании были рассмотрены случаи, когда все пациенты, представленные за последние 5 лет, были в одной грудной клетке с метастатическим раком молочной железы с участием печени при метастатической диагностике. Выживаемость с момента метастатического диагноза сравнивалась с первичной информацией о болезни, характеристиками пациента и характером метастатического заболевания в попытке установить факторы, предсказывающие результат. Следует надеяться, что эти прогностические факторы могут принести пользу при адаптации лечения, чтобы избежать токсичности для пациентов с короткой ожидаемой продолжительностью жизни, для которых паллиативная поддержка была бы наиболее подходящей.
Были изучены все пациенты, представившие Группе грудной клетки больницы Ноттингем с метастазами в печени в период с января 1997 года по январь 2002 года. При диагностике с метастатическим заболеванием проводилась полная постановка, включая анализ крови (тесты функции печени (LFTs), полный анализ крови (FBC), скорость седиментации эритроцитов (ESR), CEA и CA15-3), ультразвуковое исследование на КТ или КТ, рентгенография грудной клетки и сканирование костей. Биопсия печени проводилась только в случаях диагностических сомнений.
Уровни опухолевых маркеров (CA15-3 и CEA, либо увеличивающиеся, либо уменьшающиеся во время лечения) также оценивались. Изменения в опухолевых маркерах никогда не считались достаточными критериями для изменения терапии, что также требовало либо клинического, либо радиологического подтверждения. После подтверждения прогрессирования заболевания лечение было изменено и протокол оценки повторялся. Причина смерти была записана из заметок.
Время от метастатического диагноза до смерти или время анализа затем сравнивали с характеристиками пациента и болезни, чтобы определить прогностическое значение. Сорт определяли с использованием системы Ноттингема и классифицировали как класс 1, 2 или 3 (Elston and Ellis, 1991). Анализ рецепторов эстрогенов был получен путем подсчета гистохимического (H) показателя Маккарти (McCarty et al., 1983), причем оценка больше нуля считалась положительной ER в метастатической обстановке. Также регистрировали стадию лимфатического узла и размер первичной опухоли в миллиметрах. Прогностический индекс Ноттингема (NPI, уровень + узловой статус + 0,2 × первичный размер в см) (Haybittle et al, 1982) был рассчитан для каждого пациента при первичной презентации.
Вторичный прогностический индекс Ноттингема (Robertson et al, 1992) был рассчитан для оценки того, является ли это полезным предсказателем результата при рассмотрении одного доминантного метастатического сайта. Это было рассчитано следующим образом:
Эта система оценки имеет ценность при определении прогноза у пациентов с метастатическим заболеванием на разных участках. Пациенты с оценкой менее 8 характеризуются хорошим прогнозом, 8-16,5 — умеренным прогнозом и> 16,5 — плохим прогнозом. Оценка была рассчитана для каждого из пациентов в этой серии и сравнивалась с выживаемостью в течение нескольких месяцев.
Анализ проводили с использованием кривых выживаемости Каплана-Мейера с анализом χ2 или с анализом Kruskal-Wallis ANOVA plus Mann-Whitney U для сравнения медианов между группами. Многомерный анализ проводили с использованием переменных предварительной обработки, чтобы определить, какие факторы являются независимыми прогностическими факторами. Статистическая значимость принималась, если P 35 U мл-1) в 75,9% для CA15-3 и 44,8% случаев для CEA (> 10 нг мл-1).
Уровни СА15-3 изучались как выше, так и ниже нормального диапазона, а также выше 1000 ед. Мл-1. Хотя медианная выживаемость показала тенденцию к худшему прогнозу с более высокими уровнями, статистически значимой разницы не было обнаружено, поэтому CA15-3 не может использоваться для оценки прогноза (таблица 2).
Уровни карциноэмбрионального антигена (СЕА) изучались как выше, так и ниже нормального диапазона, а также выше 1000 нг мл-1. При отсечке 10 нг мл-1, нормальный верхний предел, не было найдено полезного предсказательного значения. Однако, если был использован уровень 1000 нг мл-1, средняя выживаемость не только резко снижалась, но и самая продолжительная выживаемость составляла всего 5,1 месяца, что свидетельствует о том, что уровень СЕА в сыворотке более 1000 нг мл-1 может иметь полезный прогностический последствия. Однако этот фактор имеет ограниченную ценность, поскольку только у восьми пациентов наблюдалось повышение ЭЭГ этой величины (таблица 2).
В большинстве случаев метастазы в печени были бессимптомными во время метастатического диагноза и были обнаружены метастатическим экраном, когда пациент с симптоматическими метастазами находился в другом месте (n = 88, 78,6%). Остальные были симптоматическими, представляя боль в эпигастральной области или полноту (n = 24, 21,4%). Симптоматическое заболевание печени имеет худший прогноз, чем бессимптомные метастазы в печени со средними выживаемостями 4,9 (0,16-26) и 9,2 (0,5-51) месяцев соответственно (P 70 лет: медианная выживаемость 3 месяца (0,16-32), 50 мкмоль-1), что указывает на начало печеночной недостаточности, средняя выживаемость составляла всего 0,6 месяца (диапазон 0,16 -1,57). Таким образом, при наличии этих находок существует худший прогноз, предсказуемый на уровне отдельных пациентов. Наличие асцита также имеет плохой прогноз.
Очень мало прогностической информации можно получить из характеристик и стадии первичной опухоли у пациентов с метастазами в печени. Единственными прогностическими факторами были уровень и статус ER первичной опухоли, хотя снова диапазон выживаемости таков, что никакой полезной информации не может быть получена на индивидуальной основе пациента, чтобы облегчить терапевтический выбор.
Возникновение метастазов на участках за пределами печени не влияло на результат для пациента, что указывает на то, что метастазы в печени являются наиболее значительными в причинении смерти пациента. Возникновение церебральных метастазов может дать худший прогноз, но очень немногие пациенты имели это во время метастатического диагноза, и поэтому статистический эффект не мог быть продемонстрирован.
Модель метастатического заболевания в печени имеет прогностические последствия; пациенты с одним метастазом имеют наилучшую долгосрочную выживаемость, а множественные конфлюэнтные и диффузные метастазы имеют наихудший результат. Из одной группы метастазов в печени только шесть не имели признаков метастатического заболевания в других местах во время презентации, и у одного из них был неоперабельный первичный рак, исключающий лечебную операцию на печени. Пять потенциальных хирургических кандидатов имели среднюю выживаемость 14 месяцев (диапазон 6-26) с тремя живыми. В настоящее время не является обычной практикой выполнять резекцию печени при метастазах в грудной клетке из-за частых сосуществований метастатического заболевания в другом месте, в целом плохого прогноза и величины операции. Тем не менее, имеются сообщения о долгосрочном выживании у тщательно отобранных пациентов после резекции печени при метастазах от рака молочной железы (Pocard et al., 2000; Selzner et al., 2000).
Опухолевые маркеры используются для мониторинга метастатического заболевания во время лечения (Tampellini et al, 1997; Cheung et al, 2000), но имеют ограничения в качестве прогностического инструмента при диагностике метастатического рака молочной железы. CA15-3 был повышен выше нормы у 75,9% пациентов при метастатической диагностике, что согласуется с другими исследованиями (Tampellini et al, 1997). Однако уровень возвышения не мог быть использован для прогнозирования выживаемости, даже если аналитическое обрезание было очень высоким (> 1000 U мл-1). Карциноэмбриональный антиген был более полезным. Этот маркер был повышен выше нормы у 44,8% пациентов, что согласуется с другими данными о метастатическом раке молочной железы (Mughal et al, 1983). Мягкое возвышение не имело прогностического значения. Однако, когда они очень высоки (т.е. выше 1000 нг мл-1), пациенты плохо справлялись с медианной выживаемостью в течение 1 месяца. Диапазон также был узким, причем наибольшая выживаемость составляла всего 5,1 месяца, а это означает, что это может использоваться на индивидуальной основе для прогнозирования плохих результатов.
Таким образом, это исследование показало, что несколько факторов могут быть полезны при прогнозировании продолжительности выживания для пациентов с метастазами в печени от рака молочной железы. Из них факторами, несущими самые зловещие последствия, являются те, которые указывают на наличие печеночной недостаточности, то есть низкий сывороточный альбумин, повышенный билирубин и присутствие асцита. Многие другие функции оказывают существенное влияние на выживаемость (распространение болезни в печени, возраст пациента и степень и статус ОО опухоли), но из-за большого количества пережитков в этих группах эти значения мало полезны для отдельного пациента основа. Что касается типа лечения и ответа, пациенты, которым дается симптоматическое лечение, выживают очень плохо, как и ожидалось, хотя это, вероятно, будет представлять как лечение, так и характер пациента и их болезнь. Пациенты, которые делали лучше всего, были теми, кто реагировал на химиотерапию и эндокринную терапию, у которых иногда достигалось выживание несколько лет, и это должно быть источником оптимизма как для пациентов, так и для врачей, поскольку терапия продолжает улучшаться.
Читайте также:

