Рак легких мутация ros1 сколько живут
Тестирование на наличие транслокации гена ROS1
Тест на наличие транслокации гена ROS1 показан больным распространенным немелкоклеточным раком легкого с отрицательным статусом мутаций EGFR и ALK для отбора пациентов на терапию кризотинибом. Тестирование ROS1 проводится пациентам ТОЛЬКО с ОТРИЦАТЕЛЬНЫМ РЕЗУЛЬТАТОМ ALK .
Онкоген ROS1 кодирует рецепторную тирозинкиназу, родственную киназе анапластической лимфомы (ALK) [16], а также ряду членов семейства инсулиновых рецепторов. ALK и ROS1 отвечают за синтез взаимосвязанных тирозинкиназ, АТФ-связывающие домены которых на 77% идентичны по аминокислотному составу (рис. 1).
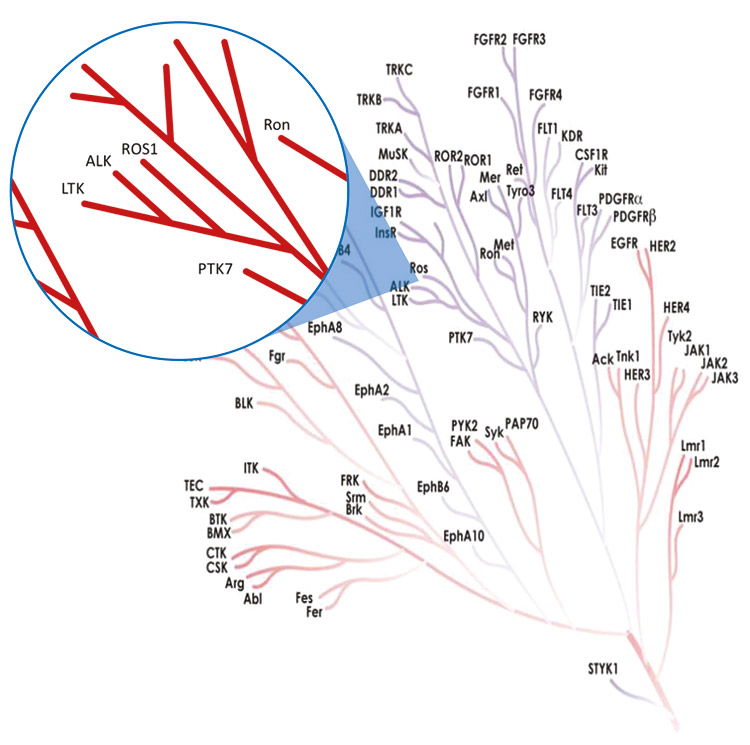
Рисунок 1. Родственные киназы ALK и ROS1.
Реаранжировка приводит к слиянию части ROS1, которая включает полный домен тирозинкиназы, с 1 из 12 различных белков-партнеров.
Полученная в результате слияния тирозинкиназа ROS1 активируются конститутивно и обуславливает клеточную трансформацию.
Зачем определять статус транслокации ROS1?
Обнаружение транслокации ROS1 при немелкоклеточном раке легкого принципиально для проведения терапии таргетным препаратом кризотиниб, являющимся единственным зарегистрированным ингибитором тирозинкиназы ROS1.
Кому нужно проводить тестирование?
Реаранжировки ROS1 развиваются примерно у 1-2% пациентов с НМРЛ. Как и реаранжировки ALK, реаранжировки ROS1 чаще выявляются у пациентов, которые никогда не курили или у которых в анамнезе имеется курение в небольших количествах, и отмечаются гистологические признаки аденокарциномы.
Методы диагностики
Методика диагностики реаранжировки ROS1 полностью соответствует алгоритму выявления реаранжировки ALK и на сегодняшний день производится с использованием метода FISH, ИГХ и OТ-ПЦР. Важно помнить, что на генетическом уровне реаранжировки ALK и ROS1 редко развиваются в одной и той же опухоли, и каждая из них определяет уникальную подгруппу НМРЛ [21].
В рамках Программы алгоритм диагностики по выявлению транслокации ALK и ROS1 у пациентов с немелкоклеточным раком легкого представлен на рис. 2.
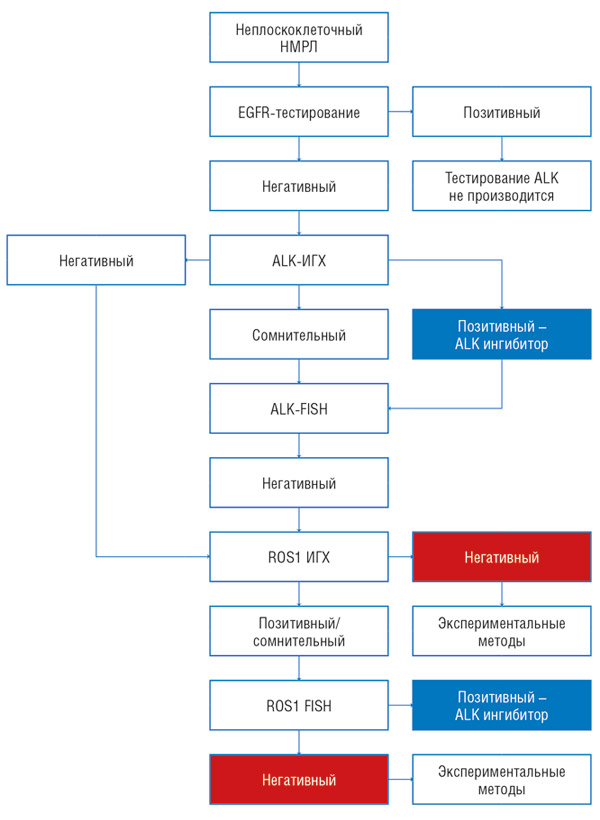
Рисунок 2. Алгоритм тестирования.
- Soda M, Choi YL, Enomoto M, et al. Identification of the transforming EML4-ALK fusion gene in non-small-cell lung cancer. Nature. 2007; 448(7153): 561-566.
- Iwahara, T, Fujimoto J, Wen D, et al. Molecular characterization of ALK, a receptor tyrosine kinase expressed specifically in the nervous system. Oncogene 1997, 14: 439-449.
- Stoica, GE, Kuo A, Aigner A, et al. Identification of anaplastic lymphoma kinase as a receptor for the growth factor pleiotrophin. J. Biol. Chem. 2001; 276: 16772-16779.
- Bai RY, Ouyang T, Miething C, et al. Nucleophosmin-anaplastic lymphoma kinase associated with anaplastic large-cell lymphoma activates the phosphatidylinositol 3-kinase/Akt antiapoptotic signaling pathway. Blood 2000; 96: 4319-4327.
- Marzec M, Kasprzycka M, Liu X, et al. Oncogenic tyrosine kinase NPM/ALK induces activation of the rapamycin-sensitive mTOR signaling pathway. Oncogene 2007; 26: 5606-5614.
- Medves S, Demoulin JB. Tyrosine kinase gene fusions in cancer: translating mechanisms into targeted therapies. J. Cell. Mol. Med. 2012; 16(2): 237-248.
- Crystal AS, Show AT. Variants on a Theme: A Biomarker of Crizotinib Response in ALKPositive Non–Small Cell Lung Cancer. Clin Cancer Res 2012; 18(17): 4479-81.
- Horn L, Pao W. EML4-ALK: Honing In on a New Target in Non–Small-Cell Lung Cancer. J Clin Oncol 2009, 27(26): 4232-4235.
- Camidge DR, et al. Activity and safety of crizotinib in patients with ALK-positive nonsmall-cell lung cancer: updated results from a phase 1 study. Lancet Oncol 2012; 13: 1011-1019.
- Kim, et al. Updated Results of a Global Phase II Study with Crizotinib in Advanced ALK-positive Non-small Cell Lung Cancer. ESMO 2012; Abstract 1230PD.
- Food and Drug Administration. Summary review (application number: 202570Orig1s000). Food and Drug Administration 2011, Silver Spring.
- Camidge DR, Hirsch FR, Varella-Garcia M, Franklin WA. Finding ALK-positive lung cancer: what are we really looking for? J Thorac Oncol. 2011; 6(3); P.411-3.
- Meno-Kenudson M, Chirieac LR, Law K, et al. A novel, highly sensitive antibody allows for the routine detection of ALK-rearranged lung adenocarcinomas by standard immunohistochemistry. Clin Cancer Res. 2010; Vol.1; No.16(5; P.1561-71.
- Sanders HR, Li HR, Bruey JM, et al. Exon scanning by reverse transcriptase-polymerase chain reaction for detection of known and novel EML4-ALK fusion variants in non-small cell lung cancer. Cancer Genet. 2011; Vol.204; No.1; P.45-52.
- Lindeman NI, Cagle PT, Beasley MB, Chitale DA, Dacic S, Giaccone G, Jenkins RB, Kwiatkowski DJ, Saldivar JS, Squire J, Thunnissen E, Ladanyi M. Molecular Testing Guideline for Selection of Lung CancerPatients for EGFR and ALK Tyrosine Kinase Inhibitors. Guideline from the College of American Pathologists, International Association for the Study of Lung Cancer, and Association for Molecular Pathology. J Mol Diagn. 2013 Jul; 15(4): 415-53. doi: 10.1016/j.jmoldx.2013.03.001. Epub 2013 Apr 4. P.21-24.
- Acquaviva J, Wong R, Charest A. The multifaceted roles of the receptor tyrosine kinase ROS in development and cancer. Biochim Biophys Acta 2009; 1795: 37-52.
- Charest A, Lane K, McMahon K, et al. Fusion of FIG to the receptor tyrosine kinase ROS in a glioblastoma with an interstitial del(6)(q21q21). Genes Chromosomes Cancer 2003; 37: 58-71.
- Rikova K, Guo A, Zeng Q, et al. Global survey of phosphotyrosine signaling identifies oncogenic kinases in lung cancer. Cell 2007; 131: 1190-203.
- Gu TL, Deng X, Huang F, et al. Survey of t yrosine kinase signaling revea ls ROS kinase fusions in human cholangiocarcinoma. PLoS One 2011; 6(1): e15640.
- Davies KD, Doebele RC. Molecular pathways: ROS1 fusion proteins in cancer. Clin Cancer Res 2013; 19: 4040-5.
- Gainor JF, Shaw AT. Novel targets in non-small cell lung cancer: ROS1 and RET fusions. Oncologist 2013; 18: 865-75.
в базу данных
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.
- ROS1 Gene перегруппировка
- Диагностическое тестирование
- ROS1 Положительный рак легких
- Слово от DipHealth
Таргетная терапия ALK-позитивного немелкоклеточного рака легкого. (Июль 2020).
Перегруппировка ROS1 является аномалией в хромосоме, которая может происходить в раковых клетках, таких как клетки рака легких. Хромосомы - и гены, которые составляют наши хромосомы - несут код для таких вещей, как цвет наших глаз. Они также кодируют (действуют как план) для белков, которые регулируют рост и деление клеток. Когда один из этих генов или хромосом поврежден, видоизменен или реорганизован, они кодируют аномальный белок, который может затем выполнять аномальные функции, такие как стимулирование роста рака.
ROS1 Gene перегруппировка
Не все генные мутации и перестройки одинаковы. Некоторый код для белков, которые действуют как драйверы. Ген ROS1 кодирует белок, который действует как драйвер, который может запустить шоу, когда дело доходит до роста и деления клеток. Когда ген переупорядочен, аномальный белок может, таким образом, управлять аномальным ростом и делением клетки.
Этот белок является одним из ряда белков (ферментов), известных как тирозинкиназы. Эти белки посылают сигналы в центр роста клетки, давая ей знать, когда делиться и размножаться.
До настоящего времени перестройки ROS1 были обнаружены только у людей с немелкоклеточным раком легких и, в данном случае, только у людей с аденокарциномой легкого. Он не был обнаружен у людей с мутациями в перегруппировках EGFR, KRAS или ALK.
По сравнению с другими формами рака легких, исследование 2015 года показало, что:
- Средний возраст людей с перестройками ROS1 был 50,5. (Средний возраст для рака легких, как правило, составляет 72 года.)
- Это было немного чаще встречается у женщин в том, что 64,5 процента были женщины. (Рак легких у мужчин встречается несколько чаще, чем у женщин.)
- Больший процент - 67,7% - никогда не курили. (Рак легких, безусловно, встречается у никогда не курящих, по крайней мере, 20 процентов рака легких у женщин никогда не курят.)
- Из людей с аденокарциномой легкого 3,1% имели перестройку ROS1.
Хотите знать, будет ли ингибитор тирозинкиназы, который работает для другой генной перестройки - рак легкого с ALK-перестройкой или ALK-положительный рак легкого - работать, чтобы блокировать эффекты аномального белка, продуцируемого перестроенным геном ROS1? Ну, исследователи попробовали препарат, который успешно использовался для людей с ALK-положительным раком легких. Удивительно, но он работал на ROS1-положительный рак легких еще сильнее.
Диагностическое тестирование
Есть несколько способов, которыми люди с раком легких могут быть проверены, чтобы видеть, есть ли у них перестройка ROS1. Тест проводится на образце ткани от биопсии легкого или хирургии рака легкого. Есть надежда, что в будущем тестирование будет доступно с помощью жидкостной биопсии - теста, проведенного на крови, который можно получить простым взятием крови.
Методы испытаний включают иммуногистохимию и флуоресцентную гибридизацию in situ (FISH). Исследования продолжаются, чтобы определить лучшие методы тестирования.
Считается, что любой с немелкоклеточным раком легких, особенно аденокарциномой легкого, должен пройти генетическое тестирование (молекулярное профилирование) на опухолях легких. Тестирование особенно важно для молодых людей с раком легких, которые имеют высокую частоту излечимых мутаций и могут хорошо реагировать на одно из лекарств в категории ингибиторов тирозинкиназы. Кроме того, очень важно, чтобы те, кто никогда не курил, проходили тестирование, так как среди тех, кто никогда не курит, наблюдается высокий уровень мутаций и перестроек.
ROS1 Положительный рак легких
Перестройки ROS1 были впервые обнаружены при мультиформной глиобластоме, типе рака головного мозга, а также были обнаружены при некоторых других раковых заболеваниях, включая рак яичников, колоректальный рак, рак желудка и холангиокарциному.
Важно подчеркнуть, что тип перестройки генов, о котором мы говорим, является приобретенным генетическим изменением. В отличие от некоторых генетических мутаций и перестроек, с которыми рождаются люди, некоторые из которых могут предрасполагать людей к раку, перегруппировка гена ROS1 отсутствует с рождения. Вам не нужно беспокоиться, что ваши дети унаследуют перестановку.
лечение
- Хирургия- Для людей со стадии от I до стадии IIIA, хирургия рака легких может быть вариантом. Не все опухоли этих стадий являются работоспособными, но когда они есть, операция может дать шанс на излечение.
- химиотерапия- Помимо целевой терапии, некоторые химиотерапевтические агенты также эффективны при ROS1-положительных опухолях. ROS1-положительный рак легких, по-видимому, особенно чувствителен к химиотерапевтическому препарату Алимта (пеметрексед), причем более 50 процентов людей ответили на препарат в одном исследовании.
- Таргетная терапия-Xalkori (кризотиниб) - ингибитор тирозинкиназы, первоначально одобренный для ALK-положительного рака легких. Рекомендуется первая линия, то есть перед любым другим лечением (хотя одновременно могут использоваться и другие виды лечения), а также для всех, кто ранее проходил лечение по этому заболеванию. Этот препарат был одобрен для лечения ALK-положительного рака легких в 2013 году и вызвал волнение позже, когда клинические испытания I фазы с людьми с раком легких ROS1 отреагировали на препарат еще лучше. В этих клинических испытаниях число людей, ответивших на препарат, составляло от 70 до 80 процентов. В апреле 2015 года препарат получил революционное назначение для лечения рака легких с положительной реакцией на ROS1. Лоратиниб одобрен для тех, у кого рак прогрессировал на Ксалкори. Ignyta (entretinib), как правило, не работает в тех, для кого Xalkori потерпел неудачу, но может быть полезен для тех с метастазами в мозг.
- Клинические испытания-Другие лекарственные препараты, особенно целевые методы лечения, изучаются в клинических испытаниях для людей с ROS1-положительным раком легкого. Некоторые из них включают Zykadia (церитиниб), другой препарат, похожий на кризотиниб, который одобрен для ALK-положительного рака легких. Другие лекарства, которые изучаются при раке легких, положительные для перегруппировки ROS1, включают Cometriq (кабозантиниб) и другие. Чтобы узнать больше о клинических исследованиях рака легких, рассмотрите возможность обращения в бесплатную службу соответствия клинических испытаний, доступную для всех пациентов с раком легких.
Метастазы в мозг
ROS1-положительный рак легких слишком часто распространяется в мозг. По оценкам, от 25 до 40 процентов людей с диагнозом немелкоклеточный рак легких будут иметь метастазы в мозг в течение первых двух лет лечения.
К сожалению, Xalkori (кризотиниб) не очень хорошо подходит для метастазов в мозг у людей с ROS1-положительным раком легких. Это лекарство, как многие, не очень хорошо проникает через гематоэнцефалический барьер.Гематоэнцефалический барьер - это система контроля специализированных мембран, которые предотвращают попадание токсинов (а также химиопрепаратов) в чувствительную среду мозга.
Лучевая терапия метастазов в мозг у людей с раком легких может работать довольно хорошо. И было обнаружено, что у людей с перестройками ROS1 есть опухоли, которые могут быть особенно чувствительны к этим методам лечения. Излучение может быть дано несколькими способами:
Выбор между этими двумя методами лечения является предметом споров. Стереотаксическая лучевая терапия - поскольку она лечит только небольшую часть мозга - имеет меньше побочных эффектов. Тем не менее, лучевая терапия всего мозга может уменьшить вероятность повторных метастазов в мозг - что очень часто встречается у людей, у которых уже были метастазы в мозг.
Устойчивость к лекарству
Большинство людей в конечном итоге становятся устойчивыми к Xalkori (кризотиниб) из-за новых приобретенных мутаций. Новый препарат в этой категории, Cometriq (кабозантиниб), кажется очень перспективным в начальных исследованиях. Похоже, что в ранних исследованиях удалось преодолеть устойчивость от этих вторичных мутаций.
Осторожно в отношении витамина Е и Кризотиниба
Исследования в 2017 и 2018 годах показывают, что компонент витамина Е, называемый а-токоферол, может значительно снизить эффективность кризотиниба. Поскольку большинство добавок с витамином Е, а также витамины, содержащие витамин Е, являются частично или в значительной степени альфа-токоферолом, следует избегать этих добавок, если это не предписано вашим онкологом.
Прогноз
ROS1-положительный рак легких имеет тенденцию быть агрессивным, расти и распространяться довольно быстро, но также практически беспрецедентно реагирует на целевую терапию. Поскольку лечение было одобрено совсем недавно, трудно понять, какова средняя продолжительность жизни человека. Но ответы до сих пор обнадеживают.
В одном исследовании среднее время работы Xalkori (время, после которого он перестал работать для половины людей, но продолжал работать для другой половины), составило 17 месяцев; большинство лечивших людей ответили на препарат.
Есть надежда, что когда люди станут резистентными к этому лекарству, другие будут доступны, одобрены или в клинических испытаниях, которые могут заменить лекарство, которое перестало работать. Как уже отмечалось, есть признаки того, что это может быть так.
Надеемся, что в ближайшем будущем рак легких с этими мутациями и перестройками будет рассматриваться как хроническое заболевание, например, как мы лечим диабет. Даже если рак еще не излечим, мы надеемся, что он поддается контролю.
Поддержка и Сообщество
Прекрасная группа людей с ROS1-положительным раком легкого собралась вместе. ROS1Ders связаны с ускорением исследований в области лечения ROS1-положительных опухолей. Поскольку это относительно редкий молекулярный профиль опухоли, многие онкологи не знакомы с последними доступными исследованиями и клиническими испытаниями. На их сайте есть ссылки на ведущих клиницистов и исследователей, изучающих ROS1-положительный рак легких, на случай, если ваш врач захочет проконсультироваться с кем-то, кто находится в центре исследования. Глобальная инициатива ROS1 - это партнерство, которое объединяет исследователей, пациентов, лиц, обеспечивающих уход, и врачей во всем мире для улучшения результатов лечения пациентов и ускорения исследований.
Слово от DipHealth
Никто не должен пройти через рак легких в одиночку. Если у вашего близкого человека был диагностирован рак легких, проверьте эти мысли о том, когда у вашего близкого есть рак легких.
Участие в сообществе по раку легких может быть очень полезным, даже для тех, кто обычно избегает групп. Поскольку ROS1-положительный рак легкого довольно редок, маловероятно, что вы найдете много людей в вашем сообществе, которые испытывают те же физические и эмоциональные проблемы, что и вы.
В 2015 году на саммите LUNGevity HOPE была сформирована группа, состоящая исключительно из людей, столкнувшихся с ROS1-положительным раком легких. Это захватывающая эпоха для людей с раком легких, поскольку пациенты работают бок о бок с врачами не только для того, чтобы понять их болезнь, но и внести вклад в исследования, которые еще предстоит сделать.

Мутация EGFR
Эта мутация встречается преимущественно у некурящих людей. Обнаружение такой мутации на поздних стадиях рака представляет собой обнадеживающий признак, поскольку предполагает восприимчивость к лечению ингибиторами тирозинкиназы (препараты эрлотиниб и гефитиниб).
Транслокации ALK
По данным исследований, эта мутация при раке легкого более характерна у молодых и некурящих пациентов. Её обнаружение говорит о чувствительности к кризотинибу.
Мутация KRAS
Обычно данная мутация при лаке легкого встречается у курильщиков. Особой роли для прогноза не играет. При анализе статистических данных указано – встречались и случаи ухудшения состояния, и улучшения, что не позволяет сделать однозначный вывод о её влиянии.
Транслокация ROS1
Эта мутация, подобно транслокации ALK, преимущественно встречается у молодых, некурящих пациентов. В ходе клинических испытаний установлена высокая чувствительность таких опухолей к лечению кризотинибом, сейчас ведутся исследования препаратов нового поколения.
Мутация HER2
Обычно изменения представлены точечными мутациями. Опухолевые клетки в своей жизнедеятельности не зависят критическим образом от этой мутации, однако по результатам новых испытаний выявлен частичный положительный эффект у пациентов с комбинированным лечением посредством трастузумаба и цитостатических средств.
Мутация BRAF
Некоторые больные с мутациями этого гена (вариант V600E) поддаются лечению дабрафенибом, ингибитора белка B-RAF, кодируемого геном BRAF.
Мутация МЕТ
Ген МЕТ кодирует тирозинкиназный рецептор фактора роста гепатоцитов. Встречается увеличение числа копий этого гена (амплификация), при этом сам ген редко подвергается мутациям, и их роль изучена недостаточно.
Амплификация FGFR1
С данной амплификацией сталкиваются 13-26% пациентов с плоскоклеточным раком легких. Обычно распространена среди курящих пациентов, на практике предполагает неблагоприятный прогноз. Однако ведется соответствующая работа по разработке препаратов, направленных на это нарушение.
Основные принципы диагностики мутаций рака легкого
Чтобы точно диагностировать рак легких, предусмотрена бронхоскопия с забором биоптата для проведения цитологического и гистологического исследований. После того как из лаборатории поступит заключение о наличии мутации и выявленном типе мутации, будет составляться подходящая тактика медикаментозного лечения, назначаются соответствующие биологические препараты.
Биологическая терапия при злокачественных опухолях легких
Каждая программа терапии индивидуальна. Биологическая терапия предполагает работу с двумя типами лекарств, которые различаются по принципу воздействия на опухоль, но направлены на одинаковый окончательный эффект. Их цель – блокирование мутации клеток на молекулярном уровне, без вредного последствия для здоровых клеток.
За счет стабильного целевого действия исключительно на клетки опухоли удается приостановить рост злокачественных клеток уже спустя несколько недель. Чтобы поддержать достигнутый эффект, требуется продолжение курса приема препаратов. Лечение с помощью препаратов практически не сопровождается побочными эффектами. Но постепенно возникает невосприимчивость клеток к действующим компонентам лекарств, поэтому нужно корректировать лечение по мере необходимости.
Различия в лечении мутаций рака легкого
На долю мутации гена EFGR приходятся порядка 15% всех случаев. В таком случае для лечения может использоваться один из ингибиторов EGFR: эрлотиниб (Тарцева) или гефитиниб (Иресса); созданы и более активные препараты нового поколения. Данные лекарства обычно не вызывают тяжелых побочных эффектов, выпущены в форме капсул либо таблеток.
Транслокация генов ALK/EML4, на долю которой приходятся 4-7% всех случаев, предполагает назначение кризотиниба (Ксалкори); разрабатываются его более активные аналоги.
При опухолевом ангиогенезе для его подавления предполагается терапия с препаратом бевацизумаб (Авастин). Назначается препарат вместе с химиотерапией, значительно повышая эффективность данного лечения.

Переменные, влияющие на выживание при раке легких
Ожидаемая продолжительность жизни при раке легких 4 стадии может значительно различаться у разных людей.
Некоторые из этих переменных включают:
Статистика
В дополнение к различиям организмов разных людей важно иметь в виду, что статистика часто основана на людях, которых лечили несколько лет назад. Например, самые последние статистические данные, которые мы имеем о раке легких на 2015 год, основаны на людях с этим диагнозом в период с 2007 по 2011 год. С тех пор новые методы лечения были одобрены для людей с прогрессирующим раком легких, и еще большее количество новых методов лечения изучается в клинических исследованиях.
Если у вас или вашего близкого человека рак легких 4 стадия - сколько осталось жить? Средняя продолжительность жизни на 4 стадии рака легких (когда 50% пациентов живы и 50% скончались) составляет лишь около 8 месяцев. Пятилетняя выживаемость, то есть процент людей, которые, как ожидают, будут жить через пять лет после постановки этого диагноза – составляет, к сожалению, всего 4%.
В то время как эти цифры звучат пессимистично, есть много людей, которые очень долго живут после того, как им поставили диагноз рака легких 4 стадии. На саммите HOPE в 2016 году в Вашингтоне, округ Колумбия, представили фотографии, на которых изображены более чем 300 человек, перенесших рак легких, успешно живущих с этим заболеванием, а также группа людей, переживших 4 стадию этого недуга, и живут без болезни в течение по меньшей мере 10 лет. Помните: вы не являетесь статистикой. Есть надежда, и это не ложная надежда.
Управление раком легкого 4 стадии с метастазами
Последнее что очень важно иметь в виду.
В то время как рак легких 4 стадии обычно не излечим, он все-таки поддается лечению. Эти методы лечения могут не только улучшить выживаемость, но и помочь с симптомами этого заболевания.
Недавнее одобрение двух препаратов иммунотерапии в 2015 году (и других препаратов в этой категории, оцениваемых в клинических испытаниях), говорит о том, что может быть возможен долгосрочный контроль заболевания у некоторых людей с прогрессирующим раком легкого. Для людей с целевыми мутациями переход на недавно разработанные препараты, когда опухоли становятся устойчивыми, свидетельствует о том, что для некоторых людей прогрессирующий рак легких может в будущем рассматриваться как хроническое заболевание, такое как сахарный диабет.
Что вы можете сделать, чтобы улучшить свои шансы на выживание
После многих лет небольшого прогресса в лечении рака легких варианты лечения и персонализации лечения этого заболевания увеличились экспоненциально. Это означает, что любому человеку, даже специалисту по онкологическому заболеванию, трудно быть осведомленным о каждом новом прогрессе и клинических испытаниях, проводимых по всему миру.
Исследования показывают, что люди, которые узнают больше о своем раке и становятся своим собственным защитником в лечении рака, могут иметь лучшие результаты. Отличный способ не только получать поддержку, но и узнавать о последних достижениях в лечении – это участвовать в группе поддержки рака легких или в сообществе поддержки в социальных сетях и в живую.
Кроме того, существует несколько высокоэффективных альтернативных методов лечения рака, таких как терапия Герсона и противораковая диета Джоанны Бадвиг (протокол Бадвиг), а также множество других средств и методов лечения этого страшного заболевания, о которых вы можете узнать в этом разделе нашего сайта – Рак (онкология) - раковые заболевания, их причины, симптомы и лечение.
Эта статья была полезна для вас? Поделитесь ей с другими!
Индивидуальное лечение немелкоклеточного рака легких
Биохимик доктор Кохен в 1956 году заинтересовался механизмом, лежащим в основе роста злокачественных клеток, и в начале периоде своего наблюдения обнаружил, что если дать опухолевые клетки, полученные от крыс, эмбрионам цыплят, то вырабатывается вещество, которое приводит к нервному развитию и росту у эмбрионов, данный процесс получил название фактор эпидермального роста. После проведенных испытаниях на животных было обнаружено, что фактор эпидермального роста играет важную роль не только для злокачественных клеток, но и в эмбриональном развитии и обеспечении нормального баланса работы организма. После открытия фактора эпидермального роста доктором Кохеном ушло еще 20 лет для того, чтобы суметь объяснить структуру молекулы, а нобелевская премия была им получена только в 1986 году.
Фактор эпидермального роста представляет собой датчик (рецептор), расположенный в структуре белка на поверхности клетки.
Этот рецептор образован из трех частей: часть, связанная с поверхностью клетки, часть оболочки клетки и часть, указывающая на ферментную активность внутри клетки. При активации рецептора идет передача сигнала внутри клетки и в результате происходят изменения внутри клетки. При наступлении аномального процесса (изменение, мутация) в гене, который кодирует фактор эпидермального роста, рецептор начинает работать сильнее, что, в свою очередь, приведет к росту и размножению раковых клеток.
При немелкоклеточном раке легких чрезмерное увеличение фактора эпидермального роста (оверэкспрессия) наблюдается у 70% больных. Однако мутация фактора эпидермального роста – это и есть то, что определяет ответ на лечение. Вероятность наличия мутации при немелкоклеточном раке легких составляет 20%.
Скрининг мутации особенно рекомендуется для немелкоклеточного рака легких следующих подвидов:
- Аденокарценома
- Крупноклеточный тип
- Рак, при котором невозможно определить подтипа
- Плоскоклеточный рак у людей, которые никогда не курили сигареты
- аденоплоскоклеточный рак (смешанный тип)
Самый распространенный тип мутации: экзон 19-21 (90%) и экзон 18-21. При наличии этих мутаций без внешнего возбуждения клетки внутри самой клетки образуется постоянный сигнал. Это приводит к росту опухоли, размножению, увеличению образования сосудов и образованию метастаз.
Процент ответной реакции на лечение при немелкоклеточном раке легких с мутацией рецептора фактора эпидермального роста составляет 50-60%.
Мутация рецептора фактора эпидермального роста сегодня может быть определена и из опухолевой ткани, и в анализе крови. Ниже перечислены методы целенаправленного лечения, которые можно использвать для лиц, у которых была обнаружена данная мутация:

Эффективность Эрлотиниба у больных с мутацией фактора эпидермального роста при лечении на первом этапе

После того, как стало известно о молекулярных путях немелкоклеточного рака легких и об аномальных изменениях (мутациях) в этих путях, удалось разработать целенаправленные лекарства именно под эти мутации. Выше мы рассказали о трех (EGFR, ALK и ROS1) мутациях среди всех, которые были лучше всего описаны для рака легких, и о разработанных целенаправленных лекарствах.
Эти мутации встречаются редко. Существуют лекарства, разработанные специально для этой цели, но вместе с тем продолжаются клинические исследования, которые должны будут показать эффективность лекарств при немелкоклеточном раке легких. Мутации перечислены ниже:
- BRAF V600 E
- Met мутации
- Реструктурирование RET
- HER2 мутация
Путь VEGF
Раковым клеткам для роста необходимо питание в крови и кислород. Опухоль образует кровеносные сосуды через молекулы VEGF (рецептор фактора роста сосудов). Лекарства, разработанные против рецептора поверхности, который присоединяется к VEGF, нарушают структуризацию раковых сосудов и предотвращают их рост.

План лечения немелкоклеточного рака легких 4ой стадии – краткое содержание
Читайте также:

