Рак легких и платина
Цель
При испытании индивидуальных химиотерапевтических агентов, проведенном ВКОГ, ТАКСОЛ и параплатин обеспечивали наиболее длительное выживание [1,2]. Эффективность этой комбинации оценивалась на больных с раком яичника, причем были получены обнадеживающие результаты и приемлемая токсичность [3]. На основании этих и других данных было начато настоящее исследование по схеме Фазы II для оценки эффективности и токсичности ТАКСОЛА и параплатина у первичных больных с распространенной формой немелкоклеточного рака легкого [4].
Больные и методы
У выбранных для испытания больных был немелкоклеточный рак легкого на поддающейся количественной оценке стадии 111В или IV; больные не получали в прошлом никакой химиотерапии; функциональный статус по ВКОГ соответствовал 0,1 или 2; функция костного мозга, печени и почек была нормальной [5]. Характеристики контингента больных представлены в Таблице 1.
Перед лечением ТАКСОЛОМ больным проводилась стандартная медикаментозная терапия с целью профилактики связанных с применением ТАКСОЛА реакций гиперчувствительности. Больные были разделены на три группы: группа 1 получала ТАКСОЛ в дозе 135 мг/м 2 в форме внутривенного вливания продолжительностью 24 часа и параплатин в дозе 300 мг/м 2 ; группа 2 получала ТАКСОЛ (паклитаксел концентрат для инъекций) в дозе 135 мг/м 2 в форме 24-часового внутривенного вливания и параплатин (карбоплатин для инъекций), доза которого была ориентирована на значение AUC равное 6 (при расчете по формуле Кальверта); группа 3 получала ТАКСОЛ в дозе 175 мг/м 2 на протяжении 24 часов и параплатин в дозе, соответствующей AUC равной 6 [5].
Курсы химиотерапии повторялись с интервалами 28 дней, всего было проведено шесть курсов. Больные оценивались после двух курсов; больных с прогрессирующей формой заболевания снимали с испытания. Других больных продолжали лечить до появления неприемлемых токсических эффектов или указаний на прогрессирование заболевания [5].
В исследовании использовался разработанный ВКОГ инструмент для оценки качества жизни, Факт-Л или шкала Функциональной оценки противоракового лечения при раке легкого [5,6].
РЕЗУЛЬТАТЫ
Токсичность
Основным токсическим эффектом была миелосупрессия (Таблица 2). Только 4,5% курсов химиотерапии сопровождались тромбоцитопенией степени 3/4 по классификации ВКОГ. Инфекции степени 3 отмечались в девяти курсах (5%) и инфекции степени 4 еще в пяти курсах. Большая часть этих эпизодов отмечалась при дозе ТАКСОЛА 135 мг/м 2 и при дозе параплатина, обеспечивавшей AUC равное 6. По-видимому, миелосупрессия носила кумулятивный характер. В связи с последними данными о менее выраженной миелосупрессии при меньшей продолжительности вливания ТАКСОЛА [7], план этого исследования будет изменен: после одночасового вливания ТАКСОЛА будет проводиться вливание параплатина в дозе, обеспечивающей AUC=6; это лечение будет проводиться в амбулаторных условиях [8].
Таблица 1. Испытание по Фазе II в Университете Вандербильт:
Характеристики контингента больных
| Число больных | 51 |
| Мужчин | 34 |
| Женщин | 17 |
| Средний возраст (медиана (интервал) | 60 (38-74) |
| Средний функциональный статус (интервал) | 1 (0-3) |
| Стадия: | |
| IIIa | 6 |
| IV | 45 |
| Гистология: | |
| Аденокарцинома | 39 |
| Плоскоклеточная карцинома | 6 |
| Крупноклеточная карцинома | 8 |
Только 4% курсов химиотерапии было отложено в связи с миелосупрессией, средний интервал между курсами (медиана) составлял 29 дней [5].
Из не связанных с системой кроветворения токсических эффектов в настоящем исследовании отмечались главным образом легкая тошнота, эпизодические миалгии и артралгии, а также алопеция у всех больных. Не наблюдалось анафилактических реакций, а также каких-либо кардиологических или неврологических осложнений [5].
Таблица 2. Испытание по Фазе II в Университете Вандербильт:
Дозы и гематологическая токсичность [9]
| Доза ТАКСОЛА (мг/м 2) | Доза параплатина | Число больных | Минимум КБК (интервал) | Минимум ТРМ (интервал) |
| 135 | 300 мг/м 2 | 16 | 1,5 (0,7-4,3) | 212 (4-459) |
| 135 | AUC=6 | 12 | 2,9 (0,4-6,6) | 226 (79-445) |
| 175 | AUC=6 | 23 | 2,1 (0,7-5,2) | 173 (5-412) |
| КБК=клетки белой крови; ТРМ=тромбоциты; AUC=площадь под кривой | ||||
В этом исследовании объективные ремиссии наблюдались в 27% случаев, причем отмечалось 14 частичных ремиссий (ЧР) (Таблица 3). Среднее время выживания в группе из 51 больного (медиана) составляло 38 недель, а выживание в течение года составляло 37% [5, 8]. Важно отметить, что процент объективных ремиссий в этой группе был лишь незначительно большим, чем при применении ТАКСОЛА в форме монотерапии [1]. Это могло быть связано с дозой, использовавшейся в настоящем испытании, поскольку в других испытаниях, проводившихся на более высоких дозах ТАКСОЛА, Параплатина(карбоплатин для инъекций) или обоих препаратов, сообщалось о более высоких процентах ремиссии [9,10].
Таблица 3. Испытание по Фазе III в Университете Вандербильт:
Ремиссии [8]
| Таксол, доза (мг/м 2 ) | Параплатин, доза | Параплатин, доза (мг/м 2 ) | Ремиссии, всего (%) |
| 135 | 300 мг/м 2 | 300 (0-303) | 4/16 (25) |
| 135 | AUC=6 | 346 (0-489) | 1/12 (8) |
| 175 | AUC=6 | (349 (130-567) | 9/23 (39) |
| AUC=площадь под кривой | |||
Выводы
Хотя для определения оптимальной дозы ТАКСОЛА в комбинации с параплатином при лечении больных с немелкоклеточным раком легкого необходимо провести рандомизированное испытание, предварительные результаты показывают, что в таком контексте может существовать соотношение доза-эффект [5].
Кроме того, профиль токсичности использованной комбинации был приемлемым, поскольку наблюдались лишь немногочисленные тяжелые побочные эффекты, за исключением лейкопении и лихорадки нейтропенического происхождения. Примечательно отсутствие такой проблемы как тромбоцитопения (отмечалась только в 4,5% всех проведенных курсов лечения) при использовании комбинации ТАКСОЛА и параплатина, особенно когда доза параплатина рассчитывается по формуле Кальверта [5].
Исходя из полученных данных, в настоящее исследование будут набираться новые больные для проведения лечения по измененной схеме. Больные будут получать ТАКСОЛ в дозе 175 мг/м 2 который будет вводиться путем одночасового внутривенного вливания, после чего будет вводиться параплатин в дозе, необходимой для достижения AUC=6.
Литература
1. Chang AY, Kirn K, Glick J, et al. Phase II study of Taxol, merbarone, and pirox-antrone in stage IV non-small cell lung cancer: the Eastern Cooperative Oncology Group results. JNCI. 1993; 85: 388-394.
2. Bonomi PD, Finkelstein DM, Ruckdeschel JC, et al. Combination chemotherapy versus single agents followed by combination chemotherapy in stage IV non-small-cell lung cancer: a study of the Eastern Cooperative Oncology Group. JClinOncol. 1989; 7: 1602-1613.
3. Ozols RF, Kilpatrick D, O'Dwyer P, et al. Phase I and pharmacokinetic study of Taxol and carboplatin in previously untreated patients with advanced epithelial ovarian cancer: a pilot study of the Gynecologic Oncology Group. Proc Am Soc Clin Oncol 1993; 12: 259. Abstract 824.
4. Paul DM, Johnson DH, Hande KR, et al. Carboplatin and Taxol: a well tolerated regimen for advanced non-small cell lung cancer. Proc Am Soc Clin Oncol. 1994; 13-352. Abstract 1181.
5. Johnson DH, Paul DM, Hande KR, et al. Paclitaxel plus carboplatin for advanced lung cancer: preliminary results of a Vanderbilt University Phase II trial-LUN-46. Semin Oncol. 1995; 22 (suppl 9): 30-33.
6. Cella DF, Tulsky DS, Gray G, et al. The functional assessment of cancer therapy scale: development and validation of the general measure. J Clin Oncol 1993; II: 570-579.
7. Eisenhauer EA, ten BokkelHuinink WW, Swenerton KD, et al. European-Canadian randomized trial of paclitaxel in relapsed ovarian cancer: high-dose versus low-dose and long versus short infusion. J Clin Oncol. 1994; 12: 2654-2666.
8. Paul D, DeVore RD, Hande K, et al. Carboplatin and paclitaxel: an active regimen for advanced non-small cell lung cancer. Poster presented at American Society of Clinical Oncology; May 20-23. 1995; Los Angeles, CA.
9. Bunn PA Jr, Kelly K. A phase I study of carboplatin and paclitaxel in non-small cell lung cancer: a University of Colorado Cancer Center study. Semin Oncol. 1995; 2-2 (suppl 9): 2-6.
10. Belani CP, Aisner J, Hiponia D, et al. Paclitaxel and carboplatin with and without filgrastim support in patients with metastatic non-small cell lung cancer. Semin Oncol 1995; 22 (suppl 9): 7-12.

Скрытое течение
Максим Руденко: Если брать всех вообще, кто умер от онкологических заболеваний, то среди мужчин рак лёгких как причина смерти стоит на первом месте (среди женщин – рак молочной железы). Этот вид рака вообще больше распространён среди мужчин, поскольку среди них больше курящих.
- То есть курение – фактор риска?
- Начнём с того, что рак лёгкого – собирательное понятие, на самом же деле его видов немало. Так вот, возникновение плоскоклеточного рака лёгкого, растущего из бронхов (его отличительная особенность в том, что он наименее поддаётся лекарственному лечению), обусловлено табакокурением. То есть это не просто фактор риска, это причина заболевания.
Среди всех пациентов, у кого выявлен рак лёгкого, один год переживает всего 50%. У более чем 70% пациентов злокачественное новообразование лёгкого выявляется на третьей и четвёртой стадиях. Тогда как самая высокая выживаемость (от 75 до 90%) регистрируется среди людей, у которых заболевание выявлено на первой стадии, но доля этих пациентов в среднем по России всего 11–12%. Плюс 14% - это вторая стадия, при которой 50% пациентов на фоне лечения переживают пятилетний рубеж.
- Печальная статистика. С чем это связано? С тем, что рак лёгких долго не выдаёт себя очевидными симптомами?
- Совершенно верно, для этого вида рака характерно скрытое течение, на ранней стадии заболевание не имеет выраженных клинических симптомов. Кроме того, это довольно агрессивная опухоль, которая выявляется тогда, когда уже есть либо метастазы, либо распространение в другие органы.

Кроме того, наш диспансер участвует в пилотном проекте по скринингу злокачественных новообразований лёгкого. Кто участвует в скрининге? Группа риска – это, прежде всего, курящие мужчины в возрасте от 45-50 лет или те, которые бросили курить ранее 15 лет назад.
Но выявление выявлением, а всё же лучше всего начать с профилактики рака лёгкого.

А смысл?
- Однозначно – в отказе от курения! Причем не только активного, но и пассивного.
- Ну да, при этом бросив курить, 15 лет человек всё равно будет числиться в группе риска. В чём тогда смысл?
- Смотрите, после отказа от курения в течение 20 минут происходит снижение артериального давления и частоты сердечных сокращений. В течение 12 часов – снижение уровня оксида углерода в крови до нормального значения. В течение 48 часов восстанавливаются нервные окончания, ощущения запаха и вкуса. Трёх месяцев достаточно для улучшения кровообращения и функции лёгких. Если человек продержался без курения год, риск возникновения ишемической болезни сердца снижается вдвое; если пять лет, риск возникновения инсульта снижается до уровня некурящих людей, плюс значительное снижение риска развития некоторых видов рака (ротовой полости, глотки, мочевого пузыря, шейки матки). За десять лет вдвое снижается риск смерти от рака лёгкого, наблюдается значительное снижение развития рака гортани и поджелудочной железы. А за 15 – риск развития ишемической болезни сердца и обструктивной болезни лёгких. Как видите, причины отказа от курения весьма убедительны. И в этом отношении российское законодательство справедливо ограничивает нас от табачного дыма во многих общественных местах.
- Отказ от курения – единственная мера профилактики рака лёгких?
- Главная, но не единственная. Другими мерами профилактики также не следует пренебрегать. Скажем, стоит стараться избегать воздействия на организм канцерогенов, придерживаться рационального питания: употребление достаточного количества витаминов, бета-каротина, антиоксидантов, витамина Е также снижает риск возникновения рака лёгкого. Но! На фоне отказа от курения. Замечу, что до эпохи массового производства сигарет и их широкой доступности рак лёгкого был казуистикой.

- Таких исследований пока нет, думаю, судить о воздействии вейпов на организм можно будет позже, когда в поле зрения учёных попадут люди, имеющие многолетний опыт нового на сегодняшний день увлечения. То есть нынешняя молодежь. О результатах будущих исследований сегодня судить сложно, но есть ли смысл рисковать? Бог не дал нам, людям, дымохода, так зачем нам дымить?
- Какие методы лечения рака лёгких сегодня применяются?
- На сегодняшний день самый эффективный метод лечения – это хирургический (он применяется на первой стадии заболевания). Кроме того, используется химеотерапия, лучевые методы лечения и их комбинация.
Хирургическое лечение подразумевает удаление поражённой части лёгкого или всего лёгкого. Понятно, что при удалении доли лёгкого качество жизни не так страдает, как при удалении целого органа – в этом случае, бывает, люди погибают не от развития рака, а от осложнений со стороны сердечно-сосудистой системы, поскольку сердцу сложно работать с одним лёгким. Но мы в отделении торакальной хирургии Свердловского областного онкологического диспансера идём по пути органосохраняющих операций, делаем их всё больше и больше, тем более что сегодня в России и в нашем диспансере активно развивается малоинвазивная хирургия.
- Вернёмся к началу разговора. Я правильно понимаю, что рак лёгких на ранней стадии у человека – это, как правило, случайная находка?
- Совершенно верно. Люди, например, идут делать операцию на глаза или на сердце, и у них выявляется рак лёгкого.
- Специфических симптомов у рака лёгкого нет, они все схожи с симптомами любых лёгочных заболеваний. Допустим, кровохарканье может быть и при туберкулёзе, и при пневмонии (особенно вирусной), и при раке лёгкого. Одышка, повышение температуры также могут быть при банальной пневмонии. Но должна быть онкологическая настороженность. То есть, если пациент входит в группу риска, на эти симптомы следует обратить внимание с точки зрения онкологии. Но это больше касается медиков. А людям при любом длительном кашле следует идти к врачу, который выслушает и сопоставит жалобы, направит на флюорографию.
- Специалисты первичного звена здравоохранения, то есть врачи в поликлиниках, имеют настороженность по отношению к раку?
- Я не могу сказать за каждого конкретного человека. Но мы со своей стороны делаем всё возможное для повышения этой настороженности. Специалисты онкологического диспансера регулярно проводят лекции для первичного звена здравоохранения (есть даже клинические рекомендации по выявлению рака лёгкого для первичного звена), активно используют возможности телемедицины.
- Какие индивидуальные особенности влияют на то, что у одних курящих людей возникает рак лёгкого, а у других нет?

Понимаете, мы не говорим, что если человек курит, то он обязательно заболеет раком лёгкого. Но те, кто болеет, все курят. Думаю, больше половины пациентов не оказались бы в нашем отделении, если бы не курили.
- Мы всё больше говорим про мужчин, а есть ли среди ваших пациентов женщины?
- Конечно. Более того, в последнее время женщин, у которых диагностирован рак лёгких, становится всё больше. Простой пример. Двадцать лет назад, когда я только начинал работать, у нас была одна женская палата, потом появилась необходимость открыть ещё одну, потом ещё…
- Сколько лет было самому молодому вашему пациенту?
Платиновая химиотерапия представляет собой современный и достаточно эффективный метод лечения онкологических заболеваний.
Взять, к примеру, препарат Цисплатин . Впервые он был опробован ещё в 1978 году в Соединённых штатах Америки. Прежде всего, он разрабатывался для лечения рака яичка, но в результате, используется и для лечения рака лёгких, при лимфоме , при раке яичника у женщин и ещё нескольких видов рака. Однако и в этом случае без побочных эффектов обойтись, никак не удалось. Они проявляются в сильно выраженном токсическом воздействии, в результате чего, наблюдается процесс формирования на клеточном уровне лекарственной резистентности.
Среди страдающих раковыми заболеваниями пациентов, давно прижилось мнение, что если начали капать платину, то значит, дела совсем плохи. На самом деле это совсем не так. Дело в том, что химиотерапия платиной назначается в тех случаях, когда лечение опухоли, в силу её особенности, другими препаратами попросту не эффективно. Это касается как раз таких случаев, как: рак мочевого пузыря, яичников, рака лёгких и ещё при ряде онкологий . И только в случаях ярко выраженной почечной недостаточности, врачи осуществляют лечение этих заболеваний без препарата платины. При этом, конечно же, учитывается тот факт, что такая терапия будет гораздо менее прогрессивной.
Совсем иное дело, когда при лечении рака молочной железы назначают платиновую химиотерапию только в том случае, когда опухоль отказывается реагировать на традиционную схему лечения. Но, тем не менее, говорить о том, что химиотерапия платиной эффективна или нет, было бы как-то не очень корректно. Потому как, при лечении определённых видов опухолей ей равных нет, а при лечении других видов, она становится попросту бесполезной.
Сегодня, на смену Цисплатину пришёл Фенантриплатин , который гораздо легче проникает в раковые клетки и ингибирует транскрипцию.
По сути, платиновые препараты оказывают цитостатическое воздействие, которое основано на появлении в ДНК внутрицепочечных поперечных и продольных связей, создающих препятствия её репликации. По сути, это продиктовано химическим составом лекарственных препаратов, в центре которых расположен платиновый атом, связанный с двумя аммониевыми лигандами и двумя ионами хлора. Вся эта структура, или можно сказать комплекс, целиком и полностью имеет отрицательный заряд. Однако, в случае проникновения в раковую клетку, он гидролизуется с замещением хлорид-ионов на ОН-группы и меняет свою полярность на положительную. ОН-группы, в свою очередь, легко вытесняются и дают возможность платиновому комплексу полноценно воздействовать на ДНК раковых клеток.
Когда-то, считалось, что цитостатический эффект возможно реализовать исключительно при условии совокупности с двумя центрами ДНК, потому как это даёт возможность пересекающиеся связи между отдельными участками ДНК. Но уже в восьмидесятых годах, учёные стали проводить исследования заряжённых платиновых комплексов, которые не просто связывались с центром ДНК, но и производили цитостатический эффект. В результате, у онкологических пациентов появилось достойное оружие против ракового недуга.
Задать вопрос врачу онкологу
Диагностка и лечение онкологии в медицинских центрах Израиля подробная информация
Подпишитесь на рассылку Новости онкологии и будьте в курсе всех событий и новостей в мира онкологии.

Научный центр терапии рака Венского университета и MedUni Vienna получили новые данные о лечении рака химиотерапией на основе платины. Этот метод давно используется в медицине, но считалось, что его применение приводит к повреждению иммунной системы. Был отмечен цитотоксический эффект повреждения здоровых клеток.
Однако, последние исследования выявили, что химиотерапия с платиной делает раковые клетки более видимыми для лейкоцитов и борьба происходит эффективнее.Пациенты с раком легких, которые получали химиотерапию на основе платины, с большей вероятностью выживали через 6, 12 и 24 месяца после лечения по сравнению с пациентами, которые получали лечение не на основе платины. Плоскоклеточный рак легких и другие его виды являются одной из причин смерти от онкологии во всем мире. Ежегодно умирают 1,76 млн. человек. Поэтому так важно найти наиболее эффективные методы лечения для пациентов с этим заболеванием.
Химиотерапия на основе платины показала более высокую частоту полного ответа опухоли (полное исчезновение опухолей, по крайней мере, в течение определенного периода времени после лечения) по сравнению с химиотерапией не на основе платины. Недостаток терапии состоит в том, что она чаще вызывала некоторые побочные эффекты, включая тошноту и рвоту, а также низкий уровень тромбоцитов. Эти явления не опасны, но снижают качество жизни больных.
Вальтер Бергер, заместитель руководителя Венского института онкологических исследований MedUni считает, что будущее лечения рака за комбинацией иммунотерапии с химиотерапией на основе платины. Злокачественная опухоль разрастается после проигрыша иммунной системы при активизации раковых клеток. Новообразование ослабляет организм и тормозит лечебное действие лейкоцитов, которые не могут распознать чужеродные агенты. Лейкоциты перестают обнаруживать переродившиеся клетки и прекращают борьбу.
Химиотерапия с платиной разрушает раковые клетки и как бы делает их видимыми для лейкоцитов. Происходит самообновление иммунной системы, которая начинает активно бороться с болезнью. Раковые клетки склонны к мутации, но активировавшиеся лейкоциты уже способны распознать и новые разновидности. Если подкрепить химиотерапию иммунокрректорами, то лечение будет более эффективным.
Несмотря на побочные эффекты, применение химиотерапии с платиной в комбинации с препаратами для усиления иммунного ответа считается теперь перспективной методикой для борьбы с онкологией. Именно комбинированная терапия дает больным шансы на выживаемость даже с метастазами.
Целью проводимых исследований является повышение успешности лечения, в то же время, уменьшая или лучше контролируя любые связанные побочные эффекты. В долгосрочной перспективе ожидается, что комбинированная терапия вылечит большинство пациентов или, по крайней мере, приведет к долгосрочной ремиссии.

Рак лёгкого — это опухоль, которая развивается из ткани, выстилающей изнутри поверхность бронхов, бронхиол и слизистых бронхиальных желез, — эпителия. В большинстве случаев рак лёгкого развивается у мужчин после 60 лет. Это заболевание — самое распространённое из всех онкологических: ежегодно насчитывается больше 1 миллиона новых случаев рака лёгкого, и число это растёт.
- Симптомы рака лёгкого
- Симптомы опухоли Панкоста
- Симптомы периферического рака лёгкого
- Виды рака лёгкого
- Центральный и периферический рак
- Мелкоклеточный рак лёгкого
- Стадии рака легкого
- Как распознать рак лёгкого на ранней стадии?
- Что повышает риск развития рака лёгкого?
- Возможно ли снизить риск?
- Метастазы в лёгкие
- Лечение рака легких на разных стадиях
Симптомы рака лёгкого
Если каждый год делать флюорографию грудной клетки, в большинстве случаев диагноз удастся поставить на более ранних стадиях, когда прогноз выглядит наиболее оптимистичным.
Это особенно важно ещё и потому, что симптомов, благодаря которым можно на раннем этапе заподозрить онкологию, практически нет. То, как проявляется рак лёгкого, зависит от разных факторов: стадии развития опухоли, её расположения в лёгком, нарушений, которые она вызывает и т. д. Рак лёгкого может маскироваться под различные заболевания. Например, иногда он выглядит, как длительно текущая и плохо поддающаяся лечению пневмония. Растущая опухоль может стать причиной кашля, выделения слизистой или слизисто-гнойной мокроты. Иногда в мокроте есть примесь крови — это случается при воспалении слизистой оболочки поражённого бронха. У таких пациентов бывает боль в груди, одышка, охриплость.
Из-за того, что опухоль выделяет вредные вещества, возникают и другие симптомы рака лёгкого, которые могут приниматься за проявления совершенно иных заболеваний. Это утомляемость, снижение трудоспособности, слабость, повышение температуры (обычно небольшое), а также потеря веса.
Симптомы опухоли Панкоста
Рак верхушки лёгкого (опухоль Панкоста) из-за близкого расположения других органов и нервных стволов зачастую вызывает более ярко выраженные симптомы: слабость мышц кисти, боль в плечевом поясе, по передней поверхности груди и между лопатками, также в области кисти или предплечья возникают неприятные ощущения или нарушается чувствительность, атрофируются мышцы. К сожалению, такие симптомы часто дезориентируют врача, и человек тратит время на лечение несуществующего шейно-грудного остеохондроза.
Можно ли этого избежать? Да. Достаточно обратить внимание на синдром Горнера. Из-за поражения шейных симпатических узлов верхнее веко одного глаза опускается (птоз), сужается один зрачок (миоз) и значительно уменьшается потоотделение только с одной стороны лица (ангидроз). Также голос человека может стать хриплым из-за повреждения возвратного гортанного нерва.
Симптомы периферического рака лёгкого
О том, что в организме появилась или начала появляться опухоль, в редких случаях может сообщать паранеопластический синдром. Это комплекс различных проявлений, которые возникают не из-за непосредственного воздействия опухоли на ткани, а с помощью производства раковыми клетками различных веществ. При раке лёгкого чаще, чем при любом другом онкологическом заболевании, паранеопластический синдром затрагивает нервную систему. Это, в частности, проявляется трудностями при ходьбе, нарушением координации, проблемами с удержанием равновесия, такому человеку становится трудно глотать, его речь невнятна. Помимо этого может наблюдаться ухудшение памяти, сна, зрения и т. д.
Паранеопластический синдром иногда включает в себя повышение уровня кальция. В некоторых случаях опухоль может даже производить гормоны, которые в здоровом организме синтезируют поджелудочная и паращитовидная железы, гипофиз и гипоталамусом. Именно поэтому врач должен обратить особое внимание на настораживающие признаки, чтобы провести углубленное обследование и, возможно, выявить рак лёгкого на ранней стадии.

Обычно первый симптом заболевания – упорный сухой кашель. Если он беспокоит в течение нескольких недель, и не связан с аллергическими или инфекционными заболеваниями, нужно посетить врача и пройти обследование. Еще один ранний признак – повышение температуры тела. Обычно оно незначительное, до 37,5 градусов, но сохраняется в течение длительного времени. Беспокоят такие неспецифические симптомы, как повышенная утомляемость, слабость, частые недомогания. Зачастую эти проявления списывают на бронхиты и пневмонии.
Возникают свистящие звуки во время дыхания, голос становится охриплым. Со временем кашель становится все более мучительным, во время него отходит мокрота, в которой можно заметить примесь крови. Это уже однозначно повод обследоваться на рак легких.
В легочной ткани нет болевых рецепторов. Поэтому на ранних стадиях болей практически не будет. Они возникают периодически и быстро проходят. Уже позже, когда опухоль успевает сильно вырасти, распространиться в плевру и межреберные нервы, беспокоят длительные мучительные боли в грудной клетке. Они могут распространяться в плечо, наружную часть руки.
Появление одышки говорит о том, что опухоль поражает большое количество легочной ткани, из-за чего сокращается дыхательная поверхность. Этот симптом может быть связан с экссудативным плевритом .
Виды рака лёгкого
В зависимости от типа клеток различают:
- мелкоклеточный рак (овсяноклеточный, комбинированный овсяноклеточный, промежуточно-клеточный);
- плоскоклеточный, или эпидермальный рак лёгкого (низкодифференцированный, ороговевающий, неороговевающий);
- аденокарциному лёгкого (ацинарная, папиллярная, бронхиоло-альвеолярный рак, солидный рак с образованием муцина);
- крупноклеточный рак (гигантоклеточный, светлоклеточный);
- железисто-плоскоклеточный рак;
- рак бронхиальных желёз (аденокистозный, мукоэпидермоидный и др.).
Встречаются и другие, более редкие разновидности рака лёгкого — всего их не менее двадцати. Одна опухоль может содержать разные типы клеток. Если в лёгких — метастазы , то клетки, из которых они состоят, будут выглядеть, как клетки материнской опухоли.
В 40% случаев злокачественные опухоли легких представлены аденокарциномами, которые образуются из клеток, вырабатывающих слизь. Преимущественно аденокарциномы легких встречаются у курильщиков, или у людей, которые когда-то курили. Однако, у некурящих это тоже самый распространенный тип рака легкого. Кроме того, это один из распространенных видов злокачественных опухолей у молодых людей.>
Аденокарцинома – относительно медленно растущая злокачественная опухоль. Шансы обнаружить ее на ранних стадиях довольно высоки. Впрочем, это индивидуально, у некоторых пациентов такой рак ведет себя более агрессивно.
Чтобы подобрать оптимальную схему лечения для пациента с нетипичным течением заболевания мы используем международные базы данных, включающие случаи из практики ведущих онкологических клиник, результаты медицинских исследований, научные статьи. Если возникают сомнения относительно оценки проведенного гистологического анализа, мы обращаемся к нашим зарубежным коллегам: сканируем изображения гистологических срезов и отправляем в партнерскую клинику. В течение 2-5 дней мы получаем второе экспертное мнение с гистологическим заключением и вариантом схемы лечения.
Благодаря достижениям науки можно ещё до начала лечения определить чувствительность опухоли к химиопрепаратам. Молекулярный анализ позволяет разработать более эффективный план борьбы с раком лёгкого. В Европейской клинике мы используем именно такой подход: он даёт максимально хороший шанс на успех лечения.

Центральный и периферический рак
Но при выборе лечения очень важно учитывать не только тип клеток: расположение опухоли также имеет большое значение. Существуют центральный и периферический рак лёгкого. При центральном раке поражаются крупные бронхи (главные, долевые и сегментарные), при периферическом — более мелкие бронхи.
В свою очередь, выделяют четыре типа периферической карциномы легкого:
- Субплевральный узел – к этому варианту в том числе относят опухоль Панкоста.
- Внутридолевой узел.
- Диффузная и милиарная формы.
- Полостная форма.
Кроме того, отдельно выделяют медиастинальный рак – эти злокачественные опухоли в легких обычно имеют небольшие размеры, но быстро метастазируют в лимфатические узлы средостения.
Куда растёт опухоль — тоже немаловажный фактор при определении тактики лечения. Если она растёт в просвет бронха (экзофитный рак), то может частично или полностью закупорить просвет. Тогда крайне вероятно развитие вторичной пневмонии. Если опухоль растёт в толщу лёгочной ткани (эндофитный рак), это довольно долго не влияет на проходимость бронха. Также встречается разветвлённый рак — опухоль располагается вокруг бронха и равномерно сужает просвет. Чтобы окончательно составить представление о характере роста опухоли, нужно удалить ткани хирургическим путём и изучить их.
Периферический рак бывает трёх основных типов:
- круглая или узловатая опухоль;
- пневмониеподобный рак — не имеет чётких границ и по симптоматике напоминает пневмонию;
- рак верхушки лёгкого (опухоль Панкоста).
Также существуют атипичные формы, которые имеют различные особенности метастазирования. Чтобы оценить распространённость рака лёгкого, во всём мире применяется классификация по системе TNM. Благодаря ей можно систематизировать различные клинические ситуации, определить тактику лечения, а также сделать прогноз развития заболевания — и всё это, опираясь на анатомические характеристики опухоли.
Мелкоклеточный рак лёгкого
Мелкоклеточный рак лёгкого — наиболее злокачественный из всех. Такая опухоль не только быстро растёт, но и активно метастазирует. Есть и ряд других неприятных особенностей этого вида рака.
Эти ситуации нередко бывают крайне опасны для жизни человека, и без срочной хирургической помощи зачастую невозможно обойтись.
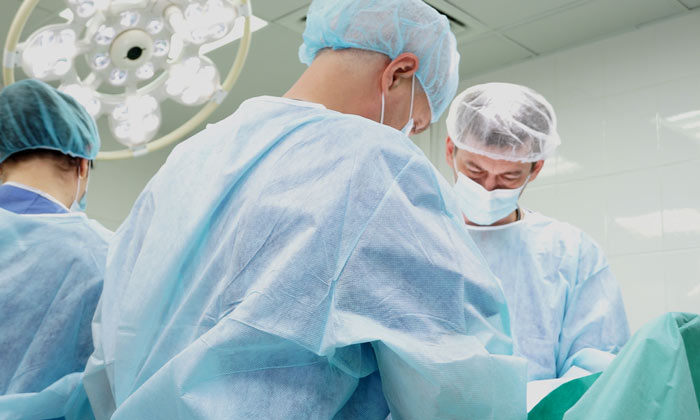
Стадии рака легкого
Стадию злокачественных опухолей легкого определяют в соответствии с общепринятой классификацией TNM:
- Буква T обозначает размеры первичной опухоли. Рядом с ней могут стоять обозначения is, 1, 2, 3 и 4. Tis – это очень небольшая опухоль, которая находится в самых верхних слоях слизистой оболочки дыхательных путей. T4 – рак, который прорастает в соседние органы.
- N – распространение рака в близлежащие лимфатические узлы. N0 означает, что очаги в лимфатических узлах отсутствуют. Цифры 1,2 и 3 характеризуют разную степень вовлеченности лимфоузлов.
- M – наличие отдаленных метастазов. К этой букве может быть приписана одна из двух цифр: 0 – отдаленных метастазов нет, 1 – обнаружены отдаленные метастазы.
Классификация по стадиям несколько различается при немелкоклеточном и мелкоклеточном раке легкого. При НМРЛ, в зависимости от характеристик T, N и M, выделяют пять стадий, их обозначают римскими цифрами:
При мелкоклеточном раке легкого также применяется система TMN, но в клинической практике более важное значение имеет деление на две стадии:
- Местно-распространенная: опухоль обнаруживается только на одной стороне, затрагивает только одну часть легкого и близлежащие лимфатические узлы.
- Распространенная: рак распространяется на другие органы, имеются отдаленные метастазы.

Как распознать рак лёгкого на ранней стадии?
Когда центральный рак лёгкого находится на ранней стадии, распознать его очень трудно. Осмотр терапевта, рентгенологические исследования — малоэффективны. Если сделать такому человеку бронхоскопию с биопсией, то правильный диагноз может быть поставлен. Иногда распознать болезнь на ранних стадиях помогает компьютерная томография.
Если рак периферический, то сделать биопсию невозможно, так как добраться до подозрительного места с помощью бронхоскопии просто не получится. Поэтому проводится трансторакальная игловая биопсия, то есть забор кусочка ткани через прокол в грудной стенке. Если очаги есть в области средостения (части грудной полости, находящейся между грудиной, позвоночником, диафрагмой, плеврой и поверхностями лёгких), проводится медиастиноскопия (осмотр с целью биопсии через разрез на шее). Иногда нельзя обойтись без диагностических торакоскопии и торакотомии (вскрытия грудной полости). Чтобы уточнить, насколько опухоль распространена, применяются самые разные диагностические методы: УЗИ, бронхоскопия, мультиспиральная компьютерная, магнитно-резонансная и позитронно-эмиссионная томография, а также радионуклидные исследования . Без этого невозможно выбрать лучший подход к лечению конкретного пациента.
Что повышает риск развития рака лёгкого?
На данный момент связь рака лёгкого и курения не подвергается никакому сомнению. Особенно это актуально для центрального плоскоклеточного и крупноклеточного рака: в 70–95 процентах случаев такие пациенты курили или курят. Международное агентство по изучению рака (International Agency for Research on Cancer) пришло к выводу, что курильщики в 10 раз чаще заболевают раком лёгкого. В табачном дыме содержится масса канцерогенных веществ. Это, в частности, полоний-210, полиароматические углеводороды (нафтиламин, 2-толуидин, бензпирен, 4-аминобифенил), никель, ряд N-нитрозосоединений и др. Чем дольше человек курит, тем выше его риски. Кроме курения, на вероятность развития рака лёгкого негативно влияют и некоторые профессиональные факторы: например, длительный контакт с асбестом и другими опасными веществами. Вероятность возникновения рака лёгкого также зависит от загрязнения воздуха канцерогенными веществами .
Возможно ли снизить риск?
Метастазы в лёгкие
Примерно у каждого пятого пациента с метастазами в лёгких возникают кашель, кровохарканье, одышка, боль в грудной клетке, повышение температуры до невысоких значений, а также потеря веса. Зачастую возникновение этих симптомов говорит о том, что процесс зашёл довольно далеко. В большинстве случаев метастазы удаётся обнаружить при рентгенологическом исследовании, которое проводится два раза в год после лечения первичной опухоли. Если найдены метастазы, необходимо провести ряд важных исследований, чтобы выбрать наиболее подходящий метод лечения. Речь идёт о компьютерной, магнитно-резонансной и позитронно-эмиссионной томографии органов грудной клетки, а также бронхоскопии.
Лечение рака легких на разных стадиях
На ранних стадиях основным видом лечения рака легкого является хирургия. Если опухоль небольшая, можно удалить небольшую часть легкого, в которой она находится – выполнить клиновидную резекцию или сегментэктомию. В большинстве же случаев выполняют лобэктомию (удаление доли легкого) или пневмэктомию (удаление всего легкого) – это помогает снизить риск того, что в легком останутся раковые клетки, из-за которых потом может произойти рецидив.
Хирургическое вмешательство может быть дополнено курсом химиотерапии, лучевой терапией. Если есть подозрение, что рак мог распространиться в близлежащие лимфатические узлы, их также удаляют.
Начиная с III стадии хирургическое удаление опухоли становится возможным не всегда. Тем не менее, у некоторых пациентов может быть выполнена циторедуктивная операция, во время которой хирург старается удалить как можно большее количество опухолевой ткани.
При неоперабельном раке легкого на поздних стадиях основными методами лечения становятся химиотерапия, лучевая терапия, иммунотерапия.
Узнайте подробнее о лечении и химиотерапии рака легкого в Европейской клинике.
Читайте также:


