Рак из матки в брюшную полость
- Брюшная полость и брюшина — что это такое?
- Виды рака брюшной полости
- Симптомы
- Осложнения
- Диагностика рака брюшной полости
- Лечение
- Прогноз и профилактика
Брюшная полость и брюшина — что это такое?
Брюшная полость — это пространство в животе, заполненное кишечником и другими внутренними органами. Сверху она ограничена диафрагмой, снизу — тазом, по бокам и спереди — мышцами брюшного пресса, сзади — позвоночником и поясничными мышцами.
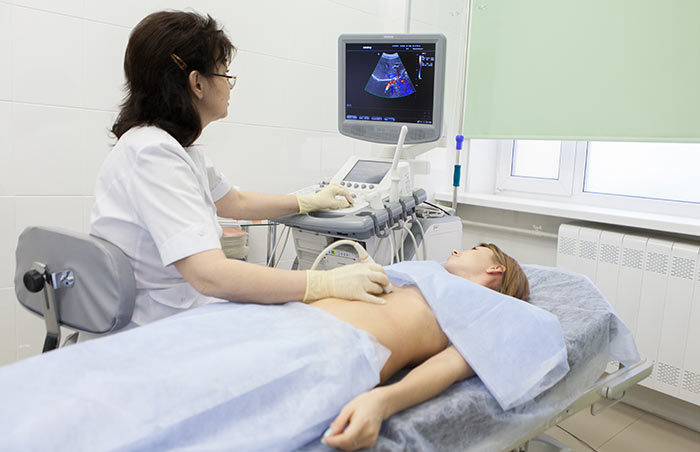
Изнутри полость живота выстилает тонкая пленка из соединительной ткани — брюшина. Ее висцеральный листок, покрывает внутренние органы, париетальный — стенки брюшной полости. Между листками брюшины находится замкнутое щелевидное пространство, а в нем — минимальное количество жидкости, выполняющей функцию смазки и обеспечивающей свободное скольжение органов. В некоторых местах брюшина образует складки: брыжейки, на которых подвешены органы, сальники.
Внутренние органы могут быть расположены по отношению к брюшине по-разному:
- Интраперитонеально — покрыты брюшиной со всех сторон.
- Мезоперитонеально — покрыты частично.
- Ретроперитонеально (забрюшинно) — покрыты только с одной стороны.
Виды рака брюшной полости
Первичные опухоли брюшной полости встречаются редко. Они бывают разных типов: мезотелиальные, эпителиальные, гладкомышечные неопределенные. Особая разновидность злокачественных опухолей брюшины — псевдомиксома. Она развивается из клеток, которые продуцируют большое количество желеобразной жидкости. Чаще всего такие опухоли распространяются на брюшину из аппендикса.
Зачастую первичные злокачественные опухоли брюшной полости имеют строение и ведут себя, как рак яичников. Они вызывают сходные симптомы, и врачи применяют для борьбы с ними примерно одни и те же методы лечения.
Известно, что в целом вероятность развития первичного рака брюшной полости выше у женщин, чем у мужчин. Риски повышаются с возрастом. Есть связь между вероятностью развития заболевания и изменениями в генах BRCA1, BRCA2.
При разных типах рака на поздних стадиях опухолевые клетки отделяются от первичного новообразования, распространяются по организму и образуют новые очаги в различных органах, в том числе в брюшной полости. Этот процесс называется метастазированием. Чаще всего в брюшину метастазирует рак толстой и прямой кишки (в 15% случаев), желудка (в 50% случаев), яичника (в 60% случаев), поджелудочной железы. Иногда метастазы распространяются из органов, которые находятся за пределами брюшной полости: молочной железы, плевры (пленки из соединительной ткани, покрывающей легкие и выстилающей стенки грудной полости), легкого.

Симптомы
Зачастую в течение длительного времени симптомы при раке брюшной полости отсутствуют, поэтому нередко его диагностируют на поздних стадиях. Проявления патологии неспецифичны, их можно легко принять за признаки других заболеваний:
- Дискомфорт, спазмы, вздутие живота.
- Повышенное газообразование в кишечнике.
- Жидкий стул.
- Запоры.
- Тошнота.
- Снижение аппетита.
- Частые мочеиспускания.
- Одышка.
- Быстрый набор или потеря массы.
- Кровотечения из прямой кишки, у женщин — из влагалища.
Если канцероматоз брюшины возник в результате метастазирования злокачественной опухоли из другого органа, сильно ухудшается прогноз. Противоопухолевая терапия начинает работать хуже, потому что многие препараты плохо проникают через брюшину.
Осложнения
Главное осложнение данного заболевания — асцит. Этим термином называют состояние, при котором в животе скапливается жидкость. В норме между листками брюшины ежедневно вырабатывается и всасывается около 1,5 жидкости. При канцероматозе нарушается отток лимфы, и жидкость всасывается хуже. Она начинает скапливаться внутри живота.
Пока жидкости немного, больной не испытывает каких-либо симптомов. Затем начинают беспокоить тяжесть, тупые боли в нижней части живота. Затрудняется дыхание, возникает одышка. Из-за того что жидкость сдавливает органы, больной жалуется на отрыжку, тошноту, проблемы со стулом и мочеиспусканием. Живот увеличивается в размерах, может возникать пупочная грыжа. При выраженном асците развивается сердечная недостаточность, отеки.
Диагностика рака брюшной полости
Злокачественную опухоль помогают выявить следующие методы диагностики:
- Ультразвуковое исследование. Зачастую его назначают в первую очередь, как простой, доступный, безопасный и в то же время информативный метод диагностики.
- Компьютерная и магнитно-резонансная томография помогают оценить состояние брюшины и внутренних органов, выявить патологические образования, оценить степень распространения рака.
- ПЭТ-сканирование в настоящее время является золотым стандартом для поиска отдаленных метастазов.
- Биопсия — самый точный метод диагностики злокачественных опухолей. Врач может получить образец опухолевой ткани во время диагностической лапароскопии — процедуры, во время которой через проколы в брюшной стенке в живот вводят миниатюрную видеокамеру и специальные инструменты. Образец отправляют в лабораторию, проводят его гистологическое, цитологическое исследование, молекулярно-генетический анализ. Это помогает не только диагностировать рак, но и установить природу опухолевых клеток, разобраться, какими препаратами с ними лучше бороться.
- Рентгеноконтрастные исследования помогают оценить состояние пищеварительного тракта, выявить опухолевые очаги и другие патологии.
- Анализ на онкомаркер CA-125 (углеводный антиген 125). Уровень этого вещества повышается в крови при раке брюшины и яичников. Но для диагностики этих заболеваний данный анализ недостаточно точен. Как правило, его применяют для контроля течения рака и эффективности лечения.
- Женщины должны пройти осмотр у гинеколога.
Обычно врачи-онкологи устанавливают диагноз на основании таких признаков, как асцит, утолщение брюшины, появление на ней узелков, смещение, сдавление петель кишки, патологические изменения со стороны печени и складок брюшины — сальников.

Лечение
Выбор тактики лечения зависит от локализации, размеров, стадии злокачественной опухоли, количества узлов. Врач также должен учитывать общее состояние больного, его возраст, наличие сопутствующих заболеваний.
Зачастую при поражении брюшины опухолевых очагов очень много, многие из них мелкие, и полностью их удалить невозможно. Хирургическое лечение направлено на удаление как можно большего числа очагов, как правило, оно предшествует химиотерапии. Обычно удаляют матку, яичники, участки кишечника, — словом, всё, что поражено злокачественной опухолью. Если злокачественное новообразование вызывает кишечную непроходимость или другие осложнения, проводят паллиативные хирургические вмешательства.
Для того чтобы уничтожить опухолевые клетки при первичном раке в полости живота, применяют химиопрепараты, зачастую те же, что при раке яичников. Лекарства вводят внутривенно или в брюшную полость — такая химиотерапия называется интраперитонеальной (внутрибрюшинной).
С 2018 года врачи Европейской клиники практикуют инновационный метод лечения канцероматоза брюшины — гипертермическую интраперитонеальную химиотерапию (HIPEC). Суть ее заключается в том, что хирург удаляет все достаточно крупные опухолевые очаги, а затем промывает полость живота подогретым раствором химиопрепарата. Это помогает уничтожить максимальное количество опухолевых клеток и существенно продлить жизнь больного.
При асците наши доктора проводят лапароцентез (прокол в брюшной стенке и выведение жидкости), устанавливают перитонеальные катетеры для постоянного оттока, проводят хирургические вмешательства, которые препятствуют дальнейшему накоплению асцитической жидкости.
На поздних стадиях проводится паллиативное лечение, которое помогает уменьшить симптомы и продлить жизнь больного.

Прогноз и профилактика
Прогноз при первичном раке брюшины напрямую зависит от того, удалось ли удалить все опухолевые очаги во время хирургического вмешательства. К сожалению, зачастую заболевание диагностируют на поздней стадии, поэтому после лечения часто развиваются рецидивы. Обычно пациентам требуется более одного хирургического вмешательства, курса химиотерапии.
Канцероматоз брюшины при метастазах других типов рака резко ухудшает прогноз. Обычно продолжительность жизни таких больных измеряется месяцами. Но HIPEC может ее существенно продлить, до нескольких лет — в случае, если проведение такого лечения возможно у конкретного пациента.
Специальных мер профилактики данного заболевания не существует. Нужно в целом вести здоровый образ жизни, женщинам — регулярно проходить осмотры у гинеколога. Мера профилактики метастазов в брюшину — своевременная диагностика и лечение злокачественных опухолей.
Средняя продолжительность жизни при карциноматозе брюшины без лечения – от 1,5 до 6 месяцев. Лечить же таких больных еще совсем недавно было нечем. Ни хирургия, ни химиотерапия не справлялись. Пациентов признавали инкурабельными (неизлечимыми). Показатель 5-летней выживаемости в начале 90-х был практически равен 0.
Но последние 20 лет активно развивается методика лечения перитонеального канцероматоза с применением HIPEC (англ. hyperthermic intraperitoneal chemotherapy) – гипертермической интраперитонеальной (внутрибрюшинной) химиотерапии. Методика дает отличные результаты: увеличивает 5-летнюю выживаемость до 40-50%, а иногда дает полное излечение.
Самое плохое – даже многие врачи не знают, что при канцероматозе существует способ продлить жизнь. Поэтому сегодня мы расскажем про HIPEC подробно: кому это поможет, какие дает результаты и сколько стоит.
Цель – уничтожить максимум опухолевых клеток, которые неизбежно останутся даже после самого тщательного хирургического удаления очагов и спровоцируют рецидив.
Свойства, которые делают HIPEC действительно уникальной методикой, мы разъясним чуть ниже, а сначала определимся, при каких диагнозах она может помочь и почему она иногда оказывается единственным способом продлить жизнь человеку на последних стадиях рака.
При каких опухолях образуется канцероматоз брюшины, и почему он так опасен
В брюшную полость распространяются многие из часто встречающихся видов рака.
- рак яичников – в 60-70% случаев приводит к канцероматозу;
- рак желудка – канцероматоз в 40-50% случаев;
- рак поджелудочной железы – в 30-40% случаев;
- рак толстой и прямой кишки (колоректальный рак) – в 10-15% случаев;
- рак печени;
- рак шейки матки;
- рак червеобразного отростка (аппендикса);
- редкие первичные опухоли брюшины (мезотелиома и псевдомиксома).
Все эти злокачественные новообразования распространяют раковые клетки либо когда первичная опухоль физически прорастает в брюшную полость, либо вместе с током крови и лимфы – иногда это происходит во время хирургических операций по поводу первичных опухолей.
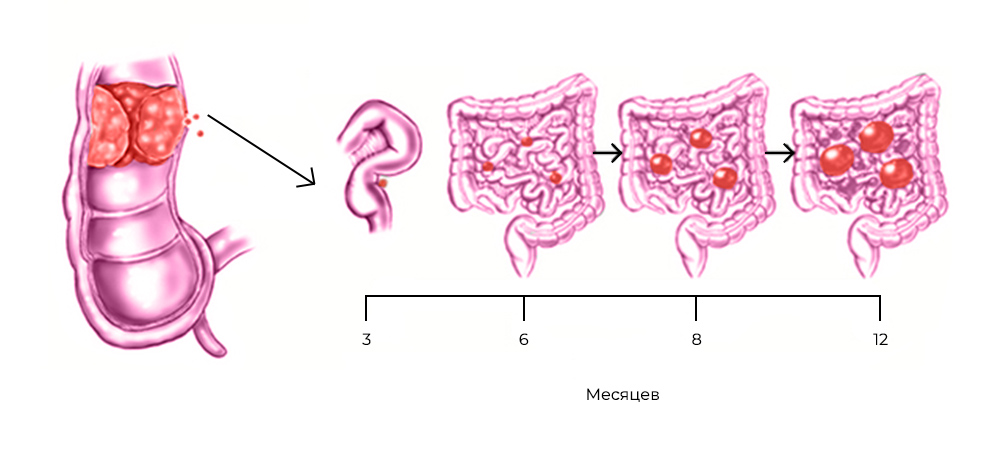
Развитие канцероматоза при колоректальном раке: из прямой кишки в брюшную полость
Стоит раковым клеткам попасть в полость, ограниченную брюшиной – они, скорее всего, дадут начало вторичным опухолям, метастазам. Перитонеальная ткань – богатый источник факторов роста и комфортная среда для их развития. Микроскопические метастазы распространяются по поверхности брюшины, поражают внутренние органы.
Метастазы нарушают кровоток и лимфоток, лишают внутренние органы питания и пространства, зачастую становятся причиной непроходимостей (например, кишечной, или сдавливают мочеточники). Кроме того, это провоцирует асцит – выпот и скопление жидкости в брюшной полости – наиболее распространенный симптом при канцероматозе.
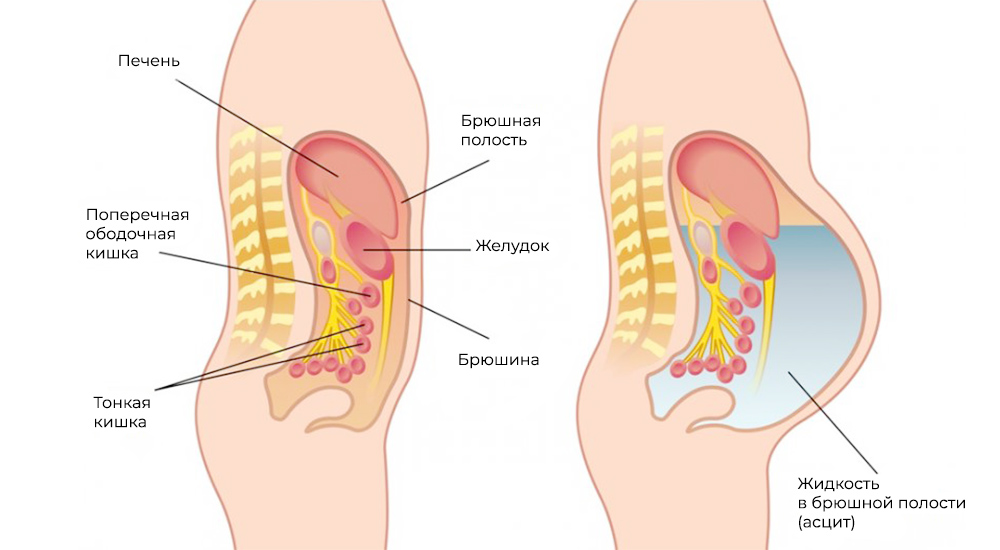
Асцит – скопление жидкости в брюшной полости
Застой крови и лимфы, интоксикация, сдавление внутренних органов метастазами и/или скопившейся жидкостью при асците – это причины, почему пациенты с канцероматозом без лечения не проживают и года.
На протяжении почти всей истории онкологии считалось, что перитонеальный карциноматоз и опухоли брюшины не поддаются никакому из существующих видов лечения.
Лучевая терапия в лечении канцероматоза не применяется, поскольку высокие дозы облучения такой обширной области живота опасны для пациента еще более серьезными осложнениями.
Хирургическое лечение малоэффективно, т.к. метастазы на поверхности брюшины могут быть микроскопического размера, либо расположены в недоступных местах, и врач не видит их во время операции. А для быстрого рецидива канцероматоза достаточно и единичных раковых клеток, оставшихся в полости брюшины.
Системная химиотерапия почти не дает чувствительного воздействия на опухоли брюшины –опухолевые очаги размером до 3 мм (таких при канцероматозе большинство) практически не развивают систему собственных кровеносных сосудов – и поэтому слабо доступны для системной внутривенной химиотерапии.
Вводить химиотерапию в более высоких дозах, чтобы повысить концентрацию препаратов в перитонеальной области – невозможно, т.к. это может необратимо навредить остальным органам и тканям, до которых доберется перенасыщенный химиопрепаратом кровоток.
Во второй половине 20 века появились первые работы, рассказывающие о возможностях применения внутрибрюшинной химиотерапии. Последние 20 лет это направление активно развивается, а создал его еще в 80-х годах XX века американский хирург-онколог Пол Шугабейкер – он первым придумал совместить циторедуктивную операцию с горячей химиотерапией, вводимой непосредственно в брюшную полость. И это дало результат
Гипертермия – это повышение температуры.
- Высокая температура сама по себе способна вызывать повреждение и гибель опухолевых клеток. К тому же, делает их более уязвимыми для действия химиопрепаратов: усиливает проницаемость клеточных мембран.
- Причем чувствительность увеличивается избирательно – опухолевые клетки начинают гибнуть при температуре 40 °C, а здоровые – сохраняются до 44°C. В условиях гипертермии особенности опухолевых тканей (иное кровоснабжение, степень оксигенации, особенности репарации ДНК) становятся для них не преимуществом, а слабым местом.
- Кроме того, повышение температуры обычно вызывает иммунную реакцию: растет количество лимфоцитов – клеток иммунитета, способных уничтожать опухолевые клетки. В плазме крове увеличивается уровень интерлейкинов, интерферонов, факторов некроза опухоли и т.д. Все они имеют собственную противоопухолевую активность, и дополнительно способны усиливать эффект некоторых химиопрепаратов.
- Еще один важный плюс гипертермии – она способствует более активному проникновению препарата в ткани – на глубину до 3 мм – этого хватит, чтобы охватить большинство микро-метастазов, которые останутся после хирургической операции.
Внутри брюшины – химиотерапия работает лучше. Для HIPEC используются стандартные химиопрепараты, но их локальное применение при перитонеальном карциноматозе – куда эффективнее.
Процедура HIPEC – это, строго говоря, вторая половина целого комплекса мероприятий. Без циторедуктивной хирургической операции HIPEC может проводиться в считанном количестве случаев по особым показаниям. Обычно процедура – продолжение хирургической операции, которое дает серьезное улучшение прогноза выживаемости.
Вместе с удалением опухолевых очагов, все вмешательство занимает от 6 до 18 часов. Процесс можно разделить на 4 этапа.
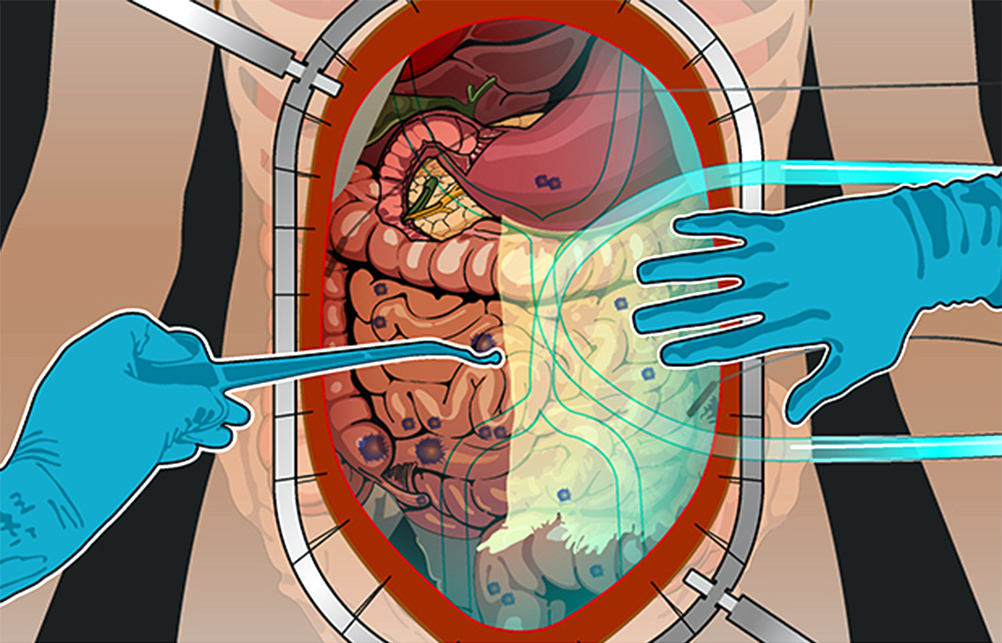
1) Ревизия брюшной полости. Проводится она для того, чтобы понять, показано ли лечение с помощью HIPEC для этого пациента, принесет ли оно увеличение продолжительности жизни и улучшение ее качества. Во время ревизии хирург внимательно осматривает брюшную полость и определяет перитонеальный индекс рака (peritoneal cancer index – PCI).
Чтобы его рассчитать, брюшную полость и тонкую кишку условно делят на 13 областей-квадрантов, в каждом из них оценивают самый крупный опухолевый очаг по шкале от 0 до 3:
- очагов не обнаружено — 0 баллов;
- очаги размером менее 0,5 см — 1 балл;
- очаги размером менее 0,5–5 см — 2 балла;
- очаг более 5 см или несколько узлов меньшего размера— 3 балла.
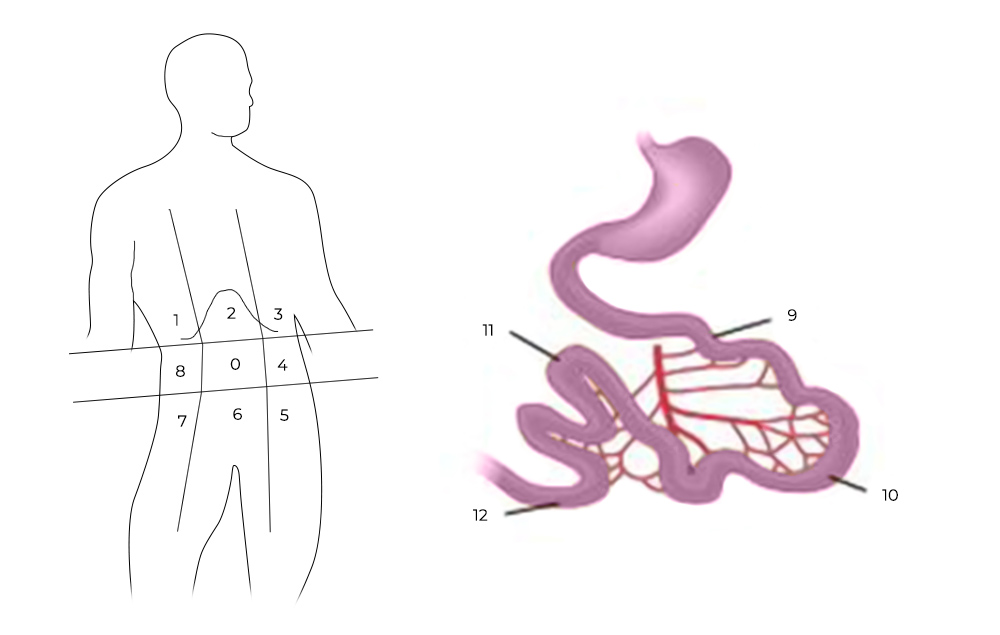
Разделение брюшной полости на участки для определения PCI
Баллы суммируются по всем квадрантам – это и есть значение PCI. Чем больше баллов – тем хуже прогноз. Если PCI выше критического (принимая во внимание тип опухоли и состояние пациента) – то и операцию, и процедуру HIPEC могут признать нецелесообразными.
Проводят ревизию интраоперационно – т.е. непосредственно перед проведением основной операции. В некоторых случаях ее можно провести в виде отдельной диагностической лапароскопической операции – малотравматичной, через небольшие проколы в стенке живота.
2) Циторедуктивная операция. Если по результатам ревизии PCI оценен как удовлетворительный, то хирург приступает к удалению всех видимых и пальпируемых (те, что чувствуются наощупь) опухолевых узлов.
Удаляют отдельные участки брюшины, орган, в котором находится первичная опухоль, соседние внутренние органы или их части, если они тоже поражены метастазами. Часто это участки кишечника, селезенка, желчный пузырь.
3) Гипертермическая интраперитонеальная химиотерапия. Собственно, HIPEC. В брюшную полость вводят катетеры и температурные датчики, соединенные со специальным аппаратом и емкостью с раствором химиопрепарата. Эта перфузионная система (под контролем врачей, конечно) поддерживает заданную температуру и давление циркулирующей жидкости. Раствор химиопрепарата в течение 60–90 минут циркулирует в брюшной полости пациента.
После процедуры препарат удаляют из брюшной полости, промывают ее физраствором, удаляют датчики и катетеры.
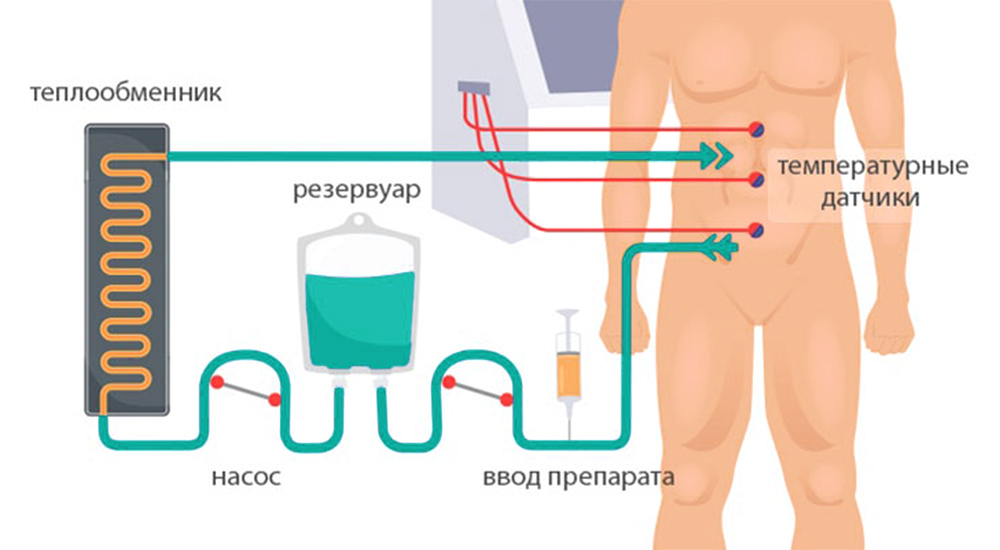
Схема проведения HIPEC
4) Реконструктивная операция. Если удалены части кишечника, хирург восстанавливает непрерывность кишки – формирует анастомоз, выводит верхний конец толстой/тонкой/слепой кишки на поверхность живота для отхождения каловых масс.
В среднем, в клинике пациент проводит 2-4 недели. Через 2-3 недели после операции проводится контрольное обследование. Его необходимо повторять через 3 месяца, и постепенно частоту проверок снижают до 1 раза в год.
В этом видео наши коллеги проводят процедуру HIPEC пациентке с раком яичников.
Как любое лечение, HIPEC имеет риски и противопоказания
Послеоперационный период стоит отдельным этапом, но он не менее важен. Мы всегда понимаем, насколько сложным для наших пациентов (а многие попадают к нам в крайне тяжелом состоянии) может быть период восстановления после такого длительного и достаточно агрессивного вмешательства, как циторедуктивная операция + HIPEC. Поэтому сразу после операции мы переводим пациента в отделение интенсивной терапии, под круглосуточное наблюдение.
Осложнения могут быть те же, что и после любого хирургического вмешательства на брюшной полости, поэтому за пациентом внимательно следят на случай появления признаков кровотечения или воспаления послеоперационной раны – и готовы в любую минуту оказать помощь.
Побочные действия от химиотерапевтического препарата при внутрибрюшной гипертермической химиотерапии даже менее выражены, чем при внутривенном введении – при том, что дозировки, а значит, и противоопухолевое действие, при HIPEC в десятки раз выше.
К сожалению, при всем нашем желании и мастерстве наших хирургов, есть пациенты, для которых полезный эффект вмешательства не оправдает сложностей послеоперационного восстановления.
Чтобы циторедуктивная операция с последующей процедурой HIPEC была эффективной, нужно соблюдение нескольких условий:
- Пациент должен быть в состоянии перенести и хирургическую операцию, и химиотерапию одновременно. Возраст или показатели здоровья не должны этому препятствовать – например, не должно быть почечной или печеночной недостаточности. Перед процедурой мы обязательно всесторонне обследуем пациента.
- Процесс распространения метастазов должен быть ограничен только брюшной полостью. Если есть метастазы в других органах, которые нельзя удалить – они будут распространяться дальше, и сведут эффект HIPEC на нет.
- Метастазы размером более 2,5 мм не должны покрывать всю поверхность брюшины – удалить их все будет невозможно.
Мы провели ей циторедуктивную операцию и процедуру HIPEC, и после этого она уже 10 месяцев живет без прогрессирования заболевания.
В некоторых случаях HIPEC приводит к устойчивому излечению. Например, коллеги из США сообщали о женщине с мезотелиомой брюшины. С помощью HIPEC она преодолела болезнь, уже 3 года живет без признаков рака и смогла родить ребенка.

Jessica Blackford-Cleeton, которой HIPEC позволила выжить и стать мамой.
К сожалению, HIPEC пока применяется в считанном количестве клиник. Причин этому несколько, и они характерны для всех новых технологичных способов лечения.
- Методика все еще считается инновационной, не все врачи имеют нужный опыт работы. К тому же, для проведения процедуры нужен не 1 и не 2, а целая бригада медиков самой высокой квалификации – это длительная, сложная и напряженная операция.
- Оборудование дорогое, не все страны и не все клиники могут потратиться на перфузионную систему и расходные материалы.
- Врачи бывают довольно консервативны. Кто-то считает, что процедура требует более подробного изучения. А кто-то из них не любит участвовать в проведении гипертермической химиотерапией, потому что опасается за собственное здоровье – испарения химиопрепаратов во время HIPEC могут быть вредными для медиков, которые при этом присутствуют. Хотя, в целом, испарения из закрытого контура минимальны, негативные последствия, даже если есть – не являются необратимыми, врачу нужно лишь более внимательно следить за состоянием почек и печени.
Однако более 70 ведущих хирургов-онкологов из 55 онкоцентров в 14 странах мира, включая США (где и родилась эта процедура), Канаду, Францию и Великобританию, пришли к выводу о том, что HIPEC может существенно повысить ожидаемую продолжительность жизни у пациентов, страдающих канцероматозом, особенно при колоректальном раке.
Клинические исследования из разных стран показывали результаты, когда пациенты после лечения канцероматоза брюшины с применением HIPEC жили 7 лет при опухолях аппендикса, более 5 лет при мезотелиоме брюшины, 5 лет при колоректальном раке, 2 года при раке яичников – тогда как при стандартном лечении их выживаемость колебалась от 2 до 14 месяцев.
Мы в свою очередь убедились в эффективности HIPEC на собственном обширном клиническом опыте. Мы надеемся, что через несколько лет HIPEC будет внедряться в стандарты лечения по ОМС и станет доступна по всей стране. А пока – мы даем пациентам возможность не искать подобную помощь за рубежом, а получить ее в Москве.
Что такое метастазы?
Именно из него впоследствии с током лимфы и крови начнется диссеминация, или распространение, злокачественных элементов, которые проникнут в другие органы и ткани, давая толчок формированию метастазов. Получается, что метастатический рак — осложнение онкозаболевания.
Брюшная полость человека представлена щелевидным пространством, в котором содержится определенное количество серозной жидкости, необходимое для естественного увлажнения внутренних органов. Серозная оболочка, покрывающая стенки брюшной полости, называется брюшиной. Она может растягиваться во время беременности, роста доброкачественного или злокачественного новообразования, воспалительных процессов, к примеру, водянки.
Серозная оболочка, увлажняя органы брюшной полости, способствует их двигательной активности и препятствует сращиванию друг с другом. Первичный рак в этой области практически не развивается, исключением являются женские половые органы — яичники, или придатки. Метастазы в брюшине имеют собственный код по классификации МКБ-10: С48.2 Злокачественное новообразование брюшной полости и забрюшинного пространства неуточненной локализации.
Другие причины гинекологических опухолей
В зависимости от типа опухоли, пик заболеваемости приходится на разные возрастные группы. Так, рак шейки матки чаще поражает молодых женщин. А онкология яичников обычно встречается у пациенток в период менопаузы. Опухоль яичников у женщин при менопаузе заканчивается удалением органов.
Клиническая картина и симптомы
В начальной стадии рак брюшной полости не проявляется какими-либо субъективными симптомами. Только когда злокачественное новообразование начинает расти (около 5 см), формируется клиническая картина, состоящая из симптомов:
- Болевые ощущения в области живота – в брюшной полости расположено много нервных окончаний. При росте опухоли нервные окончания затрагиваются, вызывая боль.
- Увеличение живота в объеме – опухоль вырастает до больших размеров. В брюшине может начать накапливаться жидкость.
- Оттек ног, живота, области гениталий – является серьезным осложнением.
- Быстрый набор в весе – происходит за счет чрезмерного накопления жидкости в брюшине.
- Чувство насыщения (даже если было съедено немного) – связано с кишечной непроходимостью. У пациента может наблюдаться рвота, в ее массе находится пища, съеденная несколько дней назад. Пища не переваривается и остается в желудке.
- Похудение (характерно для саркомы забрюшного пространства) – пациент может потерять в течение двух-трех месяцев около 10 кг своего веса. Симптом относиться ко всем злокачественным процессам.
- Высокая утомляемость – связана с поражением печени. Нарушается работа нервной системы. Это приводит к заторможенности пациента, сонливости.
- Кишечная непроходимость (регулярная) – связано с тем, что опухоль разрастается до больших размеров и закупоривает кишечник. Если не выполнить своевременного вмешательства – это приведет к смерти пациента.
Эпителиальный рак брюшины состоит из четырех стадий. Они распределены в зависимости от зоны распространения патологии и размера опухоли:
- Болезнь ограничивается яичниками – бессимптомно.
- Рак распространяется за пределы яичников, но остается в пределах малого таза – бессимптомно.
- Патология распространилась на выстилку брюшины – могут проявляться вышеперечисленные симптомы.
- Болезнь распространилась на близкие и дальние органы – пациент ощущает проявления болезни и ее осложнения, которые приводят к смерти.
Обзор
Рак желудка — один из самых распространенных типов рака. Его признаками может быть длительные проблемы с пищеварением, снижение массы тела и общее недомогание.
Существует несколько различных типов рака желудка. В 95% случаев встречается аденокарцинома — рак слизистой оболочки. Реже встречаются лимфома желудка — опухоль, растущая из лимфатической ткани и гастроинтестинальная стромальная опухоль — из мышечной и соединительной тканей стенки живота.
Не все виды рака желудка поддаются лечению. Но даже в запущенных случаях можно облегчить симптомы и улучшить качество жизни при помощи химиотерапии, лучевой терапии и хирургической операции. Наилучшие результаты лечения рака желудка дает хирургическое вмешательство. До и после хирургического вмешательства иногда используют химиотерапию, чтобы уменьшить размер опухоли или предотвратить появление новых злокачественных клеток.
Прогноз при раке желудка зависит от возраста, общего состояния здоровья человека, масштабов распространения опухоли и других факторов. К сожалению, большая часть новообразований желудка диагностируется уже на поздних стадиях, поэтому перспективы лечения этого типа рака хуже, чем злокачественных опухолей других органов. Пятилетняя выживаемость у людей с раком желудка составляет около 15%. 11% людей живут с диагнозом рака желудка не менее 10 лет.
Рак желудка и последствия операции сильно снижают качество жизни. Однако существуют различные виды социальной, психологической и финансовой помощи для больных злокачественными новообразованиями.
Желудок — это полый мышечный мешковидный орган, расположенный между пищеводом и начальным отделом кишечника — двенадцатиперстной кишкой.
Основная функция желудка — подготовка пищи к перевариванию и усвоению в кишечнике, расщепление твердой пищи до полужидкого состояния под действием желудочного сока.
Образование в брюшной полости
Опухоли органов брюшной полости, требуют детального физического исследования.
Подлежат обязательной идентификации увеличенная левая доля печени, измененная почка (блуждающая, подковообразная и дистопированная с тазовым расположением, при гидронефротической трансформации), переполненный мочевой пузырь, увеличенные мезентериальные ЛУ абсцессы и грыжевые выпячивания. Даже пальпаторно определяемый привратник требует проведения детального обследования для исключения рака выходного отдела желудка.
5 основных задач при обследовании больного с образованием в брюшной полости:
- По возможности точное определение органа, из которого исходит опухоль;
- Диагностика вызываемых опухолью функциональных расстройств;
- Определение анатомического характера опухоли;
- Выявление оказываемого опухолью воздействия на весь организм;
- Решение вопроса о резектабельности опухоли.
Место расположения внутри- и забрюшинных опухолей определяют у лежащего на спине больного (со слегка приподнятой головой и полностью расслабленной мускулатурой всего тела) с учетом топографоанатомической схемы отделов брюшной полости.
Самый нижний отдел брюшной полости (находящийся в малом тазу) содержит мочевой пузырь, прямую кишку, петли тонкой кишки, внутренние женские половые органы, предстательную железу и семенные пузырьки. Указанная схема имеет лишь сугубо ориентировочное значение, поскольку даже в норме возможно выхожение того или иного органа в соседний отдел.
Образования в передней брюшной стенке
Опухоли брюшной стенки могут исходить из всех ее тканей. К доброкачественным опухолям передней брюшной стенки относят липому, фибролипому, нейрофиброму, рабдомиому; все они (за исключением липом) наблюдаются редко. Из злокачественных опухолей следует назвать фибросаркому и метастазы рака других локализаций.
Образования в брюшной стенке, располагаясь более поверхностно, обычно легко распознаются уже при осмотре. Пальпаторно они мало смещаемы и, сопровождая движения брюшной стенки, втягиваются или выпячиваются, опускаются вниз и поднимаются вверх вместе с ней. Для подтверждения их связи с брюшной стенкой больному предлагают немного приподняться на локтях и в таком положении прощупывают место их расположения — при сокращении мышц эти опухоли определяются хуже, но не исчезают. Опухоли, располагающиеся в животе, при напряжении мышц передней брюшной стенки перестают определяться.
Своеобразной и характерной доброкачественным образованием в передней брюшной стенке является десмоид (desmoideum; десмо греч. — eides — подобный; син.: десмома, опухоль десмоидная, фиброма десмоидная, фиброма инвазивная, фиброматоз агрессивный) — соединительнотканное новообразование, развивающееся из сухожильных и фасциально-апоневротических структур, характеризующееся инфильтративным ростом.
Эта опухоль, встречаясь нечасто, развивается преимущественно у молодых (25-35 лет) женщин в послеродовом периоде. Излюбленной локализацией десмоидных опухолей служат нижнебоковые отделы передней стенки живота. Иногда вместе с опухолью прощупывается ножка — тяж, идущий к передневерхней ости подвздошной кости. Реже десмоид локализуется в эпигастрии (проекция прямых мышц живота). Опухоли встречаются и у мужчин.
Признаки и симптомы рака брюшины
Первичный перитонеальный рак проявляется по-разному. Пациенты со злокачественными мезотелиомами брюшной полости обычно испытывают следующие симптомы:
- боли в животе;
- быстрое похудение;
- асцит;
- кровотечения, рвота с кровью;
- вздутие живота;
- отрыжка;
- зловонный запах изо рта;
- ощущение переполненности живота;
- расстройства пищеварения;
- поносы, запоры.
Саркомы, как наиболее опасный вид опухолей, тем не менее, часто протекают бессимптомно. Средний возраст пациента с забрюшинной саркомой – примерно 50 лет. И мужчины, и женщины одинаково склонны к развитию этого типа опухолей. Обычно такие саркомы имеют размеры до 5 см. Если опухоль начинает расти, появляются и симптомы. Основные из них:
- быстрое насыщение при употреблении пищи;
- желудочно-кишечные обструкции;
- отек нижних конечностей;
- боль в животе;
- рвота.
Если опухоль имеет крупный размер, она может давить на почку (в зависимости от стороны расположения). В обязательном порядке после обнаружения рака брюшины онколог проверяет пациента на наличие других опухолей внутренних органов: почек, поджелудочной железы, надпочечников, половых органов. Важно установить, первичная опухоль или вторичная. От этого зависят и методы лечения, и прогноз, и общее состояние здоровья пациента.
Стадии рака желудка
Рак желудка делят на ранний (начальный) и распространенный. При раннем опухоль не прорастает глубже слизистой оболочки и подслизистой основы. Такие опухоли проще удалить (в том числе эндоскопическим путем), при них лучше прогноз. Также используют классификацию TNM, которая учитывает размеры и прорастание в разные ткани первичной опухоли (T), метастазы в регионарных (близлежащих) лимфатических узлах (N), отдаленные метастазы (M).
Классификация в зависимости от состояния первичной опухоли (T):
- Tx – первичную опухоль невозможно оценить;
- T0 – первичная опухоль не обнаруживается;
- T1 – тяжелая дисплазия клеток слизистой оболочки, опухоль находится в поверхностном слое слизистой оболочки (“рак на месте”);
- T2 – опухоль проросла в мышечный слой стенки органа;
- T3 – рак достиг серозной (наружной) оболочки желудка, но не пророс в нее;
- T4 – опухоль проросла в серозную оболочку (T4a), в соседние структуры (T4b).
Классификация в зависимости от наличия поражения в регионарных лимфатических узлах:
- Nx – невозможно оценить метастазы в лимфатических узлах;
- N0 – метастазы в регионарных лимфоузлах не обнаружены;
- N1 – поражены 1-2 лимфоузла;
- N2 – опухолевые клетки распространились в 3-6 лимфоузлов;
- N3 – метастазы в 7-15 (N3a) или в 16 и более (N3b) лимфоузлах.
Классификация в зависимости от наличия отдаленных метастазов:
- M0 – отдаленные метастазы не обнаружены;
- M1 – обнаружены отдаленные метастазы.
Аденокарциному делят на 4 стадии:
- I стадия (T1M0N0 – стадия Ia; T1N1M0, T2N0M0 – стадия Ib). Опухоль находится в пределах слизистой оболочки и подслизистой основы, не прорастает вглубь стенки желудка. Иногда раковые клетки обнаруживают в близлежащих лимфатических узлах.
- II стадия (T1N2M0, T2N1M0, T3N0M0 – стадия IIa; T1N3aM0, T2N2M0, T3N1M0, T4aN0M0 – стадия IIb). Опухоль прорастает в мышечный слой стенки желудка и распространяется в лимфатические узлы.
- III стадия (T2N3aN0, T3N2M0, T4aN1M0, T4aN2M0 – стадия IIIa; T1N3bM0, T2N3bM0, T3N3aM0, T4aN3aM0, T4bN1M0 – стадия IIIb; T3N3bM0, T4aN3bM0, T4bN3aM0 – стадия IIIc). Рак пророс через всю стенку желудка и, возможно, распространился на соседние органы, успел сильнее поразить близлежащие лимфатические узлы.
- IV стадия (любые T и N, M1). Есть отдаленные метастазы.
Терапия
При подтверждении болезни, пациенту с онкологией брюшной полости незамедлительно назначается лечение. Основой лечения остается хирургическое вмешательство, его дополняют другие методы.
- Удаление опухоли – проводится полостная операция, в результате которой удаляются очаги болезни, включая метастатические узлы. Брюшную мембрану обрабатывают специальным раствором.
- Лучевая терапия – выполняется в сочетании с полостной операцией. Проводится курс до хирургического вмешательства и после него.
- Химиотерапия – часть комплексного лечения. При невозможности проведения операции проводят паллиативную химиотерапию.
- Иммунотерапия – вводятся специальные препараты, которые в короткие сроки активизируют защитные свойства в организме.
- Промывание брюшной полости – проводится обработка специальным раствором. Его температура должна быть 40° С. Манипуляция относится к сложнейшим процедурам. Врач-онколог должен быть высококвалифицированным специалистом.
В этом видео показано, как выкачивают жидкость из брюшной полости:
Читайте также:

