Рак двенадцатиперстной кишки клинические рекомендации

По раку двенадцатиперстной кишки не создано клинических рекомендаций в онкологии, но их удостоилась анатомически крошечная её структурная часть — дуоденальный большой или фатеров сосочек, в который открывается общий для желчи и панкреатических ферментов проток.
Традиционно все серьёзные дуоденальные заболевания автоматически рассматриваются вместе с патологий желудка, хотя двенадцатиперстная — начальная часть кишечника, а с желудком 12-перстную объединяет только анатомическая близость.
- Анатомия двенадцатиперстной кишки
- Причины рака двенадцатиперстной кишки
- Диагностика рака двенадцатиперстной кишки
- Стадии двенадцатиперстного рака
- Прогноз при дуоденальной аденокарциноме
- Как проявляется рак двенадцатиперстной кишки
- Лечение рака двенадцатиперстной кишки
Анатомия двенадцатиперстной кишки
Задача у двенадцатиперстной одна — получив обработанную кислотой желудочного сока пищевую массу, смешиванием с желчью и панкреатическими ферментами подготовить её к вхождению в щелочную среду кишечника.
Похожий на подкову отрезок пищеварительной трубки — длиной всего 12 перстов или пальцев (в поперечнике), соединяется с желудком луковицей, снаружи к 12-перстной плотно прилежит поджелудочная железа.
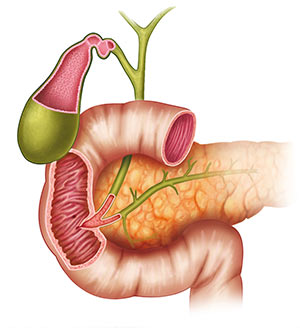
Луковица двенадцатиперстной названа так за большое сходство, и складки слизистой тоже как у лука — сверху вниз, тогда как в остальных отделах кишечника преимущественно поперечные. В луковице кислый желудочный секрет смешивается с щелочным кишечным и именно здесь чаще всего зарождаются язвы, а злокачественные опухоли, наоборот, развиваются редко — у каждого седьмого из всех страдающих дуоденальными карциномами.
Далее нисходящая часть с открывающимися в неё сосочком панкреатическим и общим желчным протоками, в этот отдел поступает выработанная печенью желчь и агрессивные панкреатические ферменты. В двух из трех случаев именно в этой части двенадцатиперстной развивается злокачественный процесс.
Далее идут горизонтальная и восходящие части, частота злокачественной опухоли тоже идёт по нисходящей — новообразования в этих отделах довольно редки.
Причины рака двенадцатиперстной кишки
Считается, что причины развития злокачественной опухоли 12-перстной кишки почти такие же, как у рака желудка, о них тоже мало известно.
- Предполагается связь с хеликобактерной инфекцией. Ассоциированные с бактерией язвы в 12-перстной встречаются чаще — в восьми из десяти случаев, тогда как в желудке только у шести больных. Язвенная болезнь вчетверо чаще поражает дуоденальную слизистую, нежели желудочную. Болеют дуоденальными язвами преимущественно женщины, а язвой желудка — мужчины.
- Замечена связь рака 12-перстной с ожирением.
- Есть предположение о влияние национальных особенностей питания, не доказанное статистикой.
По большому счёту — ясности нет ни с причинами желудочного рака, тем более с первопричинностью дуоденальных карцином.
Диагностика рака двенадцатиперстной кишки
Злокачественные новообразования справедливо относят к болезням старения, абсолютное большинство пациентов уже встретило свой 65 день рождения, у женщин процесс возникает лет на 5–10 позже.
Российская онкологическая статистика про карциному 12-перстной кишки молчит, никто не знает числа заболевших и не анализирует характеристики пациентов по стадиям на момент выявления. В зарубежье дела обстоят ничуть не лучше.
Как проверить двенадцатиперстную кишку на рак? Так же, как и желудок — сделать ФГДС или фиброэзофагогастродуоденоскопию. При гастроскопии по любой желудочной проблеме обязательно осматривается двенадцатиперстная, с подозрительных участков берётся биопсия. При патологии желчевыводящих путей и поджелудочной железы также в первую очередь обследуется 12-перстная кишка.
Очень эффективна комплексная диагностика — сочетание эндоскопии с УЗИ или эндосонография, позволяющие увидеть всю толщину кишечной стенки.
Доступно и рентгенологическое исследование в разных проекциях — полипозиционное с контрастированием. Прекрасно выявляет патологию КТ, а вот лапароскопия, в отличие от карциномы желудка, используется не всегда, а только при продвинутых стадиях.
Стадии двенадцатиперстного рака
В подавляющем большинстве в дуоденальной стенке развивается слизистая аденокарцинома, анатомические особенности позволяют диагностировать её на ранних стадиях.
Стадирование базируется на степени вовлечения кишечной стенки в злокачественный процесс и наличии метастазов в лимфатическом коллекторе:
- Опухоль в пределах слизистой оболочки — 1 стадия;
- Новообразование в пределах стенки с метастазированием в лимфатические узлы рядом с органом — 2 стадия;
- Прорастание раком кишечной стенки с выходом в брюшную полость и вовлечение рядом находящихся анатомических структур — 3 стадия;
- При любом размере опухолевого поражения дуоденальной стенки появление метастазов в других органах — безоговорочно устанавливается 4 стадия.
Прогноз при дуоденальной аденокарциноме
В общем у большинства пациентов прогноз заболевания хороший, потому что и метастазы в ближайшие к органу лимфатические узлы находят только у каждого седьмого больного и рецидивы после лечения карциномы очень нечасты.
Выявление на ранней стадии — залог долгой жизни пациента, после операции 80% переживают первую пятилетку.
Как проявляется рак двенадцатиперстной кишки
Признаки раннего рака малозаметны и не отличаются от симптомов любого другого желудочного заболевания:
- непонятный дискомфорт,
- несвязанные с приёмами пищи неясные боли в подложечной области,
- эпизодическое подташнивание,
- периодический метеоризм.

Клинические проявления новообразования в 12-перстной в большинстве случаев обусловлены сужением или полным перекрытием просвета пищеварительной трубки:
- При локализации опухоли в начальном отделе на первый план выходят симптомы стеноза выходного отдела желудка: постоянное переполнение и перерастяжение его застоявшейся пищей, рвотой недавно съеденным.
- При расположении карциномы в нисходящей части первым симптомом может стать механическая желтуха вследствие блокирования оттока желчи по общему протоку, а также клинические признаки острого панкреатита.
- При поражении нижней части 12-перстной или полной обтурации просвета кишечника на любом уровне может развиться клиника кишечной непроходимости: прогрессивно ухудшающееся состояние со зловонными рвотами и отсутствием стула более 3 дней, нарастанием интоксикации.
- Прорастание всей толщи кишечной стенки может манифестировать кровотечением с черным поносом и коричневой рвотой на фоне прогрессирующей слабости.
- Вовлечение поджелудочной железы в опухолевый конгломерат осложнится выраженным болевым синдромом, похожим на симптомы острого панкреатита.
- При метастатической стадии симптомы отражают локализацию очагов в органах и тканях, с параллельно прогрессирующей потерей веса и нарастающей слабостью.
Лечение рака двенадцатиперстной кишки
Радикальное лечение включает операцию с удалением поражённого дуоденального сегмента с прилежащими тканями — гастропанкреатодуоденальная резекция или полное удаление всего органа — панкреатодуоденэктомия.
Во всех ситуациях вместе с 12-перстной единым блоком удаляется выходной отдел желудка, головная часть поджелудочной железы с клетчаткой, где расположены лимфатические узлы.
Стандарт лечения аденокарциномы 12-перстной не разработан, поэтому ориентируются на лечебный подход при раке желудка, так при сомнительной операбельности проводят несколько курсов химиотерапии с включением фторурацила и платиновым производным.
Нет доказательств безусловной эффективности профилактической химиотерапии после операции по поводу 2–3 стадии, тем не менее при низкодифференцированной аденокарциноме или большом поражении такое лечение возможно, но не раньше, чем через 6–8 недель после хирургического вмешательства при полном заживлении раны.
Рак двенадцатиперстной кишки не относится к онкологическим раритетам с заболеваемостью один-два на миллион, но исследователи уделили ему недостаточно внимания и не разработали стандартного подхода, дающего наилучший результат у подавляющего большинства пациентов.
Для каждого больного дуоденальной карциномой разрабатывается персональная программа лечения с учётом всего известного о морфологии рака, поэтому требуется внимание к деталям и отличное знание научного материала, что для нашей клиники абсолютная норма клинической практики.
Рак двенадцатиперстной кишки — это редкая злокачественная опухоль (аденокарцинома) развивающаяся из клеток дуоденального эпителия. Хотя большая часть случаев рака тонкого кишечника приходится именно на 12-перстную кишку (55,7%), дуоденальная аденокарцинома (ДА) в итоге составляет менее 1% всех онкопатологий желудочно-кишечного тракта. В целом, по сравнению с некоторыми другими периампуллярными злокачественными опухолями, ДА имеет более благоприятный исход. Она с большей вероятностью поддается лечащей резекции и имеет более благоприятные отдаленные результаты.

Причины возникновения и факторы риска
Причинные факторы развития дуоденального рака не определены. Достоверных факторов риска два.
- Полипы двенадцатиперстной кишки достоверно связаны с высоким риском развития ДА.
- Наследственные факторы, такие как семейный аденоматозный полипоз и синдром Гарднера почти всегда приводят к возникновению дуоденального рака.
Диетические факторы, такие как увеличение потребления хлеба, макаронных изделий, сахара, красного мяса или снижение потребления фруктов и овощей можно отнести к относительным факторам риска развития аденокарциномы тонкой кишки, так же как и колоректального рака. Прием алкоголя, кофе и употребление табака также факторы риска для онкозаболеваний кишечника.
Тем не менее, значимость этих ассоциаций невелика, и большинство случаев ДА не связаны ни с какими известными причинами или факторами риска.
Признаки и симптомы
Рак двенадцатиперстной кишки симптомы не проявляет до момента достижения опухолью определенного размера.
А когда первые признаки рака двенадцатиперстной кишки появляются, они неспецифичны и включают:
- боль в животе;
- тошноту;
- рвоту;
- усталость;
- слабость;
- потерю веса.
Анемия, желудочно-кишечная непроходимость и желтуха присоединяются уже на запущенных стадиях заболевания. Боль в животе — наиболее распространенный симптом, связанный с 56% случаев.
В итоге болезнь выявляется чаще всего уже на поздних стадиях. Очень редко у пациентов, проходящих программы скрининга, удается обнаружить ДА на ранней стадии или даже аденому с дисплазией до появления признаков ее малигнизации.

Виды дуоденального рака
Гистопатологические подтипы дуоденальной аденокарциномы в зависимости от типа могут напоминать рак соседних органов.
Фенотип
Гистологические характеристики
Гистологически сходные типы
Иммунофенотипические маркеры
Прогноз
Трубчатые/крибообразующие железы, выстланные столбчатыми опухолевыми клетками
Аденокарцинома толстой кишки
Трубчатая/папиллярная пролиферация с дифференцировкой фовеолярного или пилорического типа
Простые железы кубовидных / столбчатых клеток с закругленными плеоморфными ядрами; выраженная десмопластическая строма
Аденокарцинома поджелудочной железы и внепеченочных желчных протоков
Стадии
В настоящее время принятая международная система стадирования (8-е издание) для дуоденальной карциномы подчеркивает важность инвазии опухолью поджелудочной железы и метастазов в лимфатические узлы. Размер мало влияет на клиническую стадию опухоли.
Первичная опухоль 12 перстной кишки определяется следующим образом:
- TX — Первичная опухоль не может быть оценена;
- T0 — нет признаков первичной опухоли;
- Тis — Карцинома in situ;
- T1a — опухоль ограничена эпителиальным слоем;
- T1b — опухоль проникает в подслизистую оболочку;
- T2 — опухоль проникает в мышечный слой двенадцатиперстной кишки;
- T3a — опухоль перфорирует висцеральную брюшину, или проникает в поджелудочную железу (до 0,5 см);
- T3b — опухоль распространяется более чем на 0,5 см в поджелудочную железу или распространяется на перипанкреатическую ткань без вовлечения верхней брыжеечной артерии
- T4 - опухоль поражает верхнюю брыжеечную артерию и/или общую печеночную артерию, независимо от размера
Регионарные лимфатические узлы определяются следующим образом:
- NX — регионарные лимфатические узлы не могут быть оценены;
- N0 — отсутствие регионарных метастазов в лимфатических узлах;
- N1 — метастазирование в один-три регионарных лимфатических узла;
- N2 — метастазирование в четыре или более регионарных лимфатических узла.
Отдаленные метастазы определяются следующим образом:
- MX — наличие отдаленных метастазов не может быть оценено;
- М0 — нет отдаленных метастазов;
- М1 — отдаленные метастазы.

Диагностика
Эндоскопия на сегодня остается предпочтительным диагностическим методом. Оценка опытным эндоскопистом имеет основное значение, так как она позволяет проводить одновременно и визуализацию, и биопсию. Следует уделять особое внимание состоянию соответствующих структур, таких как Фатеров сосочек.
Поражения в третьей или четвертой части двенадцатиперстной кишки могут быть технически сложными для эндоскопического обзора. Поэтому сейчас в клиниках Бельгии в ходу использование современных эндоскопов с удлиненным тонким наконечником, имеющим повышенную гибкость. Такие аппараты дают возможность осмотреть двенадцатиперстную кишку целиком.
Поражения в дистальной двенадцатиперстной кишке могут быть пропущены при первичной эндоскопической оценке, если используется устаревшее оборудование или квалификация эндоскописта недостаточна. Это приводит к дальнейшим диагностическим задержкам.
Эндоскопическое ультразвуковое исследование может проводиться одновременно с прямой визуализацией для оценки локального расширения или лимфаденопатии. Кроме того, это может облегчить диагностику, если попытки биопсии через просвет не увенчались успехом.
Компьютерная томография с контрастом важна для оценки поражения соседних структур, определения резектабельности (возможности удаления) и планирования операции. Однако МРТ способна предоставить больше информации врачу на начальных этапах диагностики, и потому ее назначение в приоритете.

Лечение
Опухоли, расположенные во второй части двенадцатиперстной кишки, обычно требуют панкреатдуоденэктомии (операция Уиппла) из-за близости к головке поджелудочной железы, дистальному желчному протоку и Фатерову сосочку.
И наоборот, опухоли, возникающие в первой, третьей или четвертой части двенадцатиперстной кишки, могут лечиться как операцией Уиппла, так и сегментарной резекцией (с сохранением поджелудочной железы).
В онкологической практике США считается, что панкреатдуоденэктомию следует использовать для всех ДА, независимо от их положения, чтобы обеспечить широкие поля и адекватную регионарную лимфаденэктомию (удаление лимфоузлов).
Такое мнение основано на результатах ранних серий докладов по нескольким группам долгосрочно выживших пациентов.
Большинство же Европейских исследований, в которых сравнивались результаты двух подходов, не выявили статистически значимых различий в результатах. Но они были ограничены небольшими размерами выборки.
В исследовании, проведенном Кокрейновским центром и включавшим данные 1611 пациентов, с 1988 по 2010 гг., радикальная панкреатдуоденэктомия не была связана с улучшением общей выживаемости.
В Бельгии онкологи придерживаются европейской точки зрения — хотя панкреатдуоденэктомия может потребоваться по техническим причинам в некоторых ситуациях, сегментарная резекция с сохранением поджелудочной железы будет подходящей стратегией, если можно добиться полного удаления первичной опухоли.

Среди пациентов с локализованной ДА приблизительно у 43-67% встречается резектабельная онкология двенадцатиперстной кишки. Остальные пациенты для сохранения приемлемого качества жизни требуют паллиативного лечения.
Цели паллиативной хирургии при ДА включают:
- устранение обструкции на выходе из желудка;
- облегчение обструкции желчных путей;
- облегчение боли.
Оперативные вмешательства при гастродуоденальной обструкции могут включать гастроеюностомию или дуоденоеюностомию.
Хирургическое вмешательство по поводу обструкции желчных путей обычно включает в себя эндоскопическое стентирование протоков. И только если невозможно проведение эндоскопической операции при высокой степени желчной непроходимости рекомендуется выполнение операции через лапароскопический доступ.
Такая рекомендация оправдана тем, что закупорка желчных протоков возникает, как правило, на конечных стадиях заболевания. Прогноз при этом сильно ограничен, и врачи стараются избегать ненужного травмирования пациента.

Дуоденальная аденокарцинома — редкое заболевание. Поэтому в настоящее время мало данных, позволяющих определить правильную стратегию адъювантной химиотерапии после полной хирургической резекции.
Учитывая редкость заболевания, в большинстве терапевтических исследований ДА традиционно сочетается либо с другими периампулярными раками, либо с аденокарциномами других отделов тонкой кишки. По этой причине химиотерапевтические схемы не стандартизированы, но все чаще ДА лечат аналогично колоректальной аденокарциноме химиотерапией на основе оксалиплатина. Учитывая склонность этой болезни к системному рецидиву, роль адъювантной химиотерапии требует дальнейшего изучения.
Современная практика в онкологических центрах Бельгии заключается в лечении пациентов с признаками высокого риска (например, узловыми метастазами) с помощью химиотерапии на основе оксалиплатина.
В многоцентровом рандомизированном контролируемом исследовании ESPAC-3 фазы III, сравнивалось консервативное наблюдение с адъювантной терапией фторурацилом и адъювантной терапией гемцитабином у пациентов с раком двенадцатиперстной кишки.
Все пациенты подверглись панкреатдуоденэктомии. Хотя медиана выживаемости достоверно не различалась между группами наблюдения и адъювантной терапии в первичном анализе (35 мес. против 43 мес.), адъювантная химиотерапия была связана с улучшением общей субъективной симптоматики заболевания.

Окончательная или паллиативная химиотерапия должна предлагаться всем подходящим пациентам с метастатическим или неоперабельным заболеванием.
В проспективном исследовании II фазы изучались 30 пациентов с метастатической или неоперабельной формой ампулярной аденокарциномы, которые получали капецитабин и оксалиплатин. В результате было зарегистрировано 50% случаев частичного ответа и 10% случаев полного ответа. Среднее время до прогрессирования было 11 месяцев с медианной общей выживаемостью 20 месяцев. Пациенты также должны быть рассмотрены для клинических испытаний при необходимости.
Роль адъювантной лучевой терапии в лечении ДА недостаточно четко определена. Ни одно исследование не продемонстрировало положительное влияние на опухоль с использованием лучевой терапии.
В отношении же комплексного подхода ситуация выглядит более оптимистично.
Исследование 14 пациентов проведенное в центре Джона Хопкинса с положительным узлом ДА, прошедших панкреатдуоденэктомию и получавших адъювантную химиолучевую терапию (средняя доза 50 Гр, одновременно с 5-FU), привело к улучшению местного контроля по сравнению с одной только хирургией (93% против 67%).
Аналогичным образом, ретроспективное исследование 32 пациентов из медицинского центра Университета Дьюка показало умеренное улучшение местного контроля (70% против 49%) с адъювантной химиолучевой терапией.
Но, к сожалению, ни одно из исследований не показало, что адъювантное химиолучевое воздействие способствовало значительному улучшению общей выживаемости. 5-летняя выживаемость 44% против 43% в первом исследовании и 44% против 57% во втором соответственно.
Другие ретроспективные серии показали аналогичные результаты с улучшениями в региональном контроле, но не в общей выживаемости.

Тем не менее, этот подход, нацеленный на улучшение контроля над местным пространством, может сделать химиолучевую терапию особенно полезной у пациентов с метастазами в лимфатических узлах.
В исследовании 122 пациентов с дуоденальным раком, которым была проведена лечебная резекция, были получены интересные результаты. Адъювантная химиолучевая терапия у пациентов с более высокой распространенностью регионарных метастазов в лимфатических узлах привела к тому же уровню общей выживаемости, как и в группе пациентов с ограниченными или отсутствующими узловыми метастазами, которые не получали адъювантную терапию.
Прогноз выживаемости
ДА представляет собой агрессивный рак, но у пациентов с резектабельным заболеванием отдаленные результаты лучше, чем при других периампулярных злокачественных новообразованиях.
В ретроспективном исследовании 122 пациентов, перенесших БП по поводу ДА в течение 22 лет в MSKCC, десятилетняя общая выживаемость составила 41%.
В проспективном когортном исследовании 150 пациентов в шести онкологических центрах Европы, имевших в 2000-2013 гг. рак 12 перстной кишки, выживаемость составила:
- 1 год — 83,9%;
- 3 года —66,7%;
- 5 лет — 51,2%.
Медиана безрецидивной выживаемости в этом исследовании составила 53 мес.

Другое недавнее исследование, поведенное в нескольких онкоцентрах США показало, что у пациентов с диагнозом рак двенадцатиперстной кишки прогноз во многом зависит о стадии заболевания на момент диагностики. Итоговая пятилетняя выживаемость составила:
- 1 стадия — 65,9%;
- 2 стадия — 50,4%;
- 3 стадия — 31,4%;
- 4 стадия — 11,9%.
Пациенты с метастатическим или неоперабельным заболеванием имеют медиану выживаемости от 2 до 8 месяцев.
Профилактика
Причины развития дуоденального рака не установлены. Поэтому никаких специфических мер профилактики не существует. Однако, есть некоторые принципы, основываясь на которых можно снизить риск развития заболевания.
Проведение периодической гастродуоденоскопии (1 раз в 2-3 года) позволит своевременно выявить наличие полипов и принять соответствующие меры еще до их перерождения в злокачественную опухоль.
На стадии полипа достаточно удалить сам полип, и если в области ножки не будет найдено атипичных клеток, можно проходить эндоскопический скрининг с той же частотой.
Стоит также соблюдать обычные меры профилактики онкологических заболеваний, такие как отказ от курения, сокращение употребления крепких спиртных напитков, ограничение красного и переработанного мяса в рационе и т.д.
Получите больше информации о возможностях лечения рака двенадцатиперстной кишки в Бельгии. Напишите нам или закажите обратный звонок. Мы дадим исчерпывающие ответы на ваши вопросы.
3 ЗЕТ – Гастроэнтерология, Детская хирургия, Лечебное дело, Общая врачебная практика (семейная медицина), Педиатрия, Скорая медицинская помощь, Терапия, Хирургия, Эндоскопия
Следует искать:
Диагностика язвенной болезни (по утвержденным клиническим рекомендациям)
У меня иначе не находился модуль. Всего 1 балл дали.
1) В патогенезе язвенной болезни играют роль гормональные факторы
– половые гормоны
– гормоны коры надпочечников
– гастроинтестинальные пептиды
2) Язвенную болезнь желудка и двенадцатиперстной кишки подразделяют на стадии течения заболевания
– обострения
– рубцово-язвенной деформации
– рубцевания
– ремиссии
3) Исследование биоптатов слизистой оболочки желудка проводится с применением окрасок
– серебрение по Вартину-Старри
– краситель Гимзы
– акридиновый оранжевый
5) Ослабление защитных свойств слизистой оболочки желудка может возникнуть в результате
– уменьшения секреции бикарбонатов и содержания простагландинов
– снижения выработки и нарушения качественного состава желудочной слизи
– ухудшения кровоснабжения
6) Серологический метод исследования Н.pylori
– позволяет обнаружить Н.pylori у больных с низкой обсемененностью
– применяется при язвенных кровотечениях
8) Язвенное поражение в желудке необходимо дифференцировать с
– инфильтративно-язвенной формой рака желудка
– малигнизацией язв
– доброкачественными язвами
9) Осложнениями язвенной болезни являются
– стеноз
– прободение, пенетрация
– рубцово-язвенный стеноз привратника
10) Основными методами в диагностике язвенной болезни являются
– магнитно-резонансная томография (МРТ)
– рентгенологическое исследование
11) Язвенную болезнь необходимо дифференцировать с
– симптоматическими язвами желудка
– симптоматическими язвами двенадцатиперстной кишки
12) Диагностика синдрома Золлингера-Эллисона включает
– компьютерную томографию поджелудочной железы
– ультразвуковое исследование
– провокационные тесты с (секретином, глюкагоном)
13) Агрессивными факторами язвообразования называют
– нарушение желудочного кислотовыделения
– повышение выработки пепсина
– гиперпродукцию гастрина
– обсеменение слизистой оболочки желудка H.pylori
14) Эндоскопическое исследование язвенной болезни выполняет следующие функции
– уточняет локализацию язвенного дефекта, глубину, форму, размеры
– позволяет выявить сопутствующие изменения слизистой оболочки
– подтверждает наличие язвенного дефекта
15) К факторам риска развития лекарственных язв относят
– наличие в анамнезе язвенной болезни
– сопутствующие заболевания сердечно-сосудистой системы и печени
– высокая доза нестероидных противовоспалительных препаратов (НПВП)
– пожилой возраст больных
16) Примесь неизмененной крови в рвотных массах может отмечаться при
– невысокой секреции соляной кислоты
– локализации язвы в кардиальном отделе желудка
– массивном кровотечении
19) К недостаткам микробиологического метода относится наличие
– определенной температуры
– определенной влажности
– специальных сред
20) Стрессовые язвы характеризуются
– протекают малосимптомно
– отличаются наклонностью к желудочно-кишечным кровотечениям
– высокой летальностью
21) Основным этиологическим фактором развития язвенной болезни является
– H.pylori
22) Определение ДНК Н.pylori предполагает определение Н.pylori
– в слизистой оболочке желудка, в кале с помощью иммуноферментного анализа
23) Боль при язвах тела желудка возникает
– через полчаса-час после еды
24) Ведущим симптомом обострения язвенной болезни являются боли в
– эпигастральной области
25) Морфологический (гистологический) метод предполагает определение Н.pylori
– при проведении биопсии и исследовании биоптатов
26) Язвенный дефект, ассоциированный с Н.pylori, наиболее часто локализуется
– в двенадцатиперстной кишке
28) Проведение эрадикации Н.pylori показано при выявлении штамма
– штамм не имеет значения
29) В диагностике язвенной болезни наиболее информативным лабораторным исследованием считается
– суточная рН-метрия желудка
30) По классификации язвенный дефект среднего размера составляет
– 0,6-1,9 см
31) Контроль эрадикации Н.pylori после окончания эрадикационной терапии проводят через
– 4-6 недель
32) При контрольном исследовании эрадикации Н.pylori прекращают прием ингибиторов протонной помпы (ИПП) за
– 2 недели
33) Основной патогенетической причиной формирования язвенного дефекта является
– действие соляной кислоты на слизистую оболочку
34) По классификации язвенный дефект большого размера составляет
– 2,0-3,0 см
35) По классификации язвенный дефект малого размера составляет
– до 0,5 см
36) Причиной развития эрозивно-язвенных поражений желудка и двенадцатиперстной кишки является длительный прием
– нестероидных противовоспалительных препаратов (НПВП)
37) Боль при язвах кардиального и субкардиального отделов желудка возникает
– сразу после приема пищи
38) Быстрый уреазный тест (CLO-тест) предполагает определение Н.pylori
– во время проведения гастродуоденоскопии
39) Уреазный дыхательный тест предполагает определение Н.pylori
– при использовании масс-спектрографа для улавливания мочевины, меченной изотопами 13С или 14C в выдыхаемом воздухе
40) Микробиологический (бактериологический) метод определения Н.pylori
– определяет чувствительность микроорганизмов к тому или иному антибактериальному препарату
41) Факторами риска возникновения язвенного кровотечения служат
– прием ацетилсалициловой кислоты и НПВП
– инфекция Н.pylori
– размеры язв более 1 cм
42) После окончания эрадикационной терапии Н.pylori рекомендуется применять
– определение антигена Н.pylori в кале
– уреазный дыхательный тест
45) Недостатками серологического метода исследования Н.pylori являются
– обладает более низкой чувствительностью у детей
– нельзя применять для контроля эрадикации
46) При обострении язвенной болезни часто встречаются симптомы
– тошнота
– болезненность в эпигастральной области
– запоры
– отрыжка кислым
47) При пенетрации язвы желудка или двенадцатиперстной кишки происходит проникновение в окружающие ткани
– малого сальника
– поджелудочной железы
– желчного пузыря
– общего желчного протока
48) К язвам желудка и двенадцатиперстной кишки, возникающим на фоне эндокринных заболеваний, относят язвы у больных с
– синдромом Золлингера-Эллисона
– гиперпаратиреозом
49) Косвенные признаки язвенной болезни при рентгенологическом исследовании
– рубцово-язвенная деформация желудка и луковицы двенадцатиперстной кишки
– местный циркулярный спазм мышечных волокон на противоположной стенке желудка по отношению к язве
– гиперсекреция натощак, нарушение гастродуоденальной моторики
50) Гастродуоденальные язвы у больных гиперпаратиреозом отличаются от язвенной болезни
– наличием признаков повышенной функции паращитовидных желез
– тяжелым течением с частыми рецидивами
– наклонностью к кровотечениям и перфорации
51) Симптоматические гастродуоденальные язвы
– стрессовые язвы
– лекарственные язвы
– язвы при эндокринных заболеваниях
Читайте также:



