Пролиферация в доброкачественной опухоли
При диагностике опухолевого процесса пациента в первую очередь интересует, не злокачественно ли новообразование. В зависимости от общего состояния больного, проводится ряд диагностических мер, позволяющих определить тип аномальных тканей. Заниматься самодиагностикой ни в коем случае нельзя, так как доброкачественные новообразования могут представлять не меньшую опасность, чем рак.
По данным ВОЗ, неагрессивные опухоли встречаются у каждого второго человека в мире. В большинстве своем это небольшие новообразования, сохраняющие форму и размер в течение жизни пациента. Но некоторые из них разрастаются до особо крупных размеров и начинают давить на близлежащие ткани.
В чем тогда отличие между доброкачественной и злокачественной опухолью? Ответ на данный вопрос необходимо знать, чтобы своевременно предупредить развитие смертельно опасного заболевания.
Что такое доброкачественная опухоль?
Доброкачественное новообразование — это патологическое разрастание тканей. Процесс зарождения опухоли запускается при трансформации отдельных сегментов организма. Клетки начинают бесконтрольно делиться, при этом сохраняя способность к дифференцировке. Данный процесс называется неопластической трансформацией.
Ткань доброкачественной опухоли не имеет структурных отличий от природного материала окружающих органов и систем, в которых образуется. Что такое доброкачественная опухоль? Это уплотнение, состоящее из клеток:
- Эпителия
- Мышцы
- Соединительной ткани
Аномальное новообразование частично сохраняет специфические функции, характерные для здоровых тканей. Оно плотно прилегает к пораженному органу, но никогда не внедряется в него и не метастазирует.
Признаки доброкачественной опухоли зависят от локализации и степени развития новообразования. Конкретных симптомов, характеризующих все типы заболевания, не существует. На ранних стадиях опухолевого процесса человек может не ощущать дискомфорта и чувствовать себя совершенно здоровым.
Если новообразование появляется в мышцах или кожных покровах, со временем больной начинает жаловаться на:
- Дискомфорт в области пораженного участка тела.
- Осязаемую или видимую невооруженным глазом опухоль.
- Затруднение в движениях (в частности, при поражении мышцы), усиливающиеся болевые ощущения.
При поражении внутренних органов, признаками доброкачественной опухоли являются:
- Функциональные нарушения (к примеру, при опухоли кишечника — проблемы с перистальтикой).
- Болевые ощущения, тяжесть и сдавленность в области поврежденного органа.
- Небольшое повышение температуры тела.
- Слабость и отсутствие аппетита.
Конкретная симптоматика напрямую зависит от того, где располагается опухоль. К примеру, если это миома матки, у женщины появляются нарушения менструального цикла с обильными кровотечениями.
Что такое доброкачественная опухоль? В большинстве случаев это новообразование, с которым человек может прожить до глубокой старости без риска ухудшения состояния. Но встречаются тяжелые формы заболевания, которые, при отсутствии терапии, приводят к гибели пациента.
Чем опасна доброкачественная опухоль подобного типа? Прежде всего, неконтролируемым ростом. Разрастаясь внутри органа, аномальные ткани давят на здоровые, вызывая воспалительные и некротические процессы. В функциональную паренхиму пораженной части тела поступает недостаточное количество крови и питательных веществ. По этой причине развивается недостаточность этого органа.
Рассуждая о том, чем опасна доброкачественная опухоль, нельзя обойти стороной патологическое явление — малигнизацию. Аномальные клетки начинают активно мутировать. Помимо ускоренного деления, они приобретают свойства дифференцировки, характерной для раковых клеток. Безобидное новообразование постепенно трансформируется в злокачественную опухоль.
Способ лечения доброкачественной опухоли определяет врач. При подозрении на наличие новообразований во внутренних органах рекомендуется пройти полноценное обследование. Диагностика включает МРТ, УЗИ и прочие аппаратные методы.
По результатам обследования специалист определит размеры опухоли и план дальнейшего лечения. При подозрении на злокачественный процесс назначается биопсия тканей пораженного органа.
В настоящее время лучшим методом лечения доброкачественной опухоли признается хирургическое вмешательство. Специалист рекомендуют своевременно удалять новообразование до того момента, как оно преобразуется в злокачественное. В таком случае рецидив маловероятен. После удаления опухоли пациент полностью выздоравливает.
Одним из способов терапии доброкачественных опухолевых процессов является метод криокоагуляции, заключающийся в разрушении тканей экстремально низкими температурами. Если опухоль неоперабельна (к примеру, гормонально-активна), применяются лекарственные средства, подавляющие выработку гормонов.
Доброкачественная и злокачественная опухоли: отличие
Любое поражение внутренних органов опасно. Но в чем заключается отличие доброкачественной и злокачественной опухолей? По сути, это совершенно разные заболевания. Злокачественный опухолевый процесс характеризуется повышенной агрессивностью течения.
Рассмотрим основные отличия рака от доброкачественного разрастания тканей:
- Аномальные клетки обладают способностью внедряться в здоровые структуры организма.
- Раковая опухоль развивается стремительно и агрессивно, поражая существенную площадь органа.
- На поздних стадиях метастазы рака появляются в других частях тела, помимо очага поражения.
- Если заболевание не лечить, оно гарантированно приведет к мучительной смерти пациента.
- При злокачественном опухолевом процессе возможны рецидивы и резкие ухудшения состояния пациента.
- Раковое поражение тяжело лечится. Оперировать пациента можно только на первых двух стадиях (реже на третьей). При запущенном заболевании лечение проводится посредством химической и лучевой терапии.
Таким образом, отличий рака от доброкачественного новообразования действительно много.
Как определить: доброкачественная или злокачественная опухоль
Ни один человек в мире не застрахован от доброкачественной или злокачественной опухоли. В организме каждого из нас присутствуют аномальные клетки. Катализаторами развития опухолевого процесса становятся тяжелые вирусные, бактериальные или паразитарные поражения, механические травмы внутренних органов. Серьезную роль в проявлении заболевания играет и заниженный иммунитет.
Но как определить: доброкачественная или злокачественная опухоль у пациента? Самостоятельно больной не сможет этого сделать. Некоторые виды наружного рака отличаются от стандартных родинок или пигментных пятен неправильной формой, неровными краями и необычными выделениями (сукровица, лимфа). Если опухоль находится во внутренних тканях организма, определить ее наличие и свойства без участия специалиста невозможно.
При подозрении на опухоль рекомендуется обратиться к терапевту, который даст направление на первичные анализы. При подтверждении диагноза результаты тестирований передаются онкологу. Данный узкопрофильный специалист решает, как определить, доброкачественная или злокачественная опухоль у больного. При подозрении на рак берутся пробы новообразования.
В любом случае, важно следить за собственным состоянием и появлением тревожных симптомов. О ранних признаках развития рака читайте по ссылке→
Пролиферация – это процесс размножения клеток, приумножающий объем тканей. Интенсивно протекает в период эмбрионального развития, когда клетки развивающегося эмбриона активно и непрерывно делятся. Процессом пролиферации управляют гормоны, способные как ускорить её, так и замедлить рост клеток.
Пролиферация, являясь основным процессом, обеспечивающим нормальное развитие и рост тканевых структур, способствует их постоянному обновлению и нормальной работе организма.
Клеточным структурам многих видов тканей необходимо регулярное обновление. Этот физиологический процесс осуществляется путем деления клеток. Процесс обновления клеток явно выражен в кожном покрове, слизистых оболочках желудочно-кишечного тракта, системы дыхания и матки. Это означает, что пролиферация в них является необходимым и нормальным процессом.
- Клеточная пролиферация с медицинской точки зрения
- Виды пролиферации
- Пролиферация эндометрия и шейки матки
- Пролиферация клеток в гастроэнтерологии
- Пролиферация молочной железы
- Пролиферация при воспалениях
- Что делать при выявлении пролиферации?
Клеточная пролиферация с медицинской точки зрения

Изучив процесс клеточной пролиферации, врачи выяснили, что она контролирует процесс нормального функционирования защитных сил организма – иммунитета. Пролиферация способствует уничтожению тканевых дефектов и восстановлению прежнего функционирования органов, работа которых была нарушена. Но нельзя назвать пролиферацию полностью безвредным процессом. Она может принимать участие и в патологических процессах, например, при выработке большого количества соматотропного гормона (гормона роста) наблюдается увеличение конечностей и некоторых органов.
Нарушение процесса пролиферации и дифференцировки клеток может сопровождаться атипией (внешнее и функциональное изменение клеток) и дать толчок образованию злокачественных опухолей. Клетки начинают активно размножаться, что называется гиперпролиферация. Так происходит потому, что пролиферация уже не дифференцирующихся клеток приводит к началу опухолевого процесса. Но не следует забывать о том, что в различных органах тканевая пролиферация протекает неодинаково.
Ведущие клиники в Израиле



В зависимости от индекса пролиферативной активности и способности делиться клетки организма в медицине подразделяются на 3 группы:
- Лабильные;
- Стабильные;
- Статические.
Лабильным клеткам присущи выраженные пролиферативные процессы, вследствие чего они могут регенерировать быстро и восстанавливать свою деятельность.
В процессе регенерации наблюдаются такие процессы как:
- Рост соединительной ткани;
- Формирование новых сосудов;
- Устранение тканевых дефектов.
В эту группу можно включить клетки крови, эпителиальной ткани и эпидермиса, слизистого покрова желудочно-кишечного тракта. Наиболее быстро пролиферация протекает в слизистой желудка.
Стабильным клеткам свойственны умеренные пролиферативные процессы из-за чего способность их к быстрому размножению и восстановлению несколько хуже. Пролиферирующие клетки здесь образуются исключительно в результате серьезных повреждений тканей или органов. Сюда можно отнести печень, поджелудочную железу, поперечно-полосатую мышечную ткань, слюнные железы и др.
К статическим клеткам можно отнести кардиомиоциты и нервные клетки. Они практически не поддаются пролиферации, не способны восстанавливаться и размножаться. Однако, если на кардиомиоциты долгое время действует какое-либо напряжение, они способны восстановиться за счет пролиферирующих внутриклеточных структур внутри здоровых клеток. Это, в конечном счете, может привести к гипертрофии миокарда.
Виды пролиферации
Медицине на сегодняшний день известны следующие виды пролиферации клеток:
- Физиологическая пролиферация – восстанавливает тканевые и клеточные структуры естественным путем. Сюда можно отнести пролиферацию плоского эпителия ЖКТ и клеток крови;
- Репаративная — способствует регенерации тканей и клеточных структур при воспалительных процессах после каких-либо повреждений;
- Патологическая пролиферация клеток – процесс развития атипичных тканей, отличающихся структурой от здоровых. В пример можно привести рубцы в месте ожогов, разрастание соединительных тканей в месте разрыва стенки миокарда, хрящи в месте перелома. Но самым сложным проявлением патологической пролиферации является возникновение раковых опухолей.
Изучение процессов пролиферации имеет немаловажное значение для понимания процесса гомеостаза (поддержания постоянства внутренней среды организма).
Пролиферация эндометрия и шейки матки
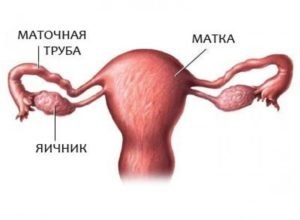
Пролиферация в гинекологии – явление нередкое. Деление клеток женских половых органов итак происходит довольно быстро, а при патологиях этот процесс протекает еще активнее. Пролиферация клеток призматического эпителия в половых органах выявляется после гистологического анализа слизистой оболочки матки, шейки матки или ее фрагмента, который забирается путем конизации. По итогам анализа врач-гинеколог делает вывод о наличии или отсутствии патологического процесса.
Рассмотрим подробнее пролиферацию в матке. В разных частях матка имеет неодинаковую структуру и выстилку. Шейку ее выстилает многослойный плоский без атипии эпителий, зону цервикального канала – цилиндрический эпителий, а слизистую эндометрия выстилает железистая ткань.
В течение одного менструального цикла на матку воздействуют гормональные всплески, готовящие ее к возможной беременности, поэтому клетки ее начинают пролиферировать и подготавливать эндометрий для более удобной имплантации оплодотворенной яйцеклетки. Именно поэтому процесс пролиферации не просто нормальный, но еще и необходимый.
У беременной женщины в результате гормональных изменений активная пролиферация железистого эпителия маточной шейки считается нормальным явлением.
Ускоренный пролиферативный процесс может свидетельствовать о следующем:
- О наличии воспалительного процесса – цервицита;
- О повреждениях различного рода (выскабливание при абортах, послеродовые разрывы, удаление фрагмента шейки матки);
- О возможных опухолевых процессах (дисплазия, полипы, рак).
Иными словами, в шейке матки наблюдается воспалительная, гиперпластическая и посттравматическая пролиферация.
Бактериальные, грибковые и вирусные цервициты приводят к повреждениям покровного эпителия, который вследствие этого начинает усиленно пролиферировать для восстановления своей целостности.
Похожие явления наблюдаются при эрозии, повреждении шейки матки при родовых потугах, абортах и прочих манипуляциях. Такая пролиферация, способствующая регенерации многослойной плоской эпителиальной ткани, считается физиологической.
Пролиферация в перечисленных выше ситуациях не приносит вреда, но все же требует лечения под наблюдением врача. При полном восстановлении слизистой оболочки волноваться не о чем.
Пролификация с атипией имеет несколько другой характер. Базальноклеточная гиперплазия может способствовать развитию псевдоэрозий шейки матки, которые при несвоевременном лечении могут преобразоваться в раковую опухоль.
Псевдоэрозия представляет собой явление, когда снаружи шейки матки появляются участки железистого эпителия, который обычно выстилает стенки в цервикальном канале. Это происходит из-за гормонального сбоя, который в свою очередь вызывается вирусными заболеваниями. При псевдоэрозиях может пролиферировать, как плоский эпителий, так и участки цилиндрического, из которого и формируются эрозии.
Опасным явлением выступает пролиферация с дисплазией многоклеточного плоского эпителия шейки матки, так как дисплазия – это предраковый процесс.
Поговорим о пролиферации эндометрия.
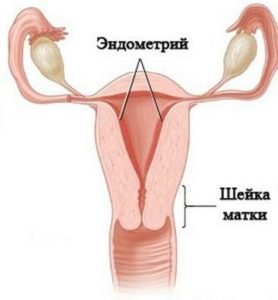
Эндометрий представляет собой внутренний слой матки, постоянно обновляющийся и имеющий сложное строение. В период менструации он отторгается из-за не наступившей беременности и образуется вновь до следующего цикла. Этот процесс является постоянным и не обходится без пролиферации. Более активно клетки эндометрия пролиферируют в первую половину менструального цикла, когда слизистая оболочка матки находится под действием гормонов эстрогенов. В случае, когда пролиферация не прекратилась вовремя, возникает гиперплазия эндометрия. Это может повлечь за собой образование кист, полипов, что грозит перерождением их в онкологию.
Получается, процесс пролиферации в матке не всегда является патологией. В некоторых случаях этот процесс жизненно необходим.
Пролиферация клеток в гастроэнтерологии
Обновление клеток железистого эпителия желудка происходит регулярно, так как она нуждается в постоянной пролиферации. Любое повреждение слизистой ускоряет процесс деления клеток. Причинами активной пролиферации обычно выступают язвенная болезнь, гастрит, различные полипы, а также опухоль.
При острой форме гастрита на фоне воспаления, выраженного в виде отечности слизистого покрова и кровоизлияний, выявляются также участки покровно-ямочного эпителия, который пролиферируя, способствует регенерации поврежденной слизистой оболочки.
Хронический гастрит, встречающийся сегодня у людей всех возрастных групп, также протекает с усиленным процессом пролиферации эпителия. Этот процесс особенно проявляется при гиперплазиях, когда утолщается слизистая и возможно возникновение различного рода полипов.
При обострении язвенной болезни наблюдается повреждение стенок органа. Для устранения этого дефекта по краям язвы начинается активная пролиферация слизистого эпителия. Такая пролиферация особенно характерна для гиперпластических полипов, обнаруживаемых по краям язвы.
Наиболее опасной считается предраковая пролиферация желудочной стенки, когда начинает умножаться количество темных вытянутых клеток в зоне шеек желез желудка.
В самом начале процесс несет регенеративный характер, но из-за нарушенной дифференцировки клеток полного восстановления слизистой не наблюдается. Железы в результате покрываются несвойственными ими темными вытянутыми клетками, которые в норме находятся лишь в шейках этих желез. В дальнейшем это приводит к развитию злокачественного образования – карциномы.
Пролиферация молочной железы
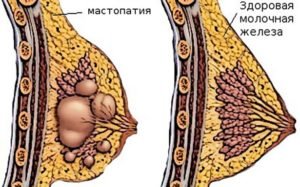
Молочные железы часто подвержены различным изменениям. Они регулярно испытывают на себе воздействие половых гормонов, которое проявляется в изменениях груди во время менструации, в период беременности и грудного вскармливания. По этой причине орган подвержен различным патологиям. Согласно статистическим данным около 60% женщин в возрасте 25-35 лет подвержены развитию мастопатии.
Несмотря на то, что мастопатия является доброкачественным процессом, наличие ее повышает риск развития рака груди. Пролиферативное действие здесь еще более опасно. Оно повышает риск развития онкологии в 25 раз. Именно поэтому пролиферуриющая мастопатия называется предраковой.
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную цену на лечение.
Выделяют 3 степени мастопатии:
- При первой степени не наблюдается пролиферации;
- При второй имеются признаки пролиферации;
- При третьей степени наблюдается выраженная пролиферация атипичных клеток эпителия.
Получается, процесс пролиферации является не только признаком развития мастопатии, но и показателем возможного развития онкологии. Поэтому при наличии каких-либо изменений в груди делается цитограмма для изучения структуры ткани груди.
Пролиферация при воспалениях
Любой воспалительный процесс завершается пролиферацией. Очаговая воспаленная часть ограничивается от нормальных тканей именно за счет пролиферации. Однако, этот процесс может наблюдаться на начальной стадии воспаления фолликулярного эпителия. В этом случае причины пролиферации могут быть разнообразными.
В процессе пролиферации может наблюдаться активное деление различных клеток, а именно:
- Клеток мезенхимы;
- Эндотелиальных клеток;
- В — и Т-лимфоцитов;
- Клеток адвентиция;
- Тучных клеток;
- Макроцитарных клеток.
Рассмотрим пролиферацию в фибробластах. При ней наблюдается активная выработка белков. В дальнейшем фибробласты преобразуются в зрелые клетки, именуемые фиброцитами. На конечном этапе пролиферация приводит к отделению очага воспаления от нормальных тканей с помощью коллагена. Смотря на наличие такой структуры, можно установить диагноз пролиферация.
Что делать при выявлении пролиферации?

Где бы ни был выявлен процесс пролиферации, первое, что сделает квалифицированный специалист – это определит причину, только потом подберет необходимую терапию. Не существует однозначного метода лечения пролиферации, так как она не является самостоятельной патологией, а лишь служит спутником других болезней.
Для лечения пролиферации при воспалительных процессах назначается противовоспалительная терапия, дополняющаяся противовирусными и антибактериальными препаратами, оказывающими антипролиферативное действие.
Предраковый пролиферат с атипией на фоне фовеолярной дисплазии требует более серьезных мер лечения вплоть до удаления пораженной части органа или ткани. Пролиферация, протекающая на фоне карциномы, требует лечения по правилам онкологической терапии и не исключает удаления пораженного органа.
Пролиферация, которая свидетельствует о патологии, служит сигналом, призывающим к немедленному лечению. В связи с этим пациенты с диагностированной у них пролиферацией, находятся под надзором врача. Завершив лечение основного заболевания, следует провести дополнительное исследование (биопсию или цитологический анализ), которое позволит оценить насколько эффективно прошло лечение и определить есть ли риск образования в будущем злокачественной опухоли.
Пролиферативная активность клеток отражает интенсивность роста опухолей. В статье приведены данные изучения уровня пролиферации клеток базалиомы — наиболее частой злокачественной опухоли кожи. Исследование проводили иммуногистохимическим методом с маркером пролиферации Ki67. По характеру пролиферации базалиома представляла гетерогенную группу. Солидный, аденоидный, поверхностный мультицентрический тип базалиомы отличались низкой пролиферативной активностью с преимущественным распределением клеток, экспрессирующих Ki67, по периферии комплексов. Высокую пролиферативную активность выявляли в инфильтративном, склерозирующем и микронодулярном типе при равномерном распределении пролиферирующих клеток.
Пролиферативная активность клеток отражает интенсивность роста опухолей. В статье приведены данные изучения уровня пролиферации клеток базалиомы — наиболее частой злокачественной опухоли кожи. Исследование проводили иммуногистохимическим методом с маркером пролиферации Ki67. По характеру пролиферации базалиома представляла гетерогенную группу. Солидный, аденоидный, поверхностный мультицентрический тип базалиомы отличались низкой пролиферативной активностью с преимущественным распределением клеток, экспрессирующих Ki67, по периферии комплексов. Высокую пролиферативную активность выявляли в инфильтративном, склерозирующем и микронодулярном типе при равномерном распределении пролиферирующих клеток.
В структуре злокачественных эпителиальных опухолей кожи первое место занимает базалиома, на долю которой приходится от 75 до 94% [1, 2]. В подавляющем большинстве случаев регистрируются солитарные опухоли, локализующиеся на открытых участках кожи, подверженных инсоляции. Опухоль отличается медленным течением и относительно благоприятным прогнозом. Однако в ряде случав она может значительно увеличиваться в размере, характеризуясь выраженным экзофитным ростом, либо приобретать инвазивные черты, проникая в окружающие и подлежащие ткани, приводя к их разрушению. Подобный рост опухоли обычно ассоциируется с определенными морфологическими типами, которые рассматривают как агрессивные [3].
Показателем интенсивности роста ткани является пролиферативная активность клеток. Она относительно спокойна в доброкачественных процессах и резко возрастает в злокачественных опухолях. Аналогичные тенденции присущи и эпителиальным опухолям кожи. Так, пролиферативная активность клеток базальноклеточного рака кожи выше, чем в очагах лейкоплакии [4], а при раке in situ индекс пролиферации превосходит таковой при предраковом актиническом кератозе [4,5]. Плоскоклеточный рак кожи отличается высоким уровнем пролиферации, который следует за снижением степени его дифференцировки [6, 7, 8].
Предыдущие исследования показали, что по характеру пролиферативной активности клеток базалиома представляет гетерогенную группу. Наиболее интенсивный рост имела язвенная форма, тогда как нодулярная и поверхностная характеризовались умеренными и низкими показателями [9]. Высокий уровень пролиферации отмечали в микронодулярном, метатипическом типе базалиомы и типе морфеа [10, 12]. Также отмечали повышение индекса Ki67 в инфильтративном и метатипическом типе по сравнению с нодулярным и поверхностным [11, 13]. В то же время единого мнения о связи уровня пролиферации с гистологическим типом базалиомы до сих пор нет, так как другие исследования свидетельствовали, что индекс Ki67 в нодулярном и поверхностном мультицентрическом типе базальноклеточного рака значительно превосходил аналогичный показатель в склерозированном и типе морфеа [14, 15]. Учитывая противоречивые данные, представляется интересным и актуальным продолжить изучение пролиферативной активности клеток в различных морфологических типах базалиомы, что позволит более детально понимать маркеры и предикторы агрессивного течения опухоли.
Материалы и методы
В работе исследования использовали 36 биоптатов кожи больных базальноклеточным раком кожи. Биопсию кожи размером 0,5 х 0,5 см проводили под местной анестезией 2% раствором новокаина, биоптаты фиксировали в 10% растворе формалина, забуфференом по Лилли при рН-7,4. Материал заливали в парафин по обычной методике. Серийные срезы толщиной 3–5 мкм депарафинировали по стандартной схеме, затем окрашивали гематоксилином и эозином. Иммуногистохимическое исследование проводили в соответствии со стандартным протоколом. Парафиновые срезы наносили на стекла с адгезивным покрытием, депарафинировали по стандартному протоколу. Срезы, погруженные в цитратный буфер, инкубировали в микроволновой печи при мощности 690 Вт два раза по пять минут. Двадцать минут при комнатной температуре, срезы охлаждали, подсушивали и наносили первичные антитела. Для определения уровня пролиферации использовали моноклональные антитела к протеину Ki67 (DAKO), разведение 1:200. Использовались соответствующие позитивные и негативные контроли – иммунные и неиммунные сыворотки. Срезы промывали в буфере, подсушивали, затем на них наносили EnVision (anti-mouse и anti-rabbit, фирмы DAKO, Дания) на 30–40 минут. Для визуализации реакции наносили DAB+ (3, 3 ґ– диаминобензидин), что позволяло получать специфическую коричневую окраску. Затем срезы докрашивали гематоксилином Майера. Определение уровня пролиферации оценивалась с помощью индекса, который вычислялся как среднее от числа меченных ядер на 100 учтенных ядер (при учете 500–1000 опухолевых клеток). Подсчет меченных ядер проводился в репрезентативных полях зрения с относительно равномерным распределением опухолевых клеток, сверху вниз и слева направо. Клетки на периферии срезов, где чаще всего наблюдается фоновое окрашивание, не учитывались.
Для статистической обработки данных использовались методы t-Стьюдента с поправкой для множественных сравнений; хи-квадрат. Расчеты проводились при помощи программы BIOSTAT. Полученные различия считались достоверными при значениях p ? 0,05.
Среди 36 базалиом пять имели поверхностный мультицентрический тип строения, четыре – поверхностный мультицентрический в сочетании с солидным, семь – солидный, два – аденоидный, два – солидно-аденоидный, пять – инфильтративный, три – микронодулярный. В восьми случаях отмечали различные варианты сочетания солидного, инфильтративного, микронодулярного, склерозирующего строения.
Индекс пролиферации Ki67 в поверхностном мультицентрическом типе и при сочетании его с солидным компонентом варьировал от 14,9 до 31,1%. Средний индекс составлял 22,2%. Пролиферирующие клетки в шести случаях располагались преимущественно по периферии клеточных комплексов, в трех – равномерно по клеточным комплексам. При солидных опухолях средний индекс составил 26,5%, он варьировал от 14,5 до 38,2% (рис.1). Периферическое распределение наблюдали в четырех случаях, равномерное – в трех. При аденоидном строении пролиферирующие клетки распределялись равномерно, индекс пролиферации составлял 22,6 и 31,3%. В случаях, когда имелось сочетание солидного и аденоидного компонентов, индекс пролиферации составлял 36,8 и 19,2%, В первом случае клетки распределялись равномерно, во втором – равномерно в аденоидном компоненте и по периферии – в солидном. В опухолях инфильтративного, микронодулярного строения и при их сочетании клетки, экспрессирующие маркер Ki67, диффузно регистрировались по всем клеточным комплексам. В инфильтративном типе минимальное и максимальное значение индекса было 27,6 и 47,8% (среднее значение – 35,4%) (рис.2). Микронодулярные базалиомы имели средний индекс Ki67 26,9%. В случаях инфильтративно-склерозирующего строения индекс имел значение 40,2 и 31,6%, пролиферирующие клетки равномерно распределялись в комплексах (рис.3). При сочетании инфильтративного, солидного и микронодулярного строения преимущественно отмечали равномерное распределение пролиферирующих клеток, и средний индекс составлял 36,5% (значения варьировали от 22,1 до 50,4%). Солидное строение в сочетании с инфильтративным склерозирующим имели опухли с индексом Ki67 26,7 и 35,3%, в солидном компоненте пролиферирующие клетки располагались преимущественно по периферии комплексов, инфильтративном склерозирующем – равномерно.
При анализе пролиферативной активности клеток мы сгруппировали опухоли в зависимости от характера течения и роста. В группу неинвазивного роста мы включили опухоли, имеющие поверхностный мультицентрический, солидный, аденоидный, сочетание поверхностного мультицентрического и солидного компонентов. В группу с инвазивным ростом нами были включены опухоли инфильтративные, микронодулярные, инфильтративно склерозирующие, а также опухоли сложного строения (инфильтративный + микронодулярный + солидный и солидый + инфильтративный склерозирующий).
Средний индекс пролиферации неагрессивных типов составил 24,77 ± 7, 47 с доверительным интервалом 95% 21,27–28,26 (табл. 1). Средний индекс Ki67 агрессивных типов составлял 33,53 ± 8,94 с доверительным интервалом 95% 28,77–38,29 (табл. 1). Различия в уровне пролиферации между агрессивными и неагрессивными типами носили статистически значимый характер (р = 0,003). Анализ характера распределения пролиферирующих клеток в опухолевых комплексах показал, что в неагрессивных типах периферическое распределение клеток наблюдалось в 50% случаев, равномерное – в 45%, в 5% случаев ряд комплексов в опухоли имели один тип распределения, другие комплексы – иной тип распределения (табл.2). В агрессивных типах 81,25% случаев имели равномерное распределение пролиферирующих клеток, сочетание двух типов распределения – 18,75% (табл. 2). Периферическое распределение пролиферирующих клеток в агрессивных типах не встречалось. При сравнении распределения клеток между агрессивными и неагрессивными типами опухоли было показано, что различия носят статистически достоверный характер (р = 0,003).
Таблица 1. Индекс пролиферации Ki67 в агрессивных и неагрессивных морфологических типах базалиомы
Читайте также:

