Прогноз при раке тела
ФАКТОРЫ ПРОГНОЗА У БОЛЬНЫХ РАКОМ ТЕЛА МАТКИ.
Прогноз при раке тела матки и выживаемость больных во многом зависят от стадии заболевания, определенной на основании интраоперационных находок и результатов гистологического исследования.
Не маловажное значение имеет и своевременность точного прогноза. Наиболее точная диагностика с визуализацией опухолей выполняется с помощью позитронно-эмиссионной томографии, совмещенной с компьютерной томографией.
Факторами неблагоприятного прогноза, статистически достоверно влияющими на отдаленные результаты лечения больных раком тела матки I-III клинических стадий, являются стадия, возраст, глубина инвазии миометрия, степень дифференцировки и размер опухоли, наличие опухолевых эмболов в кровеносных и лимфатических сосудах миометрия, опухолевых клеток в смывах из брюшной полости, дис-семинации и лимфогенных метастазов. Метастазы в лимфатических узлах - наиболее важный фактор прогноза при раке тела матки ранних стадий.
Результаты лечения опровергают традиционное представление о благоприятном клиническом течении рака тела матки (РТМ). Так, 5-летняя общая выживаемость больных РТМ I и II стадий составляет 82 и 65% соответственно, а прогрессирование возникает у 25% больных, лечившихся по поводу РТМ ранних стадий [5].рак матки
В мире РТМ занимает 4-е место в структуре заболеваемости женщин злокачественными новообразованиями и 7-е место в структуре смертности от них. РТМ чаще встречается у женщин в пре- и постменопаузе (75%), однако в последние годы отмечается тенденция омоложения больных РТМ. Значительные темпы прироста заболеваемости РТМ отмечаются в возрастных группах 40-49 (на 12,3%) и 50-56 лет (на 15,6%) [2].
Прогноз при РТМ и выживаемость больных во многом зависят от стадии рака тела маткия, определенной на основании интраоперационных находок и результатов гистологического исследования [3]. При этом учитываются глубина инвазии миометрия, состояние придатков и шейки матки, результаты ревизии брюшной полости и малого таза, биопсии всех подозрительных объемных образований и увеличенных тазовых и парааортальных лимфатических узлов [1]. Данные предоперационного обследования и установленная на этом основании клиническая стадия не совпадают с операционными находками и результатами гистологического исследования у 51% больных РТМ [4]. Таким образом, при РТМ оптимальным является определение морфологической стадии заболевания.
Риск метастазов РТМ в регионарных лимфатических узлах, а также прогрессирования болезни определяется в
Длительное время ведутся научные споры об объемах хирургических вмешательств при РТМ. Эта проблема имеет два аспекта: целесообразность расширения их объема с учетом особенностей лимфогенного метастази-рования и возможность выполнения расширенных операций у больных, обычно страдающих выраженными эн-докринно-обменными нарушениями и сопутствующими заболеваниями сердечно-сосудистой системы. Существуют разные методики визуальной и морфологической оценки состояния регионарных лимфатических узлов при РТМ: УЗИ, пальпация и биопсия увеличенных лимфатических узлов, биопсия одного увеличенного лимфатического узла, селективная и тотальная лимфаденэкто-мия. К сожалению, до сих пор нет единых рекомендаций FIGO по определению морфологической стадии РТМ.
С учетом изложенного целью проведенного исследования являлось изучение эффективности трех методик комбинированного лечения РТМ, выявление факторов прогноза и разработка научно обоснованных рекомендаций по выполнению расширенных операций при РТМ.
В исследование включены 395 больных РТМ IA- IIIC стадий в возрасте 30-89 лет, которым проведено лечение в ГУ РОНЦ им. Н. Н. Блохина РАМН с 1995 по 2005 г. Диагноз у всех пациенток установлен впервые на основании результатов гистологического исследования.
Средний возраст пациенток составил 60,4±0,5 года:
15 (3,8%) - в возрасте до 40 лет, 37 (9,4%) - в возрасте 40-49 лет, 143 (36,2%) - в возрасте 50-59 лет, 137 (34,7%) - в возрасте 60-69 лет, 63 (15,9%) - в возрасте 70 лет и старше. Таким образом, подавляющее большинство больных РТМ (343 больные, 86,8%) были в возрасте 50 лет и старше.
Все больные наблюдались от 1 до 10 лет. Пятилетняя общая выживаемость больных РТМ I-III стадий составила 75,9±2,6%, 10-летняя - 71,5±3,2%, 5-летняя безрецидивная выживаемость - 71,3±3,1%.
Стадия заболевания статистически достоверно связана с прогнозом больных РТМ (р = 0,00001). Так, при I стадии заболевания в течение 5 лет без признаков про-грессирования болезни наблюдались 81,3% пациенток. Десятилетняя выживаемость больных в этой группе составила 77,1±3,3%. При III стадии болезни 50% больных умерли от рецидивов и отдаленных метастазов в сроки до 42,5 мес, а 25% больных - в сроки до 20,8 мес. Не выявлено статистически достоверных различий в отдаленных результатах лечения больных РТМ IIA и IIB, IIIA, IIIB и IIIC стадий (p > 0,05). Пятилетняя общая выживаемость больных РТМ IIIA-IIIC стадий статистически достоверно ниже, чем больных РТМ IA-IC (p = 0,0001) и IIA-IIB (p = 0,01) стадий. Аналогичные результаты выявлены при изучении безрецидивной выживаемости больных РТМ. Так, 5-летняя безрецидивная выживаемость больных РТМ I стадии составила 80,5±2,1%, II стадии - 69,8±7,9%, III стадии - 41,9±11,3% (p = 0,00001). Медиана безрецидивного периода при РТМ III стадии составила 27,9 мес.
Пятилетняя общая выживаемость при РТМ T1N0M0 статистически достоверно выше, чем при РТМ T1N1M0 (81,3±2,8 и 30,9±17,9% соответственно, р = 0,001). В связи с небольшим количеством пациенток с опухолями Т2а-3bN1 сравнение результатов лечения в этой группе в зависимости от наличия лимфогенных метастазов не проводили. Однако следует отметить, что при наличии регионарных лимфогенных метастазов 5-летняя выживаемость больных была менее 50%. При опухолях Т3а 5-летняя выживаемость больных РТМ с метастазами и без таковых оказалась сопоставимой.
Статистически достоверные различия выявлены при изучении отдаленных результатов лечения больных РТМ разных возрастных групп. Установлено, что 5-летняя выживаемость больных старше 60 лет статистически достоверно ниже, чем в других возрастных группах (p 0,05). Пятилетняя безрецидивная выживаемость больных аденокарциномой эндометрия I-III стадий составила при высокой дифференцировке опухоли 91,4±3,8%, при умеренной - 70,1±5,4%, при низкой - 65,3±10,9%, при смешанной - 65,2±7,9% (р = 0,04).
При анализе 10-летней общей выживаемости в зависимости от глубины инвазии миометрия отмечено, что она была наибольшей при прорастании менее половины толщины миометрия (80,9±3,4%). Результаты лечения больных, у которых опухоль прорастала более половины толщины миометрия, и больных, у которых опухоль прорастала до серозной оболочки, оказались одинаковыми. Обе больные с прорастанием опухолью серозной оболочки матки умерли от прогрессирования заболевания через 9 и 10 мес. У 11 пациенток инвазии миометрия при гистологическом исследовании не выявлено. При этом метастазы в регионарных лимфатических узлах выявлены у 2 больных, а переход опухоли на шейку матки - у 1. В целом выживаемость в этой группе была низкой и составила 18,2±1,3%, что обусловлено сочетанием неблагоприятных факторов прогноза. Пятилетняя безрецидивная выживаемость больных РТМ в зависимости от глубины инвазии миометрия составила 81,3±2,9% при прорастании опухолью менее половины толщины миометрия и 62,8±5,9% при прорастании опухолью более половины толщины миометрия (р = 0,000001).
Отмечена тенденция к ухудшению отдаленных результатов лечения больных РТМ с переходом на строму шейки матки по сравнению с таковыми у больных с переходом опухоли на слизистую цервикального канала (5-летняя общая выживаемость 55,9±10,1 и 74,6±6,6% соответственно, р = 0,08). Пятилетняя безрецидивная выживаемость больных РТМ при переходе опухоли на слизистую шейки матки составила 71,3±9,3%, на стро-му - 52,1±19,8% (р = 0,061).
Статистически достоверно ухудшают отдаленные результаты лечения больных РТМ опухолевые эмболы в кровеносных и лимфатических сосудах миометрия (р = 0,035). Пятилетняя общая выживаемость больных РТМ в зависимости от наличия опухолевых эмболов различалась недостоверно, в то время как 10-летняя имела достоверные различия (р = 0,013). Пятилетняя безрецидивная выживаемость больных РТМ составила 59,3±9,4 и 75,7±3,3% соответственно (р = 0,049).
По результатам нашего исследования выявлена тенденция к снижению выживаемости больных РТМ с метастазами в яичниках. Пятилетняя безрецидивная выживаемость при наличии метастазов в яичниках составила 68,6±16,8%, в отсутствие метастазов - 81,8±2,5% (р = 0,35).
Регионарные лимфогенные метастазы, по нашим данным, являются одним из наиболее значимых факторов неблагоприятного прогноза, статистически достоверно влияющим на выживаемость больных. Четверть больных РТМ с метастазами в регионарных лимфатических узлах умерли от прогрессирования болезни в сроки до 20 мес, половина - в сроки до 44,5 мес. Пятилетняя общая выживаемость больных РТМ с метастазами в регионарных лимфатических узлах и без них составила 47,6±11,7 и 82,0±6,3% (р = 0,0018), 5-летняя безрецидивная выживаемость - 41,3±12,1 и 80,9±6,9% (р = 0,01), медиана безрецидивного периода - 30,8 мес.
Диссеминация по брюшине статистически достоверно снижает отдаленные результаты лечения больных РТМ (р = 0,00005). Четверть больных этой группы умерли от прогрессирования заболевания в сроки до 9,6 мес. Медиана продолжительности жизни больных этой группы составила всего 21,6 мес, тогда как в группе больных без диссеминации по брюшине не была достигнута. Пятилетняя общая выживаемость больных РТМ при наличии опухолевой диссеминации по брюшине и без нее составила 28,7±17,0 и 77,6±2,6% (р = 0,0025), 5-летняя безрецидивная выживаемость - 24,3±16,8 и 75,4±3,2% (р = 0,00016), медиана безрецидивного периода - 12,5 мес.
Выявлены статистически достоверные различия в выживаемости больных РТМ в зависимости от размеров первичной опухоли. При первичных опухолях более 4 см 5-летняя безрецидивная выживаемость больных составила 61,4±5,2%, при опухолях менее 4 см - 78,9±3,8% (р = 0,018).
Установлена тенденция улучшения 10-летней общей выживаемости больных с опухолями, содержащими рецепторы прогестерона, и ухудшения 5-летней общей выживаемости больных с опухолями, не содержащими рецепторы эстрогенов и прогестерона (р = 0,25). Пятилетняя безрецидивная выживаемость больных РТМ в зависимости от рецепторного статуса опухоли не различалась и составила в группе больных с рецептороотри-цательными опухолями 54,3±11,0%, с опухолями, содержащими только рецепторы прогестерона, - 69,8±12,6%, с опухолями, содержащими только рецепторы эстрогенов, - 65,4±12,9%, с рецептороположительными опухолями - 68,5±8,1%.
Проведенный анализ показал статистически достоверные различия в отдаленных результатах лечения больных РТМ в зависимости от наличия опухолевых клеток в смывах из брюшной полости (р = 0,0001). Так, в отсутствие опухолевых клеток в смывах медиана продолжительности жизни больных не достигнута, а при наличии опухолевых клеток составила 26,7 мес. Пятилетняя общая выживаемость оказалась равной 77,4±2,6 и 30,5±15,0% соответственно (р = 0,00001). Пятилетняя безрецидивная выживаемость больных РТМ составила в отсутствие опухолевых клеток в смывах 84,1±2,7%, при наличии опухолевых клеток в смывах - 26,5±15,7% (р = 0,00012), медиана безрецидивного периода - 19,7 мес.
Таким образом, факторами неблагоприятного прогноза, статистически достоверно влияющими на отдаленные результаты лечения больных РТМ I-III клинических стадий, являются стадия, возраст, глубина инвазии ми-ометрия, степень дифференцировки и размер опухоли, наличие опухолевых эмболов в кровеносных и лимфатических сосудах миометрия, опухолевых клеток в смывах из брюшной полости, диссеминации, лимфогенных метастазов.
Источник
Научная статья для специалистов
Вестник РОНЦ им. Н. Н. Блохина РАМН, т. 17, №3, 2006
А. В. Налбандян, В. В. Кузнецов, В. М. Нечушкина
НИИ клинической онкологии ГУ РОНЦ им. Н. Н. Блохина РАМН, Москва
ЛИТЕРАТУРА
1. Бохман Я. В. Руководство по онкогинекологии. - Л.: Медицина, 1989. - С. 275-340.
2. Трапезников Н. Н., Аксель Е. М. Статистика злокачественных новообразований в России и странах СНГ (состояние онкологической помощи, заболеваемость и смертность). - М., 2001. - 296 с.
3. Cohn D. E, Horowitz N. S, Mutch D. G. et al. Should the presence of lymphovascular space involvement be used to assign patients to adjuvant therapy following hysterectomy for unstaged endometrial cancer? // Gynecol. Oncol. - 2002. - Vol. 87. - P. 243-246.
4. Creasman W. T., Morrow C. P., Bundy B. N. Surgical pathologic spread patterns of endometrial cancer // Cancer. - 1987. - Vol. 60, N 8. - P. 2035-2041.
5. Lurain J. R. Uterine cancer / Berek J., Adashi E., Hillard P. (eds.). Novak‘s Gynecology. - 12th ed. - Baltimore: Williams & Wilkins, 1996. - P. 1057-1092.
6. Mizuuchi H., Nasim S., Kudo R. Clinical implications of K-ras mutations in malignant epithelial tumors of the endometrium // Cancer Res. - 1992. - Vol. 52, N 10. - P. 2777-2781.
Но это совсем не так.
Сейчас лечение онкологических заболеваний ушло далеко вперед, даже по сравнению с лечением онкологических пациентов всего десять лет назад. Сегодня рак - скорее хроническое заболевание, чем фатальное.
Например, пациенты с 4-й стадией рака кишечника сейчас живут минимум 5-6 лет, тогда как 10 лет назад продолжительность жизни составляла максимум 1-2 года.
Рак в современном мире приобрел черты хронического заболевания, время от времени требующего лечения.
Например, сахарный диабет - неизлечимое заболевание, которое стало хроническим и требует ежедневной коррекции инсулином. Но жить с ним можно!
Также и рак. Излечить его нельзя, но жить с ним можно. Причем с хорошим качеством жизни. Ранние стадии рака в настоящее время лечатся очень эффективно. Поздние стадии также поддаются успешному лечению. Ниже мы опишем, какие прогнозы у самых распространенных видов рака на самой серьезной, 4-й стадии. На стадии, которая раньше считалась безнадежной. Раньше, но не сейчас.
Рак молочной железы прогноз
При раке молочной железы четвертой стадии, средняя 5-летняя выживаемость составляет около 25%. Но нужно понимать, что прогноз сильно зависит от объема проводимой терапии. Оптимально она должна включать в себя: паллиативную хирургическую операцию, обычно это радикальная мастэктомия.
В случаях, когда провести операцию невозможно, проводят предоперационную химиотерапию рака молочной железы, а только потом операцию. После оперативного лечения следует проведение паллиативной химиотерапии совместно с таргетной терапией (при наличии экспрессии Her2neu), которая позволяет затормозить опухолевый процесс и существенно повысить качество жизни пациентки на этом этапе.
Если же проведение химиотерапии противопоказано, то при гормонозависимом рака молочной железы возможно назначение длительной гормональной терапии. Также важно учитывать состояние органов, пораженных метастазами, и принимать меры по их поддержке.
Например, при поражении печени следует принимать гепатопротекторы (препараты, облегчающие работу печени) и т.д.
В целом, при качественном проведении всех этапов лечения процент 5-летней выживаемости при раке молочной железы резко увеличивается.
Рак легких прогноз
При четвертой стадии рака лёгкого общий показатель 5-летней выживаемости, в среднем, составляет около 16%.
При мелкоклеточном варианте рака легкого этот показатель составляет около 4%, а при немелкоклеточном раке легкого средняя выживаемость доходит до 12%.
В случае рака легких прослеживается та же самая тенденция, что и при раке молочной железы. Если ранее пациенту была выполнена радикальная операция (резекция легкого или лобэктомия), процент выживаемости резко увеличивается.
Если операция невозможна, и очаг опухоли один, его можно подвергнуть воздействию лучевой терапии. При 4-й стадии рака лёгкого лучевая терапия проводится больше с целью облегчения симптомов, чем уменьшения самой опухоли, то есть это паллиативная лучевая терапия.
В целом, общая выживаемость при раке легких в последнее время выросла незначительно, но качество жизни таких пациентов улучшилось многократно.

Рак печени прогноз
Рак печени 4-й стадии имеет наименее благоприятный прогноз, средняя 5-летняя выживаемость составляет около 9%.
Четвертая стадия рака печени характеризуется поражением большого объема ткани печени, что ведет к снижению работоспособности печени и сложностями при проведении лечения.
Рак печени является агрессивным видом рака, и для него характерно быстрое течение. Если оперативным путем опухоль удалить невозможно, в современной онкологии применяется таргетная терапия. Только потом, при неэффективности первой линии лечения, назначается классическая химиотерапия.
Совсем недавно, в практике начал применяться новый метод - химиоэмболизация печени. Смысл химиоэмболизации заключается во временном перекрытии сосудистого кровообращения печени, и введении цитостатика в ткани печени. Это позволяет доставить цитостатический препарат непосредственно сразу в ткани опухоли. Процедуру проводят только пациентам с хорошими печеночными показателями и общим самочувствием, иначе она нанесет больше вреда, чем пользы.


Также можно рассмотреть применение радиочастотной абляции очагов печени.


Рак печени 4-й стадии также характеризуется появлением асцита (жидкости в брюшной полости). Для лечения используют лапароцентез - это введение катетера в брюшную полость и постепенное извлечение асцитической жидкости.
Для предотвращения появления асцита вновь, после лапароцентеза делают внутрибрюшинное введение цитостатика.
Рак желудка прогноз
При 4-й стадии рака желудка, показатель 5-летней выживаемости составляет около 20-25%. Хороший ответ на лечение отмечен у больных плоскоклеточным раком кардиальной части желудка.
В настоящее время появилось множество эффективных схем лечения, что значительно улучшило прогноз при раке желудка.
Рак поджелудочной железы прогноз
Прогноз при раке поджелудочной железы 4-й стадии раньше действительно был крайне неблагоприятный. Средняя пятилетняя выживаемость пациентов составляла менее 2%.
Сегодня эта цифра увеличилась до 15%.
Если опухоль операбельна, то практически всегда проводят радикальную панкреатодуоденальную резекцию. Операция включает удаление поджелудочной железы, части двенадцатиперстной кишки, части желудка, жёлчного пузыря, а также лимфодиссекцию. При невозможности проведения операции, с целью нормализации оттока жёлчи, выполняется чрескожная чреспеченочная холангиостомия.
Химиотерапия при поздних стадиях рака поджелудочной железы носит паллиативный характер и направлена на повышение качества жизни, так как опухоли поджелудочной железы плохо реагируют на химиотерапевтическое лечение.

Рак кишечника прогноз
При 4й стадии рака кишечника средняя 5-летняя выживаемость варьируется от 15 до 20 %.
При операбельной опухоли проводится резекция пораженной части кишечника и выведение стомы на переднюю брюшную стенку. Если же опухоль неоперабельна, и есть признаки непроходимости кишечника, выполняется только илиостомия или сигмостомия, что восстанавливает проходимость кишечника и дает возможность проводить дальнейшее лечение.
Химиотерапия и таргетная терапия применяются как при неоперабельных вариантах рака кишечника, так и при операбельных. Для применения таргетной терапии необходимо сделать анализ на наличие мутаций (KRAS, NRAS, RAS).
В настоящее время существует множество эффективных линий химиотерапии, успешно применяемых в лечении рака кишечника 4-й стадии.

Рак предстательной железы прогноз
Рак предстательной железы 4-й стадии в последнее время стал одним из наиболее успешно поддающихся лечению, поэтому прогноз у рака предстательной железы благоприятный.
На ранних стадиях, показатель пятилетней выживаемости в Германии составляет 90%.
Средняя пятилетняя выживаемость при 4-й стадии рака предстательной железы составляет около 40%.
При операбельной опухоли выполняется трансуретральная резекция предстательной железы. Если же опухоль не операбельна, в большинстве случаев назначают гормональную терапию.
Именно при своевременной и адекватной терапии, рак предстательной железы успешно поддается лечению.
Рак яичников прогноз
Рак яичников 4й стадии в настоящее время хорошо поддается лечению и имеет благоприятный прогноз. Средняя пятилетняя выживаемость составляет около 34%.
При операбельной опухоли выполняют оментэктомию. Если же опухоль нельзя удалить хирургическим путем, то проводится химиотерапия совместно с таргетной терапией.
Если у больной раком яичников диагностирована асцитическая форма болезни, то возможно появление асцита. Для удаления асцита используют лапароцентез - это введение катетера в брюшную полость и постепенное извлечение асцитической жидкости. Для предотвращения появления асцита, после лапароцентеза возможно внутрибрюшинное введение химиопрепаратов.
В последнее время при адекватной и своевременной терапии 4-й стадии рака яичников, идет тенденция к увеличению процента выживаемости.
Рак тела матки прогноз
Рак тела матки на четвертой стадии подразумевает обширное распространение за пределы органа. Пятилетняя выживаемость при 4-й стадии рака тела матки не превышает 10%.
Лечение у пациенток с раком тела матки комплексное и включает в себя паллиативное хирургическое лечение, химиотерапию и гормональную терапию, что, в целом, делает терапию эффективной, насколько это возможно в каждой конкретной ситуации.
Рак шейки матки прогноз
При четвертой стадии рака шейки матки средняя 5-летняя выживаемость не превышает 12%.
Если опухоль операбельна, пациентке назначается операция Вертгейма. Если рак шейки матки неоперабельный, то прогноз менее благоприятный, тактика лечения будет индивидуальной и включать в себя паллиативную химиотерапию, лучевую терапию, брахитерапию.
Также в последнее время появился новый метод лечения рака шейки матки - фотодинамика, он позволяет успешно воздействовать на опухолевые клетки и тем самым повышать эффективность от лечения.
Опухоли головного мозга прогноз
При 4-й стадии опухолей головного мозга многое зависит от гистологического типа и агрессивности опухоли.
У молодых пациентов обычно прогноз лучше, чем у пациентов в возрасте. Коэффициент средней пятилетней выживаемости варьируется от 75% (для лиц в возрасте до 20 лет) до 10% (для лиц старше 75 лет).
При эпендимомах и олигодендроглиомах средняя пятилетняя выживаемость равна 85%.
Прогноз при мультиформной глиобластоме относительно неблагоприятный - средняя пятилетняя выживаемость равна 19%.
Сегодня существует множество методик хирургического удаления опухолей головного мозга, также применяются лучевая и химиотерапия.
Возможно лечение новейшими аппаратами кибер-нож и гамма-нож, которые позволяют облучить максимум опухолевой ткани и минимум здоровой.


Прогноз при лимфомах и лейкозах
При 4-й стадии рака крови многое зависит от морфологических особенностей и распространенности процесса.
Обычно лимфомы и лейкозы хорошо реагируют на медикаментозное лечение. Совокупность методов химиотерапии и лучевой терапии дает возможность получать хороший ответ и регресс опухолей.
В общем, средняя выживаемость при онкологических заболеваниях крови около 44%.
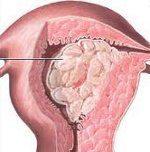
Рак тела матки – злокачественное поражение эндометрия, выстилающего полость матки. Рак тела матки проявляется кровянистыми выделениями, водянистыми белями из половых путей, болями, ацикличными или атипичными маточными кровотечениями. Клиническое распознавание рака тела матки проводят на основе данных гинекологического исследования, цитологического анализа аспиратов, УЗИ, гистероскопии с раздельным диагностическим выскабливанием, результатов гистологии. Лечение рака тела матки – комбинированное, включающее хирургический (пангистерэктомию), лучевой, гормональный, химиотерапевтический компоненты.
- Причины и этапы развития
- Классификация рака тела матки
- Симптомы рака тела матки
- Диагностика рака тела матки
- Лечение рака тела матки
- Прогноз при раке тела матки
- Профилактика
- Цены на лечение
Общие сведения
Рак тела матки занимает первое место среди злокачественных новообразований женских половых органов, а в структуре всей женской онкопатологии - промежуточное место между раком молочной железы и раком шейки матки. Тенденция к росту заболеваемости раком эндометрия в гинекологии отчасти объясняется увеличением общей продолжительности жизни женщин и времени их нахождения в постменопаузе, а также стремительным нарастанием частоты такой патологии, как хроническая гиперэстрогения, ановуляция, бесплодие, миома матки, эндометриоз и др. Чаще рак тела матки развивается у женщин перименопаузального и постменопаузального периода (средний возраст – 60-63 года).
Причины и этапы развития
В онкогинекологии этиология рака тела матки рассматривается с точки зрения нескольких гипотез. Одна из них – гормональная, связывает возникновение рака тела матки с проявлениями гиперэстрогении, эндокринных и обменных нарушений, что отмечается у 70% больных. Гиперэстрогения характеризуется ановуляторными циклами и кровотечениями, бесплодием, поздней менопаузой, опухолевыми и гиперпластическими процессами в яичниках и матке. Гормонозависимый рак тела матки чаще встречается у пациенток с ожирением, гипертонической болезнью, сахарным диабетом, феминизирующими опухолями яичника, неоднократными прерываниями беременности, получающих ЗГТ эстрогенами, имеющих отягощенную наследственную по раку яичников, эндометрия, молочной железы, толстой кишки.
Фоновыми заболеваниями для рака тела матки служат гиперплазия эндометрия, полипы матки. На фоне гиперэстрогении, как правило, развивается высокодифференцированный рак тела матки, имеющий медленный темп прогрессирования и метастазирования, который в целом протекает относительно благоприятно. Такой вариант рака эндометрия высокочувствителен к гестагенам.
Другая гипотеза опирается на данные, свидетельствующие об отсутствии эндокринно-обменных нарушений и расстройств овуляции у 30% пациенток с раком тела матки. В этих случаях онкопатология развивается на фоне атрофического процесса в эндометрии и общей депрессии иммунитета; опухоль преимущественно низкодифференцированная с высокой способностью метастазирования и нечувствительностью к препаратам гестагенового ряда. Клинически данный вариант рака тела матки протекает менее благоприятно.
Третья гипотеза связывает развитие неоплазии эндометрия с генетическими факторами.
В своем развитии рака тела матки походит этапы:
- функциональных нарушений (гиперэстрогении, ановуляции)
- морфологических фоновых изменений (железистокистозная гиперплазия эндометрия, полипы)
- морфологических предраковых изменений (атипической гиперплазии и дисплазии)
- злокачественной неоплазии
Метастазирование рака тела матки происходит по лимфогенному, гематогенному и имплантационному способу. При лимфогенном варианте поражаются паховые, подвздошные, парааортальные лимфоузлы. В случае гематогенного метастазирования отсевы опухоли обнаруживаются в легких, костях, печени. Имплантационное распространение рака тела матки возможно при прорастании опухолью миометрия и периметрия, вовлечении висцеральной брюшины, большого сальника.
Классификация рака тела матки
Согласно гистопатологической классификации, среди форм рака тела матки выделяют аденокарциному, мезонефроидную (светлоклеточную) аденокарциному; плоскоклеточный, серозный, железистоплоскоклеточный, муцинозный и недифференцированный рак.
По типу роста различают рак эндометрия с экзофитным, эндофитным и смешанным (эндоэкзофитным) ростом. По степени дифференцировки клеток рак тела матки может быть высокодифференцированным (G1), умереннодифференцированным (G2) и низкодифференцированным (G3). Наиболее часто рак тела матки локализуется в области дна, реже в области нижнего сегмента.
В клинической онкологии используются классификации по стадиям (FIGO) и системе TNM, позволяющие оценить распространенность первичной опухоли (Т), поражение лимфоузлов (N) и наличие отдаленных метастазов (М).
0 стадия (Tis) – преинвазивный рак тела матки (in situ).
I стадия (Т1) - опухоль не распространяется за пределы тела матки:
- IA (T1а) – рак тела матки инфильтрирует менее 1/2 толщи эндометрия
- IB (T1b) – рак тела матки инфильтрирует половину толщи эндометрия
- IC (T1с) – рак тела матки инфильтрирует более1/2 толщи эндометрия
II стадия (T2) – опухоль переходит на шейку матки, но не распространяется за ее границы:
- IIA (T2а) – отмечается вовлеченность эндоцервикса
- IIB (T2b) – рак инвазирует строму шейки
III стадия (T3) – характеризуется местным или регионарным распространением опухоли:
- IIIA (T3a) – распространение или метастазирование опухоли в яичник или серозную оболочку; наличие атипичных клеток в асцитическом выпоте или промывных водах
- IIIB (T3b) – распространение или метастазирование опухоли во влагалище
- IIIC (N1) – метастазирование рака тела матки в тазовые либо парааортальные лимфоузлы
IVA стадия (Т4) – распространение опухоли на слизистую толстого кишечника или мочевого пузыря.
IVB стадия (М1) – метастазирование опухоли в отдаленные лимфоузлы и органы.
Симптомы рака тела матки
При сохранной менструальной функции рак тела матки может проявляться длительными обильными менструациями, ациклическими нерегулярными кровотечениями, в связи с чем женщины могут длительное время ошибочно лечиться по поводу дисфункции яичников и бесплодия. В постменопаузе у пациенток возникают кровяные выделения скудного или обильного характера.
Кроме кровотечений при раке тела матки часто наблюдается лейкорея - обильные водянистые жидкие бели; в запущенных случаях выделения могут иметь цвет мясных помоев или гнойный характер, ихорозный (гнилостный) запах. Поздним симптомом рака тела матки служат боли внизу живота, пояснице и крестце постоянного или схваткообразного характера. Болевой синдром отмечается при вовлечении в онкопроцесс серозной оболочки матки, сдавлении параметральным инфильтратом нервных сплетений.
При нисходящем распространении рака тела матки в шейку возможно развитие стеноза цервикального канала и пиометры. В случае сдавливания мочеточника опухолевым инфильтратом возникает гидронефроз, сопровождающийся болями в области поясницы, уремией; при прорастании опухоли в мочевой пузырь отмечается гематурия. При опухолевой инвазии прямой или сигмовидной кишки возникают запоры, появляется слизь и кровь в кале. Поражение тазовых органов нередко сопровождается асцитом. При запущенном раке тела матки нередко развивается метастатический (вторичный) рак легких, печени.
Диагностика рака тела матки
Задачей диагностического этапа служит установление локализации, стадии процесса, морфологической структуры и степень дифференцировки опухоли. Гинекологическое исследование позволяет определить увеличение размеров матки, наличие инфильтрации рака параметральную и ректовагинальную клетчатку, увеличенные придатки.
Обязательным при раке тела матки является цитологическое исследование мазков цервикального канала и содержимого аспирационной биопсии из полости матки. Материал для гистологического исследования получают при помощи биопсии эндометрия микрокюреткой или раздельного диагностического выскабливания в ходе гистероскопии. УЗИ малого таза – важный диагностический скрининг-тест при раке тела матки. При ультразвуковом сканировании определяются размеры матки, ее контуры, структура миометрия, характер опухолевого роста, глубина инвазии опухоли, локализация, метастатические процессы в яичниках и лимфоузлах малого таза.
С целью визуальной оценки распространенности рака тела матки выполняют диагностическую лапароскопию. Для исключения отдаленного метастазирования рака тела матки показано включение в обследование УЗИ органов брюшной полости, рентгенографии грудной клетки, колоноскопии, цистоскопии, экскреторной урографии, КТ мочевыводящей системы и брюшной полости. При диагностике рак тела матки необходимо дифференцировать с полипами эндометрия, гиперплазией эндометрия, аденоматозом, подслизистой миомой матки.
Лечение рака тела матки
Вариант лечения при раке тела матки определяется стадией онкопроцесса, сопутствующим фоном, патогенетическим вариантом опухоли. При раке тела матки гинекология применяет методы хирургического, лучевого, гормонального, химиотерапевтического лечения.
Лечение начального рака тела матки может включать проведение абляции эндометрия – деструкции базального слоя и части подлежащего миометрия. В остальных операбельных случаях показана пангистерэктомия, или расширенное удаление матки с двусторонней аднексэктомией и лимфаденэктомией. При формировании пиометры проводится бужирование цервикального канала расширителями Гегара и эвакуация гноя.
При инвазии миометрия и распространенности рака тела матки в постоперационном периоде назначается лучевая терапия на область влагалища, малого таза, зоны регионарного метастазирования. В комплексную терапию рака тела матки по показаниям включают химиотерапию цисплатином, доксорубицином, циклофосфамидом. С учетом чувствительности опухоли к гормональной терапии назначаются курсы лечения антиэстрогенами, гестагенами, эстрогенгестагенными средствами. При органосохраняющем лечении рака тела матки (абляции эндометрия) в дальнейшем проводится индуцирование овуляторного менструального цикла с помощью комбинированных гормональных препаратов.
Прогноз при раке тела матки
Дальнейшее развитие ситуации зависит от стадии рака тела матки, возраста пациентки, патогенетического варианта и дифференцировки опухоли, наличия метастазирования и диссеминации. Более благоприятный прогноз отмечается у пациенток до 50 лет при гормонозависимом варианте рака тела матки и отсутствии метастазов: 5-летняя выживаемость в этой группе достигает 90%. Худший прогноз отмечается у женщин старше 70 лет с автономным вариантом рака тела матки – у них 5-летний порог выживаемости не превышает 60%. Выявление метастатического поражения лимфоузлов повышает вероятность прогрессирования рака эндометрия в 6 раз.
Все пациентки с раком тела матки находятся под динамическим контролем онкогинеколога и гинеколога-эндокринолога. У женщин, перенесших органосохраняющее лечение по поводу рака тела матки, после гормональной реабилитации и восстановления овуляторных циклов возможно наступление беременности. Ведение беременности у этих лиц требует учета имеющейся гинекологической ситуации. После радикального лечения рака матки путем гистерэктомии у пациенток репродуктивного возраста может развиваться постгистерэктомический синдром.
Профилактика
Комплекс превентивных мер включает устранение гиперэстрогении: контроль массы тела и течения сахарного диабета, нормализацию менструальной функции, грамотный подбор контрацепции, своевременное оперативное удаление феминизирующих опухолей и т. д.
Вторичная профилактика рака тела матки сводится к своевременному выявлению и пролечиванию фоновой и предраковой пролиферативной патологии, проведению регулярного онкоскрининга для женщин, наблюдению пациенток групп риска по раку эндометрия.
Читайте также:

