Прогностическая группа рака предстательной железы
Шкала Глисона и классификация рака простаты

Американский ученый Глисон предложил использовать шкалу для оценки рака простаты: степени злокачественности (агрессивности) клеток при карциноме предстательной железы.
Прогностическое значение имеет показатель Глисона.
Чем более дифференцированы клетки, тем благоприятнее прогноз при раке простаты.
- 1 балл соответствует самой самой высокой степени дифференциации (малоагрессивный рак предстательной железы).
- При 5 баллах по шкале Глисона – самая низкодифференцированная степень (высокоагрессивный рак простаты).
Сумма баллов по шкале Глисона
Поскольку при раке предстательной железы образуется, как правило, несколько онкологических очагов, то для изучения гистологического материала изучаются пробы двух самых больших опухолей. Изменения клеток в каждом (степень их дифференциации) оценивается по шкале от 1 до 5 баллов.
Сумма исследований двух образцов биоптата (ткани простаты, полученной при биопсии) и является индексом рака простаты по шкале Глисона. Таким образом, минимальная сумма составляет 2 балла — максимальная 10.
Для практического значения интересны следующие показатели шкалы Глисона при определении рака простаты:
- Индекс по шкале Глиссона от 2 до 6 говорит о медленнорастущем типе рака предстательной железы (опухоль малоагрессивна);
- Шкала Глиссона 7 единиц говорит о средних показателях агрессивности опухоли;
- Показатели Глиссона от 8 до 10 свидетельствуют об агрессивном типе рака простаты, большой вероятности раннего метастазирования и быстром росте и распространении рака.
Классификация рака простаты по системе TNM
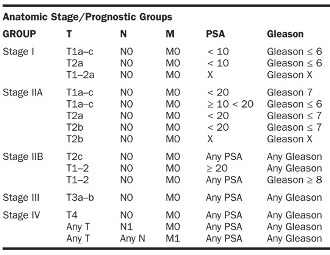
Таким образом, к примеру диагноз рак простаты T1N0M0 говорит о первой стадии заболевания, когда опухоль не пальпируется, ничем себя не проявляет и была обнаружена только при биопсии простаты. Значение T3N1M1 свидетельствует о стадии, когда уже имеются пораженные лимфатические узлы и отдаленные метастазы.
Значение Т2NxMx к примеру, говорит лишь о подозрении на вовлеченность в процесс лимфатических узлов и подозрении на метастазирование.
Таблица стадий рака простаты по классификации TNM
Прогностические факторы выживаемости больных при раке предстательной железы
Грицкевич А.А., Медведев В.Л., Костин А.А., Русаков И.Г.
В Российской Федерации рак предстательной железы (РПЖ) является одним из наиболее распространенных онкологических заболеваний у мужчин, занимая второе место после опухолей легких. Доля РПЖ в структуре онкозаболеваний составляет 14,4%. Стандартизированный показатель заболеваемости в 2015 году составил 40 на 100 000 мужчин. В РФ число мужчин, заболевших РПЖ в 2015 г., составило 38 812, тогда как в 2005 г. было зафиксировано 16 861 больных, прирост заболеваемости за последние 10 лет составил +105,7%. Важно отметить, что при общем снижении смертности от всех онкозаболеваний, смертность от РПЖ растет: в 2005 г. было 8192 летальных исходов, в 2015 г. – уже 11987. Несмотря на значительное увеличение числа больных с ранними формами заболевания, 45% пациентов при выявлении заболевания имеют местно-распространенные и метастатические формы [1].
Зная неагрессивный характер большинства типов РПЖ, а также тот простой факт, что это заболевание скорее связано с возрастом, чем с другими факторами, большой клинической проблемой является определение абсолютных показаний для назначения адекватного лечения. Риск чрезмерной диагностики и чрезмерного лечения во многих случаев РПЖ является реальным и вызывает много вопросов. В последние годы сформировалась устойчивая тенденция к изучению выбора наиболее подходящей стратегии и наиболее подходящего вида лечения РПЖ. Учитывая медленные темпы развития и прогрессирования РПЖ и возраст больных, риск смерти от сопутствующих заболеваний часто превышает риск смерти от РПЖ. В то же время лечебные вмешательства, которые проводят при РПЖ, обладают выраженными побочными эффектами и существенно влияют на качество жизни больных. В связи с этим при планировании тактики необходимо тщательно проанализировать факторы риска, связанные с одной стороны с потенциалом прогрессирования рака и с другой стороны – с состоянием соматического здоровья и ожидаемой продолжительностью жизни 5. Настоящая работа предполагает изучение прогностических факторов выживаемости для понимания адекватного клинического подхода в стратегии лечения РПЖ.
Цель исследования: улучшение результатов лечения больных РПЖ на основании выделенных факторов прогноза выживаемости в зависимости от клинико-морфологической характеристики опухоли, соматических данных, тяжести интеркуррентных заболеваний, вида лечения и осложнений.
МАТЕРИАЛЫ И МЕТОДЫ
Возраст больных на момент включения в исследование колебался от 41 до 89 лет, средний возраст – 65,4±5,2 года. В группу хирургического лечения (радикальная простатэктомия – РПЭ) включено 495 больных, в группу лучевых (гормонолучевых) методов лечения – 256 больных, в группу андрогенной депривации – 305 больных и в группу отсроченного лечения (активное наблюдение/выжидательная тактика) – 71 больной. У 447 (39,7%) больных был локализованный РПЖ, у 399 (35,4%) – местно-распространенный и у 281 (24,9%) больного – метастатический РПЖ. У 435(38,6%) больных сумма баллов по шкале Глисона (индекс Глисона) был ≤ 6 баллов, у 478 (42,4%) – 7 баллов и у 198 (17,6%) – 8-10 баллов. Из 478 больных с индексом Глисона равным 7, у 238 (21,1%) больных сумма складывалась как 3+4, и у 240 (21,3%) – как 4+3. У 16 (1,4%) больных после РПЭ при тотальном морфологическом исследовании опухоли не было обнаружено (рТ0).
При сравнении всех групп лечения по ряду клинико-морфологических и соматических признаков имели место статистически значимые отличия, связанные с селекцией больных для различных видов специального лечения из-за степени распространенности опухолевого процесса и сопутствующей патологии.
Общие сроки наблюдения за больными составили 1–213 месяцев, средний период – 43,5±10,5 месяцев. При медиане наблюдения 49 месяцев (ИКР: 31-77 месяцев) из 1127 больных 704 (62,5%) были живы. В процессе специального лечения находился 251 (22,3%) больной. За время наблюдения всего погибло 423 (37,5%) больных: 189 (16,8%) – от прогрессирования кастрат резистентного РПЖ (КРРПЖ), 228 (20,2%) – от причин, не связанных с РПЖ. От осложнений лечебных мероприятий умерло 6 (0,5%) больных: 4 (0,3%) – из группы радикальной простатэктомии и 2 (0,2%) – из группы дистанционного лучевого лечения (ДЛТ).
Для решения поставленных в исследовании задач проведен подгрупповой анализ результатов лечения локализованного, местно-распространенного и метастатического РПЖ с многофакторным анализом влияния на выживаемость больных клинико-морфологических и соматических прогностических факторов.
РЕЗУЛЬТАТЫ
Группа хирургического лечения
В группу хирургического лечения включено 325 (65,7%) больных с локализованным РПЖ, 94 (19%) больных местно-распространенным РПЖ и 76 (15,4%) больных метастатическим РПЖ .
Наличие опухолевого роста по линии резекции (ПХК) было выявлено у 15,6% больных. Наиболее частой (29,9%) локализацией являлась зона апекса предстательной железы (ПЖ). У 24,7% пациентов ПХК был отмечен в зоне шейки мочевого пузыря, у 14,3% – в боковых отделах, у 31,1% – в базальных отделах ПЖ. У 20,8% больных имел место мультифокальный ПХК. При сравнении частоты выявления ПХК у больных с интракапсулярными и экстракапсулярными опухолями отмечены статистически достоверные различия (р 20 нг/мл составила 41,2% и 38,4% , при ПСА ≤10 нг/мл – 89,8% и 88,9%, соответственно (р=0,005);
РПЖ был причиной смерти у 11 (2,2%) из 495 оперированных больных (21,6% от всех смертей после операции). Независимыми прогностическими факторами ОСВ явились:
- метастазы в лимфатические узлы. При наличии метастазов в ЛУ 5-ти и 10-летняя ОСВ составила 86,9% и 65,9% по сравнению с 99,4% и 97,5% выживаемостью при стадии N0 (р=0,012);
- множественные метастазы в лимфатические узлы. При множественном метастазировании в ЛУ уровень 5-ти и 10-летней ОСВ составил 76,4% и 0% при 97,8% и 66,9% выживаемости в случае отсутствия метастазирования (р=0,018);
- юкстарегионарное метастазирование. 5-летняя ОСВ при отсутствии метастазирования составило 99,4% и 56,0% – при метастазировании (р=0,013);
- послеоперационный индекс Глисона. 5-ти и 10-летняя ОСВ составила 99,6% и 99,3% при индексе Глисона ≤6, соответственно, и 95,7% и 91,5% при сумме баллов >6 (р=0,039);
- костные олигометастазы. Пациенты с костными олигометастазами после простатэктомии на фоне андроген-депривационной терапии (АДТ) от РПЖ не погибли (р=0,055).
За время наблюдения в группе хирургического лечения умер 51 (10,3%) больной: 11 (2,2%) – от прогрессирования КРРПЖ, 36 (7,3%) – от причин, не связанных с РПЖ. От осложнений простатэктомии умерло 4 (0,8%) больных: ОИМ (один больной; 0,2%), ТЭЛА (3 больных; 0,6%). Причины смерти приведены в таблице 1
Таблица 1. Характеристика летальности у больных после простатэктомии
Рак простаты
Рак предстательной железы (РПЖ) — злокачественная опухоль, происходящая из железистого эпителия альвеолярно-трубчатых структур преимущественно периферической зоны простаты и возникающая чаще у мужчин пожилого возраста.
РПЖ считается сегодня одной из самых серьезных медицинских проблем среди мужского населения. В Европе он является наиболее распространенным видом рака, заболеваемость которым составляет 214 случаев на 1000 мужчин, опережая рак легких и колоректальный рак. К тому же в настоящее время РПЖ занимает 2-е место среди онкологических заболеваний по смертности у мужчин. Более того, с 1985 года наблюдается небольшое увеличение числа летальных исходов от РПЖ в большинстве стран, включая регионы, в которых он нераспространен.
РПЖ встречается чаще у пожилых мужчин. В связи с этим он представляет большую проблему в развитых странах, где процент пожилых мужчин выше. Так, в развитых странах РПЖ составляет около 15 % случаев рака у мужчин, тогда как в развивающихся странах – 4 %. Следует отметить, что уровень заболеваемости РПЖ существенно различается в зависимости от региона. Например, в Швеции, которая отличается высокой продолжительностью жизни и относительно незначительной смертностью от заболеваний, связанных с курением, РПЖ – наиболее распространенная злокачественная опухоль у мужчин, на долю которой пришлось 37% всех новых случаев рака в 2004 г.
Т – первичная опухоль
Тх Недостаточно данных для оценки первичной опухоли
Т0 Первичная опухоль не определяется
Т1 Клинически не определяемая опухоль, непальпируемая и не выявляемая при визуализации (невизуализируемая)
Т1а Опухоль, случайно выявленная при патоморфологическом исследовании не более чем в 5 % удаленной ткани
Т1b Опухоль, случайно выявленная при патоморфологическом исследовании более чем в 5 % удаленной ткани
Т1с Опухоль выявлена при пункционной биопсии (выполненной, например, по поводу повышенного уровня простатспецифического антигена – ПСА)
Т2 Опухоль локализована в предстательной железе (ПЖ)1
Т2а Опухоль занимает не более половины одной доли ПЖ
Т2b Опухоль занимает более половины одной доли ПЖ, но не распространяется на 2-ю долю
Т2с Опухоль занимает обе доли ПЖ
Т3 Опухоль прорастает за пределы капсулы ПЖ2
Т3а Экстракапсулярное прорастание (1-стороннее или 2-стороннее), включая микроскопическое прорастание в шейку мочевого пузыря
Т3b Опухоль прорастает в один или оба семенных пузырька
Т4 Опухоль срастается или распространяется на окружающие ткани, помимо семенных пузырьков (к наружному сфинктеру, прямой кишке, мышцам, поднимающим задний проход, и/или передней брюшной стенке), либо прорастает в них.
N – Регионарные лимфатические узлы (ЛУ)3
Nх Недостаточно данных для оценки регионарных ЛУ
N0 Метастазы в регионарных ЛУ отсутствуют
N1 Метастазы в регионарных ЛУ
М – Отдаленные метастазы4
Мх Недостаточно данных для оценки отдаленных метастазов
М0 Отдаленные метастазы отсутствуют
М1 Отдаленные метастазы
М1а Метастазы в 1 или более нерегионарных ЛУ
М1b Метастазы в кости (-ях)
М1с Метастазы в других тканях и органах
1Опухоль, выявленная в одной или обеих долях ПЖ при помощи пункционной биопсии, но непальпируемая и невидимая при визуализации, классифицируется как T1c.
2Инвазия опухоли в верхушку или капсулу (но не за ее пределы) ПЖ классифицируется как pT2, а не как pT3.
3Метастазы до 0,2 см можно обозначить как pN1 mi.
4При наличии более 1 локализации метастазов используют более высокую стадию (стадирование следует проводить с учетом наиболее распространенного процесса).
В статье представлены международные классификации рака предстательной железы, которыми пользуются урологи и онкологи во всем мире. Это международная система TNM, шкала Глисона и система Джюит-Уайтмора, а также прогностические факторы риска по DAmico и таблицам Партина.
Классификация рака предстательной железы по системе TNM
Классификация стадий развития рака была разработана P. Denoix (Франция) в период с 1943 по 1952 года, дальше она претерпела ряд изменений, и в 2002 году было принято международное решение о прекращении внесения изменений, пока не произойдут радикальные перемены в диагностике и лечении злокачественных опухолей. Последняя классификация системе TNM была поддержана всеми национальными комитетами TNM, ей пользуются во всем мире, так как это помогает при исследованиях и интерпретации полученных результатов, а также в выработке алгоритмов лечения. Система TNM используют в постановке диагноза и определение стадии рака простаты.
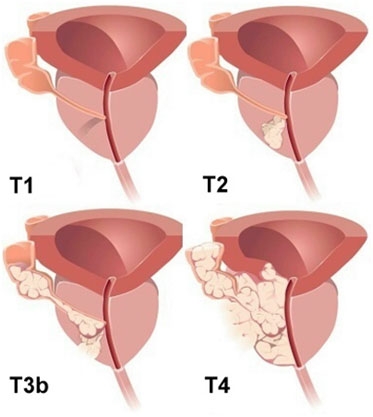
ТХ - недостаточно данных для оценки первичной опухоли.
Т0 - первичная опухоль не определяется.
Т1 - опухоль клинически не проявляется, не пальпируется и не визуализируется специальными методами.
• Т1а - опухоль случайно обнаруживается при гистологическом исследовании и составляет менее 5% резецированной ткани.
• Т1b - опухоль случайно обнаруживается при гистологическом исследовании и составляет более 5% резецированной ткани.
• Т1с - опухоль диагностируется с помощью игольной биопсии простаты (производимой в связи с высоким уровнем ПСА).
Т2 - опухоль ограничена предстательной железой или распространяется в капсулу.
• Т2а - опухоль поражает половину одной доли или меньше.
• Т2b - опухоль поражает более половины одной доли, но не обе доли.
• T2c - опухоль поражает обе доли.
Т3 - опухоль распространяется за пределы капсулы предстательной железы.
• Т3а - опухоль распространяется за пределы капсулы (одно- или двустороннее).
• Т3b - опухоль распространяется на семенной пузырек.
Т4 - несмещаемая опухоль или опухоль, распространяющаяся на соседние ткани и органы, но не на семенные пузырьки: шейку мочевого пузыря, наружный сфинктер, прямую кишку, мышцу, поднимающую задний проход, и/или тазовую стенку.
По отношению к предстательной железе регионарными лимфатическими узлами являются узлы малого таза, которые находятся ниже бифуркации общих подвздошных артерий. Категория N не имеет зависимость от стороны локализации регионарных метастазов.
NX - недостаточно данных для оценки регионарных лимфатических узлов.
N0 - метастазы в регионарных лимфатических узлах отсутствуют.
N1 - имеются метастазы в регионарных лимфатических узлах.
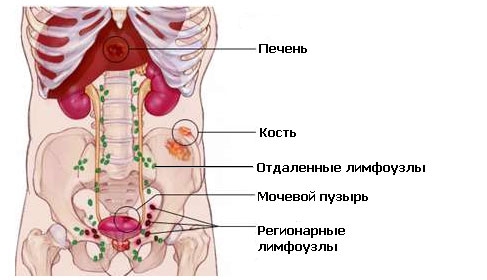
МX - определить наличие отдаленных метастазов не представляется возможным.
М0 - признаки отдаленных метастазов отсутствуют.
М1 - есть отдаленные метастазы.
• M1a - поражение нерегионарных лимфоузлов.
• M1b - присутствует поражение костей.
• M1c - присутствуют другие локализации отдаленных метастазов (лёгких, печени и т.д.).
Классификация рака простаты по шкале Глисона (Gleason score)
Шкала Глисона рассчитывает степень злокачественности опухоли, которую обнаружили при биопсии предстательной железы. Чем больше баллов получается по шкале Глисона, тем более агрессивной является опухоль. При оценки опухоли по шкале Глисона в расчет берется отличие раковых клеток, которые были получены в ходе биопсии простаты, от нормальных клеток предстательной железы. Если раковые клетки не отличаются от обычных клеток, то по шкале Глисона опухоль получает 1 балл. В противном случае, при полном различие, опухоли засчитывается максимальное количество баллов - 5.

Сумма Глисона заключается в суммировании баллов по шкале Глисона (от 1 до 5 баллов) по 2 самым большим или злокачественным опухолям, которые обнаружили в тканях предстательной железы.
• low-grade Gleason score (менее злокачественные опухоли) при сумме Глисона ≤ 6 баллам.
• intermediate Gleason score (средне-злокачественные опухоли) при сумме Глисона равной 7 баллов.
• high-grade Gleason score (сильно-злокачественные опухоли) при сумме Глисона от 8 до максимальных 10 баллов.
Для примера возьмем сумму Глисона, которая равна 5 баллам, это будет означать, что 2 самые большие или злокачественные опухоли имеют по 2 и 3 балла. То есть это менее злокачественные опухоли.
Классификация рака простаты по системе Джюит-Уайтмор
По системе Джюит-Уайтмор классификация рака предстательной железы делится на стадии А, В, С и D. Стадии А и В считаются излечимыми, а стадии С и D также лечатся, но прогноз их более неблагоприятный.
Это самая ранняя стадия. Нет никаких симптом. Раковые клетки расположены в простате.
А1 - раковые клетки хорошо дифференцируются, отмечается их умеренная аномалия.
А2 - умеренно или плохо дифференцируемые раковые клетки в нескольких местах простаты.
Опухоль не выходит за пределы простаты. Прощупывается при пальпации и/или определяется повышенный уровень ПСА.
В0 - опухоль в пределах простаты, непальпируется; уровень ПСА повышен.
В1 - одиночный опухолевый узел в одной доле простаты.
В2 - экстенсивный рост опухоли в одной или обеих долях простаты.
Опухоль выходит за пределы капсулы простаты и распространяется на соседние ткани и органы, в том числе и на семенные пузырьки.
С1 - опухоль прорастает за пределы капсулы простаты.
С2 - опухоль перекрывает просвет уретры или мочевого пузыря.
Опухоль дает метастазы в регионарные лимфоузлы или в отдаленные органы и ткани (легкие, печень, кости, желудок и т. д.).
D0 - метастазы, обнаруживаемые клинически, при этом повышается уровень ПСА.
D1 - поражаются регионарные лимфоузлы.
D2 - поражаются отдаленные лимфоузлы, органы и ткани.
D3 - метастазы после лечения.
Классификация прогностических факторов риска по DAmico
По этой классификации смотрится вероятность прогрессирования рака на начальных стадиях до клинических симптомов и/или летального исхода, а также риск возникновения рецидивов после локального лечения рака. По классификации рака предстательной железы Дамико пациентов определяют к одной из групп прогрессирования болезни: низкой, средней или высокой. Для оценки берутся следующие показатели:
- классификация рака по системе ТNM, а именно показатель Т - распространенность первичной опухоли;
- степень рака простаты по шкале Глисона,
- уровень простат-специфического антигена в крови (ПСА).
К группе низкого риска относят пациентов, у которых:
Уровень ПСА ≤ 10 нг/мл,
шкала Глисона ≤ 6 баллов,
клиническая стадия T1-2a.
К группе среднего риска относят пациентов, у которых:
Уровень ПСА 10-20 нг/мл,
Шкала Глисона – 7 баллов,
Клиническая стадия T2b.
К группе высокого риска относят пациентов, у которых:
Уровень ПСА > 20 нг/мл,
Шкала Глисона ≥ 8 баллов,
Клиническая стадия T2c-3a.
Таблицы Алана Партина или номограммы
График Партина представляет собой шкалы, которые учитывают математические модели высчитанные на основании значения уровня ПСА, баллов по шкале Глисона и клинической стадии рака простаты по классификации по системе ТNM, а именно показатель Т - распространенность первичной опухоли. График Партина позволяет прогнозировать дальнейшую прогрессию заболевания. Номограммы были составлены на основании исследования данных о мужчинах, которые проходили лечение рака предстательной железы. На основании этих данных были составлены таблицы, которые делятся:
- Степень рака простаты от Т1с до Т2с.
- По уровню ПСА в крови выделяют следующие категории от 0 до 10 нг/мл, и более 10,0 нг/мл.
- Баллы шкалы Глисона делятся на 3 категории от 2 до 4, от 5 до 6, или от 8 до 10.
Вот так выглядят модифицированные номограммы Партина, по которым можно определить вероятность дальнейшего прогрессирования рака простаты.
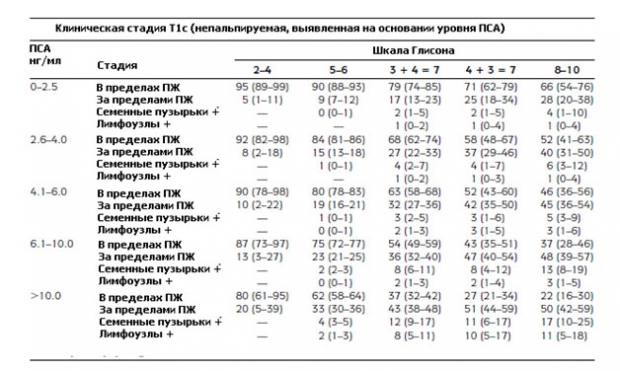
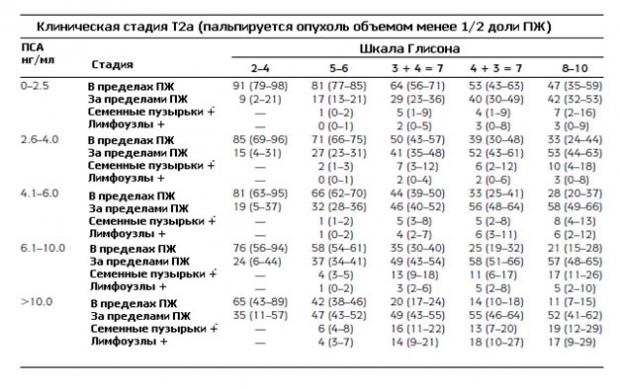
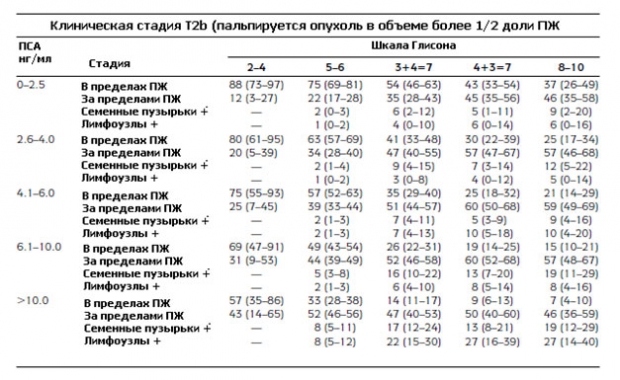
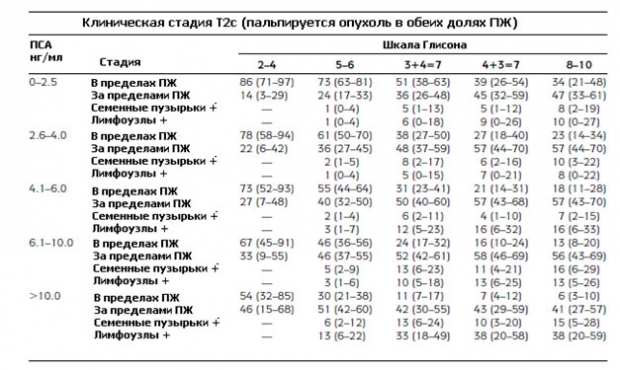
Давайте рассмотрим подробно, как пользоваться таблицами Партина. Например у пациента уровень ПСА 3,1 нг/мл, сумма по шкале Глисона 3+4=7, клиническая стадия Т2a (опухоль пальпируется и поражает меньше половины одной доли). Во второй таблице в значение ПСА ищем диапазон от 2,6-4,0 нг/мл, баллы по шкале Глисона 3+4=7. Смотрим пересечение и на 4-х строках смотрим процент прогрессирования: вероятность развития опухоли, ограниченной пределами предстательной железы составляет 50% (от 43 до 57%), рост за пределы простаты 41% (от 35 до 48%), поражение семенных пузырьков 7% (от 3 до 12%), распространение на лимфоузлы 2% (от 0 до 4%).
Для облегчения получения данных по таблицам Партина существуют компьютерные программы, где надо только ввести исходные данные.
Кроме таблиц Партина существуют номограммы Каттана, которые позволяют прогнозировать результаты лечения рака предстательной железы и делать прогноз по продолжительности жизни.
Выводы
Использование классификации для обозначения стадий рака простаты помогает онкологам определиться с тактикой лечения (сочетание методик или монотерапия: гормональная терапия рака предстательной железы, химиотерапия, лучевая терапия, хирургическая операция), сделать прогноз по прогрессированию заболевания и продолжительности жизни пациента. Кроме этого единая классификация помогает обработать выводы из разных исследований, что в свою очередь ведет к накоплению опыта и усовершенствованию существующих методов лечения и диагностики рака предстательной железы.
Рак предстательной железы – это распространенное заболевание среди мужчин старше 50 лет, занимает 3 место после злокачественных опухолей легких и желудка. Болезнь представляет проблему в онкоурологии, так как в 80-92% случаев выявляется только на 3-4 стадии. Это связано с бессимптомным протеканием патологии и неправильной организацией ранней диагностики. Наиболее распространенная форма новообразования (более 90% диагнозов) – аденокарцинома.
Узнайте симптомы на начальных стадиях, признаки рака простаты, способы лечения, прогноз – сколько живут с метастазами.
- Классификация и обозначение стадий рака ↓
- Особенности клинической картины ↓
- 1 стадия ↓
- 2 стадия ↓
- 3 и 4 стадия ↓
- Эректильная функция при раке простаты ↓
- Эффективные методы лечения и прогноз ↓
- Лечение 1 стадии рака простаты ↓
- Как проходит лечение на 2 ↓
- Лечение на 3 и 4 ↓
- Продолжительность жизни при разных стадиях рака простаты ↓

Классификация и обозначение стадий рака
По системе TNM (международный классификатор стадий злокачественных опухолей) новообразование обозначают буквами: T – первичная опухоль, N – распространение метастазов в близлежащие лимфатические узлы, M – отдаленные метастазы.
Степени рака предстательной железы обозначается буквами:
- TX – полученных данных не хватает для постановки утвердительного диагноза.
- T0 – первичная опухоль не обнаружена.
- T1 (a, b, c) – рак чаще выявляют случайно при взятии тканей на биопсию, не выявляется при других методах диагностики (пальпация, рентгенологическое исследование), не проявляется клиническими симптомами.
- T2 (a, b, c) – опухоль локализуется только в предстательной железе, поражает одну или обе доли.
- T3 (a, b) – рак выходит за границы капсулы простаты, распространяется в семенные пузырьки.
- T4 – неподвижное новообразование, рак распространяется на прямую кишку, мочевой пузырь, стенку малого и большого таза.
- NX – оценить изменения в лимфоузлах невозможно.
- N0 – метастазы в лимфатической системе отсутствуют.
- N1-N2 – региональные узлы поражены метастазами.
- MX – нет возможности выявить отдаленные метастазы.
- M0 – признаков наличия метастазов нет.
- M1(a, b, c) – отдаленные метастазы в лимфоузлах, костях, других внутренних органах.

Особенности клинической картины
Для злокачественной опухоли предстательной железы характерно длительное латентное течение. Специфических симптомов, отличающих патологию от других заболеваний, нет.
Рак простаты на этапе зарождения протекает бессимптомно. Мужчина не испытывает никакого дискомфорта при мочеиспускании, эректильная функция и трудоспособность не нарушена.
При осмотре (пальпации) уролога отсутствуют такой признак, как увеличение железы. На лабораторных анализах общие показатели крови и мочи в норме.


Признаки второй стадии рака:
- Начало акта мочеиспускания затруднено;
- Прерывистая или слабая струя урины;
- Недержание;
- Болезненность, жжение при семяизвержении, опорожнении пузыря;
- Частые позывы к мочеиспусканию;
- Эректильная дисфункция;
- Наличие крови или семенной жидкости в моче;
- Боли над лобком, в области промежности, в тазу, связанные с нарушением оттока мочи и ее скоплением в почечной лоханке.

Симптомы заболевания на поздних стадиях обусловлены наличием метастазов в близлежащие и отдаленные внутренние органы.
Мужчины испытывают стойкие, постоянно длящиеся тупые боли в ребрах, позвоночнике. Эти признаки напрямую указывают на метастазы в костной системе. Из-за лимфостаза (застоя лимфы) появляются отеки нижних конечностей.
На последних стадиях мужчины стремительно теряют в весе на фоне крайнего истощения организма, развивается анемия. Пациенты физически слабые, вялые, происходят изменения в психике больных.
Сохранение эрекция – один из важных вопросов, который беспокоит мужчин с опухолями простаты. Предстоящее лечение и его воздействие на функциональность предстательной железы тревожит мужчин всех возрастов.
В зависимости от методики лечения, эректильная дисфункция наблюдается у 14-97% пациентов. Малоинвазивная дистанционная радиотерапия позволяет избежать проблемы 80% мужчинам.
После радикального удаления дисфункция сохраняется у 70% пациентов. Такой метод лечения не является приговором. Если хирург выбрал правильную тактику и сохранил нервно-сосудистый комплекс, это сохраняет эрекцию на высоком уровне. При этом мужчина должен выполнять одно условие – систематический прием ингибиторов ФДЭ (препараты для лечения эректильной дисфункции).
Эффективные методы лечения и прогноз
Варианты лечения опухоли предстательной железы зависят от степени запущенности патологии. Нет клинических выводов о том, что какой-то один из методов превосходит другие. Комплекс и схемы терапии подбирает врач в индивидуальном порядке.

В начале зарождения опухоли, когда отсутствуют симптомы, и нет возможности дифференцировать атипичные клетки, рекомендуют активное наблюдение пациента. Мужчинам молодого возраста при точном определении злокачественного процесса проводят радикальную простатэктомию (полное удаление). Если опухоль трудно дифференцировать, назначают лучевую терапию. Прогноз благоприятный с долгой продолжительностью жизни.
Если по показаниям пациенту нельзя проводить операцию, прибегают к малоинвазивным методикам – брахитерапия простаты, высокоинтенсивная фокусированная УЗ-абляция, криоабляция. Но в этом случае есть высокий риск рецидива заболевания.
Стандартное лечение включает такие методики:
![]()
Радикальная простатэктомия;- Лучевая терапия – при противопоказаниях к хирургическому лечению, ослабленным пациентам с хроническими внутренними болезнями;
- Гормональная терапия;
- Комбинированные методы – научных отчетов об улучшении выживаемости пациентов нет, лучшим вариантом считают гормонотерапию в течение 2-3 лет в сочетании с облучением.
Прогноз благоприятный, выживаемость более 10 лет.
Выработка мужских гормонов провоцирует стремительное разрастание опухоли и распространению метастазов. Поэтому пациентам проводят энуклеацию яичек – удаление части органа, продуцирующего тестостерон.
Параллельно проводят химиотерапию и гормонотерапию.

Для пациентов, проходивших лечение на первой стадии, велика вероятность полного излечения, продолжительность жизни у 86% случаях – более 10 лет.
На второй стадии при удачно проведенном лечении жизнь мужчины продлится долго без негативных последствий для репродуктивной функции. Для пациентов с плохо дифференцированным раком, ослабленным, пожилым после облучения прогноз составляет от 5 до 10 лет.
Выживаемость после разных способов лечения рака простаты:
- простатэктомия – 10 лет и более до 55-60% пациентов, 5 лет – 74-82%;
- лучевая терапия – 10-летний прогноз у 48% больных, 5-летний – 80%;
- после удаления яичек при постоянной гормональной терапии – выживаемость 5 лет у 55% пациентов.
Для своевременного выявления рака предстательной железы мужчинам старше 45 лет рекомендуют обследование у уролога раз в год. Скрининг включает пальцевой (ректальный) метод, трансректальное ультразвуковое исследование, лабораторные анализы на определение простатического специфического антигена.
Читайте также:


