Профессиональный рак легких может вызвать воздействие

Профессиональный рак – злокачественные опухоли различной локализации, которые возникают в результате длительного контакта со специфическими канцерогенами при выполнении профессиональных обязанностей и выявляются у людей определенных специальностей достоверно чаще, чем в среднем по популяции. Располагаются в области различных органов, чаще всего выявляются поражения кожи, легких, верхних дыхательных путей и мочевого пузыря. При постановке диагноза учитываются анамнез, клинические данные и результаты дополнительных исследований. Тактика лечения определяется типом, локализацией и стадией опухоли. Большое значение имеют профилактические мероприятия.

- Причины развития профессионального рака
- Диагностика профессионального рака
- Профилактика профессионального рака
- Цены на лечение
Общие сведения
Профессиональный рак – группа злокачественных новообразований, развивающихся под действием производственных канцерогенов. Могут поражать практически любые органы и системы. Нередко развиваются через годы и даже десятилетия после прекращения контакта с канцерогеном, что усложняет дифференцировку профессиональных раков и непрофессиональных онкологических заболеваний и требует тщательного сбора анамнеза. Средняя продолжительность временного отрезка между началом воздействия канцерогена и появлением первых симптомов профессионального рака составляет от 15 до 18 лет.
Отмечается взаимное усиление неблагоприятного влияния профессиональных вредностей и других факторов риска (неблагоприятной экологической обстановки, особенностей образа жизни и пр.). Важнейшей задачей врачей различных специальностей, осуществляющих мониторинг состояния здоровья работников различных предприятий, является разработка адекватных мер профилактики, позволяющих снизить риск развития профессиональных раков. Лечение осуществляют онкологи, дерматологи, отоларингологи, пульмонологи, гастроэнтерологи и т. д. (в зависимости от локализации онкологического поражения).
Долгое время статистические данные о заболеваемости профессиональным раком в нашей стране не соответствовали действительности. Профессиональным факторам риска уделялось недостаточно внимания, отсутствовала специальная экспертиза по оценке условий труда и выявлению связи между развитием рака и действием канцерогенов при выполнении пациентом своих должностных обязанностей. За период с 1963 по 1986 год в России было диагностировано всего 160 онкологических поражений, обусловленных профессиональными вредностями. Между тем, исследователи указывают, что реальная доля профессиональных раков в общей структуре онкологической заболеваемости составляет около 4%.
Отсутствие единой отлаженной системы выявления профессиональных злокачественных новообразований усложняет разработку профилактических мер и своевременное обнаружение заболеваний этой группы. Вместе с тем, в настоящее время исследователи отмечают две тенденции, связанные с возникновением профессионального рака. Первая – постоянное увеличение количества специальностей, ассоциированных с развитием профессиональных онкологических заболеваний. Вторая – частые случаи обнаружения профессиональных раков, ранее считавшихся нетипичными для того или иного канцерогена. Все перечисленное повышает значимость теоретических исследований и практических действий по решению проблем, связанных с диагностикой и профилактикой данной группы заболеваний.

Причины развития профессионального рака
Причиной развития профессионального рака являются соматические мутации, возникающие под влиянием различных (в основном химических) канцерогенов. Онкологи выделяют органы-мишени, страдающие при воздействии тех или иных канцерогенных соединений. Риск развития рака кожи увеличивается при длительном профессиональном контакте с асфальтом, парафинами, битумом, смолой, дегтем, мышьяком и минеральными маслами. Кроме того, профессиональным раком кожи страдают специалисты, получающие повышенные дозы ионизирующего излучения, и люди, работающие на открытом воздухе, в условиях чрезмерной инсоляции, высокой влажности и низких температур.
Профессиональный рак верхних дыхательных путей провоцируется контактом с хромом, соединениями никеля, древесной пылью, а также аэрозольными формами серной кислоты и газовыми фазами некоторых смол. Злокачественные опухоли легких, трахеи и бронхов возникают под воздействием мышьяка, соединений хрома, кадмия и никеля, технических эфиров, пыли радиоактивных руд, газов дизельных двигателей и аэрозолей, содержащих бензапирен, тальк или асбест. Профессиональный рак мочевого пузыря диагностируется у специалистов, участвующих в переработке нефтяной и каменноугольной смолы, перегонке каменного угля, газификации угля, производстве толуидина, органических красителей и резиновых изделий.
Профессиональный рак желудка выявляется у сотрудников нефтеперерабатывающих производств, предприятий по изготовлению резиновых, графитовых и угольных изделий. Риск возникновения профессионального рака печени повышается при работе с радиоактивными веществами (плутонием, торием, полонием) и производстве винилхлорида. Злокачественные поражения системы кроветворения, а также опухоли спинного и головного мозга диагностируются у работников нефтехимических и нефтеперерабатывающих производств, предприятий по производству винилхлорида, изготовлению резины и резиновых изделий. Новообразования костей обнаруживаются у лиц, контактирующих с радиоактивными соединениями.
Большинство онкологических заболеваний развивается под действием нескольких факторов. Профессиональные раки не являются исключением из этого правила. При сочетании контакта с профессиональными канцерогенами и других неблагоприятных воздействий вероятность возникновения опухолей существенно возрастает. К воздействиям, увеличивающим риск возникновения профессионального рака, относятся проживание в регионах с неблагоприятной экологической обстановкой, курение, злоупотребление алкоголем, нарушения иммунитета и т. п. В числе прочих факторов риска исследователи отмечают мужской пол. Установлено, что мужчины страдают профессиональным раком чаще женщин, что может быть связано как с различными условиями труда (наличием большего количества профессиональных вредностей), так и с более высокой распространенностью вредных привычек у представителей сильного пола.
Диагностика профессионального рака
Диагноз профессионального рака выставляют при участии профпатолога с учетом анамнеза, клинической симптоматики, данных лабораторных и инструментальных исследований. При этом большое внимание уделяют различным аспектам профессиональной деятельности больного, в первую очередь – интенсивности воздействия и продолжительности экспозиции канцерогена. Кроме того, в процессе диагностики профессионального рака учитывают результаты предшествующих медицинских осмотров, наличие профессиональных заболеваний и продолжительность периода между началом воздействия канцерогена и появлением клинической симптоматики заболевания.
В остальном диагностические мероприятия по выявлению профессионального рака соответствуют стандартам диагностики непрофессиональных онкологических заболеваний аналогичной локализации. При выявлении раков кожи используют данные внешнего осмотра, гистологического или цитологического исследования. При подозрении на профессиональный рак легких и бронхов назначают бронхоскопию, КТ и рентгенографию органов грудной клетки. При опухолях верхних дыхательных путей проводят риноскопию, фарингоскопию и микроларингоскопию. При профессиональном раке мочевого пузыря применяют КТ мочевого пузыря, УЗИ мочевого пузыря и цистоскопию. При новообразованиях пищеварительной системы используют УЗИ, КТ, МРТ брюшной полости и эндоскопические методики.
Профилактика профессионального рака
Комплекс мер по предупреждению профессионального рака включает в себя разработку теоретических положений и две основные группы практических профилактических мероприятий: медицинские и немедицинские. Теоретические положения представляют собой требования к возрасту, полу и состоянию здоровья специалистов, занятых на вредных производствах, и перечень обязательных мер, позволяющих снизить уровень риска развития профессионального рака и других профессиональных заболеваний.
Немедицинские профилактические мероприятия включают в себя исключение или минимизацию использования канцерогенов в различных производственных процессах, установку вентиляционных систем, контроль над соблюдением правил индивидуальной защиты (использованием спецодежды, противогазов, респираторов), разъяснительную работу с сотрудниками предприятий и пр. Медицинские мероприятия по профилактике профессионального рака предполагают обязательное медицинское обследование перед началом работы и регулярные медосмотры через определенные периоды времени.
К элементам медицинской профилактики профессиональных раков также относят лечение и реабилитацию пациентов с хроническими заболеваниями, вызванными воздействием профессиональных канцерогенов (хроническим бронхитом, силикозом, асбестозом, хроническим гастритом и др.). При необходимости больным обеспечивают щадящие условия труда, разъясняют важность отказа от вредных привычек, увеличивающих риск развития профессионального рака, рекомендуют специальную диету, осуществляют стационарное и амбулаторное лечение обострений, выдают путевки в специализированные санатории и т. д.
- Сервисы
- Пресс-центр
- Кабинет

Просмотр, проверка и анализ результатов аттестации рабочих мест.
Обследования состояния здоровья работников с использованием дистанционных технологий.

Прохождение обучения по охране труда без отрыва от производства.
Сервис находится в разработке.
![]()
![]()

![]()
Профессиональные онкологические заболевания работников, вызванные вредным воздействием производственных факторов
31 августа 2018 г.
Теория канцерогенеза впервые была описана в 1775 г. П. ПОТТОМ. С этого момента стало известно, что каменноугольные смолы являются канцерогенными агентами. Механизм действия этого агента в то время объясняли хроническим неспецифическим раздражением тканей, согласно Р. ВИРХОВУ. В результате воздействия смолы на кожу наступали некробиоз и некроз ткани, длительное воспаление, на почве которого происходила повторная извращенная регенерация, переходившая в предопухолевую пролиферацию. Следует подчеркнуть, что и в то время многие экспериментальные наблюдения не укладывались в эту концепцию. Так, смазывание кожи мышей канцерогенной смолой приводило к возникновению опухолей не только на месте смазывания, но и в некоторых отдаленных органах – молочных, сальных железах, в легких.

В 1895 г. появились сообщения о развитии рака мочевого пузыря у рабочих анилинокрасочной промышленности, а в конце XIX – начале XX столетия было описано развитие рака легких у горных рабочих Шнееберговских копий в Саксонии и Яхимовских рудников в Чехословакии. В дальнейшем была показана возможность развития профессионального рака и вследствие воздействия других промышленных вредностей, в частности химических веществ и физических агентов.
В настоящее время известно более 100 химических соединений, способных вызвать опухоли у животных. Есть основания думать, что аналогичное действие могут оказывать эти соединения и на организм человека. Большинство из этих веществ не имеет между собой химического сродства, они относятся к органическим и неорганическим соединениям.
Наиболее распространенными и активными канцерогенами из неорганических соединений считаются следующие:
— полициклические ароматические углеводороды (7,12-диметилбензатрацен, 3,4-бензпирен, 20-метилхолантрен и др.);
— химические красители, широко применяемые в промышленности (2-нафтил-амин, 2-аминофлюорен, 4-аминодифелин, аминоазокрасители, 4-аминостильбен, 4-диметиламиноазобензол, бензидин, ортоаминоазотолуол);
— нитрозосоединения – алифатические циклические соединения, обязательно имеющие в своей структуре аминогруппу (диметилнитрозамин, диэтилнитрозамин, N-метил-N-нитро-N-нитрозогуанидин, нитрозометилмочевина и др.);
— гетероциклические ароматические углеводороды (1,2,5,6-дибензакридин, 1,2,5,6- и 3,3,5,6-дибензокарбазол и др.);
— прочие (четыреххлористый углерод, этионин, уретан, тиоацетамид, эпоксиды, металлы, пластмассы, никель, мышьяк, асбест, соединения хрома, бериллий).

ХИМИЧЕСКАЯ СТРУКТУРА И ЭТИОПАТОГЕНЕЗ КАНЦЕРОГЕНОВ
При рассмотрении химической структуры канцерогенов видно, насколько различна их природа, а многие из этих веществ инертны. При проведении исследований было установлено, что большинство химических канцерогенов приобретают способность вызывать опухоли после метаболической активации в организме животных и человека. Известно, что у рабочих анилинокрасочных производств, имеющих контакт с 2-нафтиламином, часто возникает профессиональный рак мочевого пузыря. Добавление в пищу этого канцерогена собакам приводит к развитию рака мочевого пузыря. Однако, если 2-нафтиламин вводят непосредственно в полость этого органа, рак мочевого пузыря не развивается. Выяснилось, что 2-нафтиламин метаболизирует в печени с образованием 2-амино-1-нафтола, который в виде соединения с глюкуроновой кислотой выводится с мочой. В мочевом пузыре под влиянием глюкуронидазы это соединение расщепляется, и 2-амино-1-нафтол высвобождается. Последний и является истинным, или конечным, канцерогеном, а 2-нафтиламин — лишь проканцерогеном.
Изучение механизмов действия большинства химических канцерогенов показало, что они почти все являются только проканцерогенами, а активизируются только в организме, после чего возникают метаболиты с бластогенной (образование клеток, которые дают начало раковым клеткам) активностью.
Считается, что нитрозамидам, лактонам, галаэфирам для проявления бластомогенного действия не требуется предварительного преобразования в условиях организма, поэтому их рассматривают как прямые канцерогены.
.jpg)
В настоящее время доподлинно известно, что химические канцерогены необратимо реагируют с ДНК и РНК клетки. Большинство канцерогенов разных классов образуют in vivo комплексы с нуклеиновыми кислотами, причем количество связанного с ними канцерогена достигает максимума в первые сутки после поступления в организм, которые сохраняются достаточно длительно. Алкилирующие продукты метаболизма нитрозаминов, этионина, циказина, некоторых ароматических аминов in vivo чаще всего взаимодействуют с атомом азота гуанина в седьмом положении (строение ДНК). Атака этого атома азота в количественном отношении является главной и часто рассматривается как мера реакционной способности канцерогена. Однако следует отметить, что атомы углерода и кислорода гуанина, находящиеся в 1-м, 3-м и 7-м положениях, и цитозина в 3-м положении могут быть также местами присоединения канцерогенов. Пока еще не известно, атакуемость какого атома имеет критическое значение для проявления канцерогенного действия.
Еще не выяснено место присоединения к молекулам нуклеиновых кислот афлотоксина, четыреххлористого углерода и некоторых алкалоидов. Строгая избирательность взаимодействия отдельных канцерогенов с ДНК или РНК не установлена, хотя производные азокрасителей, циказин, аминоакридины связываются преимущественно с ДНК, тогда как некоторые другие канцерогены (этионин, диазометан и др.) интенсивнее связываются с РНК. Выдвигаются предположения, что связывание с ДНК, а не с РНК или белком имеет существенное значение для проявления инициирующей способности канцерогенов.
В конечном итоге прямые и конечные канцерогены действуют на молекулярный аппарат, ответственный за размножение, дифференцировку и наследственность клеток. Следует подчеркнуть, однако, что пока мало данных о том, что же происходит в клетке после активации канцерогенов и взаимодействия их с ДНК и РНК.
На этот счет существуют 2 теории: генетическая и эпигенетическая. Согласно первой теории в процессе малигнизации (перерождения в клетки злокачественной опухоли) нормальных клеток под действием канцерогенов происходит модификация генетического материала, т.е. нуклеиновых кислот. По второй теории в процессе химического канцерогенеза изменениям подвергаются главным образом белки, что влияет на транскрипцию ДНК, т.е. на генную экспрессию.
В последнее время особое внимание уделяется исследованию процессов репарации ДНК – устранению вызванных канцерогенами нарушений в структуре ДНК. Уже в первые часы после введения канцерогены вызывают разрывы отдельных спиралей ДНК. В результате репарации ДНК происходят элиминация и замена измененных нуклеотидов (структурная единица молекулы ДНК) путем ресинтеза удаленных участков и присоединения вновь синтезированных нуклеотидных последовательностей к ДНК. Восстановление ДНК обеспечивается сложным ферментным аппаратом, включающим эндо- и экзонуклеазы, щелочную фосфатазу и ДНК-полимеразу. Репарация ДНК, если она полноценна, может в значительной степени лимитировать канцерогенез. Недостаточность и незавершенность репарации ДНК могут повлечь за собой эпигеномные изменения, нарушение матричных свойств этого полинуклеотида, количественно и качественно изменить синтез РНК, что может быть одной из причин малигнизации клеток и роста опухоли.
Канцерогенез – многоэтапный процесс. От начальных нарушений, возникающих в пострадавших от канцерогена клетках, до появления измененных злокачественных клеток проходит значительный период времени, который сопровождается сложными структурно-химическими перестройками в клетках и сменой нескольких клеточных поколений. Несмотря на важную роль начальных инициирующих изменений нуклеиновых кислот и белков под действием канцерогенов, необходимо знать, что их недостаточно для развития опухолей. Онкогенез тесно связан с иммунной системой организма, его гормональным гомеостазом и многими другими факторами.
Кроме экзогенных канцерогенных веществ, имеются эндогенные канцерогены. Учение об эндогенном бластомогенезе, то есть о возможности образования в организме химических веществ, которые могут вызвать развитие опухоли, было научно обосновано 40-45 лет назад. Знаменитым этапом в развитии учения об эндогенных химических канцерогенах явились работы Л.М. ШАБАДА и его учеников 1937-1938 гг., в которых впервые были приведены доказательства (впоследствии подтвержденные зарубежными исследователями) наличия активных канцерогенных веществ в бензольных экстрактах из тканей умерших от рака. В настоящее время учение об эндогенных бластомогенных веществах обогатилось новым содержанием в связи с установлением их конкретной химической природы. Доказаны бластомогенные свойства эндогенно образующихся веществ – метаболитов триптофана и тирозина.

Бластомогенными свойствами обладают некоторые физические факторы, в наибольшей степени – ионизирующая и ультрафиолетовая радиации. Данное действие ионизирующего излучения известно давно. Вскоре после открытия К. РЕНТГЕНОМ Х-лучей появились сообщения о раке кожи у людей, принимавших участие в изготовлении и испытании излучающих трубок.
В дальнейшем было установлено, что наследственные изменения могут быть вызваны также всеми другими видами проникающей радиации. Излучения вызывают в клетках ионизацию, в результате которой одни атомы теряют электроны, а другие присоединяют их, образуются отрицательно и положительно заряженные ионы. Если подобный процесс внутримолекулярной перестройки возникает в хромосомах, могут произойти генные мутации и структурные хромосомные перестройки. Кроме того, в результате облучения образуются свободные радикалы в результате радиолиза находящейся в тканях воды, которые обладают высокой реакционной способностью в отношении многих макромолекулярных соединений, прежде всего ДНК и РНК. Однако окончательный механизм бластомогенного действия радиации недостаточно изучен. В нижеизложенном материале остановимся поподробнее на онкологических заболеваниях, вызванных профессиональными вредностями.
Подавляющее большинство профессиональных опухолей составляют рак кожи, рак легких, рак мочевого пузыря. Достаточно редко встречается рак других локализаций – гортани, пищевода, желчных проходов, а также саркома печени и других органов. Локализация профессиональных опухолей характеризуется некоторыми особенностями. Так, профессиональный рак кожи локализуется чаще всего на не закрытых одеждой участках кожи.

Видное место среди профессиональных видов рака занимает рак легких, развивающийся при хроническом вдыхании различных пылей, газов и паров. При некоторых пневмокониозах опухоль чаще всего возникает на участках наибольшего развития склероза. Особую локализацию опухоли отмечают при раке от никеля. Многие из этих опухолей происходят, помимо легких, из носовых ходов, решетчатой кости. Канцерогенные вещества (бензидин), выделяющиеся из организма через органы мочевыделения, вызывают рак мочевого пузыря.
Большинство профессиональных видов рака возникают после длительного воздействия канцерогенных факторов. Латентный период исчисляется годами, нередко десятками лет. Рак часто развивается у рабочих спустя длительный срок после оставления ими своей профессии. Очень редко наблюдается необычайно быстрое развитие опухоли после однократного воздействия вредного вещества.
Почти во всех случаях возникновению профессионального рака предшествуют предраковые изменения в виде папиллом, лейкоплакий слизистых оболочек. Гистологически в этих случаях отмечают метаплазию и атипическое разрастание эпителия. Имеются данные мультицентричного возникновения профессионального рака, например в легких при асбестозе.
Существует мнение, что профессиональный рак редко дает метастазы. В известной мере это относится к раку кожи и мочевого пузыря, но рак легких часто сопровождается метастазами в различные органы.
(основана на локализации опухоли и характере
контакта с канцерогенным фактором).
Опухоли, возникающие от непосредственного контакта с тем или иным веществом:
— опухоли кожи, вызываемые непосредственным воздействием на нее минеральных масел, необработанного парафина, креозота, антрацена, ультрафиолетовых и ренгеновых лучей, радиоактивных веществ;
— опухоли легких, возникающие от вдыхания радиоактивных субстанций, пыли асбеста, соединений хрома, никеля (никель-карбонила), мышьяка, смол, иприта и др.;
— опухоли носовых ходов, решетчатой кости, возникающие от воздействия радиоактивных веществ, никель-карбонила;
— рак верхних отделов пищеварительного тракта, вызываемый мышьяком, некоторыми индустриальными канцерогенными веществами, действующими большей частью непосредственно на слизистые оболочки при их соприкосновении с последними.
— эпителиальные опухоли кожи, возникающие от принимаемых внутрь соединений мышьяка; — опухоли мочеполовой системы, возникающие от воздействия некоторых ароматических аминов при их выделении с мочой.
Опухоли, возникающие при отложении канцерогенных веществ в тканях:
— рак кожи, обусловленный отложением в ее тканях соединений мышьяка;
— саркомы костей, вызываемые отложением в них радиоактивных веществ.
Опухоли тканей, обладающих особой чувствительностью к некоторым канцерогенным факторам: бластоматозные и бластомоподобные реакции (лейкемии) гемопоэтической ткани, возникающие от воздействия рентгеновских лучей, радиоактивных веществ, бензола и химически родственных ему веществ.
Рак мочевого пузыря, печени, толстого кишечника, вызываемый некоторыми гельминтами, живущими в этих органах (трематода Shistosomum haematobium, Schistosomum japonicum), проникающими в организм при земледельческих работах.
К числу гипотетических канцерогенных агентов, повышающих риск развития немелкоклеточного рака легкого, относят акрилонитрил, хлорметиловые эфиры, соединения некоторых металлов (железо, кадмий, хром, никель), кремния, мышьяка, а также формальдегид, пестициды, бумажную и древесную пыль, горчичный газ.
Экспозиция этих канцерогенов чаще всего связана с профессиональной деятельностью (J.F. Fraumeni, W.J. Blot). Установлена мультипликативная связь большинства указанных веществ с курением. Курение повышает риск развития плоско-, крупно- и мелкоклеточного рака.
Большинство профессиональных канцерогенов обусловливает развитие новообразований определенного гистологического типа. Так, очевидна строгая корреляция между воздействием хлорметилового эфира и развитием мелкоклеточного рака легкого.
Соединения кремния, испарения металлов, формальдегид — факторы риска у рабочих предприятий по производству стали. В аналитических исследованиях показаны причинно-следственные отношения интенсивности и продолжительности воздействия указанных агентов и степеней риска, а при метаанализе выявлена их количественная зависимость.
Высокая заболеваемость немелкоклеточным раком легкого отмечена среди рабочих производств по очистке, плавлению, электролизу сульфатов, оксидов, растворимых (но не чисто металлических) форм никеля. Схожие результаты получены при изучении влияния длительного контакта с соединениями меди. Доказано канцерогенное действие соединений шестивалентного хрома, проявляющееся в повышении риска развития рака легкого у работников соответствующих производств и красильной промышленности.
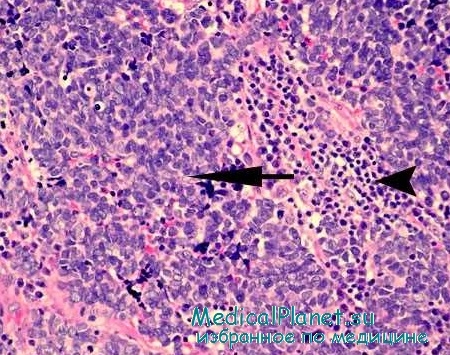
M.G. Ott и соавт. установили относительное увеличение смертности от мелкоклеточного рака легких рабочих, в процессе профессиональной деятельности подвергающихся воздействию неорганических солей мышьяка высоких концентраций. Эти данные приобретают особое значение в связи со все более широким применением инсектицидов и гербицидов, содержащих мышьяк. Использованием мышьяковистых пестицидов объясняют высокие уровни заболеваемости раком легкого среди виноградарей Франции и Германии. Риск развития рака легкого у рабочих, занятых в производстве инсектицидов и гербицидов, в 2,5 раза выше, чем в контрольной группе.
Еще во второй половине 1960-х гг. был выявлен повышенный риск развития рака легкого у рабочих, подвергающихся воздействию хлорметиловых эфиров, широко используемых в производстве ионообменных смол. О канцерогенах данного вида собран обширный материал: доказана зависимость доза-эффект, выявлено преобладание среди обусловливаемых ими новообразований опухолей мелкоклеточного и анапластического гистотипов, закономерности возрастного распределения заболевших, альтерация с другими канцерогенами. Показано, что хлорметиловые эфиры могут активизировать канцерогенез как в ранних, так и в поздних стадиях.
Канцерогенное действие иприта доказано при изучении заболеваемости немелкоклеточным раком легких среди рабочих предприятий военной промышленности и лиц, пострадавших при использовании его в период военных действий. Опухоли локализуются в верхних отделах дыхательного тракта и главных бронхах. Преобладают недифференцированные формы.
Одним из наиболее канцерогенных факторов, повышающих риск развития рака легкого, служит асбестоз — диффузный интерстициальный фиброз легких, развивающийся в результате систематического вдыхания пыли асбеста. Минералы асбестовой группы имеют волокнистую структуру и расщепляются на прочные эластические волокна.
Попадание в легкие ингаляционным путем натуральных асбестовых, а также искусственных минеральных волокон любого типа — фактор риска развития рака легкого всех гистологических типов. Опухоли чаще локализуются в периферических отделах и нижних долях легких. Механизмы индукции пролиферативных процессов не определены, но показано, что асбестовая пыль не является мутагеном. Ее канцерогенная активность связана с физическим воздействием, и наиболее вредоносны тонкие длинные волокна, пенетрирующие легочную ткань.
Асбест широко применяли во многих отраслях промышленности: горнорудной, текстильной, производстве цемента и строительных материалов. В некоторых профессионально экспонированных группах рак легкого служит причиной смерти до 20 % членов наблюдаемой когорты. Немелкоклеточный рак легких у контактировавших с асбестом рабочих развивается почти исключительно у лиц с асбестозом. Сходную ситуацию отмечают при силикозе.
Читайте также:



