Продолжительность жизни после химиотерапии рака кишечника
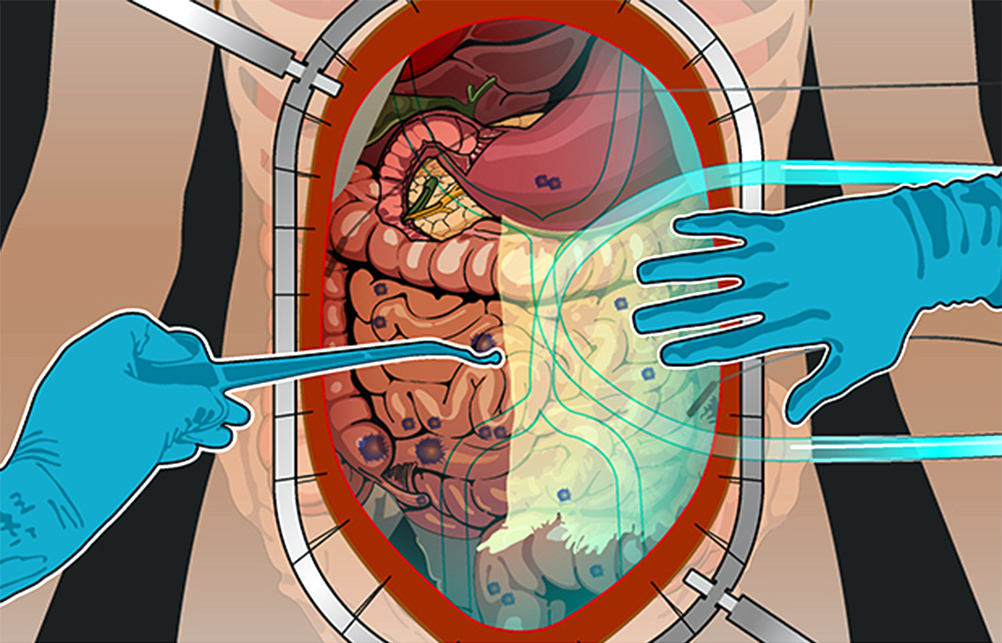
Средняя продолжительность жизни при карциноматозе брюшины без лечения – от 1,5 до 6 месяцев. Лечить же таких больных еще совсем недавно было нечем. Ни хирургия, ни химиотерапия не справлялись. Пациентов признавали инкурабельными (неизлечимыми). Показатель 5-летней выживаемости в начале 90-х был практически равен 0.
Но последние 20 лет активно развивается методика лечения перитонеального канцероматоза с применением HIPEC (англ. hyperthermic intraperitoneal chemotherapy) – гипертермической интраперитонеальной (внутрибрюшинной) химиотерапии. Методика дает отличные результаты: увеличивает 5-летнюю выживаемость до 40-50%, а иногда дает полное излечение.
Самое плохое – даже многие врачи не знают, что при канцероматозе существует способ продлить жизнь. Поэтому сегодня мы расскажем про HIPEC подробно: кому это поможет, какие дает результаты и сколько стоит.
Цель – уничтожить максимум опухолевых клеток, которые неизбежно останутся даже после самого тщательного хирургического удаления очагов и спровоцируют рецидив.
Свойства, которые делают HIPEC действительно уникальной методикой, мы разъясним чуть ниже, а сначала определимся, при каких диагнозах она может помочь и почему она иногда оказывается единственным способом продлить жизнь человеку на последних стадиях рака.
При каких опухолях образуется канцероматоз брюшины, и почему он так опасен
В брюшную полость распространяются многие из часто встречающихся видов рака.
- рак яичников – в 60-70% случаев приводит к канцероматозу;
- рак желудка – канцероматоз в 40-50% случаев;
- рак поджелудочной железы – в 30-40% случаев;
- рак толстой и прямой кишки (колоректальный рак) – в 10-15% случаев;
- рак печени;
- рак шейки матки;
- рак червеобразного отростка (аппендикса);
- редкие первичные опухоли брюшины (мезотелиома и псевдомиксома).
Все эти злокачественные новообразования распространяют раковые клетки либо когда первичная опухоль физически прорастает в брюшную полость, либо вместе с током крови и лимфы – иногда это происходит во время хирургических операций по поводу первичных опухолей.
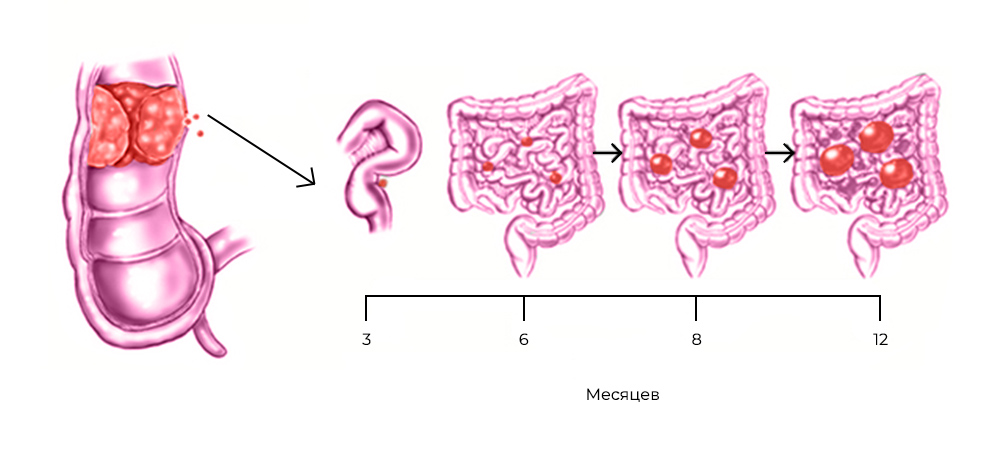
Развитие канцероматоза при колоректальном раке: из прямой кишки в брюшную полость
Стоит раковым клеткам попасть в полость, ограниченную брюшиной – они, скорее всего, дадут начало вторичным опухолям, метастазам. Перитонеальная ткань – богатый источник факторов роста и комфортная среда для их развития. Микроскопические метастазы распространяются по поверхности брюшины, поражают внутренние органы.
Метастазы нарушают кровоток и лимфоток, лишают внутренние органы питания и пространства, зачастую становятся причиной непроходимостей (например, кишечной, или сдавливают мочеточники). Кроме того, это провоцирует асцит – выпот и скопление жидкости в брюшной полости – наиболее распространенный симптом при канцероматозе.
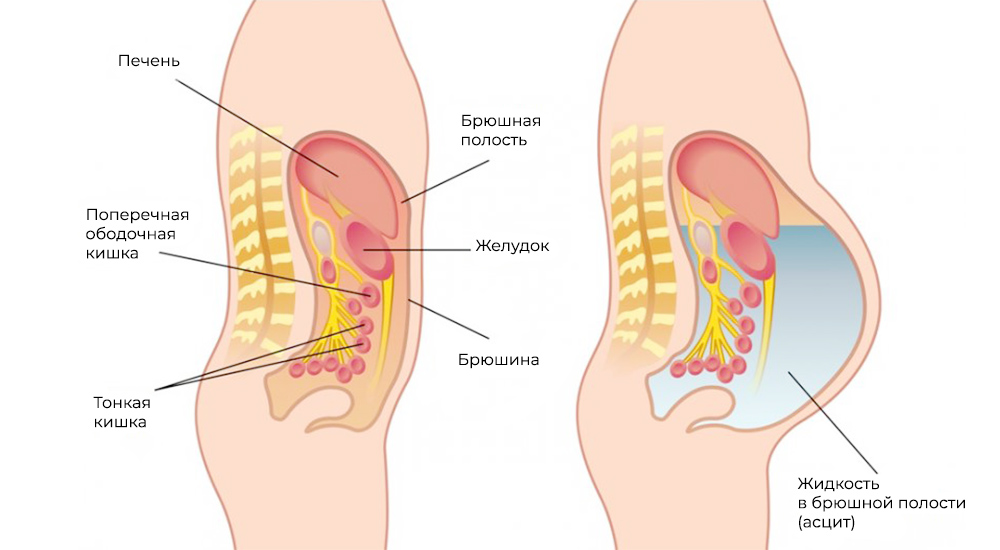
Асцит – скопление жидкости в брюшной полости
Застой крови и лимфы, интоксикация, сдавление внутренних органов метастазами и/или скопившейся жидкостью при асците – это причины, почему пациенты с канцероматозом без лечения не проживают и года.
На протяжении почти всей истории онкологии считалось, что перитонеальный карциноматоз и опухоли брюшины не поддаются никакому из существующих видов лечения.
Лучевая терапия в лечении канцероматоза не применяется, поскольку высокие дозы облучения такой обширной области живота опасны для пациента еще более серьезными осложнениями.
Хирургическое лечение малоэффективно, т.к. метастазы на поверхности брюшины могут быть микроскопического размера, либо расположены в недоступных местах, и врач не видит их во время операции. А для быстрого рецидива канцероматоза достаточно и единичных раковых клеток, оставшихся в полости брюшины.
Системная химиотерапия почти не дает чувствительного воздействия на опухоли брюшины –опухолевые очаги размером до 3 мм (таких при канцероматозе большинство) практически не развивают систему собственных кровеносных сосудов – и поэтому слабо доступны для системной внутривенной химиотерапии.
Вводить химиотерапию в более высоких дозах, чтобы повысить концентрацию препаратов в перитонеальной области – невозможно, т.к. это может необратимо навредить остальным органам и тканям, до которых доберется перенасыщенный химиопрепаратом кровоток.
Во второй половине 20 века появились первые работы, рассказывающие о возможностях применения внутрибрюшинной химиотерапии. Последние 20 лет это направление активно развивается, а создал его еще в 80-х годах XX века американский хирург-онколог Пол Шугабейкер – он первым придумал совместить циторедуктивную операцию с горячей химиотерапией, вводимой непосредственно в брюшную полость. И это дало результат
Гипертермия – это повышение температуры.
- Высокая температура сама по себе способна вызывать повреждение и гибель опухолевых клеток. К тому же, делает их более уязвимыми для действия химиопрепаратов: усиливает проницаемость клеточных мембран.
- Причем чувствительность увеличивается избирательно – опухолевые клетки начинают гибнуть при температуре 40 °C, а здоровые – сохраняются до 44°C. В условиях гипертермии особенности опухолевых тканей (иное кровоснабжение, степень оксигенации, особенности репарации ДНК) становятся для них не преимуществом, а слабым местом.
- Кроме того, повышение температуры обычно вызывает иммунную реакцию: растет количество лимфоцитов – клеток иммунитета, способных уничтожать опухолевые клетки. В плазме крове увеличивается уровень интерлейкинов, интерферонов, факторов некроза опухоли и т.д. Все они имеют собственную противоопухолевую активность, и дополнительно способны усиливать эффект некоторых химиопрепаратов.
- Еще один важный плюс гипертермии – она способствует более активному проникновению препарата в ткани – на глубину до 3 мм – этого хватит, чтобы охватить большинство микро-метастазов, которые останутся после хирургической операции.
Внутри брюшины – химиотерапия работает лучше. Для HIPEC используются стандартные химиопрепараты, но их локальное применение при перитонеальном карциноматозе – куда эффективнее.
Процедура HIPEC – это, строго говоря, вторая половина целого комплекса мероприятий. Без циторедуктивной хирургической операции HIPEC может проводиться в считанном количестве случаев по особым показаниям. Обычно процедура – продолжение хирургической операции, которое дает серьезное улучшение прогноза выживаемости.
Вместе с удалением опухолевых очагов, все вмешательство занимает от 6 до 18 часов. Процесс можно разделить на 4 этапа.
1) Ревизия брюшной полости. Проводится она для того, чтобы понять, показано ли лечение с помощью HIPEC для этого пациента, принесет ли оно увеличение продолжительности жизни и улучшение ее качества. Во время ревизии хирург внимательно осматривает брюшную полость и определяет перитонеальный индекс рака (peritoneal cancer index – PCI).
Чтобы его рассчитать, брюшную полость и тонкую кишку условно делят на 13 областей-квадрантов, в каждом из них оценивают самый крупный опухолевый очаг по шкале от 0 до 3:
- очагов не обнаружено — 0 баллов;
- очаги размером менее 0,5 см — 1 балл;
- очаги размером менее 0,5–5 см — 2 балла;
- очаг более 5 см или несколько узлов меньшего размера— 3 балла.
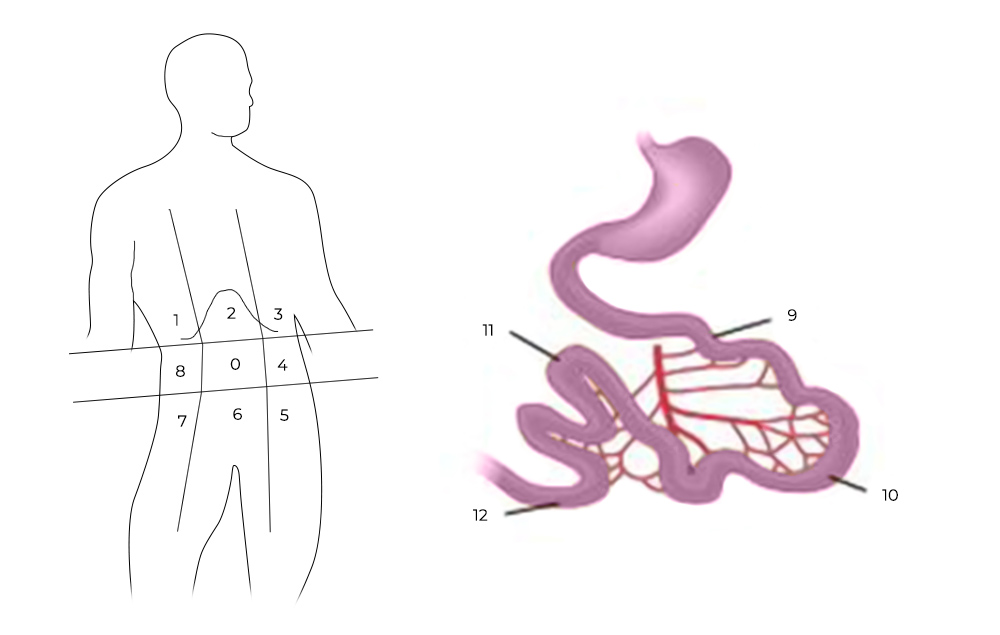
Разделение брюшной полости на участки для определения PCI
Баллы суммируются по всем квадрантам – это и есть значение PCI. Чем больше баллов – тем хуже прогноз. Если PCI выше критического (принимая во внимание тип опухоли и состояние пациента) – то и операцию, и процедуру HIPEC могут признать нецелесообразными.
Проводят ревизию интраоперационно – т.е. непосредственно перед проведением основной операции. В некоторых случаях ее можно провести в виде отдельной диагностической лапароскопической операции – малотравматичной, через небольшие проколы в стенке живота.
2) Циторедуктивная операция. Если по результатам ревизии PCI оценен как удовлетворительный, то хирург приступает к удалению всех видимых и пальпируемых (те, что чувствуются наощупь) опухолевых узлов.
Удаляют отдельные участки брюшины, орган, в котором находится первичная опухоль, соседние внутренние органы или их части, если они тоже поражены метастазами. Часто это участки кишечника, селезенка, желчный пузырь.
3) Гипертермическая интраперитонеальная химиотерапия. Собственно, HIPEC. В брюшную полость вводят катетеры и температурные датчики, соединенные со специальным аппаратом и емкостью с раствором химиопрепарата. Эта перфузионная система (под контролем врачей, конечно) поддерживает заданную температуру и давление циркулирующей жидкости. Раствор химиопрепарата в течение 60–90 минут циркулирует в брюшной полости пациента.
После процедуры препарат удаляют из брюшной полости, промывают ее физраствором, удаляют датчики и катетеры.
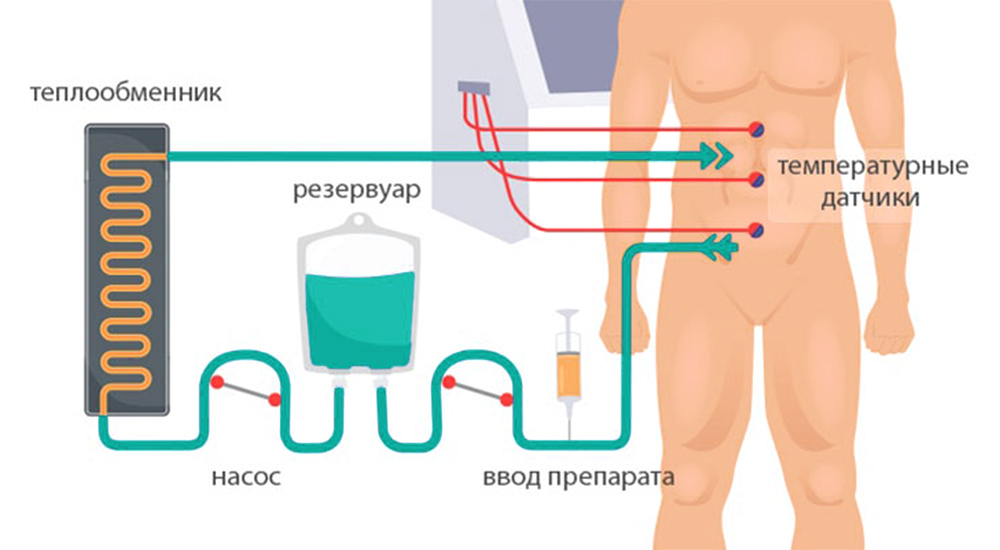
Схема проведения HIPEC
4) Реконструктивная операция. Если удалены части кишечника, хирург восстанавливает непрерывность кишки – формирует анастомоз, выводит верхний конец толстой/тонкой/слепой кишки на поверхность живота для отхождения каловых масс.
В среднем, в клинике пациент проводит 2-4 недели. Через 2-3 недели после операции проводится контрольное обследование. Его необходимо повторять через 3 месяца, и постепенно частоту проверок снижают до 1 раза в год.
В этом видео наши коллеги проводят процедуру HIPEC пациентке с раком яичников.
Как любое лечение, HIPEC имеет риски и противопоказания
Послеоперационный период стоит отдельным этапом, но он не менее важен. Мы всегда понимаем, насколько сложным для наших пациентов (а многие попадают к нам в крайне тяжелом состоянии) может быть период восстановления после такого длительного и достаточно агрессивного вмешательства, как циторедуктивная операция + HIPEC. Поэтому сразу после операции мы переводим пациента в отделение интенсивной терапии, под круглосуточное наблюдение.
Осложнения могут быть те же, что и после любого хирургического вмешательства на брюшной полости, поэтому за пациентом внимательно следят на случай появления признаков кровотечения или воспаления послеоперационной раны – и готовы в любую минуту оказать помощь.
Побочные действия от химиотерапевтического препарата при внутрибрюшной гипертермической химиотерапии даже менее выражены, чем при внутривенном введении – при том, что дозировки, а значит, и противоопухолевое действие, при HIPEC в десятки раз выше.
К сожалению, при всем нашем желании и мастерстве наших хирургов, есть пациенты, для которых полезный эффект вмешательства не оправдает сложностей послеоперационного восстановления.
Чтобы циторедуктивная операция с последующей процедурой HIPEC была эффективной, нужно соблюдение нескольких условий:
- Пациент должен быть в состоянии перенести и хирургическую операцию, и химиотерапию одновременно. Возраст или показатели здоровья не должны этому препятствовать – например, не должно быть почечной или печеночной недостаточности. Перед процедурой мы обязательно всесторонне обследуем пациента.
- Процесс распространения метастазов должен быть ограничен только брюшной полостью. Если есть метастазы в других органах, которые нельзя удалить – они будут распространяться дальше, и сведут эффект HIPEC на нет.
- Метастазы размером более 2,5 мм не должны покрывать всю поверхность брюшины – удалить их все будет невозможно.
Мы провели ей циторедуктивную операцию и процедуру HIPEC, и после этого она уже 10 месяцев живет без прогрессирования заболевания.
В некоторых случаях HIPEC приводит к устойчивому излечению. Например, коллеги из США сообщали о женщине с мезотелиомой брюшины. С помощью HIPEC она преодолела болезнь, уже 3 года живет без признаков рака и смогла родить ребенка.

Jessica Blackford-Cleeton, которой HIPEC позволила выжить и стать мамой.
К сожалению, HIPEC пока применяется в считанном количестве клиник. Причин этому несколько, и они характерны для всех новых технологичных способов лечения.
- Методика все еще считается инновационной, не все врачи имеют нужный опыт работы. К тому же, для проведения процедуры нужен не 1 и не 2, а целая бригада медиков самой высокой квалификации – это длительная, сложная и напряженная операция.
- Оборудование дорогое, не все страны и не все клиники могут потратиться на перфузионную систему и расходные материалы.
- Врачи бывают довольно консервативны. Кто-то считает, что процедура требует более подробного изучения. А кто-то из них не любит участвовать в проведении гипертермической химиотерапией, потому что опасается за собственное здоровье – испарения химиопрепаратов во время HIPEC могут быть вредными для медиков, которые при этом присутствуют. Хотя, в целом, испарения из закрытого контура минимальны, негативные последствия, даже если есть – не являются необратимыми, врачу нужно лишь более внимательно следить за состоянием почек и печени.
Однако более 70 ведущих хирургов-онкологов из 55 онкоцентров в 14 странах мира, включая США (где и родилась эта процедура), Канаду, Францию и Великобританию, пришли к выводу о том, что HIPEC может существенно повысить ожидаемую продолжительность жизни у пациентов, страдающих канцероматозом, особенно при колоректальном раке.
Клинические исследования из разных стран показывали результаты, когда пациенты после лечения канцероматоза брюшины с применением HIPEC жили 7 лет при опухолях аппендикса, более 5 лет при мезотелиоме брюшины, 5 лет при колоректальном раке, 2 года при раке яичников – тогда как при стандартном лечении их выживаемость колебалась от 2 до 14 месяцев.
Мы в свою очередь убедились в эффективности HIPEC на собственном обширном клиническом опыте. Мы надеемся, что через несколько лет HIPEC будет внедряться в стандарты лечения по ОМС и станет доступна по всей стране. А пока – мы даем пациентам возможность не искать подобную помощь за рубежом, а получить ее в Москве.
Прогнозы жизни при онкологии кишечника индивидуальны, но, в то же время, связаны с основными факторами: стадией, на которой было выявлено новообразование, расположением и типом опухоли, наличием сопутствующих заболеваний, методикой лечения. Всемирные статистические данные.
Прогнозы жизни при онкологии кишечника индивидуальны, но, в то же время, связаны с основными факторами: стадией, на которой было выявлено новообразование, расположением и типом опухоли, наличием сопутствующих заболеваний, методикой лечения. Всемирные статистические данные постоянно обновляются и позволяют предположить, насколько успешным будет лечение на каждой стадии.
Поскольку ответ на вопрос сколько живут с раком кишечника зависит от физического размера первичной опухоли и качественного выявления метастазов, важно вовремя пройти специальное обследование при появлении настораживающих симптомов: постоянной боли в животе и проблем со стулом, появлении крови или гноя в кале.
При выявлении болезни на первой стадии прогнозы при онкологии толстой кишки максимально благоприятны. Согласно данным Национального института рака, 5-тилетняя выживаемость достигает 92 %.
Это означает, что при проведении лечения согласно стандартному протоколу более 92 % заболевших людей хорошо его перенесут, достигнут ремиссии и успешно проживут после этого более пяти лет.
Прогнозы при онкологии отделов кишечника 2 стадии напрямую зависят от масштабов поражения злокачественной опухолью стенки кишки. На стадии 2a заболевание поражает стенку кишки полностью, но не выходит за ее пределы. При этом онкологический очаг можно четко отделить от окружающих тканей, что повышает эффективность оперативного лечения.
На стадии 2b опухоль переходит на соседние органы – печень, мочевой пузырь, матку у женщин. Относительно благоприятный прогноз и высокая продолжительность жизни при раке кишечника связаны с полным отсутствием метастазов в других участках тела или распространения онкологического заболевания по лимфатической системе.
Согласно данным Национального института рака, 5-тилетняя выживаемость на этой стадии рака кишечника достигает 87 % на стадии 2a и 63 % на стадии 2b. При этом женщины имеют более благоприятный прогноз при поражении различных отделов кишечника – это связано с особенностями роста опухолевого очага на фоне влияния женских половых гормонов. Изучая цифры статистики, стоит помнить о том, что они, по сути, отражают ситуацию пятилетней давности. Хирургические методики постоянно совершенствуются, позволяя устранять патологические очаги более тщательно, а иногда и выполнять малоинвазивные оперативные вмешательства. Соответственно, с течением времени накопятся обновленные, более благоприятные и актуальные, статистические данные.
Понимание того, сколько живут больные раком кишечника, и какую именно методику лечения стоит выбрать, основывается на результатах предварительного медицинского обследования. Важно максимально корректно определить стадию заболевания и не пропустить его распространение в абдоминальной полости, метастазирование в другие органы или вовлечение в патологический процесс лимфоузлов.
То, сколько лет осталось прожить пациенту с онкологией кишечника, определяется профессионализмом оперирующего врача и полнотой выполнения операции. В случае полноценного удаления онкологического очага период послеоперационного восстановления протекает легче, а в перспективе требуется минимальный курс химиотерапии.
Прогноз и клинические признаки онкологического поражения кишечника зависят от размера и расположения опухоли в стенке толстой кишки в сочетании с количеством и расположением пораженных лимфоузлов. На стадии 3a опухолевое образование достигает небольшого размера и располагается преимущественно в просвете кишечника, она не влияет на смежные органы. Несмотря на это, при тщательном обследовании доктор выявляет распространение процесса на близкорасположенные лимфоузлы. При этом прогноз онкологии кишечника на стадии 3a относительно благоприятен – 89 % заболевших преодолевают 5-летний рубеж вслед за точной постановкой диагноза.
Следующая стадия, 3b, отличается большим размером опухоли и ее более агрессивным распространением по стенке кишечникам и органам брюшной полости. На то, сколько лет живут пациенты с раком кишечника 3b стадии, дополнительно влияет развитие осложнений заболевания.
К наиболее частым осложнениям относятся:
- Острая непроходимость кишечника, которая чаще развивается при расположении новообразования в начальных отделах кишечника
- Инфекционные осложнения, флегмоны и абсцессы забрюшинной клетчатки
- Симптомы поражения смежных с опухолью органов
Сколько лет проживут пациенты с онкологией толстой кишки этой стадии – 5-летная выживаемость достигает 69 %.
Стадия 3с отличается от предыдущих стадий распространением патологического процесса на большое количество лимфоузлов. В то же время сама опухоль может быть компактной, не выходить за пределы кишки и не приводить к развитию типичных осложнений. Невозможность полного удаления всех онкологических очагов на стадии 3с снижает 5-летнюю выживаемость до 53 %. В этом случае за хирургическим лечением обязательно последует второй этап – полихимиотерапия. Современные фармакологические разработки позволяют улучшить ожидания в отношении того, сколько времени проживет пациент с онкологией кишечника.
Важная отличительная черта стадии 4 – выявление метастазов в отдаленных участках тела. На ранних стадиях метастазы формируются в печени, через которую проходит кровь от органов абдоминальной полости и малого таза. Реже очаги появляются в легких, половых органах, костях, поджелудочной железе и надпочечниках. Число и локализация метастазов существенно влияют на то, сколько времени живут пациенты с онкологией кишечника на 4 стадии. В частности, при поражении легких применяются дополнительные методики – интенсифицированный курс полихимиотерапии либо же эмболизация метастазов химиопрепаратами. По ответу на лечение, уменьшению метастазов в размерах или их полному исчезновению на КТ / МРТ, доктор может определить, сколько времени осталось жить пациенту с 4 стадией онкологии кишки.
Согласно данным Национального института рака, 5-тилетняя выживаемость пациентов с онкологией кишечника 4 стадии достигает лишь 11 %. Зачастую это обусловлено поздним диагностированием рака или некорректным подбором индивидуального лечения. Несмотря на неутешительные статистические данные, прогнозы при онкологии кишки 4 стадии крайне индивидуальны.
Наибольшее значение имеют следующие факторы:
- Возраст, у пациентов в возрасте до 60 лет шансы на восстановление более высоки
- Пол, при этом прогноз более благоприятен у мужчин
- Наличие сопутствующих заболеваний, наиболее важны в этом отношении нарушения функции печени и почек, состояние сердечно-сосудистой системы
- Наличие онкологии в анамнезе, при первичном диагностировании прогноз при раке кишечника 4 стадии более благоприятен
- Чувствительность опухолевых клеток к химиотерапии
Для прогнозирования того, сколько осталось прожить пациенту с раком кишечника 4 стадии, важно оценивать не только медицинские факторы и возможность проведения специализированного лечения, но и психо-эмоциональный настрой пациента. Безусловно, важно своевременно выполнить операцию, а также провести химиотерапию для борьбы с метастазами. Тем не менее, грамотная психологическая поддержка помогает человеку найти силы для борьбы с болезнью и поверить в достижимость ремиссии.
Имеет значение не только то, сколько времени живут пациенты при онкологии кишечника 4 степени, но и качество и полноценность жизни.
- Посещение индивидуальных и групповых сеансов поддерживающей психотерапии
- Подбор лечащим врачом грамотного режима физической нагрузки
- Общение с пациентами в посвященных заболеванию сообществах, знакомство с теми, кто вылечился от заболевания
К сожалению, в определенных ситуациях заболевание быстро распространяется и не отвечает на лечение. То, как быстро умирают от рака кишечника, зависит от осложнений заболевания и возможности их лечения.
Наиболее грозными осложнениями и частыми причинами смерти являются:
- Хроническая интоксикация продуктами распада опухоли
- Кровотечение из сосудов опухоли или пораженных ею органов
- Поражение метастазами жизненно важных органов (головной мозг, печень, почки)
Стоит помнить, что симптомы новообразований кишечника не всегда легко распознать. При отсутствии тщательного обследования пациенты могут длительно получать бесполезные медикаменты от колита или хронического панкреатита, в то время, как умирают от рака кишечника.
В настоящее время отмечается рост числа больных раком толстой кишки преимущественно за счет роста злокачественных опухолей ободочной кишки. Результаты лечения нельзя признать удовлетворительными, если делать только операцию и химиотерапию. Нужно подключать все возможности противоопухолевого лечения в комплексе: операция, химиотерапия, общая электромагнитная гипертермия.

Болезнь течет бессимптомно. И до того момента, как опухоль достигает большого размера и появляются осложнения в виде анемии или непроходимости кишечника, клиническая симптоматика отсутствует. Поэтому больные обращаются к врачам поздно, диагноз ставится преимущественно в 3 и 4 стадии болезни.
Рак толстой кишки: поможет ли операция?
Согласно принятым в России клиническим рекомендациям, сначала выполняются операции: резекция/гемиколэктомия/субтотальная колэктомия в зависимости от расположения опухоли и распространенности процесса. На практике хирургическое вмешательство носит в лучшем случае паллиативный характер. Например, при проявлении непроходимости – освободить проход; при проявлении выраженной анемии – ликвидировать кровотечение. Сама опухоль в этом случае может быть удалена, но, как правило, в организме уже есть метастазы. Поэтому операция не остановит онкологию кишечника. Необходима противоопухолевая терапия.
Химиотерапия рака толстой кишки
Применяемые схемы введения химиопрепаратов на основе оксалиплатина и фторпиримидинов, иринотекана и бевацизумаба в России и за границей приносят незначительный эффект. Не более чем у 15 процентов больных может быть получена ремиссия заболевания. Т.е. у остальных 85 процентов химиотерапией не удается сдержать развитие опухоли и метастазирования при раке толстой кишки.
Если после 2-3 курсов проводимой химиотерапии в рамках стандартного лечения по ОМС нет заметной положительной динамики, улучшения самочувствия, уменьшения размеров опухоли и метастазов, то следует задуматься о необходимости усиления химиотерапии нагревом. Дальнейшее продолжение стандартной химиотерапии при отсутствии динамики, даже со сменой химиопрепаратов, приведет только к устойчивости опухоли толстой кишки к лекарствам.
Усиление химиотерапии температурой: какой прогноз?
Улучшить результаты лечения можно усилив химиотерапию методом общей электромагнитной гипертермии. В этом случае на опухоль и метастазы губительной действие оказывают два фактора – высокая температура и химиопрепараты, которые под нагревом лучше проникают в ткани злокачественных новообразований.
Более оптимистичный прогноз при диагнозе рак толстой кишки дает предоперационная химиотерапия (неоадъювантно) в условиях нагрева при гипертермии. Это позволяет уменьшить размеры и подавить рост первичной опухоли и метастазов, например, в печени, до операции. Затем выполнить операцию, которая становится более радикальной, а не паллиативной (симптоматической). Проведение дальнейшего противоопухолевого лечения, позволяет получать лучшие результаты, чем при традиционной схеме:
- операция после гипертермии с химиотерапией не дает такого агрессивного всплеска метастазирования и роста опухоли, как без нее. Опухолевые клетки уже не имеют первоначальной жизнеспособности к делению и росту – активность подавлена.
- размер опухоли уменьшается, позволяя в ходе оперативного вмешательства удалить более радикально затронутые злокачественным процессом ткани.
- Если изначально обнаруженная опухоль не удалима, то проведение лечения до операции позволяет перевести опухоль в операбельное состояние.
Послеоперационные курсы лечения гипертермией с химиотерапией позволят максимально остановить рост опухоли и метастазов.
Рак сигмовидной кишки
В толстой кишке выделяют отделы: слепая кишка, восходящая кишка, печеночный угол, поперечно-ободочная кишка, селезеночный угол, нисходящая кишка и сигмовидная кишка.
Наиболее часто рак локализуется в сигмовидной кишке. Лечение рака сигмовидной кишки отличается от рака других отделов кишечника только объемом операции. Если при раке слепой, восходящей кишки, печеночного и селезеночного угла, нисходящей кишки минимальной операцией является геликолэктомия (удаление от половины толстой кишки до 3 отделов), при раке поперечно-ободочной кишки возможна резекция (участок или также геликолэктомия), при раке сигмовидной кишки наиболее часто выполняется резекция, поскольку эта кишка имеет довольно длинную брыжейку и особенности кровоснабжения таковы, что возможно удаление только пораженного участка кишки.
Непосредственные результаты лечения рака толстой кишки гипертермией:
Если сравнивать результаты при раке прямой или толстой кишки, то наблюдается разница. В первом случае мы можем получить эффект в виде полного исчезновение или уменьшения опухоли и метастазов более чем в два раза. При онкологическом заболевании толстой кишки, не удается получить заметных результатов, но продолжительность жизни этих больных увеличивается. Улучшается самочувствие и качество жизни.
Оценка результатов проводилась через месяц после процедуры. Учитывались пациенты с запущенным раком и обширными метастазами, у которых на фоне проведенного в других больницах лечения отмечалось прогрессирование на нескольких линиях химиотерапии. В клинике “К-тест” рак толстой кишки лечат методом общей электромагнитной гипертермии более 25 лет.
Больные раком толстой кишки принимаются из всех регионов России и зарубежья. Для размещения пациентов и их сопровождающих созданы комфортные условия.
Выживаемость после лечения рака толстой кишки общей гипертермией?
Показатель выживаемости, % | 1 год | 3 года | 5 лет |
| Рак толстой (ободочной) кишки, 4-я стадия | 64,5 | 15,2 | 15,2 |
| Рак прямой кишки, 4-я стадия | 61,3 | 52,5 | 27,3 |
Закрытие колостомы
Нередко больные с диагнозом рак толстой кишки обращаются к нам после уже проведенной операции колостомирования, имеют отдаленные метастазы в брюшной полости, в печени. На операции удалена первичная опухоль, наложена колостома.
Возникает вопрос, когда закрывать колостому и можно ли ее закрывать? Опыт профессора Карева И.Д. показывает что нужно проводить гипертермию и химиотерапию, чтобы подавить метастазы и после этого уже производить закрытие колостомы. Если же выполнять закрытие колостомы без гипертермии с химиотерапией через 3 месяца, как в стандарте, то это приводит к агрессивному усилению роста метастазов.
Читайте также:

