Причинами позднего выявления злокачественного новообразования могут быть



Показатель запущенности является одним из основных критериев качества диагностики онкологических заболеваний в учреждениях общей лечебной сети [1]. Одной из важных проблем остается позднее выявление злокачественных новообразований в амбулаторно-поликлинических учреждениях, в том числе и в Новосибирской области. При первичном обращении пациентов к врачу запущенные формы рака (III-IV стадии) уже имеют более 70% пациентов с раком ободочной кишки и более 60% пациентов с раком прямой кишки, при этом хирургическому лечению подвергается около 40% больных [2]. По данным Российского онкологического научного центра им. Н.Н. Блохина, среди онкологических заболеваний в России колоректальный рак (КРР) находится на 3 месте: у мужчин – после рака легких и желудка, у женщин – после рака молочных желез и желудка. В Санкт-Петербурге рак ободочной кишки встречается в 22,5% у мужчин, в 17,7% у женщин. Около 85% случаев КРР приходится на возраст старше 55 лет, максимальная заболеваемость наблюдается у пациентов старше 70 лет. Несмотря на инновации последних лет, современную диагностическую аппаратуру, новые химиопрепараты и методики, пятилетняя выживаемость больных КРР в России не превышает 40% [3].
По данным Новосибирского областного клинического онкологического диспансера, за 2015 год показатель запущенности злокачественных новообразований вырос на 4,3% по сравнению с 2014 и составил 21,6% (2014 г. – 20,7%), при этом запущенный рак прямой кишки выявлялся в 41,3% случаев по сравнению с 48,3% в РФ [4]. Рост заболеваемости КРР в России, вероятно, связан со старением населения.
Цель работы – изучить адекватность выполнения должностных рекомендаций по скринингу колоректального рака у пациентов с впервые диагностированным заболеванием (по архивным историям болезней двух крупных лечебных учреждений города Новосибирска) и установить ведущие причины поздней диагностики КРР.
Материалы и методы
Статистическая обработка данных выполнена с использованием программы SPSS, ver.17. Определялся характер распределения количественных признаков методом Колмогорова-Смирнова. В случае нормального распределения вычислялось среднее значение (М) и стандартная ошибка среднего (m). Достоверность различия показателей оценивали по критериям Стьюдента, Пирсона (при нормальном распределении), в случаях отклонения распределения от нормального использовались непараметрические критерии (U-критерий Манна-Уитни, Колмогорова-Смирнова, хи-квадрат). Во всех процедурах статистического анализа критический уровень значимости нулевой гипотезы (p) принимался равным 0,05.
Результаты и обсуждение
Среди пациентов с впервые выявленным колоректальным раком оказалось 76 мужчин в возрасте от 39 до 85 лет, 64 женщины в возрасте от 42 до 83 лет. Средний возраст у мужчин составил 65±2 года, у женщин 67±3 года. Пациентов в возрасте старше 50 лет оказалось 136 человек. По данным популяционного регистра рака НИИ терапии и профилактической медицины, за два с половиной десятилетия отмечается увеличение возраста клинических проявлений КРР почти на 2 года. Такое увеличение может быть связано как с поздним выявлением рака (качество диагностики), так и с развитием опухоли в более позднем возрасте (качество жизни) [5].
Проанализировано распределение случаев КРР по возрастным группам (до 45 лет, 45-59 лет, 60-74 года, 75 лет и старше) и соотношение показателей у мужчин и женщин (рис. 1).
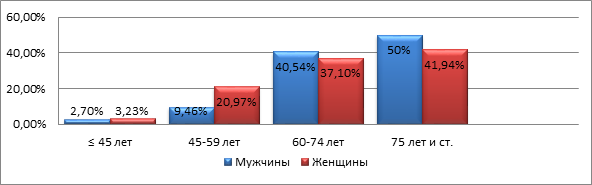
Рис. 1. Распределение случаев КРР по возрастным группам (%)
В возрасте до 45 лет число случаев выявленного КРР у мужчин и женщин оказалось сходным. В возрасте 45-59 лет - у женщин в 2 раза больше, чем у мужчин (p
Совершенно очевидно, что только при раннем выявлении злокачественных новообразований существующие на сегодняшний день методы лечения могут привести к успеху.
Однако состояние диагностики злокачественных опухолей в настоящий момент еще не вполне отвечает современным требованиям.
Так, по данным Белорусского канцер-регистра, среди впервые выявленных онкологических больных процент запущенных случаев достаточно высок (в 2004 г. у 15,7% больных диагноз был установлен в IV стадии), что закономерно сопровождается высокой смертностью в течение первого года после постановки диагноза (одногодичная летальность составила 31,0%).
Основной причиной поздней диагностики онкологической патологии и запущенности являются врачебные ошибки (по некоторым данным — до 45% случаев), обусловленные, прежде всего, недостаточными знаниями онкосемиотики рака и тактическими ошибками (длительное наблюдение и лечение хронических воспалительных процессов без верификации диагноза), а также назначением неадекватных методов лечения (физиотерапия при злокачественных опухолях и т.д.).
Таким образом, не вызывает сомнений тот факт, что в основе врачебных ошибок лежит отсутствие онкологической настороженности. В русскоязычной литературе этот термин впервые был предложен Савицким А.И. (1948).
Данное понятие предполагает формирование во врачебном мышлении целенаправленной психологической установки — подозрение является основой ранней диагностики злокачественной опухоли. Всегда каждому врачу необходимо помнить известное изречение: если диагноз не ясен — думай о раке.
На судьбу больного в негативном плане значительно больше может повлиять гиподиагностика, чем гипердиагностика злокачественного процесса, Поэтому не надо бояться постановки предположительного диагноза рака, а необходимо тщательно и систематизирование провести дальнейшее обследование и подтвердить или отвергнуть его.
1. Знание клинических симптомов злокачественных опухолей в ранних стадиях;
2. Знание предраковых заболеваний и принципов их диагностики и лечения;
3. Тщательное обследование каждого больного, обратившегося к врачу любой специальности, с целью выявления возможного рака (индивидуальный профосмотр);
4. Исключение необоснованного оптимизма и привычка в трудных случаях диагностики соматической патологии думать и о возможности атипичного или осложненного течения рака;
5. Знание принципов организации онкологической помощи и быстрое направление больного с обнаруженной или подозреваемой опухолью в специализированные онкологические учреждения.
Таким образом, во избежание трагических ошибок необходимо формировать у врачей любой специальности онкологическую грамотность, и понимание того, что выявление опухоли в ранней стадии (ранний рак) вполне осуществимо при своевременном и рациональном применении средств и методов ранней диагностики. Врач, обладающий онкологической грамотностью и не пренебрегающий ею, безусловно, в большей мере гарантирован от диагностических ошибок.
Существенной причиной запущенности онкологической патологии являются также позднее обращение больных за помощью или отказ от обследования (лечения), в основе которых лежат представления пациентов об опухолевом процессе как о фатально неизбежной смерти.
В этом плане важное значение имеют активизация противораковой пропаганды, искоренение среди широких масс населения этих негативных установок, что, несомненно, приведет к уменьшению числа лиц, поздно обратившихся к врачу и/или отказывающихся от обследования и лечения. Подтверждением этому служат данные канцер-регистра: в республике число больных, отказавшихся от лечения, снизилось с 8,1% в 1993 г. до 3,2% в 2005 г.
Методология диагностического алгоритма в онкологии

Рис. 8.1. Этапы диагностического алгоритма злокачественных новообразований.
При этом сохраняется общепринятая в онкологии установка, требующая во всех случаях при обследовании пациента искать, а на исключать опухоль.
Первый этап диагностического алгоритма — устанавливающая диагностика — находится в ведении врачей общей лечебной сети. Анализ клинических симптомов, анамнестических и физикальных данных, развитое клиническое мышление врача, как правило, позволяет заподозрить у пациента злокачественное новообразование, что предполагает последующую визуализацию вероятной опухоли.
Сделать это сравнительно не сложно для опухолей наружных локализаций (кожа, мягкие ткани, молочная железа, прямая кишка, половые органы и т.д.) и требует порой целого комплекса инструментальных методов диагностики для выявления опухолей внутренних органов (брюшная полость, органы грудной клетки и т.д.). При этом не обязательно использовать весь арсенал диагностического алгоритма.
В каждом конкретном случае избирается оптимальный набор тестов, но диагностические методы всегда используются по принципу от простых к сложным, от неинвазивных к инвазивным, вплоть до операции, для морфологического подтверждения (верификации) диагноза, что и является конечной целью данного этапа.
На рисунке 8.2 схематически представлены возможности диагностических методов в зависимости от распространенности опухолевого процесса.

Рис. 8.2. Особенности диагностики в зависимости от стадии развития опухоли [Петерсон Б.Е., Чиссов В.И., 1985].
Второй этап диагностики — уточняющая диагностика — находится в компетенции онкологов и проводится в онкологических стационарах.
Детальное уточнение онкологического диагноза проводится с целью получения максимально возможной информации об опухолевом процессе и соматическом состоянии пациента и предполагает ответы на следующие вопросы:
• локализация и распространение опухоли в пределах органа;
• возможное распространение опухоли на соседние анатомические структуры;
• анатомическая форма роста и размеры опухоли, ее гистологическая принадлежность;
• наличие регионарных и отдаленных метастазов;
• функциональное состояние систем и органов больного, метаболические нарушения и др.
Угляница К.Н., Луд Н.Г., Угляница Н.К.
В структуре онкоофтальмологической заболеваемости опухоли придаточного аппарата глаза занимают лидирующие позиции, составляя до 80 % всех опухолей органа зрения [2]. Несмотря на относительно благоприятный прогноз для жизни, новообразования данной локализации представляют потенциальную угрозу для зрения и могут привести к гибели глазного яблока [1]. В последние годы сохраняется тенденция к росту заболеваемости злокачественными новообразованиями век и коньюктивы. Несмотря на визуальную локализацию опухоли на сегодняшний день остается достаточно высоким процент больных поступивших на лечение к онкологу с запущенными стадиями заболевания, когда излечение от опухоли возможно только ценой потери органа зрения. У данных пациентов злокачественная опухоль диагностируется уже на том этапе, когда экзентерация орбиты остается единственным и безальтернативным способом лечения. Все вышеизложенное побудило нас к проведению настоящего исследования.
Цель исследования: изучение причин поздней диагностики злокачественных новообразований придаточного аппарата глаза.
Материалы и методы исследования
Нами изучены истории болезни 1100 пациентов со злокачественными опухолями, находившимися на лечении в отделении опухолей головы и шеи Ростовского научно- исследовательского онкологического института. Всем больным проводились общеклинические исследования, осуществлялось комплексное офтальмологическое обследование. При подозрении на прорастание опухолью костных структур лицевого скелета для уточнения степени распространенности процесса выполняли спиральную компьютерную томографию зон интереса.
Результаты исследования и их обсуждение
Среди исследуемых пациентов женщин было – 628 (57 %), мужчин – 472 (43 %).
Возраст больных колебался от 11 до 107 лет. Наибольшее количество пациентов находилось в возрасте от 50 до 70 лет – 725 (66 %) человек.
В связи с тем, что в ряде случаев определить локализацию первичной опухоли не представлялось возможным, мы принимали наиболее пораженную зону за первичную локализацию опухолевого процесса. Среди исследуемого контингента больных ведущее место занимали пациенты с локализацией первичного опухолевого процесса на коже нижнего века 531 (48,27 %) и в области внутреннего угла глаза 339 (30,82 %). Поражение верхнего века и области наружного угла глаза отмечено у 68 (6,18 %) и 65 (5,91 %) соответственно. Обширное поражение обоих век с прорастанием опухоли в орбиту, инфильтрацией глазного яблока, разрушением костных стенок орбиты диагностировано у 97 (8,82 %) пациентов. Пациенты с местно-распространенным опухолевым процессом составили 44,2 % от общего числа больных. По нашему мнению такое преобладание распространенных форм опухоли – выше среднестатистического, можно объяснить следующим: исследование проводилось по материалам специализированного онкологического центра, а потому вполне ожидаема концентрация в данном учреждении больных именно с запущенными, распространенными процессами, требующими индивидуального комплексного подхода к лечению.
Метастазы в регионарные лимфатические узлы диагностированы у 21 (1,9 %) пациента. Отдаленные метастазы на момент установления диагноза злокачественной опухоли были выявлены у 1 пациента с плоскоклеточным раком кожи век. У всех больных злокачественные опухоли кожи век были верифицированы посредством биопсии с последующим морфологическим анализом. В нашем исследовании преобладали базальноклеточные формы рака, которые наблюдались в 821 (74,64 %) случае. Наиболее часто в нашем исследовании встречалась язвенная форма опухоли, у 56, 73 % больных, тогда как рост опухоли в форме узла отмечен в 42,45 % случаях. Периодические кровотечения из опухоли наблюдались у трети больных (33,82 %). Воспалительные изменения со стороны глазного яблока различной степени выраженности развились у 770 (70 %) человек. Явления панофтальмита наблюдались в основном при местно-распространенных процессах и практически во всех случаях сочетались с гнилостным запахом. Диплопия, диагностированная у 5,55 % больных, свидетельствовала о поражении опухолевым процессом глазодвигательных мышц. К моменту обращения в лечебное учреждение больные отмечали наличие опухолевого образования на коже век в сроки от нескольких недель до нескольких десятилетий. Зачастую, только присоединение воспалительных изменений со стороны глазного яблока побуждало больных обратиться за медицинской помощью. Наиболее часто (в 51,64 % случаев) больные обращались за медицинской помощью через 1-3 года от момента появления опухолевого образования на коже. Чаще всего пациенты первично обращались к офтальмологам и дерматологам общей лечебной сети. У 285 (25,9 %) больных имела место неправильная первичная диагностика заболевания при обращении в медицинские учреждения общей лечебной сети. Пациентам устанавливались диагнозы: дематит, блефарит, ячмень, халазион, герпетическое поражение кожи, кератопапиллома и др. В результате у данной категории больных проводилось неадекватное лечение и продолжалось развитие злокачественной опухоли.
Необходимо отметить, что 76 (6,9 %) пациентам с подозрением на рак было выполнено морфологическое исследование новообразования, но оно оказалось неинформативным и больные не были направлены в специализированное учреждение. Следует подчеркнуть, что отсутствие клеток опухоли в биопсийном материале не должно являться обоснованием выжидательной тактики при подозрении на злокачественную опухоль. Особенно это относится к плоскоклеточному раку кожи, на поверхности которого находится большое количество ороговевших масс и дооперационная верификация процесса оказывается зачастую неэффективной, а проведение нерадикального лечения приводит к прогрессированию первичной опухоли и метастазированию в лимфатические узлы. Выполнение же биопсии опухоли при меланоме кожи вообще является недопустимым. Из 38 пациентов с меланомой кожи век 12 (31,58 %) поступили на лечение после проведенной биопсии опухоли, после которой был отмечен быстрый рост опухоли.
Таким образом, в результате проведенного исследования мы пришли к следующим выводам:
1. Почти половина больных (44,2 %) поступила на лечение с запущенными злокачественными опухолями.
2. Основной причиной запущенности рака кожи век является позднее обращение пациентов за медицинской помощью. Более чем в половине случаев (51,64 %) больные обращались к врачу через 1-3 года от момента появления первых признаков заболевания.
3. Повышение онкологической настороженности врачей общей лечебной сети позволит снизить процент врачебных ошибок и, как следствие, увеличит удельный вес пациентов с начальными формами рака.
4. При подозрении на злокачественную опухоль врачу общей лечебной сети не следует многократно пытаться верифицировать процесс, а необходимо своевременно направить пациента к онкологу.

Результаты лабораторных исследований, кроме подтверждения злокачественного процесса, должны свидетельствовать о типе опухоли, степени распространения опухолевого процесса. Диагностика злокачественных опухолей отличается от процесса распознавания доброкачественных участков.
Развитие опухоли начинается с того, что группа клеток под влиянием неблагоприятных факторов выходит из-под контроля и начинает самостоятельную деятельность – безудержное размножение. Данные клетки составляют первичный участок опухоли.
Отличие злокачественного процесса от доброкачественной опухоли
Опухоли могут быть схожи. Одновременно с этим они разнообразны, что затрудняет их классификацию. Индивидуальность каждого опухолевого образования зависит от факторов возникновения, механизма роста, расположения опухоли и степени проникновения в окружающие анатомические структуры.
Опухоли разделяют на доброкачественные и злокачественные образования.
К доброкачественным опухолям относятся образования, которые не опасны для жизни. Доброкачественные опухоли растут медленно. Для них не характерно рецидивирование и рост в окружающие органы. Доброкачественные опухоли не метастазируют.
Однако опухоль доброкачественной природы может значительно ухудшить качество жизни. Если опухоль локализуется в железах внутренней секреции, происходит нарушение гормональной регуляции. Доброкачественное образование больших размеров в кишечнике сдавливает петли кишечника. Как следствие - кишечная непроходимость. Доброкачественные опухоли могут перерождаться в злокачественные опухолевые образования.
Злокачественные новообразования – опухоли, отличием которых является бесконтрольное размножение клеток с проникновением в соседние ткани. Опухолевые клетки переносятся кровью в другие органы, образуя метастазы. Метастазы способны формироваться в костях, печени, головном мозге. Злокачественные опухоли нуждаются в обязательном лечении. Без терапевтических мероприятий раковые опухоли прогрессируют, вплоть до летального исхода.
Особенности диагностики
Диагностика доброкачественных новообразований основана на признаках наличия опухоли. Зачастую пациенты самостоятельно обнаруживают опухоль. Внешне доброкачественная опухоль выглядит как округлое, четко ограниченное новообразование с гладкой поверхностью. Беспокойство вызывает существование опухоли.
Диагностика доброкачественных процессов не вызывает трудностей. Опухоль сама не несет опасности жизни больного. Угроза кроется в нарушенной функции органа, где локализовалось опухолевое образование. Диагностика доброкачественных и злокачественных образований различна.
Клинические проявления злокачественного процесса довольно разнообразны. Поэтому диагностика злокачественных опухолей часто затруднена. В комплексе симптомов злокачественных опухолей выделяют четыре главных:
Синдром патологических выделений. Патологические кровянистые или гнойные выделения свидетельствуют о развитии онкологического процесса. Если раковая опухоль локализуется в желудке, то ее симптом - желудочное кровотечение. Злокачественная опухоль матки дает о себе знать обильными кровянистыми выделениями, а рак молочной железы – серозно-геморрагическим отделяемым из соска.
Нарушение функции органа. Прижившись в органе, раковая опухоль активно увеличивается в размерах, выделяет токсические вещества. При этом изменяется функционирование органа или ткани. Например, рак кишечника симптоматически проявляется кишечной непроходимостью. Основным признаком злокачественного образования в гортани является снижение или потеря голоса, кашель, трудности при проглатывании пищи.
Определение клинических признаков опухолевого процесса и применение индивидуальных методов диагностики важно для определения диагноза и выбора оптимального лечения. Диагностировать злокачественную опухоль необходимо как можно быстрее, так как рак на ранней стадии полностью поддается лечению. Своевременно поставленный диагноз – выявление злокачественного образования во второй или третьей стадии. Поздняя диагностика – запущенный процесс онкологии четвертой степени. Вероятность побороть болезнь низкая.
Методы диагностики злокачественных опухолей
Рентгенологические методы
Рентгенографическое обследование – основной метод диагностики опухолей желудка, легких, кишечника. Новейшим методом исследования в современной рентгенологии является томография – послойное исследование с контрастированием органа. Широко применяется ангиография, бронхография. Флюорография играет большую роль при профилактических осмотрах.
Маммография – методика обследования женской груди с использованием малой дозы рентгеновских лучей. С помощью маммографии обнаруживают опухоли, которые невозможно обнаружить при пальпации. Обследование груди при помощи маммографии врачи рекомендуют всем женщинам, особенно пациенткам, достигшим сорокапятилетнего возраста.
Компьютерная томография – метод диагностики, основанный на использовании рентгеновского излучения. Главным преимуществом КТ является возможность получить за минимальный промежуток времени большое количество поперечных проекций, что немаловажно для планирования хирургической операции и последующего радиолечения.
Ультразвуковая томография – информативный метод исследования, помогающий обнаружить опухоль печени, желчного пузыря, головки поджелудочной железы, почек, мочевого пузыря, внутренних половых органов. Популярно УЗИ - исследование совместно с доплерографией. Это позволяет наблюдать направление кровотока в сосудах органа, где локализовалась опухоль.
Эндоскопия
Метод эндоскопического исследования, благодаря новейшим достижениям оптики, приобрел решающее значение в диагностике начальных стадий онкологического процесса. Применение эндоскопической аппаратуры дает возможность внимательно осмотреть слизистые покровы внутренних органов, выполнить цитологическое исследование. При подозрении на онкологию – произвести забор кусочка ткани для гистологического анализа.
Лабораторные исследования
Клинические анализы крови, мочи, желудочного сока необходимы. Следы крови в моче или каловых массах являются показателями развивающегося патологического процесса онкологического характера. Снижение гемоглобина указывает на анемию. В диагностике рака большое значение имеют биохимические методы исследования. Биохимические тесты обнаруживают эндокринную природу опухоли. Влияние генетических нарушений, лежащих в основе опухоли, позволяет выявить специфические молекулярные маркеры. На основе маркеров создаются тесты для диагностики раковых заболеваний в стадии зарождения.
Онкомаркеры
Онкомаркеры – специфические вещества-индикаторы, которые образуются в результате жизнедеятельности раковых клеток. Высокие показатели онкомаркеров говорят о прогрессирующей онкологии.
Цитологический метод. Гистология
Цитология - доступный метод исследования, который дает возможность выявить атипичные клетки и диагностировать онкопатологию на ранних стадиях. Цитологический метод применяется для диагностики ракового процесса в шейке матки. Образцы мокроты рассматривают при подозрении на злокачественную опухоль легких. Атипичные клетки, обнаруженные при исследовании пунктата из опухоли, подтверждают рак.
Гистология. В современной медицине недопустимо химиотерапевтическое лечение или хирургические операции без предварительного гистологического анализа тканей. Для получения наиболее достоверных результатов гистологического исследования важно строго соблюдать пункты забора биологического материала. Гистологическое исследование бывает срочным и плановым. При срочном анализе биологические образцы замораживают, затем выполняют срезы. Далее врач оценивает состояние тканей под микроскопическим увеличением. Процедура занимает сорок минут времени. Плановое гистологическое исследование заключается в помещении биологических тканей в специальный раствор, заливают парафин, и только после этого делают срез и прокрашивают. Результаты оценивают через десять дней.
После диагностирования рака необходимо выбрать метод лечения. Хирургическая операция - самый конструктивный метод борьбы с раковой опухолью. Химиотерапия – метод лечения онкологических болезней с использованием медикаментозных средств, действие которых направлено на угнетение процесса деления онкоклеток. Иммунотерапия назначается для поддержания защитных сил организма в борьбе с онкологией.

Большинство видов рака излечимы, если болезнь была выявлена на начальной стадии и новообразование носит локальный характер. Это значит, что злокачественные клетки еще не распространились с кровью и лимфой в другие органы и системы.
К сожалению, большое количество злокачественных процессов долгое время протекает бессимптомно или с незначительными недомоганиями. Пациенты нередко обращаются за медицинской помощью уже на III или даже IV стадиях, когда прогноз неутешителен, поэтому так важна ранняя диагностика рака.
Когда нужно начинать беспокоиться
Симптомы рака зависят от его вида и локализации (расположения опухоли) и могут существенно отличаться. Однако есть проявления общего плана, которые характерны для злокачественных процессов всех видов:
- Слабость, утомляемость, хроническая усталость).
- Необъяснимая потеря веса.
- Повышение температуры тела.
- Бледность кожных покровов.
- Потеря аппетита.
- Периодически возникающая боль в какой-либо области тела, не имеющая видимой причины.
Возможно беспричинное покашливание, одышка, кровь в кале или моче, появление странных пятен и язв на теле, и так далее – в зависимости от вида заболевания.
Если симптомы не проходят в течение некоторого времени, нужно немедленно обращаться за медицинской помощью.
Методики выявления злокачественных опухолей
Диагностика рака обычно проходит в два этапа – обнаружение неполадок в организме неспецифическими и скрининговыми методами, а затем узконаправленный поиск болезни.
Справка! Неспецифические исследования – результаты которых свидетельствуют о наличии заболевания, но не дают возможности установить точный диагноз. Однако указывают направление для дальнейшего обследования.
Специфические – узконаправленное исследование, которое позволяет выявить вид заболевания и его локализацию в органе.
- Анализы крови на онкомаркеры.
- Цитологические и гистологические исследования биологического материала.
- Рентгенологические исследования конкретных органов (например, маммография, рентген желудка).
- Компьютерная томография (КТ), мультиспиральная компьютерная томография (МСКТ).
- Магнитно-резонансная томография (МРТ).
- Ультразвуковое исследование (УЗИ).
- Эндоскопические методы с взятием образца ткани.
Некоторые виды неспецифических исследований:
- Общий анализ крови.
- Биохимический анализ крови.
- Флюорография.
- Общий анализ мочи.
- Анализ кала на скрытую кровь.
Женщинам важно проходить ежегодные гинекологические осмотры и пальпацию молочных желез.
Первичные исследования
Его еще называют клиническим или общеклиническим. Это скрининговое исследование, которое дает развернутую общую картину работы организма, наличия в нем воспалений, анемий, нарушений свертываемости крови.
О возможной локальной онкопатологии могут говорить такие изменения показателей:
- Увеличение СОЭ (скорость оседания эритроцитов) с нормальным или повышенном значением лейкоцитов (белых кровяных телец).
- Падение количества гемоглобина без видимых причин. Может происходить при злокачественных процессах желудка и кишечника.
- Одновременное повышение уровня СОЭ, гемоглобина и эритроцитов (красных кровяных телец) может свидетельствовать в пользу рака почек.
Однако, если ОАК показал такие результаты, не следует пугаться. Повторим – это неспецифическое исследование, которое гораздо чаще свидетельствует о других, менее опасных болезнях.
Подозрения на лейкоз устанавливают при таких показателях:
- Очень большое или предельно низкое количество лейкоцитов.
- Сдвиг лейкоцитарной формулы.
- Появление в крови незрелых лейкоцитов.
- Повышение СОЭ.
- Падение показателей гемоглобина (анемия).
- Снижение количества тромбоцитов.
При локализованной онкопатологии (опухоль определенного органа) ОАК может не меняться, особенно на ранней стадии.
Может помочь в диагностике рака мочевыводящих путей: почек, мочевого пузыря, мочеточников. В урине в этом случае будет обнаружена кровь плюс атипичные клетки. Чтобы уточнить диагноз назначается цитологический анализ мочи.
При злокачественных новообразованиях почек и паращитовидной железы наблюдается существенный рост показателя кальция.
При раке печени, почек, поджелудочной железы повышается количество печеночных ферментов.
Изменения количества и соотношения гормонов разных типов могут свидетельствовать в пользу злокачественных заболеваний эндокринной сферы.
Помогает обнаружить рак легких.
Диагностика рака специальными методами

Если жалобы пациента и предварительные исследования дают основания заподозрить онкологию, начинается целенаправленный поиск.
Онкомаркеры – вещества, которые выделяют злокачественные опухоли в процессе своей жизнедеятельности. Специфичность этих анализов может варьироваться как по органам (возможность определить, где именно находится новообразование), так и заболеваниям (какой именно тип рака).
Наличие онкомаркеров не всегда говорит о злокачественности болезни. Поэтому после получения положительного результата по какому-либо из них, обязательно назначают дополнительные обследования.
Чаще всего используются такие тесты:
- РЭА (раковоэмбриональный антиген) – применяется в гинекологии для выявления опухолей матки, яичника, молочной железы.
- АФП (альфа-фетопротеин) – служит для диагностики карцином, в частности, желудка и кишечника.
- СА-125 – используется для ранней диагностики рака яичников, но также и других органов (груди, легких, печени).
- СА-15-3 – маркер с относительно невысокой специфичностью по органам. Позволяет заподозрить рак груди, яичников, поджелудочной железы, разных отделов кишечного тракта.
- ПСА (простатспецифический антиген) – тест новообразований предстательной железы.
- СА-19-9 – служит для распознавания онкологии желудочно-кишечного тракта, и в особенности поджелудочной железы.
- СА-242 – маркер высокочувствительный к раку желудка и кишечника.
Эти тесты выполняют также в профилактических целях, если пациент находится в группе риска.

Современная медицина располагает большим количеством неинвазивных и малоинвазивных методов, которые позволяют увидеть даже самые маленькие новообразования в труднодоступных местах.
Рентгенологическая диагностика:
- Рентгеноскопия – изображение выводится на экран монитора в режиме реального времени. Позволяет отследить особенности работы органа. Чаще выполняются рентгеноскопические осмотры желудка, кишечника, легких.
- Рентгенография – рентгеновский снимок органа. Примером рентгенографического исследования служит маммография (снимок молочной железы).
- Компьютерная томография (КТ) – послойные рентгеновские снимки в разных плоскостях. При диагностике новообразования выполняется с введением контрастной жидкости, что дает возможность четко увидеть его контуры.
- Мультиспиральная компьютерная томография (МСКТ) – срезы органов выполняются при спиральном вращении рентгеновской трубки и постоянном движении стола, где находится пациент. Высокая разрешающая способность метода, тонкие срезы до 0,5мм, дают возможность обнаружить самые мелкие опухоли недоступные обычному КТ. При этом лучевая нагрузка на пациента не увеличивается.
Магнитно-резонансная томография
Принцип работы такой же, как у рентгеновского КТ – получение послойных изображений органов. Но работает оборудование МРТ на основе электромагнитных волн.
Ультразвуковое исследование
Метод основан на способности ультразвука по разному отражаться от разных тканей и жидких сред. Безболезненное недорогое исследование, которое позволяет выявить патологии большинства органов.
Ограничение методов
Рентгенологическое, магнитно-резонансное или ультразвуковое исследования дают возможность увидеть наличие опухоли, оценить ее форму размер и локализацию. Но, чтобы судить о злокачественном или доброкачественном ее характере нужен образец ее ткани, который можно взять только при эндоскопическом исследовании или в ходе хирургической операции.
Это исследование, выполняемое при помощи оптического прибора, который вводится внутрь полого органа или в ходе операции (лапароскопия). При помощи эндоскопа можно осмотреть состояние его стенок, удалить подозрительное новообразование или взять биологический образец для проведения цитологического или гистологического анализа.
К эндоскопической технике относятся:
- лапароскопия;
- гастроскопия;
- гистероскопия;
- колоноскопия;
- бронхоскопия и т. д.
Если при эндоскопической процедуре была проведена операция или обнаружены подозрительные участки тканей, образец обязательно направляется на цитологическое или гистологическое исследование.

Гистологическое исследование – это изучение строения ткани под микроскопом, а цитологическое — клетки.
По результату этих анализов можно обнаружить наличие клеток с атипичной структурой, выявить их озлокачествление, определить вид и стадию опухоли. Цитологический анализ выполняется быстро, и его обычно используют в качестве скрининга. Для цитологии делают соскобы со слизистой оболочки органов (например, шейки матки), берут аспираты (жидкости), выполняют пункции лимфатических узлов, биопсии молочной и щитовидной желез.
Для проведения гистологии нужно больше времени и более сложное оборудование, но именно ее результат становится основанием для постановки окончательного диагноза.
Существует метод иммуногистохимии, который основан на связывании помещенных в образец ткани антител с соответствующими антигенами. Это очень информативный анализ, который способен выявлять недифференцируемые опухоли, метастазы из невыявленного первичного очага, а также прогнозировать дальнейшее развитие злокачественного процесса. Лабораторное оборудование для иммуногистохимии дорогое, поэтому возможность ее проведения существует не во всех клиниках.
Выявление рака различных органов
Выше были описаны способы, которые применяются при диагностике злокачественных заболеваний всех видов. Но каждый тип онкопатологии имеет свою специфику и локализацию, поэтому инструменты и методы их диагностики будут различаться. Ознакомимся с некоторыми из них.
Занимает первое место, как по распространению среди населения России, так и по смертности. Прогрессирует быстро, склонен к возникновению ранних метастаз.
Существует два вида этой болезни. Центральная, которая развивается в крупных бронхах, и периферическая – локализуется в бронхиолах и паренхиме легких. Симптомы центрального вида рака легких проявляются уже на ранних стадиях из-за уменьшения просвета бронхов, поэтому он достаточно хорошо диагностируется. А периферический тип долгое время протекает бессимптомно, и нередко выявляется на поздней стадии.
Техники определения рака легких:
- Общеклинический анализ крови.
- Флюорограмма.
- Бронхоскопия с биопсией.
- МРТ легких.
- Плевроцентез с биопсией плеврального выпота.
- Торакоскопия с забором материала.
- Торакотомия с взятием образца ткани из основного новообразования и близлежащих лимфатических узлов. Это хирургическая операция, к которой прибегают в крайнем случае.
Широко применяются рентгенологические исследования. Но при периферическом раке они нередко выявляют болезнь уже на III–IV стадиях.

Может поражать женщин любого возраста, но гораздо чаще он встречается у пациенток после 40 лет и старше. При его выявлении на I–II стадиях возможно органосохраняющее лечение.
Для ранней диагностики рака молочной железы ежегодно нужно посещать гинеколога или онколога-маммолога. Выполнять профилактическую маммографию необходимо после 40 лет – раз в 2 года, после 50 – 1 раз в год. Более молодым женщинам рекомендовано регулярно проходить УЗИ молочной железы.
Каждая женщина должна периодически выполнять самообследование – это делается стоя перед зеркалом, а потом в положении лежа. Насторожить должно изменение формы груди, появление выделений из соска, пальпация уплотнений, изменение внешнего вида и структуры кожи груди.
Если первичная диагностика дает основание заподозрить рак груди, выполняются такие обследования:
- Анализ крови на онкомаркер СА-15-3 и уровень эстрогенов.
- КТ и МРТ груди.
- Маммография с введением в молочные протоки контрастного вещества (дуктография).
- Пункция молочной железы с цитологическим или гистологическим анализом.
В крупных онкологческих центах возможно выявление онкогенных мутаций, методами молекулярной генетики. Женщинам из группы риска есть смысл выполнить такой анализ.
Если человека беспокоят тошнота, рвота, схваткообразные боли в животе, кишечные колики, вздутие живота, запоры или поносы, недержание газов и кала, кровь и гной в кале – есть вероятность злокачественного процесса в кишечнике. Для его диагностики назначают такие процедуры:
- УЗИ органов брюшной полости.
- Анализ кала на скрытую кровь.
- Тест крови на онкомаркер СА-19-9.
Опухоль может быть локализована в разных отделах кишечника.
Для обследования прямой кишки применяют ректороманоскопию. Этот способ позволяет увидеть участок протяженностью до 25 см, что существенно сокращает возможности метода.
Толстый кишечник диагностируют двумя способами – ирригоскопией и колоноскопией.
Ирригоскопия – рентгенография кишечника с применением контрастного вещества (барий).
Колоноскопия – эндоскопическая процедура осмотра стенок органа при помощи гибкой трубки с оптическим прибором.
Ирригоскопия переносится легче колоноскопии, но последняя позволяет выполнить биопсию. В нашей клинике есть возможность провести это исследование под наркозом.
Для уточнения локализации процесса и наличия метастаз может быть назначены ПЭТ-КТ и МРТ.
Как правило, выявляется на поздней стадии. Его ранние симптомы довольно смазаны – умеренные боли в животе, потеря веса, бледность кожных покровов. Обычно это списывают на проявления панкреатита или нарушения питания. Изменения биохимических показателей умеренны, онкологический маркер СА-19-9 на начальной стадии может не повыситься.
Для первичной диагностики используют УЗИ, КТ, МРТ поджелудочной железы.
Чтобы взять образец ткани, используют такие инструменты:

Жалобы на боли в области эпигастрия, стул и рвоту с кровью, тошноту, изжогу, отрыжку, потерю веса, могут свидетельствовать, как о язвенной болезни желудка, так и о раковой опухоли. В этом случае назначается:
Если у пациента были найдены бактерии Helicobacter pylori, это помещает его в зону риска по болезням желудка (гастриты, язва, рак). В этом случае требуется обязательное лечения антибиотиками, а также более тщательный контроль состояния ЖКТ.
Подавляющее большинство злокачественных заболеваний женской половой сферы протекает бессимптомно или с незначительными симптомами вплоть до поздних стадий. Поэтому их профилактика начинается с ежегодного гинекологического осмотра, независимо от наличия жалоб.
Обязательное первичное обследование – осмотр в кресле гинеколога с зеркалами. По его результатам врач предпринимает дальнейшие действия.
В рамках гинекологического осмотра врач берет у пациентки мазок на цитологию – это скрининг рака шейки матки и предраковых состояний. Если результаты мазка показали наличие атипичных или злокачественных клеток, выполняется кольпоскопия (эндоскопический осмотр слизистой оболочки шейки матки) со взятием образца измененных участков для гистологического анализа.
Технологии определения рака шейки матки:
- Аспирационная биопсия полости матки.
- Гистероскопия – осмотр цервикального канала и полости матки с помощью оптического прибора (гистероскопа) с забором биоматериала.
- Диагностическое выскабливание.
Диагностируется такими методами:
- Мануальный осмотр – ректовагинальный или влагалищный.
- УЗИ яичников.
- КТ и МРТ.
- Тест на онкомаркеры.
- Лапароскопия со взятием образца ткани.
Этот вид болезни склонен к метастазированию, поэтому часто поиск ведется и в других органах.
Чаще всего болеют мужчины старше 50, и особенно, 60 лет. Поэтому мужчинам старшего возраста обязательно нужно проходить профилактические осмотры простаты. Это же касается лиц из группы риска, особенно, учитывая, что ранние стадии протекают бессимптомно.
- Ректальный пальцевый осмотр.
- Анализ крови на онкомаркер ПСА.
При подозрении на онкопроцесс обследование продолжают такими инструментами:
- Трансректальным УЗИ. Выполняется через прямую кишку пациента. Позволяет исследовать предстательную железу, семенные пузырьки, уретру и окружающие ткани.
- Мультифокальной игольчатой биопсией под ультразвуковым контролем. Это наиболее надежный способ диагностики рака предстательной железы.
Заподозрить злокачественную опухоль почек можно на основании клинических тестов.
Это появлении в моче крови и атипичных клеток в сочетании с повышением СОЭ и уровня эритроцитов крови. Биохимия крови покажет увеличение количества кальция и трансаминазы.
Для дальнейшей диагностики применяют:
- УЗИ почек и брюшной полости.
- Контрастная рентгенография почки.
- КТ почек.
- Ретроградная пиелография. Это рентгенография почечной лоханки, которая выполняется с введением цистоскопа в мочевую систему и контрастного красителя в мочеточники. Рентгеновские снимки используются для визуализации движения красителя и функционирования системы.
- Прицельная биопсия под контролем УЗИ.
- Селективная почечная ангиография. Определяет почечно-клеточный рак. При новообразованиях лоханок не применяется.
Тесты на онкомаркеры при раке почек не информативны.
Читайте также:

