Презентация на тему миелоидный лейкоз

- Скачать презентацию (0.33 Мб) 144 загрузки 3.3 оценка


















- 1
- 2
- 3
- 4
- 5
Рецензии
Аннотация к презентации
Содержание

Подготовила :Жолдасбекова А. Группа 50-2 Факультет : ОМ Проверила : Искакова З.А.
Хронический миелоидный лейкоз (ХМЛ, хронический миелолейкоз) — форма лейкоза, которая характеризуется ускоренной и нерегулируемой пролиферацией преимущественно миелоидных клеток в костном мозге с их накоплением в крови. 2
В большинстве случаев (80-88%) хронического миелолейкоза выявляется хромосомный маркер опухолевого клона Ph'-хромосома, называемая филадельфийской, которая присутствует почти во всех клетках костного мозга гранулоцитах, моноцитах, эритрокариоцитах и мегакариоцитах, в лимфоцитах ее нет. Эта аномалия часто сочетается с трисомией 8, 9, 19, 21, делецией 5 и с другими дефектами хромосом. До 95% случаев хронический миелолейкоз-Ph-позитивный и лишь 5-8% регистрируются как Ph-негативный. Хотя возникновение заболевания связано с изменением хромосомного материала, семейной предрасположенности не выявлено, также не установлена ассоциация с HLA-генотипом 3
Клиническая картина зависит от стадии заболевания. Выделяют 3 стадии хронического миелолейкоза: начальную, развернутую и терминальную (ВОЗ 2001 г.). В начальной стадии хронический миелолейкоз практически не диагностируется или выявляется при случайном исследовании крови, поскольку симптоматика в этот период почти отсутствует. Имеются жалобы на слабость, потливость, снижение аппетита, похудание, тошноту, повышение температуры тела, одышку, сердцебиение, боли в сердце, боли в костях, в левом или правом подреберье, увеличение периферических лимфатических узлов. Уже в этой стадии увеличивается селезенка, что вызывает неприятные ощущения в левом подреберье, чувство тяжести, особенно после еды . Практически эту стадию выделить не удается. Ведущий клинический симптом - спленомегалия как следствие миелоидной метаплазии (инфильтрации) селезенки 4
В периферической крови: постоянный и немотивированный лейкоцитоз (40-70.109/л) с нейтрофильным профилем, сдвигом влево до миелоцитов. Важным гематологическим признаком является увеличение количества базофилов и эозинофилов различной зрелости. Анемия в этот период не наблюдается. Отмечается тромбоцитоз до 600-1500.109/л. Костный мозг: гиперклеточный, Л/Э 10:1 увеличение миелокариоцитов происходит за счет незрелых и зрелых форм гранулоцитов количество бластных клеток не превышает 5% изредка эритробластоз в 1/3 случаев - гиперплазия мегакариоцитов 5
Болезнь, как правило, диагностируется на стадии тотальной генерализации опухоли по костному мозгу, то есть в развернутой стадии. Развернутая стадия характеризуется появлением клинических признаков заболевания, связанных с лейкемическим процессом. При объективном исследовании почти постоянным признаком в этот период является увеличение селезенки, достигающие значительных размеров. При пальпации селезенка безболезненной. Быстрый рост селезенки часто приводит к перисплениту и у половины больных инфарктам селезенки, проявляющиеся острыми болями в левом подреберье с иррадиацией в левый бок, левое плечо, усиливающейся при глубоком вдохе 7
В периферической крови: анемия имеет нормохромный характер, нередко выражен анизо- и пойкилоцитоз. В лейкоцитарной формуле представлен весь гранулоцитарный ряд включительно до миелобластов (бластные клетки 5-10%). Количество лейкоцитов достигает 250-500.109/л. Костный мозг: гиперклеточный, число незрелых форм гранулоцитов повышается количество эритро-кариоцитов уменьшается содержание мегакариоцитов в норме Продолжительность этой стадии без цитостатической терапии составляет 1,5-2,5 года. Клиническая картина при лечении заметно изменяется. Самочувствие больных длительно остается удовлетворительным, сохраняется работоспособность, количество лейкоцитов около 10-20.109/л, прогрессирующего увеличения селезенки не наблюдается. Развернутая стадия у больных, принимающих цитостатики, длится 4-5 лет, а иногда и больше 8
В терминальной стадии отмечается резкое ухудшение общего состояния, усиление потливости, стойкое немотивированное повышение температуры. Появляются сильные боли в костях и суставах. Важным признаком является появление рефрактерности к проводимой терапии. Значительно увеличена селезенка. Нарастает анемия, тромбоцитопения. При умеренном повышении количества лейкоцитов формула омолаживается за счет увеличения процента незрелых клеток (промиелоцитов, миелобластов и недифференцируемых клеток). Геморрагический синдром, отсутствовавший в развернутой стадии, почти постоянно появляется в терминальном периоде 10
Опухолевый процесс в терминальной стадии начинает распространяться за пределы костного мозга: возникает лейкемическая инфильтрация нервных корешков, вызывающая радикулярные боли, образуются подкожные лейкемические инфильтраты (лейкемиды), наблюдается саркомный рост в лимфоузлах. Лейкемическая инфильтрация на слизистых оболочках способствует развитию в них кровоизлияний с последующим некрозом. В терминальной стадии больные склонны к развитию инфекционных осложнений, которые нередко являются причиной смерти 11
В течении хронического миелолейкоза может наблюдаться развитие бластного криза. У больных отмечаются резкое ухудшение общего состояния, признаки интоксикации, лихорадка, боли в костях, метастазы в селезенку, печень, лимфатические узлы, кости, другие органы и ткани, анемия, геморрагии. В гемограмме и/или в костном мозге обнаруживается значительное количество миелобластов. В единичных случаях выявляются лимфобласты, что свидетельствует о поражении кроветворения на уровне полипотентной стволовой клетки. Диагностические признаки бластного криза хронического миелолейкоза: увеличение суммарного количества бластных клеток, промиелоцитов в периферической крови или костном мозге до 20% и более. С учетом морфологических, цитохимических, иммунофенотипических особенностей бластных клеток различают несколько вариантов бластного криза - миеломонобластный, миелобластный, лимфобластный, монобластный, промиелоцитарный, эритробластный, мегакариобластный 13
Стадия хронического миелолейкоза устанавливается на основании комплекса клинических данных и изменений со стороны кроветворения с учетом данных гемограммы, миелограммы, гистологического исследования. Иногда недостаточно явная клинико-гематологическая картина на начальном этапе заболевания не позволяет уверенно поставить диагноз хронического миелолейкоза. В этих случаях важное значение для диагностики имеет обнаружение Ph'-хромосомы в гранулоцитах, моноцитах, эритро- и мегакариоцитах костного мозга (следует помнить о вариантах хронического миелолейкоза без Ph'-хромосомы) 14
Лечение хронического миелолейкоза определяется стадией заболевания. В случаях слабо выраженных клинико-гематологических проявлений хронической стадии рекомендуют общеукрепляющую терапию, полноценное питание, богатое витаминами, регулярное диспансерное наблюдение. Имеются сведения о благоприятном влиянии на течение заболевания а-интерферона. Лечение хронического миелолейкоза в развернутой и терминальной стадии имеет свои отличия. В развернутой стадии терапия направлена на уменьшение массы опухолевых клеток и ставит своей целью сохранить как можно дольше соматическую компенсацию больных и отсрочить наступление бластного криза. Цитостатическая терапия начинается с момента установления диагноза. применяют моно- и полихимиотерапию 15
Препараты: - миелосан действует на стволовые кроветворные клетки, менее активен на клетки-предшественники отдельных ростков кроветворения и не действует на быстро пролиферирующие клетки, - гидроксимочевина (гидреа) влияет на пролиферирующие клетки, - интерфероны-«модификаторы биологического. - гливек – противоопухолевый препарат, ингибитор протеинтирозинкиназы - анормального фермента, продуцируемого филадельфийской хромосомой, подавляет пролиферацию, индуцируя их апоптоз, - новые ингибиторы тирозинкиназ: нилотиниб, дисатиниб. Лучевая терапия в качестве первичного лечения, особенно при спленомегалии, Лимфоцитаферез при резистентности к цитостатической терапии 16
Лечение в терминальной стадии хронического миелолейкоза при наличии бластных клеток в периферической крови проводят по схемам острого миелобластного лейкоза. ВАМП, ЦАМП, АВАМП, ЦОАП, сочетание винкристина с преднизолоном, цитозарасрубомицином. Терапия направлена на продление жизни больного, так как получить ремиссию в этом периоде трудно. При развитии бластного криза проводится лечение по соответствующему протоколу, в зависимости от его варианта (лимфобластный или миелобластный) 17
Презентация была опубликована 6 лет назад пользователемВиктория Загнибеда
Презентация на тему: " Острый миелоидный лейкоз Подготовила: Студентка 5 курса 2 мед. фак. Абибуллаева Зарема." — Транскрипт:
1 Острый миелоидный лейкоз Подготовила: Студентка 5 курса 2 мед. фак. Абибуллаева Зарема
2 Острый миелоидный лейкоз (ОМЛ, острый нелимфобластный лейкоз, острый миелогенный лейкоз) это злокачественная опухоль миелоидного ростка крови, при которой быстро размножаются изменённые белые кровяные клетки. Накапливаясь в костном мозге, они подавляют рост нормальных клеток крови.
3 Классификация острого миелоидного лейкоза по системе Всемирной системы здравоохранения Система классификации острого миелоидного лейкоза ВОЗ разработана с учётом системы ФАБ и имеет целью более эффективное клиническое применение и учитывает наиболее прогностически значимые признаки заболевания. Каждый из видов (категорий) ОМЛ по классификации ВОЗ включает в себя несколько подвидов (подкатегорий) описательного характера, представляющих интерес для гематологов и онкологов; однако, бо́льшая часть клинически важной информации в классификации ВОЗ взаимосвязана через распределение по перечисленным ниже подвидам.
4 ОМЛ с характерными генетическими изменениями Включает:ОМЛ с транслокациями между хромосомой 8 и 21 [t(8;21)] (МКБ-О 9896/3); ОМЛ инверсиями в хромосоме 16 [inv(16)] (МКБ-О 9871/3); ОМЛ с транслокациями между хромосомой 15 и 17 [t(15;17)] (МКБ-О 9866/3); У больных с таким подвидом ОМЛ обычно высок уровень ремиссий и прогноз лучше сравнительно с ОМЛ других подвидов. ОМЛ с дисплазией нескольких ростков Этот подвид включает больных с предшествующим миелодиспластическим синдромом (МДС) или миелопролиферативной болезнью (МПБ), которые переходят в ОМЛ. Этот подвид ОМЛ чаще встречается у пожилых людей и отличается неблагоприятным прогнозом. ОМЛ и МДС, связанные с предыдущим лечением Этот подвид ОМЛ включает больных, получавших химиолечение и/или лучевое лечение, после которых возник ОМЛ или МДС. При этих лейкозах могут быть характерные изменения в хромосомах, прогноз при них часто бывает хуже. ОМД не подпадающие под признаки перечисленных подвидов.Включает подвиды ОМЛ, не входящие в перечисленные выше.
5 Франко-американско-британская классификация Франко-американско-британская классификационная (ФАБ) система разделяет ОМЛ на 8 подвидов, от М0 по M7, основываясь на типах клеток предшественниц лейкоцитов, и на степени зрелости изменённых клеток. Определение злокачественных клеток проводят на основании внешних признаков при световой микроскопии и/или цитогенетически, выявляя лежащие в основе отклонений изменения в хромосомах. У разных подвидов ОМЛ разные прогноз и ответ на лечение. Несмотря на преимущества классификации ВОЗ, система ФАБ до сих пор широко применяется. По ФАБ существует восемь подтипов ОМЛ.
6 M0 минимально-дифференцированный острый миелобластный лейкоз M1острый миелобластный лейкоз без созревания M2острый миелобластный лейкоз с созреванием гранулоцитовt(8;21)(q22;q22),t(6;9) M3промиелоцитарный, или острый промиелоцитарный лейкоз(ОПЛ)t(15;17)M4острый миеломоноцитарный лейкозinv(16)(p13q22),del(16q) M4eoмиеломоноцитарный сочетанный с эозинофилией костного мозгаinv(16),t(16;16) M5острый монобластный лейкоз(M5a) или острый моноцитарный лейкоз (M5b) (M5b)del (11q), t(9;11), t(11;19) M6острые эритроидные лейкозы, включая эритроцитарный лейкоз (M6a) и очень редкий чистый эритроидный лейкоз (M6b) M7острый мегакариобластный лейкозt(1;22)M8острый базофильный лейкоз
7 Проявления острого миелолейкоза Бо́льшая часть симптомов ОМЛ вызывается замещением нормальных клеток крови лейкозными клетками. Недостаточное образование лейкоцитов обусловливает высокую восприимчивость больного к инфекциям несмотря на то, что лейкемические клетки происходят от предшественников лейкоцитов, способность противостоять инфектам у них отсутствует. Снижение количества красных кровяных телец (анемия) может вызывать усталость, бледность, и одышку. Недостаток тромбоцитов может привести к легкой повреждаемости кожи и повышенной кровоточивости.
8 Ранние признаки ОМЛ часто неопределённы и неспецифичны, и могут походить на признаки гриппа или других распространённых болезней. Вот некоторые общие симптомы ОМЛ: лихорадка,усталость, потеря веса или снижение аппетита, одышка, анемия, повышенная повреждаемость кожи и слизистых оболочек и кровоточивость, петехии(плоские, размером с булавочную головку пятнышки внутри кожи на месте кровоизлияний), гематомы, боль в костях и суставах, и стойкие или частые инфекции. При ОМЛ может быть увеличение селезёнкино обычно оно незначительно ибессимптомно. Увеличение лимфоузлов при ОМЛ случается нечасто, в отличие отострого лимфобластного лейкоза. В 10 % случаев развиваются изменения кожи в видекожного лейкоза. Изредка при ОМЛ возникает Синдром Свита, он жепаранеопластический синдром воспаление кожи вокруг поражённых хлоромой участков.
9 У некоторых больных ОМЛ появляется припухлость дёсен из-за инфильтрации тканей лейкозными клетками. Изредка первым признаком лейкоза оказывается хлорома плотная лейкемическая масса за пределами костного мозга. Иногда заболевание протекает бессимптомно, и лейкоз выявляется общим анализом крови в ходе профилактического осмотра.
10 Причины : Воздействие химических веществ Ионизирующее излучение Генетические факторы
11 Диагностика Изменения соотношения клеточных элементов в общем анализе крови первое, что наводит на мысль о возможности ОМЛ. Наиболее частым оказывается лейкоцитоз- повышение общего количества лейкоцитов, иногда с появлением бластных (незрелых) форм, но бывает так, что ОМЛ проявляется изолированным снижением тромбоцитов, эритроцитов, а количество лейкоцитов может оказаться даже сниженным (лейкопения).Предварительный диагноз ОМЛ может быть определён в случае выявления в мазках периферической крови бластных форм лейкоцитов, но для окончательного диагноза должны быть выявлены соответствующие изменения в анализе аспирационного биоптата костного мозга.
12 Костный мозг и кровь исследуют световым микроскопированием и поточной цитометриейдля установления диагноза и дифференцирования ОМЛ от других лейкозов, например, подострого лимфобластного лейкоза, а также для уточнения подтипа ОМЛ. Образец крови или костного мозга обычно проверяют на присутствие хромосомныхтранслокацийобычными цитогененитчески ми способами, или способом флуоресцентной гибридизации in situ. Генетические исследования проводят и для выявления характерных мутаций, которые могут влиять на исход заболевания например, в FLT3, в нуклеоплазмине, или в KIT. Цитохимические красители для мазков крови и костного мозга оказываются очень полезными для дифференциальной диагностики ОМЛ и ОЛЛ, а также для выделения подтипов ОМЛ. Сочетание миелопероксидазы или красителя Суданский чёрный и неспцифического эстеразного красителя обеспечивает получение нужной информации в большинстве случаев. Реакции миелопероксидазы или Суданского чёрного оказываются самыми полезными для установления диагноза ОМЛ и его дифференцирования от ОЛЛ. Неспецифический краситель эстеразы используется для моноцитаронй составляющей острых миелолейкозов и для дифференцирования от незрелой формы монобластного лейкоза от ОЛЛ. [
13 Диагноз и классификация ОМЛ может оказаться непростой задачей, этим должен должен заниматься квалифицированный гематопатолог или гематолог. В явных случаях наличие некоторых характерный морфологических признаков, таких, как тельца Ауэра, или специфических для АМЛ результаты поточной цитометрии дают возможность надёжно отделять ОМЛ от других лейкозов; однако при отсутствии таких явных признаков диагностика существенно осложняется. В соответствии с широко используемыми критериями классификации ВОЗ диагноз ОМЛ устанавливаетсяв том случае, если доказано если в крови и\или костном мозге более 20 % клеток представлены миелобластами. ОМЛ следует тщательно дифференцировать от так называемых прелейкозных состояний, в частности, от миелодиспластического синдрома или миелопролиферативного синдрома, которые лечатся по разному. Поскольку острый промиелоцитарный лейкоз (ОПЛ), требуя уникального способа лечения очень хорошо ему поддаётся, очень важно быстро подтвердить или отвергнуть этот подвид лейкоза. Для этого част о используют флюоресцентную гибридизацию in situ, выполненную на крови или костном мозге, поскольку ею легко выявляется хромосомная транслокация (t[15;17]) специфичная для ОПЛ.
14 Лечение Лечение ОМЛ состоит в основном из химиотерапии, и делится на два этапа: индукция и постремиссионное лечение(или консолидация). Цель индукционной терапии является достижение полной ремиссии за счет уменьшения количества лейкозных клеток до не обнаруживаемого уровня; цель консолидирующей терапии заключается в ликвидации остаточных, не обнаруживаемых современными методами остатками болезни и излечение.
16 Целью индукционного этапа лечения является достижение полной ремиссии. Полная ремиссия не означает, что заболевание полностью вылечено. Скорее, состояние полной ремиссии говорит о невозможности обнаружить болезнь существующими способами диагностики.Полная ремиссия достигается у % взрослых больных с впервые выявленным ОМЛ, разница зависит от прогностических факторов, о которых сказано выше.Длительность ремиссии зависит от прогностических качеств исходного лейкоза. В основном, все случаи ремиссии без дополнительного, консолидирующего лечения закачиваются рецидивом
17 Консолидационное лечение Даже после достижения полной ремиссии вероятно, немногие лейкозные клетки всё же выживают. Их так мало, что обнаружить их пока невозможно. В случае не проведенияпослеремиссионного, или консолидационного лечения почти у всех больных в конце концов возникает рецидив.Поэтому для того, чтобы избавиться от неопределимых больных клеток и предотвратить рецидив то есть, достичь полного излечения, нужна дополнительная терапия. Вид лечения после достижения ремиссии определяется индивидуально в зависимости от прогностических факторов и общего состояния здоровья больного. При прогностически благоприятных подвидах лейкозов (например, при inv(16), t(8;21) и t(15;17) обычно назначают 3-5 дополнительных курса интенсивной химиотерапии, известной как консолидационное лечение. Больным с высоким риском рецидива (например, при наличии цитогенетических изменений, сопутствующего миелодиспластического синдрома, или при ОМЛ, связанном с предшествующим лечением обычно рекомендуется транплантация аллогенных стволовых клеток гемопоэтического ряда, если позволяет общее состояние и есть подходящий донор.При ОМЛ со средней вероятностью рецидива (при нормальных цитогенетических показателях или с такими цитогенетическими изменениями, которые не попадают в группы риска)вопрос консолидационного лечения не столь ясен и определяется рядом специфических показателей возрастом больного, общим состоянием его здоровья, системой ценностей, и наконец, наличием донора подходящих стволовых клеток. Тем больным, которым пересадка стволовых клеток после консолидационного лечения не показана, проводят иммунотерапию комбинацией гистамина гидрохлорида и пролейкина Такое лечение позволяет снизить вероятность рецидива на 14 %, удлиняя ремиссию на 50 %. Таким образом, стандартной терапией ОМЛ признаны высокоинтенсивная химиотерапия (ВХТ) и трансплантация костного мозга..
18 Однако результаты лечения, несмотря на относительно высокие ответы у молодых, остаются неудовлетворительными у лиц старше 65 лет (30-50%) связанные с ранней летальностью (10%) и непродолжительностью ремиссии. Больше половины с ОМЛ – это больные старшего возраста и/или со значимой сопутствующей патологией, которые, как правило, не могут получать высокотоксичные схемы химиотерапии, поэтому для их терапии применяют низкие дозы цитарабина цитарабина и поддерживающее лечение:антибиотики и гемотрансфузии. С 2010 года в США для лечения ОМЛ рекомендовано применять гипометилирующие агенты (5-азацитидин, децитабин) у пациентов, которые не подходят для трансплантации костногомозговых клеток/интенсивной химиотерапии.В процессе метилирования ДНК ипометилирующие агенты ковалентно связываются с ДНК-метилтрансферазой, что приводит к реактивации генов, после чего восстанавливается дифференцировка гемопоэтических клеток-предшественников и нормальное кроветворение. 5- азацитидин обладает двойным механизмом действия. Он встраивается не только в молекулу ДНК, но и в молекулу РНК. Тем самым 5- азацитидин понижает количество РНК в клетках, что приводит к цитостатическому эффекту вне зависимости от клеточной фазы. На основании результатов исследования 3 фазы AZA международное, мультицентровое, контролируемое исследование в параллельных группах, в котором пациенты МДС высокого риска/ОМЛ (ВОЗ критерии) сравнивались со стандартно используемой терапией (сопроводительная терапия, интенсивная химиотерапия, низкие дозы цитарабина), азацитидин был зарегистрирован, в том числе и в РФ, для лечения этих групп больных. Было показано, что азацитидин в 2,5 раза увеличивает общую выживаемость пациентов с ОМЛ (критерии ВОЗ).
19 Рецидив ОМЛ При рецидиве ОМЛ единственным испытанным способом лечения, который может оказаться действенным, оказывается пересадка стволовых клеток при условии, если она ещё не применялась. При рецидиве ОМЛ больным, которым не планируется пересадка стволовых гемопоэтических клеток, или в случае рецидива после пересадки стволовых клеток можно предложить лечение в рамках клинического испытания, поскольку выбор среди обычных способов лечения весьма ограничен. В настоящее время проходит клинические испытания цитостатическое вещество клофарабин, также испытываются различные способы прицельной терапии с использованием ингибиторов фарнезилтрансферазы децитабина и ингибиторов белка множественной лекарственной устойчивости ингибиторы гистондеацетилазы цитарабина, блокаторы ангиогенеза, аналоги дезоксиаденозина. Иногда ограниченное количество методов терапии рецидивов ОМЛ вынуждает обращаться к паллиативному лечению. После клинических испытаний триоксида мышьяка Управление по контролю за качеством пищевых продуктов и лекарственных препаратовСША одобрило его применение в качестве паллиативного средства лечения рецидивирующего острого промиелоцитарного лейкоза (ОПЛ). Также как и ПТРК триоксид мышьяка неэффективен при других подвидах ОМЛ. В 2000 году в США для лечения рецидивов ОМЛ у больных старше 60-ти лет, которых нельзя лечить высокими дозами химиопрепаратов, было разрешено применятьгемтузумаб озогамицин, препарат, в котором, как предполагалось, цитотоксическое вещество противоопухолевый антибиотик калихимицин связан смоноклональным антителом, обеспечивающим доставку антибиотика точно в лейкозную клетку.В настоящее время данный препарат снят с производства, т.к. в результате исследований было выявлено отсутствие разницы у пациентов принимавших и не принимавших милотарг
20 Прогноз Благоприятный исход :t(8;21), t(15;17), inv(16),70 % -5 летняя выживаемость,33 % - частота рецидивов. Удовлетворительный.Не выявлено, +8, +21, +22, del(7q), del(9q), нарушения 11q23, все остальные структурные или численные изменения;48 % 5 летняя выживаемость,50 %- частота рецидивов Неблагоприятный5, 7, del(5q), нарушения 3q, комбинированные цитогенетические нарушения,15 %- 5 летняя выживаемость, 78 %- частота рецидивов
Текст этой презентации

Презентация на тему: Острый миелобластный лейкоз (ОМЛ)
выполнила студенка группы 341-4 лаб(уг) Волкова ольга

Острый миелобластный лейкоз (ОМЛ)
онкопатология, при которой спинной мозг вырабатывает аномальные миелобластные клетки, тромбоциты или эритроциты. Другие названия этой патологии — острый миелоцитарный лейкоз, острый миелоидный лейкоз, острый нелимфобластный лейкоз. Острый миелобластный лейкоз у детей возникает редко. В основном эта патология поражает взрослых. Средний возраст обнаружения патологии — 63 года. Острый и хронический миелобластный лейкоз никогда друг в друга не переходят.
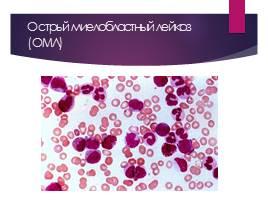
Острый миелобластный лейкоз (ОМЛ)

Распространенность острого миелобластного лейкоза
ОМЛ — это относительно редкая злокачественная патология. В США ежегодно обнаруживают около 10 500 случаев. Смертность от ОМЛ — 1,2% от всей онкологической смертности на территории США. Среди взрослых наивысший уровень заболеваемости — в Европе, Северной Америке и Океании. Значительно ниже показатели в Латинской Америке и в Азии. Детский ОМЛ в Азии выявляется чаще, чем в Северной Америке. Из азиатский стран низкие показатели детского ОМЛ обнаруживаются в Индии. Такие различия могут быть связано с генетическими особенностями и с условиями окружающей среды.

Причины острого миелобластного лейкоза
Выявлено несколько факторов, способствующих развитию ОМЛ. В их числе — воздействие химических веществ, пре-лейкоз, излучение, неблагоприятная наследственность. Очень высока вероятность заболеть ОМЛ в течение первых 3-5 лет после химиотерапии по поводу другой опухолевой патологии. Опасны алкилирующие вещества, а также эпиподофилотоксины и антрациклины. В данном случае лейкозы часто объясняют специфическими метаморфозами в хромосомах патологических клеток. Спорной остается связь ОМЛ и бензола, а также прочих ароматических органических растворителей. Определенные наблюдения показывают, что работа с этими веществами действительно опасна. Но другие исследования доказывают, что если и есть риск, то он выступает скорее добавочным фактором, чем основным.

Причины острого миелобластного лейкоза
Зафиксировано множество случаев, когда данная болезнь обнаруживалась у нескольких членов одной семьи. Это говорит в пользу того, что наследственность играет роль в заболеваемости ОМЛ. Если человек болен острым миелобластным лейкозом, то для его ближайших родственников вероятность заболеть в три раза выше среднестатистической. Риск повышают некоторые врожденные состояния. Опасен с этой точки зрения синдром Дауна. При нем вероятность заболеть ОМЛ повышается в 10-18 раз.

Симптомы острого миелобластного лейкоза
Они включают в себя особенности течения и клинических проявлений в зависимости от преобладания поражения тех или иных органов: центральной и периферической нервной системы, сердца, печени, кишечника, костей и суставов, лимфатических узлов. Симптомы миелобластного лейкоза состоят из:

Симптомы острого миелобластного лейкоза
Общая слабость, быстрая утомляемость, недомогание. Профузная потливость без видимой причины. Бледность кожных покровов и слизистых оболочек. Отеки конечностей и одутловатость шеи и лица. Стойкая постоянная гипертермия (повышение температуры) от 37,1˚С до 39˚С и выше. Увеличение лимфатических узлов всех групп одновременно или в определенных участках. Боли в мышцах, костях и суставах. Одышка и тахикардия (учащенное сердцебиение). Тошнота, рвота и диарея. Тяжесть в правом подреберье и увеличение печени. Увеличение селезенки (спленомегалия). Повышенная кровоточивость и ломкость сосудов.

Для подтверждения диагноза или первичного выявления лейкоза необходимо провести определенный объем диагностических мероприятий, который также четко регламентирован. Он включает в себя: Общеклинический анализ крови. Данный метод является первым шагом на пути правильной и ранней диагностики. От того насколько четко он выполнен зависит своевременное лечение. При микроскопии определяется повышение уровня незрелых форм (бластных клеток) лейкоцитов на фоне общего снижения количества эритроцитов и тромбоцитов. Данное состояние носит название бластного криза и лейкемического провала, когда отсутствуют зрелые и переходные формы лейкоцитов.
Диагностика

Диагностика
Пункция костного мозга и миелограмма является золотым стандартом диагностики и единственным достоверным методом для подтверждения диагноза миелобластный лейкоз. Применяется в виде стернальной пункции (взятие образцов костного мозга из грудины) или такого же исследования из крыла подвздошной кости. Биохимическое исследование крови. Не несет непосредственной информации о характере болезни, а лишь указывает на степень нарушения функций внутренних органов на фоне лейкоза. Другие методы: ЭКГ, общий анализ мочи, пульсоксиметрия, рентгенография легких, УЗИ брюшной полости носят дополнительный характер и назначаются при необходимости.

Лечение (омл)
Цель терапии при данной патологии — максимальное уничтожение патологических клеток. По сравнению с острым лимфобластным лейкозом ответ достигается при использовании меньшего числа препаратов. Кроме традиционной химиотерапии применяются и экспериментальные методы. Один из них — воздействие на кроветворение при помощи биологически активных препаратов. Специалисты пытаются использовать средства с мощным моделирующим воздействием на иммунитет. В их числе циклоспорин и антилейкоцитарный иммуноглобулин. Предметом дискуссий является использование ростковых факторов (они могут вызывать разрастание опухолевого клона клеток). Некоторые исследователи доказывают, что целесообразно применять колониестимулирующие факторы. Трансплантация костного мозга может быть аллогенной
Читайте также:

