Показатели анализов крови при опухоли гипофиза
Лабораторные показатели, используемые при заболеваниях гипофиза
Тиреотропин. Оценка изменений тиреотропного гормона гипофиза приведена в разделе, посвященном заболеваниям щитовидной железы.
Соматотропин, или гормон роста (СТГ). Основная функция соматотропина — это регуляция роста организма. Для определения содержания СТГ в сыворотке крови рекомендуется определять уровень последнего в течение 3 дней подряд, и среднее значение этих показателей будет соответствовать базальной концентрации гормона роста в крови. У здоровых людей содержание СТГ в крови составляет 0-7,5 нг/мл.
Повышение уровня СТГ в сыворотке крови встречается при акромегалии и гигантизме (СТГ-продуци-рующей аденоме гипофиза), неврогенной анорексии, хронической почечной недостаточности, циррозе печени, голодании, недостаточности белкового питания.
Аденома гипофиза при акромегалии может быть проявлением множественного эндокринного аденоматоза (МЭА 1типа).
К снижению уровня гормона роста в анализах крови могут приводить как изолированная недостаточность СТГ (гипофизарный нанизм), так и недостаточность СТГ в сочетании с недостаточностью других гормонов (гипопитуитаризм). Низкий уровень гормона роста в анализе может носить наследственный характер или быть связан с дефектом рецепторов к гормону роста (синдром Ларона). Низкий СТГ наблюдается у больных с врожденными дефектами развития (отсутствие передней доли гипофиза, гипоплазия зрительных нервов, заячья губа или волчья пасть). Приобретенная недостаточность СТГ может развиться как результат опухоли (краниофарингиома, герминома, гамартрома, глиома, саркома) или травмы (роды в ягодичном предлежании, внутричерепное кровоизлияние, черепно-мозговая травма, состояние после хирургического вмешательства на головном мозге) или сосудистой патологии (аневризмы сосудов гипофиза, ангиомы, инфаркт гипофиза). Кроме того, к снижению СТГ могут привести туберкулез, сифилис, саркоидоз и облучение гипофиза.
Адренокортикотропный гормон (АКТГ) представляет собой гормон гипофиза, играющий важнейшую роль в регуляции гипофизарно-надпочечниковых взаимоотношений. Уровень АКТГ в сыворотке (или плазме) крови здоровых людей колеблется от 10 до 70-80 пг/мл. Кроме того, имеется суточный ритм секреции АКТГ.
Содержание АКТГ в анализах крови повышено у больных с вторичной недостаточностью коры надпочечников, синдромом эктопированного АКТГ, когда АКТГ продуцируется опухолью внегипофизарного происхождения (рак легкого, бронхогенный карциноид, рак поджелудочной железы, медуллярный рак щитовидной железы, карциноид тимуса, феохромоцитома, карциноид желудочно-кишечного тракта), гипофиззависимой формой синдрома Иценко-Кушинга.
Секреция АКТГ существенно снижена при первичной надпочечниковой недостаточности, кортикостероме и раке коры надпочечников.
Пролактин — это гормон гипофиза полипептидной структуры, необходимый для созревания молочной железы и стимулирующий образование и выделение молока молочными железами. Подавляет секрецию половых гормонов. В норме к повышению уровня пролактина могут приводить сон, физическая нагрузка, половой акт. Концентрация пролактина в сыворотке крови взрослых мужчин составляет 80-265 мкЕд/мл, у менструирующих женщин — 130-540 мкЕд/мл и у женщин в менопаузе — 107-290 мкЕд/мл.
Повышение содержания пролактина в анализах наблюдается у беременных женщин и при целом ряде патологических состояний. К последним относятся синдром галактореиаменореи (синдром Чиари-Фромеля и синдром Дель Кастильо), инфекции (менингит, энцефалит и др.), аденомы гипофиза (пролактиномы), опухоли (глиома, менингиома, краниофарингиома), патология гипоталамуса (травмы, кровоизлияния, облучение, нейрохирургические операции), акромегалия (смешанная соматототропно-пролактиновая аденома), синдром Нельсона, гипотиреоз, саркоидоз, туберкулез, синдром Штейна-Левенталя, врожденная дисфункция коры надпочечников, почечная и печеночная недостаточность, внегипофизарные опухоли, выделяющие пролактин.
На результатах анализа может сказаться прием ряда фармпрепаратов. Так, могут давать завышение пролактина в крови следующие медикаменты: меток-лопрамид, домперидон, амитриптилин, галоперидол, верапамил, резерпин, альдомет, карбидофа, прием противозачаточных средств и циметидин.
Снижение концентрации пролактина в анализах наблюдается при гипофизарной недостаточности.
Фолликулостимулирующий гормон (ФСГ) представляет собой гормон гипофиза, регулирующий работу половых желез. ФСГ стимулирует рост и созревание половых клеток — яйцеклеток и сперматозоидов. У мужчин выделяется постоянно равномерно, у женщин — циклически, повышаясь в первую фазу менструального цикла. Яйцеклетка в яичнике растет в составе фолликула, состоящего из фолликулярных клеток. Эти клетки при росте фолликула под влиянием ФСГ синтезируют женские половые гормоны — эстрогены, которые, в свою очередь, подавляют выделение ФСГ (принцип отрицательной обратной связи). В норме уровень ФСГ у мужчин составляет 1,5-7 мЕд/мл. У здоровых женщин содержание ФСГ зависит от фазы менструального цикла: в фолликулиновую — 3-11 мЕд/мл, в середине цикла — 10-45 мЕд/мл, в лютеиновую фазу — 1,5-7 мЕд/мл.
Уровень ФСГ повышается при недостаточности функции половых желез генетического или аутоиммунного характера (первичный гипергонадотропныи гипогонадизм), кастрации, вследствие хирургического или лучевого лечения, при хроническом алкоголизме, орхите, в периоде менопаузы по механизму отрицательной обратной связи, а также опухолях гипофиза, продуцирующих фолликулостимулирующий гормон.
Снижение концентрации ФСГ в анализах может быть выявлено при гипофункция гипофиза или гипоталамуса (вторичный и третичный гипогонадотропный гипогонадизм) и при беременности.
Лютеинизирующий гормон (ЛГ) — это второй гормон гипофиза, отвечающий за деятельность половых желез. Л Г стимулирует выработку половых гормонов.
У женщин — прогестерона, у мужчин — тестостерона. У мужчин лютеинизирующий гормон, как и ФСГ, выделяется постоянно на одном уровне, у женщин — циклически, увеличиваясь во время овуляции и во вторую фазу менструального цикла. В норме уровень ЛГ у мужчин составляет 4-11 мЕд/мл. У здоровых женщин содержание ЛГ зависит от фазы менструального цикла: в фолликулиновую — 2-14 мЕд/мл, в середине цикла — 24-150 мЕд/мл, в лютеиновую фазу — 2-17 мЕд/мл.
Если в анализах имеет место повышение ЛГ, то следует предполагать наличие одного из следующих состояний: недостаточности функции половых желез, синдрома поликистозных яичников, опухоли гипофиза. Следует иметь в виду, что сильная эмоциональная нагрузка в виде стресса также может привести к увеличению содержания ЛГ в крови.
Снижение уровня ЛГ выявляется при гипофункции гипофиза или гипоталамуса, ряде генетических синдромов (синдром Кальмана), неврогенной анорексии.
Необходимо отметить, что у одного больного в анализах возможно снижение уровней сразу нескольких гормонов гипофиза. В этом случае говорят о гипопи-туитаризме — заболевании, развитие которого связано со снижением или полным выключением функции передней доли гипофиза.
Анализы крови и мочи, подробнее…
Сегодня 03.03.2020
с 10:00 до 19:00 на звонки
отвечает врач.

Опухоли гипофиза – группа доброкачественных, реже – злокачественных новообразований передней доли (аденогипофиза) или задней доли (нейрогипофиза) железы. Опухоли гипофиза, по статистике, составляют около 15% новообразований внутричерепной локализации. Они одинаково часто диагностируются у лиц обоих полов, обычно в возрасте 30-40 лет. Подавляющее большинство опухолей гипофиза составляют аденомы, которые подразделяются на несколько видов в зависимости от размеров и гормональной активности. Симптомы опухоли гипофиза представляют собой сочетание признаков объемного внутримозгового процесса и гормональных нарушений. Диагностика опухоли гипофиза осуществляется проведением целого ряда клинических и гормональных исследований, ангиографии и МРТ головного мозга.
Общие сведения
Опухоли гипофиза – группа доброкачественных, реже – злокачественных новообразований передней доли (аденогипофиза) или задней доли (нейрогипофиза) железы. Опухоли гипофиза, по статистике, составляют около 15% новообразований внутричерепной локализации. Они одинаково часто диагностируются у лиц обоих полов, обычно в возрасте 30-40 лет.
Гипофиз является железой внутренней секреции, осуществляющей регулятивно-координирующую функцию в отношении некоторых других эндокринных желез. Гипофиз расположен в ямке турецкого седла клиновидной кости черепа, анатомически и функционально связан с отделом головного мозга – гипоталамусом. Вместе с гипоталамусом гипофиз составляет единую нейроэндокринную систему, обеспечивающую постоянство гомеостаза организма.
В гипофизе выделяют две доли: переднюю – аденогипофиз и заднюю – нейрогипофиз. Гормонами передней доли, вырабатываемыми аденогипофизом, являются: пролактин, стимулирующий секрецию молока; соматотропный гормон, влияющий на рост организма через регуляцию белкового обмена; тиреотропный гормон, стимулирующий метаболические процессы в щитовидной железе; АКТГ, регулирующий функцию надпочечников; гонадотропные гормоны, влияющие на развитие и функцию половых желез. В нейрогипофизе образуются окситоцин, стимулирующий сократительную способность матки, и антидиуретический гормон, регулирующий процесс реабсорбции воды в канальцах почек.
Аномальное разрастание клеток железы приводит к образованию опухолей переднего или заднего отдела гипофиза и нарушению гормонального баланса. Иногда в область гипофиза прорастают менингиомы – опухоли мозговых оболочек; реже железа поражается метастатическими отсевами злокачественных новообразований других локализаций.
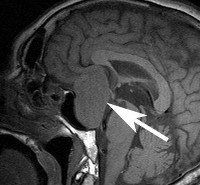
Причины опухолей гипофиза
Достоверные причины развития опухолей гипофиза до конца не изучены, хотя известно, что некоторые виды новообразований могут быть обусловлены генетически.
В число факторов, предрасполагающих к развитию опухолей гипофиза, входят нейроинфекции, хронические синуситы, черепно-мозговые травмы, гормональные изменения (в том числе вследствие длительного применения гормональных препаратов), неблагоприятное воздействие на плод в период беременности.
Классификация опухолей гипофиза
Опухоли гипофиза классифицируются с учетом их размеров, анатомического расположения, эндокринных функций, особенностей микроскопического окрашивания и т. д. В зависимости от размера новообразования выделяют микроаденомы (менее 10 мм в максимальном диаметре) и макроаденомы (при наибольшем диаметре более 10 мм) гипофиза.
По локализации в железе различают опухоли аденогипофиза и нейрогипофиза. Опухоли гипофиза по топографии относительно турецкого седла и окружающих его структур бывают эндоселлярными (выходящими за границы турецкого седла) и интраселлярными (расположенными в пределах турецкого седла). С учетом гистологической структуры опухоли гипофиза подразделяются на злокачественные и доброкачественные новообразования (аденомы). Аденомы исходят из железистой ткани передней доли гипофиза (аденогипофиза).
- соматотропная аденома
- соматотропинома – опухоль гипофиза, синтезирующая соматотропин — гормон роста;
- пролактиновая аденома
- пролактинома – опухоль гипофиза, синтезирующая гормон пролактин;
- кортикотропная аденома
- кортикотропинома — опухоль гипофиза, секретирующая АКТГ, стимулирующий функцию коры надпочечников;
- тиротропная аденома
- тиротропинома — опухоль гипофиза, секретирующая тиротропный гормон, стимулирующий функцию щитовидной железы;
Фоллтропинпродуцирующие или лютропинпродуцирующие аденомы (гонадотропные). Эти опухоли гипофиза секретируют гонадотропины, стимулирующие функцию половых желез.
Гормонально-неактивные опухоли гипофиза и пролактиномы встречаются наиболее часто (в 35% случаев соответственно), соматотропинпродуцирующие и АКТГ-продуцирующие аденомы – в 10-15% случаев от всех опухолей гипофиза, другие виды опухолей образуются редко. По особенностям микроскопии различают хромофобные опухоли гипофиза (гормонально-неактивные аденомы), ацидофилиные (пролактиномы, тиротропиномы, соматотропиномы) и базофильные (гонадотропиномы, кортикотропиномы).
Развитие гормонально-активных опухолей гипофиза, продуцирующих один или несколько гормонов, может приводить к развитию центрального гипотиреоза, синдрома Кушинга, акромегалии или гигантизма и т. д. Повреждение гормонопродуцирующих клеткок при росте аденомы может вызывать состояние гипопитуаризма (гипофизарной недостаточности). У 20% пациентов отмечается бессимптомное течение опухолей гипофиза, которые обнаруживаются лишь при аутопсии. Клинические проявления опухолей гипофиза зависят от гиперсекреции того или иного гормона, размеров и скорости роста аденомы.
Симптомы опухолей гипофиза
По мере увеличения опухоли гипофиза развиваются симптомы со стороны эндокринной и нервной систем. Соматотропинпродуцирующие аденомы гипофиза приводят к возникновению акромегалии у взрослых пациентов или гигантизма, если они развиваются у детей. Пролактинсекретирующие аденомы характеризуются медленным ростом, проявляются аменореей, гинекомастией и галактореей. Если такие опухоли гипофиза продуцируют неполноценный пролактин, то клинические проявления могут отсутствовать.
АКТГ-продуцирующие аденомы стимулируют секрецию гормонов коры надпочечников и ведут к развитию гиперкортицизма (болезни Кушинга). Обычно такие аденомы растут медленно. Тиротропинпродуцирующие аденомы нередко сопровождают течение гипотиреоза (функциональной недостаточности щитовидной железы). Они могут вызывать упорный тиреотоксикоз, чрезвычайно устойчивый к медикаментозному и хирургическому лечению. Гонадотропные аденомы, синтезирующие половые гормоны, у мужчин приводят к развитию гинекомастии и импотенции, у женщин – к нарушению менструального цикла и маточным кровотечениям.
Увеличение размеров опухоли гипофиза ведет к развитию проявлений со стороны нервной системы. Поскольку гипофиз анатомически соседствует с перекрестом зрительных нервов (хиазмом), то при увеличении размеров аденомы до 2 см в диаметре развиваются зрительные нарушения: сужение полей зрения, отек сосочков зрительного нерва и его атрофия, ведущие к падению зрения, вплоть до слепоты.
Аденомы гипофиза больших размеров вызывают сдавление черепных нервов, сопровождающееся симптомами поражения нервной системы: головные боли; двоение в глазах, птоз, нистагм, ограничение движений глазных яблок; судороги; упорный насморк; деменцию и изменения личности; повышение внутричерепного давления; кровоизлияния в гипофиз с развитием острой сердечно-сосудистой недостаточности. При вовлеченности в процесс гипоталамуса могут наблюдаться эпизоды нарушения сознания. Злокачественные опухоли гипофиза встречаются крайне редко.
Диагностика опухолей гипофиза
Необходимыми исследованиями при подозрении на опухоль гипофиза являются тщательное офтальмологическое и гормональное обследования, нейровизуализация аденомы. Исследование мочи и крови на содержание гормонов позволяет установить вид опухоли гипофиза и степень ее активности. Офтальмологическое обследование включает оценку остроты и полей зрения, позволяющих судить о вовлеченности в процесс зрительных нервов.
Нейровизуализацию опухоли гипофиза позволяет осуществить рентгенография черепа и зоны турецкого седла, МРТ и КТ головного мозга. Рентгенологически могут определяться увеличение размеров турецкого седла и эрозия его дна, а также увеличение нижней челюсти и пазух носа, утолщение костей черепа, и расширение межзубных промежутков. С помощью МРТ головного мозга возможно увидеть опухоли гипофиза диаметром менее 5 мм. Компьютерная томография подтверждает наличие аденомы и ее точные размеры.
При макроаденомах ангиография сосудов головного мозга указывает на смещение сонной артерии и позволяет дифференцировать опухоль гипофиза с внутричерепной аневризмой. В анализе спинномозговой жидкости может определяться повышенный уровень протеинов.
Лечение опухолей гипофиза
На сегодняшний день в лечении опухолей гипофиза эндокринология применяет хирургический, лучевой и лекарственный методы. Для каждого вида опухолей гипофиза существует специфический, наиболее оптимальный вариант лечения, который подбирается эндокринологом и нейрохирургом. Наиболее эффективным считается хирургическое удаление опухоли гипофиза. В зависимости от размеров и локализации аденомы проводится либо ее фронтальное удаление через оптический прибор, либо резекция через клиновидную кость черепа. Оперативное удаление опухолей гипофиза дополняется лучевой терапией.
Гормонально-неактивные микроаденомы лечатся с помощью лучевой терапии. Проведение лучевой терапии показано при наличии противопоказаний к оперативному лечению, а также пожилым пациентам. В послеоперационном периоде проводится гормонозаместительная терапия (кортизоном, тиреоидными или половыми гормонами), при необходимости — коррекция электролитного обмена и инсулинотерапия.
Из лекарственных препаратов используют агонисты дофамина (каберголин, бромокриптин), вызывающие сморщивание пролактин- и АКТГ-секретирующих опухолей гипофиза, а также ципрогептадин, понижающий уровень кортикостероидов у пациентов с синдромом Кушинга. Альтернативным методом лечения опухолей гипофиза является замораживание участка ткани железы при помощи зонда, введенного через клиновидную кость.
Прогноз при опухолях гипофиза
Дальнейший прогноз при опухолях гипофиза во многом определяется размерами аденом, возможностью их радикального удаления и гормональной активностью. У пациентов с пролактиномами и соматотропиномами полное восстановление гормональной функции наблюдается в четверти случаев, при адренокортикотропинпродуцирующих аденомах — в 70-80% случаев.
Макроаденомы гипофиза размером более 2 см полностью удалить невозможно, поэтому возможны их рецидивы в течение 5-летнего срока после операции.
Какие анализы нужно сдавать на гормоны гипофиза
Гипофизом называется мозговой придаток, который имеет форму округлого образования, находится на нижнем участке головного мозга в турецком седле (костном кармане). Гипофиз в человеческом организме производит гормоны, которые контролируют обмен веществ, рост, репродуктивную функцию и так далее.
Комплексное обследование, целью которого является уровень концентрации гормонов гипофиза в организме пациентов, как правило, включает в себя анализы, описанные ниже.
-
анализы на гормоны гипофиза
Эти анализы на гормоны гипофиза назначаются эндокринологом и гинекологом.
Зачем нужно сдавать анализы на гормоны гипофиза
Сдача крови на гормоны гипофиза – анализ, проведение которого позволяет врачу выявить или подтвердить диагноз при следующих заболеваниях:
- гигантизм;
- акромегалия (увеличение у пациента частей тела);
- несахарный диабет;
- гипофизарный нанизм;
- заболевание Иценко-Кушинга;
- гипофизарный гипогонадизм;
- гипофизарный гипотиреоз;
- gipyerprolaktinyemiya;
- синдром Шихана.
Сроки проведения анализов крови на вещества гипофиза зависят от того, в какой лаборатории проводится исследование. Срок действия гормональных анализов обязательно следует уточнить у врача.
Как подготовиться к анализам на гормоны гипофиза
Гормоны гипофиза отвечают за регулировку функционирования всех прочих эндокринных желез человека, сдача анализа крови на данные гормоны может потребоваться в целях диагностики множества заболеваний. Для получения корректных результатов крайне важно правильно подготовиться к исследованию.
анализ гормонов гипофиза
Анализ на гормоны гипофиза: подготовка
Правила подготовки к анализам могут изменяться в зависимости от того, какой гормон является объектом врачебного интереса.
- Если планируется анализ крови на фолликулостимулирующий гормон (ФСГ), обязательно нужно сдавать биологический материал на голодный желудок (минимум 12 часов без пищи). Мужчины могут проходить данное исследование абсолютно в любой день, тогда как женщинам рекомендуется делать это на 19-21 или 3-8 дни цикла.
- Если объектом исследования является лютеинизирующий гормон, женщинам рекомендуется выбирать для проведения анализа крови те же самые дни цикла, как и в предыдущем варианте, мужчинам – сдавать в любое время. Обязателен отказ от пищи в течение приблизительно 8 часов перед проведением исследования.
- Пролактин у женщин диагностируется дважды в месяц, в первых двух фазах цикла, обязательна сдача крови на анализ в утренние часы и натощак. Необходим также примерно получасовой отдых перед забором биологического материала.
Общие правила подготовки к анализу крови на гормоны гипофиза
Готовясь к сдаче крови на гормоны гипофиза, пациенты вне зависимости от пола должны соблюдать следующие правила.
- Где-то за двое суток до проведения анализа необходимо отказаться от курения, спиртных напитков. Под запретом также значительные физические нагрузки, к которым причисляются и сексуальные контакты.
- На результаты исследования могут оказать непосредственное влияние такие факторы как перегрев или переохлаждение. Профессиональный врач обязательно расскажет пациенту о том, что посещение зимней рыбалки или бани (сауны, парной) перед проведением анализа не допускается.
- Обязательно нужно поставить в известность врача, если пациент принимает те или иные медицинские препараты, так как это также определяет корректность диагноза. В большинстве случаев врач предлагает больному прервать курс медикаментозного лечения, если речь касается приема гормональных средств и препаратов, в составе которых присутствует йод.
- Анализы на гормоны гипофиза всегда рекомендуется проводить в утренние часы (8-11), это позволяет получить максимально достоверную картину исследования. Кровь берется в среднем спустя 12 часов после еды, желательно воздерживаться также от напитков, разумеется, исключая чистую воду, которую можно пить. Накануне анализа нужно следить за тем, чтобы в меню не включалась тяжелая и жирная пища.
Если пациент будет четко придерживаться всех правил подготовки, которые приводятся ниже, корректные результаты анализов на гормоны гипофиза обеспечены.
При частых головных болях, беспричинной слабости, повышенной утомляемости, перепадах настроения, ухудшении зрения, резком изменении веса нужно посетить эндокринолога. При углубленном обследовании медики нередко выявляют опухоль гипофиза. У женщин патологический процесс в важной железе встречается чаще.
При подтверждении развития доброкачественной либо злокачественной опухоли нужно пройти курс лечения под руководством эндокринолога, при необходимости требуется помощь онколога. Своевременное удаление новообразования снижает риск осложнений, избавляет от негативной симптоматики, мешающей привычной жизни.
Общая информация о гипофизе и опухолевом процессе

Важный орган находится между полушариями головного мозга. Небольшая структура отвечает за правильное функционирование всей эндокринной системы, развитие, рост, работу организма. Одна часть аденогипофиз продуцирует пролактин, соматотропин, тиреотропин, гонадотропины, адренокортикоидный гормон. Второй элемент гипофиза нейрогипофиз проводит распределение регуляторов, продуцируемых гипоталамусом.
На фоне опухолевого процесса нарушается синтез гормонов, происходит сдавление структур эндокринной железы, что приводит к неправильному функционированию гипофиза. Негативная симптоматика у большей части пациенток появляется, вне зависимости от характера опухолевого процесса (злокачественный либо доброкачественный).
Нередко новообразование само вырабатывает гормоны, что приводит к избыточной концентрации определенных веществ. Признаки гормонального сбоя у женщин проявляются в разных органах и системах, изменяется самочувствие и внешний вид, нередко развивается слабость, ухудшается сон и работоспособность.
Наиболее распространенный вид опухоли аденома гипофиза. У женщин эта разновидность доброкачественных новообразований формируется на фоне нарушения метаболизма, вирусных инфекций, заболеваний эндокринной системы.
Что такое кистозная мастопатия молочной железы и как лечить образование? У нас есть ответ!
О характерных симптомах сахарного диабета 1 типа и об особенностях терапии заболевания прочтите по этому адресу.
Причины возникновения образования
Патологические изменения вызывают несколько факторов, но точно определить причину опухолевого процесса медики могут не всегда. Существует несколько теорий о развитии аденомы, пролактиномы, других видов новообразований в гипофизе у женщин.
Врачи считают наиболее вероятными следующие факторы:
- обменные нарушения,
- генетическая предрасположенность,
- воздействие высоких доз радиации,
- травмы головного мозга, сильные ушибы, поражение костей черепа,
- отрицательное влияние на плод во время беременности,
- часто повторяющиеся синуситы. Наиболее опасны заболевания, протекающие глубоко в пазухах носа,
- врожденные аномалии,
- тяжелые вирусные инфекции, распространяющиеся на ткани мозга,
- бесконтрольный прием гормональных составов,
- аутоиммунные патологии.
Первые признаки и симптомы
Клиническая картина при росте и развитии гормонпродуцирующей опухоли:

- сонливость,
- частые головные боли, которые сложно подавить при помощи мощных анальгетиков,
- резкие колебания веса,
- отечность и одутловатость лица,
- ладони и ступни имеют размер больше привычного,
- исчезают либо заметно редеют волосы на бровях, теле, голове,
- нарушается регулярность менструального цикла,
- периодически беспокоят судороги,
- снижается сексуальное влечение,
- без причины появляется насморк,
- мужчины сталкиваются с гинекомастией увеличением грудных желез,
- изменяется состояние эпидермиса: усиливается сухость либо жирность кожных покровов, появляются трещины, морщины,
- повышается чувствительность к воздействию жары и холода,
- у женщин активно растут волосы на теле и над верхней губой,
- повышается давление,
- нарушается чувствительность кожных покровов,
- часто слезятся глаза, снижается зрение,
- возникают расстройства интеллекта, памяти, речи,
- изменяются контуры и форма элементов лица.
Развитие гормонпродуцирующей опухоли гипофиза провоцирует патологии:
- синдром Кушинга,
- гипотиреоз,
- гигантизм или акромегалию,
- гипопитуитаризм,
- формирование пролактиномы.
На заметку! Более 80 % пациентов ощущают негативное влияние опухоли гипофиза. Признаки развития гормонпродуцирующего новообразования выражены слабо или более ярко. Если опухоль не вырабатывает гормоны, то отрицательное влияние незначительное, симптоматика практически отсутствует. Некоторые люди не догадываются, что в тканях гипофиза сформировалось новообразование.
Виды опухоли гипофиза

Опухолевый процесс бывает доброкачественным и злокачественным. У 75 % пациенток и более обследование подтверждает развитие гормонпродуцирующего новообразования. Опухоль вырабатывает тиреотропин, кортикостероиды, пролактин, соматотропин, гонадотропины.
В зависимости от размеров и вида образования, появляются местные и периферические симптомы. Чем дольше протекает патологический процесс с активной выработкой дополнительного количества гормонов, тем сильнее нарушается неврологический статус, ухудшается обмен веществ, возникают признаки, указывающие на избыток определенного регулятора.
Основные виды опухолей гипофиза:
- образование, вырабатывающее адренокортикотропный гормон. Пациентки жалуются на растяжки, истончение конечностей при увеличении живота, поредение и выпадение волос, странные кровоподтеки на поверхности эпидермиса. Характерный признак луноподобное (круглое) лицо,
- пролактинома. Избыток гормона пролактина отрицательно влияет на функционирование яичников и состояние молочных желез. Грудь набухает, появляются выделения из молочных желёз, отсутствуют менструации, развивается гормональное бесплодие. Пока уровень пролактина не придет в норму, зачатие невозможно,
- опухоль, вырабатывающая половые гормоны. Избыток гонадотропинов приводит к маточным кровотечениям вне привычного режима менструаций, снижению периодичности месячных либо к их полному отсутствию. Опасное осложнение аденома в тканях гипофиза провоцирует развитие вторичного бесплодия,
- тиреотропинома. Нарушение выработки ТТГ провоцирует избыток либо недостаток гормонов щитовидной железы Т3 и Т4. Гормональный дисбаланс приводит к гипо- или гипертиреозу. Специфические признаки: экзофтальм, нарушение аппетита и сна, повышение температуры либо озноб, отеки, сухость кожи либо усиленная потливость. При тиреотоксикозе женщины часто раздражаются, страдают от панических атак и депрессивных состояний,
- опухоль, вырабатывающая соматотропин. Специфический признак повышение объема соединительной ткани. При этой разновидности опухолевого процесса происходит утолщение кончика носа, губ, фаланг пальцев, скул, мочек ушей, надбровных дуг, подбородка. Симптомы акромегалии изменяют внешность, провоцируют появление комплексов, нервозность, замкнутость. Один из специфических признаков акромегалии деформирующий артрит, нарушающий способность к активному передвижению.
Диагностика

Симптомы опухолевого процесса в важной железе повод для обращения к эндокринологу. Врач назначает МРТ гипофиза для получения подробных срезовых снимков железы. По результатам томограммы профильный специалист подбирает оптимальный вид оперативного вмешательства. Обязательна консультация нейрохирурга. При подозрении на злокачественный процесс нужна консультация онколога, анализ крови для уточнения значений онкомаркеров.
Эффективные методы лечения
Прием препаратов малоэффективен, пока опухоль находится в тканях гипофиза. Медикаментозную терапию для коррекции гормонального фона назначают после удаления аденомы гипофиза либо другого вида опухоли. В зависимости от размера новообразования, извлечение тканей опухоли выполняют через носовые ходы либо проводят трепанацию черепа.
При активном разрастании всех видов новообразований, появлении комплекса негативных признаков важно выяснить, какие факторы провоцируют быстрое прогрессирование патологического процесса. Периферические и местные симптомы исчезают спустя определенный период после удаления опухоли, но при сохранении провоцирующих факторов возможны рецидивы.
При малом размере тела пролактиномы, аденомы, тиреотропиномы, других видов образований, отсутствии местных негативных признаков возможная лучевая терапия. Воздействие специфических частиц подавляет рост клеток опухоли. При низкой эффективности метода назначают операцию для удаления новообразования.
Важно обратиться к опытному нейрохирургу: оперативное вмешательство, затрагивающее ткани гипофиза, требует высокой квалификации врача, правильного подбора гормональных составов после резекции опухоли.
Узнайте о том, как проявляется острый аднексит у женщин и как лечить воспалительное заболевание.
О причинах повышенного эстрадиола у женщин и о норме показателей гормона по возрасту написано на этой странице.
Возможные осложнения
При отсутствии грамотной терапии возможны хронические патологические процессы в организме, особенно, при формировании в тканях гипофиза гормонпродуцирующей опухоли. Чем дольше сохраняется повышенная концентрация пролактина, соматотропина, ТТГ, гонадотропных гормонов, АКТГ, тем больше негативных признаков проявляется у женщин.
При гормональном дисбалансе страдает репродуктивная система, появляются стойкие неврологические нарушения, изменяется внешность и характер. Дефицит сна, постоянные головные боли, стеснение из-за внешних признаков опухолевого процесса, снижение работоспособности факторы, отрицательно влияющие на повседневную жизнь и профессиональную деятельность. Гормональное бесплодие (вторичная форма) распространенное осложнение на фоне гормонпродуцирующих новообразований гипофиза.
Если вовремя не лечить злокачественные опухоли, то промедление с началом терапии может окончиться плачевно для пациента. Даже при доброкачественном характере опухоли нельзя оставлять новообразование без внимания: разрастание тела аденомы, тиреотропиномы, пролактиномы, синтез дополнительной порции гормонов, избыточное давление на соседние ткани нарушает функционирование мозга, отрицательно влияет на рост и развитие организма.
Опухоли гипофиза часто продуцируют собственные гормоны, что приводит к сбоям в работе эндокринной системы. Следствие патологических процессов нарушение функций и общего состояния организма. Женщины должны знать: опухоли гипофиза, особенно, пролактинома, негативно влияют на способность к зачатию. При своевременном лечении патологии прогноз благоприятный. Если сохраняется действие провоцирующих факторов, то возможны рецидивы опухолевого процесса.
В следующем видео выпуск телепередачи Жить здорово!, из которого можно узнать подробнее о лечении аденомы гипофиза:
Читайте также:



