Пгз онкология что это такое

Внимание! Регистрация желающих принять личное участие в конференции завершена.
Зарегистрироваться для онлайн-участия вы можете перейдя по ссылке
- Чем ЦАОП отличается от первичного онкологического кабинета?
Центр амбулаторной онкологической помощи (ЦАОП) создается как структурное подразделение медицинской организации для оказания первичной специализированной медико-санитарной помощи. Его основными задачами будут являться диагностика и лечение онкологических пациентов.
В первичном онкологическом кабинете в первую очередь ведется учет пациентов, наблюдение, контроль за их своевременной госпитализацией, оказывается всесторонняя помощь больному. Во многих субъектах вся диагностика и лечение проводятся на базе онкологического диспансера, иногда это может существенно влиять на время ожидания пациентами медицинской помощи.
Создание ЦАОП предполагает наличие всего спектра диагностического оборудования, необходимого для полного обследования пациента при подозрении на наличие злокачественного новообразования еще до его направления в онкодиспансер. Это позволяет сократить сроки начала его диагностики. Дополнительно в ЦАОП планируется создание коек дневного стационара.
Установление диагноза и определение методов лечения пациента, конечно, происходит на базе онкодиспансера. При этом для проведения некоторых схем химиотерапии пациента можно направлять в ЦАОП. Здесь же можно осуществлять оценку эффективности и переносимости проводимого лечения, проводить восстановительную и корригирующую терапию, связанную с возникновением побочных реакций на фоне лечения. И все это теперь пациент сможет получать ближе к своему дому.
ЦАОП может быть организован на базе поликлиники, центральной районной больницы, многофункционального медицинского центра, иногда даже онкодиспансера. Все зависит от индивидуальных особенностей каждого субъекта РФ. Как правило, ЦАОП организуется на базе той медицинской организации, которая уже достаточно оснащена всем необходимым диагностическим оборудованием. Если же его недостаточно, то многие региональные власти берут на себя решение этой задачи. В большинстве случаев это оборудование используется не только для пациентов ЦАОП, но и для других посетителей данной медицинской организации. Поэтому поддержка региональных властей проектов по организации ЦАОП крайне важна для жителей региона.
Организация ЦАОП не предполагает ликвидацию первичных онкологических кабинетов. Пациент может быть направлен врачом поликлиники в первичный онкологический кабинет или в ЦАОП. Это зависит от особенностей региона – его площади, плотности населения, транспортной доступности и в целом состоянии ресурсной базы онкологической службы региона. Поэтому принимать решение об открытии ЦАОП, определять их требуемое количество, место их организации, количество прикрепленного населения необходимо только по результатам глубокого анализа ситуации.
- Как пациенты попадают в ЦАОП?
Они могут обратиться туда самостоятельно, а могут быть направлены из поликлиники или первичного онкологического кабинета. Никаких ограничений нет. Многие регионы стараются широко информировать население об открытии ЦАОП, где он находится, как туда можно попасть, как добраться. Подробно прописывают маршрутизацию пациента с подозрением на онкологическое заболевание так, чтобы каждый врач знал, какие шаги он должен предпринять, чтобы направить пациента в ЦАОП.
- В чем еще особенность ЦАОП?
Хотите узнать больше о конференции? Подробности здесь
На основе гистологического заключения. Злокачественность опухоли напрямую влияет на исход болезни: чем выше степень, тем агрессивнее рак, и тем хуже прогноз для выздоровления.
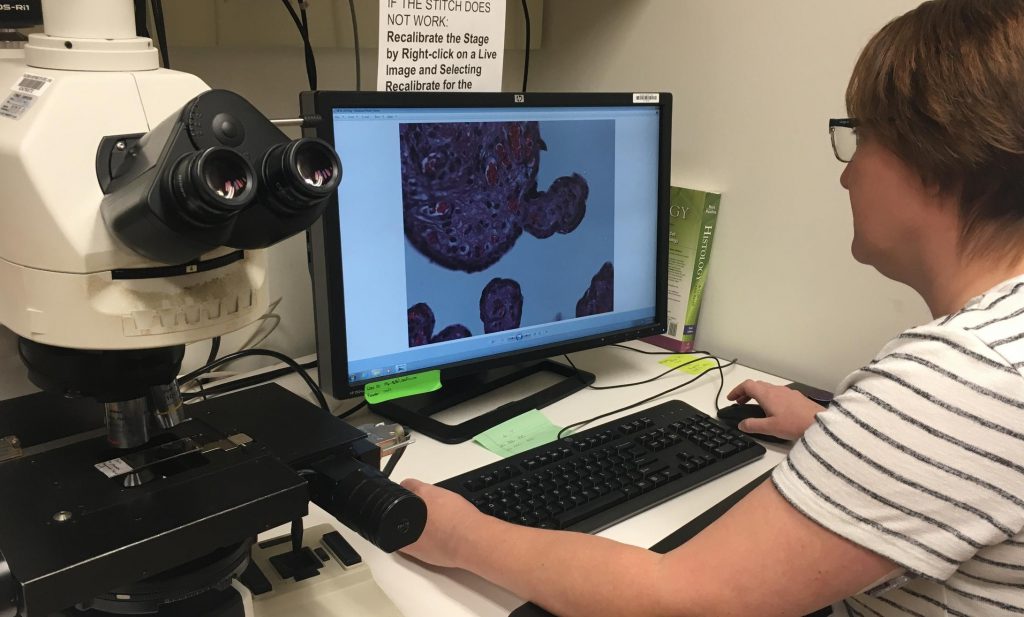
Врач-гистолог оценит степень злокачественности
Злокачественность опухоли
Морфологическое исследование удаленных раковых тканей, как обязательный этап диагностики, помогает определить злокачественность опухоли. В организме человека триллионы клеточных структур, основой которых являются около 100 различных типов клеток: каждая из них может переродиться в раковую. При этом результат перерождения-трансформации может быть морфологически очень близок к исходно нормальной клетке. Или настолько сильно отличаться, что, кажется, и сравнивать не с чем.
Злокачественность опухоли – это степень клеточных изменений, указывающая на агрессивность Карциномы: чем выше цифра после буквы G, тем сильнее отличается злокачественное новообразование от исходной ткани в месте возникновения рака.
Степени злокачественности
Гистологический диагноз – это морфологический вариант опухоли и степень злокачественности. Выделяют 3 степени:
- Высокая степень дифференцировки опухолевой ткани (G1) – клетки первичного очага отличаются от нормальных клеточных структур удаленного органа или ткани, но морфологически похожи: у врача-гистолога нет никаких сомнений в том, что основой злокачественного перерождения стали клетки именно из этого органа или ткани;
- Средняя степень дифференцировки (G2) – схожие черты исходной ткани сохраняются, но различий больше: гистологически опухоль сильно отличается от нормы, но отошла еще не так далеко;
- Низкая степень (G3) – раковые клетки имеют крайне мало сходства с органом или тканью в первичном очаге: гистолог сразу понимает, что это чужеродный и агрессивный зверь.
Необходимо обращать внимание на цифровое значение критерия G в диагнозе: низкодифференцированные опухоли всегда прогностически хуже, при G1 шансы на выздоровление значительно выше.
Значимость клеточных изменений опухоли
Важно понимать: злокачественность опухоли – это одно из значений диагноза, необходимое для реального понимания силы Карциномы. Это вовсе не означает, что при G3 нет никаких шансов для выживания, а при G1 можно радостно подбрасывать чепчики – типа, мы уже почти победили врага.
Высокодифференцированные опухоли – это:
- Сравнительно медленная скорость прогрессирования;
- Низкий риск быстрого и раннего метастазирования;
- Высокая чувствительность к лекарственной терапии;
- Высокие шансы на длительную ремиссию.
Низкодифференцированные раки – это:
- Быстрый рост первичного опухолевого очага;
- Ранние метастазы в лимфоузлы и отдаленные органы;
- Отсутствие положительного ответа на химиотерапию;
- Низкие шансы на выживаемость.
Казалось бы, все просто: G1 – это благоприятно, G3 – это плохо. Но в жизни все значительно сложнее, потому что на прогноз при онкологии влияют масса факторов. Злокачественность опухоли – это важный элемент диагностики, на который надо обращать внимание: низкая степень дифференцировки раковых клеток указывает на то, что враг силен, зол, беспринципен и агрессивен. Война будет изнурительно-длительной, не каждая битва будет успешной, после каждого боя будет казаться, что Карцинома становится сильнее, но, тем не менее, шансы на победу есть всегда.

- ИГХ исследования – что это такое
- Суть методики
- Кому показано
- ИГХ исследования: что это такое и как проводятся
- Расшифровка
ИГХ исследования – что это такое
ИГХ представляет собой методику, используемую в патологической анатомии для диагностики раковых и доброкачественных опухолей. Его назначают, когда установить точный диагноз стандартным гистологическим способом невозможно или необходима детализация клинически значимых параметров новообразований на молекулярном уровне.
Очень часто гистологии бывает недостаточно. В большинстве случаев причиной этому является крайне нетипичная структура патологического образования, что существенно затрудняет постановку точного диагноза. В частности, при лимфоме и лейкозе ИГХ делают практически всегда.
Нужно отметить, что всего насчитывается около 70 разновидностей лейкозов и лимфом. Верифицировать некоторые их них удается лишь путем нескольких исследований – гистологического, иммуногистохимического и молекулярно-генетического.
Суть методики
При развитии любого опухолевого процесса формируются чужеродные организму белки – антигены, в противовес которым иммунная система человека вырабатывает антитела – иммуноглобулины. Они прикрепляются к антигенам и связываются с эпитопами – основными частями антигенных макромолекул. Антитела выполняют сразу две функции: связывающую и эффекторную. Проще говоря, они напрямую мешают антигенам наносить вред и одновременно активируют комплемент, запуская ответную реакцию иммунитета.
Роль антигенов в данном случае принадлежит атипичным опухолевым клеткам. Перед тем как провести иммуногистохимическое исследование, срезы биометариала маркируются специфическими антителами к ним. В целях дальнейшей визуализации эти антитела окрашиваются ферментами. Далее, используя высокоточную оптику, наблюдают за поведением испытуемых клеток.
Если белковые соединения, помеченные как антитела, связываются с опухолевыми клетками, будет видно свечение – флюоресценцию, свидетельствующую о наличии искомых веществ. Так выявляют, например, рецепторы к гормонам и онкомаркеры. При подозрении на рак молочной железы таким образом обнаруживаются рецепторы к эстрогену и прогестерону.
Кому показано
В отдельных случаях иммуногистохимический анализ позволяет установить источник метастазов, когда локализация первичного очага неизвестна, а также провести дифференциальную диагностику при нескольких новообразованиях разного происхождения.
ИГХ может назначаться при бесплодии, хронических патологиях эндометрия, матки и яичников, привычных выкидышах. Ее целесообразно делать и в том случае, если беременность не наступает после нескольких процедур ЭКО.
Иммуногистохимия поможет обнаружить наличие клеток, препятствующих зачатию, и определить дальнейшую тактику лечения бесплодия.
Методом ИГХ оценивают и лекарственную чувствительность путем выявления:
- рецепторов половых гормонов – эстрогена, прогестерона и андрогенов. Необходимо при поражении женской репродуктивной системы;
- фактора роста опухоли Her2/neu. Биомаркер и терапевтическая мишень агрессивных типов рака груди;
- соматостатиновых рецепторов 2а и 5 типа, важных при карциноидах;
- мембранного белка иммуноглобулинов PD-L1, гена ALK и рецептора тирозинкиназы ROS. Данные показатели исследуются преимущественно при немелкоклеточном раке легких;
- микросателлитной нестабильности;
- индекса пролиферативной активности.
Трудно переоценить важность микросателлитной нестабильности (MSI), которая существенно расширяет прогностические и лечебные возможности у пациентов со злокачественными поражениями ЖКТ. Новообразования с низкой MSI медленнее растут и реже дают метастазы. Поэтому своевременное выявление MSI позволяет избежать назначения агрессивной, но заведомо неэффективной терапии.
ИГХ исследования: что это такое и как проводятся
Для выполнения ИГХ необходим биоматериал, забор которого осуществляется в основном путем взятия биопсии. Несколько реже его получают в ходе эндоскопической или классической открытой операции. Способ изъятия пораженной ткани зависит от типа и локализации рака. При этом следует учесть, что брать материал на анализ следует до начала терапии. В противном случае возможно искажение результатов исследования.
Этапы проведения анализа:
- Полученный биоматериал фиксируют, обрабатывая в формалине, и отправляют в лабораторию.
- Затем его обезжиривают и подвергают повторной фиксации, после чего заливают парафином.
- Далее производится микротомирование – с готовых парафиновых блоков делаются тонкие срезы, которые помещаются на специальные стекла. Толщина среза составляет не больше 1 мкм.
Когда ткани лежат на стеклах, их обрабатывают раствором антител. Количество их видов ограничено несколькими десятками. Исследование реакций с применением до 5 разных антител проводится на малой панели. При более масштабном эксперименте нужна большая панель.
В ходе ИГХ рак любого органа проявляется эффектом свечения – флюоресценции, – благодаря чему выявляются злокачественные клетки, определяются рецепторы гормонов или другие заданные параметры.
Расшифровка
Изучением срезов биоматериала занимаются врачи-патологоанатомы. Они же первыми составляют прогноз, исходя из выявленного типа и объема онкогенных клеток. При расшифровке результатов особое внимание обращают на показатель К-67 – специфический белок, антиген ракового процесса. Он вырабатывается только при активном делении клеток, а в состоянии покоя не продуцируется.
К-67 – это именно тот онкомаркер, что показывает степень озлокачествления процесса. Если его уровень в процентном содержании составляет 85% и выше, то заболевание прогрессирует стремительно и с высокой вероятностью вскоре приведет к смерти.
Благоприятным будет прогноз при К-67=10%. В случае грамотно составленного плана терапии есть все шансы на полное выздоровление, зачастую без риска рецидива. При К=30% констатируют среднюю степень тяжести болезни, что означает достаточно быстрый рост рака. С помощью курсовой химиотерапии его можно замедлить и даже остановить.
Однако К-67 – это не единственный показатель, который указывается в медицинском заключении. Также записываются антитела, к которым выявлены соответствующие антигены, тип и количество последних.
Полученное заключение врач-патологоанатом передает лечащему онкологу, который подбирает лечение. Для оценки его эффективности иммуногистохимию проводят еще раз после завершения терапевтического курса.
гос., сетевое
филиал СУАЛа: ПГЗ-СУАЛ
г. Пикалёво
Ленинградская обл.
Словарь сокращений и аббревиатур . Академик . 2015 .
- ИБОР ОМУ
- ПГЗУ
ПГЗ — Микросхемы звукогенераторов специализированные микросхемы для генерации звука. Они могут использоваться для воспроизведения звуковых эффектов и синтезированной музыки (см. chiptune) в компьютерах, игровых системах (консолях, автоматах) и бытовой… … Википедия
Закрытие ПЗРО (ПГЗ ЖРО) — 4. Закрытие ПЗРО (ПГЗ ЖРО) деятельность, осуществляемая после завершения размещения РАО в ПЗРО (ПГЗ ЖРО) и направленная на приведение ПЗРО (ПГЗ ЖРО) в состояние, которое будет оставаться безопасным в период потенциальной опасности размещенных в… … Словарь-справочник терминов нормативно-технической документации
Безопасность ПЗРО (ПГЗ ЖРО) — 1. Безопасность ПЗРО (ПГЗ ЖРО) свойство ПЗРО (ПГЗ ЖРО) при нормальной эксплуатации и нарушениях нормальной эксплуатации, включая аварии, ограничивать радиационное, а также другие сопровождающие его воздействия на работников (персонал), население… … Словарь-справочник терминов нормативно-технической документации
Ближняя зона ПЗРО (ПГЗ ЖРО) — 2. Ближняя зона ПЗРО (ПГЗ ЖРО) часть природного геологического образования, окружающего предназначенные для захоронения РАО сооружения ПЗРО (ПГЗ ЖРО), характеристики которого меняются или могут измениться под воздействием захороненных РАО.… … Словарь-справочник терминов нормативно-технической документации
Комплексное инженерное и радиационное обследование ПЗРО (ПГЗ ЖРО) — 8. Комплексное инженерное и радиационное обследование ПЗРО (ПГЗ ЖРО) комплекс мероприятий, необходимых для получения исходных данных для разработки проекта реконструкции или проекта закрытия ПЗРО (ПГЗ ЖРО). Источник: НП 055 04: Захоронение… … Словарь-справочник терминов нормативно-технической документации
Мониторинг системы захоронения радиоактивных отходов после закрытия ПЗРО (ПГЗ ЖРО) — 9. Мониторинг системы захоронения радиоактивных отходов после закрытия ПЗРО (ПГЗ ЖРО) комплексная система наблюдений и контроля за состоянием барьеров и компонентов природной среды, а также оценки и прогноза изменений в ближней зоне ПЗРО (ПГЗ… … Словарь-справочник терминов нормативно-технической документации
Полигон глубинного захоронения жидких радиоактивных отходов (ПГЗ ЖРО) — 11. Полигон глубинного захоронения жидких радиоактивных отходов (ПГЗ ЖРО) природно техническая система, предназначенная для захоронения ЖРО, располагающаяся в пределах определенной проектом территории, включающая участок недр поглощающий горизонт … Словарь-справочник терминов нормативно-технической документации
Пределы безопасной эксплуатации ПЗРО (ПГЗ ЖРО) — 12. Пределы безопасной эксплуатации ПЗРО (ПГЗ ЖРО) установленные проектом значения параметров технологического процесса, отклонения от которых могут привести к аварии. Источник: НП 055 04: Захоронение радиоактивных отходов. Принципы, критерии и… … Словарь-справочник терминов нормативно-технической документации
Условия безопасной эксплуатации ПЗРО (ПГЗ ЖРО) — 17. Условия безопасной эксплуатации ПЗРО (ПГЗ ЖРО) установленные проектом условия по количеству, характеристикам, состоянию работоспособности и условиям технического обслуживания систем (элементов), важных для безопасности, при которых… … Словарь-справочник терминов нормативно-технической документации
- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
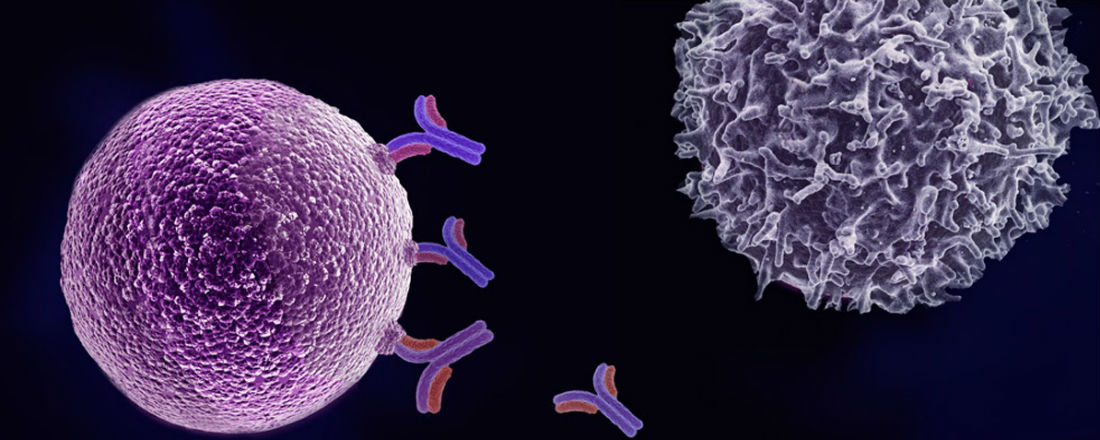
Что такое иммунотерапия?
Объясните, как это работает?
Откуда вообще взялся этот метод лечения?
Первые попытки вылечить пациентов, больных раком, с помощью иммунотерапии были предприняты более ста лет назад. Одним из родоначальников метода считается хирург Уильям Коли. Он заметил, что у некоторых пациентов с рожистым воспалением (бактериальной кожной инфекцией) онкологическое заболевание полностью регрессировало. Коли предположил, что инфекция стимулирует иммунитет на уничтожение опухолевых клеток, и решил подтвердить свои догадки экспериментально. В 1891 году он ввел стрептококковые бактерии пациенту с саркомой кости и смог добиться сокращения злокачественной опухоли.
Тогда его исследования подверглись активной критике, так как не имели внятного теоретического обоснования. Постепенно накапливались знания о физиологии иммунитета, вместе с этим предпринимались новые попытки активировать собственные защитные силы организма для борьбы со злокачественными опухолями — иммунотерапия получила развитие.
Если иммунотерапия существует так давно, почему о ней активно заговорили только сейчас?
Потому что настоящие прорывы произошли лишь в последние годы. Так, в 2018-м Нобелевскую премию по медицине вручили ученым Джеймсу Эллисону из США и Тасуку Хондзё из Японии за открытие контрольных точек — благодаря этому было создано несколько иммунотерапевтических препаратов. Короткий промежуток между теоретическим открытием и внедрением его результатов в медицинскую практику — еще одна причина того, что о новой методике активно говорят. Иммунотерапия открыла новые возможности для борьбы с онкологическими заболеваниями, которые лечатся с большим трудом, например с меланомой и раком легких. Теперь некоторые такие пациенты могут жить на несколько лет дольше без прогрессирования болезни.
Любой ли рак можно вылечить с помощью иммунотерапии?
Это зависит от препарата и особенностей опухоли. Так, препарат пембролизумаб стал первым, который можно назначать вне зависимости от места возникновения рака, если опухоль имеет специфический биомаркер — микросателлитную нестабильность, или PDL-экспрессию. Иммунотерапию применяют для лечения меланомы, рака легких, почки, желудка, мочевого пузыря, простаты, поджелудочной железы, глиобластомы, лимфомы Ходжкина и еще нескольких видов опухолей. Но пока лучшие результаты терапия показала в лечении меланомы и рака легких. Определить, какое лечение подойдет в конкретном случае, может только лечащий врач.
А побочные эффекты есть?
Есть. Так же как и у других эффективных методов лечения онкологических заболеваний — но они отличаются от нежелательных явлений при химиотерапии: причина их возникновения не токсическое действие самих препаратов, а сильный иммунный ответ. Нередко пациенты на иммунотерапии могут сталкиваться с усталостью, кашлем и тошнотой, теряют аппетит, а на коже может появиться сыпь. Реже эти лекарства могут вызывать более серьезные проблемы в легких, кишечнике, печени, почках и других органах. Обычно так бывает, если иммунитет начинает атаковать не только опухолевые клетки, но и здоровые. Пациенты, которые проходят лучевую терапию, также нередко испытывают усталость, у них могут быть проблемы с кожей, а люди, которые получают химиотерапию, сталкиваются с потерей волос, анемией, тошнотой и рядом других проблем.
Объясните, как проходит лечение. Обязательно ложиться в больницу?
В России этот метод лечения популярен?
Нет. Некоторые препараты, например пембролизумаб, ниволумаб, ипилимумаб и атезолизумаб, зарегистрированы в России. Но о широком доступе к терапии говорить не приходится. Препараты зарегистрированы не по всем показаниям, и во многих ситуациях назначить их можно только офлейбл (не по инструкции), но тогда лечение нельзя будет получить бесплатно по полису ОМС.
Рак является одним из самых страшных и в то же время распространенных заболеваний. При своевременном обнаружении онкология хорошо поддается терапии.
Однако если патология не была диагностирована на начальной стадии, то раковые клетки начинают распространяться по всему организму, развивается инвазивный рак.
Что такое инвазия в онкологии знают далеко не все люди. А ведь от данного процесса метастазирования зависит течение онкологии, возможные осложнения.

Понятие инвазии опухоли
Инвазия опухоли – что это такое? Это патологический процесс, при котором раковые клетки отсоединяются от первичного новообразования и распространяются по организму, прорастая сквозь ткани других органов. Так формируются вторичные опухолевые очаги.
Некоторые считают, что инвазия и метастазирование – это одинаковые понятия, на самом деле – это различные вещи. В нормальном состоянии клетки обладают способностью к инвазивному росту. Это проявляется в ситуациях:
- в период вынашивания ребенка (плацента врастает в стенку матки);
- период роста, развития эмбриона;
- регенерация крупных ран.
Инвазия в онкологии является начальным процессом развития метастаз в разных частях организма. Инвазивный рак очень сложно поддается лечению. Объясняется это тем, что раковые клетки, будучи за пределами базальной мембраны, усиленно питаются и насыщаются кислородом, вследствие этого иммунитет ослабляется и происходит обширное поражение организма.
Если терапия не была проведена своевременно, то рак перейдет в запущенную фазу и вероятность излечения будет минимальной.
Этапы инвазивного процесса
Инвазия опухоли протекает постепенно. Весь процесс развития инвазивного рака происходит в несколько этапов:
- Первая стадия . Межклеточные контакты ослабляются, мембранные белки, которые связывают между собой раковые клетки, отдаляются друг от друга, их количество уменьшается. В это же время концентрация клеток, обеспечивающих мобильность новообразований, повышается. При инвазионном раке размеры опухоли не превышают 2 см,
- Вторая стадия . Раковые клетки крепятся к тканям матрикса (межтканевый барьер организма, состоящий из соединительнотканных структур и базальных клеточных мембран). Размеры опухоли на данном этапе инвазивного рака достигают 2-5 см.
- Третья стадия . Раковые клетки вырабатывают особые ферменты, способствующие ослаблению матрикса. В результате это провоцирует разрушение тканевых барьеров. На этом этапе новообразование не обладает четкими границами, наблюдается склеивание патологических клеток в лимфоузлах.
- Четвертая стадия . Запущенная форма инвазионного рака, при которой патологические клетки мигрируют в соседние структуры, все больше поражая организм пациента. Наблюдаются метастазы в отдаленных органах.
Стандартный процесс инвазии в онкологии состоит из 4 этапов, их длительность в каждом случае может отличаться. И если у одного человека инвазивный рак развивается в течение нескольких лет, то у других переход с первой стадии в последнюю может занять всего пару месяцев.

Как развивается в разных органах
Инвазия опухоли – патологический процесс, способный поражать абсолютно любой орган человеческого организма. Наименее подвержены инвазивному раку органы с плотной фиброзной тканью, плотными артериальными стенками и хрящевой структурой. Редко патология затрагивает почки и печень. Часто диагностируется инвазия шейки матки или молочных желез.
Инвазия шейки матки является распространенным онкологическим заболеванием, которое чаще всего диагностируется у женщин 45-55 лет. Вероятность развития патологии повышается при наличии предрасполагающих факторов:
- заражение папилломавирусом человека;
- венерические заболевания;
- беспорядочные половые связи;
- прием гормональных средств;
- перенесенная онкология мочеполовой системы;
- множественные роды;
- некоторые женские заболевания;
- ранее начало сексуальной жизни;
- курение.
Заподозрить развитие инвазивного процесса в шейке матки можно по симптомам:
- нерегулярные менструации;
- кровотечения во время полового акта;
- водянистые выделения;
- зловоние;
- нарушение мочеиспускания;
- боли внизу живота.
Помимо этого могут присутствовать неспецифические признаки, как гипергидроз, потеря аппетита, головокружение и слабость.
Инвазия молочной железы (инвазивная карцинома) представляет собой быстропрогрессирующий тип раковой опухоли, который при попадании в лимфотоки разносится по всему организму. Такая разновидность онкологии развивается по ряду причин:
- мастопатия;
- фиброаденома;
- отказ от грудного вскармливания;
- аборт при первой беременности;
- хронические патологии репродуктивной системы;
- нерегулярная половая жизнь;
- генетическая предрасположенность.
Проявляется инвазивный рак молочной железы по-разному. Если раковые клетки не распространяются за пределы груди, то пациентка может изредка ощущать дискомфорт и болезненность при ощупывании молочных желез. При развитии патологии возникают симптомы:
- болезненность сосков;
- кровянистые выделения из сосков;
- изменение формы груди;
- уплотнения в груди, не имеющие точных границ.
При данном заболевании наблюдаться покраснение, побледнение или сморщивание кожи в области грудной клетки.

Факторы инвазивности процесса
Для того чтобы злокачественная опухоль проросла сквозь базальную мембрану, необходимо наличие таких предрасполагающих факторов:
- Давление. Чем больше атипичных клеток, тем выше сила давления в тканях первичного ракового очага. В результате оказывающегося давления имеющиеся межтканевые барьеры разрушаются, происходит поражение соседних тканей.
- Подвижность клеток. Раковые клетки мигрируют в направлении тканей, которые обладают высоким уровнем pH, а также большей концентрацией кислорода и питательных веществ.
- Контакты между клетками. Раковые клетки имеют слабые связи, из-за чего вероятность их попадания в кровоток и соседние структуры существенно возрастает.
- Лизосомальные ферменты. Раковые новообразования продуцируют литические ферменты, которые способствуют разрушение здоровых клеток, провоцируя развитие инвазии.
- Пролиферативное свойство. Благодаря данному свойству ткани увеличиваются в размерах. При разрастании ткани, окружающей опухоль, раковые клетки могут свободно перемещаться по организму.
- Особенности иммунитета. От состояния иммунной системы во многом зависит течение патологии. Если иммунная система ослаблена, то скорость распространения раковых клеток за пределы первичного очага существенно увеличивается. Сильный иммунитет, напротив, максимально затормаживает процесс инвазии.
Процесс инвазии также зависит и от таких факторов, как травмы и повреждения, воспалительные процессы, отеки и клеточная пролиферация.
Способы диагностики
На начальной стадии развития инвазивного рака специфические симптомы отсутствуют, из-за чего появляются трудности со своевременным обнаружением проблемы. Чтобы выявить инвазию необходимо проходить регулярные скрининговые обследования. И поскольку инвазионные опухоли чаще всего диагностируются в молочных железах и шейке матки, женщины после 20 лет должны каждый год проверяться у гинеколога и маммолога.
При появлении подозрений на инвазию опухоли следует пройти детальное обследование, включающее в себя проведение таких методов диагностики:
- общие анализы крови и мочи;
- ультразвуковое исследование;
- рентгенография;
- КТ, МРТ.
Потребуется прохождение позитронно-эмиссионной томографии, дуктографии, пиелографии, ректороманоскопии. Обязательно проводится гистологическое обследование, иммуногистохимические тесты.

Методы лечения
Лечение инвазивного рака зависит от степени патологического процесса, особенностей протекания онкологии, расположения опухоли и многого другого. В зависимости от стадии онкологического процесса врачи могут назначать терапию следующего типа:
- нулевая, первая стадия – хирургическое вмешательство;
- вторая – лучевая терапия в сочетании с операцией;
- третья – химиотерапия, комбинированная с радиационной терапией;
- четвертая – лучевая, паллиативная терапия.
Могут проводиться и другие методики лечения, в том числе и экспериментальные. Курс терапии подбирается только опытным специалистом, после прохождения летального обследования.
Прогноз при инвазии опухоли зависит от того, на каком этапе была обнаружена проблема. Если лечение было начато на первой стадии, то выживаемость составляет 90%. При поздней диагностике срок жизни пациента не превышает 1 года.
Читайте также:





