Периампулярный рак что это такое
Московский государственный медико-стоматологический университет
ПЕРИАМПУЛЯРНЫЕ ОПУХОЛИ
Рассмотрены проблемы хирургического лечения опухолей панкреатодуоденальной зоны периампулярной локализации. Подробно изложены особенности диагностики рака, доброкачественных и нейроэндокринных новообразований с применением современных методов инструментального, биохимического и морфологического исследования. Подчеркивается разумная радикальность хирургических вмешательств, так как опухоли периампулярной локализации часто имеют непредсказуемое течение, а окончательный диагноз становится возможным только после их удаления. Прогноз жизни пациентов со злокачественными периампулярными новообразованиями после своевременной операции и комплексной химиотерапии значительно улучшается.
В лечении опухолей такой локализации остается нерешенным ряд проблем:
- опухоли диагностируются поздно даже у лиц группы риска;
- сложен дифференциальный диагноз с доброкачественными опухолями и воспалительными процессами;
- не определены предпочтительный метод и срок би-лиарной декомпрессии при механической желтухе;
- не всегда очевиден выбор метода паллиативной и радикальной операции;
- сложности представляет профилактика послеоперационных осложнений;
- нужно совершенствование адъювантной терапии.
В скрининговом обследовании и ранней диагностике периампулярных опухолей основную роль в настоящее время играют опухолевые маркеры, спиральная компьютерная томография и эндоскопическая соно-графия. Диагностические возможности транскутан-ного ультразвукового исследования повышаются при дуплексном сканировании с использованием цвето-
Кубышкин Валерий Алексеевич - член-кор. РАМН, д-р мед. наук, профессор, заведующий кафедрой общей хирургии МГМСУ; тел.: 8 (495) 359-02-46; e-mail: info@DrSurgion.ru.
вого допплеровского картирования для оценки кровоснабжения новообразования и состояния прилежащих сосудов. Злокачественные опухоли характеризуются усиленным кровоснабжением, наряду с изменением анатомической позиции и просвета артерий. Важным признаком злокачественной опухоли является изменение просвета магистральных вен (селезеночной, верхней брыжеечной и воротной) и появление в них тромбов [4, 6]. Высокое диагностическое значение имеет магнитно-резонансная томография, которая дает также полную картину состояния желчевыводящих и панкреатического протоков [1-3, 5, 7].
Дифференциальный диагноз при периампуляр-ных опухолях сложен, потому что многочисленные доброкачественные новообразования, нейроэндок-ринные опухоли или псевдоопухолевые воспалительные изменения могут проявляться схожей клинической и инструментальной семиотикой [4, 5, 7, 10].
Для хронического панкреатита с увеличением железы, напоминающим опухоль, в отличие от рака характерен продолжительный анамнез с эпизодами острого панкреатита, превалирование болевого синдрома, связанного с приемом пищи или погрешностями в диете. При ультразвуковом, компьютерном томографическом обследовании в пользу хронического воспаления могут свидетельствовать конкременты в паренхиме или протоках, мелкие кистозные образования в зоне измененной железы [1, 11].
В исходе острых и хронических воспалительных процессов часто развиваются псевдокисты, которые могут иметь различную форму, стенку и содержимое. Поэтому дифференциальная диагностика между ними и кистозными формами рака по данным лучевых методов исследования также во многих случаях оказывается сложной задачей [11]. Воспалительные кистозные образования имеют ровные контуры, а опухолевые обычно имеют папиллярные разрастания в просвете и толстую, плотную капсулу. Достоверно диагноз можно установить только после биопсии стенки образования во время операции [3, 5, 13].
Ряд особенностей присущ инструментальной семиотике нейроэндокринных опухолей поджелудочной железы. Они могут иметь гиперваскулярную структуру и содержать кальцинаты. При размерах более 3 см в этих опухолях всегда регистрируются гистологические признаки злокачественности, но при этом не всегда возникают метастазы в лимфатические узлы и печень [12]. Кроме того, их отличает, с одной стороны, медленный рост, а с другой - редко возникающая инвазия в соседние анатомические структуры даже при значительных размерах [4, 8, 16].
Тихоокеанский медицинский журнал, 2009, № 2
В процессе инструментального обследования нередко трудно отличить опухоли поджелудочной железы от неэпителиальных опухолей желудка, кист и опухолей левого надпочечника или неорганных забрю-шинных новообразований, и окончательный диагноз удается установить также только во время операции [4, 5]. Доброкачественные новообразования выявляют здесь чаще случайно, при профилактических осмотрах. По данным инструментального обследования для них характерны отчетливые границы или даже капсула, часто - полости распада в структуре образования.
Нейроэндокринные опухоли (карциноиды) относятся к редкой разновидности опухолей поджелудочной железы и происходят из клеток диффузной нейроэндокринной системы, включенных в процессе эмбриогенеза в различные органы и ткани (кишечник, бронхи, щитовидная железа и др.). Такие опухоли чаще бывают изолированными, но могут быть связаны и с наследственным заболеванием - множественной эндокринной неоплазией 1-го типа или, по существу, - множественным эндокринным аденоматозом, при котором могут поражаться гипофиз, щитовидные и паращитовидные железы, надпочечники, поджелудочная железа и другие органы [17, 20].
Эти опухоли имеют особые клинические проявления, отличающие их от аденокарцином. При них редко наблюдается развернутый синдром онкологического заболевания и мало изменяется общее состояние больных. Но в зависимости от уровня или структурной полноценности продуцируемых гормонов нейроэн-докринные опухоли могут иметь как бессимптомное течение, так и разнообразные системные проявления, соответствующие характеру гормонов [23].
Гормонально-неактивные опухоли даже больших размеров, при которых незначительный уровень или неполноценность продуцируемых ими гормонов не дает клинических проявлений, обнаруживают обычно случайно в процессе инструментального обследования. Даже при локализации их в головке поджелудочной железы нехарактерно развитие механической желтухи или непроходимости двенадцатиперстной кишки. Такие опухоли нередко выявляют и сами больные при пальпации живота. Часто большие размеры таких опухолей не исключают радикального их удаления вследствие отсутствия метастазов и прорастания в соседние органы. Нейроэндокринную природу таких новообразований устанавливают только при иммуногистохимическом исследовании после биопсии или удаления [12]. Типичными разновидностями гормонально-активных нейроэндокринных опухолей являются инсулинома, гастринома, ВИПо-ма, соматостатинома, глюкагонома и крайне редко - истинные карциноиды, продуцирующие серотонин. Независимо от выраженности клинических проявлений, при размерах более 2-3 см эти опухоли имеют абсолютный риск малигнизации [16, 21].
Инсулинома происходит из ((-клеток островков Лангерганса. Обычно имеет размер до 1-2 см, а при большем размере часто малигнизируется и дает гормонально-активные метастазы. Может локализоваться в любом отделе поджелудочной железы, но чаще в ее теле или хвосте. Функциональная активность не зависит от размеров, основные проявления связаны с гипогликемией, которая проявляется развитием резкой слабости, вплоть до потери сознания или беспричинного возбуждения, галлюцинациями, нарушениями зрения, дезориентацией, тремором конечностей, потливостью, после длительного голодания. Такое состояние часто возникает после пробуждения от сна, по утрам. При этом уровень глюкозы в крови может составлять 1-2 ммоль/л. Самостоятельное употребление углеводов или внутривенное введение глюкозы быстро нормализует состояние пациентов. Чтобы избежать развития такого состояния, больные нередко вынуждены постоянно потреблять огромное количество углеводов в чистом виде, что обычно приводит к ожирению [18].
Превалирование мозговой симптоматики из-за частых эпизодов гипогликемии обычно вынуждает к бесплодному психиатрическому обследованию. Это связано и с тем, что при малых размерах опухоли диагностика ее любыми инструментальными методами сложна. Здесь важна проба с голоданием и параллельным определением уровня глюкозы в крови. Наиболее информативно определение в крови содержания иммунореактивного инсулина и его предшественника С-пептида. Инсулиномы размером более 1 см чаще выявляются при ультразвуковом или компьютерно-томографическом исследовании [19].
Гастринома (ульцерогенная аденома) развивается из 01-клеток поджелудочной железы и локализуется чаще в проксимальных отделах железы, но может располагаться и в стенке двенадцатиперстной кишки, в печени, надпочечниках и других органах. Часто малигнизируется при размерах более 2-3 см. Опухоль продуцирует гастрин, стимулирующий секрецию соляной кислоты в желудке и создает синдром Золлин-гера-Эллисона [15].
Заболевание характеризуется частыми приступами коликообразных болей в животе, поносами и язвенным симптомокомплексом. Нередко первым проявлением болезни является тяжелое желудочно-кишечное кровотечение. Изъязвление двенадцатиперстной кишки может сочетаться с язвой желудка, которая не поддается консервативной терапии. Резекция желудка в таких случаях приводит к быстрым рецидивам язвенного процесса, развитию пептичес-ких язв анастомозов и к тяжелым повторным желудочным кровотечениям.
При диагностике обращают внимание на желудочную гиперсекрецию по объему и базальному уровню соляной кислоты. Исследование желудочной секреции с введением гистамина или глюконата кальция показывает повышение уровня стимулированной секреции над базальной более чем на 60%. Радиоим-мунологически после стимуляции может быть выявлено повышение уровня гастрина в крови. Наиболее
информативны ультразвуковое и компьютерно-томографическое исследование с контрастным усилением. Нередко гастриномы удается выявить только при интраоперационной ревизии поджелудочной железы и других органов брюшной полости [5].
Доброкачественные периампулярные опухоли сравнительно редки и могут иметь различный гистогенез - эпителиальный (аденомы и цистаденомы), мышечный (лейомиомы), соединительно-тканный (фибромы и липомы), неврогенный (невриномы и ганглионевриномы) и ангиогенный (гемангиомы, лимфангиомы). В поджелудочной железе среди доброкачественных опухолей чаще встречаются серозная и муцинозная цистаденома, а также внутрипротоковая папиллярно-муцинозная аденома, в зоне большого сосочка двенадцатиперстной кишки - папиллярная аденома, а в двенадцатиперстной кишке - аденома-тозный полип, липома, миома, невринома и пр. [12].
Доброкачественные новообразования периампу-лярной зоны имеют различный прогноз. Так, аденомы и муцинозные кисты поджелудочной железы обладают высоким потенциалом малигнизации.
Доброкачественные периампулярные опухоли редко дают проявления, связанные со сдавлением общего желчного протока с механической желтухой или окклюзией панкреатического протока с острым панкреатитом, а также с кровотечением или обтура-цией двенадцатиперстной кишки и появлением симптомов дуоденальной непроходимости.
Диагностика периампулярных опухолей и выбор методов обследования зависит от их характера и локализации, которые определяют ведущие клинические проявления, но в целом они те же, как и при раке поджелудочной железы [6].
Опухоли большого сосочка двенадцатиперстной кишки проявляются, главным образом, симптомами холестаза и реже - симптомами скрытого кровотечения. В диагностике здесь приоритетное значение принадлежит эндоскопическому исследованию, при котором возможно выполнить биопсию новообразования. Большие трудности возникают при дифференциации рака большого дуоденального сосочка и его аденом с высокой степенью дисплазии. В таких случаях следует выбирать метод лечения как при раке. При последнем для определения стадии и резекта-бельности опухоли используют весь комплекс лучевой диагностики [4, 5, 7].
Опухоли любой морфологической структуры пери-ампулярной локализации подлежат хирургическому лечению. Даже при малых их размерах недопустимо динамическое наблюдение, так как многие доброкачественные новообразования здесь с полным основанием могут рассматриваться как факультативный или облигатный предрак [5-7, 10, 12].
Больным с механической желтухой показана кратковременная (до стабилизации показателей системы гемостаза) билиарная декомпрессия. При планировании радикальной операции предпочтительная транспеченочная холангиостомия, а при планировании паллиативной - холецистостомия, первичный били-одигестивный анастомоз или стентирование. Химио-и лучевая терапия в лечении периампулярных опухолей в качестве самостоятельных методов практически неэффективны. После радикальных операций назначение химиотерапевтических препаратов (5-фтор-урацил, гемзар и др.), особенно в сочетании с лучевой терапией, снижает частоту рецидивов заболевания и несколько увеличивает продолжительность жизни.
Радикальным методом оперативного лечения рака большого дуоденального сосочка является панкре-атодуоденальная резекция. Промежуточное положение между радикальной и паллиативной операциями занимает чрездуоденальная папиллэктомия при ма-лигнизированных аденомах, раннем раке большого дуоденального сосочка без инвазии в стенку двенадцатиперстной кишки. Такое вмешательство допустимо только у лиц с высоким операционным риском, который не позволяет осуществить панкреатодуоде-нальную резекцию [14].
При доброкачественных периампулярных опухолях в большинстве случаев можно прибегнуть к щадящим органосберегающим операциям. Так, опухоли малых размеров большого сосочка двенадцатиперстной кишки, терминального отдела общего желчного протока или самой двенадцатиперстной кишки возможно удалить в процессе гастродуоденоскопии путем электроэксцизии или с использованием лазерного излучения. Если размеры доброкачественного новообразования велики, проводят традиционную дуоденотомию с иссечением опухоли.
Доброкачественные новообразования поджелудочной железы (главным образом аденомы
Тихоокеанский медицинский журнал, 2009, № 2
и цистаденомы) удаляют только путем традиционной операции. Чаще оказываются возможны энуклеация опухоли, краевая или дистальная резекция железы. Любой метод удаления должен обязательно сопровождаться срочной морфологической верификацией, так как при выявлении рака объем операции необходимо расширить.
Удаление доброкачественных периампулярных опухолей путем оперативного вмешательства или при гастродуоденоскопии благоприятно для прогноза жизни, здоровья и социальной реабилитации больных [1, 3, 7]. Прогноз жизни при злокачественных пе-риампулярных новообразованиях после однотипных оперативных вмешательств (панкреатодуоденальной резекции) даже с расширенной лимфаденэктомией существенно различается. Так, при протоковой аде-нокарциноме поджелудочной железы любой локализации 5-летняя выживаемость не превышает 20%, а медиана выживаемости колеблется между 12 и 20 месяцами. При опухолях другой локализации эти показатели достигают 30-50% и 36-60 месяцев соответственно. Продолжительность жизни больных с неудаленной опухолью редко превышает 6-12 месяцев. При большем сроке жизни нужно, как правило, морфологическое уточнение диагноза. Особо благоприятный прогноз жизни имеют больные нейро-эндокринными опухолями поджелудочной железы, среди которых 5-летняя выживаемость даже при наличии метастазов наблюдается в 50-70% случаев. Литература
1. Анзимиров В.Л., Баженова А.П., Бухарин В.А. и др. Клиническая хирургия: справочное руководство / под ред. Ю.М. Панцирева. М.: Медицина, 2000. 640 с.
2. Битти А.Д. Диагностические тесты в гастроэнтерологии. М., Медицина,1995. 220 с.
3. Губергриц Н.Б., Христич Т.Н. Клиническая панкреатоло-гия. Донецк, 2000. 416 с.
4. Егоров А.В., Кузин Н.М., Ветшев П.С. и др. Спорные и нерешенные вопросы диагностики и лечения гормонопро-дуцирующих нейроэндокринных опухолей поджелудочной железы // Хирургия. 2005. № 9. С. 19-24.
5. Избранные лекции по клинической онкологии / под ред. Чиссова В.И., Дарьяловой С.Л. М. : Медицина, 2000. 736 с.
6. Клемашев И.С. Практическая гастроэнтерология. М.: Медицина, 2002. 224 с.
7. Кубышкин В.А., Вишневский В.А. Рак поджелудочной железы. М.: Медпрактика, 2003. 386 с.
8. Кузин Н.М., Егоров А.В., Казанцева И.А. и др. Нейроэн-докринные опухоли поджелудочной железы: руководство для врачей. - М.: Медицина, 2001. 208 с.
9. Кузин Н.М., Егоров А.В., Кондрашин С.А. и др. Диагностика и лечение гастринпродуцирующих опухолей поджелудочной железы//Клин. мед. 2002. № 3. P. 71-76.
10. Лапкин К.В., Пауткин Ю.Ф. Билиопанкреатодуоденаль-ныйрак. М.: Изд-во Ун-та дружбы народов, 2001. 112 с.
11. Ошибки в клинической онкологии: руководство для врачей / под ред. В.И. Чиссова, А.Х. Трахтенберга. М.: Медицина, 2001. 544 с.
12. Патолого-анатомическая диагностика опухолей человека: руководство в 2 томах / под ред. Н.А. Краевского. М.: Медицина, 1993.
13. Тревис С.П.Л., Тейлор Р.Х., Мисевич Д.Д. Гастроэнтерология. М.: Медицинская литература, 2002. 628 с.
14. Шалимов А.А. Хирургическое лечение больных раком поджелудочной железы и панкреатодуоденальной зоны // Анн. хирургической гепатологии. 1996. Т. 1. С.62-68.
15. Alexander H.R., Fraker D.L., Norton J.A. et al. Prospective study of somatostatin receptor scintigraphy and its effect on operative outcome in patients with Zollinger-Ellison syndrome // Ann. Surg. 1998. Vol. 228, No. 2. P. 228-238.
16. Calender A., Vercherat C., Gaudray P., Chayvialle J.A. GEN-EM (Groupe d‘ Etude des Neoplasies Endocriniennes Multiples). Deregulation of genetic pathways in neuroendocrine tumors // Ann. Oncol. 2001. - Vol. 12, Suppl. 2. P. 3-11.
17. Eriksson B. Management of neuroendocrine foregut tumours //
Neuroendocrinology. 2004. Vol. 80. P. 396-404.
18. Fendrich V., Bartsch D.K., Langer P. et al. Diagnosis and surgical treatment of insulinoma-experiences in 40 cases // Dtsch. Med. Wochenschr. 2004. Vol. 129, No. 17. P. 941-946.
19. Grant C.S. Gastrointestinal endocrine tumours. Insulinoma. Bail-
lieres // Clin. Gastroenterol. 1996. Vol. 10, No. 4. P. 645-671.
20. Lairmore T.C., Piersall L.D., DeBenedetti M.K. et al. Clinical genetic testing and early surgical intervention in patients with multiple endocrine neoplasia type 1 (MEN 1) //Ann. Surg.
2004. Vol. 239, No. 5. P. 637-647.
21. Modlin I.M., Lye K.D., Kidd M. A 5-decade analysis of 13,715 carcinoid tumors// Cancer. 2003. Vol. 97. P. 934-959.
22. Norton J.A., Kivlen M., Li M. et al. Morbidity and mortality of aggressive resection in patients with advanced neuroendocrine tumors //Arch. Surg. 1999. Vol. 138, No. 8. P. 859-866.
23. Rosch T., Lightdale C.J., Botet J.F. et al. Localization of pancreatic endocrine tumors by endoscopic ultrasonography // New
Engl. J. Med. 1992. Vol. 326, No. 26. P. 1721-1726.
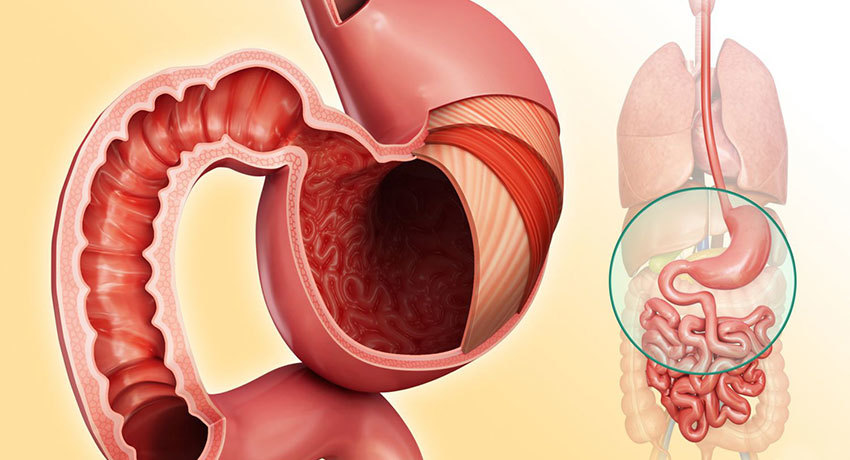
Двенадцатиперстная кишка — это короткий начальный отдел тонкой кишки, он начинается сразу же после желудка и переходит в тощую кишку. Она получила свое название за то, что ее длина составляет около 12 поперечников пальца человека. Злокачественные опухоли в этом отделе кишечника встречаются редко.
Несмотря на свою небольшую длину, двенадцатиперстная кишка выполняет важные функции. В неё открываются проток поджелудочной железы и желчный проток, здесь происходит расщепление и всасывание некоторых питательных веществ. При злокачественных опухолях эти процессы нарушаются.

В клинике Медицина 24/7 доступны наиболее современные методы диагностики, которые помогут точно диагностировать рак двенадцатиперстной кишки и своевременно начать лечение. Наши врачи выполняют сложные хирургические вмешательства в условиях операционной, оснащенной современным оборудованием, проводят противоопухолевую терапию в соответствии с последними версиями международных протоколов.
Какие методы лечения применяются при раке двенадцатиперстной кишки?
Тактика лечения рака двенадцатиперстной кишки может быть разной, и в первую очередь это зависит от того, на какой стадии была диагностирована злокачественная опухоль. Стадию определяют в зависимости от размеров опухоли, наличия очагов поражения в регионарных лимфатических узлах и отдаленных метастазов. В общем виде классификация выглядит следующим образом:
Если рак двенадцатиперстной кишки диагностирован достаточно рано, обычно выполняют хирургическое вмешательство, зачастую его дополняют курсом химиотерапии или лучевой терапией.
Радикальное, то есть направленное на удаление злокачественной опухоли, лечение рака двенадцатиперстной кишки может быть выполнено, если злокачественная опухоль находится только в пределах органа или незначительно распространилась на соседние структуры.
Чаще всего выполняют операцию Уиппла — гастропанкреатодуоденальную резекцию. Удаляют двенадцатиперстную кишку, часть желудка, поджелудочной железы, желчный пузырь и часть желчного протока, регионарные лимфатические узлы.
В некоторых случаях, на ранних стадиях, может быть выполнена менее радикальная операция — удаление части двенадцатиперстной кишки, пораженной опухолью. Это вмешательство можно провести лапароскопически — через проколы в брюшной стенке.
Если опухоль неоперабельна, но мешает прохождению пищи, показано паллиативное хирургическое вмешательство. Наиболее современная методика — стентирование. В заблокированном участке двенадцатиперстной кишки устанавливают стент — трубочку с сетчатой стенкой из металла или пластика. Стентирование выполняют эндоскопически, без разреза.
Аденокарцинома — наиболее распространенный гистологический тип злокачественных опухолей двенадцатиперстной кишки — не очень чувствительна к химиопрепаратам. Тем не менее, в некоторых случаях курсы химиотерапии могут быть полезны. Чаще всего их назначают при неоперабельных злокачественных опухолях на поздних стадиях.
В некоторых случаях проводят курсы адъювантной химиотерапии после хирургического вмешательства. Их цель — уничтожить раковые клетки, которые могли остаться в теле пациента, и снизить риск рецидива. На сегодняшний день нет точных данных о том, насколько эффективна адъювантная химиотерапия при раке тонкой кишки.
Обычно пациентам с раком двенадцатиперстной кишки назначают химиопрепараты , капецитабин, иринотекан, оксалиплатин. Так как эти опухоли встречаются очень редко, пока не удалось провести крупные исследования, которые бы показали, какие химиопрепараты помогают лучше всего. Наиболее распространенные комбинации химиотерапии при раке тонкой кишки:
- CAPOX: капецитабин и оксалиплатин;
- FOLFIRI: , иринотекан и лейковорин;
- FOLFOX: , оксалиплатин и лейковорин.
Отзывы наших пациентов
7 апреля 2020 г.
14 января 2020 г.
25 ноября 2019 г.
11 ноября 2019 г.
Лучевую терапию назначают в следующих случаях:
- При неоперабельных злокачественных опухолях на поздних стадиях.
- Для борьбы с симптомами и осложнениями рака: кишечной непроходимостью, кровотечением.
- После хирургического удаления рака, в качестве адъювантного лечения. Однако, как и в случае с химиотерапией, польза от применения лучевой терапии в данном случае не доказана.
Процедура напоминает рентгенографию, но во время нее используют более высокие дозы излучения, и пациента облучают немного дольше, обычно в течение нескольких минут.
Оставьте свой номер телефона
Итак, для того чтобы определиться с тактикой лечения, в первую очередь врач должен решить, является ли злокачественная опухоль в двенадцатиперстной кишке резектабельной, то есть можно ли её в принципе удалить хирургически. Для этого проводят обследование, которое включает эндоскопическое исследование (фиброгастродуоденоскопию), рентгенографию с контрастированием бариевой взвесью, компьютерную томографию, томографию, биопсию.
При резектабельном раке чаще всего выполняют операцию Уиппла. Если оказывается, что опухоль распространилась в регионарные лимфатические узлы, после операции проводят адъювантную химиотерапию или лучевую терапию.
Если опухоль блокирует просвет двенадцатиперстной кишки, выполняют паллиативную операцию для восстановления её проходимости.
У некоторых пациентов, при наличии определенных генетических маркеров, лечение рака двенадцатиперстной кишки предусматривает применение иммунопрепаратов из группы ингибиторов контрольных точек. Для того чтобы обнаружить соответствующие генетические изменения, выполняют анализ. Его можно провести в клинике Медицина 24/7.
Если злокачественная опухоль привела к канцероматозу брюшины, может быть выполнена гипертермическая интраперитонеальная химиотерапия — HIPEC. Выполняют хирургическое вмешательство, во время которого удаляют все крупные опухолевые узлы в брюшной полости, после чего брюшную полость промывают нагретым раствором химиопрепарата, чтобы уничтожить мелкие опухолевые очаги. Иногда HIPEC помогает продлить жизнь на годы, но эту методику можно применять только при локальном поражении брюшной полости без метастазов за ее пределами, у пациентов, состояние которых позволяет перенести серьезное хирургическое вмешательство, и если все крупные очаги в брюшной полости являются резектабельными.
Каковы прогнозы при раке двенадцатиперстной кишки?
В целом рак двенадцатиперстной кишки лечится довольно успешно. Пятилетняя выживаемость составляет:
- Если опухоль находится только в пределах стенки кишки — 85%.
- Если рак распространился на соседние органы или в регионарные лимфоузлы — 75%.
- Если выявлены отдаленные метастазы — 42%.
Прогноз сильно зависит от того, насколько быстро и правильно диагностировано заболевание, от своевременного лечения. В клинике Медицина 24/7 онкологические пациенты могут быстро получить все виды медицинской помощи. Наши опытные хирурги выполняют вмешательства любой сложности в операционной, оснащенной современным оборудованием, мы применяем препараты последних поколений. Свяжитесь с нами — мы обязательно постараемся помочь.
Источники:
- Ершов В. В., Рябков М. Г., Саратов М. Б. Двухэтапное лечение осложненного рака двенадцатиперстной кишки // Соврем. технол. мед.. 2012. №2.
- Коваленко В. Л., Леонов В. П., Свистун А. П., Еременко А. В. Наблюдение первичного рака двенадцатиперстной кишки, осложнённого анемией тяжелой степени // Вестн. хир.. 2011. №1.
- Дайчман Даворин, Генслицкая Екатерина. Периампулярный рак двенадцатиперстной кишки // Казанский мед.ж.. 2009. №3.
Папиллярный рак получил свое название из-за особого строения опухоли — она образует сосочковые структуры, в которых имеются соединительнотканные стержни, пронизанные кровеносными и лимфатическими сосудами мелкого калибра. При этом часто зоны папиллярных образований чередуются с зонами солидного или фолликулярного строения. В подавляющем большинстве случаев папиллярный рак поражает щитовидную железу. Реже папиллярные злокачественные новообразования возникают в почках, органах ЖКТ, молочной железе и яичниках.
- Причины возникновения папиллярного рака
- Классификация
- Локализация папиллярного рака
- Симптомы папиллярного рака
- Диагностика папиллярного рака
- Лечение папиллярного рака
- Прогноз при папиллярном раке щитовидной железы
- Профилактика папиллярного рака
- Осложнения папиллярного рака щитовидной железы
Причины возникновения папиллярного рака
Причины возникновения папиллярного рака сложны и многогранны. При этом для разных органов могут быть разные факторы риска. Например, к развитию папиллярного рака щитовидной железы приводят следующие факторы:
- Хроническое воздействие на орган тиреотропного гормона в высоких дозах. Такие состояния наблюдаются при хронических гипертиреозах и при тиреотоксикозе.
- Воздействие ионизирующего излучения, в том числе радиоактивных изотопов йода.
- Наличие доброкачественных новообразований щитовидной железы.
- Дефицит йода.
- Наследственные синдромы — синдром Карни, Каудена, МЭН и др.
Для новообразований других органов может быть своя специфика. Например, папиллярный рак желудка может возникать на фоне полипов, язвенной болезни, инфицирования хеликобактером и др. Рак яичников и молочной железы часто имеет гормональнозависимую природу, при этом новообразования чаще встречаются у нерожавших женщин. Практически для всех локализаций большую роль играют химические канцерогены, курение, неблагоприятная экологическая обстановка, несбалансированное и избыточное питание.
Классификация
Папиллярный рак классифицируют в зависимости от его гистологического варианта, места первичной локализации и стадии заболевания. Ключевое значение имеет первично пораженный орган, поскольку именно от этого будет зависеть гистологический вариант новообразования и прогноз его течения. Что касается стадии заболевания, то здесь учитывается размер опухоли, инвазия в соседние ткани, наличие метастазов в лимфоузлы и отдаленные органы. В целом для каждого органа определены параметры установления стадии рака по системе ТNM (опухоль, лимфогенные и гематогенные метастазы).
Локализация папиллярного рака
Чаще всего папиллярный рак локализуется в щитовидной железе. В других органах он встречается значительно реже. В целом папиллярные новообразования могут развиваться в следующих органах:
- Молочная железа.
- Почки.
- Яичники.
- Кожа.
- Желудок.
- Поджелудочная железа.
Поскольку в подавляющем большинстве случаев локализацией папиллярного рака является именно щитовидная железа, в данной статье рассмотрим данную нозологию.
Симптомы папиллярного рака
На ранних этапах папиллярный рак щитовидной железы не вызывает никаких симптомов. В более позднем периоде могут возникать некоторые признаки, но они неспецифичны и часто присутствуют при других заболеваниях эндокринной системы:
- Наличие узловых образований в органе. Узлы в щитовидной железе еще не являются критерием постановки диагноза, поскольку часто они являются доброкачественными. А вот что должно насторожить, так это возникновение узлов у молодых людей в возрасте до 20 лет, поскольку в этой возрастной группе доброкачественные узловые гиперплазии встречаются редко.
- Лимфаденопатия шейных лимфоузлов (увеличение лимфоузлов). Это также неспецифический признак, поскольку может быть симптомом инфекций верхних дыхательных путей или лимфом.
- Симптомы гипертиреоза: нестабильность настроения, снижение веса, учащенное сердцебиение, повышение аппетита, потливость, слабость и др.
- На распространенных стадиях, когда опухоль выходит за пределы органа, может меняться конфигурация шеи, ее объемы и контуры. Некоторые больные могут отмечать необычные ощущения, например, першение, комок в горле, изменение голоса, затруднение глотания, боль в горле и др.
Все эти симптомы могут быть и при других заболеваниях, поэтому для подтверждения диагноза требуется специальное обследование.
Диагностика папиллярного рака
Для диагностики папиллярного рака применяется ряд специальных тестов:
- Ультразвуковое исследование щитовидной железы. При папиллярном раке будут обнаруживаться узловые новообразования. Заподозрить их злокачественную природу можно по нечеткому контуру и размытым краям.
- Биопсия обнаруженных новообразований. Как правило, для диагностики папиллярного рака используется тонкоигольная аспирационная биопсия, с помощью которой пунктируют узловые новообразования и аспирируют их содержимое. Полученный материал направляется в лабораторию для цитологического исследования. Увеличенные лимфатические узлы также пунктируют. Чтобы результат был максимально достоверным, материал берут из нескольких точек. Если лаборатория выдает неопределенный результат, исследование следует повторить.
- Радиоизотопное сканирование. Это исследование позволяет максимально точно определить объем опухолевой ткани и обнаружить метастазы при их наличии.
- Лабораторные анализы. Всем пациентам, при подозрении на папиллярный рак, назначают анализ на тиреоидные гормоны, а также на тиреоглобулин. При успешном лечении его уровень снижается, а при развитии рецидива или прогрессировании заболевания опять начинает нарастать.
Лечение папиллярного рака
Ключевым моментом в лечении папиллярного рака щитовидной железы является хирургическая операция. Как правило, проводится тотальное удаление органа вместе с капсулой. Также выполняется шейная диссекция, которая подразумевает удаление жировой клетчатки лимфатических узлов. Если рак распространился на окружающие ткани и органы, по возможности проводится их резекция.
Следующим этапом лечения папиллярного рака является радиойодтерапия. Ее суть заключается в следующем — пациент принимает радиоактивный йод, который избирательно аккумулируется в клетках щитовидной железы, в том числе и злокачественных. Это приводит к их локальному облучению и гибели. Перед тем как начинать такую терапию, искусственно создают дефицит йода в организме. Для этого отменяют прием заместительной гормональной тиреоидной терапии на несколько недель и исключают из рациона продукты, богатые йодом (йодированная соль, морепродукты и др).

Кроме того, крайне не рекомендуется в это время проходить компьютерную томографию с контрастированием, поскольку в контрасте содержится йод. На момент начала радиотерапии уровень ТТГ должен превышать 30 мЕд/л. Лечение проводится курсами до полного исчезновения очагов накопления йода и снижения ТГ до 2 нг/л и менее.
И, наконец, заключительным этапом лечения является гормональная терапия. Поскольку при операции полностью удаляется щитовидная железа, продуцировать тиреоидные гормоны просто нечему, и у человека развивается тяжелый гипотиреоз. Чтобы его компенсировать, назначается искусственный гормон, аналогичный тироксину — L-тироксин. Однако его назначают в дозировках, значительно превышающих заместительные уровни гормона. Это необходимо для подавления гормона гипофиза, который стимулирует ткань щитовидной железы, и в том числе злокачественные клетки. Уровень L-тироксина подбирается таким образом, чтобы ТТГ было в пределах 0,05-01 мЕд/л.
Прогноз при папиллярном раке щитовидной железы
Прогноз при папиллярном раке щитовидной железы благоприятный, поскольку эта опухоль является высокодифференцированной. Более чем у 95% пациентов удается добиться полного выздоровления. Однако они вынуждены будут пожизненно принимать искусственный тироксин.
Профилактика папиллярного рака
Профилактика папиллярного рака заключается в следующих мероприятиях:
- Восполнение дефицита йода для людей, проживающих в эндемичный районах. Для этого подходит йодированная соль, увеличение в рационе количества морепродуктов, применение специальных препаратов.
- Своевременное лечение заболеваний щитовидной железы.
- Динамический контроль пациентов из группы риска — лица, проживающие в эндемичной по йод-дефициту районах, лица с обнаруженными узлами в щитовидной железе, пациенты, подвергавшиеся облучению.
Осложнения папиллярного рака щитовидной железы
Осложнения при раке щитовидной железы могут быть связаны с действием опухоли и с лечением заболевания. При прорастании новообразования за пределы органа может происходить поражение органов шеи и головы. При этом отмечается выраженная боль и неврологическая симптоматика. При прорастании в крупные кровеносные сосуды может возникнуть тяжелое кровотечение. Если объем опухоли большой, она может сдавливать пищевод и даже трахею, приводя к нарушению дыхания и прохождению пищевого комка.
Что касается лечения, то как мы уже говорили, удаление щитовидной железы приводит к тяжелому гипотиреозу, который при отсутствии лечения может привести к инвалидизации больного и даже его гибели. Поэтому очень важно принимать L-тироксин.
Читайте также:





