Папиллярный рак лоханки и мочеточника
Опухоли верхних мочевых путей (ВМП) начали изучать с середины XIX в.
Первое описание первичного рака мочеточника принадлежит французскому патологоанатому P. Rayer (1841).
Однако только в 1902 г. J. Albarran впервые диагностировал опухоль мочеточника до операции.
Улучшение диагностики опухолей ВМП сопровождалось разработкой тактики лечения. С начала XX в. при злокачественных опухолях верхних мочевых путей стали производить нефроуретерэктомию, однако результаты операций не были успешными. И только в 1914 г. описан первый случай выживания после нефроуретерэктомии по поводу рака мочеточника.
Эпидемиология
Первичные опухоли ВМП встречаются довольно редко и составляют 5-7% всех случаев опухолей почки и 5% всех уротелиальных раков. Большинство (до 80%) новообразований верхних мочевых путей обнаруживают у больных в возрасте 60-79 лет. Пик заболеваемости приходится на возраст 65 лет. Частота возникновения первичной опухоли почечной лоханки составляет 1,4 на 100 тыс. мужчин и 0,6 на 100 тыс. женщин в год.
Первичные опухоли мочеточника встречаются реже и составляют примерно 1% всех опухолей почек и ВМП. Опухоли чашечно-лоханочной системы почки с одинаковой частотой исходят из верхней и нижней чашечек и почечной лоханки. Реже опухоли развиваются в средней чашечке или поражается вся чашечно-лоханочная система. Согласно другим исследованиям опухоли чашечно-лоханочного комплекса чаще возникают в верхней чашечке.
Опухоли мочеточника преимущественно развиваются в его дистальном отделе. Такая локализация наблюдается в 68% случаев, в 20,3% поражается средняя треть мочеточника, в 9,4% — верхняя треть и в 2,3% — весь мочеточник. С одинаковой частотой опухоль обнаруживают справа и слева, в 2-4 случаях — двустороннее поражение. Значительное количество (60%) впервые выявленных новообразований ВМП локализуется в лоханке почки, 40% образований выявляется в мочеточнике.
Наличие уротелиального рака верхних мочевых путей значительно увеличивает риск развития рака мочевого пузыря. Установлено, что переходно-клеточный рак мочевого пузыря развивается у 30-50% больных раком мочеточника. Значительно выше (до 75%) частота последующего выявления рака мочевого пузыря при мультифокальном поражении ВМП.
Риск развития рака мочевого пузыря значительно возрастает в группах пациентов с распространенными формами рака ВМП, также большое значение в развитии рака мочевого пузыря имеет степень опухолевой дифференцировки опухоли. В 70% случаев опухоли мочевого пузыря развиваются в первые два года после возникновения рака верхних мочевых путей.
Этиология и патогенез
Уротелий весьма чувствителен к различным химическим канцерогенам, находящимся в моче. Для возникновения опухоли помимо канцерогенов также необходимы так называемые ко-канцерогены. или инициаторы онкогенеза. Последние вызывают гиперплазию уротелия, что увеличивает его чувствительность к химическим канцерогенам. Важную роль в развитии переходно-клеточного рака отводят длительности контакта канцерогенов и клеток уротелия.
Роль застоя мочи в возникновении ВМП подтверждается чрезвычайно высокой (до 30%) частотой развития опухолей в дивертикулах мочеточников. Значительное число химических веществ — канцерогены для уротелия: бензидин, нафтиламин, аминобифенил, нитробифенил, диаминобифенил и др. Установлена связь между количеством потребляемого с водой мышьяка и заболеваемостью переходно-клеточным раком ВМП.
Наличие химических канцерогенов объясняет также большую частоту переходно-клеточного рака верхних мочевых путей у городских жителей по сравнению с сельскими. Многие исследователи считают важным фактором развития опухолей верхних мочевых путей курение: около 77% наблюдавшихся ими больных с новообразованиями ВМП курили. Риск возникновения опухолей ВМП находится в прямой зависимости от числа выкуренных за день сигарет и продолжительности курения.
Считается, что у курящих в моче повышается концентрация промежуточных продуктов метаболизма триптофана, имеющих подобную ортоаминофенолу структуру и являющихся сильными канцерогенами. Большое значение в развитии рака верхних мочевых путей играет также потребление большого количества кофе. По данным различных авторов, потребление более семи чашек кофе в день значительно повышает риск .развития опухоли.
Установлено, что длительное нахождение конкрементов в почечной лоханке вызывает гиперплазию уротелия и приводит к увеличению риска развития плоскоклеточного рака почечной лоханки. С этим связано до 60% случаев плоскоклеточного рака лоханки и мочеточника. Более чем в 2 раза возрастает риск развития опухоли при наличии инфекции верхних мочевых путей. Частота рака лоханки и мочеточника повышается при некоторых заболеваниях.
В частности, балканская эндемическая нефропатия повышает риск развития новообразований мочеточника и почечной лоханки в 100 раз. У больных с артериальной гипертензией частота развития опухолей верхних мочевых путей увеличена. При этом риск возникновения новообразований повышается в 2 раза при лечении таких больных диуретиками. Указывают также на незначительное возрастание риска развития переходно-клеточного рака при наличии наследственных факторов по этому заболеванию.
Классификация
Различают первичные и вторичные опухоли почечной лоханки и мочеточника. Первичными образованиями являются исходящие непосредственно из верхних мочевых путей, в то время как вторичные опухоли представляют собой метастазы злокачественных новообразований других органов.
Вторичные поражения встречаются чрезвычайно редко, причем преимущественно в мочеточнике. Опухоли почечной лоханки и мочеточника можно разделить на доброкачественные и злокачественные. Первые наблюдаются крайне редко. Из-за чрезвычайно высокого потенциала малигнизации доброкачественных эпителиальных опухолей отношение к ним должно быть как к высокодифференцированному неинвазивному раку.
При злокачественных опухолях часто обнаруживают несколько очагов малигнизации уротелия, поэтому клинически и прогностически важно выделить единичные и множественные (мультифокальные) новообразования. Последние определяют примерно в 20% случаев первичного рака ВМП.
Развитие опухоли почечной лоханки и мочеточника происходит как из эпителиальной, так и мезенхимальной ткани. Частота последних крайне низка и составляет менее 1% всех случаев впервые выявленных опухолей почечной лоханки и мочеточника. К неэпителиальным доброкачественным опухолям относятся фиброма, нейрофиброма, ангиофиброма, липома, рабдомиома. Описаны единичные случаи злокачественных лейомиосаркомы и фибросаркомы.
По гистологическому строению среди злокачественных эпителиальных новообразований выделяют переходно-клеточный рак, плоскоклеточный рак и аденокарциному. Большинство новообразований почечной лоханки и мочеточника представлено переходно-клеточным раком. Его частоту оценивают в 92-99% всех опухолей почечной лоханки и мочеточника. Частота плоскоклеточного рака составляет 1-8%. Опухоли такого гистологического строения чаще обнаруживают в почечной лоханке. Аденокарциномы встречаются исключительно редко.
Первичная опухоль (Т)
Тх — первичная опухоль не выявлена
T0 — нет доказательств наличия первичной опухоли
Та — неинвазивный рак
Тis — carcinoma in situ
T1 — инвазия в подслизистый слой
Т2 — инвазия в мышечный слой
Т3 — для почечной лоханки: опухоль прорастает в перипельвикальную клетчатку или паренхиму почки
Т3 — для мочеточника: опухоль прорастает в периуретеральную клетчатку
Т4 — опухоль прорастает в соседние органы или через почку в околопочечную клетчатку
Регионарные лимфатические узлы (N)
Nx — регионарные лимфатические узлы не оценивались
N0 — отсутствие метастазов в регионарные лимфатические узлы
N1 — метастазы в один лимфатический узел до 2 см
N2 — метастазы в один или несколько лимфатических узлов до 2 см, но не более 5 см
N3 — метастазы в лимфатические узлы более 5 см
Отдаленные метастазы (М)
Мх — отдаленные метастазы не оценивались
М0 — отсутствие отдаленных метастазов
М1 — наличие отдаленных метастазов
По данным некоторых авторов, дифференцировка клеток при переходноклеточном раке лоханки мочеточника высокая (G1) в 4,8% случаев, умеренная (G2) — в 68% случаев, низкая или отсутствует (G3 и G4) — в 26,8% (табл. 6.1).
Таблица 6.1. Степень дифференцировки опухолевых клеток

Все опухоли верхних мочевых путей разделяют на локализованные, региональные и метастатические. К локализованным относятся новообразования, не выходящие за пределы почечной лоханки, почки или мочеточника, при отсутствии поражения лимфатических узлов и отдаленных метастазов.
При региональной форме заболевания опухоль распространяется за пределы почечной лоханки или паренхимы почки и прорастает в перипельвикальную, периренальную или периуретеральную клетчатку, лимфатические узлы, лимфатические сосуды и соседние органы.
Симптоматика
Наиболее частым симптомом опухолей почечной лоханки и мочеточника является микро- либо макрогематурия. Она присутствует у 70-95% больных. Макрогематурия у 65-70% больных является первым симптомом наличия опухоли ВМП. Промежуток времени с момента появления гематурии до установления диагноза опухоли составляет в среднем 1 год.
Другим частым симптомом являются боли в поясничной области. Последние возникают у 20-50% больных и связаны с обструкцией мочеточника или лоханочно-мочеточникового сегмента опухолью. Значительно реже опухоли верхних мочевых путей проявляются дизурией (5-10%) и общими симптомами (5-15%), такими как похудание, снижение аппетита и субфебрилитет. В запущенных случаях и значительной распространенности опухоли (10-20%) образование определяется пальпаторно. В 13% случаев опухолей верхних мочевых путей клинические симптомы болезни отсутствуют.
Диагностика
Цитологическое исследование мочи позволяет выявить атипичные опухолевые клетки. Однако при данном исследовании высока частота отрицательных результатов — до 65%. Наибольшую информативность цитология имеет в выявлении низкодифференцированных опухолей и рака in situ, тогда как при высокодифференцироваиных поверхностных опухолях вероятность ошибки довольно высока и составляет 96%.
Экскреторная урография является важным и обычно первичным методом обследования пациентов с подозрением на опухоль ВМП. Особенно высока ценность экскреторной урографин при опухолях почечной лоханки. Наиболее частым рентгенологическим признаком является дефект наполнения, выявляемый в 50-75% случаев. Реже наблюдается гидронефротическая трансформация, обусловленная обструкцией мочеточниково-лоханочного сегмента, либо отсутствие функции почки (нефрограмма). При новообразованиях мочеточника экскреторная урография менее информативна.
Важным методом исследования служит ретроградная уретеропиелография. Характерными признаками опухоли мочеточника является дефект наполнения мочеточника с характерным контуром его нижнего края в виде бокала и локальное расширение мочеточника дистальнее дефекта наполнения. Во время подготовки к ретроградной уретеропиелографии при катетеризации мочеточника можно выявить два достаточно специфичных для опухоли мочеточника симптома.
Первый из них заключается в выделении мочи с примесью крови до и во время прохождения препятствия в мочеточнике и прекращение гематурии после его преодоления (симптом Шевассю). Другим признаком опухоли мочеточника является изгиб мочеточникового катетера в расширенном пространстве дистальнее опухоли мочеточника (симптом Бергмана).
Цитоскопия позволяет выявить пролабирующую из устья мочеточника опухоль, состояние слизистой оболочки вокруг устья, обнаружить выделение крови из устья мочеточника. При цистоскопии также выявляют наличие опухолевых отсевов на слизистой мочевого пузыря, имеющее важное прогностическое значение и значительно изменяющее тактику и объем хирургического лечения.
Уретеропиелоскопия является одним из наиболее ценных методов исследования при опухолях верхних мочевых путей, особенно при наличии гибких манипуляторов. Помимо визуальной оценки стенок мочеточника и почечной лоханки во время уретеропиелоскопии возможно выполнить биопсию подозрительных участков для проведения гистологического исследования материала. Диагностическая уретеропиелоскопия не повышает риска диссеминации опухолевых клеток и не оказывает влияния на отдаленные исходы и выживаемость пациентов с уротелиальный раком.
Компьютерная томография позволяет выявить инвазию опухоли в почечную паренхиму, распространение за пределы почки в соседние ткани и органы, поражение лимфатических узлов и наличие отдаленных метастазов.
Ультразвуковое исследование позволяет выявить инфильтрацию переходно-клеточного рака в почечную паренхиму. Ультразвуковое исследование (УЗИ) играет важную роль в дифференциальной диагностике новообразований почечной лоханки и рентгенонегативных камней почки.
При диагностическом поиске по поводу опухолей верхних мочевых путей необходимо проведение дифференциальной диагностики с мочекаменной болезнью, туберкулезом мочевой системы, тампонадой лоханки почки или мочевого пузыря, повреждением мочеточника и лоханки почки, пиелитом, парауретеритом.
Лечение
Основным методом лечения опухолей почечной лоханки и мочеточника является хирургический. Выбор тактики лечения новообразований верхних мочевых путей зависит от стадии заболевания, степени дифференцировки опухолевых клеток, локализации, множественности поражения, состояния контралатеральной почки, а также наличия противопоказаний к хирургическому лечению. Стандартными методами лечения больных локализованным переходно-клеточным раком почечной лоханки и мочеточника являются нефроуретерэктомия с резекцией мочевого пузыря и в некоторых случаях сегментарная резекция мочеточника.
Нефроуретерэктомия с резекцией мочевого пузыря показана при локализованных злокачественных опухолях почечной лоханки и мочеточника (кроме дистального отдела) при сохраненной функции контралатеральной почки. Выбор этой операции основан на высоком риске распространения опухоли по мочеточнику дистальнее первичного очага. Некоторые исследователи рекомендуют выполнять нефроуретерэктомию после предварительной эндоскопической резекции стенки мочевого пузыря в окружности устья мочеточника.
Другим направлением является выполнение лапароскопической нефроуретерэктомии с предварительной резекцией мочевого пузыря из трансуретрального доступа. Некоторые авторы считают лапароскопическую нефроуретерэктомию методом выбора при минимально инвазивном раке. Лапароскопическая нефроуретерэктомия рекомендована пациентам с отягощенным соматическим статусом, так как, по мнению ряда авторов, переносимость лапароскопической операции значительно выше, чем открытой.
Сегментарная резекция мочеточника выполняется при высоко- (G1) и умеренно дифференцированных (G2) поверхностных (неинвазивных) опухолях дистальной трети мочеточника при отсутствии проксимального поражения. Такая операция возможна из-за исключительной редкости распространения опухолевых клеток проксимальное первичного очага.
После сегментарной резекции дистального мочеточника по поводу поверхностного высоко- или умеренно дифференцированного переходно-клеточного рака 3- и 10-летняя выживаемость не отличалась от таковой после нефроуретерэктомии. При низкодифференцированных и инвазивных опухолях дистальной трети мочеточника методом выбора является нефроуретерэктомия с резекцией мочевого пузыря.
В настоящее время изучают возможности эндоскопических методов лечения опухолей почечной лоханки и мочеточника. Однако отсутствие данных об отдаленных результатах и выживаемости после этих операций делает преждевременным рассмотрение их в качестве стандартов лечения опухолей данной локализации. Эндоскопические методы лечения включают уретеропиелоскопическую и перкутанную электрорезекцию, электрокоагуляцию и лазерную коагуляцию опухоли.
Применение данных методов лечения оправданно только в случаях поверхностного высокодифференцированного локального переходно-клеточного рака. Эндоскопические методы лечения в основном применяются у пациентов при хронической почечной недостаточности, единственной почке, двустороннем поражении и тяжелых сопутствующих заболеваниях, когда невозможно выполнить более радикальное оперативное вмешательство.
При распространенности на лимфатические узлы эффективность лечения остается низкой. Злокачественные новообразования верхних мочевых путей отличаются высоким уровнем метастазирования. Весьма высока частота рецидивирования рака, составляющая 12-18%. Прогноз для больных с и/или рецидивными опухолями почечной лоханки и мочеточника, как правило, неблагоприятный.
Лечение при метастатическом раке лоханки и мочеточника
Химиотерапия при распространенном раке лоханки и мочеточника полностью копирует химиотерапию распространенного рака мочевого пузыря. Первая линия может включать различные схемы, однако цисплатинсодержащие комбинации химиопрепаратов являются стандартом лечения.
Доказана лучшая эффективность цисплатина по сравнению с карбоплатином. Это означает, что всем пациентам, которые могут перенести введение цисплатина, учитывая тяжесть их состояния и сопутствующие заболевания, должны назначаться схемы с его включением.
Метотрексат — 30 мг/м2 в/в в 1-й день.
Винбластин — 3 мг/м2 в/в во 2-й день.
Доксорубицин (Адриамицин) — 30 мг/м2 в/в во 2-й день.
Цисплатин — 70 мг/м2 в/в капельно во 2-й день. Циклы повторяются каждые 4 нед.
Дозы метотрексата и винбластииа повторяют на 15-й и 22-й день при нормальных показателях крови.
Цисплатин — 50-60 мг/м2 в/в капельно в 1-й день.
Гемцитабин (Темзар) — 800-1000 мг/м2 в/в капельно в 1-й и 8-й день.
Повторные курсы на 28-й день.
Гемцитабин (Гемзар) — 1000 мг/м2 в/в в 1-й день.
Оксалиплатин — 100 мг/м2, 2-часовая в/в иифузия во 2-й день.
Повторные курсы каждые 2 нед.
Паклитаксел — 175 мг/м2, 3-часовая в/в инфузия в 1-й день.
Цисплатин — 75 мг/м2 в/в капельно в 1-й день. Повторные курсы каждые 3 нед.
Доцетаксел — 75 мг/м2, 1-часовая в/в инфузия в 1-й день.
Цисплатин — 75 мг/м2 в/в капельно в 1-й день. Повторные курсы каждые 3 нед.
Метотрексат — 30 мг/м2 в/в в 1-й день.
Винбластин — 3 мг/м2 в/в во 2-й день.
Эпирубицин (Фарморубицин) — 50 мг/м2 в/в во 2-й день.
Цисплатин — 70 мг/м2 в/в капельно во 2-й день.
Циклы повторяются каждые 4 нед.
Дозы метотрексата и винбластина повторяют на 15-й и 22-й день при нормальных показателях крови.
Цисплатин — 100 мг/м2 в/в капельно во 2-й день.
Метотрексат — 30 мг/м2 в/в в 1-й и 8-й день.
Винбластин — 4 мг/м2 в/в в 1-й и 8-й день. Повторные курсы через 3 нед.
Циклофосфамид — 400 мг/м2 в/в в 1-й день.
Доксорубицин (Адриамицин) — 40 мг/м2 в/в в 1-й день.
Проведение дистанционной лучевой терапии целесообразно выполнять с симптоматической целью, при одиночных костных метастазах с болевым синдромом или при возможном патологическом переломе. При множественных болевых костных метастазах возможно проведение системной лучевой терапии (метастрон, строиций-89-хлорид).
В.И. Чиссов, Б.Я. Алексеев, И.Г. Русаков
Симптомы папиллярного рака почки
Формы
Паппилярный рак лоханки почки и мочеточника может быть:
- единичным (при наличии одного опухолевого узла);
- множественным(при одновременном наличии нескольких очагов опухолевого роста).
Классификация рака почки.
По свойствам опухолевого узла.
Лимфатические узлы (органы иммунной защиты организма, имеют вид плотных узелков):
- N3 – метастазы в лимфатических узлах, более 5 см в диаметре.
- N2– метастазы в одном или более, чем одном регионарном лимфатическом узле, от 2 до 5 см в размере;
- N1– метастазы (вторичные очаги роста опухоли) в одном регионарном лимфатическом узле, менее 2 см в размере;
- N0– регионарные (близлежащие) лимфатические узлы без признаков опухолевого роста.
Отдаленные метастазы (в легкие, в головной мозг, в печень, в кости, в надпочечники):
- M0– отдаленных метастазов нет;
- М1 – отдаленные метастазы есть.
Причины
Причины развития паппилярного рака почки и мочеточника неизвестны.
Факторами риска возникновения рака почки являются:
- табакокурение;
- артериальная гипертензия (стойкое повышение артериального давления выше 140/90 мм рт. ст.);
- прием диуретиков (мочегонных препаратов);
- терминальная (финальная) стадия хронической почечной недостаточности (нарушение работы почек со значительным снижением их функций);
- контакт с канцерогенами (веществами, способствующими развитию рака);
- длительное нахождение камня в лоханке (полость внутри почки, продолжающаяся в мочеточник, собирающая и выводящая мочу) и мочеточнике при мочекаменной болезни;
- хронические воспалительные заболевания почки и мочеточника.
LookMedBook напоминает: чем раньше Вы обратитесь за помощью к специалисту, тем больше шансов сохранить здоровье и снизить риск развития осложнений:
Диагностика
- Анализ жалоб (когда (как давно) появились выделение крови с мочой, боли в поясничной области, с чем больной связывает возникновение этих симптомов).
- Анализ анамнеза жизни (перенесенные болезни в детско-юношеском периоде, контакт с токсическими химическими веществами, вредные привычки, наличие артериальной гипертензии (стойкое повышение артериального давления выше 140/90 мм рт. ст.)).
- Общий анализ мочи – исследование мочи на наличие эритроцитов (красных кровяных телец), лейкоцитов (белых клеток крови), белка, глюкозы (сахара крови), бактерий, солей и т.д. Позволяет выявить воспалительный процесс в почках и обнаружить выделение крови с мочой, незаметное для глаза.
- Цитологическое исследование мочи (исследование под микроскопом клеточного осадка мочи) позволяет визуализировать злокачественные клетки.
- Ультразвуковое исследование (УЗИ) почек – определение размеров, формы почек, структуры лоханки почки (полость внутри почки, продолжающаяся в мочеточник, собирающая и выводящая мочу), наличие камней и опухолевых образований.
- Компьютерная томография (КТ) области живота – выявление новообразования лоханки почки, определение его размеров, отношения к окружающим тканям, наличия метастазов (вторичного роста опухоли) в регионарных (близлежащих) лимфатических узлах и наличия отдаленных метастазов (надпочечники, печень).
- Компьютерная томография (КТ) грудной полости – определяется ли наличие отдаленных метастазов в легких.
- Экскреторная урография (введение контрастного вещества в вену, выполнение снимков органов мочевыделительной системы в разные моменты выделения контрастного вещества, как правило, через 7, 15 и 30 минут с момента введения препарата). Метод позволяет определить степень нарушения оттока мочи из почки, визуализировать образования в мочеточнике и почечной лоханки, а также определить степень расширения выделительной системы почки и мочеточника.
- Ретроградная уретропиелография (введение контрастного вещества в мочеточник через мочеточниковый катетер (трубку, введенную в мочеточник через мочеиспускательный канал и мочевой пузырь) и выполнение серии рентгеновских снимков) позволяет обнаружить образование мочеточника и почечной лоханки, оценить его размер и расположение.
- Цистоскопия (осмотр полости мочевого пузыря с помощью оптического прибора, введенного через мочеиспускательный канал) для обнаружения опухоли, выступающей из устья мочеточника в мочевой пузырь.
- Уретеропиелоскопия (исследование мочеточника и почечной лоханки с помощью оптического прибора, введенного через мочеиспускательный канал и мочевой пузырь в мочеточник) для осмотра опухоли почечной лоханки и мочеточника, определения ее размеров и расположения. Предоставляет возможность выполнения биопсии (забор кусочка опухолевой ткани и исследование ее под микроскопом).
- Возможна также консультация нефролога, онколога.
Лечение папиллярного рака почки
Лечение паппилярного рака почки исключительно хирургическое.
- Лапароскопическая (выполняемая с помощью специальной оптики и инструментов через проколы брюшной стенки) резекция (операция по удалению части органа) мочеточника – может быть применима в случае, если опухоль имеет небольшой размер и высокую степень дифференцировки (то есть клетки опухоли не сильно отличаются от нормальных).
- Лапароскопическая нефроуретерэктомия (удаление почки и мочеточника) с резекцией мочевого пузыря (удаление части мочевого пузыря, куда впадает мочеточник) – золотой стандарт для операций по поводу рака мочеточника и лоханки почки.
- Открытая радикальная нефроуретерэктомия с резекцией мочевого пузыря (полостная операция).
- Удаление отдаленных метастазов (при их единичном количестве).
Паппилярный рак лоханки почки (полость внутри почки, продолжающаяся в мочеточник, собирающая и выводящая мочу) и мочеточника относительно чувствителен к терапии химиопрепаратами (токсические вещества, убивающие быстро делящиеся клетки, в том числе и клетки опухоли).
Иммунотерапия (введение препаратов, действующих на иммунную систему организма, активирующих борьбу организма с опухолью) может применяться при лечении больных с метастатическим (имеющим отдаленные метастазы (вторичные очаги роста опухоли)) раком почки.
Осложнения и последствия
- Кровотечение с развитием анемии (малокровия).
- Летальный исход (смерть).
- Истощение, быстрое снижение массы тела.
- Гидроуретеронефроз — расширение собирательных структур (та часть почки, куда оттекает готовая моча (чашечно-лоханочная система почки) и мочеточника).
- Отдаленные метастазы (вторичные очаги роста опухоли в печени, надпочечниках, костях, легких, головном мозге).
- Амилоидоз – нарушение белкового обмена, сопровождающееся отложением в тканях амилоида (белка с неправильным строением).
Профилактика папиллярного рака почки
- Своевременное лечения хронических заболеваний (артериальной гипертензии (стойкого повышения артериального давления выше 140/90 мм рт. ст.) и мочекаменной болезни (образования камней в почках)).
- Отказ от табакокурения, употребления алкоголя, наркотиков.
- Исключение контакта с вредными химическими веществами.
- Правильное питание (уменьшение количества жирной и белковой пищи, употребление овощей, круп, фруктов, ограничение употребления соли (2-3 грамма в день)).
- Прием витаминных комплексов.
- Исключение психоэмоциональных нагрузок.
Дополнительно
Опухоль одинаково часто поражает правую и левую лоханки почки.
У мужчин рак лоханки и мочеточника возникает намного чаще, чем у женщин.
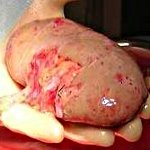
Папиллярная аденокарцинома почки – это гистологическая разновидность рака, поражающего чашечно-лоханочную систему почки. Проявляется гематурией, болью в пояснице, характер и интенсивность которой может достигать степени почечной колики; слабостью, похуданием. Диагностика требует проведения УЗИ почек, урографии, почечной ангиографии, КТ, радиоизотопной сцинтиграфии, МРТ. Радикальным оперативным объемом при папиллярной аденокарциноме почки является нефруретерэктомия; при диссеминации опухоли проводится химиотерапия.
- Причины
- Классификакция
- Симптомы аденокарциномы
- Диагностика
- Лечение папиллярной аденокарциномы почки
- Прогноз и профилактика
- Цены на лечение
Общие сведения
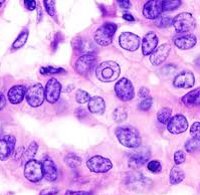
Папиллярная аденокарционома почки в клинической онкоурологии диагностируется в 7-16% от всех случаев рака почки. Опухоль развивается из клеток переходного эпителия, выстилающего чашечно-лоханочный комплекс. Макроскопически имеет вид мягкого узлового образования, на разрезе приобретающего характерную пеструю окраску. При микроскопическом рассмотрении имеет (сосочковую) папиллярную или тубулярную структуру. Как и рак паренхимы почки, папиллярная аденокарцинома чаще развивается у мужчин, достигая возрастного пика заболеваемости в 50-70 лет.

Причины
Заболевание является полиэтиологическим. Определяющую роль в развитии папиллярной аденокарциномы могут играть генетические дефекты и наследственные заболевания. Риск развития рака лоханки почки увеличивается при длительном приеме анальгетиков, НПВП, мочегонных средств; воздействии ионизирующего излучения, никотина и алкоголя. Трансформацию переходного эпителия почечных лоханок могут вызывать состояния иммунодефицита, длительное проведение гемодиализа, артериальная гипертензия, сахарный диабет, ожирение. У пациентов в анамнезе нередко отмечается цистэктомия по поводу карциномы мочевого пузыря.
Классификакция
TNM-классификация выделяет следующие стадии папиллярной аденокарциномы почки:
По распространенности первичной опухоли (T):
- Т0 – первичный очаг не выявляется
- Tis – преинвазивная аденокарцинома in situ
- Т1 – аденокарцинома прорастает субэпителиальный слой лоханки
- Т2 - аденокарцинома прорастает мышечный слой лоханки
- Т3 – аденокарцинома распространяется в окололоханочную клетчатку или почечную паренхиму
- Т4 - аденокарцинома прорастает в стенки соседних органов или паранефральную клетчатку.
По наличию метастазов в регионарных лимфоузлах (паракавальных, парааортальных, в воротах печени) (N):
- N0 - в регионарных лимфоузлах метастазы отсутствуют
- N1 - единичные метастазы в лимфоузлах до 2-х см в диаметре
- N2 – единичные метастазы в лимфоузлах до 5 см в диаметре
- N3 - метастазы в лимфоузлах более 5 см в диаметре
По наличию отдаленных метастазов (M) в легких, костях, печени, головном мозге, плевре, брюшине:
- М0 – отсутствие данных за отдаленные метастазы
- М1 – наличие данных за отдаленные метастазы
Симптомы аденокарциномы
Опухоль почки протекает бессимптомно у 10-25 % пациентов. Обычно манифестирует с тотальной гематурии (70-90% случаев), которая у трети больных сочетается с болевым синдромом в области поясницы. При обтурации мочеточника кровяным сгустком болевой приступ может протекать по типу почечной колики. В 10% наблюдений имеет место классическая триада симптомов рака почки: гематурия, боль, пальпируемая опухоль.
Обычно наличие типичной триады указывает на распространенность опухолевой инвазии и неблагоприятный прогноз. О далеко зашедшей стадии заболевания также свидетельствует похудание, слабость, субфебрилитет, артериальная гипертензия, анемия, нарушение аппетита. Метастазирование происходит гематогенным или лимфогенным способом. На момент выявления рака почечной лоханки метастазы в лимфоузлах и отдаленных органах имеются уже у четверти пациентов. Чаще всего аденокарцинома почки метастазирует в легкие, плевру, кости, печень, мозг.
Диагностика
Распознавание папиллярной аденокарциномы почки производится врачом-онкоурологом, нередко связано с существенными затруднениями. Проведение трехкратного цитологического исследования осадка мочи позволяет обнаружить атипичные клетки лишь в 30% случаев. Иногда для получения биоматериала прибегают к катетеризации мочеточника или забору промывных вод в процессе уретеропиелоскопии.
При экскреторной урографии папиллярная аденокарцинома определяется по дефекту заполнения почечной лоханки контрастным веществом, а при нарушении пассажа мочи – по признакам гидронефроза. Данные экскреторной урографии уточняются с помощью ретроградной уретеропиелографии, КТ почек с контрастным усилением, МСКТ, МРТ, сцинтиграфии. Почечная ангиография информативна при прорастании аденокарциномы в паренхиму почки и позволяет точно определить локализацию первичного очага (в лоханке или паренхиме).
Ценность УЗИ почек заключается в возможности выявления гидронефрротической трансформации, а также дифференциации рентгенонегативных камней почки и опухолей лоханки. Более информативные данные получают в ходе эндолюминальной эхографии: неоплазия выявляется в виде эхопозитивного образования; также метод позволяет выяснить глубину инвазии опухоли в слои почечной лоханки.
Для исключения имплантационных метастазов в мочеточник и мочевой пузырь проводится эндоскопическое обследование мочевых путей – уретероскопия, цистоскопия, при необходимости – биопсия. Папиллярную аденокарциному дифференцируют с туберкулезом почки, пиелитом, нефролитиазом. При подозрении на отдаленные метастазы выполняется рентгенография легких, головного мозга, костей, УЗИ печени.
Лечение папиллярной аденокарциномы почки
При операбельном процессе показано выполнение нефруретерэктомии и резекции мочевого пузыря, что позволяет предупредить имплантационное распространение новообразования по мочевым путям. Меньший объем вмешательства (пиелотомия с удалением опухоли, резекция почки или тотальная нефрэктомия) могут привести к рецидиву аденокарциномы и генерализации процесса. Органосохраняющая тактика может быть оправдана при поражении единственной почки либо выраженной недостаточности функции почек.
Целесообразность выполнения лимфаденэктомии при неизмененных лимфоузлах остается предметом дискуссий, однако удаление лимфоузлов имеет значение для стадирования опухолевого процесса. При распространенном раке лоханки операция дополняется химиотерапией или лучевой терапией.
Прогноз и профилактика
Исход определяется стадией процесса и степенью дифференцировки опухоли. Прогноз пятилетней выживаемости после радикальной нефруретерэктомии и резекции мочевого пузыря при неинвазивном росте переходноклеточной аденокарциномы составляет 75-90%. При метастазировании или нерадикальной операции прогноз крайне неблагоприятный – выживаемость не превышает 2-3-х лет. Профилактика предусматривает исключение предрасполагающих факторов.
Читайте также:

