Паллиативная помощь больным раком желудка
Паллиативное лечение – подход, направленный на улучшение качества жизни онкобольных и уменьшения страданий при протекании болезни.
Онкологические заболевания в последнее время диагностируются часто. В медицине разработано немало методов ранней диагностики, но больше половины больных онкологией обращаются к врачам уже в запущенной форме. Ситуация усложняется для медиков тем, что совместно с применением передовых методов лечения приходится искать возможности помощи людям, которым уже нельзя помочь.
Сущность паллиативной помощи
Онкологических больных на последней неоперабельной стадии мучают мучительные боли и страх перед смертью. Людям требуется поддерживающая терапия, которая снизит болевые симптомы. Также требуется обеспечить таким больным максимально возможные комфортные условия в последние дни или месяцы жизни. Паллиативное лечение старается эти нужды выполнить и поддержать близких родственников – понятие метода заключается в упомянутых принципах. Уход за человеком с онкологией и переживания ложатся на плечи ближайших родственников.
Обеспечение комфорта в жизни человека с неизлечимым диагнозом – это главная цель сотрудников паллиативной медицины. В онкологии задача врачей – удалить злокачественное новообразование и вернуть пациента к привычному ритму. Паллиативная медицина таких задач перед собой не ставит – этого не требуется. Пациент, нуждающийся в паллиативном лечении, имеет диагноз – 4 стадия рака.
Последние месяцы перед смертью для больного и родственников – непростое испытание. Человек знает, что его ждёт, также это знают и родные. Изменить ситуацию невозможно. Здесь требуется придерживаться многих принципов – этических, эмоциональных, физических и проч. Помощь требуется и умирающему, и близкому окружению. Паллиативная медицинская помощь в период тяжёлого напряжения приносит ощутимое облегчение каждой стороне.
Применение паллиативной помощи обширно – в онкологии, кардиологии, болезнях опорно-двигательного аппарата, патологиях неврологического характера и прочих.
Этапы паллиативной помощи
Метод паллиативной медицины иногда применяется к людям на раннем сроке заболевания. В этой ситуации используется основная терапия с дополнительным курсом паллиативного ухода. С прогрессированием болезни основная терапия отходит на второй план.
При паллиативном способе оказание помощи применяется:
- В условиях стационара, когда для пациента используется хирургическое, лучевое лечение и химиотерапия;
- Оказание помощи в отделении дневного пребывания;
- Роль медсестры важна, она заключается в уходе за больным в домашних условиях;
- Переоценить значение сестринского ухода в хосписе за пациентами нельзя.
Хосписы заменяют людям перед уходом дом и близких родственников. От рака лёгких, печени, желудка, головного мозга зафиксирован высочайший процент смертности. Люди переносят сильнейшие боли и психологические страдания, которые требуется снять.

Медицинский паллиативный метод в хирургии применяется при удалении части опухоли, что помогает продлить жизнь. Проводится мероприятие по купированию тяжёлых симптомов при раке и прочих заболеваниях. К примеру, делают выходное отверстие в брюшной стенке при тяжёлой кишечной непроходимости. Это помогает человеку устранить дискомфорт и вернуться к социальному окружению.
Лучевая терапия совместно с курсом химиотерапии уменьшает размер злокачественного новообразования и позволяет блокировать прогрессирование на некоторое время. В этот период снижается интоксикация организма продуктами ракового образования.
Больные в области онкологии больше находятся дома под присмотром родственников. Здесь требуется опыт специалиста, который разъяснит правила приёма лекарственных средств, поддержит общение с больным и поможет советом в трудный момент.
При невозможности проводить симптоматическое лечение дома пациента помещают в хоспис. Хосписные движения обрели популярность в России после 2011 года. Хоспис – это специализированное учреждение, где оказывается специализированная медицинская помощь бесплатно. Здесь находятся люди, у которых нет родственников либо отсутствует возможность присматривать дома.
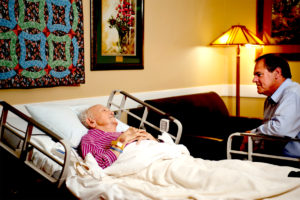
Принципы паллиативной медицины
- Манипуляции, направленные на купирование болевых ощущений;
- Устранение симптомов расстройства органов пищеварения – запора и тошноты с рвотой;
- Корректировка рациона питания;
- Психологическая помощь.
Смерть, которая может наступить в любой момент, приносит эмоциональные страдания и психологический дискомфорт. Усугубляет положение присутствие постоянных болей и нарушений в функционировании организма. Помощь сотрудников заключается в максимальном купировании нежелательных симптомов.
Большинство злокачественных новообразований на последней стадии протекает с интенсивной и мучительной болью. Испытывая боли, человек не может заниматься обычными делами – общаться, самостоятельно совершать прогулки, делать домашние дела. Значит, требуется правильно подобранный курс терапии по устранению неприятных признаков. В условиях стационара используют лучевое облучение. Для дома подбирается комплекс лекарств из группы анальгетиков.
Препараты подбираются индивидуально. Рассчитывается режим приёма, однократная доза и схема ввода. Учитывается физическое состояние пациента и характер болезненного течения. Схема приёма применяется с учётом того, чтобы действие предыдущей дозы пока не прекратилось. Это снижает болевой синдром.

Иногда используется другой метод борьбы с болью – начинать с анальгетиков без наркотического воздействия, затем меняется на препарат со слабым наркотическим действием и уже на последней стадии используется сильнодействующий опиат (к примеру, морфин). Подобная схема часто применяется в лечении детей. Многие родители против применения сильных опиатов, но приём позволяет снять боль и облегчить состояние ребенка. А это означает, что сотруднику паллиативной помощи требуется объяснить родителям необходимость данной процедуры.
Приём различных лекарственных средств, интоксикация от продуктов жизнедеятельности опухоли, курсы химиотерапии часто приводят к расстройствам в органах пищеварения. В этом случае применяется патогенетическое лечение. Присутствие тошноты с рвотными позывами демонстрирует интенсивный мучительный характер, купируемый приёмом специальных противорвотных препаратов. Рекомендуется использовать данный метод в лечении детей – это поможет сохранить доверие к лечащему доктору и предотвратит развитие нежелательного рефлекса на процедуры химиотерапии.
Часто использование опиоидных препаратов и химиотерапия провоцирует развитие запоров. Восстановить стул помогает комплекс слабительных средств. Детям рекомендуется лактулоза.
В онкологии большую роль играет правильно составленный рацион питания. Требуется это для хорошего самочувствия больного, чтобы восполнить дефицит витаминов с микроэлементами, предотвратить потерю веса и тошноту с рвотой. Паллиативная медицина призвана направлять пациентов и родных к правильному питанию.

Рацион составляется с учётом того, чтобы ослабленный болезнью организм получал необходимую суточную норму белков, жиров и углеводов. Пища должна быть приемлемо калорийной и с содержанием требуемых витаминов с микроэлементами.
Для отдельных людей (особенно детей) большую роль играет внешний вид блюда. Привлекательный вид и соответствующая атмосфера способствуют хорошему аппетиту и усвояемости пищи. Задача профессионалов – объяснить это родственникам и научить, как добиться подобного.
Этичное отношение во время неоперабельной стадии рака играет огромную роль в данный период. Люди, знающие о диагнозе и прогнозе, самостоятельно справиться с тяжким грузом не смогут. Также тяжело родственникам – они не знают, как себя вести, говорить о диагнозе, возникает масса других вопросов. Психологическая помощь требуется каждой стороне. Больному назначается курс успокоительных средств. Психолог общается со всеми – спокойные, наполненные любовью и радостью последние дни жизни необходимы не только больному, но и родным людям.
В рассуждениях, говорить либо нет диагноз пациенту – врачи склоняются к тому, что человек имеет право знать. Считается, что правда помогает легче перенести последние дни. Избранные люди с онкологией успевают за этот период совершить ряд невозможных действий, которые откладывали прежде долгие годы. Справиться со страхом перед смертью не удастся до конца, но можно как-то притупить эмоцию. В этом помогут специалисты.
Лечение онкологического заболевания – тяжёлый труд для врачей и родных людей. Медицинский персонал выполняет действия по устранению физических неприятных симптомов. Психологический комфорт создают родственники. Паллиативная медицина помогает снизить тяжесть эмоционального груза и физического дискомфорта.
Работы, посвященные статистике и эпидемиологии злокачественных новообразований, свидетельствуют о том, что первое место в структуре онкологической заболеваемости населения России занимают злокачественные заболевания органов пищеварения, составляя 31,7% всех злокачественных опухолей (Чиссов В.И. с соавт., 1998).
Совершенствование методов исследования и организационно-методических мероприятий по ранней диагностике рака желудочно-кишечного тракта не привело пока к стойким изменениям в соотношении стадий рака среди первично выявленных больных: процент пациентов с IV стадией опухолевого процесса по-прежнему очень высок.
Так, в 1998 году диагноз рака желудка установлен в IV стадии заболевания в 41,9% случаев, при этом умерли в течение первого года после установления диагноза 56% больных (Трапезников Н.Н. с соавт., 2000).
Возможности радикального хирургического лечения этой категории больных исчерпаны. Благодаря созданию и внедрению в практику противоопухолевых химиопрепаратов, появились предпосылки для оказания помощи больным с неоперабельным раком желудочно-кишечного тракта.
Нами была поставлена цель — улучшить результаты лечения генерализованного рака данной локализации: уменьшить клинические проявления заболевания, облегчить состояние этого тяжелого контингента больных, улучшить качество жизни и увеличить ее продолжительность путем применения химиопрепаратов после пробных и паллиативных операций, а также как самостоятельного метода лечения больных раком желудочно-кишечного тракта IV стадии.
Результаты аутогемохимиотерапии у больных раком желудка IV стадии
Результаты неоадъювантной аутогемохимиотерапии, являющейся рациональным и эффективным компонентом комплексного лечения больных раком желудка III стадии (Малейко М.Л., 1998; Орловская Л.А. с соавт., 2000; Сидоренко Ю.С. с соавт., 2000), послужили основанием для применения этого метода в терапии тяжелой и бесперспективной категории больных раком желудка, имеющих генерализацию опухолевого процесса.
Аутогемохимиотерапия была проведена 22 пациентам с IV стадией рака желудка в возрасте от 40 до 75 лет в качестве самостоятельного метода лечения. В исследование были включены пациенты с морфологически подтвержденным диагнозом, объективными проявлениями болезни, компенсированными сердечной, печеночной и почечной функциями, удовлетворительными гематологическими показателями.
Генерализация процесса выявлена у больных либо при первичном обследовании, либо после диагностической лапаротомии. При первичном обследовании генерализация чаще всего определялась на основании наличия у больных метастатического поражения печени, асцита или метастазов в надключичные лимфоузлы слева (метастаз Вирхова).
При оперативном лечении критериями запущенности опухолевого процесса являлись канцероматоз брюшной полости, метастатическое поражение печени, наличие обширных забрюшинных метастазов с местно-неоперабельным процессом.
Методика проведения аутогемохимиотерапии заключается во введении противоопухолевых химиопрепаратов на 150 мл аутокрови больного, взятой из периферической вены в стерильный флакон с 50 мл глюгицира. В это же флакон сразу после забора крови вводятся химиопрепараты, разведенные в 10 мл 0,9% раствора NaCl.
После экспозиции в течение 30 минут в термостате при температуре 36,8° С производится внутривенная капельная реинфузия аутокрови с цитостатиками. С целью частичной синхронизации цикла опухолевых клеток за 24 часа до начала процедуры внутривенно вводилась онкостатическая доза — 10 мг винбластина, который вызывает блокирование клеток опухоли в фазах G и G0.
Проведенный анализ литературы показал, что наиболее целесообразным является включение в различные схемы химиотерапии 5-фторурацила, как самого активного агента при лечении рака желудка (Мурованная Ю.В., 1993; Шевченко В.В. с соавт., 1996) и метотрексата, который оказывает модулирующее действие на 5-фторурацил, усиливая его противоопухолевый эффект (Nakagomi M. et al., 1997; Sasaki T., 1996).
Используемая нами комбинация химиопрепаратов включала три цитостатика с различным механизмом действия и различной точкой приложения их в цепи метаболизма опухолевых клеток.
Достигалось это применением антиметаболитов — 5-фторурацила и метотрексата, блокирующих синтез нуклеиновых кислот в S-фазе клеточного цикла, а также алкилирующего препарата — циклофосфана, активного в G2 фазе.
Разовые дозы химиопрепаратов составили: 5-фторурацил 750-1000 мг, метотрексат 20-25 мг, циклофосфан 400-600 мг. Введение химиопрепаратов на аутокрови осуществлялось 2 раза в неделю с интервалом в 2-3 дня в течение двух недель, т.е на курс лечения — 4 процедуры аутогемохимиотерапии. При этом курсовые дозы цитостатиков составили 5-фторурацил — 3000-4000 мг, метотрексат — 80-100 мг, циклофосфан — 1600-2400 мг.
Несмотря на тяжесть состояния некоторых пациентов, аутогемохимиотерапия начиналась одновременно с симптоматической терапией. Обязательным компонентом лечения в этих случаях являлась дезинтоксикационная терапия.
Непосредственные результаты аутогемохимиотерапии оценивались через 5-7 дней после окончания лечения. Эффективность определялась на основании данных рентгенографии, желудка, фиброгастроскопии, ультразвукового исследования брюшной полости, а также изменения частоты общих симптомов рака желудка.
В связи с распространенностью опухолевого процесса лечебный эффект считался положительным не только при наличии регрессии первичной опухоли или ее метастазов, но и на основании изменения клинических проявлений заболевания.
При анализе эндоскопических и рентгенологических данных нами выявлено, что проведение курса аутогемохимиотерапии вызывало различной степени регрессию опухоли желудка. Так, лечение оказалось эффективным у 8 (36,3%) больных. Однако дальнейший рост опухоли, т.е. прогрессирование процесса в ходе применения аутогемохимиотерапии не наблюдалось ни у одного пациента. Прослеживалась зависимость степени регрессии опухоли от макроскопической формы роста, гистологического типа и локализации ее в желудке.
Выявлена тенденция, когда наибольшая регрессия достигалась при наличии аденокарцином различной степени дифференцировки с экзофитной или смешанной формой роста, поражающих проксимальные отделы желудка.
Проведение контрольного ультразвукового исследования желудка после аутогемохимиотерапии показало уменьшение метастатически пораженных забрюшинных лимфатических узлов более чем на 50% у 8 (44,4%), а полное их исчезновение — у 3 (16,7%) из 18 пациентов.
Также отмечена различной степени регрессия (25-50%) метастатических очагов в печени у 5 из 14 (35,7%) больных. Дополнительно ультразвуковое исследование показало уменьшение асцита у 4 из 11 (36,4%) пациентов.
Однако, в связи с неоперабельностью данной категории больных, эти данные представляют больше научный интерес. Анализ же непосредственных результатов аутогемохимиотерапии на основании уменьшения клинических проявлений болезни, с нашей точки зрения, представляет практический интерес, так как отмечаемое стихание общих симптомов рака желудка существенно облегчает состояние больных и улучшает их самочувствие.
Основными клиническими проявлениями были: болевой синдром (20 пациентов), отрыжка (15), тошнота (12), рвота (10), лихорадка при метастатическом поражении печени (11), снижение аппетита (17) и слабость (18).
Полученные нами данные изменения частоты общих симптомов рака желудка представлены в таблице 11.2.5.1.
Таблица 11.2.5.1. Влияние аутогемохимиотерапии на клинические проявления у больных раком желудка IV стадии 
Из таблицы видно, что уменьшение или стихание болей отмечено у 13 из 20 больных — 65%. Такие симптомы, как отрыжка и тошнота, уменьшились или исчезли в 7 из 15 (46,7%) и в 5 из 12 (41,7%) случаев, соответственно. Рвота, которая отмечалась у 10 больных, исчезла в 3 наблюдениях (30%). Улучшение аппетита зарегистрировано у 13 из 17 (76,4%) пациентов, а исчезновение слабости — у 12 из 18 (66,7%) больных. Нормализация температуры отмечена у 4 из 11 пациентов (36,4%).
К основным объективным критериям эффективности противоопухолевой терапии в настоящее время, наряду с уменьшением размеров опухоли, относят и увеличение продолжительности жизни больных. Учитывая, что контроль за динамикой регрессии опухоли желудка затруднителен, данные о выживаемости больных следует рассматривать как наиболее важный показатель эффективности химиотерапии.
Нами прослежены исходы лечения больных раком желудка IV стадии, которые получали аутогемохимиотерапию в качестве самостоятельного метода лечения. Данные о средней продолжительности жизни этого контингента больных в сравнении с реферативным контролем представлены в таблице 11.2.5.2.
Таблица 11.2.5.2. Исходы лечения больных раком желудка IV стадии, получавших аутогемохимиотерапию в качестве самостоятельного лечения в сравнении с контрольной группой 
Из таблицы следует, что средняя продолжительность жизни у больных генерализованными формами рака желудка, которым был проведен курс аутогемохимиотерапии, выше, чем в контроле и составляет 9,8±2,6 мес (р
Паллиативные операции при раке желудка включают в себя симптоматические операции, временно облегчающие состояние пациентов, и направленные на устранение тех или иных тяжелых или опасных для жизни симптомов онкологического заболевания, а также циторедуктивные операции, которые существенно уменьшают размер первичной опухоли и метастазов, уменьшая степень опухолевой интоксикации.
В каких ситуациях проводятся паллиативные операции при раке желудка?
В лечении рака желудка главная роль до сих пор принадлежит хирургическому методу, однако, на поздних стадиях рака желудка при распространенных поражениях окружающих тканей с вовлечением регионарных лимфатических узлов и наличием отдалённых метастазов, тяжелом состоянии пациента, проведение радикальных операций невозможно. Радикальные операции при раке желудка (субтотальная резекция желудка, гастрэктомия, проксимальная резекция) – это всегда обширные операции, которые помимо вмешательства собственно на желудке сопровождаются удалением большого и малого сальника, а во время комбинированных операций одновременно удаляют полностью или частично пораженные раковым процессом соседние органы (поджелудочную железу, печень, поперечно-ободочную кишку, селезенку).
Радикальная операция при раке желудка является серьезным хирургическим вмешательством, которое требует существенной компенсации функций организма. Многим больным отказывают в операции из-за высокой степени операционного риска. Между тем при раке желудка на 4-й стадии на фоне специфической терапии 5-летняя выживаемость достигает 15-20%, а с развитием высокотехнологичных методов лечения можно рассчитывать и на большее продление жизни пациентов. Поэтому сейчас активно разрабатываются хирургические методики, позволяющие облегчить состояние и значительно улучшить качество жизни пациентов с раком желудка, радикальная операция у которых невозможна.
Выполнение паллиативных операций у пациентов с раком желудка делают возможным проведение лучевой и химиотерапии, введение индивидуальных противоопухолевых вакцин и моноклональных антител (SU11248), что позволяет добиться стойкой стабилизации течения заболевания и увеличить ожидаемую продолжительность жизни.
Когда необходимо паллиативное хирургическое вмешательство?
Диагноз 4 стадии рака желудка устанавливается при инвазивном поражении опухолью соседних органов, близлежащих лимфатических узлов, или при наличии метастазов в отдаленные органы и ткани. Хирургическое лечение в таких ситуациях применяется преимущественно для лечения жизнеугрожающих состояний – кровотечения из опухоли, прободения (перфорации) стенки желудка, стенозе желудка с развитием тяжелых водно-электролитных расстройств и невозможностью питания, желтухе при поражении опухолью печени и желчевыводящих путей.
В хирургическом стационаре лечение начинают с попытки остановки кровотечения с помощью кровоостанавливающих средств и установке зонда Блэкмора для прекращения желудочного кровотечения. Одновременно начинается инфузия препаратов плазмы крови с целью профилактики ДВС-синдрома, а при массивной кровопотере также проводится переливание эритроцитарной массы. Малоинвазивные вмешательства выполняются с целью поиска источника кровотечения и точечной ликвидации кровотечения, для чего проводится эндоскопическое вмешательство, позволяющее выполнить клипирование и прошивание кровоточащего сосуда, провести электро- или плазменную коагуляцию. Все эти методики остановки желудных кровотечений при раке желудка и других осложнениях онкологических заболеваний используются в Европейской онкологической клинике.
При неэффективности предпринятых мер по устранению желудочного кровотечения проводится экстренная хирургическая операция.
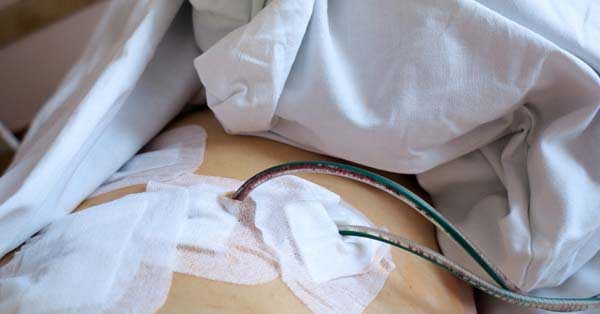
Желтуха - прямое противопоказание для проведения плановых химио- и лучевой терапии. Единственным радиальным методом снижения высокого уровня билирубина является восстановления оттока желчи из печени путем проведения рентгенохирургического вмешательства. Дренирование позволяет наладить временный отток наружу на поверхность кожи (наружный дренаж) или как наружу, так и в естественном направлении в кишечник (наружно-внутренний дренаж). В некоторых случаях, когда опухолевое сдавление изолирует несколько разных сегментов желчного дерева, например, как левую, так и правую доли печени, может потребоваться установка нескольких дренажей.
После снижения уровня билирубина до нормальных величин и уменьшения явлений холангита дренаж заменяется на стент или стенты – специальные эндопротезы, которые поддерживают желчный проток в открытом состоянии. Выполнение одномоментного дренирования и стентирования проводится только по строгим медицинским показаниям, чаще всего эти операции разделены по времени. В целом, дренирование и стентирование желчных протоков существенно улучшает качество жизни больных.

У 10-15% пациентов раком желудка развивается требующий хирургического вмешательства стеноз (сужение просвета) кардиального или пилорического отдела желудка. Симптомами этого состояния служат затруднение при проглатывании пищи при поражении верхних (кардиальных) отделов, тяжесть, чувство переполнения и рвота давно съеденной пищей при вовлечении перехода из желудка в 12-перстную кишку(пилоростеноз).
Стеноз при раке желудка чреват развитием опасных для жизни водно-электролитных расстройств и усугублением кахексии (истощения). Для восстановления прохождения пищи по желудочно-кишечному тракту, коррекции и профилактики водно-электролитных нарушений при иноперабельном раке желудка со стенозом пилорического отдела проводят операцию гастроэнтеростомии, т.е. наложение соустья между желудком и тощей кишкой.
C целью коррекции стеноза при неоперабельном раке проксимального (кардиального) отдела желудка c переходом на пищевод при нарушении прохождения пищи может использоваться стентирование желудка – установка специальных стентов, которые восстанавливают нормальное прохождение пищи через желудок в кишечник. Альтернативным способом хирургического лечения является наложение гастростомы – гастростомия - формирование отверстия в желудке и передней брюшной стенке, для обеспечения питания больного через зонд. В результате уменьшаются симптомы интоксикации и обеспечение питание больного.
Операции раке с метастазами
Рак желудка в большинстве случаев довольно рано дает метастазы. Из числа наиболее часто поражаемых метастазами органов следует указать печень, поджелудочную железу, легкие, яичники (метастаз Крукенберга), а также брюшину, которая покрывается множественными раковыми узелками, что сопровождается выпотом жидкости в брюшную полость (асцитом). Помимо того, что метастазы могут приводить к развитию острых осложнений, требующие экстренной хирургической помощи (сдавление нижней полой вены), они существенно нарушают функционирование пораженных органов, значительно ухудшают общее состояние, нередко сопровождаясь нестерпимыми болями, требующими постоянного обезболивания.
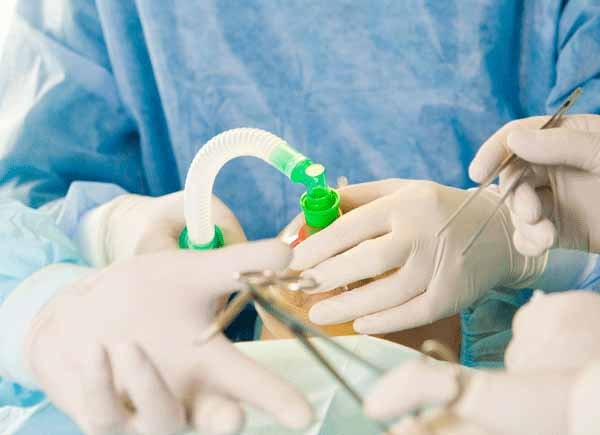
Как в ведущих, в т.ч. зарубежных клиниках, так и в Европейской онкологической клинике для лечения метастазов рака желудка, в частности в печень, используется чрескожная чреспеченочная радиочастотная абляция (РЧА) – методика, вызывающая контролируемый асептический некроз метастатического очага, без повреждения окружающих тканей. Результатом такого некроза становится полная гибель опухолевых клеток метастаза. При ее выполнении, которое проводится под общим обезболиванием, под ультразвуковым контролем сквозь кожу вводится монополярный радиоволновой электрод, разогревающий именно нужный участок печени и вызывающий локальный некроз метастаза. РЧА может также проводится во время открытой операции на желудке и органах брюшной полости. РЧА метастазов печени дает возможность надолго продлить жизнь пациента без возникновения рецидивов. У нас накоплен опыт неодократного проведения РЧА для полного устранения множества мелких метастазов печени, а также в случае появления новых метастатических очагов.
В отделении интервенционной онкологии и эндоваскулярной хирургии Европейской онкологической клиники выполняется химиоэмболизация артерий, питающих крупные метастазы, преимущественно в печени, с целью уменьшения негативного влияния метастазов рака на организм пациента. Прекращение кровотока в опухоли уже само по себе оказывает лечебное воздействие. Одновременная доставка в ткань опухоли химиопрепаратов разрушает ее изнутри, избавляя пациента от токсического действия лекарства на весь организм в целом.
В мире используется также такая методика лечения метастазов печени, как радиоэмболизация метастазов рака желудка в печень. Она проводится под контролем ангиографа с помощью внутрисосудистой селективной катеризации сосудов печени. В сосуд, питающий опухоль, вводятся эмболизирующие частицы с радиоактивным изотопом иттрий-90, которые в последующие после операции 64 часа продолжают изнутри воздействовать на опухоль. К сожалению, в нашей стране данная методика не доступна. Для этих целей мы направляем пациентов в клиники Израиля и Германии.
Малотравматичные резекции печени, включая радиочастотную аблацию метастазов рака в печень, в нашей клинике проводятся учеником профессора, д.м.н. Юрия Ивановича Патютко, заместителем главного врача клиники, к.м.н. Андреем Львовичем Пылёвым. Кроме того, наиболее сложные операции выполняются самим Юрием Ивановичем Патютко, руководителем хирургического отделения опухолей печени РОНЦ им. Н. Н. Блохина.
При распространении опухолевого процесса – диссеминации метастазов опухоли желудка по брюшине (т.н. канцероматоз брюшины) может происходить накопление жидкости в брюшной полости. Это состояние называется асцит, оно довольно мучительно для пациента. В основном, оно обусловлено механическим препятствием обратному всасыванию жидкости из брюшной полости, в норме происходящему очень интенсивно (до 1,5 л в сутки) и закупоркой лимфатических сосудов. При метастатическом поражении паренхимы печени, в основе развития асцита лежит, кроме того, препятствие венозному оттоку крови.
Когда жидкости становится больше 5 л и больше сдавление внутренних органов, нарушение экскурсии диафрагмы, повышение внутрибрюшного давления приводят к смещению органов вверх, в грудную полость, вызывают дыхательную недостаточность и нарушение нормального крово- и лимфотока. При этом создаются благоприятные условия для быстрого и обширного метастазирования опухоли. Однако одномоментное удаление большого количества асцитической жидкости может привести к возникновению тяжелых осложнений, поэтому в Европейской онкологической клинике для дренирования асцитов применяются современные методики лапароцентеза с использованием специальных помп для постепенного и дозированного удаления серозной жидкости.
Параллельно проводится инфузионная терапия для коррекции водно-электролитных нарушений, инфузии альбумина, коллоидов и объёмо-замещающих растворов. Для предотвращения возникновения асцита, после первичной эвакуации асцитической жидкости, мы активно используем цитостатические препараты, т.е. лекарственные вещества, способствующие уменьшению объема выпота и более медленному накоплению жидкости, в том числе внутриполостное введение лекарственных препаратов. Внутриполостная химиотерапия эффективна в 40-60% случаев и позволяет сохранить положительный эффект брюшинной пункции на срок более 2 месяцев. Лапароцентез производится под ультразвуковой навигацией и при необходимости завершается установкой дренажа для длительной эвакуации жидкости.
Применяемые в нашей клинике катетеры не ограничивают естественную двигательную активность и обеспечивают возможность возвращения пациента к привычной деятельности. При рефрактерных и массивных асцитах возможно проведение паллиативных операций (установка перитонеовенозного шунта, частичная деперитонизация стенок брюшной полости, оментогепатофренопексия и другие). При таком комплексном подходе процедуру лапароцентеза требуется делать в 2-3 раза реже, чем при классическом проведении пункции брюшинной полости.
Насколько оправданы вмешательства в 4 стадии рака желудка, ведь они не приводят к излечению?
Философия оказания медицинской помощи в Европейской онкологической клинике заключается в том, что пациенту надо стараться помочь всегда. Человеческая жизнь бесценна, и ее нужно продлить на максимально больший срок при поддержании максимально возможного качества жизни. Вмешательства на поздней стадии онкологического заболевания, включая 4-ю стадию рака желудка, должны предприниматься, поскольку они позволяют существенно улучшить качество жизни пациентов, уменьшить интоксикацию и выраженность болевого синдрома, продлить жизнь и возможность общения с родными и близкими на существенный срок. Например, проведение перитонэктомии в сочетании с гипертермической внутрибрюшной химиотерапией у больных с канцероматозом брюшины при раке желудка позволяет увеличить продолжительность жизни до 18 месяцев. При единичных изолированных метастазах рака желудка в печень ее резекция позволяет достичь 5-летней выживемости у 18–34% больных.
Для лечения 4 стадии рака желудка в отделении паллиативной и симптоматической терапии используются все возможные варианты лечения онкологических больных: все виды химиотерапии, лучевая терапия, которая позволяет уменьшать болевой синдром, а также выполняются паллиативные операции. С целью облегчения введения препаратов возможна имплантация венозных и артериальных инфузионных порт-систем для химиотерапии, проводится регионарная интраартериальная инфузия химиопрепаратов, местная терапия.
— Необходима ли какая-либо особая подготовка для проведения паллиативных операций?
Безусловно, из-за тяжести болезни наши пациенты требуют особенно тщательной подготовки и ведения послеоперационного периода. Обычно предоперационная подготовка заключается в общеукрепляющем лечении, инфузионной терапии белковыми препаратами, солевыми и коллоидными растворами, витаминами, в применении тонизирующих средств. Существуют методики предоперационной инфузионной подготовки, позволяющие уменьшить кровопотерю в процессе операции, они активно используются в нашей клинике. Как правило больные нуждаются в гипералиментации – введении питательных веществ высокой энергетической ценности.
В послеоперационном периоде на несколько дней исключают прием пищи и воды через рот. Необходимые количества жидкости и питательных веществ восполняют путём внутривенных вливаний питательных растворов с инсулином, витаминами, а также крови и белковых препаратов. Пациенту назначают антибиотики, сердечные средства, наркотики и кислород. Важным компонентом является тщательный уход, дыхательная гимнастика, внимательное наблюдение за течением послеоперационного периода. В дальнейшем огромное значение имеет правильное сбалансированное дробное питание, приём необходимых препаратов и уход за больным.
Читайте также:

