Острый лейкоз по латыни
Острый лейкоз — злокачественное заболевание кроветворной системы; морфологический субстрат — властные клетки. Частота. 13,2 случаев на 100000 населения среди мужчин и 7,7 случаев на 100 000 населения среди женщин. Классификация и эпидемиология. По цитохимическим исследованиям (определение ферментов, характерных для разных бласт-ных клеток) различают лимфобластные и миелобластные лейкозы. Франко-американо-британская (FAB) классификация основана на морфологии лейкемических клеток (строение ядра, соотношение размеров ядра и цитоплазмы)
● Острый миелобластный (нелимфоб-ластный) лейкоз (ОМЛ)
● М0- без созревания клеток, миелогенная дифференцировка доказывается только иммунологически
● М, — без созревания клеток
● М2 — ОМЛ с дифференцировкой клеток
● М5- моно-бластный лейкоз
● М7 — мегакариобластный лейкоз
● Острый лимфобластный лейкоз (ОЛЛ)
● L, — без дифференцировки клеток (морфологически гомогенные клетки)
● L2 — с дифференцировкой клеток (морфологически гетерогенная популяция клеток)
● L3 — беркеттоподобные лейкозы
● Недифференцируемый лейкоз — к этой категории относят лейкозы, клетки которых невозможно идентифицировать как миелобластные или лимфобластные (ни химическими, ни иммунологическими методами)
● рефрактерная анемия без бластоза (в костном мозге бласты
● рефрактерная анемия с бластозом (в костном мозге бласты
● промиелоциты 10-30%). Иммуногистохимическое исследование (определение клеточного фенотипа) необходимо для уточнения иммунологического варианта лейкоза, влияющего на схему лечения и клинический прогноз
● Острый лимфобластный лейкоз (247640, р, мутация соматических клеток) — 85% всех случаев диагностируют у детей, составляя до 90% всех лейкозов детского возраста. У взрослых развивается достаточно редко. Цитохимические реакции — положительная на терминальную дезоксинуклеотидил трансферазу, отрицательные на миелопероксидазу, гликоген. Использование маркёров клеточной мембраны позволило выделить подвиды
● В-клеточные (75% всех случаев) с отсутствием розеткообразования
● реже -другие варианты. Дифференциальная диагностика подвидов важна для прогноза, т.к. Т-клеточные варианты плохо поддаются лечению
● Острый миелобластный лейкоз (острая гранулоцитарная лейкемия, острая миелоцитарная лейкемия) чаще возникают у взрослых, подтип зависит от уровня дифференцировки клеток. В большинстве случаев миелобластный клон клеток происходит из стволовых кроветворных клеток, способных к множественной дифференцировке в колониеобразующие единицы гранулоцитов, эритроцитов, макрофагов или мегакариоцитов, поэтому у большинства больных злокачественные клоны не имеют признаков лимфоидных или эритроидных ростков
● ОМЛ наблюдают наиболее часто; имеет четыре варианта (М0 — М3)
● mo и М1 — острый без дифференцировки клеток
● М2 — острый с дифференцировкой клеток
● М3 — промиелобласт-ный лейкоз, характеризуется наличием аномальных промиелоцитов с гигантскими гранулами; часто сочетается с ДВС, обусловленным
тромбопластическим эффектом гранул, что подвергает сомнению целесообразность применения гепарина при терапии. Прогноз при М:, более благоприятен, чем при М0-М,
● Миеломонобластный и монобластный лейкозы (соответственно М4 и М5) характеризуются преобладанием неэритроидных клеток типа монобластов. М
● Эрит-ролейкоз (Мв). Вариант острого миелобластного лейкоза, сопровождающийся усиленной пролиферацией эритроидных предшественников; характерно наличие аномальных бластных ядросодержащих эритроцитов. Эффективность лечения эритролейкоза сходна с результатами терапии других подтипов или несколько ниже
● Мегакариобластный лейкоз (М7) — редкий вариант, сочетающийся с фиброзом костного мозга (острый миелосклероз). Плохо поддаётся терапии. Прогноз неблагоприятный.
Патогенез обусловлен пролиферацией опухолевых клеток в костном мозге и их метастазированием в различные органы. Угнетение нормального кроветворения связано с двумя основными факторами
● Повреждение и вытеснение нормального ростка кроветворения низкодифференцированными лейкемическими клетками
● Выработка властными клетками ингибиторов, подавляющих рост нормальных кроветворных клеток.
✎ Клиническая картина острых лейкозов определяется степенью инфильтрации костного мозга бластными клетками и угнетения ростков кроветворения
● Угнетение костномозгового кроветворения
● Анемический синдром (миелофтизная анемия)
● Геморрагический диатез (вследствие тромбоцитопении отмечают кожные геморрагии — петехии, экхимозы; кровотечения из слизистых оболочек — носовые кровотечения, внутренние кровотечения)
● Инфекции (нарушение функции лейкоцитов)
● Увеличение лимфатических узлов
● Поражения кожи (лейкемиды), мозговых оболочек (нейролейкоз) и внутренних органов
● Снижение массы тела
✎ Диагноз: острого лейкоза подтверждают наличием бластов в костном мозге. Для идентификации подтипа лейкоза применяют гистохимические, иммунологические и цитогенетические методы исследования.
● Панцитопения при увеличении бластных форм (в 50% случаев -- гиперлейкоцитоз)
● Гиперурикемия вследствие ускоренного жизненного цикла клеток
● Гипофибри-ногенемия и повышение содержания продуктов разрушения фибрина вследствие сопутствующего ДВС.
Влияние лекарственных препаратов. Глюкокортикоиды не следует назначать до постановки окончательного диагноза. Высокая чувствительность к преднизолону бластных клеток приводит к их разрушению и трансформации, затрудняющим диагностику.
✎ Лечение комплексное; цель — достижение полной ремиссии.
● Химиотерапия состоит из нескольких этапов
● При ОЛЛ — одна из схем: комбинации винкри-стина в/в еженедельно, преднизолона внутрь ежедневно, даунорубицина (рубомицина гидрохлорид) и L-аспарагиназы в течение 1-2 мес непрерывно
● При остром миелобластном лейкозе — сочетание цитарабина в/в капельно или п/к каждые 12 ч в течение 6-7 дней, даунорубицина (рубомицина гидрохлорид) в/в в течение 3 дней, иногда в сочетании с тиогуанином. Более интенсивная постиндукционная химиотерапия, уничтожающая оставшиеся лейкозные клетки, увеличивает длительность ремиссии
● Консолидация ремиссии: продолжение системной химиотерапии и профилактика нейролейкоза при ОЛЛ (эндолюмбальное введение метотрексата при ОЛЛ в сочетании с лучевой терапией на головной мозг с захватом сегментов С1-С2 спинного мозга)
● Поддерживающая терапия: периодические курсы реиндукции ремиссии.
● Трансплантация костного мозга — метод выбора при острых миелобластных лейкозах и при рецидивах всех острых лейкозов. Главное условие для проведения трансплантации — полная клинико-гематологическая ремиссия (бластов в костном мозге
● Оптимальный донор — однояйцевый близнец или сибс; чаще используют доноров с 35% совпадением по Аг HLA. При отсутствии совместимых доноров используют аутотрансплантацию костного мозга, взятого в период ремиссии
● Главное осложнение — реакция трансплантат против хозяина. Развивается вследствие пересадки Т-лимфоцитов донора, распознающих Аг реципиента как чужеродные и вызывающих иммунную реакцию против них. Острая реакция развивается в течение 20-100 дней после трансплантации, отсроченная — через 6-12 мес
● Основные органы-мишени — кожа (дерматит), ЖКТ (диарея) и печень (токсический гепатит)
● Лечение длительное, обычно ограничено назначением комбинаций преднизолона, циклоспорина и малых доз азатиоприна
● На течение посттрансплантационного периода влияют также подготовительные схемы лечения, развитие интерстициальной пневмонии, отторжение трансплантата (редко).
● Трансфузия эритроцитарной массы. Показания: Нb ниже 70 г/л при клинических проявлениях анемии, перед предстоящим введением цитостатиков. При компенсированном состоянии больного следует ограничить показания к заместительной терапии, во избежание заражения посттрансфузионным гепатитом и нежелательной сенсибилизации
● Трансфузия свежей тромбоцитарной массы (снижает риск кровотечений). Показания: содержание тромбоцитов менее 20х109/л; геморрагический синдром при содержании тромбоцитов менее 50х109/л.
● Профилактика инфекций — главное условие выживания пациентов с нейтропенией, возникшей вследствие химиотерапии
● Полная изоляция пациента
● Строгий санитарно-дезинфекционный режим — частые влажные уборки (до 4-5 р/сут), проветривание и кварцевание палат; использование одноразового инструментария, стерильной одежды медицинского персонала
● Профилактическое применение антибиотиков, противовирусных препаратов (при количестве сегментоядерных нейтрофилов
● При повышении температуры тела проводят клиническое и бактериологическое исследования и немедленно начинают
лечение комбинациями бактерицидных антибиотиков широкого спектра действия: цефалоспоринов, аминогликозидов (тобрамицин) и полусинтетических пенициллинов
● При вторичных подъёмах температуры тела, возникших после лечения антибиотиками широкого спектра действия, эмпирически применяют противогрибковые средства (амфотери-цин В)
● Для профилактики и лечения нейтропении можно назначить молграмостим.
✎ Прогноз
● Прогноз у детей с острым лимфолейкозом хороший: у 95% и более наступает полная ремиссия. У 70-80% больных проявлений болезни нет в течение 5 лет, их считают излечившимися. При возникновении рецидива в большинстве случаев можно достичь второй полной ремиссии. Больные со второй ремиссией — кандидаты на трансплантацию костного мозга с вероятностью долговременного выживания в 35-65% случаев
● Прогноз у больных острым миелобластным лейкозом неблагоприятный. У 75% больных, получающих адекватное лечение с использованием современных химиотерапев-тических схем, достигают полной ремиссии, 25% больных погибают (длительность ремиссии — 12-18 мес). Есть сообщения об излечении в 20% случаев при продолжении интенсивной терапии после ремиссии. Больным моложе 30 лет после достижения первой полной ремиссии можно проводить трансплантацию костного мозга. У 50% молодых больных, подвергшихся аллогенной трансплантации, развивается длительная ремиссия. Обнадёживающие результаты получены и при пересадках аутологичного костного мозга. Возрастные особенности
● Дети лучше поддаются лечению
● Пожилые. Снижена толерантность к аллогенному костному мозгу. Максимальный возраст для трансплантации — 50 лет. Аутологичную трансплантацию можно проводить пациентам старше 50 лет при отсутствии органных поражений и общем соматическом благополучии.
✎ См. также: Лейкоз, рис. 1-8-1-12
✎ Сокращения:
● ОЛЛ — острый лимфобластный лейкоз
● ОМЛ -острый миелобластный лейкоз
✎ МКБ: .
● С91 Лимфоидный лейкоз
● С92 Миелоидный лейкоз
● С93 Миелоцитарный лейкоз
● С94 Другой лейкоз уточнённого клеточного типа
● С95 Лейкоз неуточнённого клеточного типа Литература. 34: 154-159
| Лейкоз | |
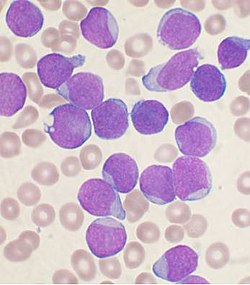 Микропрепарат костного мозга больного острой В-лимфоцитарной лейкобластной лейкемией | |
| МКБ-10 | C 91 91. -C 95 95. |
|---|---|
| МКБ-9 | 208.9 208.9 |
| МКБ-О | 9800-9940 |
| DiseasesDB | 7431 |
| MedlinePlus | 001299 |
| MeSH | D007938 |
Содержание
- 1 Факторы, ассоциированные с повышенным риском лейкозов
- 2 Патогенез
- 3 Классификация лейкозов
- 3.1 По типу течения
- 3.2 По степени дифференцировки опухолевых клеток
- 3.3 В соответствии с цитогенезом
- 3.4 На основе иммунного фенотипа опухолевых клеток
- 3.5 По общему числу лейкоцитов и наличию бластных клеток в периферической крови
- 4 Морфологические особенности
- 5 Диагностика
- 6 Лечение
- 6.1 Ранние экспериментальные методы
- 7 См. также
- 8 Примечания
- 9 Литература
- 10 Ссылки
Факторы, ассоциированные с повышенным риском лейкозов
По данным Mayo и ACS, точные причины возникновения лейкозов науке неизвестны [2] .
Среди факторов, коррелирующих с повышенным риском возникновения лейкозов (по данным Mayo): некоторые виды химиотерапии и радиотерапии, отдельные генетические нарушения, воздействие ряда химикатов, курение (выше риск острого миелобластного лейкоза), наследственность (случаи лейкозов в семье) [2] .
Патогенез
При лейкозе опухолевая ткань первоначально разрастается в месте локализации костного мозга и постепенно замещает нормальные ростки кроветворения. В результате этого процесса у больных лейкозом закономерно развиваются различные варианты цитопений — анемия, тромбоцитопения, лимфоцитопения, гранулоцитопения, что приводит к повышенной кровоточивости, кровоизлияниям, подавлению иммунитета с присоединением инфекционных осложнений.

Метастазирование при лейкозе сопровождается появлением лейкозных инфильтратов в различных органах — печени, селезенке, лимфатических узлах и др. В органах могут развиваться изменения, обусловленные обтурацией сосудов опухолевыми клетками — инфаркты, язвенно-некротические осложнения.
Лейкоз КРС Т-клеточный лейкоз человека [ источник не указан 771 день ] (см. Т-лимфотропный вирус человека) вызываются вирусами.
Классификация лейкозов
Можно выделить 5 основных принципов классификации:
- острые, из незрелых клеток (бластов), и
- хронические, созревающие и зрелые клетки.
- недифференцированные,
- бластные,
- цитарные лейкозы;
Эта классификация основывается на представлениях о кроветворении.
- Острые лейкозы по цитогенезу подразделяются на:
- лимфобластный,
- миелобластный,
- монобластный,
- миеломонобластный,
- эритромиелобластный,
- мегакариобластный,
- недифференцированный.
- Хронические лейкозы представлены лейкозами:
- миелоцитарного происхождения:
- хронический миелоцитарный лейкоз,
- хронический нейтрофильный лейкоз,
- хронический эозинофильный лейкоз,
- хронический базофильный лейкоз,
- миелосклероз,
- эритремия/истинная полицитемия,
- эссенциальная тромбоцитемия,
- лимфоцитарного происхождения:
- хронический лимфолейкоз,
- парапротеинемические лейкозы:
- миеломная болезнь,
- первичная макроглобулинемия Вальденстрема,
- болезнь тяжелых цепей Франклина,
- лимфоматоз кожи — болезнь Сезари,
- моноцитарного происхождения:
- хронический моноцитарный лейкоз,
- хронический миеломоноцитарный лейкоз,
- гистиоцитоз X.
- миелоцитарного происхождения:
В настоящее время стало возможным проводить более точное типирование опухолевых клеток в зависимости от их иммунного фенотипа по экспрессии CD19, CD20, CD5, легких цепей иммуноглобулинов и других антигенных маркеров.
- лейкемические (более 50—80×10 9 /л лейкоцитов, в том числе бласты),
- сублейкемические (50—80×10 9 /л лейкоцитов, в том числе бласты),
- лейкопенические (содержание лейкоцитов в периферической крови ниже нормы, но есть бласты),
- алейкемические (содержание лейкоцитов в периферической крови ниже нормы, бласты отсутствуют).
Морфологические особенности
При высоком блоке дифференцировки лейкозные клетки могут напоминать стволовые и бластные клетки первых четырёх классов клеток-предшественниц. Поэтому по степени дифференцировки эти лейкозы называют бластными и недифференцированными. Поскольку они протекают остро, то можно говорить, что острые лейкозы — это бластные и недифференцированные лейкозы.
При низком блоке дифференцировки лейкозные клетки напоминают процитарные и цитарные клетки-предшественницы, лейкозы протекают менее злокачественно, хронически и называются цитарными.
Основные клинические признаки острых лейкозов:
Основные клинические признаки хронических лейкозов (признаки те же, но с точностью наоборот):
Диагностика
В диагностике лейкозов большое значение имеет морфологическое исследование. Основными методами прижизненной морфологической диагностики являются исследования мазков периферической крови и биоптатов костного мозга, которые получают при трепанобиопсии гребня подвздошной кости или пункции грудины, а также других органов.
Лечение
При хронических лейкозах врач выбирает поддерживающую тактику, цель которой — отсрочить или исключить развитие осложнений. Острый лейкоз требует немедленного лечения, которое включает в себя приём высоких доз химиотерапевтических средств, что дает возможность организму очиститься от лейкозных клеток. После этого, при необходимости, назначается трансплантация здоровых донорских клеток костного мозга.
Цитостатики — это лекарственные средства, которые подавляют рост атипичных клеток. Они вводятся в организм с помощью внутривенной инъекции или перорально в виде таблеток. Разный вариант заболевания требует своей схемы лечения. Согласно рекомендациям Всемирной Организации Здравоохранения у каждого специалиста имеются различные схемы лечения. После того, как установлен точный вариант лейкемии (с учетом клеточного состава) пациенту назначаются химиопрепараты по необходимой схеме несколькими курсами. Первый курс направлен на устранение злокачественных клеток. Длительность его определяется индивидуально и составляет несколько месяцев. После успешного его проведения назначается поддерживающее лечение — пациенту вводятся те же дозы цитостатиков в таком же количестве. И последний этап — это профилактический курс. Он закрепляет полученный эффект и позволяет пациенту дольше находиться в ремиссии. После прохождения всего курса химиотерапии имеется высокая вероятность никогда более не столкнуться с этим заболеванием.
Однако медицина еще недостаточно развита, и организм может повести себя непредсказуемо. Так, после прохождения полноценного лечения болезнь может вернуться. В таком случае предлагается другой вариант терапии — пересадка костного мозга.
Исследователи из Центра исследований опухолей имени Фреда Хатчинсона в Сиэтле нашли [ значимость факта? ] способ повысить противоопухолевую активность иммунных клеток, чем удалось достичь почти 100%-й эффективности в лечении людей, ранее считавшихся безнадежно больными, уже через несколько недель применения новой терапии у 27 из 29 пациентов анализ костного мозга показал полное отсутствие злокачественных клеток. [3] [4]
1 Острый
• острый конец — acumen; cuspis, -idis f;
• острое словцо — ridiculum;
2 острый
3 острый
4 acer
5 acutus
6 coryza
7 Весьма
• соцветие весьма разнообразное — inflorescentia admodum varia;
• вид, весьма сходный с сирийским растением — species cum planta syriaca apprime congruens;
• вид, весьма сомнительный — species maxime dubia;
• виды, весьма родственные между собой — species inter se nimis affines;
• форма, весьма редкая — forma valde rara;
• весьма тонкий — pertenuis;
• весьма острый — peracutus;
• весьма трудно доказать — perarduum est demonstrare;
• Это мне будет весьма приятно — Id mihi pergratum erit perque jucundum;
• я весьма радуюсь — vehementer laetor;
• быть весьма расположенным к кому — mire favere alicui;
• весьма жалобно — perquam flebiliter;
• весьма холодно — tempestas est maxime frigida; maximum frigus est;
• он весьма богат — est praedives, longe ditissimus;
8 Вкус
• вяжущий вкус — sapor adstringens;
• горький вкус — sapor amarus;
• кислый вкус — sapor acidus;
• медово-сладкий вкус — sapor melleus;
• неприятный вкус — sapor ingratus;
• острый вкус — sapor acer;
• отвратительный вкус — sapor foedus;
• перечный вкус — sapor piperitus;
• приятный вкус — sapor gratus;
• иметь приятный вкус — jucunde sapere;
• сладкий вкус — sapor dulcis (suavis);
• солёный вкус — sapor salinus;
• терпкий вкус — sapor acebus;
• тошнотворный вкус — sapor nauseosus;
• хороший вкус — elegantia;
• со в вкусом — eleganter, venuste, scite;
• тонкий вкус — subtile judicium;
• человек с отличным вкусом — vir exquisito judicio; doctus et intelligens rerum aestimator; homo emunctae naris;
• эта выдумка пришлась по вкусу — placuit sollertia;
• у всякого свой вкус — suam cuique sponsam, mihi meam;
9 Запах
• аммиачный запах — odor ammoniacus;
• анисовый запах — odor aniseus;
• ароматный запах — odor aromaticus;
• бальзамический запах — odor balsamicus (balsameus, balsaminus);
• винный запах — odor vinosus;
• возбуждающий запах — odor excitans;
• вредный запах — odor noxius (perniciosus);
• гвоздичный запах — odor caryophyllaceus;
• гнилостный запах — odor putridus;
• долговременный запах — odor diutinus (diuturnus);
• дурной запах — odor malus; foetor;
• едкий запах — odor acer;
• зловонный запах — odor foetidus (taeter);
• камфарный запах — odor camphoratus;
• запах клопов — odor cimicinus;
• запах козла — odor hircinus;
• коричный запах — odor cinnameus;
• кратковременный запах — odor brevis (ephemerus);
• крепкий запах — odor gravis;
• запах лавра — odor laureus (laurinus);
• запах ладана — odor tureus;
• летучий запах — odor evolans;
• лимонный запах — odor citreus (citrinus);
• запах листвы — odor frondis vernalis;
• запах лука — odor cepaceus;
• запах мёда — odor melleus (mellitus);
• муравьинный запах — odor formicarum (formicinus);
• запах мускуса — odor moschatus;
• мышиный запах — odor murinus;
• запах мяты — odor menthosus;
• навозный запах — odor stercoris (stercorarius);
• нежный запах — odor mitis;
• незначительный запах — odor brevis (ephemerus);
• неизменный запах — odor immanens (perpetuus);
• неприятный запах — odor ingratus;
• нестойкий запах — odor infirmus (instabilis);
• одуряющий запах — odor stupefaciens;
• особый запах — odor peculiaris (proprius);
• острый запах — odor acer;
• отвратительный запах — odor foetidissimus;
• перечный запах — odor piperitus;
• полынный запах — odor absinthiacus;
• постоянный запах — odor constans (permanens);
• приятный запах — odor gratus (amabilis, suavis);
• пряный запах — odor aromaticus;
• раздражающий запах — odor irritans;
• резкий запах — odor acerrimus;
• запах розы — odor rosarum;
• запах свежего сена — odor feni recentis;
• свежий запах — odor egelidus;
• своеобразный запах — odor peculiaris (proprius);
• сельдяной запах — odor alecis;
• сильный запах — odor fortis;
• запах скипидара — odor terethinae;
• сладковатый запах — odor subdulcis;
• смолистый запах — odor resinosus;
• специфический запах — odor peculiaris (proprius);
• спиртовый запах — odor alcoholicus;
• стойкий запах — odor firmus;
• тошнотворный запах — odor nauseosus;
• трупный запах — odor cadaverinus;
• тяжёлый запах — odor gravis (onerosus);
• удушливый запах — odor suffocans;
• характерный запах — odor proprius (peculiaris);
• уксусный запах — odor acetatus;
• чесночный запах — odor alliaceus;
• ядовитый запах — odor virulentus;
• распространять запах — odorem emittere (exhalare, spargere, spirare);
• без запаха — inodorus;
• с запахом — odoratus;
• с приятным запахом — suaveolens;
• с сильным запахом — graveolens, fragrans;
• запах пота — capra;
• запах изо рта — gravitas (foetor) oris;
10 Насморк
• страдающий насморком — gravedinosus;
• подхватить насморк — gravedinem contrahere;
Острый лейкоз — Острый лейкоз клональное (онкологическое) заболевание, первично возникающее в костном мозге в результате мутации стволовой клетки крови. Следствием мутации является потеря потомками мутировавшей клетки способности к дифференцировке до… … Википедия
Острый миелоидный лейкоз — Мазок костного мозга при остром миелоидном лейкозе . Стрелками обозначены Тельца Ауэра … Википедия
Лейкоз — Микропрепарат костного мозга больного острой В лимфоцитарной лейкобластной лейкемией … Википедия
ЛЕЙКОЗ — (лейкемия белокровие), опухолевые заболевания кроветворной ткани с поражением костного мозга и вытеснением нормальных ростков кроветворения, увеличением лимфатических узлов и селезенки, изменениями в картине крови и другими проявлениями.… … Большой Энциклопедический словарь
ЛЕЙКОЗ ОСТРЫЙ — мед. Острый лейкоз злокачественное заболевание кроветворной системы; морфологический субстрат властные клетки. Частота. 13,2 случаев на 100000 населения среди мужчин и 7,7 случаев на 100 000 населения среди женщин. Классификация и эпидемиология.… … Справочник по болезням
лейкоз — а; м. [от греч. leukos белый] Мед. = Лейкемия. Больной лейкозом. Л. излечим. ◁ Лейкозный, ая, ое. Л. больной. * * * лейкоз (лейкемия, белокровие), опухолевые заболевания кроветворной ткани с поражением костного мозга и вытеснением нормальных… … Энциклопедический словарь
лейкоз — прогрессирующее размножение патологически измененных (незрелых) лейкоцитов, обнаруживаемых в повышенном количестве в кроветворной ткани, других органах и циркулирующей крови; классифицируют в зависимости от преобладающего типа клеток и по… … Медицинские термины
лейкоз — ЛЕЙКОЗ, а, м Спец. Заболевание кровеносной системы, проявляющееся в возникновении опухолей кроветворной ткани и в патологическом изменении состава крови; Син.: лейкемия. Причиной смерти оказался острый лейкоз … Толковый словарь русских существительных
лейкоз недифференцируемый — острый Л., морфологический субстрат которого представлен гистологически и гистохимически не дифференцируемыми бластными клетками … Большой медицинский словарь
ЛЕЙКОЗ — мед. Лейкоз (лейкемия) системное заболевание крови, характеризующееся замещением нормального костномозгового кроветворения пролиферацией менее дифференцированных и функционально активных клеток ранних предшественников клеток лейкоцитарного ряда.… … Справочник по болезням
лейкоз олигобластный — (l. oligoblastica) см. Лейкоз острый малопроцентный … Большой медицинский словарь
лейкоз тлеющий — см. Лейкоз острый малопроцентный … Большой медицинский словарь
Лейкоз — (от греч. leukós белый) лейкемия, белокровие, опухолевое системное заболевание кроветворной ткани. При Л. происходит нарушение кроветворения (См. Кроветворение), выражающееся в разрастании незрелых патологических клеточных элементов как в … Большая советская энциклопедия
лейкоз лимфобластный — (l. lymphoblastica; син. лимфолейкоз острый) острый Л., морфологический субстрат которого представлен лимфобластами … Большой медицинский словарь
лейкоз миелобластный — (l. myeloblastica; син. миелолейкоз острый) острый Л., морфологический субстрат которого представлен миелобластами … Большой медицинский словарь
лейкоз мегакариобластный — (l. megacaryoblastica) острый Л., морфологический субстрат которого представлен мегакариобластами и не дифференцированными бластными клетками … Большой медицинский словарь
Острый миелоидный лейкоз ( ОМЛ ) является раком из миелоидной линии клеток крови , характеризуется быстрым ростом аномальных клеток , которые накапливаются в костном мозге и крови и мешают нормальным клетки крови . Симптомы могут включать в себя чувство усталости, затрудненное дыхание , легко кровоподтеки и кровотечения, а также повышенный риск инфекции . Иногда распространение может произойти в мозг, кожу или десны. Как острый лейкоз , ПОД быстро прогрессирует , и , как правило , со смертельным исходом в течение нескольких недель или месяцев , если его не лечить.
Факторы риска включают курение , предыдущий курс химиотерапию или лучевую терапию , миелодиспластический синдром , и воздействие химического бензола . Основной механизм включает в себя замену нормального костного мозга с лейкозных клеток , что приводит к падению эритроцитов , тромбоцитов и нормальных белых кровяных клеток . Диагноз , как правило , основан на аспирации костного мозга и специфических анализов крови . AML имеет несколько подтипов , для которых лечение и результаты могут отличаться.
БОД , как правило , сначала обрабатывают химиотерапии , с целью индукции ремиссии . Люди могут затем перейти на прием дополнительной химиотерапии, лучевой терапии , или трансплантация стволовых клеток . Специфические генетические мутации , присутствующие в раковых клетках могут вести терапию, а также определить , как долго этот человек, скорее всего , чтобы выжить. Триоксид мышьяка может быть судимым в тех случаях , которые повторялись следующие обычные методы лечения.
В 2015 году, AML пострадало около одного миллиона людей , и в результате 147000 смертей во всем мире. Это наиболее часто встречается у пожилых людей. Мужчины страдают чаще , чем женщины. AML излечит примерно 35% человек в возрасте до 60 лет и 10% старше 60 лет. Пожилые люди , чье здоровье слишком бедна для интенсивной химиотерапии имеют типичную выживание 5-10 месяцев. Это составляет примерно 1,8% случаев смерти от рака в Соединенных Штатах.
содержание
- 1 Признаки и симптомы
- 2 Факторы риска
- 2.1 Другие заболевания крови
- 2.2 Химическое воздействие
- 2.3 Излучение
- 2.4 Генетика
- 3 Диагностика
- 3,1 Всемирная организация здравоохранения
- 3,2 франко-американо-британская
- 4 патофизиологии
- 5 Лечение
- 5,1 Индукционная
- 5.2 Консолидация
- 5,3 рецидивом AML
- 6 Прогноз
- 6.1 Цитогенетика
- 6.2 миелодиспластический синдром
- 6.3 Другие прогностические маркеры
- 6.3.1 Генотип
- 6,4 Expectation отвердения
- 6,5 Рецидив
- 7 Эпидемиология
- 8 История
- 9 Беременность
- 10 Ссылки
- 11 Внешние ссылки
Признаки и симптомы

Большинство признаков и симптомов ПОД вызваны замены нормальных клеток крови с лейкозных клеток. Отсутствие нормального производства белых клеток крови делает человек более восприимчивыми к инфекциям; в то время как лейкозных клеток сами являются производными от белых клеток - предшественников крови, они не имеют возможности борющиеся с инфекцией. Снижение количества эритроцитов ( анемия ) может вызвать усталость, бледность, и одышку. Недостаток тромбоцитов может привести к легкой помятости или кровотечение с незначительными травмами.
Ранние признаки ПОД часто расплывчаты и неспецифические, и могут быть аналогичны гриппа или других распространенных заболеваний. Некоторые обобщенные симптомы включают лихорадку , усталость , потерю веса или потерю аппетита , одышку , анемии, легко помятости или кровотечение, петехии (плоские, размер пятна контактной головки под кожей , вызванное кровотечением), костьми и боли в суставах, и стойкой или частые инфекции .
Увеличение селезенки может произойти в ОМЛ, но это , как правило , мягкая и бессимптомно . Лимфоузлов отек редко в ОМЛ, в отличие от острого лимфобластного лейкоза . Кожа участвует около 10% времени в форме лейкоза кутиса . Редко, синдром Свита , паранеопластическое воспаление кожи, может произойти с ОМЛ.
Некоторые люди с ОМЛ могут возникнуть отек десен из - за проникновения лейкозных клеток в ткани десен. Редко, первый признак лейкемии может быть развитие твердых лейкозных массы или опухоли за пределами костного мозга , называется хлорлейкоз . Иногда человек не может показать никаких симптомов , и лейкемии могут быть обнаружены случайно во время обычного анализа крови .
Факторы риска
Целый ряд факторов риска для развития ОМЛ были выявлены, в том числе: другие заболевания крови, воздействию химических веществ, ионизирующего излучения, и генетики.
Воздействие противораковой химиотерапии , в частности , алкилирующих агентов , может увеличить риск впоследствии развивающихся ОМЛ. Риск является самым высоким от трех до пяти лет после химиотерапии. Другие химиотерапевтические агенты, в частности , Эпиподофиллотоксины и антрациклины , также были связаны с связанным с лечением лейкозов, которые часто связаны с конкретными хромосомными аномалиями в лейкозных клетках.
Профессиональные химического воздействия бензола и других ароматических органических растворителей является спорным в качестве причины AML. Бензол и многие из его производных , как известно, канцерогенный в пробирке . Хотя некоторые исследования показали связь между профессиональным воздействием бензола и повышенным риском развития ОМЛ, другие предложили приходящейся риск, если таковые имеются, незначителен.
Высокое количество ионизирующего излучения воздействия может увеличить риск ОМЛ. Выжившие атомных бомбардировок Хиросимы и Нагасаки было увеличение скорости ОМЛ, как и радиологов подвергаются воздействию высоких уровней рентгеновских лучей до принятия современных методов радиационной безопасности. Люди , получавшие ионизирующей радиации после лечения рака предстательной железы , неходжкинской лимфомы , рака легких и рака молочной железы имеют высокие шансы на приобретение ОМЛ, но это увеличило доходность риска на фоне риска , наблюдаемого в общей популяции после 12 лет.
Наследственный риск ОМЛ , как представляется , существует. Несколько случаев ОМЛ развивающихся в семье со скоростью выше , чем прогнозировалось случайно в одиночку поступало. Некоторые врожденные условия могут увеличить риск лейкемии; наиболее распространенным является , вероятно , синдром Дауна , что связано с увеличением от 10 до 18-кратного в риске AML. Во втором примере, инактивирующая мутацию в одном из двух родительских GATA2 генов приводят к снижению, т.е. гаплонедостаточности , в клеточных уровнях продукта гена, в GATA2 факторе транскрипции , и тем самое к редкому аутосомно - доминантной генетической болезни , GATA2 дефицит , Это заболевание связано с очень изменчивым набором заболеваний , включая чрезвычайно высокий риск развития ОМЛ. Специфические генетические аномалии , вызывающие ОМЛ обычно варьируются в зависимости от тех , кто развивает болезнь , как ребенок по сравнению с взрослыми. Однако GATA2 дефицит индуцированных AML может сначала появиться у детей и взрослых.
диагностика
Первый ключ к диагностике ОМЛ , как правило , аномальный результат на полный анализ крови . В то время как избыток аномальных белых клеток крови ( лейкоцитоз ) является частая находка с лейкемией и лейкозных взрывы иногда видели, БОД может также представить с изолированными уменьшается в тромбоцитов , красных кровяных клеток , или даже с низким лейкоцитов в крови ( лейкопения ). В то время как предполагаемый диагноз ОМЛ может быть сделано путем исследования периферической мазка крови , когда циркулируют лейкозных бластов, окончательный диагноз обычно требует адекватной аспирации костного мозга и биопсии , а также исключает пернициозной анемии (дефицит витамина В12), фолиевую кислоту дефицит и дефицит меди .
Костный мозг или крови исследовались под световым микроскопом , а также метод проточной цитометрии , чтобы диагностировать наличие лейкоза, дифференцировать ОМЛ от других типов лейкемии (например , острый лимфобластный лейкоз - ALL) и классифицировать подтип заболевания. Образец костного мозга или крови , как правило , также протестирован на хромосомные аномалии с помощью обычной цитогенетики или флуоресцентного места в гибридизации . Генетические исследования также могут быть выполнены , чтобы искать специфические мутации в генах , такие как FLT3 , нуклеофозмин и KIT , которые могут повлиять на исход заболевания.
Цитохимические пятна на крови и костного мозга мазков полезны в отличие ОМЛ от всех, и в подклассы ОМЛ. Сочетание миелопероксидазы или Судан черного пятна и неспецифической эстераза пятна обеспечит нужную информацию в большинстве случаев. Миелопероксидазы или Судан черных реакции являются наиболее полезными в установлении личности БОДА и отличающей его от всех. Неспецифические эстеразы пятно используются для идентификации моноцитов компоненты в AMLs и отличить плохо дифференцированный монобластный лейкоз от ALL.
Диагностика и классификация AML может быть сложной задачей, и должна выполняться квалифицированным hematopathologist или гематологу . В простых случаях, наличие определенных морфологических особенностей (такие как Auer стержни ) или конкретных проточной цитометрии результатов можно выделить ПОД от других лейкозов; однако, при отсутствии таких признаков, диагноз может быть более трудным.
Из - за острым промиелолейкоз (АПЗ) имеет самую высокую излечимость и требует уникальной формы лечения, важно быстро установить или исключить диагноз этого подтипа лейкемии. Флуоресцентное место в гибридизации , выполненной на крови или костный мозге часто используются для этой цели, так как он легко идентифицирует транслокации хромосомных [T (15; 17) (q22; q12);] , который характеризует АПЗ. Существует также необходимость в молекулярно обнаружить присутствие PML / RARA слитого белка, который является онкогенным продуктом этой транслокации.
ВОЗ 2008 классификация острого миелоидного лейкоза попытки быть более клинически полезным и для получения более значимую прогностическую информацию , чем FAB критериев. Каждая из категорий ВОЗ содержит многочисленные описательные подкатегорий , представляющие интерес для hematopathologist и онколога ; Однако, в большинстве случаев клинически значимой информации в схеме ВОЗ передается по категоризации в один из подтипов , перечисленных ниже.
Подтипы ВОЗ по борьбе с отмыванием денег, являются:
Острые лейкозы неоднозначной линии (также известный как смешанный фенотип или бифенотипический острой лейкемии ) возникают , когда лейкозные клетки не могут быть классифицированы как либо миелоидной или лимфоидных клеток, или там , где оба типа клеток присутствуют.
Классификация франко-американо-британская (FAB) система делит ОМЛ на восемь подтипов, М0 до М7, в зависимости от типа клеток , из которых лейкоз развитом и степень его зрелости. Это делается путем изучения появления злокачественных клеток с световой микроскопией и / или с помощью цитогенетических , чтобы охарактеризовать любые основные хромосомные аномалии. Подтипы имеют различные прогнозы и ответы на терапию. Несмотря на то, классификации ВОЗ (смотри выше) , может быть более полезным, все еще широко используется система ФАБ.
Шесть FAB подтипов (M1 до M6) первоначально были предложены в 1976 году, хотя более поздние изменения добавлены M7 в 1985 году и M0 в 1987 году.
| Тип | название | Цитогенетика | Процент взрослых с ОМЛ |
|---|---|---|---|
| M0 | острый миелобластный лейкоз, минимально дифференцированы | 5% | |
| M1 | острый миелобластный лейкоз без созревания | 15% | |
| M2 | острый миелобластный лейкоз, с гранулоцитарным созреванием | т (8; 21) (q22; q22), т (6; 9) | 25% |
| M3 | промиелоцитарный или острый промиелолейкозе (АПЗ) | т (15; 17) | 10% |
| M4 | острый миеломоноцитарный лейкоз | INV (16) (p13q22), дель (16q) | 20% |
| M4eo | миеломоноцитарный вместе с костным мозгом эозинофилией | INV (16), т (16; 16) | 5% |
| M5 | острый лейкоз монобластный (M5A) или острый моноцитарный лейкоз (M5B) | дель (11q), т (9, 11), т (11; 19) | 10% |
| M6 | острые эритроидных лейкозы , в том числе эритролейкемии (M6A) и очень редко чистый эритроидного лейкоза (M6B) | 5% | |
| M7 | острый мегакариобластный лейкоз | т (1; 22) | 5% |
Морфологические подтипы ПОД включают также редкие виды , не включенные в системе FAB, такие как острая базофильная лейкемия , которая была предложена в качестве девятого подтипа, M8, в 1999 году.
патофизиология
Большая часть разнообразия и неоднородности ОМЛА происходит потому, что лейкозная трансформация может происходить в несколько различных шагах вдоль пути дифференцировки. Современные схемы классификации для AML признают, что характеристики и поведение лейкозных клеток (и лейкемии) могут зависеть от стадии, на которой была приостановлена дифференциация.
Эти клинические признаки и симптомы ОМЛИ в результате роста лейкозных клеток клона, который имеет тенденцию вытеснять или препятствовать развитию нормальных клеток крови в костном мозге. Это приводит к нейтропении , анемии и тромбоцитопении . Симптомы ОМЛ, в свою очередь, часто из - за низкого числа этих нормальных элементов крови. В редких случаях люди с ОМЛ могут разработать хлоромы или солидную опухоль лейкозных клеток вне костного мозга, которые могут вызывать различные симптомы , в зависимости от его расположения.
Важный патофизиологический механизмом возникновения и развитие лейкоза в ОМЛ является эпигенетической индукцией дедифференциации по генетическим мутациям , которые изменяют функцию эпигенетических ферментов, такие как ДНК деметилаза TET2 и метаболические ферменты IDH1 и IDH2, которые приводят к образованию романа oncometabolite, D -2-hydroxyglutarate, который ингибирует активность эпигенетических ферментов , такие как TET2. Гипотеза состоит в том, что такие эпигенетические мутации приводят к молчанию генов - супрессоров опухолей и / или активации протоонкогенов.
лечение
Первая линия лечения ОМЛ состоит в основном из химиотерапии , и разделен на две фазы: индукция и postremission (или консолидации) терапии. Цель индукционной терапии является достижение полной ремиссии за счет уменьшения количества лейкозных клеток к неопределяемого уровня; целью консолидации терапии является устранение любого остаточного незаметного заболевания и достичь излечения. Трансплантации гемопоэтических стволовых клеток, как правило , считается , если индукция химиотерапии не удается или после того, как человек , рецидивы, хотя трансплантация также иногда используется в качестве терапии первой линии для людей с заболеванием высокого риска. Попытки использовать ингибиторы тирозинкиназы в ОМЛ продолжают.
М3 подтип AML, известный также как острый промиелолейкозе (APL), почти повсеместно обрабатывают препарат All - транс - -retinoic кислоты ( ATRA ) в дополнении к индукционной химиотерапии, обычно антрациклин. Необходимо соблюдать осторожность , чтобы предотвратить диссеминированный внутрисосудистое свертывание крови ( ДВС ), что затрудняет лечение APL , когда промиелоциты освободить содержимое своих гранул в периферическое кровообращение. APL в высшей степени излечим, с хорошо документированных протоколов лечения.
Целью фазы индукции является достижение полной ремиссии. Полная ремиссия не означает, что заболевание было вылечить; скорее, это означает не болезнь может быть обнаружена с имеющимися диагностическими методами. Полная ремиссия достигается примерно в 50% -75% вновь выявленных взрослых, хотя это может варьироваться в зависимости от прогностических факторов, описанных выше. Продолжительность ремиссии зависит от прогностических особенностей исходной лейкемии. В общем, вся ремиссия потерпит неудачу без дополнительной консолидирующей терапии.
Даже после того, как полная ремиссия достигнута, лейкозные клетки, вероятно, останутся в числе слишком малы, чтобы быть обнаружено с современными методами диагностики. Если нет дальнейшего postremission или консолидирующей терапии не даются, почти все люди с ОМЛ, в конечном счете рецидив. Таким образом, более терапии необходимо исключить невыявляемый заболевания и предотвратить рецидивы - то есть, чтобы достичь излечения.
Конкретный тип postremission терапии индивидуализирован на основе прогностических факторов человека (см выше) и общее состояние здоровья. Для хорошего прогноза лейкозов (т.е. и (16), т (8, 21) и т (15; 17)), люди, как правило , проходят дополнительные три-пять курсов интенсивной химиотерапии, известную как консолидирующая химиотерапия. Для людей с высоким риском рецидива (например , те , с цитогенетике высокого риска, лежащих в основе МДС, или терапии , связанных с ОМЛ), аллогенной трансплантации стволовых клеток , как правило , рекомендуется , если человек находится в состоянии терпеть пересадку и имеет подходящий донор. Лучший postremission терапия для ОМЛ промежуточного риска (нормальные цитогенетики или цитогенетические изменения , не входящие в группы хорошего риска или высокого риска) менее ясна и зависит от конкретной ситуации, в том числе возраст и общее состояние здоровья человека, ценности этого лица , и является ли подходящим стволовыми клетки доступен донор.
Для людей , которые не имеют права на трансплантации стволовых клеток, иммунотерапия с комбинацией гистамина дигидрохлорида ( Ceplene ) и интерлейкина 2 (Пролекин) после завершения консолидации было показано , чтобы уменьшить абсолютный риск рецидива на 14%, перевод на 50 % увеличение вероятности поддерживается ремиссия.
Для людей с рецидивами ОМЛ, только проверенные потенциально лечебной терапии является кроветворной трансплантации стволовых клеток , если она еще не была выполнена. В 2000 году моноклональное антитело -связанной цитотоксический агент гемтузумаб озогамицина (Mylotarg) был утвержден в Соединенных Штатах для людей в возрасте более 60 лет с рецидивом ОМЛ которые не являются кандидатами для высокодозной химиотерапии. Этот препарат был добровольно отозван с рынка его изготовителем, Pfizer в 2010 году, но новые данные способствовали ее вновь в 2017 году.
Поскольку варианты лечения рецидивирующей ОМЛ настолько ограничены, паллиативная помощь или регистрация в клиническом испытании может быть предложена.
Для рецидива острого промиелоцитарного лейкоза (APL), триоксид мышьяка одобрен FDA США . Как ATRA, триоксид мышьяка не работает с другими подтипами ОМЛ.
Читайте также:


