Остеопластические материалы при кистах

Главной задачей хирургического лечения околокорневых кист челюстей является сохранение зубов, расположенных в зоне кисты, и восстановление их функции. Основным методом оперативного лечения, по мнению некоторых авторов [1, 4], остается цистоэктомия с одномоментной резекцией верхушки корня причинного зуба. Данное вмешательство показано при погружении корня зуба в полость кисты не более чем на 1/3 его длины. Более глубокое погружение корня в полость кисты делает такие зубы непригодными в функциональном отношении и приводит к ранней их потере. Кроме того, после удаления околокорневых кист остаются костные полости, которые снижают прочность челюстных костей и могут вызывать функциональные и эстетические нарушения [2, 5].
За последние полвека лечение кист практически не изменилось, хотя в нем и появились некоторые новые направления. Так, для предотвращения ранних осложнений при цистэктомии костную полость после удаления оболочки стали заполнять биокомпозиционными материалами. Это связано с тем, что при стандартном оперативном вмешательстве имеет место сокращение кровяного сгустка, и это зачастую приводит к инфицированию костной полости и последующим осложнениям. Сегодня в современной хирургической стоматологии и челюстно-лицевой хирургии достаточно широко используются различные остеорепаративные средства.
Поэтому заполнение костного дефекта челюстных костей биокомпозиционными материалами после цистэктомии направлено на предотвращение возможных осложнений, связанных с сокращением и распадом кровяного сгустка, а также вторичным инфицированием раны; ускорением регенерации костной ткани в области дефекта и восстановлением формы и функции челюстных костей.
Однако в современной литературе имеется немного работ, посвященных сравнительному изучению влияния остеопластических препаратов на динамику остеогенеза и заживления костных ран при оперативном лечении одонтогенных кист челюстей. Подобное исследование, выполненное в эксперименте на животных и в клинических условиях, представляется актуальным и своевременным способом совершенствования хирургической стоматологической помощи [3].
Цель исследования – повышение эффективности хирургического лечения больных с одонтогенными кистами челюстей путем обоснованного выбора остеорепаративных средств коллапана и обогащенной тромбоцитами плазмы крови для пластики различных по размеру костных дефектов.
Материалы и методы исследования
Собственные клинические исследования проведены у 210 больных с радикулярной кистой верхней и нижней челюсти. Мы в качестве средства, стимулирующего остеогенез, использовали аутогенную плазму крови (фракция крови, состоящая помимо тромбоцитов из лейкоцитов и белков фибринной группы (F.R.P.) и биоактивный материал коллапАн-Л с дополнением к лечению препарата Кальций–Д3 Никомед. Оперативное лечение радикулярной кисты челюстей с резекцией верхушки корня зуба и цистэктомией при диаметре костных полостей от 0,5 до 1 см произведено у 130 больных, при диаметре больше 1 см – у 80 больных, возраст от 19 до 45 лет. Сравнение сроков регенерации костной ткани в области дефекта позволило установить уровень остеоинтеграции после использования каждого препарата, тяжесть послеоперационного периода. Все больные были разделены на 3 группы соответственно остеопластическому материалу, используемому для заполнения послеоперационного костного дефекта после цистэктомии (таблица).
Клиническое обследование проводилось по общепринятой стандартной схеме. Учитывали данные анамнеза, включая выяснение жалоб, развития настоящего заболевания, наличия и отсутствия сопутствующей патологии.
1-я группа сравнения – 50 больных, у которых послекистозная костная полость заживала путем трансформации кровяного сгустка.
2-я группа основная – 90 больных, ход операции как при классической цистэктомии, послеоперационная костная полость (диаметр костной полости от 0,5 до 1 см) заполнялась препаратом – коллапАн-Л. Использование стимулирующего биоактивного материала коллапАн-Л с целью оптимизации процесса заживления костных ран, выявления новых возможностей для повышения их регенерационной способности, восстановления ткани. В качестве стимулирующего регенерацию костной ткани назначался препарат Кальций-Д3 Никомед, а также физиотерапия и полоскание антисептическим средством.
3-я группа основная – 70 больных, у которых послеоперационная костная полость от 1 до 2 см заполнялась F.R.P. аутокровью и коллапАном. Большие костные полости, дефекты костной ткани невозможно восполнить консервативным лечением или простым хирургическим вмешательством. Поэтому для восстановления утраченной костной ткани применяются биоматериалы или их синтетические аналоги, которые могут заменить утраченную кость или оказать индуцирующее влияние на процессы регенерации.
При дефектах костной ткани, образующихся от радикулярной кисты челюстей диаметром более 1 см, репаративная регенерация костной ткани стимулируется путем заполнения костной полости аутогенной плазмой крови, обогащенной тромбоцитами (F.R.P.) и остеопластическими материалами на основе гидроксиапатита коллапАна.
Мы в качестве средства, стимулирующего остеогенез, использовали аутогенную плазму крови, кровь бралась непосредственно у самого больного в количестве 10–15 мл и на центрифуге, при 2600 оборотах в течение 15 минут, происходило отделение плазмы крови с тромбоцитами. Полученным сгустком заполнялась полость кисты с добавлением коллапАна и ушивалась. В качестве стимулятора регенерации костной ткани назначался препарат Кальций-Д3 Никомед, физиотерапия и полоскание антисептическим средством.
Динамический контроль процессов репаративной остеорегенерации проводили при помощи рентгеновского исследования на 1–2 сутки после операции и далее через 3, 6, 9, 12 месяцев.
Распределение больных в зависимости от вида использованного остеопластического материала
Использованный остеопластический материал
Всего прооперировано больных
F.R.P. аутокровью и коллапАном
Результаты исследования и их обсуждение
1 группа исследуемых ‒ прооперировано 50 больных: мужчин – 15 и женщин – 35, в возрасте от 19 до 55 лет. Было выполнено 35 операций на верхней челюсти и 15 на нижней челюсти. Всего удалено 40 околокорневых и 10 фолликулярных кист. Из них малых кист диаметром до 1 см ‒ у 36 больных, свыше 1 см ‒ у 14 больных. Произведено 47 резекций верхушек корней. Послеоперационная рана у 42 (84 %) больных зажила первичным натяжением. Швы сняты на 7–8 день после операции. Расхождение швов с последующим нагноением послеоперационной раны у больных с кистами до 1 см отмечено у 3 (6 %) человек, у больных с диаметром кист более 1 см – в 5 (10 %) случаях. Всего осложнений при традиционном лечении кист ‒ 16 %.
Больным с послеоперационными осложнениями назначали антибиотики, ежедневные орошения ран антисептическими растворами, ферментами, проводились физиотерапевтические процедуры. В результате интенсивного комплексного лечения раны зажили у всех больных вторичным натяжением. При контрольном осмотре больные жалоб не предъявляли, послеоперационные рубцы были малозаметными и безболезненными. Производился рентгенологический контроль через 1, 3, 6 и 12 месяцев, по результатам было установлено, что регенерация кости в послеоперационных полостях происходит интенсивно, контуры дефекта становятся расплывчатыми. Через несколько месяцев, максимум через год, новообразованная кость в послеоперационных дефектах у кист размером до 1 см приближается по своей структуре к нормальной окружающей костной ткани. На рентгенограммах новообразованные участки кости при дефектах до 1 см, сохраняются очаги затемнения, структура кости носит мелкопетлистый рисунок. Что же касается костных дефектов размером более 1 см в диаметре, особенно в больших кистах, происходит лишь частичное возмещение послеоперационной полости костным регенератом.
Таким образом, результаты лечения кист контрольной группы, в которой заживление костной полости происходит под кровяным сгустком, вполне удовлетворительные не только при кистах диаметром до 1 см, но и более 1 см. Вместе с тем, следует отметить значительное число осложнений (16 %), а также замедленную и несовершенную регенерацию костных послеоперационных дефектов.
2 группа исследуемых ‒ 90 больных: мужчин – 28 и женщин – 62, в возрасте от 19 до 64 лет. Операция выполнялась традиционным способом, после чего послеоперационный костный дефект размером от 0,5 до 1 см заполнялся препаратом коллапан. Было выполнено 70 операций на верхней челюсти и 20 на нижней челюсти. Всего удалено: 87 околокорневых и 3 фолликулярных кист. У 3 больных киста верхней челюсти была с двух сторон. Произведено 90 резекций верхушек корней. В послеоперационный период больным назначался препарат Кальций-Д3 Никомед, физиотерапия и полоскание антисептическими средствами.
Послеоперационная рана у всех прооперированных больных зажила первичным натяжением. Швы сняты на 7–8 день после операции. Расхождение швов с последующим нагноением послеоперационной раны наступило у 2 больных. Больным с послеоперационными осложнениями, как и в предыдущей серии, назначали антибиотики, ежедневные орошения ран антисептическими средствами, ферментами, проводилось физиотерапевтическое лечение. В результате интенсивного, комплексного лечения раны зажили у всех больных вторичным натяжением. При контрольном осмотре больные жалоб не предъявляли, послеоперационные рубцы были малозаметными и безболезненными. Результаты лечения прослежены у 80 больных в сроки от 1 месяца до 2-х лет. Осложнения в послеоперационный период выявлены у 2 больных. На месте дефекта определяется плотная костная ткань. Зубы в пределах дефекта устойчивы. Рентгенологическим обследованием установлено, что активная регенерация костной ткани на месте бывшего дефекта начинается на втором месяце и уже через 3–6 месяцев контуры небольших дефектов до 0,5 см становятся малозаметными. Через 6 месяцев после операции местный статус без особенностей, пальпируется плотная костная ткань. На рентгенограмме послеоперационная кистозная полость заполнена новообразованной костью.
Таким образом, пломбировка кистозной полости обеспечивает хорошие ближайшие и отдаленные результаты хирургических вмешательств. Процессы формирования новообразованной костной ткани идут более активно. Однако полноценного возмещения кистозного послеоперационного дефекта при кистах диаметром более 1 см не происходит даже в течение года после хирургического вмешательства.
При осмотре через 1 месяц больные жалоб не предъявляли. На R-граммах определяются расплывчатые контуры костного дефекта. Через 3 месяца после удаления кист дефект уменьшился на 1/3. Контуры дефекта расплывчаты. Новообразованная костная ткань отчетливо определяется на периферии дефекта.
Через 6–9 месяцев костная полость дефекта средней величины заполнена на 2/3. Новообразованная кость интенсивно развивается в сторону верхушек корней прилегающих зубов и к центру полости. К 9–10 месяцу у большей части кист среднего размера наступало полное восстановление костных дефектов. Окончательное восстановление костных дефектов у больных этой группы отмечено через 1 год после операции.
Таким образом, исходя из результатов данного исследования, использование обогащенной аутогенной плазмы и биоактивного материала – коллапАна позволяет полностью закрыть большую полость, при этом степень репаративного остеогенеза не снижается, а дополнительное использование препаратов кальция способствует усилению процесса регенерации. У пяти (7,1 %) больных при контрольном осмотре через 1,5 года отмечено неполное восстановление костной полости (размер кисты более 2 см). У трех (4,2 %) больных отмечалось развитие воспалительных осложнений послеоперационной раны при контроле через 6 месяцев.
Дополнительное включение в процесс лечения стимулятора репаративной регенерации костной ткани – Кальций-Д3 Никомед, позволяет улучшить результаты лечения и снизить вероятность развития осложнений при одонтогенных кистах челюстей. Использование биокомпозиционных материалов на основе гидроксиапатита КоллапАн, способствует более активному течению регенерационных процессов в дефектах костной ткани, обуславливая энергетическое формирование в них соединительной ткани и на ее базе – костных структур. Заполнение послеоперационного дефекта композитным материалом положительно влияет на течение послеоперационного периода, что выражается в значительном уменьшении послеоперационного отека мягких тканей, отсутствии болевого синдрома, более низкой температурной реакции.
Рецензенты:
Осумбеков Б.З., д.м.н., профессор, зав. отделением хирургии № 2, Ошская межобластная объединенная клиническая больница, г. Ош;
Муратов А.А., д.м.н., координатор по хирургии Ошской области, г. Ош.

Рубрика: Медицина
Статья просмотрена: 1186 раз
В статье дан сравнительный анализ использования различных остеопластических материалов при оперативных лечениях радикулярных кист челюстей c последующим контролем степени регенерации костной ткани.
Ключевые слова: радикулярная киста, цистоэктомия, каллапан.
In article are reflected comparative analysis using different osteoplastic materials in surgical treatment of radicural cysts of the jaws with the following control of bone regeneration degree.
K eywords: radicular cyst, cystotomy, collapan.
Сохранение зубов, расположенных в зоне кисты, задача стоматолога при лечении околокорневых кист. Исходя из этой задачи, большое значение имеет материал, используемый для замещения дефектов челюстей после цистоэктомии. Известно, что результаты операций во многом зависят от свойств веществ, введенных в остеопластические композиции с целью стимулирования роста и минерализации костной ткани. Препараты, на основе гидроксиапатита и коллагена, отличаются наибольшей предсказуемостью, эффективностью, и широким диапазоном возможного применения.[1,2,3,4,5]
В современной литературе работ, посвященных изучению влияния остеопластических препаратов на динамику остеогенеза при оперативном лечении одонтогенных кист челюстей, имеется немного. Поэтому проведение исследований в этом направлении представляется актуальным и своевременным способом совершенствования хирургической стоматологической помощи.
Цель исследования. Сравнительная эффективность хирургического лечения больных с одонтогенными кистами челюстей при использовании различных остеорепаративных средств.
Материалы и методы исследования
Оперативное лечение радикулярной кисты челюстей с резекцией верхушки корня зуба и цистоэктомией при диаметре костных полостей от 0,5 см. до 1см. произведен у 110 больных, при диаметре больше 1см - у 70 больных, возраст от 19 до 45 лет. В качестве средства стимулирующего остеогенез использовали биоактивный материал коллапАн –Л, аутогенную плазму крови ( фракция крови состоящая помимо тромбоцитов, из лейкоцитов и белков фибринной группы F . R . P .) с дополнением препарата Кальций–Д3 Никомед, и под кровяным сгустком Сравнение сроков регенерации костной ткани в области дефекта позволило установить уровень остеоинтеграции после использования каждого препарата, тяжесть послеоперационного периода. Все больные были разделены на 3 группы соответственно остеопластическому материалу, используемому для заполнения послеоперационного костного дефекта после цистоэктомии. Обследование проводилось по стандартной схеме, включая выяснение жалоб, анамнеза, развития настоящего заболевания, наличия и отсутствия сопутствующей патологии. 1-я группа сравниваемая – 50 больных, у которых послекистозная костная полость заживала путем трансформации кровяного сгустка. У этой группы больных проводилась антибактериальная терапия и физиотерапия; полоскание полости рта антисептическим раствором без назначения препарата Кальций-Д3 Никомед. 2-я группа - основная – 80 больных, у которых костная полость (диаметр от 0,5 до 1см.) заполнялась препаратом - коллапАн. 3-я группа - основная -50 больных, у которых послеоперационная костная полость (от 1 до 2см.) заполнялась F . R . P . аутокровью и коллапАном. Второй и третьей группам больных назначались препараты Кальций-Д3 Никомед, физиотерапия и полоскание антисептическим средством. Швы у всех групп снимались на 7-8 сутки после операции. Проводилось динамическое наблюдение больных с рентгенологическим исследованием через 3, 6, 12месяцев. Для оценки плотности костной ткани до и после оперативного вмешательства использовали эходенситометрию (ЭДМ). При подготовке больных к операции проводили общее клиническое обследование включающее анализ крови и мочи. Статистическая обработка полученных данных проведена на основании общепринятых методов вариационной статистики по Стьюденту.
Результаты исследование и их обсуждения
При классической цистоэктомии (1-я группа) рентгенологическое исследование показало, что после операции с ведением раны по традиционной методике (кровяный сгусток) восстановление костной ткани в области дефекта происходит более медленно, с частым инфицированием и воспалением. Это является основанием к дополнительному использованию средств, снижающих риск развития воспалительных осложнений (антибиотики, витаминотерапия и др.). Результаты лечения этой группы больных, по данным рентгенологического исследования через полгода и год после операции, показывают значительное уменьшение размеров костного дефекта, но без полного восстановления костной ткани P >0,005. Через год после операции на рентгенограммах определялся дефект костной ткани, контуры дефекта не четкие, по краям дефекта видны костные баллочки, свидетельствующие о протекающем процессе регенерации костной ткани. Послеоперационное течение у больных данной группы проходило без выраженных болевых и температурных реакций 56,2%, однако у 34,8% пациентов мы наблюдали длительно сохранявшийся отек и гиперемию мягких тканей, даже на 5-6 сутки после операции, несмотря на проводившееся терапевтическое (антибактериальное) лечение, отмечено осложнение у 6-ти больных – повторный рецидив кисты (составляет 20%).
Использование костного материала в стоматологии широко распространено. С его помощью удается выполнять остеопластику – восстанавливать утраченный объем альвеолярного гребня. Это позволяет избежать дальнейшее разрушение костной ткани и появления ряда негативных последствий, которые возникают на фоне изменения внешнего вида и ухудшения здоровья человека. Часто к процедуре прибегают перед установкой имплантатов, когда костной ткани пациента не хватает. Рассмотрим подробнее специфику материалов, позволяющих провести данные мероприятия.
Характеристика костнопластического материала в стоматологии
Остеопластические материалы в хирургической стоматологии должны быть высокого качества, обладать следующими характеристиками:

- безопасностью для здоровья человека (использование искусственной костной ткани, способной нанести вред состоянию организма, запрещено);
- высокой эффективностью;
- пористостью (обеспечивает прорастание новой костной ткани);
- полной совместимостью с тканями, в которые будут имплантированы материалы;
- избавлением костной ткани от дефекта за счет его заполнения.
В настоящее время на рынке представлено множество видов остеопластических материалов. При выборе наиболее подходящего материала надо учитывать все вышеуказанные характеристики. Кроме того, он должен быть готов к незамедлительному использованию, иметь высокие показатели адгезии, чтобы имплантат с его помощью максимально прилегал к кости.
Классификация остеопластических материалов
Остеопластические материалы представляют собой имплантаты, способствующие формированию кости. При этом они обеспечивают локальную остеокондуктивную, остеоиндуктивную или остеогенную активность. В соответствии с происхождением все остеопластические материалы разделяют на четыре основные группы:
- аутогенные (донором выступает пациент);
- аллогенные (донором является другой человек);
- ксеногенные (донором выступает животное);
- синтетические (выполнены на основе солей кальция).
Рассмотрим подробнее особенности каждой группы в отдельности.

Аутогенный костнозамещающий материал в стоматологии используют чаще остальных. Аутокость получают путем забора с донорского внутриротового или внеротового участка с последующей пересадкой в принимающий участок. В ходе ряда клинических исследований было доказано, что он способствует ускоренному замещению послеоперационных и других костных дефектов новообразованной тканью. Он характеризуется пластичностью, не обладает свойствами иммунной несовместимости. При этом финансовые затраты, связанные с его забором, небольшие.
В соответствии с происхождением различают два вида – эндохондрального (хрящевого) и эктомезенхимального (мебранного) происхождения. Среди недостатков можно отметить вероятность инфицирования, травматичность получения аутоматериала и долгую продолжительность самого оперативного вмешательства. Зачастую аутокость применяют в сочетании с иными материалами, к примеру, аллокостью или ксенокостью. Это позволяет избежать усадки аутокости
Аллогенный костный материал для синус лифтинга в РФ в соответствии с законодательством не применяют. Аллогенные имплантаты представляют собой костнопластические материалы, которые получают из человеческих трупов, в последствие, подвергая специальной обработке. Это может быть кортикальная и губчатая часть подвздошной кости или аллоимплантат деминерализованной лиофилизированной кости. К основным достоинствам данной группы в сравнении с аутоматериалами относятся:
- ярко-выраженный остеоиндуктивный потенциал;
- отсутствие травматичности при получении материала;
- хорошая адгезия к реципиентному ложу;
- короткая продолжительность проведения оперативного вмешательства;
- хорошая микро- и макропористая структура (гарантирует быстрый ангиогенез).
Помимо этических проблем к недостаткам применения данных материалов относят вероятность возможного инфицирования реципиентов ВИЧ-инфекцией и гепатитом.

В крайне редких случаях специалисты прибегают к использованию ксеногенного костного материала для имплантации. Он обладают остеокондуктивными свойствами, сохраняет исходную минеральную структуру кости. Ксенокость (природный гидроксиапатит) получают из костной ткани млекопитающих. Структура костей животных идентична кости человека, что позволяет их использовать в стоматологической практике. Ксенокость предварительно подвергают специальной обработке и деантигенизации. Это позволяет устранить из ее состава все факторы, провоцирующие развитие иммунологической и аллергической реакции.
В зависимости от типа обработки различают ксеноматериалы с низкотемпературной обработкой, ксеноматериалы с высокотемпературной обработкой и ксеноматериалы на основе энзимных технологий. Различают два основных метода деантигенизации. Самый эффективный и популярный – термическая обработка при повышенной температуре (около 700-1000 С°), после которой все органические вещества испаряются. Ксенокость не дает усадку. За счет синхронности процессов разрушения и восстановления костной возникает физиологическое замещение искусственных костных гранул натуральной костью, без утраты объема.
Синтетический костный материал выполнен на основе солей кальция. В особо сложных клинических случаях, когда требуется наращивать большие объемы кости в горизонтальном или вертикальном направлении, ксеногенная костная ткань сочетают с аутогенной костью в равных соотношениях. Синтетика является достойной альтернативой ауто-, алло- и ксеноматериалам. По некоторым признакам они превосходят остеопластические материалы натурального происхождения (к примеру, отсутствует необходимость забора костной ткани, исключена вероятность заражения инфекционными патологиями).
Главным недостатком большинства синтетических материалов в сравнении с ауто-, алло- и ксеноматериалами, является отсутствие свойств остеоиндукции (способности вызывать эктопическое формирование костной ткани). В том случае, если в их состав добавить компоненты, которые будут стимулировать регенерацию костной ткани (к примеру, коллагена), они способны приобрести остеоиндуктивные свойства.
Необходимые процедуры перед увеличением костной ткани
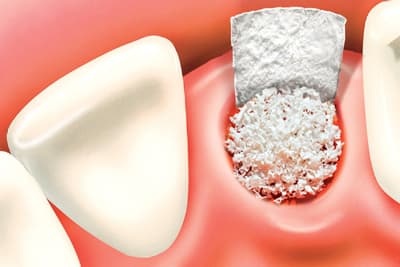
После устранения моляра или премоляра на кость больше не оказывается регулярная нагрузка, что со временем приводит к ее атрофии и утрате объема. Наряду с этим появляются воспалительные процессы в пародонтальной ткани. В результате, чем больше дней проходит после утраты моляра или премоляра, тем сильнее кость начинает испытывать дефицит. На этом фоне становится намного сложнее провести имплантацию.
Методика, к которой прибегают для увеличения объема костной ткани, в каждом клиническом случае подбирают в индивидуальном порядке. Для этого врач-стоматолог предварительно оценивает ротовую полость и при необходимости назначает инструментальную диагностику. Зачастую случается, что необходимость в применении другой методики возникает только в период проведения оперативного вмешательства. За счет этого специалист должен быть осведомлен обо всех разновидностях остеопластики и уметь применять их на практике.
Разновидность остеопластики
Ниже представлены основные виды остеопластики, чтобы разобраться, для каких оперативных вмешательств применяют конкретный тип материала:
- аутотрансплантация. Это процедура, подразумевающая перенос зуба с одного места на другое с целью восполнения визуально и функционально значимого дефекта. Чаще трансплантируются восьмые моляры (зубы мудрости). В результате проведения операции костную ткань становится значительно шире;
- синус-лифтинг. Это оперативное вмешательство, которое проводится на верхней челюсти с целью увеличения длины костной ткани в случае ее дефицита.
Увеличить объем костной ткани удается за счет применения материалов синтетического происхождения. К помощи барьерных мембран прибегают с целью фиксации пересаженных костных тканей или предохранении костной ткани человека после того, как ему устранили моляр или премоляр. Для восстановления костной ткани используют аллотрансплантаты. Наиболее распространенными являются аутотрансплантаты.

Врачи качественно проводят оперативное вмешательство любой сложности с использованием различных остеопластических материалов. Стоимость процедуры значительно ниже, чем в других частных клиниках Москвы. На официальном сайте можно подробнее ознакомиться с прайсом. Чтобы записаться на первичный прием к врачу-стоматологу достаточно позвонить в клинику по указанным номерам или оставить заявку в онлайн режиме (с указанием имени и контактного номера).
Аннотация научной статьи по клинической медицине, автор научной работы — Ибрагимов Даврон Дастамович, Гаффаров Усмон Бобоназарович, Исхакова Зухра Шарифкуловна, Имамов Камол Нурмамат Угли, Ахмедов Бинали Сахадинович
Похожие темы научных работ по клинической медицине , автор научной работы — Ибрагимов Даврон Дастамович, Гаффаров Усмон Бобоназарович, Исхакова Зухра Шарифкуловна, Имамов Камол Нурмамат Угли, Ахмедов Бинали Сахадинович
ИСПОЛЬЗОВАНИЕ ОСТЕОПЛАСТИЧЕСКОГО МАТЕРИАЛА ДЛЯ ЗАПОЛНЕНИЯ ДЕФЕКТА ПРИ РАДИКУЛЯРНЫХ КИСТАХ ЧЕЛЮСТЕЙ Ибрагимов Д.Д.1, Гаффаров У.Б.2, Исхакова З.Ш.3, Имомов К.Н.4,
1Ибрагимов Даврон Дастамович - базовый докторант; 2Гаффаров Усмон Бобоназарович - заведующий кафедрой;
3Исхакова Зухра Шарифкуловна - ассистент;
4Имамов Камол Нурмамат угли - магистр;
5Ахмедов Бинали Сахадинович - магистр, кафедра челюстно-лицевой хирургии с курсом детской челюстно-лицевой хирургии, Самаркандский государственный медицинский институт, г. Самарканд, Республика Узбекистан
Ключевые слова: радикулярная киста, цистэктомия, остеопластический материал, кистагранулема, периапикального воспаления.
Актуальность. В структуре стоматологических заболеваний больные с одонтогенными кистами и кистоподобными доброкачественными образованиями занимают определенное место, и их количество не имеет тенденцию к снижению 4. Согласно Международной гистологической классификации опухолей все опухоли и опухолеподобные образования, развитие которых связано с зубной системой, отнесены к группе одонтогенных опухолей и опухолеподобных образований, а радикулярные кисты в соответствии с пересмотренной Международной классификацией болезней, травм и причин смерти включены в раздел болезней пульпы зуба и периапикальных тканей [10].
Радикулярная киста - это полость, имеющая хорошо сформированную фиброзную стенку, для которой, примерно в 90% наблюдений [1,3] были характерны те или иные проявления воспалительной реакции и внутренняя стенка, выстланная плоским эпителием. Чаще возникает в результате хронического периапикального воспаления [4]. Пациент с радикулярной кистой может не предъявлять никаких явных жалоб, они возникают при нагноении содержимого или прорастании кисты в гайморову пазуху [5,6]. Длительное существование кисты приводит к деформации костной ткани и повышению риска перелома челюсти. Для диагностики используются данные объективного осмотра, дентальной рентгенографии, электроодонтометрии и пункции с последующим цитологическим исследованием [7,9]. Лечение радикулярной кисты производится хирургическим путем [8].
Материал и методы. Проведены операции цистэктомии однокорневых зубов верхней и нижней челюсти у 29 пациентов в возрасте от 35 до 55 лет, находящихся на стационарном лечении в городском медицинском объединении города Самарканд, показаниями для данного вмешательства было: радикулярные кисты, кистагранулемы однокорневых зубов верхней и нижней челюсти. Основную группу составили 16, контрольную - 13 пациентов с вышеперечисленными патологиями. В обеих группах, больным перед хирургическим вмешательством проводилось клинико-лабораторное обследование и был запланирован оперативный метод лечения-цистоэктомия с замещением дефекта челюстей остеопластическим материалом. Оперативное вмешательство проводилось традиционным методом. Пациентам основной группы
Результаты и их обсуждение. У всех прооперированных больных послеоперационная рана зажила первичным натяжением. На 7-8 день после операции сняты швы. Результаты лечения прослежены у больных в сроки от 2 месяца до 1,5 года. У группы больных с применением препарата Коллапан-Л определяется плотная костная ткань на месте дефекта. В пределах дефекта зубы устойчивы. Рентгенологическим обследованием установлено, что активная регенерация костной ткани на месте бывшего дефекта начинается на втором месяце и уже через 3-5 месяцев контуры небольших дефектов до 0,5 см становятся малозаметными. Через 5 месяцев после операции цистоэктомии с применением препарата Коллапан-Л местный статус без особенностей, пальпируется плотная костная ткань.
Пациентам контрольной группы проводилось аналогичное лечение без применения препарата Коллапан-Л, при котором определяется неплотная костная ткань на месте дефекта. Зубы неустойчивы в пределах дефекта, десны вокруг зубов в проекции операции отечны и наблюдается кровоточивость десневых сосочков при малейшем дотрагивании. Наше наблюдение показывает, рентгенологическое обследование больных с операцией цистоэктомии" без применения остеорегенераторного препарата регенерация костной ткани на месте бывшего дефекта в отличие от основной группы начинается на четвертом месяце уже через 4-7 месяцев контуры небольших дефектов становятся малозаметными. Через 7 месяцев после операции цистоэктомии пальпируется плотная костная ткань.
1. Зоиров Т.Э. и др. Состояние гигиены и пародонта при лечении методом шинирования у больных с переломом челюсти // Вопросы науки и образования, 2019. № 23 (71).
2. Ризаев Ж.А., Шамсиев Р.А. Причины развития кариеса у детей с врожденными расщелинами губы и нёба (обзор литературы) //Шсник проблем бюлоги i медицини,2018. Т. 1. № 2 (144).
3. Шамсиев Р.А. Особенности течения заболеваний у детей с врожденными расщелинами верхней губы и неба (Обзор литературы) //Journal of biomedicine and practice, 2018. Т. 2. С. 32-36.
5. Шамсиев А.М., Хамраев А.Ж. Малая хирургия детского возраста. O'qituvchi, 2006.
6. Юсупалиева К. Использование современных методов медицинской визуализации при диагностике деструктивных изменений зубочелюстной области // Научные разработки: евразийский регион, 2017. С. 54-57.
7. Jamshid S., Ravshan S. Accompanying defects of development in children with congenital cleft of lip and palate // European science review, 2017. №.1-2.
8. Minaev S. V. et al. Laparoscopic treatment in children with hydatid cyst of the liver // World journal of surgery, 2017. Т. 41. № 12. С. 3218-3223.
9. Kasimov S. et al. Haemosorption in complex management of hepatargia // The International Journal of Artificial Organs., 2013. Т. 36. № 8.
10. Slepov V.P. et al. Use of ethonium in the combined treatment of suppurative and inflammatory diseases in children // Klinicheskaia khirurgiia, 1981. № 6. С. 78.
АФФЕКТИВНЫЕ РАССТРОЙСТВА У БОЛЬНЫХ АЛКОГОЛЬНОЙ ЗАВИСИМОСТЬЮ КАК ФАКТОР РИСКА РАЗВИТИЯ СУИЦИДАЛЬНОГО ПОВЕДЕНИЯ Хаятов Р.Б.1, Велиляева А.С.2, Тураев Б.Т.3, Тураев Т.М.4
1Хаятов Рустам Батырбекович - ассистент;
2Велиляева Алие Сабриевна - кандидат медицинских наук, доцент, заведующий кафедрой;
3Тураев Бобир Темирпулатови - ассистент;
4Тураев ТолибМахмуджонович - ассистент, кафедра психиатрии, медицинской психологии и наркологии, Самаркандский государственный медицинский институт, г. Самарканд, Республика Узбекистан
Ключевые слова: аффективные расстройства, алкогольная зависимость, суицид.
Введение. В структуре алкогольной зависимости около 55% пациентов страдают биполярными аффективными расстройствами. Биполярная аффективная патология зачастую определяет причину формирования суицидального поведения у пациентов с алкогольной зависимостью. В течение жизни для 84% больных с алкогольной зависимостью при наличии расстройств аффективной сферы характерно развитие суицидального поведения [1, 2]. Наряду с людьми без сопутствующей соматической патологией равно как и у больных употребляющих психоактивные вещества с ВИЧ-инфекцией основными симптомами аффективных нарушений является подавленное настроение, нарушение сна, потеря аппетита, похудание, утомляемость, пониженная самооценка, ощущение беспомощности, психомоторная заторможенность, социальная изоляция и суицидальные намерения [3].
Цель исследования: изучение влияния аффективных расстройств в структуре алкогольной зависимости на возникновение суицидальных попыток.
Материалы и методы исследования:
При квалификации сочетанных особенностей личности использовались классификация П.Б. Ганнушкина, классификация акцентуаций характера К. Леонгарда, А.Е. Личко. Степень выраженности расстройств аффективной сферы в преморбиде выявлялась по патогномоничной симптоматике и в соответствии с критериями исключалась из исследования, тем самым определялась критериям нормы или акцентуации характера. Характерологические аспекты анализировались на совокупности информации объективного и субъективного анамнезов, психологического статуса, а также дополнительных данных психологического
Читайте также:

