Опухоли надпочечников синдром кушинга
Синдром Кушинга (СК) — это комплекс клинических симптомов, возникающих вследствие избытка ГКС. Субклиническая гиперкортизолемия, которую чаще всего диагностируют при исследованиях по поводу инциденталомы надпочечника — это состояние незначительного избытка ГКС, вызванное чрезмерной секрецией кортизола опухолью надпочечника, приводящее к торможению синтеза ГКС противоположным надпочечником, без характерных симптомов, но чаще всего возможны сахарный диабет, абдоминальное ожирение, артериальная гипертензия, сердечно-сосудистые события и остеопороз.
Классификация СК в зависимости от этиологии:
1. Эндогенный СК: вследствие чрезмерного синтеза ГКС надпочечниками:
1) АКТГ - независимый СК ( первичный гиперкортицизм):
а) автономные опухоли надпочечников — обычно одиночные, реже множественные аденомы; рак надпочечника →разд. 11.6. Опухоли, происходящие из пучковой зоны, секретируют в избытке исключительно кортизол, остальные типы опухолей (из сетчатой зоны или смешанные) — также и андрогены. Избыток кортизола ингибирует секрецию КРГ и АКТГ → происходит атрофия ткани коры пораженного надпочечника (расположенной за пределами капсулы опухоли), а также ткани коры второго надпочечника; нередко возникают множественные узлы коры надпочечника (описываемые как нодулярная гиперплазия), являющиеся поликлональными образованиями, в отличие от аденом, развивающихся из моноклонального источника.
б) макронодулярная гиперплазия надпочечников — причиной являются эктопические рецепторы в коре надпочечников, реагирующие на нетипичные стимулирующие раздражители, чаще всего на желудочный ингибиторный пептид (GIP), в настоящее время называемый глюкозозависимым инсулинотропным полипептидом, секретируется после еды в пищеварительном тракте; другие стимулирующие факторы — это катехоламины, вазопрессин, ТТГ, ЛГ, хорионический гонадотропин (ХГЧ), ФСГ, эстрогены в высокой концентрации, пролактин и интерлейкин 1;
в) микронодулярная гиперплазия надпочечников (первичная пигментированная микронодулярная гиперплазия [дисплазия] коры надпочечников) — генетически детерминированная семейная форма (синдром Карнея, с наличием других нарушений: миксом кожи, сердца и молочных желез, светло-коричневых пятен на коже, опухолей яичек, иногда других эндокринологических нарушений, напр. акромегалии) и спорадическая форма, при которой могут играть роль иммуноглобулины, провоцирующие гиперплазию коры надпочечников. Подобно другим АКТГ-независимым формам, ткань надпочечника между узелками может иметь атрофический характер.
2) АКТГ - зависимый СК ( вторичный гиперкортицизм) — гипофизарная форма (избыточный синтез АКТГ гипофизом, иначе говоря, болезнь Иценко-Кушинга →разд. 8.4.3; самая частая причина СК), синдром эктопической секреции АКТГ опухолью, локализированной вне гипофиза (значительно реже) или синдром эктопической секреции КРГ (реже всего).
2. Экзогенный СК: вызванный приёмом глюкокортикостероидных препаратов, в дозах, превышающих необходимые для заместительной терапии (наиболее частая причина СК), независимо от формы ЛС (таблетки, ингаляционные препараты, мази, растворы для инъекций, в т. ч. для внутрисуставных). наверх
КЛИНИЧЕСКАЯ КАРТИНА И ЕСТЕСТВЕННОЕ ТЕЧЕНИЕ наверхнаверх
1. Субъективные симптомы: изменение черт лица или фигуры тела, мышечная слабость и плохая переносимость физической нагрузки, склонность кожи к травматизации — тяжело заживающие язвы, склонность к возникновению гематом; полидипсия и полиурия (→ необходимо проконтролировать гликемию; в тяжёлых случаях может развиться гиперосмолярный гипергликемический синдром); повышенный аппетит; головная боль и головокружения (→ следует проконтролировать артериальное давление); эмоциональная лабильность, склонность к депрессии, ухудшение памяти, редко психотические состояния; боли в костях (в случае остеопороза → следует искать патологические переломы тел позвонков, ребер, лобковых и седалищных костей); склонность к инфекциям, особенно оппортунистическим (напр. грибковым), часто с тяжёлым течением, а также к туберкулезу; симптомы ишемической болезни сердца (→ выполнить контроль липидограммы), сердечной недостаточности или венозных тромбозов и тромбоэмболий (протромботическое действие ГКС), симптомы язвенной болезни желудка и двенадцатиперстной кишки (особенно у пациентов, принимающих НПВП); симптомы мочекаменной болезни (из-за гиперкальциурии и гиперфосфатурии); снижение потенции у мужчин, скудные менструации или вторичная аменорея у женщин.наверх
3. Естественное течение: при субклиническом СК, даже длительном, развитие характерного комплекса симптомов может не произойти; риск прогрессирования в выраженную форму СК невысокий, поэтому субклинический СК не следует изначально рассматривать как раннюю фазу СК. Развернутый СК диагностируется только на поздней стадии длительно протекающей болезни . Значительно чаще присутствуют только некоторые симптомы, напр. нарушение толерантности к глюкозе или сахарный диабет, дислипидемия, артериальная гипертензия и быстрое увеличение массы тела (ожирение), составляющие картину метаболического синдрома; также повышается риск остеопороза.
СК следует подозревать и диагностировать в следующих ситуациях:
1) у пациентов с множественными и прогрессирующими симптомами гиперкортизолемии, в особенности с наиболее характерными (типичные растяжки, атрофия проксимальных групп мышц нижних конечностей и плечевых областей, гиперемия лица, легкое возникновение кровоподтёков);
2) у пациентов с атипичным течением артериальной гипертензии, сахарного диабета или остеопороза, что вызывает подозрение о их вторичном происхождении (особенно при резистентности к лечению или возникновение у лиц молодого возраста);
3) при случайном выявлении опухоли надпочечника (инциденталома).
При существенном клиническом подозрении на наличие СК единичного нормального результата любого скринингового анализа недостаточно для исключения заболевания. Всегда следует исключать предварительный приём ГКС пациентом (экзогенный СК).
Дополнительные методы исследования
1. Основные биохимические исследования: гипокалиемия и гиперкалиурия, гипергликемия (нарушение толерантности к глюкозе или сахарный диабет), повышенное содержание общего холестерина, ХС-ЛПНП и триглицеридов, снижение концентрации ХС-ЛПВП.
2. Общий анализ крови: эритроцитоз, лейкоцитоз и тромбоцитоз, повышенная концентрация гемоглобина, лимфоцитопения, эозинопения, моноцитопения.
3. Гормональные исследования гипоталамо-гипофизарно-надпочечниковой системы (границы норм могут отличаться — необходимо удостовериться, какие нормы приняты в лаборатории, проводящей анализ):
1) подтверждение гиперкортизолемии — исследования в случае подозрения на наличие СК →рис. 11.2-1:
а) отсутствие суточного ритма секреции кортизола — повышенная поздневечерняя (в 23:00–24:00) концентрация кортизола в сыворотке крови >149 нмоль/л (5,4 мкг/дл) или в слюне (>4,0 нмоль/л [145 нг/дл]); утренняя концентрация кортизола часто находится в пределах референтных значений;
б) повышенная экскреция свободного кортизола с мочой (с целью исключения необходимы 3 суточные порции мочи) — в 3–4 раза, превышающий верхнюю границу нормы результат (330 нмоль/24 ч [120 мкг/24 ч]);
в) недостаточное снижение концентрации кортизола в сыворотке крови при исполнении супрессивного теста с 1 мг дексаметазона (ночной супрессивный тест с дексаметазоном, короткий супрессивный тест с дексаметазоном): следует назначить пациенту приём 1 мг дексаметазона п/о перед сном (в 22:00–23:00) и определить концентрацию кортизола в сыворотке крови на следующий день утром между 8:00 и 9:00 натощак; или при 2-дневном супрессивном тесте с 2 мг дексаметазона следует назначить пациенту приём 0,5 мг дексаметазона п/о каждые 6 ч на протяжении 2-х суток и определить кортизолемию через 48 ч после приема первой дозы — концентрация поиск причины гиперкортизолемии — исследования, подтверждающие диагноз СК и определяющие его этиологию →рис. 11.2-2:
а) уровень АКТГ в сыворотке крови — зависит от этиологии СК: уровень АКТГ 4 пмоль/л (20 нг/л) — о АКТГ-зависимом СК (болезни Иценко-Кушинга — БИК); при значении 2–4 пмоль/л (10–20 нг/л) следует провести тест стимуляции с КРГ;
б) тест стимуляции с КРГ (тест стимуляции синтеза АКТГ и посредственно кортизола с помощью КРГ): при болезни Иценко-Кушинга характерным является многократное повышение концентрации АКТГ после стимуляции КРГ, но в случае значительно повышенных исходных значений существенным принято считать повышение уровня АКТГ на ≥35–50 % и кортизола на ≥14–20 %. При АКТГ-независимом СК ответ на КРГ обычно отсутствует либо незначителен.
в) тест ингибирования 8 мг дексаметазона (2 мг каждые 6 ч в течение 2 суток; в настоящее время выполняется реже) — результаты зависят от этиологии СК; его роль состоит в дифференциации между болезнью Иценко-Кушинга и автономными формами гиперкортицизма с избытком кортизола (гормонально активная опухоль надпочечника, синдром эктопического АКТГ и нодулярная гиперплазия надпочечников). При болезни Иценко-Кушинга выделение кортизола и его метаболитов обычно снижается на ≥50 %, при этом в случае автономной секреции кортизола ингибирование отсутствует. Результат теста является недостоверным, напр., в случае наличия рецепторов к глюкокортикоидам в опухоли, эктопически секретирующей АКТГ.
г) реактивность надпочечников на нетипичные стимулы — следует проверить в случае подозрения на макронодулярную гиперплазию надпочечников; необходимо определить уровень кортизола в сыворотке изначально и на 30, 60, 90 и 120 мин после завтрака или после пероральной нагрузки 75 г глюкозы; после принятия вертикального положения; после п/о приёма 10 мг метоклопрамида, после в/в введения 100 мкг ГнРГ или 200 мкг ТРГ; в пользу диагноза свидетельствует повышение уровня кортизола.
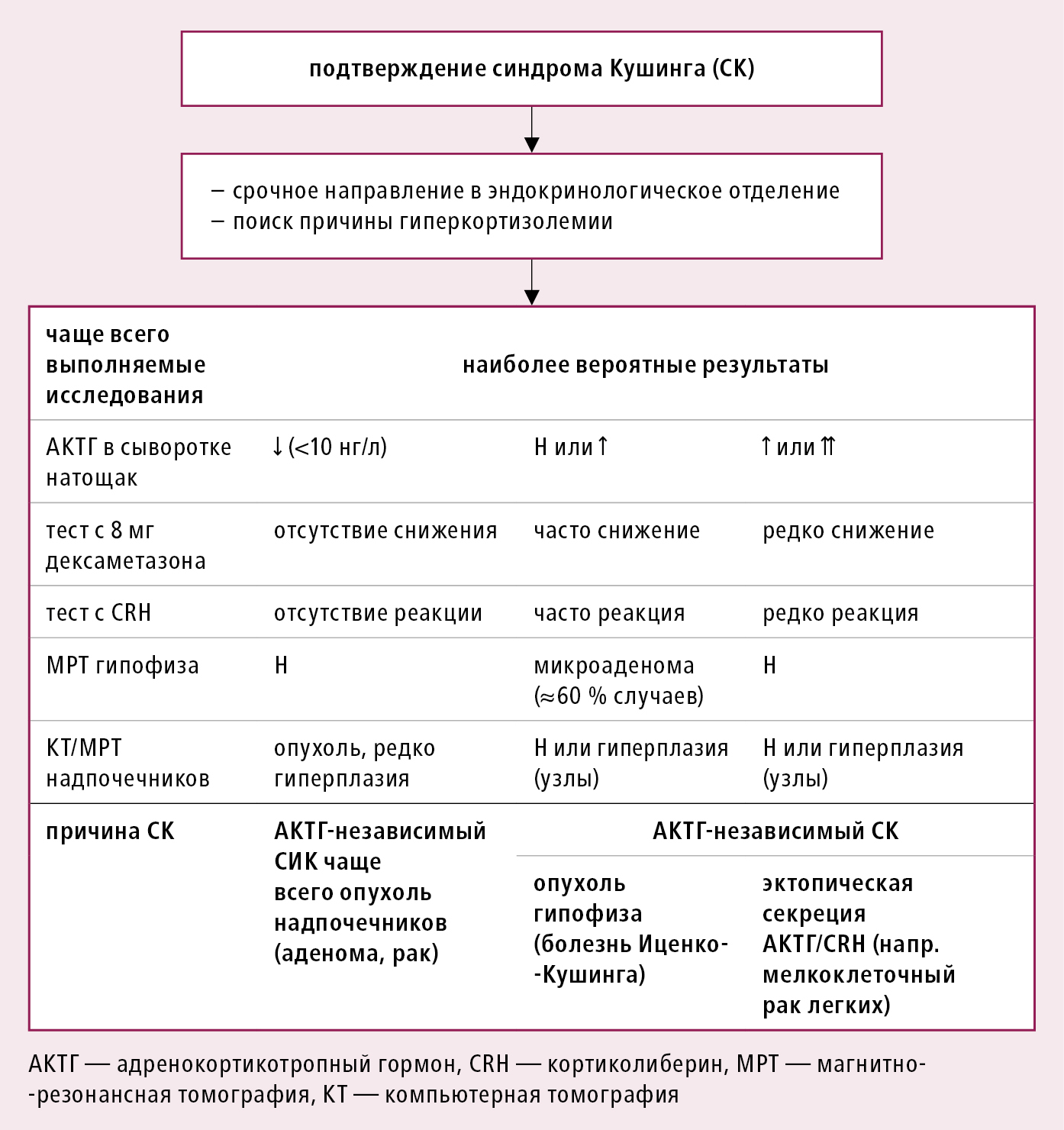
Рисунок 11.2-2. Алгоритм диагностики для определения этиологии синдрома Иценко-Кушинга
4. Визуализирующие исследования: МРТ гипофиза →разд. 8.4.3. КТ или, МРТ надпочечников — изменения, зависящие от причины СК →рис. 11.2-1:
1) автономная опухоль/опухоли коры надпочечников — при КТ односторонняя опухоль надпочечника, со свойствами аденомы →разд. 11.5; признаки атрофии другого надпочечника; реже множественные билатеральные аденомы коры надпочечников. При МРТ значительное содержание липидов, быстрое вымывание контрастного вещества. Гормонально активный рак надпочечника →разд. 11.6.
2) макронодулярная гиперплазия надпочечников — при КТ надпочечники симметричные, обычно увеличенные, часто с полициклическими контурами, а их плотность соответствует аденомам. МРТ обнаруживает в надпочечниках значительное содержание липидов.
3) микронодулярная гиперплазия надпочечников — при КТ и МРТ надпочечники симметричные, небольших или нормальных размеров; диагноз выставляется интраоперационно (характерная желто-черная окраска, вызванная присутствием липофусцина в узлах). РГ костей — признаки остеопороза, патологические переломы; в детском и юношеском возрасте часто отставание костного возраста. Денситометрия — признаки остеопении или остеопороза, особенно в поясничном отделе позвоночника и проксимальной части бедренной кости. Рецепторная сцинтиграфия с использованием аналогов соматостатина, с целью обнаружения нейроэндокринных опухолей, эктопически секретирующих АКТГ, или сцинтиграфия с йодхолестерином с целью выявления эктопически размещённой опухоли или идентификации автономно-секретирующей опухоли у пациентов с опухолями в обоих надпочечниках.
Диагностический алгоритм →рис. 11.2-1 и рис. 11.2-2. Как подтверждение, так и исключение гиперкортизолемии требует проведения ≥2 разных исследований.
1. Клинически выраженный СК: субъективные и объективные симптомы СК, гиперкортизолемия со сниженным уровнем АКТГ (надпочечниковая форма — АКТГ-независимый СК) или с повышенным уровнем АКТГ (аденома гипофиза или эктопическая секреция АКТГ или КРГ — АКТГ-зависимый СК); ответ в тесте с КРГ зависит от причин гиперкортизолемии; отсутствие ингибирования секреции кортизола (при опухоли надпочечника) или ингибирование только с помощью большой дозы [8 мг] дексаметазона (при аденоме гипофиза); иногда повышенный уровень андрогенов. Опухоль или опухоли надпочечников, обнаруженные при КТ/МРТ, или опухоль гипофиза при МРТ, либо, значительно реже, эктопический источник АКТГ или КРГ, обнаруженный методом рецепторной сцинтиграфии.
2. Субклиническая гиперкортизолемия, вызванная автономной опухолью или опухолями коры надпочечников (ранее — субклинический синдром Кушинга) вызывает много противоречий, поскольку критерии диагностики ещё не установлены. Необходимо оценить клиническую картину (обращая внимание на остеопению/остеопороз, абдоминальное ожирение, артериальную гипертензию, сахарный диабет) и следующие результаты дополнительных исследований (для постановки диагноза рекомендуется наличие 2-х или 3-х, и даже 4-х критериев):
1) тест с 1 мг дексаметазона — концентрация кортизола в сыворотке крови ≥94 нмоль/л (3,4 мкг/дл);
2) утренняя концентрация АКТГ в сыворотке верхней границы нормы;
4) концентрация кортизола в сыворотке крови в 23:00–24:00 ≥149 нмоль/л (5,4 мкг/дл).
Дифференциальная диагностика АКТГ зависимого и АКТГ независимого СК →рис. 11.2-2 .
Другие состояния с избытком ГКС:
1) синдром резистентности к ГКС — синдром частично нарушенной чувствительности ГКС рецептора (генетически обусловленный, редкий); повышенные концентрации АКТГ, кортизола, андрогенов и альдостерона в сыворотке крови, без симптомов избытка кортизола, с признаками андрогенизации у женщин и гиперальдостеронизма; сохранён суточный ритм секреции кортизола, а также ответ гипофиза и надпочечников на КРГ. Лечение: дексаметазон 1,0–1,5 мг/сут. с целью ингибирования секреции АКТГ.
2) функциональные синдромы (т. н. псевдо-СК), при которых обнаруженная гиперкортизолемия не является результатом органических изменений в пределах гипофизарно-надпочечниковой системы, но возникает вследствие других нарушений (гиперкортизолемия не требует лечения):
а) депрессия — гиперкортизолемия и нарушение ингибирования дексаметазоном, но сохранён суточный ритм секреции кортизола и нормальный уровень АКТГ;
б) беременность — в крови повышается уровень транскортина и, следовательно, кортизола. Синтез КРГ в плаценте возрастает в III триместре, увеличивается экскреция свободного кортизола с мочой; сохранён суточный ритм секреции кортизола.
в) алкоголизм — в немногих случаях наблюдаются соматические признаки СК (изменение метаболизма кортизола в печени и влияние алкоголя на ЦНС); абстиненция вызывает исчезновение симптомов;
г) психическая анорексия — повышенный уровень кортизола, в основном в результате снижения почечного клиренса, но возможен также повышенный синтез АКТГ. Нарушение ингибирования дексаметазоном является признаком приобретённой резистентности ГКС рецептора, что также объясняет отсутствие каких-либо признаков гиперфункции коры надпочечников.
Лечение осложнений СК: артериальной гипертензии, нарушений углеводного и липидного обмена, остеопороза, психических нарушений. Некоторые осложнения исчезают после успешного этиологического лечения СК. наверх
Зависит от этиологии СК; является крайне необходимым при манифестирующем СК и при наличии осложнений гиперкортизолемии. Вариантом выбора является оперативное лечение, вид которого зависит от причины СК (удаление аденомы гипофиза при болезни Иценко-Кушинга, опухоли надпочечника или — значительно реже — опухолевой ткани, эктопически секретирующей АКТГ), в то же время следует удержаться от терапевтических назначений, если диагноз СК сомнителен. Рекомендации The Endocrine Society (2015) советуют не начинать лечения в случае получения пограничных результатов гормональных исследований, если типичные клинические проявления СК отсутствуют.
1. Аденома гипофиза →разд. 8.4.3.
2. Автономная опухоль/опухоли коры надпочечников: методом выбора является хирургическое удаление опухоли надпочечника, после предоперационной подготовки ингибитором стероидогенеза → используется кетоконазол 400–800 мг/сут в 3 приёма (редко до 1200 мг/сут); сначала достигается биохимическая ремиссия, а по истечении ≈3 нед. — клиническое улучшение; следует проявлять осторожность, чтобы не спровоцировать дефицита ГКС и симптомов тяжелого криза острой надпочечниковой недостаточности (некоторые опухоли проявляют крайне высокую чувствительность к ингибиторам синтеза кортизола). Альтернативное лечение: метирапон — дозировка подбирается индивидуально, в зависимости от выраженности гиперкортизолемии и переносимости препарата, начально 250–750 мг/сут, у пациентов с тяжёлым СК — даже 1500 мг/сут (в специализированных центрах); реже применяют аминоглутетимид 500-750 мг/сут. Митотан (обычно ≈3 г/сут) используется при раке надпочечника, а этомидат — является единственным препаратом для в/в применения. Профилактика кортикостероидами при вмешательствах — как и в случае операции у больных с гипокортицизмом →см. выше. Первым критерием ремиссии первичного гиперкортицизма после оперативного лечения является утренняя концентрация кортизола 3. Макронодулярная и микронодулярная гиперплазия надпочечников: методом выбора считается билатеральная адреналэктомия; прикрытие гидрокортизоном — как при аденомэктомии.
В случаях длительного течения СК (независимо от этиологии) могут возникать сосудистые осложнения вследствие артериальной гипертензии. При наличии нелеченого СК даже лёгкой степени тяжести — смертность повышается в 4 раза (преимущественно по причине сердечно-сосудистых заболеваний и инфекций) по сравнению с общей популяцией. После эффективного оперативного лечения многие из проявлений СК, в т. ч. артериальная гипертензия и сахарный диабет, исчезают или ослабевают на протяжении 12 мес. Повышенный риск летального исхода по причине сердечно-сосудистых заболеваний сохраняется в течение ≈5 лет. наверх
1. Удаление аденомы/аденом коры надпочечников приводит к полному исчезновению симптомов СК. Рецидив опухоли происходит из-за повторного роста образования из фрагментов коры надпочечника, оставшихся в жировой ткани, в то же время рецидив радикально удаленной аденомы не возможен. Может быть необходимым периодическое заместительное лечение.
2. Билатеральная адреналэктомия при макронодулярной и микронодулярной гиперплазии надпочечников вызывает исчезновение симптомов СК, однако необходима постоянная заместительная терапия. При синдроме Карнея прогноз зависит от вида сопутствующих изменений.
3. При раке коры надпочечников (→см. ниже) прогноз зависит от степени распространенности опухоли и объёма хирургического лечения. У пациентов после билатеральной адреналэктомии обязательна постоянная заместительная терапия.

Общие сведения
Болезнь и синдром Иценко-Кушинга (кушингоид, гиперкортицизм) – это тяжелое состояние, для которого характерно нарушение регуляторных механизмов, контролирующих гипоталамо-гипофизарно-надпочечниковую систему. Впервые признаки этого заболевания описал в 1924 году невропатолог из СССР Николай Иценко. Он высказал предположение, что причиной болезни являются изменения гипоталамуса. Именно гипоталамус определяет взаимодействие нервной и эндокринной систем.
Американский нейрохирург Харвей Кушинг определил наличие связи этого заболевания с опухолью гипофиза. В настоящее время ученые доказали правоту обоих медиков. Они подтвердили, что болезнь Кушинга является следствием сбоев в функционировании гипоталамо-гипофизарной системы. Это заболевание является достаточно редким и чаще всего диагностируется у женщин в возрасте 25-40 лет. Представительниц прекрасного пола болеют этим недугом в пять раз чаще, чем мужчины.
Болезнь и синдром Кушинга не отличаются по своим клиническим проявлениям. Синдром Кушинга (или синдром гиперкортицизма) диагностируется при опухоли надпочечника либо эктопированной опухоли ряда органов, продуцирующих глюкокортикоиды. При этом синдроме на организм длительное время влияет чрезмерное количество гормонов коры надпочечников.
Патогенез
У людей с болезнью Иценко-Кушинга размеры гипофиза увеличены – развивается аденома или опухоль. Если болезнь развивается, со временем надпочечники также увеличиваются.
Чрезмерная выработка кортизола приводит к тем патологическим изменениям, которые характерны для этого заболевания. Если кортизола в организме продуцируется слишком много, это приводит к катаболическому влиянию на белковые структуры и матрицы тканей и структур. Речь идет о костной и мышечной ткани (оказывается влияние на миокард, а также гладкие мышцы), внутренние органы. Постепенно появляются выраженные атрофические и дистрофические изменения.
В таком состоянии в организме нарушен и углеводный обмен. Так как происходит стойкая стимуляция глюконеогенеза и гликогенолиза в печени и мышцах, развивается гипергликемия (стероидный диабет).
Гиперкортицизм приводит к изменениям жирового обмена. В одних местах тела происходит чрезмерное накопление жировых отложений, а в других – жировая клетчатка атрофируется. Объясняется этот тем, что разные жировые участки имеют разную чувствительность к глюкокортикоидам.
Еще одна важная составляющая патогенеза синдрома Кушинга – это электролитные расстройства (гипернатриемия, гипокалиемия). Их развитие связано с воздействием чрезмерного количества альдостерона на почки. Такие электролитные нарушения приводят к развитию артериальной гипертензии и кардиомиопатии, что, в свою очередь, ведет к сердечной недостаточности и аритмии.
Глюкокортикоиды негативно воздействуют на иммунный статус, что приводит к склонности к инфекциям.
Гиперкортицизм может развиваться и в процессе лечения разных заболеваний, когда человек принимает глюкокортикоиды – гормоны коры надпочечников — при условии передозировки.
Классификация
В процессе диагностики определяется эндогенный и экзогенный гиперкортицизм.
- Эндогенный синдром Кушинга– следствие слишком активной выработки надпочечниками глюкокортикоидов.
- Экзогенный синдром Кушинга – следствие приема глюкокортикостероидных лекарств в слишком больших дозах с целью заместительной терапии. Эта форма болезни может развиваться вне зависимости от формы лекарств: это могут быть как таблетки или растворы для инъекций, так и местные средства.
В свою очередь выделяются следующие формы эндогенного гиперкортицизма:
- АКТГ-независимый, то есть первичный. Его также подразделяют на несколько разных типов.
- АКТГ-зависимый, то есть вторичный. В таком случае чрезмерное количество АКТГ синтезирует гипофиз либо, в более редких случаях, опухоль, которая располагается вне гипофиза. Реже всего речь идет об эктопической секреции КРГ.
АКТГ-независимый гиперкортицизм связан с такими явлениями:
- Автономные опухоли надпочечников— это аденомы, как правило, одиночные, реже – множественные. Те опухоли, которые происходят из пучковой зоны, продуцируют только гормон кортизол. Другие типы опухолей – смешанные или опухоли из сетчатой зоны – кроме кортизола, синтезируют и андрогены. При избытке в организме кортизола вследствие ингибирования секреции КРГ и АКТГ атрофируются ткани коры надпочечников – как пораженной, так и здоровой железы . Иногда также появляются множественные узлы коры надпочечника.
- Макронодулярная гиперплазия надпочечников – эта форма связана с эктопическими рецепторами в коре надпочечников, которые реагируют на стимуляцию нетипичными раздражителями. Чаще всего это желудочный ингибиторный пептид, который выделяется после приема пищи в пищеварительном тракте. Но стимулирующие факторы могут быть и другими — вазопрессин, катехоламины, ТТГ, ЛГ, ХГЧ, ФСГ, большие концентрации эстрогенов, пролактина.
- Микронодулярная гиперплазия надпочечников – семейная форма и спорадическая форма, когда гиперплазию коры надпочечников провоцируют иммуноглобулины. Как и при других формах независимого гиперкортицизма может происходить атрофия ткани надпочечника между узелками.
Причины
Чаще всего кушингоидный синдром развивается при наличии базофильной или хромофобной аденомы гипофиза, которая выделяет адренокортикотропный гормон. Если развивается опухоль гипофиза, у больного появляется аденокарцинома или микроаденома.
В некоторых случаях развитие болезни Иценко-Кушинга связано с недавним инфекционным поражением ЦНС вследствие перенесенного энцефалита, арахноидита, ЧМТ, менингита, интоксикации.
Синдром Кушинга у женщин может быть связан с резкими гормональными скачками и перестройками. Иногда у женщин симптомы заболевания проявляются после беременности, родов, в период менструальной паузы.
Но в целом эксперты до сих пор ведут работу над тем, чтобы четко определить причины, вызывающие кушингоидный синдром.
Симптомы Иценко-Кушинга
И кортизол, и другие глюкокортикоиды являются в организме физиологическими регуляторами. Они снижают синтез белков и способствуют их распаду, увеличивают выработку глюкозы и стимулируют липолиз, оказывают влияние на иммунную систему.
Поэтому симптомы болезни Иценко-Кушинга связаны с чрезмерной продукций кортикостероидов, в частности ГКС. Происходит поражение большинства систем и органов, и при этом развивается характерный для болезни Иценко-Кушинга комплекс симптомов.
Определяются следующие характерные симптомы болезни Кушинга у человека:
- Диспластическое ожирение – этот признак появляется раньше всего и встречается наиболее часто. Жировые отложения под кожей перераспределяются так, что жир откладывается в плечах, над шейными позвонками, над ключицами, на животе. При этом конечности остаются сравнительно тонкими. Кушингоидное лицо округляется и приобретает багровый цвет (матронизм). Это – так называемый кушингоидный тип ожирения.
- Трофические изменения кожных покровов– кожа становится тонкой, очень сухой, имеет багрово-цианотичный оттенок. В тех местах, где откладывается чрезмерное количество жира, появляются растяжки фиолетового цвета. Появление стрий связано с тем, что кожа истончается и при этом активизируется катаболизм белков. Если человек получает незначительную травму, у него сразу появляются гематомы ввиду усиленной ломкости капилляров. В местах, где возникает сильное трение – на шее, локтях, подмышками – появляется гиперпигментация. У женщин часто появляются признаки гирсутизма – рост волос по мужскому признаку, а также гипертрихоз груди.
- Вторичный гипогонадизм – это ранний признак болезни. Симптомы синдрома Иценко-Кушинга проявляются нарушениями месячного цикла (развивается аменорея и опсоменорея). Эти симптомы у женщин могут в итоге привести к бесплодию. У мужчин ухудшается потенция, развивается гинекомастия. Если заболевание развивается в детстве, то у мальчиков в подростковом возрасте половой член и яички остаются недоразвитыми. У девочек же проявляется первичная аменорея и нормально не развиваются молочные железы. При этом в плазме крови больного понижается уровень гонадотропинов, эстрогенов, тестостерона.
- Миопатия– мышцы гипотрофируются, этот процесс затрагивает верхние и нижние конечности, переднюю брюшную стенку. Соответственно, ноги и руки становятся тонкими, а живот – увеличивается за счет отвисания и жировых отложений.
- Артериальная гипертензия– это проявление характерно для большинства таких больных. Вследствие регулярных проблем с артериальным давлением нарушается метаболизм миокарда, развивается сердечная недостаточность. В ходе электрокардиографии могут определяться признаки гипертрофии левого желудочка.
- Вторичный иммунодефицит – выражается в появлении акне и грибковых поражений на коже, а также поражений ногтей. У таких больных долго заживают раны, появляются трофические язвына голенях, развивается хронический пиелонефрит. Проявляются и многочисленные изменения вегетативной нервной системы, что приводит к развитию синдрома вегетативной дистонии с многочисленными и разнообразными проявлениями, в том числе и выраженными психозами.
- Нарушение обмена углеводов – нарушается толерантность к глюкозе, проявляется диабет второго типа с гиперинсулинемией, инсулинорезистентностью, отсутствием склонности к кетоацидозу и благоприятным течением.
- Изменения костей – если болезнь проявляется в детском возрасте, темпы роста малыша замедляются, либо он останавливается полностью. Задерживается и развитие скелета. Между реальным возрастом ребенка и возрастом его костей может отмечаться разница до 5 лет. Одним из самых тяжелых проявлений гиперкортицизма считается стероидный остеопороз, при котором происходит деминерализация костей и подавляется синтез белкового матрикса. В таком случае часто проявляются боли в позвоночнике, происходят переломы позвонков и ребер.
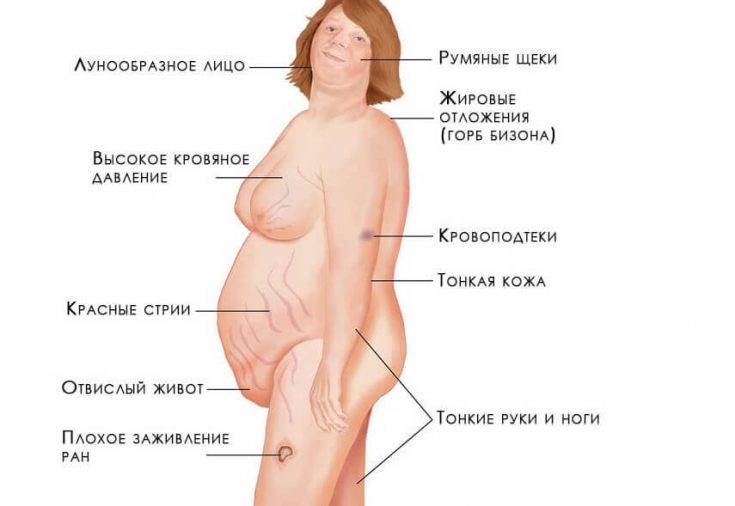
Симптомы синдрома Иценко-Кушинга
Итак, основные симптомы этого заболевания являются следующими:
- ожирение особого типа;
- истончение кожных покровов;
- слабость и атрофия мышц;
- гипертензия, проблемы с сердцем, отеки;
- нарушение месячного цикла, дисфункция половых желез;
- нервные расстройства;
- высокая частота инфекционных болезней;
- плохо заживающие раны;
- остеопороз, переломы.
Анализы и диагностика
Если человек отмечает у себя проявления части из описанных выше признаков, ему необходимо незамедлительно обращаться к эндокринологу.
Чтобы установить диагноз, врач изначально проводит осмотр, после чего назначает пациенту проведение необходимого комплекса исследований:
- Лабораторное исследование крови и мочи на содержание гормонов. Обязательно необходимо определить уровень кортикостероидов и АКТГ.
- Проводятся также гормональные пробы. Для этого изначально пациент сдает кровь для определения уровня гормонов, после чего принимает препарат (Синактен, Дексаметазони др.) и спустя определенное время снова сдает кровь.
- Биохимический анализ крови – позволяет определить наличие нарушений в организме, а также выявить сахарный диабет.
- Проводится рентген черепа и области турецкого седла, чтобы определить размеры гипофиза пациента.
- Компьютерная и магнитно-резонансная томография – проводят с целью подробного изучения особенностей гипофиза и структур мозга.
- Рентген костей скелета – проводят, чтобы определить наличие остеопороза и патологических переломов.
Лечение синдрома Иценко-Кушинга
После установления диагноза врач назначает комплексное лечение синдрома Кушинга. Лечение, в зависимости от индивидуальных особенностей течения заболевания, может быть следующим:
- Медикаментозное– назначают препараты, которые блокируют чрезмерную продукцию АКТГ или кортикостероидов.
- Лучевая терапия– ее проведение дает возможность снизить активность гипофиза.
- Хирургическое – врач принимает решение об удалении опухоли гипофиза. Проводят традиционную операцию либо используют криохирургию – разрушение опухоли влиянием низких температур (используют жидкий азот). Если болезнь развивается очень активно, проводят удаление одного или обоих надпочечников.
Как правило, в процессе терапии заболевания сочетается несколько разных методов.
Читайте также:

