Одногодичная летальность больных со злокачественными новообразованиями
МОСКВА, 3 июня. /ТАСС/. Только один показатель - удельный вес пациентов со злокачественными новообразованиями, состоящих на учете пять и более лет, федерального проекта "Борьба с онкологическими заболеваниями" нацпроекта "Здравоохранение" был достигнут в РФ в 2019 году, а показателя "Снижение смертности от новообразований" не достигли более 50 регионов России, сообщила в среду директор департамента организации медпомощи и санаторно-курортного дела Минздрава РФ Екатерина Каракулина.
"Показатели 2019 года достаточно малоутешительны. Единственный показатель был достигнут - это удельный вес больных со злокачественными новообразованиями, состоящих на учете пять лет и более. Все остальные показатели у нас хотя и имеют тенденцию к снижению, но, к сожалению, по плановым показателям за 2019 год были не достигнуты", - сказала она на заседании экспертного совета комитета Госдумы по охране здоровья по вопросам обращения лекарственных средств, развития фармацевтической и медицинской промышленности.
Каракулина также отметила, что целевых показателей по снижению смертности от новообразований, в том числе злокачественных, на 100 тыс. населения не достигли 53 региона, по доле злокачественных новообразований, выявленных на ранних стадиях, - 28 регионов, по удельному весу пациентов со злокачественными новообразованиями, состоящих на учете более пяти лет - 29 регионов, по одногодичной летальности пациентов со злокачественными новообразованиями - 26 регионов. При этом она отметила, что есть 10 регионов с "наибольшим отставанием" по плановым показателям, среди которых Кемеровская, Новосибирская, а также Астраханская области.
"Почти 14% региональных планов мероприятий не были реализованы. В целом более 7 тыс. мероприятий было запланировано и только 6 тыс. было реализовано на самом деле. Самое худшее, низкий процент выполнения реализации - [по] реабилитации онкологических пациентов, 80% [от плана] в субъектах только смогли реализовать данные направление, - сообщила директор департамента Минздрава. - Самый хороший процент выполнения мероприятий был в разделе противодействия факторов развития онкозаболеваний - 92%".
При этом хорошим показателем является перевыполнение плана по включению медорганизаций в реализацию федерального проекта. Так, в 2019 году к проекту подключились 175 медорганизаций, оказывающих онкологическую помощь, при 90 запланированных. Кроме того, в регионах РФ был открыт 141 центр амбулаторно-онкологической помощи при плановом показателе в 100 учреждений.
"В соответствии с клиническими рекомендациями [на] оказание медицинской помощи , в том числе [на] проведение химиотерапии, было использовано 92% средств, направленных на данные мероприятия. По сравнению с 2018 годом у нас в четыре раза увеличилась кратность применения химиотерапии, на 48% увеличилось применение схем лекарственной химиотерапии в дневном стационаре. Это достаточно важное достижение", - добавила Каракулина. Она также отметила прирост числа специалистов-онкологов в медучреждениях в прошлом году, в частности радиотерапевтов на 26%.
Воронежский областной клинический онкологический диспансер
Воронежская государственная медицинская академия им. Н.Н. Бурденко
Одно из направлений снижения смертности от злокачественных новообразований – уменьшение доли больных, умерших в течение первого года после установления диагноза.
В течение последних 10 лет определилась положительная тенденция данного показателя (2003 г. – 23%, 2012 г. – 18,7%).
Нами сформирована причинно-следственная диаграмма зависимости показателя одногодичной летальности от различных параметров онкологической помощи (рис. 1).
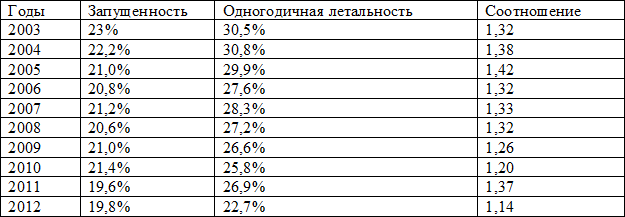
В первую очередь это своевременность диагностики онкологической патологии. Показатель поздней диагностики за последнее десятилетие с тенденцией к снижению (2003 г. – 23%, 2012 г. – 18,7%). Соотношение между показателями одногодичной летальности и запущенности заболевания (удельный вес пациентов с IV стадией заболевания в структуре всех первичных больных) характеризует несоответствие регистрируемой степени распространения опухолевого процесса действительному, так как при своевременном выявлении заболевания даже без лечения срок жизни больного в абсолютном большинстве больше года (табл.1). Недодиагностика опухолевого процесса (неточное стадирование) обусловлено дефектами уточняющей диагностики в специализированном онкологическом учреждении (неполное обследование пациента, ошибки при использовании лучевых и морфологических методов исследования, отсутствие реальной возможности поголовного использования позитронно-эмиссионной томографии и др.).
Таблица 1. Соотношение показателей одногодичной летальности и запущенности
Своевременность диагностики злокачественных новообразований зависит от качества первичной диагностики, диспансеризации пациентов с предраковой патологией, онкопрофосмотров и реализации скрининговых программ. Сформирована причинно-следственная диаграмма поздней диагностики (рис. 2).
Рис. 1. Причинно-следственная диаграмма одногодичной летальности
Качество первичной диагностики зависит от сроков и полноты обследования, онкологической грамотности медицинского персонала в первичном звене здравоохранения, финансового, материально-технического и кадрового обеспечения.
Длительность сроков обследования больных колеблется от 2-х месяцев до 1,5 лет. Несмотря на то, что ежегодно обучение по онкологии в ВГМА им. Н.Н. Бурденко проходит до 300 врачей разного профиля, осуществить тотальный онкологический всеобуч врачей общелечебной сети пока не представляется возможным из-за низкого уровня кадрового обеспечения всех ЦРБ и поликлиник города.
Рис. 2. Причинно-следственная диаграмма поздней диагностики
Качество онкопрофилактических осмотров зависит от реализации скрининговых программ, деятельности смотровых кабинетов, организации комплексных профилактических осмотров, проведения индивидуальных онкопрофосмотров.
Активная выявляемость за последнее десятилетие выросла, но резервы ее роста есть (рис. 3).
Рис. 3. Динамика активной выявляемости
Качество диспансеризации предраковой патологии, по данным курации ВОКОД лечебно-профилактическими учреждениями области, неоптимально, так как нет официальной регламентации структуры предраковой патологии, объемов обследования, не соблюдаются сроки диспансеризации.
Второй параметр онкологической деятельности, от которого зависит уровень одногодичной летальности - мониторинг больных, подлежащих специальному лечению (II клиническая группа). Он складывается из эффективной работы с отказавшимися от обследования и лечения, адекватного лечения сопутствующей патологии, жесткого контроля за больными, направленными на лечение в онкодиспансер, этапностью медицинской помощи. Целесообразно дифференцировать в системе мониторинга больных II клинической группы функции специализированного онкологического учреждения и первичного звена здравоохранении, а также параметры совместной деятельности (рис. 4).
Рис. 4. Мониторинг больных II клинической группы
В Воронежской области число отказавшихся от обследования и лечения составляет за последние годы от 2 до 4% первично зарегистрированных больных, число пациентов, которым отказано в проведении специального лечения по сопутствующей соматической патологии – около 3%.
Несмотря на то, что разработан и внедрен в практическую деятельность алгоритм работы с отказавшимися от лечения, количество таких больных не уменьшается, чему способствует активная пропаганда знахарской практики.
Лечение соматической патологии у онкологических больных в неонкологических учреждениях у многих пациентов не завершается возможностью снятия противопоказаний к специальному лечению из-за отсутствия должного контроля за ними со стороны районных онкологов. То же относится к мониторингу этапности лечения (больные прерывают лечение и уходят из поля зрения как специалистов онкодиспансера, так и районных онкологов). Причина – неукомплектованность кадров онкологов первичного звена здравоохранения.
Поэтому нами выделены совместные функции онкодиспансера и онкологических кабинетов. Двойной контроль за этапностью лечения и направленными больными на специальное лечение может обеспечить минимизацию указанных дефектов.
И, наконец, основную роль в снижении уровня одногодичной летальности играет качество управления онкологической помощью (рис.5).
Рис. 5. Управление онкологической помощью с целью снижения уровня одногодичной летальности
Управляющие воздействия распространяются как на работу онкодиспансера, так и на деятельность медицинских организаций неонкологического профиля. На онкодиспансер в плане снижения одногодичной летальности возлагаются функции управления формированием и контролем реализации скрининговых программ, онкологическим всеобучем, методической и информационной помощью по онкологическим вопросам медицинским организациям неонкологического профиля, аналитическая деятельность по оценке эффективности онкопрофилактической работы, уточняющей диагностики, отказам от специального лечения, оптимизацией кураторской деятельности, лекарственного и технического обеспечения с соответствующими оперативными и управленческими решениями.
На медицинские организации неонкологического профиля для снижения уровня одногодичной летальности возложены функции управления качеством оформления и разбора протоколов запущенности с принятием реальных решений по минимизации фактов поздней диагностики, первичной диагностики, онкопрофосмотров, диспансеризации предраковой патологии.
Определены также совместные функции онкодиспансера и медицинских организаций неонкологического профиля: реализация скрининговых программ, работа с пациентами II клинической группы, отказавшимися от обследования и лечения.
Выводы
1. Одно из направлений снижения смертности от злокачественных новообразований – уменьшение доли больных, умерших в течение первого года после установления диагноза.
2. Инструменты снижения уровня одногодичной летальности – оптимизация мониторинга онкологических больных II клинической группы, своевременной диагностики, специального лечения в соответствии с федеральными стандартами, диспансеризации предраковой патологии.
3. Совершенствование управления онкологической службой – главный фактор снижения смертности от злокачественных новообразований.
4. Дифференцированы управленческие меры по снижению одногодичной летальности для специализированной онкологической организации, медицинских организаций неонкологического профиля, определены совместные функции этих организаций.
Список использованных источников:
1. Состояние онкологической помощи населению России в 2003-2011 г.г./ под ред. В.И. Чиссова, В.В. Старинского, Г.В. Петровой. – М., 2012.
2. Состояние онкологической помощи населению России в 2012г./ под ред. В.И. Чиссова, В.В. Старинского, Г.В. Петровой. – М., 2013.
Для оценки противораковой борьбы установлен ряд показателей, которые характеризуют эпидемиологическое состояние злокачественных новообразований различной локализации. Кроме того, они дают возможность провести контроль заболеваемости злокачественными новообразованиями. Все это осуществляется, как было указано, на основании сводных отчетов, представляемых с онкологических кабинетов (отделений), диспансеров (городские, областные, краевые) в вышестоящие органы здравоохранения.
Среди статистических показателей следует особо выделить:
Подобное вычисление показателя заболеваемости можно вычислить как для всех групп больных со злокачественными новообразованиями, так и для отдельных локализаций, пола, возраста.
Например: В одном из районов города впервые было выявлено в данном году 250 больных со злокачественными новообразованиями. При среднегодовой численности в 190 тысяч показатель заболеваемости:
2. Показатель смертности населения от злокачественных новообразо- ваний- 



Подобный расчет производится для всех форм злокачественных новообразований.
Например: В целом по городу общее число умерших от всех форм злокачественных новообразований составил 120 человек. При среднегодовой численности в 450000 показатель смертности:

3. Показатель удельного веса (Ув) заболевших (умерших) раком какой-либо локализации к общему числу впервые выявленных больных со злокачественными новообразованиями. Этот показатель выводится, когда необходимо определять частоту распространения данной локализации в общей структуре заболеваемости (смертности) населения злокачественными новообразованиями. Удельный вес заболевших выражается через-

Подобные исчисления удельного веса по заболеваемости (смертности) производятся для всех локализаций в отдельности и выражаются в %.
Например: В 1983 году общее число впервые выявленных больных со злокачественными новообразованиями составило 2376 человек, из них рак желудка имел место у 378 человек.
У в рака желудка
, а в показателях на 100000
населения равнялось 31,5 (общая заболеваемость-198,0).
Вычисление показателя удельного веса тех или иных локализаций в динамике в общей структуре онкологической заболеваемости позволяет нам определить степень распространенности заболевания, наметить мероприятия по противораковой борьбе, помогает ставить и провести ряд важных задач по эпидемиологическому изучению данной проблемы,соответственно территориальному распространению рассматриваемой патологии.
По смертности онкологических больных определением показателя удельного веса можно вычислить:
1.Число умерших от рака по отношению к общему числу умерших в данном регионе.
2. Число (или %) умерших от рака в каждой возрастной группе из числа всех умерших в данном возрасте.
3. Контингенты онкологических больных - больные, которые находятся на учете в районе деятельности онкологического учреждения (диспансера)
с момента установления диагноза до конца жизни. При учете контингента онкологических больных исходят из:
а) оценки прироста или темпов прироста как общего показателя, так и числа больных, находящихся на учете с момента установления диагноза не менее 1 года, 1-2 года, 3-4 года, 5-9,10 и более лет. Расчет производят на 100000 жителей. Подобный расчет делают для общего числа онкологических больных и для отдельных локализаций, находящихся на учете на конец года;
б) индекса накопления контингентов (ИНК) -отношение больных на
конец отчетного года к впервые выявленным больным. ИНК определяется как для всех форм злокачественных новообразований, так и отдельных локализаций в динамике
С- число больных на конец отчетного года, В
- число впервые выявленных больных.
Например: 1) в 1983 г. в г.Баку на конец года состояло 441 больных раком желудка, а число выявленных больных указанной патологии имело место у 364 человек 
2) в этом же году на конец года состояло 1522 больных раком молочной железы, а число впервые выявленных больных указанной патологии имело место у 233 женщин. 
Как видно из приведенных примеров индекс накопления контингентов больных раком желудка и молочной железы происходит не одинаковыми темпами; при первом ИНК существенно не меняется, а при втором ежегодно отмечается заметное увеличение общего числа рака молочной железы за счет эффективности лечения и длительности выживания.
в) соотношение умерших и впервые выявленных больных (сколько приходится умерших на каждые 100 выявленных больных);
г) доли больных, выбывших из-под наблюдения.
4. одногодичная летальность ОЛ - этот показатель определяется отношением числа больных, состоящих при жизни на учете менее Ігода к числу больных с впервые установленным диагнозом злокачественного новообразования. Расчет проводят по всем локализациям и удельный вес умерших в течение года выражают в %.

Например: в 1983 г. по городу от рака желудка умерли 363 человека, из них 246 больных при жизни состояли на учете менее 1 года, а больных с впервые установленным диагнозом рака желудка было 364.

В то же время, следует отметить, показатель одногодичной летальности по раку молочной железы составлял 26,2 %, а по раку пищевода 74,7 %. Таким образом, показатель одногодичной летальности зависит от локализации опухоли и значительно варьирует. При этом определяющим фактором является выявление удельного веса больных с IV клинической группой(для визуальных локализаций III ст., а для остальных IV ст.) среди впервые зарегистрированных случаев злокачественными новообразованиями. Как у нас в стране,так и за рубежом выявляется высокий процент далеко зашедших форм рака внутренних органов (желудка, пищевода, легких, толстой и прямой кишки - более 75 %).
Удельный вес (в %) IV клинической группы рассчитывают отношением числа впервые выявленных запущенных форм рака к общему числу выявленных злокачественными новообразованиями в данном году, расчет проводят по всем локализациям.
При эпидемиологических исследованиях поражаемость населения злокачественными новообразованиями, особенность его распространения в зависимости от регионов, народонаселения, климатических, этнографических и экологических факторов и, наконец, от возрастно-полового различия сравниваемых групп для правильной статистической интерпретации применяют исчисление:
ют истинное положение заболеваемости по раку шейки матки. Кроме того, при расчете специальных интенсивных показателей для выявления закономерности частоты возникновения рака делают сравнение повозрастных показателей одной местности с другой, так как частота развития злокачественных новообразований находится в определенной зависимости от возраста и вида опухоли.
2. Стандартизованных показателей - при этом показателе с помощью стандартизованных коэффициентов получают сводные, обобщающие данные о заболеваемости в сравниваемых группах по возрасту, полу и тяжести заболеваний. Расчет основан на выборе одинакового состава сравниваемых групп. При этом за стандарт можно принять состав (распределение по ведущему признаку) любой из сравниваемых групп или их средний состав, а также распределение, полученное в других исследованиях (Мерабишвили В.М., 1980г.). Чаще за стандарт выбирают возрастно-половое распределение населения. Для расчета стандартизованных показателей применяют прямой, косвенный и обратный методы.
В таблице №4 мы приводим широко распространенный и наиболее приемлемый для онкологической заболеваемости расчет стандартизованных показателей прямым методом.
При подготовке официальных данных по онкологической статистике широко используются стандарты М.Сеги и мировой. В заключение необходимо отметить, что вычисление стандартизованных показателей на основании коэффициентов-стандартов, которые являются условными величинами, дает возможность оценить на каких территориях при устранении неоднородности возрастного состава населения чаще возникает рак, каков реальный (без влияния возрастной структуры) прирост и убыль показателя (В. В. Мишура с соавт.). Однако при оценке деятельности онкологических учреждений и планирования сети, как и расстановки кадров, стандартизованные показатели не могут быть взяты за основу критерия.
НИИ онкологии СО РАМН, Томск
Одним из объективных критериев оценки деятельности онкологической службы является показатель одногодичной летальности.
Целью исследования было изучение одногодичной летальности онкологических больных на территории Томской области за 2004—2009 гг.
Материал и методы
За изучаемый период в Томской области умерли в течение года после установления диагноза злокачественного новообразования 6 826 больных, в том числе в г. Томске — 2 915, в сельских административных районах — 3 134, в г. Кедровом — 24, в г. Стре-жевом — 174, в г. Северске — 579 человек. Изучена одногодичная летальность на территории Томской области за 2004—2009 гг. (таблица).

В 2009 г. одногодичная летальность в Томской области составила 33,4%, снизилась на 3,7% по сравнению с 2004 г. (РФ — 33,2% в 2004 г. и 29,2% в 2009 г.). В сельской местности одногодичная летальность в течение периода проведенных исследований значительно превышает данный показатель в г. Томске. Максимальный разрыв показателей зафиксирован в 2004 г. — 12,3%. В 2009 г. разница составила 9,3%. Высокая одногодичная летальность в 2009 г. отмечена в Бакчарском (63,6%), Зырянском (52,8%), Молчанов-ском (51,6%) районах. Снижение этого показателя до минимального по Томской области выявлено в городах Кедровом (0%), Северске (16,4%), Стрежевом (27,5%).
С учетом локализации опухолевого процесса высокая одногодичная летальность отмечена при раке легкого — 58,8% (РФ — 54,1%), желудка — 56,7% (РФ — 53,2%), пищевода — 54% (РФ — 61,0%), полости рта и глотки — 50,7%, (РФ — 61,0), ободочной кишки — 43% (РФ — 32,5%), яичника — 41,8% (РФ — 26,4%), костей и мягких тканей — 41,5% (РФ — 26,0%). Наименьшие показатели зарегистрированы при злокачественных новообразованиях кожи — 0,3% (РФ — 0,8%), губы — 7,7% (РФ — 5,1%); тела матки — 12,1% (РФ — 11,0%), молочной железы — 12,8% (РФ — 9,5%); меланоме кожи — 5,6% (РФ — 14,4%). В динамике удельного веса больных, умерших в течение года после установления диагноза ЗНО с 2004 по 2009 г., показатель снизился при раке гортани на 15,4%, мочевого пузыря — на 11,3%, губы — на 10,5%, при лейкемиях — на 14%, меланоме кожи — на 12,9% и увеличился при раке яичника на 15,4%, костей и мягких тканей — на 7,5%.
Соотношение между летальностью на первом году и долей больных с IV стадией заболевания уменьшилось в Томской области за изучаемый период с 1,8 до 1,3 и соответствует в 2009 г. среднероссийскому показателю. При раке губы, полости рта и глотки, гортани, шейки матки, тела матки, яичника и меланоме кожи это величина индекса равна или превышает 2, что свидетельствует о несоответствии регистрируемой степени распространенности опухолевого процесса действительному.
Таким образом, проведенные исследования указывают на низкую эффективность медико-социальных и профилактических мероприятий по оказанию онкологической помощи населению Томской области, о чем свидетельствует высокий уровень одногодичной летальности, особенно в сельской местности.


Андрей Дмитриевич, какие новые задачи поставлены перед онкологической службой на ближайшие годы?
Андрей Каприн: Государство поставило задачи перед всем здравоохранением: к 2024 году снизить смертность от новообразований до 185 случаев на 100 тысяч человек, увеличить охват населения профилактическими медосмотрами с 40 до 70 процентов. Удельный вес злокачественных новообразований (ЗНО), выявленных на ранних стадиях, довести до 63 процентов, а долю онкобольных, состоящих на учете 5 и более лет, до 60 процентов. Одновременно мы должны уменьшить одногодичную летальность от ЗНО до 17,3 процента. Все это возможно только при повышении доступности онкопомощи и ее качества. Для этого, кроме нашей программы, разработано еще несколько федеральных проектов: по обеспечению медучреждений квалифицированными кадрами, развитию исследовательских центров, внедрению инновационных технологий, по созданию единого цифрового контура в медицине, который, как нам обещали в правительстве, начнут выстраивать именно с онкологии. Должна измениться сама модель помощи, ее сформулировала министр здравоохранения Вероника Игоревна Скворцова: в центре этой модели - индивидуальный подход к каждому пациенту. А главным отличием от традиционного подхода является доклиническое выявление заболеваний и комплекс профилактических мер.


В рамках Национального проекта "Здравоохранение" до 2024 года предусмотрены меры по поддержке научной деятельности федеральных исследовательских центров, активизации доклинических и клинических испытаний, значительное увеличение бюджета на лекарственное обеспечение всей онкологической помощи, в т.ч. по таким современным направлениям, как иммунотерапия, таргетная терапия, лечение редких заболеваний. Поэтапно прописан механизм выстраивания трехуровневой системы онкопомощи, покрывающей всю страну, создание таких новых структур, как референсные центры, проведение необходимых скрининг-программ. Эта информация должна содержаться в паспортах программ, которые разработали субъекты Федерации в соответствии со спецификой и потребностями своих регионов. Важно и взаимодействие со многими смежными отраслями, которые помогут сети онкологической помощи перейти на современные технологии и переоснастить свой парк отечественным оборудованием.
Какие направления и разделы онкологической помощи будут приоритетными в текущем и будущем годах?
Андрей Каприн: Если говорить о приоритетных методах диагностики и лечения - это оснащение медицинских организаций, оказывающих онкологическую помощь, достаточным количеством современной техники для глубоких исследований и лечения во всех регионах страны. А также использование техники, которая есть в не онкологических подразделениях крупных клиник, возможностей телемедицины для проведения консультаций, консилиумов и различных обучающих семинаров и школ.
Мы должны научить коллег в регионах таким современным способам, как брахитерапия, рентгенохирургия, малоинвазивная хирургия разных локализаций, реконструктивная хирургия, которая позволяет не только излечить больного от рака, но и вернуть его к нормальному образу жизни, активной социальной деятельности. Все это мы умеем, вопрос только в расширении охвата, передаче опыта коллегам из регионов и оснащении необходимым оборудованием.
Как будет совершенствоваться онкологическая помощь жителям отдаленных регионов и сельской местности?


Андрей Каприн: В паспорте федерального проекта до 2024 года определены необходимые меры на каждый год.
В его рамках создаются 85 региональных программ по борьбе с онкозаболеваниями с учетом специфики каждого субъекта РФ. Например, на 2019 год в федеральном проекте заложена организация центров амбулаторной онкопомощи не менее чем в 20 регионах. Также не менее 20 субъектов РФ будут участвовать в переоснащении сети региональных медицинских организаций. За год будет создано не менее 9 референс-центров, в которых можно будет выполнить высокоточные исследования. И так по каждому году вплоть до 2024-го.
Важным направлением является повышение онконастороженности врачей первичного звена. Какие меры запланированы для этого?
Андрей Каприн: Специальное обучение пройдут не только все участковые врачи, но и узкие специалисты, работающие в амбулаторных учреждениях. Разработана специальная информационная дистанционная программа, которая позволяет врачу пройти первичное тестирование и повысить уровень своей квалификации по усвоению этого материала. 80 процентов участковых терапевтов уже прошли эту программу и получили соответствующий сертификат. Теперь нужно подключить к ней участковых педиатров, узких специалистов, врачей общей практики, семейных врачей. С помощью проекта по цифровизации онкологии мы планируем внедрить также программы, которые в автоматическом режиме будут подсказывать врачам, куда направлять пациентов разного возраста на необходимые диагностические исследования.
В онкологии сохраняется серьезный дефицит кадров. Как решить эту проблему?
Андрей Каприн: В рамках федерального проекта, который курирует Минобрнауки России совместно с нашим министерством, создаются новые учебные программы, будет расширена система повышения квалификации, использованы IT-технологии для распространения передового опыта и внедрения новых образовательных технологий в онкологии. Здравоохранение будет работать в едином информационном контуре, что позволит видеть всю картину и вовремя ее корректировать.
Известно, какую роль играет в профилактике рака здоровый образ жизни. Какие задачи в этой связи перед медиками?
Андрей Каприн: Мы не устаем повторять: любая профилактика эффективней, чем само лечение. Научить людей правильно питаться, не валяться часами на солнце, бросить курить и не злоупотреблять алкоголем проще, чем вылечить ту же меланому - рак кожи, очень агрессивное и опасное заболевание, которое очень трудно поддается лечению. Другой пример: курящие люди в 30 раз чаще страдают от рака, чем некурящие. И здесь просветительская роль и медиков, и всех средств массовой информации неоценима.
Большие надежды возлагаются на развитие радиологии. Каковы потребности онкологической службы в модернизации этого оборудования, строительстве новых учреждений этого профиля?
_t_310x206.jpg)
_t_310x206.jpg)
Андрей Каприн: Мы планируем значительно нарастить собственное производство тяжелой техники для ядерной медицины, тиражирование протонных ускорителей отечественного образца, создание собственного ускорителя МЛТ-6, под который в Обнинске уже заложен каньон. Потребность в перевооружении этого направления очень велика, и главное - чтобы это было наше оборудование, поскольку на импортном оборудовании мы не можем проводить какие-то дополнительные исследования, выстраивать новые области применения - только то, что записано в договоре о покупке данного прибора.
Мы продолжим развитие производства собственных радиофармпрепаратов, которые используются сегодня в ядерной медицине. Из них пока создан один российский аналог - на базе йода 125, который мы будем использовать для лечения не только рака предстательной железы, но и злокачественных новообразований молочной железы и шейки матки. Есть еще целый список отечественных изотопов, которые пока отправляют как сырье на переработку за границу, и лишь потом возвращают к нам в виде готового препарата с добавленной стоимостью. Здесь есть очень большие возможности развития собственной базы производства радиофармпрепаратов, и мы будем их использовать совместно с предприятиями и организациями минпромторга и "Росатома".
Улучшится ли обеспечение онкобольных современными инновационными лекарствами?
Андрей Каприн: Сейчас во многих научных центрах идет с использованием генных технологий разработка новых препаратов, действующих на новые внутриклеточные мишени. Несомненно, многие из них могут стать прорывными в борьбе с раком. В Московском онкологическом институте им. Герцена идут испытания новых костных имплантатов, полученных с помощью 3D печати. Одновременно с удалением пораженной части кости на ее место вживляется полимерная вставка, "заряженная" нужными препаратами и выполненная индивидуально для пациента. Там же разработан оригинальный аппарат, получивший название "гомункулус", или "человек-на-чипе". Это - микробиореактор, позволяющий на частице раковой ткани реального пациента, помещенной в специальный чип, выбрать эффективный метод химиотерапии, подобрать эффективное лекарство. В дальнейшем мы рассчитываем этим методом подбирать и лучевую нагрузку. Внедрение подобных разработок, без сомнения, поможет врачам сделать процесс лечения более персонифицированным.
Реальны ли цели по снижению онкологической смертности, поставленные перед онкологической службой до 2024 года?
Андрей Каприн: Задача сверхсложная и амбициозная. Финансирование национальных проектов имеет приоритетный характер, на нацпроект "Здравоохранение" предусмотрено 1,3 триллиона рублей. Более того, разрешено выделять средства из дополнительных доходов федерального бюджета. Государство по сути дает нам карт-бланш. И успех зависит от слаженной работы всех звеньев: исполнительной власти, науки, медицины, смежных отраслей. И, кстати, от участия СМИ, от поддержки общества в целом. Думаю, мы должны и можем доказать, что такие задачи нам по плечу.
Читайте также:

