Обчисліть масову частку нітрогену в його сполуці з хлором


Массовая доля азота в соединении NCl3=
14/(14+35.5*3)=14/120.5=0.116
14-масса молярная азота, 35.5-хлора






























За два дня автобус перевёз 1.015 пассажиров.В первый день он перевёз на 95 пассажиров больше,чем во второй.Сколько пассажиров перевёз автобус в каждый из этих дней?С пояснениями
Помогите решить уравнение: 3•(4-c)=6-(8c+3)
Відображення документу є орієнтовним і призначене для ознайомлення із змістом, та може відрізнятися від вигляду завантаженого документу. Щоб завантажити документ, прогорніть сторінку до кінця

ЗАДАЧІ НА МАСОВУ ЧАСТКУ ЕЛЕМЕНТА В СПОЛУЦІ
Масова частка елемента у сполуці – це відношення маси елемента до відповідної маси сполуки.
де n – кількість атомів елемента (індекс), A r – відносна атомна маса елемента; M r – відносна молекулярна маса речовини.
Картка 1. Масова частка. Прізвище, ім’я учня_________________________клас______
Задача 1. Визначте масові частки елементів у сполуці Калій оксиду К 2 O .
Задача 2. Зразок Хром оксиду ( Cr 2 O 3 ) масою 500 грам містить342 грам Хрому. Обчисліть масову частку Хрому у сполуці.
Задача 3. Скласти формулу сполуки Арсену з Оксигеном, якщо відношення мас Арсену та Оксигену в ній становить 15:16.
Задача 4. Масова частка Нітрогену в сполуці з Оксигеном становить 35%. Визначте формулу цієї сполуки, знаючи, що її відносна молекулярна маса – 108.
Задача 5. Розрахуйте співвідношення мас Літію і Оксигену в літій оксиді ( Li 2 O ).
Картка 2. Масова частка. Прізвище, ім’я учня_________________________клас______
Задача 1. Визначте масові частки елементів у сполуці Кальцій оксиду C аО.
Задача 2. Зразок Хром оксиду ( Cr 2 O 3 ) масою 1000 грам містить 684 грам Хрому. Обчисліть масову частку Хрому у сполуці.
Задача 3. Скласти формулу сполуки Сульфуру з Оксигеном, якщо відношення мас Сульфуру та Оксигену в ній становить 1:2.
Задача 4. Масова частка Карбону в сполуці з Оксигеном становить 27,3%. Визначте формулу цієї сполуки, знаючи, що її відносна молекулярна маса – 44.
Задача 5. Розрахуйте співвідношення мас Магнію і Оксигену в магній оксиді ( MgO ).
Картка 3. Масова частка. Прізвище, ім’я учня_________________________клас______
Задача 1. Визначте масові частки елементів у сполуці Алюміній оксиду Al 2 O 3 .
Задача 2. Зразок Хром оксиду ( Cr 2 O 3 ) масою 2000 грам містить 1368 грам Хрому. Обчисліть масову частку Хрому у сполуці.
Задача 3. Скласти формулу сполуки Брому з Оксигеном, якщо відношення мас Брому та Оксигену в ній становить 10:7.
Задача 4. Масова частка Купруму в сполуці з Оксигеном становить 88,9%. Визначте формулу цієї сполуки, знаючи, що її відносна молекулярна маса – 144.
Задача 5. Розрахуйте співвідношення мас Кальцію і Оксигену в кальцій оксиді (Са O ).
Картка 4. Масова частка. Прізвище, ім’я учня_________________________клас______
Задача 1. Визначте масові частки елементів у сполуці бор оксидіВ 2 O 3 .
Задача 2. Зразок Хром оксиду ( Cr 2 O 3 ) масою 250 грам містить 171 грам Хрому. Обчисліть масову частку Хрому у сполуці.
Задача 3. Скласти формулу сполуки Карбону з Оксигеном, якщо відношення мас Карбону та Оксигену в ній становить 3:4.
Задача 4. Масова частка Хлору в сполуці з Оксигеном становить 79%. Визначте формулу цієї сполуки, знаючи, що її відносна молекулярна маса – 133,5.
Задача 5. Розрахуйте співвідношення мас Неону і Оксигену в неон оксиді ( NeO 4 ).
Ви вже знаєте, що за хімічною формулою речовин можна визначити якісний і кількісний склад, назву речовини, формульну масу. Хімічна формула дає змогу обчислити ще одну важливу характеристику – масову частку, яка припадає на будь-який елемент у складі речовини.
Масова частка елемента у сполуці – це відношення маси елемента до відповідної маси сполуки.
де n – кількість атомів елемента (індекс), Ar – відносна атомна маса елемента; Mr – відносна молекулярна маса речовини.
Масова частка може бути виражена у частках від одиниці, або у відсотках. Сума масових часток усіх елементів у сполуці дорівнює одиниці або 100%, що потрібно брати до уваги під час перевірки правильності обчислень.
Приклад. Обчислити масові частки елементів в калійній селітрі KNO3.
Відповідь: w(К) = 38,6%, w (N) = 13,8%, w(О) = 47,6%.
Знаючи масову частку Нітрогену, ми легко можемо знайти масу, необхідного рослинам поживного елементу Нітрогену, в будь-якій масі селітри.
Приклад. Скільки кг Нітрогену міститься у двох кілограмах селітри?
В одному кілограмі селітри міститься: 1 • 0,138 = 0,138 кг, у двох кілограмах: 2 • 0,138 = 0,276 кг Нітрогену.
- Масова частка елемента у сполуці – це відношення маси атомів елемента до маси сполуки.
- Що таке масова частка елемента?
- У яких одиницях виражається масова частка елемента?
- Якщо формула складається з трьох елементів, то яким ще способом можна знайти масову частку третього елемента?
140. Визначте масові частки кожного елемента в молекулі вуглекислого газу (СО2) та в молекулі сульфатної кислоти (H2SO4).
141. Визначте масову частку:
а) цинку в ZnCl2;
б) феруму в FeSO4;
в) гідрогену в H2SO4;
г) купруму в Cu(NO3)2;
д) хлору в FeCl3.
142. Молекула фосфатної кислоти складається із 3 атомів Гідрогену, 1 атома Фосфору і 4 атомів Оксигену. Напишіть хімічну формулу фосфатної кислоти й обчисліть масові частки кожного з елементів.
143. У якому із двох оксидів масова частка Феруму більша: в магнітному залізняку (Fe3O4) чи в червоному залізняку (Fe2O3)?
144. Що важче: 5 молекул води (H2O) чи одна молекула сульфатної кислоти (H2SO4)?
І
145. Який із символів відповідає:
а) елементу Калію (C, Ca, K);
б) елементу Сульфуру (C, S, Si)?
146. Серед наведених формул речовин виберіть формули простих речовин: Zn, ZnCl2, H2, HCl, O2, CaO.
147. У наведеному переліку виберіть назви речовин: скло, скляна колба, парафін, залізо, ліжко, ручка.
ІІ
148. Чому CO – складна речовина, а O2 – проста?
149. Що означають такі записи: 5C, 3Fe, 4Fe2O3, 2О2?
150. Як позначити хімічними символами:
а) п’ять атомів Магнію;
б) шість молекул речовини, кожна з яких складається з одного атома Магнію, одного атома Сульфуру і чотирьох атомів Оксигену? Визначте масову частку Сульфуру в одній молекулі цієї речовини.
ІІІ
151. До складу молекули входить атом Карбону і два атоми Оксигену. Напишіть формулу речовини і визначте масову частку Карбону.
152. Обчисліть масові частки елементів у харчовій соді (NaHCO3). Яка загальна кількість атомів у молекулі цієї речовини? Що можна сказати про якісний склад цієї речовини?
153. Запропонуйте спосіб розділення суміші піску, заліза та цукру.
IV
154. Що важче: 2 молекули води чи одна молекула нітратної кислоти (HNO3)?
155. До складу молекули кальцій карбонату входить один атом Кальцію, один атом Карбону і три атоми Оксигену. Запишіть хімічну формулу сполуки та обчисліть масові частки елементів у ній.
Виведення хімічних формул, якщо відомі масові частки хімічних елементів, що входять до складу даної речовини
Приклад 1. Вивести формулу сполуки, у якій міститься 11,1 % Гідрогену і 88,9 % Оксигену.
Позначимо число атомів Гідрогену у формулі сполуки через x, а число атомів Оксигену через y, тоді формула сполуки буде – HxOy.
Маса всіх атомів Гідрогену в молекулі дорівнює 1x, а маса всіх атомів Оксигену – 16y, де 1 і 16 – відносні атомні маси Гідрогену та Оксигену (Ar(H) = 1; Ar(O) = 16).
Відношення атомних мас у молекулі відповідає масовій частці елементів: 1x : 16y = 11,1 : 88,9.
Щоб знайти атомне відношення елементів у хімічній сполуці, поділимо вміст їх у відсотках за масою на відносні атомні маси. Відношення між атомами може бути виражене тільки цілими числами, тому менше число (5,55) умовно приймаємо за одиницю і ділимо на нього решту чисел. У даному випадку 11,1 : 5,55 = 2, атомне відношення 2:1.
Отже, x = 2, y = 1, а формулі HxOy відповідає формула H2O.
Відповідь: формулу сполуки H2O.
Приклад 2. До складу речовини входять 40 масових часток Купруму, 20 масових часток Сульфуру, 40 масових часток Оксигену. Яка формула цієї речовини?
Розв’язання:
Відповідь: З обчислень випливає, що у даній сполуці на 1 атом Купруму припадає 1 атом Сульфуру і 4 атоми Оксигену, отже хімічна формула сполуки – CuSO4.
Приклад 3. Масові частки Карбону і Гідрогену в речовині відповідно становлять 80% і 20%. Відносна молекулярна маса цієї речовини дорівнює 30. Встановіть молекулярну формулу речовини.
Ar(H) = 1;
Розв’язання:
І спосіб
ІІ спосіб
Відповідь: формула речовини – С2Н6.
Слід пам’ятати, що сума всіх масових часток елементів становить 1 або 100%. Тоді масові частки виражають масу кожного елемента у 100 грамах. Поділивши ці маси на відносні атомні маси, знаходимо відношення кількості атомів і записуємо найпростіші формули.
Обчислення масової частки елементів у певній масі речовини
Приклад 4. Оксид цинку масою 81 г містить Цинк масою 65 г і Оксиген масою 16 г. Які масові частки цих елементів у оксиді?
Розв’язання:
Відповідь: w(Zn) = 80,2%, w(O) = 19,8%.
Приклад 5. Загальна формула речовини ЕО. Її відносна молекулярна маса – 80. Масова частка Оксигену в ній 20%. Знайти елемент і написати хімічну формулу оксиду.
Розв’язання:
1. Знаходимо масову частку невідомого елементу за формулою речовини:
100% – 20% = 80 %.
3. Знаходимо молекулярну масу CuO:
Mr(CuO) = 64 + 16 = 80.
Відносна молекулярна маса CuO відповідає молекулярній масі окиду, даному в умові задачі.
Відповідь: Cu, CuO.
Завдання для самоконтролю
157. До складу речовини входять Купрум (66,6%) і Сульфур (33,4%). Яка формула цієї речовини?
158. До складу речовини входять Силіцій (46,67%) і Оксиген (53,33%). Яка формула речовини?
159. Загальна формула речовини – ЕО. Її відносна молекулярна маса – 80. Масова частка Оксигену в ній – 20%. Яка хімічна формула оксиду?
160. Відносна молекулярна маса оксиду чотиривалентного елемента – 60, а масова мастка Оксигену в ньому – 53,33%. Знайдіть формулу оксиду.
161. До складу сполуки входять: Гідроген (2,46%), Сульфур (39,02%) та Оксиген. Виведіть її хімічну формулу.
162. До складу речовини входять Гідроген (5,88%), і Сульфур (94,12%). Знайдіть формулу речовини.
163. Масова частка двовалентного метала в його оксиді становить 71,43%. Відносна молекулярна маса оксиду – 56. Знайдіть формулу оксиду.
164. До складу речовини входять Магній (20%), Сульфур (6,6%) і Оксиген (53,4%). Знайдіть формулу речовини.
165. Відносна молекулярна маса невідомої речовини у 10 разів більша за відносну молекулярну масу метану (CH4). До її складу входить 70% Феруму і 30% Оксигену. Знайдіть формулу речовини.
166. Визначте масову частку NaCl у суміші із 60 г NaCl і 15 г KCl?
167. Калій карбонат, або поташ, застосовують у виробництві скла, мила тощо. Його відносна молекулярна маса дорівнює 138, а масові частки Калію, Карбону та Оксигену становлять відповідно 56,5%, 8,7%, і 34,8%. Встановіть формулу речовини.
168. Карбон дисульфід використовують як розчинник органічних речовин. Знайдіть його молекулярну формулу, коли відомо, що масові частки Карбону та Сульфуру відповідно становлять 15,8% і 84,2%, а відносна молекулярна маса – 76.
169. Виведіть формулу карборунду, в якому масові частки Силіцію і Карбону становлять відповідно 70% і 30%, а відносна молекулярна маса дорівнює 40.
170. Виведіть формулу фосфіну, молекулярна маса якого 34, а масові частки Фосфору і Гідрогену відповідно становлять 91,2% та 8,8%.
У цьому параграфі ви повторите:
• що таке масова частка хімічного елемента в сполуці;
• за якою формулою обчислюють масову частку певного елемента в сполуці.
Масова частка хімічного елемента в складній речовині показує, яка частка відносної молекулярної маси речовини припадає на даний елемент.
Її обчислюють за формулою
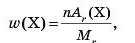
де w (X) — масова частка хімічного елемента X, виражена в частках одиниці; п — число атомів даного елемента, позначене індексом у формулі сполуки; Ar — відносна атомна маса X; Mr — відносна молекулярна або відносна формульна маса сполуки.
Часткою називають частину цілого, тому сума всіх часток дорівнює одиниці, або 100 %.
• Приклади розв’язування задач
Приклад 1. Обчисліть масові частки хімічних елементів у хлор(УП) оксиді Cl2O7.

Приклад 2. Масова частка Нітрогену в його оксиді дорівнює 36,84 %, а відносна молекулярна маса — 76. Якою може бути хімічна формула цієї сполуки: N2O, NO, N2O3 чи N2O5?

Запитання та тестові завдання
1. За якою формулою обчислюють масову частку елемента в його сполуці?
2. Чому дорівнює сума масових часток усіх елементів у сполуці?
3. У яких одиницях виміру її виражають?
4. Чи обов’язково, визначаючи масові частки елементів, потрібно враховувати число атомів цього елемента у формулі сполуки?
5. Масова частка Мангану має найбільше значення в сполуці: a) MnO2; б) Mn2O3; в) Mn3O4; г) Mn2O7.
6. Масова частка Хлору має найбільше значення в сполуці:
7. Масова частка Нітрогену в певному оксиді дорівнює 30,43 %. Його назва: а) нітроген(ІІІ) оксид; б) нітрогеи(І) оксид; в) нітроген(І\ ,г ) оксид; г) HiTporen(V) оксид.
8. Оксид з найбільшим умістом Оксигену в наведених сполуках — це: a) SO3; б) ClO3; в) CrO3; г) WO3.
9. Масова частка Сульфуру в алюміній сульфаті дорівнює:
а) 29,16%; 6) 28,07 %; в) 27,91%; г) 30,52 %.
10. Масова частка елемента в сполуці K2O5 дорівнює 56 %. Назва елемента E — це: а) Стибій; б) Арсен; в) Нітроген; г) Ванадій.
11. Масова частка Оксигеиу в оксиді чотиривалентного елемента дорівнює 65,2 %. Назва цього елемента: а) Силіцій;
б) Станум; в) Германій; г) Титан.
12. Обчисліть масові частки (%) елементів у сполуках:

13. У якій сполуці масова частка (%) Сульфуру найбільша:

* 14. Вищий оксид елемента має склад E2O5. Із Гідрогеном цей елемент утворює летку сполуку, масова частка Гідрогену в якій становить 38,46 %. Назвіть цей елемент.
Тема. Обчислення масової частки елемента в складі речовини.
Урок17
ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ
Тема 1
УСІ УРОКИ ХІМІЇ 7 клас
Цілі: поглиблення знань учнів про масову частку елемента в складі речовини; удосконалювання практичних навичок обчислення масової частки речовини, розв’язування задач на визначення формули речовини за масовими частками елементів, що входять до складу молекули речовини.
Тип уроку: поглиблення і коригування знань, закріплення практичних умінь і навичок.
Форми роботи: фронтальна робота, письмова самостійна робота.
Обладнання: періодична система хімічних елементів, картки із завданнями для фронтальної роботи, алгоритм.
І. Організація класу
ІІ. Актуалізація знань
1. Учень записує на дошці та пояснює формулу масової частки елемента в складі речовини.
2. Перевіряємо домашнє завдання (усне фронтальне опитування і коригування).
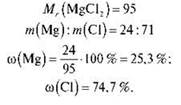
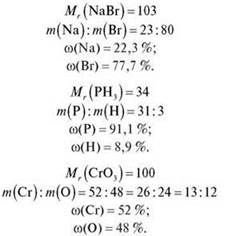
3. Обчисліть масові частки елементів у молекулі H2SO4.

ІІІ. Закріплення умінь і навичок
Завдання 1. Розташуйте речовини в порядку зростання масової частки Оксигену в складі молекули. (Заповнюємо таблицю на дошці.)
| Cu2O | Al2O3 | Fe2O3 | ZnO | WO3 | |
| Mr | |||||
| ω(О), % | 11,4 | 47,0 | 30,0 | 19,7 | 20,7 |
| Відповідь | I | V | IV | II | III |
Завдання 2. (Пояснення вчителя.) Деяка сполука Нітрогену з Окси- геном містить 63,2 % Нітрогену. Визначте формулу цієї речовини, якщо її молекулярна маса — 76 а.о.м.

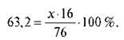

Отже, число атомів Оксигену — три.
2. m(N) = 76 – 3 · 18 = 28.
Знаючи, що Ar (N) = 14,
Отже, число атомів Нітрогену — два, а формула речовини — N2O3.
Завдання 3. Масова частка Карбону в його сполуці з Оксигеном — 27,3 %. Визначте формулу цієї сполуки, знаючи, що її відносна молекулярна маса — 44.
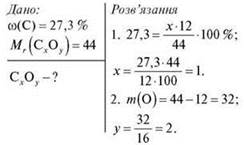
Завдання 4. Масова частка Купруму в сполуці з Оксигеном дорівнює 88,9 %. Відносна молекулярна маса цієї сполуки — 144. Визначте формулу сполуки CuxOy .

IV. Письмова самостійна робота за варіантами
Завдання 1. За хімічною формулою речовини:
• опишіть якісний склад молекули;
• опишіть кількісний склад молекули;
• обчисліть масові частки елементів у складі молекули цієї речовини.
| Варіант I | Варіант II | Варіант III |
| FeCl3 | P2O5 | C3H8 |
| Cu(OH)2 | Fe(OH)3 | Al(OH)3 |
| Na2SO4 | K2CO3 | Na3PO4 |
Завдання 2. За відомою масовою часткою Хлору в складі речовини та атомною молекулярною масою виведіть формулу цієї речовини.
| Mr (MgxClу) = 95 | Mr (AlxClу) = 133,5 | Mr (FexClу) = 162,5 |
| ω(Cl) = 74,7 % | ω(Сl) = 79 % | ω(Сl) = 65 % |
V. Домашнє завдання
Творче завдання. До складу молекули харчової соди входять атоми Натрію, Гідрогену, Карбону й Оксигену. Масові частки елементів відповідно дорівнюють: ω(Na) = 27,4 %; ω(H) = 1,2 %; ω(С) = 14,3 %; ω(О) = 57,1 %. Визначте формулу питної соди й обчисліть її відносну молекулярну масу.
ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Ви є тут

Завдання 1–40 мають чотири варіанти відповіді, серед яких лише один правильний. Виберіть правильний, на Вашу думку, варіант відповіді
1. Укажіть хімічне явище.
горіння деревини
2. У якому рядку найбільше неметалічних елементів?
S, Se, Sc
3. Скільки електронів в атомі Оксигену?
8
4. Укажіть число елементів і число атомів у складі сполуки, формула якої СН 3 СООН.
3 і 8
5. У якому рядку наведено формули лише йонних сполук?
Na 2 S, KCl, CaBr 2
6. Який тип кристалічних ґраток у бінарній сполуці хімічних елементів із протонними числами 9 і 19?
йонні
7. Укажіть порядковий номер хімічного елемента Е, який належить до III періоду періодичної системи й утворює летку сполуку з Гідрогеном складу ЕН 3 .
15
8. У прилад, що зображений на рисунку, помістили водний розчин речовини X і тверду речовину У. Укажіть формули речовин X і Y.
X - HCl
Y - Zn
9. Які речовини реагують між собою у водному розчині?
AgN0 3 і КС1
10. Необоротна реакція відбувається у водному розчині між
8
12. Укажіть правильний запис рівняння реакції між ферум (ІІ) гідроксидом і хлоридною кислотою в повній йонній формі.
13. Укажіть формулу оксиду, який реагує з водою з утворенням лугу.
BaO
14. Яку з речовин можна добути взаємодією металу з водою?
15. До складу одноосновної кислоти входять
катіон Гідрогену та аніон кислотного залишку.
16. Укажіть формулу кислої солі.
17. У якому рядку наведено формули лише тих речовин, які виявляють амфотерні властивості?
18. Яка речовина реагує із залізом з утворенням ферум(ІІ) хлориду?
HCl
19. У якій групі періодичної системи (коротка форма) містяться лише металічні елементи?
II
20. Під час виконання домашнього лабораторного досліду учневі потрібно було довести, що складовими порошкоподібного універсального засобу для чищення є карбонати Кальцію і Магнію. Йому вдалося це зробити за допомогою
cтолового оцту.
21. Укажіть формулу речовини, із якою реагує алюміній, якщо внаслідок цього утворюється алюміній сульфат.
22. Укажіть продукти термічного розкладання ферум(ІІІ) гідроксиду.
23. Спільним в електронній будові атомів Хлору та Йоду є
число електронів на зовнішньому енергетичному рівні.
24. Укажіть формулу речовини X у схемі хімічної реакції
25. Із якою речовиною реагує амоніак?
26. Між якими речовинами потрібно провести реакцію, щоб добути карбон (IV) оксид?
СаСО 3 і HNО 3
27. Укажіть назву речовини, яка належить до гомологічного ряду вуглеводнів із загальною формулою С n Н 2n-2 .
пропін
28. Укажіть за номенклатурою IUPAC назву речовини, структурна формула якої
3,4,6 -триметилоктан
29. Укажіть формулу гомолога метану.
30. Укажіть число структурних ізомерів, що відповідає формулі С4Н8.
5
32. Укажіть співвідношення між кількостями речовин бензену й водню в рівнянні хімічної реакції, продуктом якої є циклогексан.
1 : 3
33. Укажіть продукт перегонки нафти.
газойль
34. Фенол реагує з
натрій гідроксидом.
35. Укажіть формулу речовини X у схемі хімічної реакції
СН 3 СНО
36. Моносахаридами є
фруктоза і глюкоза.
37. Проаналізуйте твердження й укажіть, чи є поміж них правильні.
І. Добування твердого жиру з олії ґрунтується на реакції гідролізу.
ІІ. Добування твердого жиру з олії ґрунтується на реакції гідрування.
правильне лише II
38. Які твердження характеризують аміноетанову кислоту?
1 використовують для добування капрону
2 можна одержати гідролізом білка
3 містить лише одну функціональну групу
4 є амфотерною сполукою
Варіанти відповіді:
2,4
39. Під час лабораторного досліду учениця поклала зразок поліетилену на керамічну підставку й обережно нагріла. Коли полімер розм'якшився, вона за допомогою скляної палички змінила форму зразка. Охолоджений зразок знову нагріла і знову змінила його форму. Це свідчить про те, що досліджуваний полімер є
термопластичним.
40. Укажіть речовину X у схемі хімічної реакції
метан
У завданнях 41–46 до кожного з чотирьох рядків інформації, позначених ЦИФРАМИ, виберіть один правильний, на Вашу думку, варіант, позначений БУКВОЮ.
41. Установіть відповідність між схемою та типом хімічної реакції.
42. Установіть відповідність між схемою та типом хімічної реакції.
43. Установіть відповідність між тривіальною назвою та формулою речовини.
44. Установіть відповідність між формулою та природою речовини.
| Формула речовини | Природа речовини |
| Са(ОН) 2 | основа |
| СаО | основний оксид |
| Н 2 SO 3 | кислота |
| Мg 3 (РO 4 ) 2 | сіль |
45. Установіть відповідність між формулою та природою речовини.
| Формула речовини | Природа речовини |
| CH 3 OH | спирт |
| HCHO | альдегід |
| C 2 H 2 | алкін |
| C 6 H 5 NH 2 | амін |
46. Установіть відповідність між назвою речовини та одним зі способів її добування.
| Назва речовини | Спосіб добування |
| глюкоза | гідроліз крохмалю |
| етаналь | гідратація ацетилену |
| анілін | відновлення нітробензену |
| фенол | гідроліз хлоробензену |
У завданнях 47 48 розташуйте факти (явища, процеси тощо) у правильній послідовності.
47. Установіть послідовність використання речовин під час добування метанової кислоти
1- метан
2 - хлорометан
3 - метанол
4 - м етаналь
48. Установіть послідовність використання процесів і речовин під час здійснення ланцюжка перетворень
1 - бромідна кислота
2 - натрій гідроксид
3 - кисень і вода
4 - нагрівання
Розв'яжіть завдання 49–60. Одержані числові відповіді запишіть у зошиті та бланку
49. Масова частка води в кристалогідраті натрій сульфіту становить 50 % . Укажіть число молекул води у формулі цього кристалогідрату.
Відповідь: 7
50. Обчисліть об'єм (л) водню масою 5 г (н. у.).
Відповідь: 56
51. Обчисліть відносну молекулярну масу речовини, формула якої СН3NНС2Н5.
Відповідь: 59
52. Обчисліть відносну молекулярну масу газу, відносна густина якого за киснем 2
Відповідь: 64
53. На суміш масою 10 г, що складається із заліза та міді, подіяли надлишком розбавленої сульфатної кислоти, унаслідок чого виділився газ об'ємом 2,8 л (н. у.). Обчисліть масову частку (%) заліза в суміші.
Відповідь: 70%
54. Обчисліть масу (г) кухонної солі, яку потрібно взяти для приготування фізіологічного розчину масою 9 кг із масовою часткою солі 0,9 % .
Відповідь: 81 г
55. Скільки різновидів молекул води може утворитися з нукліда Оксигену 16 О та ізотопів Гідрогену 1 Н, 2 Н і 3 Н?
Відповідь: 6
56. Обчисліть масу (г) Фосфору у фосфор (V) оксиді кількістю речовини 0,5 моль.
Відповідь: 31
57. Використовуючи метод електронного балансу, перетворіть схему реакції
на хімічне рівняння та вкажіть коефіцієнт перед формулою окисника.
Відповідь: 2
58. Виведіть молекулярну формулу органічної речовини, що складається з Карбону, Гідрогену та Оксигену. Масова частка Карбону в ній становить 72 %, Гідрогену – 12%. Відносна густина пари цієї речонини за воднем дорівнює 50. У відповідь запишіть число, що дорівнює сумі індексів у виведеній формулі.
У відповіді запишіть число, що дорівнює сумі індексів у виведеній формулі
Відповідь: 19
59. Для проведення реакції взято метал масою 9,2 г і воду в надлишку. Унаслідок реакції виділився водень кількістю речовини 0,2 моль і утворився гідроксид одновалентного металічного елемента. Визначте молярну масу (г/моль) металу.
Відповідь: 23
60. Обчисліть масу (г) продукту реакції, для проведення якої взято водень масою 4 г і бром масою 160 г, якщо відносний вихід продукту реакції становить 50 % .
Читайте также:

