Нейроэндокринная опухоль поджелудочной железы кт
а) Терминология:
1. Аббревиатура:
• Нейроэндокринная опухоль (НЭО) поджелудочной железы
2. Синоним:
• Островковоклеточная опухоль
3. Определение:
• Опухоль из эндокринных клеток ПЖ (островков Лангерганса)
4. Ассоциированные синдромы:
• Множественная эндокринная неоплазия первого типа (МЭН 1, гастриномы), синдром Гиппеля-Линдау, нейрофиброматоз первого типа, туберозный склероз
б) Визуализация:
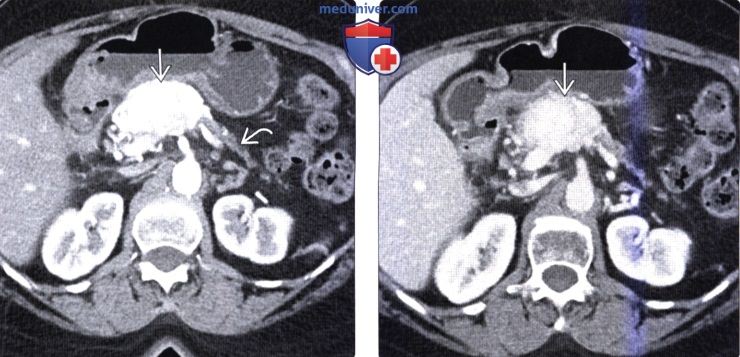
(Слева) На КТ в артериальной фазе контрастного усиления в шейке поджелудочной железы определяется объемное образование, активно накапливающее контраст (нейроэндокринная опухоль). Вышележащие отделы поджелудочной железы в значительной степени атрофированы что не является типичным признаком нейроэндокринных опухолей, которые чаще всего не становятся причиной обструкции панкреатического протока и атрофии паренхимы поджелудочной железы.
(Справа) На аксиальной КТ в венозной фазе контрастного усиления у этого же пациента опухоль по-прежнему накапливает контраст, но в значительно меньшей степени, чем в артериальной фазе. 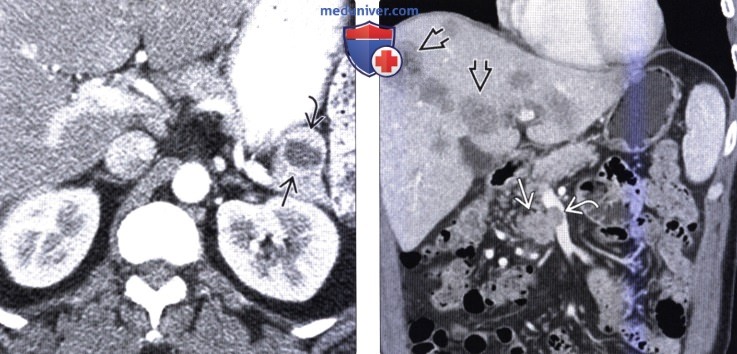
(Слева) На аксиальной КТ с контрастным усилением определяется кистозное образование в хвосте поджелудочной железы. В этом случае нельзя исключать внутрипротоковую папиллярно-муцинозную опухоль или муцинозную кистозную опухоль, но периферический характер контрастного усиления и наличие мягкотканного компонента, накапливающего контраст, позволяет сделать заключение о кистозной нейроэндокринной опухоли.
(Справа) На корональной КТ с контрастным усилением визуализируется гиповаскулярное объемное образование в крючковидном отростке поджелудочной железы на фоне многочисленных метастазов в печени.Опухоль прорастает в верхнюю брыжеечную вену, что не типично для аденокарциномы, и больше характерно для нейроэндокринной опухоли. 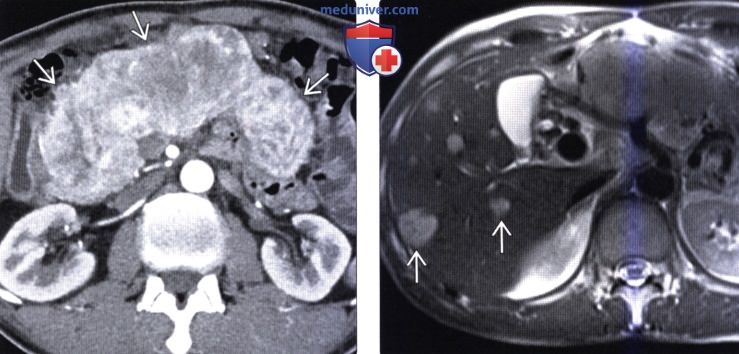
(Слева) На аксиальной КТ в артериальной фазе контрастного усиления визуализируется массивная гиперваскулярная нейроэндокринная опухоль, практически полностью замещающая поджелудочную железу. Несиндромные опухоли, как в этом случае, часто имеют большие размеры на момент их обнаружения.
(Справа) На аксиальной Т2 взвешенной томограмме у этого же пациента визуализируются гиперинтенсивные очаги в печени. Несмотря на то, что они могут с легкостью быть ошибочно расценены как кисты или гемангиомы, нужно учитывать, что метастазы нейроэндокринных опухолей в печень также могут обладать крайне высокой интенсивностью сигнала на Т2 ВИ.
3. МРТ признаки нейроэндокринной опухоли поджелудочной железы:
• Нейроэндокринные опухоли имеют тенденцию быть гипоинтенсивными по сравнению с паренхимой поджелудочной железы в норме на Т1 ВИ, являются гиперинтенсивными на Т2 ВИ, и накапливают контраст на Т1 ВИ с контрастным усилением, так же, как и на КТ:
о Небольшие опухоли 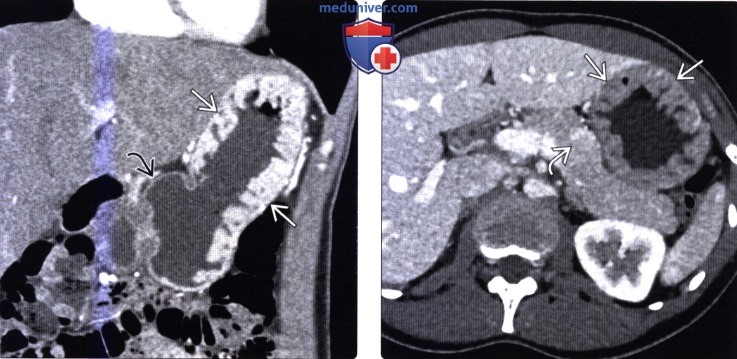
(Слева) На корональной КТ с контрастным усилением определяется выраженное утолщение складок и повышенное контрастное усиление стенки проксимальных отделов желудка. Стенка желудка в более дистальных отделах имеет нормальную толщину. Эти изменения типичны для синдрома Золлингера-Эллисона.
(Справа) На аксиальной КТ в венозной фазе контрастного усиления у этого же пациента, на фоне выраженного утолщения складок в проксимальных отделах желудка, визуализируется объемное образование в теле поджелудочной железы, слабо накапливающее контраст, и представляющее собой гастриному. В этом случае образование не было различимо в артериальной фазе, что нетипично для нейроэндокринных опухолей. 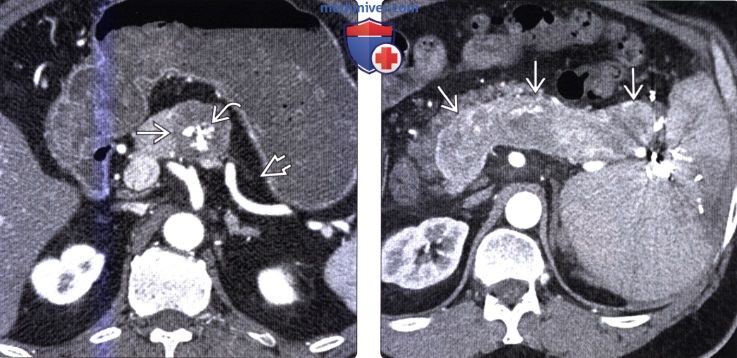
(Слева) На аксиальной КТ с контрастированием в теле поджелудочной железы визуализируется гиподенсное объемное образование с кальцинатами в центре. Обратите внимание на атрофию дистальных отделов поджелудочной железы, нетипичную для нейроэндокринных опухолей. Приблизительно 15% нейроэндокринных опухолей содержат кальцинаты (аденокарциномы поджелудочной железы практически никогда не обызвествляются).
(Справа) На аксиальной КТ с кон -трассированием визуализируется нейроэндокринная опухоль, прорастающая в селезеночную вену и вызывающая ее расширение. Нейроэндокринные опухоли в отличие от аденокарцином поджелудочной железы не вызывают окклюзию брыжеечных вен, но могут прорастать в них, образуя гиперваскулярные опухолевые тромбы. 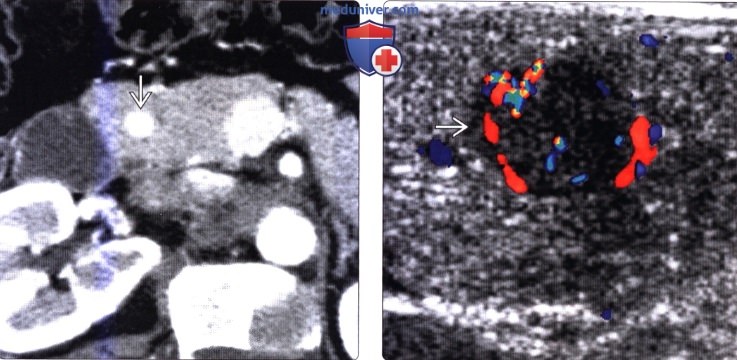
(Слева) На аксиальной КТ с контрастным усилением у пациента с клиническим подозрением на инсулиному определяется маленькое гиперваскулярное образование в головке поджелудочной железы.
(Справа) На сонограмме (интраоперационная ультрасонография) у этого же пациента определяется гиперваскулярное гипоэхогенное образование, не обнаруживаемое при пальпации. Пациенту была выполнена операция Уиппла, при патоморфологическом исследовании обнаружилась инсул и нома. Интраоперационная ультрасонография имеет очень большое значение для определения местоположения маленьких нейроэндокринных опухолей и контроля при выполнении резекционного вмешательства.
в) Дифференциальная диагностика нейроэндокринной опухоли поджелудочной железы:
1. Интрапанкреатическая долька селезенки:
• Хвост поджелудочной железы - второе по распространенности место расположения добавочной селезенки
• Характеристики контрастного усиления добавочной селезенки аналогичны основной
2. Протоковый рак поджелудочной железы:
• Гиповаскулярная опухоль инфильтративного характера, вызывающая обструкцию ППЖ и/или ОЖП и атрофию паренхимы ПЖ
• В отличие от нейроэндокринных опухолей практически никогда не содержит обызвествления
• Охватывает брыжеечные вены и вызывает сужение их просвета, но не приводит к появлению опухолевых тромбов
3. Вторичное поражение поджелудочной железы:
• Гиперваскулярные метастазы в поджелудочной железе (преимущественно почечноклеточного рака) неотличимы от НЭО
5. Гастроинтестинальная стромальная опухоль, прилежащая к поджелудочной железе:
• Новообразование желудка или двенадцатиперстной кишки может имитировать НЭО ПЖ, особенно, если активно накапливает контраст
г) Патология. Общая характеристика:
• Этиология:
о Опухоль возникает из апудоцитов (APUD-клеток), в которых происходит накопление аминов-предшественников о Патогенез и проявления:
- Инсулинома: опухоль из бета-клеток → гиперинсулинемия — гипогликемия
- Гастринома: островковоклеточная опухоль → повышение секреции гастрина → повышение кислотности желудочного сока → пептические язвы
- Глюкагонома: опухоль из альфа-клеток → ↑ уровня глюкагона → классическая кожная сыпь и сахарный диабет
• Генные изменения:
о МЭН 1 (гиперпаратиреоз, аденома гипофиза, НЭО ПЖ):
- Заболевание с аутосомно-доминантным типом наследования
- В 80% случаев приводит к развитию НЭО, часто множественных
д) Клинические особенности:
1. Проявления:
• Типичные признаки/симптомы:
о Синдромальные опухоли:
- Инсулинома: симптомы гипогликемии, I уровня глюкозы ( 2 см) напрямую связан с вероятностью ее злокачественности
3. Течение и прогноз:
• Прогноз намного лучше, чем при аденокарциноме ПЖ
• Прогноз при инсулиноме - обычно доброкачественной опухоли, очень благоприятный; при гастриноме - неблагоприятный
• При несиндромных опухолях пятилетняя выживаемость составляет лишь 44%
• Пациенты могут жить с метастазами в течение многих лет
4. Лечение:
• Аналоги соматостатина, такие как октреотид, применяются для снижения выраженности симптоматики при синдромальных опухолях за исключением соматостатиномы
• При синдромальных или доброкачественных несиндромных НЭО при отсутствии метастазов необходимо хирургическое вмешательство (резекция)
• НЭО, распространяющиеся за пределы ПЖ, при отсутствии метастазов должны удаляться если это возможно, даже если не удается добиться отсутствия клеток опухоли по краю резекции:
о Оперативное вмешательство позволяет снизить выраженность симптоматики и улучшить выживаемость
• Резекция первичной НЭО, даже при наличии метастазов в печени, может способствовать увеличению выживаемости
о В некоторых случаях может быть выполнена резекция или циторедуктивная операция (при метастазах в печени)
• У пациентов с печеночной недостаточностью и метастазами, ограниченными печенью, возможна трансплантации печени
е) Список использованной литературы:
1. Kawamoto S et аI.: Pancreatic neuroendocrine tumor with cystlike changes: evaluation with MDCT. AJR Am J Roentgenol. 200(3):W283-90, 2013
Редактор: Искандер Милевски. Дата публикации: 12.3.2020
Поджелудочная железа – один из наиболее важных органов человеческого тела. Она выполняет одновременно две абсолютно разные функции: эндокринную и пищеварительную. Заболевания поджелудочной железы изучается уже много веков. Множество информации накопилось до настоящего времени о клинических проявлениях и лабораторных признаках различных патологий данного органа. Это позволяет современным клиницистам выявлять и проводить терапию множества известных заболеваний поджелудочной железы.
Снижение трудоспособности лиц молодого возраста – важнейшая экономическая и социальная проблема настоящего, требующая от современной медицины активной деятельности в вопросах максимально раннего выявления патологического процесса и своевременно начатого лечений.
МРТ – является одним из современных и наиболее высокоточных методов диагностики, способствующий решению поставленных вопросов.
Наиболее частой патологией, с которой приходится сталкиваться клиницистам, являются воспалительные процессы в поджелудочной железе – панкреатит.
Выделяют панкреатит острый, характеризующийся активацией пищеварительных ферментов железы еще до выхода их в кишечник и, соответственно, воздействием этих ферментов на ткань самой железы.


Острый панкреатит с формированием парапанкреатических абсцессов.
Хронический панкреатит представляет собой прогрессирующее заболевание поджелудочной железы воспалительного характера с периодами ремиссий и обострений патологического процесса, приводящее к дистрофическим изменениям органа, разрастанию в нем соединительной ткани и снижению выработки ферментов и гормонов.
Клинически периоды обострения хронического панкреатита мало чем отличаются от приступа острого панкреатита.
Патоморфологически выделяют следующие типы хронического панкреатита:
Хронический атрофический панкреатит - характеризуется локальным или диффузным уменьшением размеров железы, фиброзом, кальцинозом и жировой дистрофией ее паренхимы.

Хронический атрофический панкреатит.
Хронический псевдотуморозный панкреатит - характеризуется локальным или диффузным увеличением размеров железы, фиброзом, кальцинозом, жировой дистрофией паренхимы, наличием псевдокист.

Псевдотуморозная форма хронического панкреатита.

Псевдотуморозная форма хронического панкреатита.
IPMN (Intraductal Papillary Mucinous Neoplasms) – внутрипротоковая папиллярная опухоль.

Хронический фиброзно-кистозный панкреатит.
При выявлении опухолевых заболеваний поджелудочной железы метод МРТ является наиболее информативным среди других способов диагностики.
МРТ позволяет четко визуализировать опухоль, независимо от ее размеров; проводить дифференциальную диагностику различных видов опухолей и метастатического поражения поджелудочной железы; достоверное выявлять билиарную гипертензию и расширение Вирсунгова протока.
Поджелудочная железа подвержена развитию таких опухолевых процессов, как аденокарцинома и цистаденокарцинома (низко- и высокодифференцированная), инсулинома (нейроэндокринная опухоль), лимфома, метастазы.
Представляет собой злокачественную опухоль, исходящую из клеток, выстилающих панкреатический проток.
Клинически обычно длительное время никак себя не проявляет, пока не достигнет больших размеров. Первыми симптомами являются боль в животе и потеря веса.

Рак тела поджелудочной железы (аденокарцинома). Достоверная визуализация опухоли без увеличения размеров железы, расширение Вирсунгова протока хвоста железы.
В большинстве случаев опухоль локализуется в головке поджелудочной железы, т.е. в максимальной близости в ДПК и общему желчному протоку. При крупных размерах образование приводит к развитию механической желтухи. Проявляющейся желтушным окрашиванием кожных покровов и склер.

Рак головки поджелудочной железы.
Это кистозная многокамерная опухоль с наличием узлов и перегородок разной толщины, характеризующаяся экспансивным ростом. При больших размерах также возможна обструкция протока поджелудочной железы и развитие механической желтухи.

Цистаденокарцинома поджелудочной железы.
Представляет собой гормонально-активную опухоль β-клеток поджелудочной железы, секретирующая в избыточном количестве инсулин, что приводит к гипогликемии.
Приступы гипогликемии при инсулиноме проявляются тахикардией, тремором, парестезиями, холодным потом, чувством голода и страха, а также зрительными. Речевыми и поведенческими нарушениями.
В тяжелых случаях развивается гипогликемическая кома.

Небольшая инсулинома хвоста поджелудочной железы.
Кроме первичных опухолей поджелудочная железа также подвержена метастазированию из других органов. Наиболее часто ПЖ поражают метастазы при раке желудка. При саркоме, меланоме, гепатоме, хорионэпителиоме (раке женских половых органов), раке легких, яичников, молочных желез и предстательной железы – метастазирование в поджелудочную происходит намного реже.

Высокая выявляемость метастазов печени и высокая контрастность опухоли хвоста ПЖ при МРТ.

Множественные метастазы в поджелудочную железу.
Опухоли поджелудочной железы, даже зачастую небольших размеров, способны приводить к обструкции желчевыводящих путей с развитием билиарной гипертензии.

Малых размеров объемное образование поджелудочной железы (1); билиарная гипертензия (2).
Локализация НЭО крайне разнообразна, но чаще всего они обнаруживаются в органах пищеварительной системы (более 50 %): прямая (17,2 %) и тонкая кишка (13,4 %), желудок (6,0 %), поджелудочная железа (6–7 %). НЭО занимают второе место в общей структуре онкологической патологии ЖКТ, уступая лидерские позиции лишь колоректальному раку. Около 27 % случаев НЭО возникают в легких (согласно базе данных Surveillance, Epidemiology, and End Results (SEER) 1975-2016) [1].
Еще недавно обсуждались вопросы включения НЭО в список орфанных заболеваний. Но в настоящее время отмечается увеличение частоты встречаемости этой патологии, в том числе из-за улучшения диагностических возможностей (в частности, распространение гастроскопии, колоноскопии, капсульной эндоскопии).
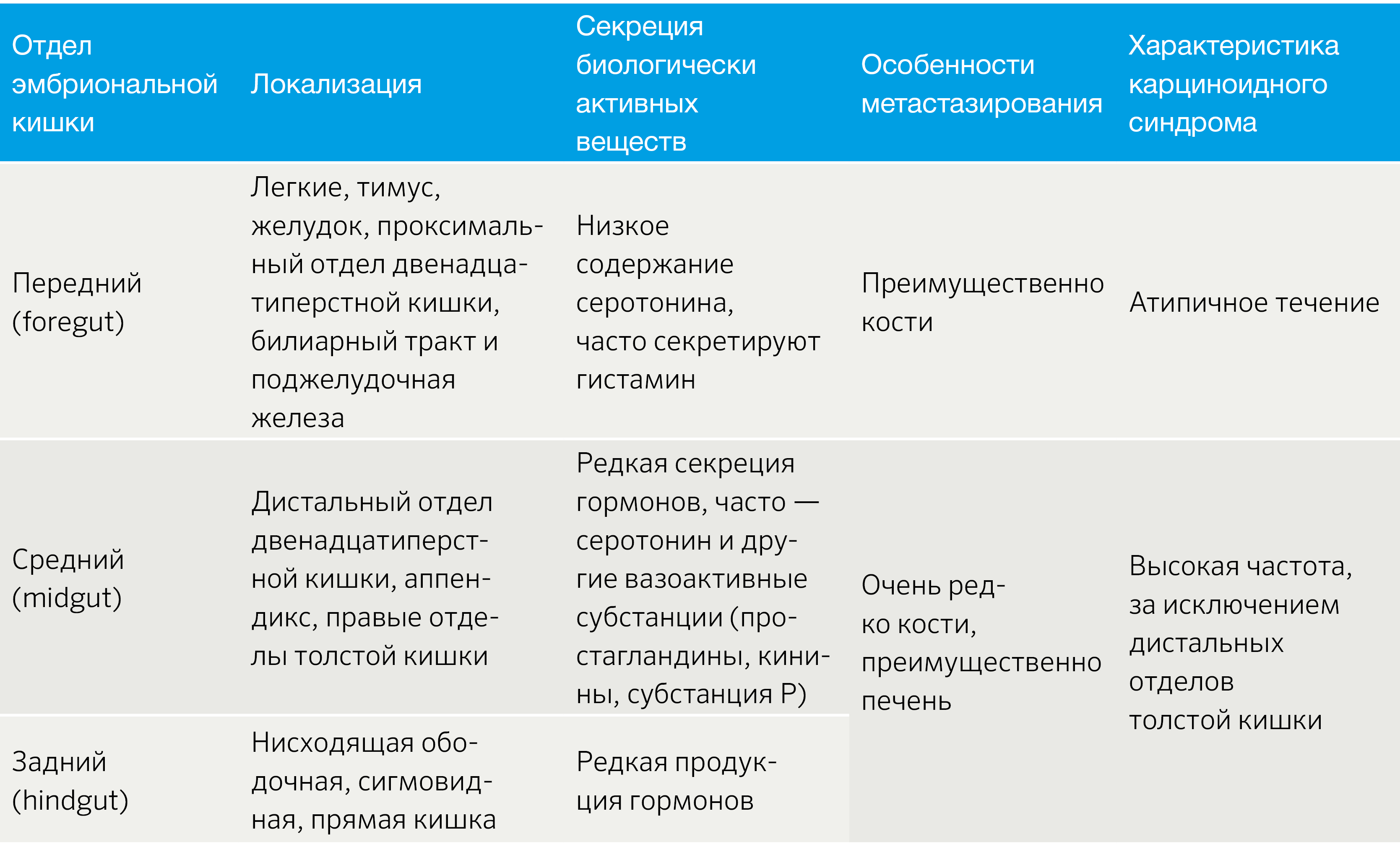
НЭО классифицируют в зависимости от отдела эмбриональной кишечной трубки: из передней, средней и задней кишки (табл. 1) [2].
Табл.1 | Классификация НЭО по эмбриогенезу [2].
Карциноидный синдром — важный клинический признак. В основном, он обусловлен эффектами серотонина, а также брадикинина, гистамина, дофамина и в меньшей степени других биологически активных веществ (БАВ).
Клинические проявления карциноидного синдрома разнообразны. Наиболее часто у пациентов отмечается гиперемия кожи лица, приливы, диарея, боль в животе. У 60 % пациентов отмечают формирование карциноидной болезни сердца, с нарушением работы преимущественно клапанного аппарата правых отделов (стеноз и/или недостаточность легочного и трехстворчатого клапанов). Серьезным осложнением является декомпенсация нарастающей сердечной недостаточности. Морфологическим субстратом служит выраженный диффузный фиброэластоз эндокарда. Возможны появления телеангиоэктазий, одышки, пеллагры, бронхоспазма. Усиливается продукция соединительнотканных компонентов, в частности, коллагена. Это ведет к фиброзированию и стенозу брыжеечных артерий, фиброзирующему стенозу уретры. Ввиду склонности к развитию спаечного процесса в брюшной полости нарастает риск формирования кишечной непроходимости.
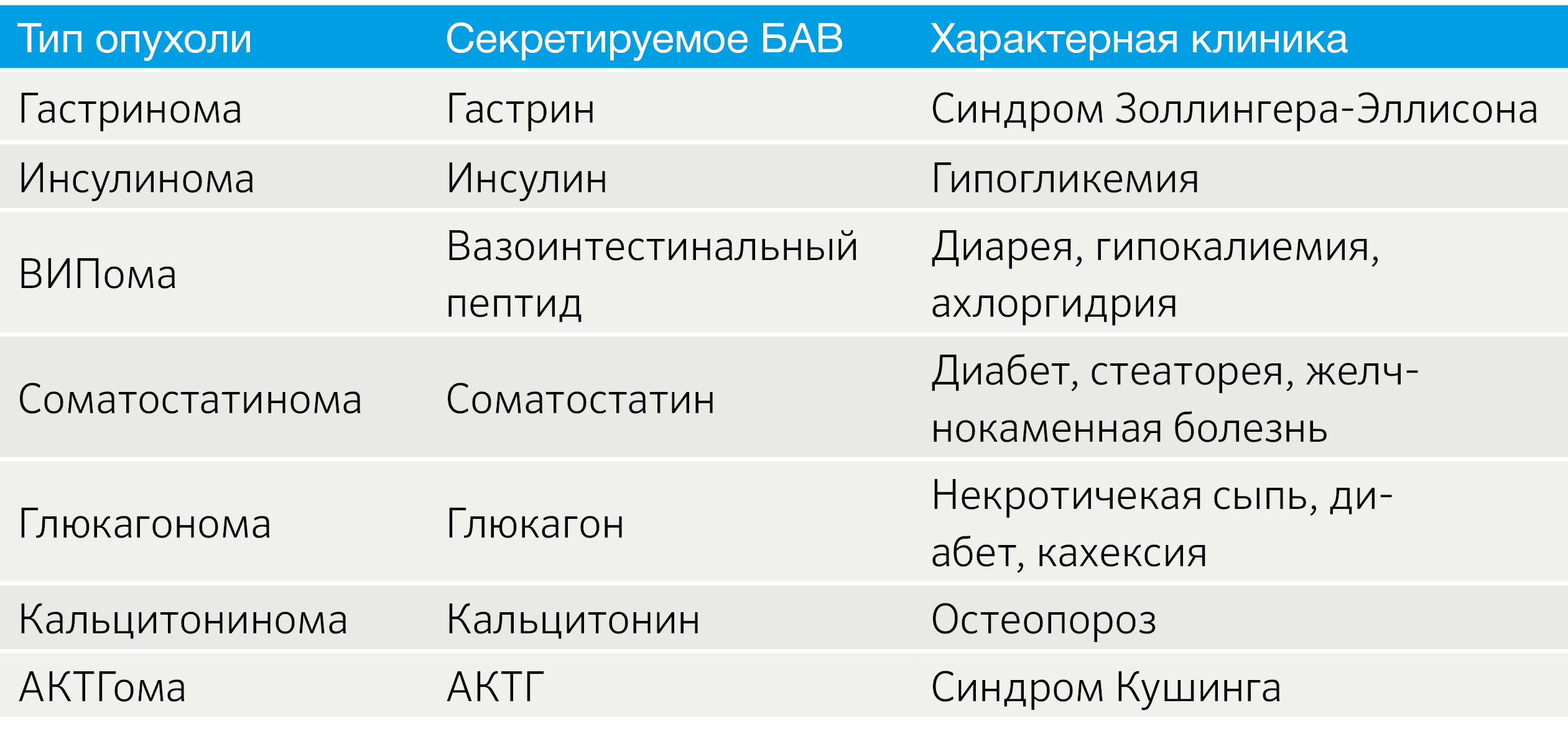
Важным аспектом является функциональный статус опухоли. В зависимости от наличия продукции БАВ выделяют функционирующие (табл. 2) и нефункционирующие новообразования [3].
Табл.2 | Функционирующие НЭО [3].
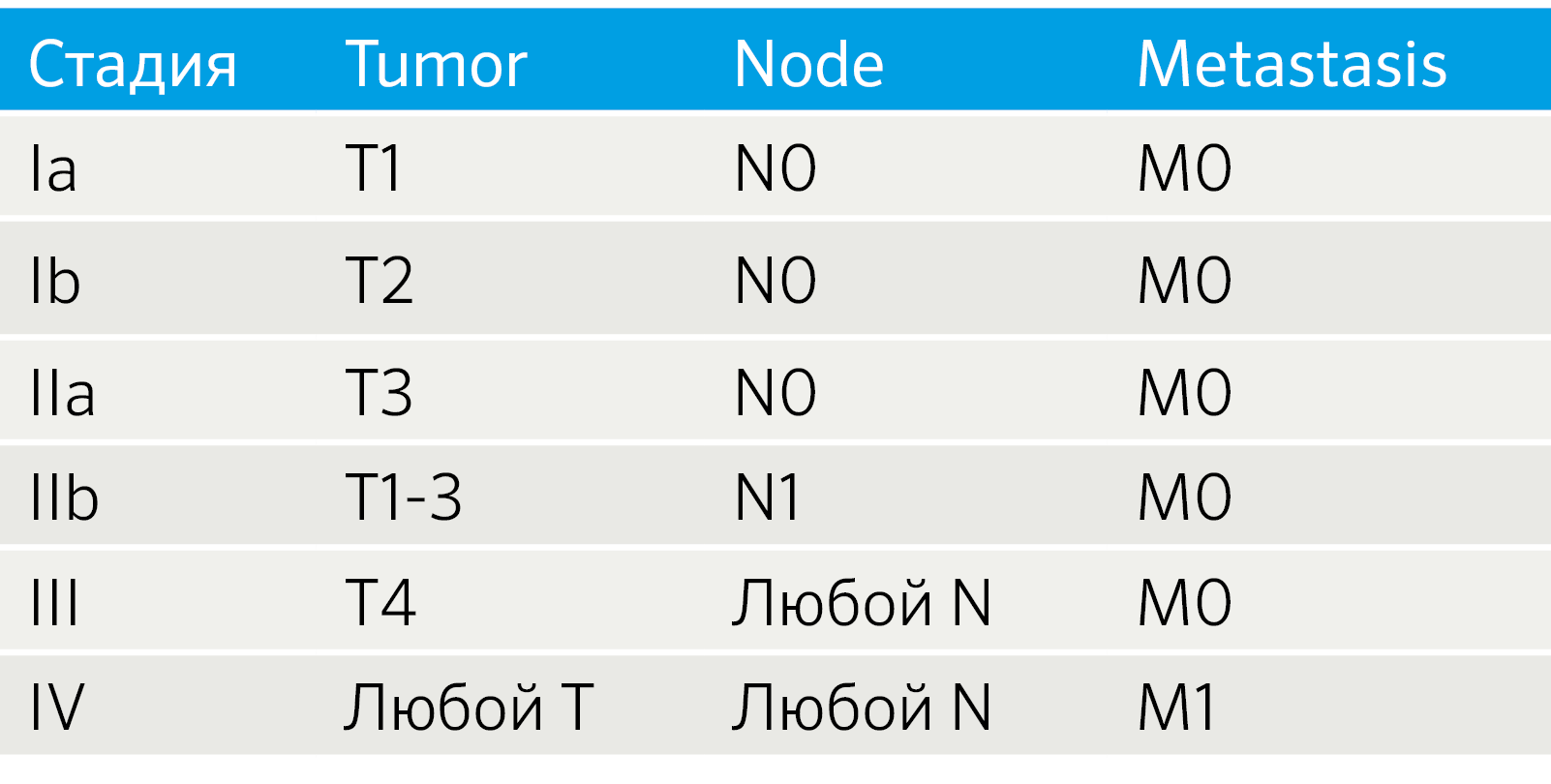
Особенности TNM-классификации определяются локализацией НЭО. НЭО легких стадируются как немелкоклеточный рак легких, для НЭО ЖКТ и поджелудочной железы разработаны рекомендации Европейского общества по изучению НЭО (ENETS) [4]. Также установление стадии TNM для всех анатомических локализаций регламентируется руководством, созданным Американским объединенным комитетом по раковым заболеваниям (the American Joint Committee on Cancer, AJCC) [5, 6]. Так как эти системы не идентичны, возникают вопросы унификации подходов к стадированию. Например, была создана модифицированная система ENETS (mENETS), для диагностики НЭО поджелудочной железы (pNET) (табл. 3) [7].
Табл.3 | Стадирование НЭО поджелудочной железы согласно модифицированной системе ENETS (mENETS) [7].
И вот мы подходим к той черепахе, на которой стоят киты онкологической диагностики. Это, несомненно, гистологическая верификация диагноза. Как и многие опухолевые заболевания, морфологические градации НЭО подвергались различным модификациям, уточнениям, дополнениям. Дискуссии в этой области в итоге привели к созданию 4-ой редакции классификации ВОЗ (2017 год) [8]. Именно она является актуальной на настоящий момент и заключение при проведении патологоанатомическом исследовании должно отвечать введенным в ней понятиям и требованиям.
Параметрами морфологической оценки нейроэндокринных новообразований являются: гистологическое строение опухоли, определение сосудистой и периневральной инвазии, митотический индекс. Несмотря на многообразия источников НЭО, морфологическая картина является сходной (рис. 1) [9].
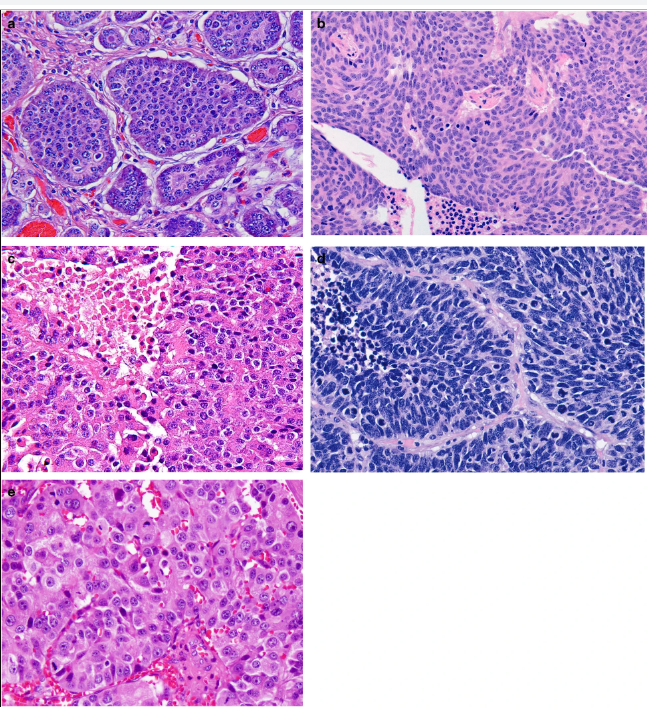
Нейроэндокринное происхождение атипичных клеток доказывает положительная экспрессия так называемых общих нейроэндокринных маркеров. Основные из них это хромогранин А, окрашивающий компоненты нейросекреторных гранул, и пептид синаптофизин, накапливающийся в мелких синаптических везикулах. Также применяется дополнительно установление экспрессии рецепторов соматостатина 2 и 5 типов (SSTR2 и SSTR5). В этом случае возможно определить чувствительность опухолевых клеток к аналогам соматостатина.
Степень злокачественности НЭО определяют на основании двух основных критериев: уровня дифференцированности опухолевых клеток и их пролиферативной активности. Традиционно выделяют три степени злокачественности (grade): G1, G2, G3. Для НЭО ЖКТ и поджелудочной железы введены понятия высокодифференцированных и низкодифференцированных новообразований (или нейроэндокринного рака (карциномы), НЭР). Высокодифференцированные НЭО объединяют G1 (менее 2 митозов на 10 репрезентативных полей зрения (РПЗ) при большом увеличении микроскопа (х400) и индекс Ki-67 ≤ 2%), G2 (2–20 митозов на 10 РПЗ и индекс Ki-67 3–20 %), G3 (> 20 митозов на 10 РПЗ и индекс Ki-67 > 20 %). Grade 3 опухоли разделяют на мелко- и крупноклеточный рак. Опухоли мелкоклеточного типа построены из однотипных клеток округлой, овальной или вытянутой формы, мелкого размера, со скудной цитоплазмой и нечеткими границами. Ядра имеют характерный вид за счет нежного хроматина и невизуализирующихся ядрышек. Определяются массивные некрозы. Крупноклеточные НЭР образованы, соответственно, клетками крупного или среднего размера, с низким ядерно-цитоплазматическим соотношением, выраженной атипией ядер, содержащих гранулярный хроматин и четкие ядрышки. В опухолевой ткани выявляются мультифокальные некрозы, значительное число митозов [8, 9].
Индекс Ki-67 определяют как средний процент окрашенных ядер при учете 500–2000 злокачественно трансформированных клеток (рис. 2) [9].
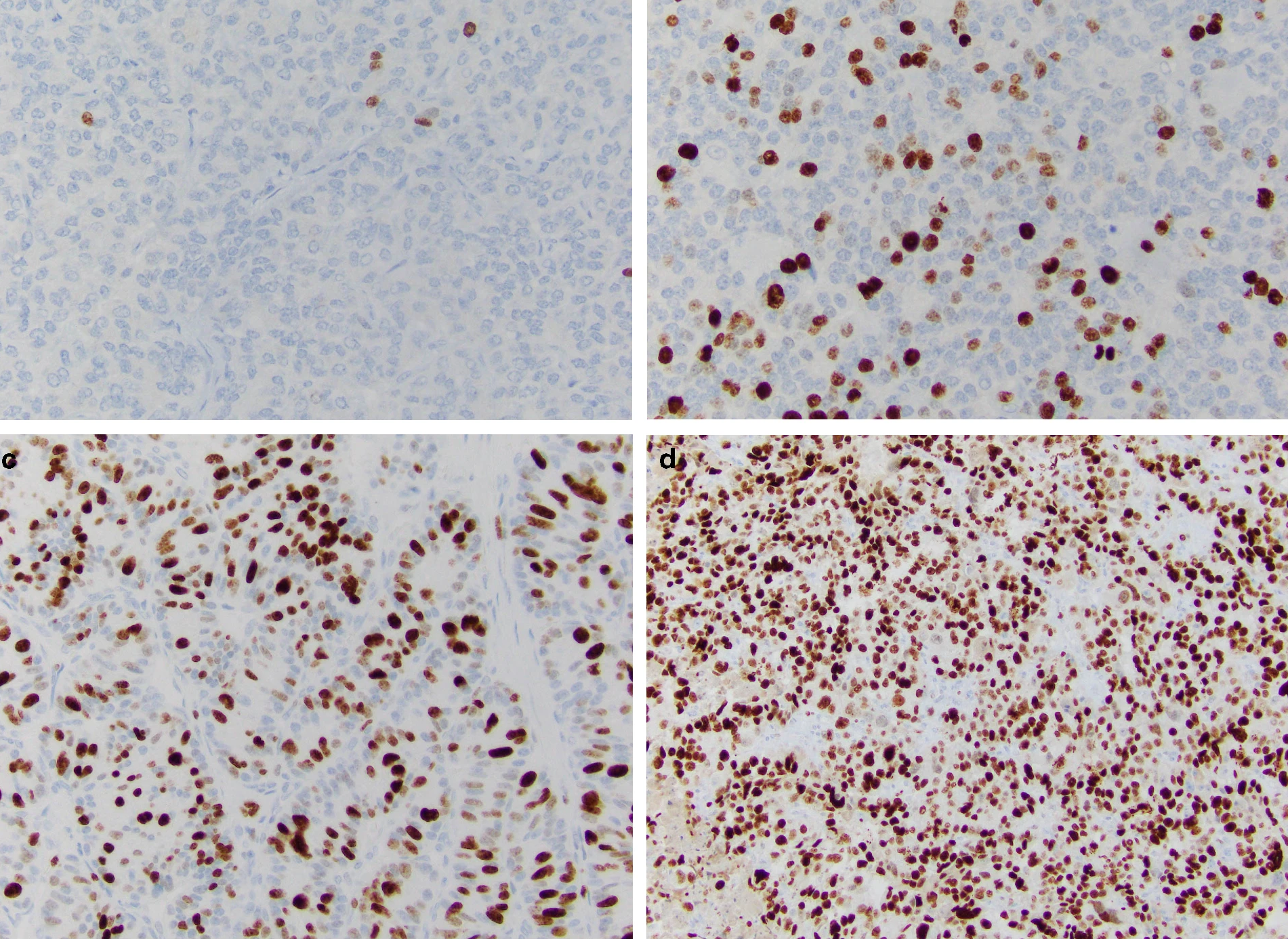
Рассмотрим различия понятий НЭО G3 и НЭР при локализации в поджелудочной железе. Несмотря на высокую степень злокачественности НЭО G3 гистологически имеют органоидную модель строения (рис. 3), отсутствие некрозов [10]. При иммуногистохимическом исследовании опухолевая ткань сохраняет экспрессию общих маркеров нейроэндокринной дифференцировки (диффузно и интенсивно определяется экспрессия синаптофизина, зачастую хромогранина А), а также панкреатические экзокринные или эктопические гормоны. Кроме того, в них отсутствует выраженная экспрессия p53 и утрата экспрессии RB (также определяются иммуногистохимически).
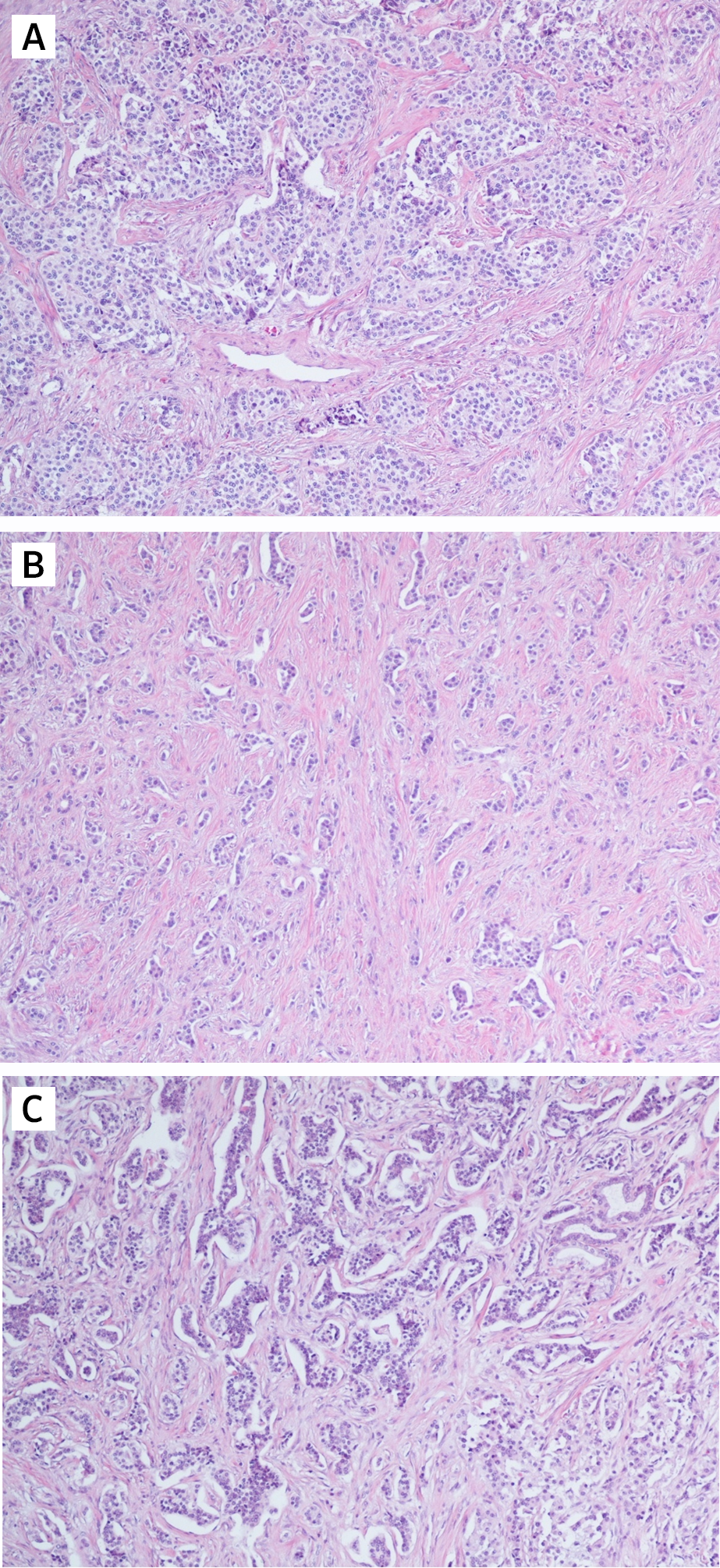
НЭР поджелудочной железы — это опухоли низкой степени дифференцировки и соответственно высокой степени злокачественности. Экспрессия общих маркеров нейроэндокринной дифференцировки атипичными клетками снижается: синаптофизин определяется слабо или диффузно, хромогранин А также слабо или фокально. Экзокринные гормоны отрицательны в таких опухолях [9]. Часто определяется экспрессия р53, белков ремоделирования хроматина DAXX (death-associated protein 6) и ATRX (АТФ-зависимая хеликаза), потеря экспрессии RB (белок ретинобластомы) и ISL1 (энхансер гена инсулина 1) [11].
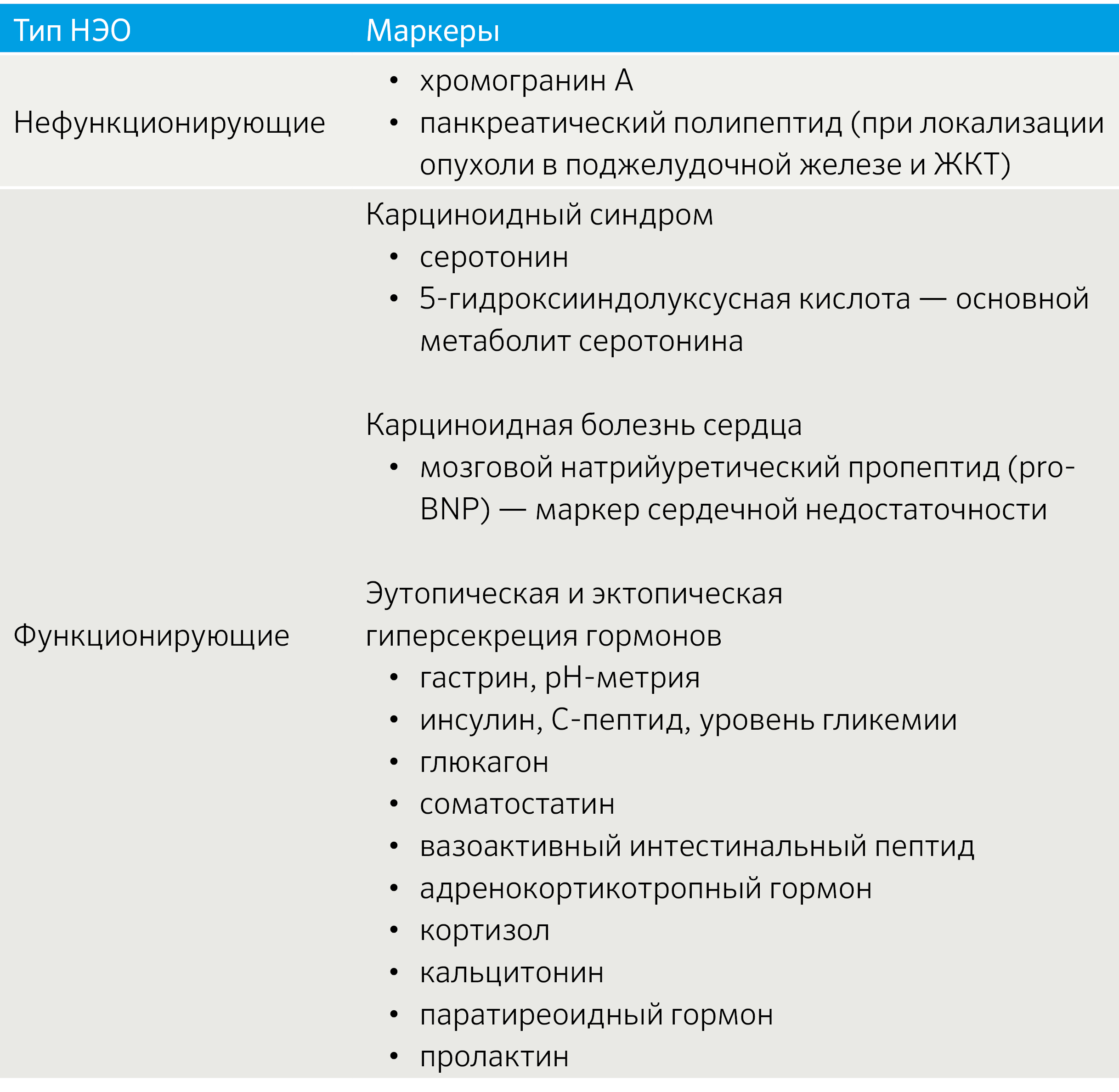
Ввиду многообразия секретирующего профиля НЭО биохимическая диагностика включает различные маркеры, комбинируемые с учетом клинической картины (табл. 4).
Табл. 4 | Спектр биохимических маркеров НЭО [2].
Радионуклидная диагностика играет важную роль в топической характеристике НЭО. Она включает методы специфической метаболической визуализации ( 123 I-MIBG), рецепторной визуализации ( 111 In-октреотид, 68 Ga-DOTA-TOС/DOTA-NOC/DOTA-TATE) и неспецифической метаболической визуализации ( 18 F-FDG, 18 F-DOPA).
123 I-метайодбензилгуанидин (MIBG) является аналогом норадреналина (норэпинефрина). Он накапливается в адренергических тканях и опухолях, происходящих из них. Сцинтиграфия с 123 I-MIBG используется для диагностики нейробластомы, феохромоцитомы, параганглиомы, карциноидов бронха и тонкой кишки [12].
Для рецепторной визуализации применяют 111 In (индий)-октеотид. Он выявляет высокодифференцированные нейроэндокринные опухоли, опухоли из клеток островкового аппарата поджелудочной железы (гастринома, глюкагонома, инсулинома). Также для верификации НЭО ЖКТ применяется соматостатин-рецепторная сцинтиграфия, так как большинство из них имеют рецепторы к соматостатину (SSTR) на поверхности опухолевых клеток (чаще 2 и 5 типа).
Выбор радионуклидного метода связан со степенью дифференцировки опухолевых клеток. Первичная диагностика НЭО Grade 1 и 2 проводится путем ПЭТ/КТ с радиофармпрепаратами (РФП), мечеными галлием 68 (является ПЭТ-радионуклидом). Сродство (аффинитет) РФП к конкретному подтипу трансмембранных рецепторов соматостатина определяет выбор диагностического индикатора (ПЭТ-лиганда, представленного различными модификациями DOTA). Например, для визуализации НЭО, экспрессирующих рецепторы подтипов SSTR2a и SSTR2b, применяют 68 Ga-DOTA-TATE (DOTA-Tyr3-октреотад). 68 Ga-DOTA-NOC (DOTA-1-Nal3-октреотид) выявляет подтипы SSTR3 и SSTR5, 68 Ga-DOTA-ТOC (DOTA-Tyr3-октреотид) — рецепторы SSTR5 [13].
При отсутствии возможности проведения данного исследования следует выполнить однофотонную эмиссионную компьютерную томографию (ОФЭКТ)/КТ (гибридный метод визуализации) с соматостатин-рецепторным радиофармпрепаратом.
Для недифференцированных НЭО Grade 3 и НЭР при отрицательных результатах соматостатин-рецепторной сцинтиграфии рекомендуется ПЭТ неспецифическая метаболическая визуализация с использованием других РФП. В частности, ПЭТ/КТ c 18F-фтордезоксиглюкозой (18F-ФДГ), которая неэффективна при высокодифференцированных НЭО [14]. Также рассматривают применение 18F-L–DOPA (дигидроксифенил-аланин) — меченого предшественника допамина, который эффективен для обнаружения медуллярного рака щитовидной железы, НЭО, параганглиомы и феохромоцитомы [15].
- Причины развития
- Особенности нейроэндокринных опухолей
- Классификация нейроэндокринных опухолей
- Виды нейроэндокринных опухолей и их симптоматика
- Диагностика заболевания
- Лечение
- Прогноз выживаемости
Нейроэндокринные опухоли (НЭО) образуются из апудоцитов, или APUD-клеток. Эти клетки разбросаны по всему организму и составляют самую древнюю часть эндокринной системы. Они одновременно похожи на нервные клетки и клетки желез внутренней секреции, так как могут реагировать на сигналы извне или изменения состояния организма, способны производить гормоны, выполняющие разные функции.
Опухоли APUD-системы встречаются редко, и их бывает сложно диагностировать. Чаще всего они возникают в желудочно-кишечном тракте, но могут поражать и другие органы. Особенность нейроэндокринных новообразований в том, что опухолевые клетки производят повышенное количество гормонов, и из-за этого могут возникать определенные симптомы.
Согласно данным американского реестра SEER, в 2004 году заболеваемость нейроэндокринными опухолями в США составила 5 случаев на 100 тысяч населения. В России статистика, к сожалению, отсутствует, но, вероятно, заболеваемость находится на аналогичном уровне.
По данным американских экспертов, распространенность нейроэндокринных опухолей ежегодно растет. В первую очередь это связывают с изменениями в характере питания, неблагоприятной экологической обстановкой.
По данным все того же реестра SEER, новообразования APUD-системы часто диагностируются на поздних стадиях: в 50% случаев опухоль успевает распространиться на окружающие ткани, в регионарные лимфоузлы, дать отдаленные метастазы.
Причины развития
У некоторых людей нейроэндокринные опухоли возникают в результате генетических заболеваний:
- Множественная эндокринная неоплазия (МЭН, MEN) вызвана мутацией в гене MEN, RET или CDKN1B. У больных может развиваться множество нейроэндокринных новообразований и опухолей в железах внутренней секреции. Некоторые из этих опухолей доброкачественные, некоторые — злокачественные. Выделяют четыре типа множественной эндокринной неоплазии: MEN1, MEN2A, MEN2B и MEN4. При MEN1 чаще всего возникают нейроэндокринные опухоли в паращитовидных железах, поджелудочной железе, гипофизе, иногда в пищеварительном тракте и легких. У большинства пациентов с MEN2A и MEN2B обнаруживают медуллярные карциномы (разновидность опухоли щитовидной железы), в некоторых случаях — аденомы паращитовидных желез, феохромоцитому. При MEN4 чаще всего встречаются аденомы гипофиза и паращитовидных желез.
- Болезнь Гиппеля-Линдау возникает при мутации в гене VHL. У больных в разных частях тела развиваются кисты и опухоли. Среди этих опухолей встречаются нейроэндокринные, в том числе НЭО поджелудочной железы, феохромоцитома.
- Нейрофиброматоз I типа вызван мутацией в гене NF1. Некоторые люди получают эту мутацию от родителей, у других она возникает спонтанно. Основное проявление заболевания — множество доброкачественных новообразований нервов и кожи. Повышен риск развития опухолей APUD-системы в желудочно-кишечном тракте, поджелудочной железе, феохромоцитомы.
- Туберозный склероз приводит к возникновению доброкачественных новообразований в разных органах, включая кожу, глаза, головной мозг, сердце, легкие, почки. Повышен риск развития НЭО.
У людей, которые не являются носителями этих мутаций, нейроэндокринные новообразования тоже могут возникать. Причины до конца не известны. Многие исследования показали, что одним из важнейших факторов риска является наследственность. Если в семье есть люди, у которых была обнаружена нейроэндокринная опухоль, то у остальных членов риски тоже повышены, особенно у ближайших родственников больных (родителей, детей, сестер и братьев). Кроме того, риск опухолей APUD-системы повышен в семьях с отягощенным анамнезом по раку толстой кишки, молочной железы, легкого.
Известны и другие факторы риска, но их роль нельзя считать полностью доказанной:
- Курение может способствовать развитию нейроэндокринных опухолей в легких, желудке, тонкой кишке и поджелудочной железе.
- Хронический атрофический гастрит, как показали некоторые исследования, способствует развитию НЕО в желудке.
- Сахарный диабет связывают с возникновением новообразований APUD-системы в поджелудочной железе, желудке.
Ученые пока не могут сказать, повышаются ли риски при частом употреблении алкоголя, нездоровом питании (много животных жиров), у людей с лишним весом. Нужны дополнительные исследования.
Особенности нейроэндокринных опухолей
Нейроэндокринные клетки не привязаны к какому-либо конкретному органу. Они разбросаны по всему организму. Хотя опухоли чаще всего и возникают в пищеварительном тракте, в более редких случаях они обнаруживаются и в других местах. В 15% случаев найти первичную опухоль не удается.
Нейроэндокринные опухоли могут производить гормоны, которые вызывают в органах определенные эффекты, и из-за этого пациент испытывает те или иные симптомы. Такие новообразования называют функционирующими. Если гормоны не вырабатываются — это нефункционирующая опухоль.
Классификация нейроэндокринных опухолей
Существуют разные классификации нейроэндокринных опухолей. Ниже в таблице представлены основные группы:
Стадию нейроэндокринных опухолей определяют в соответствии с общепринятой системой TNM:
- T — размер первичной опухоли, ее прорастание в окружающие ткани.
- N — поражение регионарных (близлежащих по отношению к опухоли) лимфатических узлов.
- M — наличие отдаленных метастазов.
Классификация по стадиям различается в зависимости от того, в каком органе находится нейроэндокринное новообразование. Например, стадию опухоли APUD-системы в легком определяют так же, как для немелкоклеточного рака легкого. Для нейроэндокринных новообразований в желудке, тонкой кишке, червеобразном отростке, ободочной, прямой кишке и поджелудочной железе разработаны собственные системы классификации по стадиям.
Виды нейроэндокринных опухолей и их симптоматика
Так как существуют разные типы нейроэндокринных опухолей, и они могут находиться в разных органах, то и симптомы различаются. Можно выделить три основные группы проявлений. Первая — это общие симптомы, характерные для любого типа рака: слабость, повышенная утомляемость, снижение аппетита, потеря веса без видимой причины.

Вторая группа симптомов связана с локализацией опухоли и ее размерами, сдавлением анатомических структур и нарушением функции пораженного органа. Беспокоят боли в определенной части тела, тошнота, упорный хронический кашель, расстройства стула, мочеиспусканий, кровотечения, необычные выделения. При поражении печени, желчных протоков, поджелудочной железы развивается механическая желтуха.
Третья группа симптомов вызвана гормонами, которые продуцируют нейроэндокринные клетки:
- диарея — жидкий стул более трех раз в сутки;
- постоянная жажда, голод, частые мочеиспускания, — признаки повышения уровня глюкозы в крови;
- повышенная утомляемость, раздражительность, дрожь, головокружение, судороги, потери сознания — признаки снижения уровня глюкозы в крови;
- язвенная болезнь, которая не поддается лечению;
- тревожность;
- сыпь на коже.
Желудочно-кишечный тракт — наиболее распространенное место локализации нейроэндокринных опухолей. Такие новообразования часто называют карциноидными опухолями. Частота поражения разных отделов пищеварительного тракта:
- тонкая кишка — 39%;
- прямая кишка — 15%;
- червеобразный отросток (аппендикс) — 7%;
- толстая кишка — 5–7%;
- желудок — 2–4%.
Опухоли в пищеварительном тракте вызывают классический карциноидный синдром. Он проявляется в виде покраснения и ощущения тепла в области лица, диареей, одышкой, симптомами, напоминающими бронхиальную астму, слабостью, учащенным сердцебиением, увеличением веса без видимой причины, высоким артериальным давлением, его частыми колебаниями.
Вторым по частоте местом локализации опухолей APUD-системы после НЭО ЖКТ являются легкие. Примерно в 30% случаев нейроэндокринное новообразование возникает в бронхиальной системе.
Феохромоцитома — опухоль надпочечников (иногда в других частях тела), которая вырабатывает гормоны стресса: адреналин и норадреналин. В результате избыточного уровня гормонов возникают приступы (кризы), во время которых человек испытывает беспокойство, страх, озноб, дрожь, головную боль и боль в грудной клетке, его кожа становится бледной, учащается сердцебиение, возникают экстрасистолы, тошнота, рвота.
Рак из клеток Меркеля — злокачественная опухоль кожи. Она встречается очень редко, но отличается высокой агрессивностью, рано распространяется в лимфатические узлы, метастазирует. Патология проявляется в виде одного или нескольких узелков на коже красного и синюшного цвета. Они могут изъязвляться. Рак из клеток Меркеля сложно диагностировать, зачастую его выявляют уже на поздних стадиях.
Диагностика заболевания
В большинстве случаев нейроэндокринные новообразования обнаруживаются случайно, когда человек проходит обследование по другому поводу. Опухоль можно обнаружить с помощью таких методов диагностики, как:
- Ультразвуковое исследование.
- Эндоскопические исследования: гастроскопия, колоноскопия, бронхоскопия.
- Рентгенография с контрастным усилением. Перед исследованием пациенту дают выпить раствор, который помогает четко увидеть контуры желудка, кишечника.
Диагноз подтверждается с помощью биопсии. Обнаружив патологическое образование, врач удаляет из него фрагмент ткани и отправляет в лабораторию для исследования под микроскопом. Если опухоль предположительно является феохромоцитомой, к биопсии прибегают только в крайних случаях, так как она сопряжена с серьезными рисками.
Компьютерная томография и МРТ помогают обнаружить опухоль, оценить ее размеры, локализацию, степень распространения в организме, обнаружить метастатические очаги. Для поиска метастазов применяют ПЭТ-сканирование. Врач может назначить анализы, которые помогают обнаружить гормоны, вырабатываемые опухолью, например, исследование мочи на 5-HIAA — продукт обмена серотонина. Определение уровня хромогранина А в крови помогает контролировать эффективность лечения.
Лечение
Выбор лечения зависит от типа опухоли, ее локализации, степени злокачественности, стадии. В некоторых случаях, если нейроэндокринное новообразование является высокодифференцированным и практически не растет, врач назначает активное наблюдение. Нужно периодически являться на осмотры, проходить КТ, МРТ, сдавать анализы крови. Как только появляются признаки роста или распространения в организме, начинают активное лечение.
В большинстве случаев нейроэндокринные новообразования успешно лечатся хирургическим путем. Во время операции удаляют саму опухоль и некоторое количество окружающих тканей. Затем удаленный материал изучают в лаборатории. Если получен негативный край резекции, это означает, что опухолевая ткань удалена полностью.
Если радикальное вмешательство невозможно, может быть выполнена циторедуктивная операция, во время которой стараются удалить как можно большее количество опухолевой ткани.
Если у пациента имеются признаки карциноидного синдрома, есть риск, что его состояние во время операции может сильно ухудшиться. Врач-анестезиолог должен быть осведомлен о такой возможности и принять необходимые меры.
При неоперабельных опухолях назначают медикаментозное лечение, лучевую терапию. Применяют различные виды химиопрепаратов, таргетные препараты, иммунотерапию. Терапия аналогами соматостатина помогает справиться с симптомами и замедлить рост опухоли.
Если нейроэндокринные опухолевые очаги имеются в печени, может быть проведена радиочастотная аблация, эмболизация артерии, питающей опухоль. Врачи Европейской клиники обладают большим опытом в проведении таких вмешательств.
Прогноз выживаемости
Прогноз зависит от того, какой вид опухоли был диагностирован, насколько она агрессивна, на какой стадии находится. Лечение преследует одну из двух целей:
- Полностью удалить опухолевые очаги. Если по результатам обследований не выявляются признаки присутствия опухоли в организме, констатируют ремиссию.
- Избавить пациента от симптомов и сдержать рост новообразования. При этом больной может прожить довольно долго.
Стоит поговорить с врачом перед началом лечения, спросить, какой будет цель, какого результата можно ожидать, и что планируется делать в случае, если ситуация ухудшится, опухоль рецидивирует.
Читайте также:

