Наночастицы железа в онкологии


Крошечные наночастицы, в разы тоньше человеческого волоса, могут помочь иммунной системе человека в борьбе с опухолями. Об этом рассказывает новое исследование , где в ходе эксперимента на мышах терапия с использованием наночастиц не только полностью уничтожила целевые опухоли молочной железы, но и избавила организм от метастазов в других частях тела. Клинические испытания, как уверяют исследователи, начнутся уже в ближайшие месяцы.
Тем не менее, существующие на сегодняшний день препараты эффективны только в 20−30% случаев. В некоторых случаях, даже когда КПП-молекулы заблокированы, вокруг оказывается недостаточно Т-клеток, и сигнал до иммунной системы не доходит, говорит Джедд Вулок, эксперт по раковой иммунотерапии из Memorial Sloan Kettering Cancer Center в Нью-Йорке. По его словам, другая частая проблема — это отсутствие на поверхности опухолевых клеток антигенов-мишеней, на которые и реагируют Т-клетки.
Однако эти проблемы, на первый взгляд практически не связанные друг с другом, в итоге натолкнули медиков на методику значительно увеличения эффективности иммунотерапии. Онкологам было известно, что после того, как пациент получает дозу облучения во время лучевой терапии, иммунная система ответит агрессивной реакцией, которая уничтожает не только опухоли, но и метастазы в тех областях, которые облучению не подвергались. Теперь исследователи полагают, что облучение иногда убивает некоторые опухолевые клетки так, что те выделяют антигены, на которые и реагируют Т-клетки.

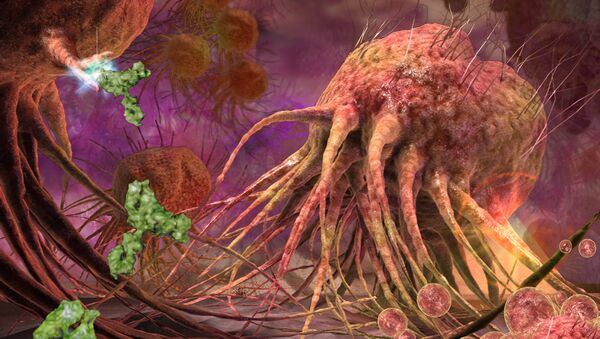
Так выглядят разрозненные раковые клетки под электронным микроскопом
Вэньбинь Лин, химик из Университета Чикаго в штате Иллинойс, и соавтор исследования, решил изучить э тот процесс и узнать, может ли он использовать нетоксичные наночастицы для сенсибилизации иммунной системы аналогичным образом. Это не так просто, как может показаться: если частицы будут слишком большими, клетки-макрофаги попросту поглотят и утилизируют их как инородные элементы. К тому же, белки крови часто коагулируют с различными частицами, облегчая их поглощение. За последние несколько лет команда Ли разработала новый метод получения частиц, размер которых колеблется от 20 до 40 нанометров — наиболее выгодный диапазон для того, чтобы их не могли засечь макрофаги. Помимо этого, частицы покрыты оболочкой из полиэтиленгликоля, который помогает им сохранять целостность во время циркуляции крови и успешно проникать в клетки-мишени. И, наконец, на внутренней стороне частицы оснащены светопоглощающими, хлорсодержащими молекулами, которые и превращают наночастицы в убийцы опухолей.
В предыдущих исследованиях ученые обнаружили, что после попадания в кровь наночастицы могут циркулировать в ней достаточно долго, прежде чем они найдут свою цель. Из-за того, что опухоли обычно обладают дырявой, деформированной сосудистой сетью, частицы могут просачиваться прямо в пораженную раком ткань и внедряться в сами опухолевые клетки. После того, как они будут поглощены, медики направляют на зону рядом с опухолью пучок инфракрасного света. Этот свет поглощается хлорсодержащими молекулами, которые потом возбуждают соседние молекулы кислорода, переводя его в высокоактивную форму, которая и разрывает соседние биомолекулы, уничтожая опухоль на корню.
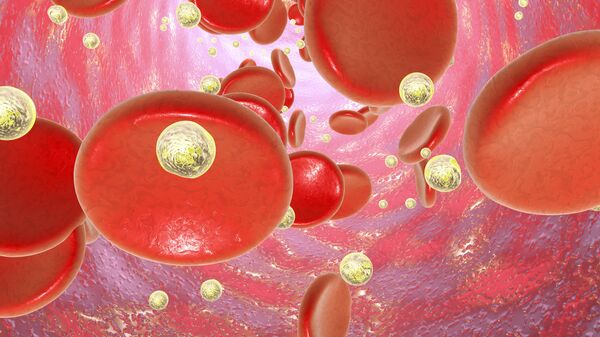
МОСКВА, 27 сен – РИА Новости. Ученые случайно обнаружили, что наночастицы из железа, которые были созданы в качестве лекарства от анемии, заставляют иммунитет обращать внимание на раковые клетки и уничтожать их, говорится в статье, опубликованной в журнале Nature Nanotechnology.
"Мы сильно удивились, что эти наночастицы заставили макрофагов атаковать раковые клетки внутри тела мыши. Мы думаем, что этот же прием сработает и при лечении опухолей в организме человека. Многие наши коллеги считают наночастицы лишь средством для доставки лекарств, но они могут вызывать интересные эффекты сами по себе, которые мы не увидим, если не приглядываться к ним вплотную", — рассказывает Хайке Далдруп-Линк (Heike Daldrup-Link) из Стэнфордского университета (США).
Далдруп-Линк и ее коллеги совершили это открытие, разрабатывая лекарство на базе наночастиц железа, которое бы помогало людям, страдающим от анемии или недавно потерявшим большое количество крови, восстановить уровень гемоглобина в организме. Это лекарство, ферумокситол, было недавно одобрено здравоохранительными органами США, и ученые проверяли его на наличие возможных побочных эффектов.
Наблюдая за воздействием этих наночастиц на различные культуры клеток мышей, ученые заметили, что они крайне необычным образом влияют на поведение макрофагов — одних из самых важных клеток иммунной системы, главная задача которых заключается в очистке организма от "биомусора", бактерий и раковых клеток. Эти клетки были открыты нобелевским лауреатом Ильей Мечниковым в 1884 году.
Это открытие натолкнуло ученых на мысль, что железные наночастицы можно использовать для борьбы с раком. Они проверили свою идею на трех группах мышей, в чье тело они имплантировали злокачественные опухоли, выращенные в пробирках. Первая популяция грызунов получала инъекции железных наночастиц, заполненных противораковым препаратом, вторая – "пустые" наночастицы, а третья служила контрольной группой.
Эксперимент показал, что и "полные", и "пустые" наночастицы одинаково хорошо подавляли рост опухолей и заставляли макрофагов атаковать раковые клетки и уничтожать их, что они не делали в организме контрольных особей, где иммунная система просто игнорировала опухоль. Схожим образом наночастицы железа предотвращали появление метастаз в легких, печени и других органах тела мышей.
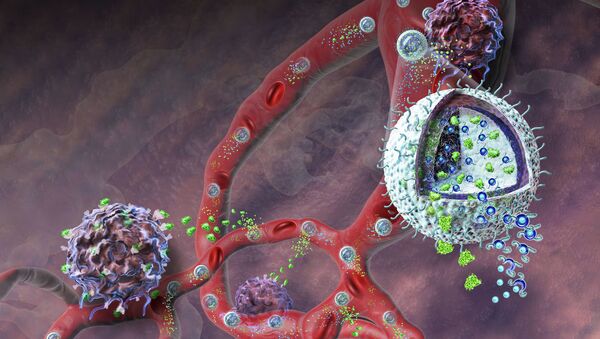
Как считают ученые, подобное благотворное действие наночастиц связано с тем, что их поглощение макрофагами меняет электрические свойства оболочки клеток иммунной системы, благодаря которым те приобретают способность "видеть" раковые клетки, до этого скрывавшиеся от них и выдававшие себя за "своих".
Учитывая то, что данный препарат уже был признан безопасным для здоровья человека, ученые предлагают начать клинические испытания на раковых больных в ближайшее время. Фактически, как отмечают Далдруп-Линк и ее коллеги, любой раковый больной может присоединиться к этим опытам, купив ферумокситол в аптеке, так как это лекарство продается без рецепта.

Группа ученых из Стэнфордского университета, США (Stanford University) провели исследования и обнаружили, что наночастицы из железа, использующиеся для лечения анемии, могут помочь в лечении онкологических заболеваний. Результаты исследований опубликованы в медицинском издании Nature Nanotechnology.
Органами здравоохранения США не так давно было одобрено к применению лекарство ферумокситол, в основе которого находятся наночастицы железа. Данный препарат помогает восстановить уровень гемоглобина у больных, страдающих анемией, а также рекомендуется тем, кто по каким-то причинам потерял большое количество крови.
Результаты эксперимента показали, что в первой и второй группе воздействие на опухолевые клетки было одинаково положительным - наноклетки железа обнаруживали раковые клетки и заставляли макрофагов атаковать и уничтожать их. В группе контрольных особей изменений не происходило – макрофаги игнорировали опухоль. Ученые обнаружили, что наночастицы железа сдерживают рост опухолей и появление метастаз в печени, легких и других органах тела животных.
Специалисты считают, что данная методика может быть использована для лечения раковых заболеваний у людей. Учитывая то, что ферумокситол уже признан безопасным для здоровья, в самое ближайшее время специалисты планируют провести клинические испытания препарата на онкологических больных.
Где лечить онкологические заболевания?
На нашем сайте собрана информация о сотнях зарубежных медицинских учреждений, в которых можно провести высокоточную диагностику и эффективное лечение различных онкологических заболеваний. Это могут быть, например, такие клиники и центры, как:

Медицинский центр Хадасса в Израиле имеет в своем составе Институт онкологии им. Моше Шаретта, который принимает на лечение пациентов из разных стран со многими видами онкологических заболеваний, оказывая им как услуги по высокоточной диагностике, так и самые передовые методы лечения рака. Перейти на страницу >>

Израильская клиника Шаарей Цедек проводит лечение практически всех известных онкологических заболеваний, применяя новые препараты и инновационные методы терапии. Основной специализацией клиники являются болезни, относящиеся к онкогинекологии, а также хирургическое лечение рака молочной железы. Перейти на страницу >>

Онкологический центр при институте Донгнам относится к числу самых крупных центров в Южной Корее, специализирующихся на диагностике и лечении онкологических заболеваний различных форм и локализаций, а также на радиологической медицине. Специалисты центра отличаются квалификацией и большим опытом работы. Перейти на страницу >>

Одним из основных направлений работы швейцарской клиники Женолье является лечение и диагностика злокачественных опухолей. При Клинике создан Институт онкологии, функция которого заключается в комплексной терапии широкого спектра онкологических заболеваний у детей и взрослых. Перейти на страницу >>

При немецкой Университетской клинике Тюбингена работает Онкологический центр, который многие специалисты считают одним из лидеров среди онкологических центров Германии. Учреждение прекрасно укомплектовано, для диагностики и лечения рака врачи используют самые современные методики. Перейти на страницу >>

Израильский Медицинский центр им. Хаима Шибы обладает одним из самых больших в стране онкологических подразделений. Врачи центра применяют индивидуальный подход к каждому пациенту, используют в работе самые современные и передовые технологии для диагностики и лечения злокачественных опухолей. Перейти на страницу >>
Каким должно быть питание при онкологических заболеваниях? Какие продукты абсолютно противопоказаны при той или иной форме рака?
Фитотерапия способна оказать существенную помощь не только в лечении онкологических заболеваний, но также и в их профилактике.
Многих людей, имеющих у себя или у родственников онкологическое заболевание, интересует вопрос: передается ли рак по наследству?
Лечение рака во время беременности является довольно сложным, ведь большинство лекарственных средств обладает токсичностью.
Какие перспективы у беременности после перенесенного онкологического заболевания? Следует ли выдерживать срок после лечения рака?
Профилактика является важной частью общей борьбы с онкологическими заболеваниями. Как же уменьшить вероятность возникновения рака?
Что представляет из себя паллиативное лечение рака? Как оно может повлиять на качество жизни онкологического больного и изменить ее к лучшему?
Учеными разработано достаточно много перспективных методов лечения рака, пока еще не признанных официальной медициной. Но все может измениться!
Как найти силы для борьбы с раком? Как не впасть в отчаяние от возможной инвалидности? Что может послужить надеждой и смыслом жизни?
Бытует такое мнение, что постоянные стрессовые ситуации способны привести к развитию онкологических заболеваний. Так ли это?
Многие онкологические больные часто страдают от резкой потери веса. Чем это вызвано и можно ли как-то справиться с этой проблемой?
Правила ухода за больными, вынужденными постоянно находиться в кровати, имеют свои особенности и их нужно обязательно знать.

Рак является причиной смерти №1 в мире.
На протяжении долгих десятилетий ученые разрабатывают противоопухолевые вакцины, вирусы, наночастицы и иммунотерапию для лечения рака.
Но насколько мы близки к победе над смертельной болезнью?
Всемирная организация здравоохранения (ВОЗ) отмечает, что каждая шестая смерть на планете связана с онкологическими заболеваниями. Только в России за 2015 году от рака умерло почти 287 тысяч человек, в США — почти 600 тысяч.
Сегодня наиболее распространенными видами лечения рака являются лучевая терапия, химиотерапия, хирургическое лечение и — в случае рака предстательной железы и рака молочной железы — еще и гормональная терапия.
На фоне традиционного лечения набирают силу новые, способные существенно улучшить результаты, а зачастую имеющие меньше побочных эффектов.
- Побочные эффекты агрессивной терапии
- Частые рецидивы заболевания после операции
- Устойчивость опухолей к химиопрепаратам
Сегодня мы расскажем о самых последних исследованиях рака, которые позволяют надеяться на скорую победу над болезнью и появление эффективной профилактики.
Иммунотерапия рака
Если раньше наука оказалась бы бессильной, то сегодня ответ нашелся быстро: новые препараты для иммунотерапии рака блокируют молекулы, маскирующие опухоль, тем самым полностью восстанавливая контроль иммунной системы над болезнью.
Терапевтические вирусы и вакцины против рака
В январе 2018 мы рассказывали о достижении швейцарских ученых, которые обучают дендритные вакцины прямо в теле пациента. Для этого достаточно ввести в клетку особые пузырьки (везикулы) с антигенами рака, и она начинает распознавать чужака.
В последнее время врачи понимают, что иммунотерапия наилучшим образом работает в тандеме с химиотерапией. Особенно, если курс химиотерапии предшествует назначению иммунотерапевтических средств. Проблема заключается в том, что эта комбинация увеличивает вероятность побочных эффектов.
Ученые из двух ведущих институтов Северной Каролины (США) нашли решение. Разработанный в начале 2018 года гелеобразный материал может использоваться для доставки химиотерапии и иммунотерапии в опухоль, без системных реакций.
Наночастицы доставляют химиопрепараты
Если говорить о точности доставки химиопрепаратов и обнаружении невидимых микроопухолей, то настоящую революцию в этом деле произвели нанотехнологии.
Наночастицы — это крошечные частицы, соизмеримые по своим размерам с молекулами. Они широко используются в разных областях медицины, включая диагностику и лечение рака. По мнению ведущих онкологов США, следующие 10 лет сделают наночастицы повседневной реальностью онкологии.
В чем секрет их успеха?
Начнем с главного: убить рак огромной дозой токсичного химиопрепарата, в принципе, не проблема. Проблема — не убить при этом человека.
Наночастицы служат идеальными транспортными средствами для доставки химиотерапевтических средств по нужному адресу. Чем точнее доставка яда, тем меньше его потребуется для лечения.
Тем ниже риск общих (системных) побочных явлений.
Но есть и другие области применения наночастиц. Например, их можно использовать для гипертермии, когда частицы сначала насыщают опухоли, а затем под действием внешнего излучения нагреваются, вызывая массовую гибель раковых клеток.
Врачи заставят рак голодать
Другая стратегия, недавно предложенная учеными – лишать рак питательных веществ, необходимых для бесконтрольного деления клеток и роста опухоли.
Авторы первого проекта научились лишать рак глутамина – жизненно важной аминокислоты, которую активно используют опухоли легких, груди и кишечника. Блокируя доступ клеток к глутамину, исследователям удалось усилить окислительный стресс и уменьшить опухоли.
Второй способ победить рак молочной железы – это лишить опухолевые клетки эссенциального фермента, который помогает им вырабатывать энергию.
Что обещают нам исследования рака?
Исследования рака проводятся на полной скорости, с применением всех доступных технических достижений Большинство из этих проектов все еще находятся на ранней стадии экспериментов in vitro и in vivo. Им предстоит пройти долгий путь до клинических испытаний на пациентах.
Это не значит, что мы должны потерять надежду.
Медицина находится на том этапе, где можно утверждать: рак излечим.
Остальное – это вопрос техники и нескольких лет времени.
Константин Моканов: магистр фармации и профессиональный медицинский переводчик
Что такое наночастица? Согласно определению метрологов, размер нанообъекта должен быть меньше 100 нанометров. Один из парадоксальных примеров — мыльный пузырь. На самом деле он тоже нанообъект: когда мы надуваем пузырь, он меняет цвет, и его стенки темнеют, делаясь почти незаметными. Как это было доказано учеными-оптиками, в этот момент толщина его стенки становится менее 100 нанометров, и, таким образом, он является наноразмерным. Впрочем, гораздо чаще ученые в науках о жизни имеют дело с наночастицами в форме круглых или вытянутых шариков. Так наночастицы нашли важное применение в онкологии: они помогают обнаружить злокачественные образования, доставить к ним лекарства и победить их.
Основная часть препаратов в онкологии — классическая химиотерапия. Врачи вводят химиотерапевтические препараты, которые по сути являются ядами, внутривенно, а те разносятся по всему организму, проникая в ткани и отравляя их. Химиотерапия воздействует не только на раковые клетки, но и на здоровые ткани, и это серьезная проблема, помочь в решении которой могут наночастицы.
Наночастицы не попадают в большую часть тканей: они не могут выйти за пределы стенок здоровых сосудов. Однако у опухолевых тканей повышенная проницаемость сосудов, и наночастицы могут в них проникнуть, что доказал японский фармаколог Хироши Маэда в 1980-х годах. Но иммунная система быстро изымает наночастицы из кровотока. Это также является серьезным вызовом для ученых.
Почему наночастицы лучше традиционных онкопрепаратов
Преимущество использования наночастиц в химиотерапии неоспоримо: они менее токсичны, чем стандартные препараты. Например, доксорубицин — противоопухолевый препарат, который повреждает ДНК клеток. Наиболее чувствительны к нему гладкомышечные клетки сердца. Под влиянием доксорубицина ритмы сердца меняются, что может привести к сердечной недостаточности или аритмии. Если доксорубицин вводить в составе наночастиц, то его концентрация в организме станет выше, но он не вызовет серьезных осложнений.
Благодаря наночастицам побочные эффекты от химиотерапии существенно уменьшились, притом что по эффективности они не уступают стандартным препаратам. Сегодня многие научные группы пытаются собрать собственные комплексы — сложные наносоединения, которые будут обладать удивительными свойствами и существенно упростят терапию рака. Например, можно сделать нанокомплексы, которые будут саморазбиваться при попадании в опухоль. Это облегчит распространение препарата по всему объему злокачественного образования. Их можно сделать контрастными, различимыми существующими системами медицинской визуализации, такими как МРТ, КТ, УЗИ, а также оптическими системами — последнее нашло широкое применение в работе с онкологическими животными моделями для изучения методов онкотерапии. Нанокомплексы можно сделать гибридными, сочетающими органическую и неорганическую природу. Биогибридные комплексы можно создать такими, чтобы они были способны избежать захвата клетками иммунной системы, что приведет к лучшему накоплению в опухоли и метастазах. И это только малая часть возможностей, открываемая нанотехнологиями.
Как наночастицы помогут защититься от солнца
Еще одно направление, где применяются наночастицы, — токсикология. Люди вдыхают, потребляют частицы разных веществ и соприкасаются с ними. Однако не все частицы из этого разнообразия безопасны, некоторые могут серьезно навредить человеку. Влияние наночастиц на наш организм и возможные подходы к снижению их воздействия изучает нанотоксикология.
Самый простой пример — солнцезащитный крем. Вы пришли на пляж и, чтобы защитить себя от ультрафиолетовых лучей, нанесли крем на кожу. Казалось бы, что может угрожать? Дело в том, наночастицы крема могут проникать в клетки кожи и повреждать их. Особенно выделяются наночастицы органических фильтров — например, октокрилен или энсулизол. Они обесцвечиваются под лучами солнца, как одежда, и теряют свои защитные свойства, поэтому крем приходится наносить повторно. Еще органика может привести к неприятным последствиям, таким как раздражение кожи.
В солнцезащитных кремах используются не только органические соединения. В большинстве современных продуктов основной компонент — неорганические частицы, а именно оксид цинка и диоксид титана. Эти два оксида металлов хороши тем, что они фотостойкие, не разрушаются под воздействием солнечных лучей. Однако и у них есть свои минусы: под лучами солнца они становятся фотокаталитами и начинают производить активные радикалы, которые безопасны, потому что остаются в составе крема.
Наночастицы оксида цинка считаются самым эффективным солнцезащитным фильтром. Они поглощают свет в опасном диапазоне — ультрафиолет типа А, который может привести к ожогам разной степени и повредить ДНК. В результате у человека могут возникнуть мутации, приводящие к развитию меланомы — злокачественного образования.
Но в 2016 году в научной статье[1] появилось сообщение, что частицы цинка, оказавшись на коже, растворяются и попадают внутрь организма. Роговой слой эпителия — верхнего слоя кожи — закислен секретом сальной железы, который защищает ее от микробов. Как оказалось, наночастицы растворяются в секрете и проникают в клетки в качестве ионов.
Клеточная машинерия построена на том, что цинк участвует в регенерации клеток и заживлении ран. Но будет ли дополнительный цинк, который проникает в кожу после солнцезащитного крема, токсичен для организма? Над этим вопросом мы долгие годы работали в лаборатории Университета Маккуори (Австралия) и Сеченовском университете, а сейчас готовим результаты исследований к публикации.
Почему эта проблема так важна? Солнечные лучи вызывают рак кожи. Особенно это актуально для тех, кто много времени проводит под солнцем. Например, у двух из трех жителей Австралии, рожденных в этой стране, к семидесяти годам будет диагностирована та или иная форма рака кожи[2] . Не все типы рака кожи столь злокачественны, как меланома, но защититься хотелось бы от всех. Именно поэтому в Австралии развернулась общественная кампания против этой формы онкологии. Рак кожи возникает, когда клетки повреждаются в результате чрезмерного воздействия ультрафиолетового излучения солнца. Чтобы уберечь людей от меланомы, фармкомпании разрабатывают новые соединения для солнцезащитных кремов, в том числе основываясь на последних достижениях наномедицины.
Диагностика, терапия и применение наночастиц
Кроме того, наночастицы используются в тераностике — это подход в медицине, объединяющий терапию и диагностику. Главное направление, в котором задействована тераностика, — онкология. Предположим, раковую опухоль трудно обнаружить. В этом случае нам помогут наночастицы. Когда наночастицы вводят в организм, недоброкачественное образование накапливает их. Чтобы его обнаружить, ученые делают наночастицы способными к контрасту — различимыми имиджинговыми инструментами, включая МРТ, КТ, УЗИ, а также оптическими камерами. В последнем случае регистрация происходит следующим образом: когда в опухоли скопилось нужное количество таких частиц, их облучают светом, который наночастицы переизлучают с изменением цвета, и их можно зарегистрировать с помощью, например, камеры. Такой способ называется флуоресцентным имиджингом, и он позволяет выявлять онкологические заболевания, а также обнаруживать и удалять оставшиеся после хирургической операции злокачественные ткани.
Но есть более стандартные методы, например радиоактивный имиджинг. В организм вводятся радиоактивные трейсеры — специальные нановещества, которые используются для наблюдения за химической реакцией или биологическим процессом. Благодаря имиджинговым системам можно обнаружить опухоль. Также применяются магнитные частицы оксида железа: они накапливаются в опухолях, и в системах МРТ видны места скоплений. Так можно обнаружить опухоль и сопутствующие ей метастазы. Эти методы сейчас находятся в активном развитии, и есть основания полагать, что они будут использованы в клинической практике.
Тераностика применяется по отношению к людям, но наночастицы задействованы меньше, чем стандартные препараты. Один из примеров тераностики, если не привязываться к наночастицам, — визуализация при операции по удалению глиомы — рака мозга. Глиома образуется таким образом, что узел виден, но нитеобразные метастазы, которые проникают в ткани головного мозга, — нет. Эти метастазы необходимо удалить: если этого не сделать, опухоль может развиться снова. Чтобы понять, где расположены метастазы и сама опухоль, в раковые ткани вводят флуоресцентные маркеры.
Один из таких флуоресцентных маркеров — препарат аласенс, который используется для лечения и диагностики онкологических заболеваний. Он накапливается в опухолевых клетках и заставляет их вырабатывать порфирин — пигмент, который в больших количествах распространен в живой природе. Порфирин ценен тем, что если на него светить зеленым светом, то он будет отсвечивать красным, что говорит о потенциале пигмента в медицине. Врачам достаточно поставить фильтр, который блокирует зеленый свет, и фильтр, который выделяет красный. Таким образом, во время операции хирург смотрит не на опухоль, а на монитор, на котором злокачественное образование подсвечено красным цветом.
В НМИЦ нейрохирургии имени академика Н. Н. Бурденко стандартно проводятся операции с использованием аласенса. Аласенс — препарат, позволяющий проводить фотодинамическую терапию. Если на него сильно посветить, то он будет токсичен для опухоли. Такая операция возможна, но хирурги предпочитают оперировать. Это пример того, как диагностический препарат помогает в хирургии человека.
Тераностика активно развивается, но, к сожалению, сегодня нанотехнологии не нашли широкого применения в онкологии. Ученые предпочитают химиотерапию в устоявшемся виде, а не с помощью наночастиц. Одна из причин — долгое и дорогостоящее тестирование нанопрепаратов и одобрение надзорных медицинских ведомств, что является вполне обоснованным: в первую очередь нельзя навредить пациенту. Кроме того, препараты наномедицины являются высокотехнологичными, а потому дорогостоящими. Поэтому тераностика с применением наночастиц в основном используется в исследованиях на животных, но подобные типы имиджинговых систем крайне полезны: доктора вводят препарат и видят, где он накопился. Так легко обнаружить раковые опухоли и прооперировать человека в нужный момент.
Андрей Звягин
доктор физико-математических наук, заведующий Отделом биомедицинской инженерии Института молекулярной медицины Сеченовского университета, профессор Университета Маккуори, Австралия.
источник
Ученые из Массачусетского Технологического Института (Massachusetts Institute of Technology, сокращенно MIT, США) создали наночастицы, которые стимулируют противоопухолевый иммунитет и повышают эффективность иммунопрепаратов из группы ингибиторов контрольных точек.
Иммунотерапия — современное направление в лечении рака, которое предполагает использование ресурсов иммунной системы для уничтожения опухолевых клеток. Особенно успешно применяются иммунопрепараты из группы ингибиторов контрольных точек. Они помогают повысить выживаемость пациентов с поздними стадиями рака. Проблема в том, что у части онкобольных эти препараты неэффективны.
Специалисты из MIT создали наночастицы, которые стимулируют иммунитет, и вводили их мышам с искусственно вызванными злокачественными опухолями в комбинации с ингибиторами контрольных точек. Эффективность такого лечения оказалась значительно выше, чем терапия ингибиторами контрольных точек без наночастиц.
Доктор Колин Басс (Colin Buss), ведущий автор исследования, отмечает:
Эти методы лечения [иммунотерапия ингибиторами контрольных точек] хорошо работают у небольшой части пациентов, а у других пациентов они вообще не работают. На данный момент не совсем понятно, почему существует такая большая разница.
Ученые надеются, что созданные ими наночастицы в будущем помогут повысить эффективность иммунопрепаратов.
Наночастицы представляют собой упакованные небольшие отрезки ДНК. Они активируют иммунную реакцию против опухолевых клеток и, таким образом, работают в синергии с ингибиторами контрольных точек.
Отключить тормоза
Предыдущие клинические исследования с олигонуклеотидами не увенчались успехом, потому что эти молекулы плохо достигают раковых клеток и не накапливаются в опухолевой ткани. Специалисты из MIT упаковали фрагменты ДНК в пептиды, которые могут специфически присоединяться к раковым клеткам и проникать в них.
Два препарата усиливают друг друга
Ученые провели эксперименты на мышах с разными типами злокачественных опухолей. Животных поделили на три группы, в которых проводили разное лечение:
- Только ингибиторами контрольных точек.
- Только наночастицами с олигонуклеотидами.
- Комбинацией двух препаратов.
Наилучшие результаты получились в группе, где применяли сразу два препарата.
Далее исследователи решили проверить, можно ли лечить таким способом рак с метастазами. Мышам имплантировали по две опухоли в разные части тела, затем им вводили системно ингибиторы контрольных точек, а наночастицы — локально только в одну из опухолей. После этого активированные успешно уничтожали и второе новообразование. То есть, стимулируя иммунитет только в одном месте, можно получить системный ответ.
Теперь, когда эффективность наночастиц доказана, нужно проверить их безопасность. После этого, если испытания пройдут успешно, можно будет планировать клинические испытания с участием онкологических больных. Специалисты из MIT надеются, что их разработка поможет пациентам, у которых неэффективна терапия ингибиторами контрольных точек.
В Европейской клинике применяются все новейшие иммунопрепараты, зарегистрированные на территории России. Мы закупаем только оригинальные лекарственные средства с доказанной эффективностью у ведущих производителей. Все иммунопрепараты в наличии, лечение может быть начато в кратчайшие сроки после поступления пациента в клинику.
Читайте также:

