Моноклональные антитела при раке предстательной железы
Иммунотерапия при раке простаты
.jpg)
Как действует иммунотерапия?
Иммунотерапия при раке простаты — многообещающее инновативное направление, которое пока находится в стадии экспериментального изучения.
Основное средство лечения при иммунной терапии рака простаты – это сама иммунная система пациента. Самостоятельно она неспособна в достаточной мере противодействовать опухолевому процессу: злокачественные клетки умеют скрывать от иммунной системы свой вредоносный потенциал и поэтому безнаказанно распространяются в организме.
Суть иммунной терапии – усилить работу иммунной системы или научить ее распознавать раковые клетки, чтобы запустить процесс их уничтожения.
Виды иммунотерапии
Иммунотерапию рака простаты можно разделить на два основных направления: пассивная и активная иммунотерапия.
При пассивной иммунотерапии используются активированные компоненты иммунной системы – например, антитела. Они поддерживают работу иммунной системы, избирательно присоединяясь к опухолевым клеткам и вызывая различные реакции в клетке.
Активную иммунотерапию можно сравнить с вакцинацией. Но в случае с онкологической иммунотерапией речь идет не о профилактической, а лечебной вакцинации. При активной вакцинации пациенту вводятся субстанции, которые вызывают защитную реакцию организма. В идеальном случае ответ иммунной системы должен привести если не к уничтожению раковых клеток, то к существенному замедлению роста опухоли.
При этом различают специфическую и неспецифическую иммунную терапию: при неспецифической стимуляции иммунная система активируется в общем, при специфической стимуляции осуществляется активация только определенных компонентов для целенаправленной борьбы с клетками рака простаты. Например, с помощью ввода опухолевых антигенов, вызывающих защитную реакцию, стимулируется выработка антител (как при прививке против гриппа). Но борьба с опухолями методом вакцинирования осложнена тем, что злокачественные опухоли в прогрессирующей стадии меняют свой антиген и ускользают от иммунного ответа.
Опухолевые вакцины при раке простаты могут быть получены различными способами: они могут быть изготовлены из раковых клеток пациента, из опухолевых клеток других пациентов, специальных защитных клеток организма пациентов, из протеинов, аналогичных опухолевым антигенам, вирусов, заряженных опухолевым антигеном и пр.
Какие медикаменты применяются?
На сегодняшний момент в Германии и других странах мира ведутся клинические исследования по тестированию различных препаратов иммунной терапии при раке простаты.
Поскольку это совершенно новое направление в лечении рака простаты, пока лишь один препарат — Sipuleucel-T (Provenge®) — преодолел все стадии клинических испытаний и применяется в клинической практике (по состоянию на 2016 год).
Этот вакцинный препарат стал использоваться в Европе в сентябре 2013 года для пациентов с гормонорезистентным раком простаты с метастазами при отсутствии или слабом проявлении симптомов и отсутствии показаний к химиотерапии. В мае 2015 года допуск препарата на европейский рынок был отозван производителем по неизвестной причине. Но большого прорыва этот препарат не произвел — согласно исследованиям, применение препарата продлевает жизнь пациентов в среднем на 4-5 месяцев. Для сравнения: применение химиотерапии у пациентов с раком простаты может продлить жизнь на 10-17 месяцев.
Исследовалось также воздействие другого иммунного препарата — Ipilimumab — на клетки рака простаты. Это препарат из класса моноклональных антител. Никакого значительного преимущества в отношении выживаемости пациентов с гормонорезистентным раком простаты установлено не было.
Продолжаются исследования в отношении препарата Prostvac-VF. Это генетически изготовленная вакцина, базирующаяся на вирусе оспы. Содержит ПСА и три стимулирующих молекулы.
В Германии в 2016 году клинически тестируется другое вещество для иммунотерапии рака простаты – РНК-активный препарат CV9104. Он активирует иммунную систему, чтобы атаковать определенные протеины, которые обнаруживаются практически только на поверхности клеток рака предстательной железы.
Насколько эффективна иммунная терапия?
Пока ни один из тестируемых иммунных препаратов при лечении рака простаты не превзошел эффекта применяющихся методов лечения карциномы предстательной железы. Вероятно, однажды ученым удастся совершить революцию, и появятся медикаменты, которые смогут излечивать поздние стадии рака простаты.
Но пройдет еще не один год, пока будет найден препарат, который на самом деле эффективней других методов лечения рака простаты – операции, лучевой терапии, химиотерапии. Поэтому пока не стоит возлагать на иммунную терапию большие надежды, а лучше использовать хорошо зарекомендовавшие себя способы лечения рака простаты.
Иммунотерапия для лечения рака простаты
Существует три вида иммунотерапии для лечения рака простаты. Активная иммунотерапия направлена на стимулирование реакций иммунной системы организма. Пассивная иммунотерапия предполагает применение для лечения рака создаваемых в лаборатории средств, таких как искусственные антитела, а специфическая иммунотерапия – это оказание направленного воздействия на клетки определенного типа без повреждения клеток других типов. В качестве метода лечения рака предстательной железы все эти три различных вида иммунотерапии работают по-разному.
Наиболее распространенным видом иммунотерапии при раке простаты является пассивная иммунотерапия, которая включает применение моноклональных антител. Моноклональные антитела (МАТ) создаются в лаборатории.
Конъюгированные моноклональные антитела – это антитела, которые также содержат какой-либо токсин, например препарат химиотерапии, или радиацию в небольшом количестве. Они обнаруживают и уничтожают клетки рака простаты, не нанося вреда нормальным, здоровым клеткам. Простые моноклональные антитела не содержат токсинов и либо маркируют раковые клетки для последующего их уничтожения иммунной системой, либо предотвращают их развитие.
Активная химиотерапия при раке простаты – это метод лечения, который основывается на разрушении раковых клеток в простате.
Точно так же как иммунизация инициирует создание иммунной системой защиты от заболеваний и вирусов, вакцины против рака провоцируют иммунную систему на борьбу с раковыми клетками. Хотя эти вакцины зачастую создаются в лабораторных условиях, они специально предназначены для того, чтобы запускать выработку лимфоцитов. Нередко определенные клетки рака простаты берутся от пациента и объединяются с вакциной. Раковые белки связываются с вакцинированными клетками и позволяют вакцине помогать иммунной системе в распознавании раковых клеток как инородных тел и последующем их уничтожении.
Специфическая иммунотерапия при раке простаты – это более нацеленная терапия. Многие примеры специфической иммунотерапии сочетают пассивную или активную иммунотерапию с традиционными методами лечения, такими как лучевая терапия и химиотерапия. Первые два вида иммунотерапии используются, чтобы маркировать клетки рака простаты, делая их более уязвимыми для воздействия традиционных методов лечения. К помощи этого вида иммунотерапии часто прибегают при запущенном раке простаты. Такой рак обычно хуже поддается лечению, так как развивается и дает метастазы быстрее.
Иммунотерапия вообще редко применяется в качестве первоочередного метода лечения при раке простаты, развитие которого находится на начальных стадиях. Запущенный или рецидивирующий рак часто не отвечает на традиционные методы лечения. А агрессивный рак простаты более устойчив, чем неагрессивный. И когда другие методы не справляются с заболеванием или их применение невозможно, используется иммунотерапия. Кроме того, применение иммунотерапии может рассматриваться, когда рак простаты вызывает стремительное появление множественных опухолей.
Видео
Моноклональные антитела при раке простаты
Журнал добавлен в корзину.
В этом году Нобелевскую премию по медицине вручили за разработку одного из видов противораковой иммунотерапии, когда у иммунитета отключают регуляторный механизм, и иммунная система начинает в полную силу охотиться за раковыми клетками. Чтобы заставить иммунитет работать, как надо, обычно используют моноклональные антитела.
Насколько эффективны препараты на основе MAB при лечении широкого спектра онкологических заболеваний? Или их использование приносит пользу только при некоторых видах рака?
При обычной терапии, когда опухоль стараются убить какими-то токсичными молекулами, часто возникает проблема лекарственной устойчивости – раковые клетки становятся нечувствительны к лекарству. С другой стороны, обычная химиотерапия печально знаменита сильными побочными эффектами. А в случае терапии моноклональными антителами – может ли у раковых клеток появиться к ним устойчивость? И существуют ли побочные действия применения МАБов?
Каковы последние достижения в разработке MAB?
Связана ли эффективность разных типов антител с конкретным видом рака? И может ли быть так, что один и тот же вид рака реагирует на антитела у одного больного и не реагирует у другого?
Каждый конкретный тип MAB разрабатывают под определенный вид рака с определенным механизмом развития. Универсальных антител здесь просто не существует, поэтому и эффективность может быть разной. Индивидуальное восприятие больного тоже играет очень важную роль. Все механизмы индивидуальны и работают по-разному.
Есть ли какие-то виды опухолей, которые упорно не хотят поддаваться лечению с помощью MAB, и почему? И наоборот – какие лечатся исключительно хорошо?
Однако зачастую механизм возникновения рака неизвестен, непонятно, какова ключевая молекула и, следовательно, какова цель для разработки таргетной терапии. Можно сказать, что опухоли, которые не поддаются лечению это те, о которых мы ещё мало знаем. В таких случаях предстоит ещё многое исследовать, чтобы разработать такие препараты, которые действовали бы на организм без побочных действий.
С какими другими видами противораковой терапии комбинируют MAB?
Например, моноклональные антитела против иммунного чек-пойнта PD1 комбинируют с иммунотерапией CAR-T (в которой используются Т-клетки, перепрограммированные на поиск раковых клеток), причем комбинируют достаточно успешно. В СМИ не так давно был описан случай: при лечении женщины, больной раком молочной железы четвертой стадии, использовали такой вариант комбинированной терапии, и у больной без операционного вмешательства сами по себе стали уходить и опухоль, и метастазы.
Портал функционирует при финансовой поддержке Федерального агентства по печати и массовым коммуникациям.
Поддержка и развитие сайта – KTC Digital Production


Моноклональные антитела — это новейшее достижение медицины, которое применяется при лечении тяжелых заболеваний. Среди них злокачественные новообразования, аутоиммунные, системные, заболевания сердечно-сосудистой системы, некоторые инфекции и многое другое. Помимо этого, моноклональные антитела широко используются в диагностике, например, в иммуногистохимии, иммуноферментном анализе, проточной цитофлуориметрии и др. Таким образом, данная технология используется во многих отраслях современной медицины.
- Способы получения моноклональных антител
- Механизм действия моноклоналных антител
- Препараты с моноклональными антителами
- Проблемы при использовании моноклональных антител
Человечество уже давно открыло для себя действие антител — особых молекул, которые вырабатываются клетками иммунной системы для распознавания чужеродных агентов — антигенов и их уничтожения. Антитела обладают специфичностью. Это значит, что они узнают только свой антиген, причем не просто антиген, а отдельный его фрагмент — детерминантную группу. В одном антигене может быть несколько таких детерминантных групп, и к ним будут образовываться разные антитела. Более того, к одной детерминанте может образовываться сразу несколько видов антител, которые могут отличаться по структуре, степени родства и прочности связывания. Таким образом, при введении антигена в организм образуется большое количество разных видов антител, направленных исключительно на один вид антигена. Это позволяет обеспечить адекватную иммунную защиту.
Антитела образуются специальными антителообразующими клетками. Причем каждый их вид образуется отдельной группой генетически однородных клеток — клонов. Чем больше необходимо видов антител, тем больше образуется клонов. Соответственно, антитела, которые вырабатываются одним клоном клеток называются моноклональными антителами.
Раньше для производства антител применялась иммунизация животных, после которой отбиралась их плазма и использовалась для приготовления отдельных препаратов — иммунных сывороток для борьбы с различными токсинами (дифтерия, столбняк), вирусами, ядами и др. Но бывают ситуации, когда нужно конкретное антитело, направленное на конкретную детерминанту антигена. Здесь уже обычной иммунизацией не обойтись. Требуются более прицельные технологии.
Способы получения моноклональных антител
Получение моноклональных антител — это сложный многоступенчатый процесс, который проходит следующие этапы:
- Иммунизация животных. Обычно используются мыши или крысы. Это нужно для того чтобы увеличить количество лимфобластов — клеток, продуцирующих нужные антитела и перевести эти клетки в активное состояние. После выделения из организма эти клетки не могут долго существовать в лабораторных условиях, они погибнут даже на питательных средах с содержанием ростовых факторов. Чтобы это предотвратить, их скрещивают со злокачественными миеломными клетками.
- Подготовка миеломных клеток. Параллельно с иммунизацией животных проводят подготовку опухолевых миеломных клеток. Они, во-первых, обладают способностью синтезировать моноклональные антитела, а во-вторых, обладают неограниченным жизненным потенциалом (они бессмертны и способны к бесконечному воспроизведению). Для того чтобы миеломные клетки не погибли вне организма, их культивируют на специальных средах с использованием факторов роста.
- Гибридизация (слияние) лимфобластов и миеломных клеток для образования гибридомы. Для этого клетки обрабатывают различными антителами, чтобы изменить строение их мембран и спровоцировать образование цитоплазматических контактов. При этом образуются разные типы клеток, имеющих двойной набор хромосом (дикарионы). Это могут быть дикарионы, образованные только лимфоцитами, или только миеломными клетками. Но для производства моноклональных антител нужны именно дикарионы, образованные лимфоцитом и миеломной клеткой — гибридные клетки.
- Отбор гибридных клеток. Для этого используют специальные растворы, которые позволяют выжить только лимфобластным и гибридомным дикарионам. Первые в скором времени погибают, т. к. не обладают возможностью безграничного деления, а гибридомные клетки остаются жизнеспособными.
- Реклонирование гибридомных клонов.
- Определение и отбор гибридом, продуцирующих моноклональные антитела. Обычно для этого используется иммуноферментный анализ.
- Массовое наращивание антител.
- Очистка полученных антител. Степень очистки будет определяться областью применения препарата. Если это диагностика, достаточно 70-95% степени чистоты. Если препарат предполагается использовать для иммунотерапии, требуется более высокая степень чистоты. Для очистки используется аффинная и ионообменная хроматография.
- Удаление оставшихся примесей и обеззараживание полученного препарата от вирусов и бактерий.
В настоящее время идет тенденция отказа в использовании антител животных для лечебных целей. Во-первых, они являются чужеродными агентами для организма и могут спровоцировать аллергические реакции, вплоть до анафилаксии, что напрямую угрожает жизни пациентов. Во-вторых, иммунная система человека, распознавая такие антитела как чужеродные, будет пытаться их инактивировать, что снизит эффективность противоопухолевого лечения. Получить человеческие моноклональные антитела вышеописанным методом не представляется возможным, ввиду следующих проблем:
- Иммунизация человека различными антигенами неэтична.
- Даже если получить иммунизированные лимфоциты человека, будут проблемы на этапе их слияния с клетками миеломы мыши — полученные гибридомы будут нестабильны.
- Клеточные линии миеломы человека, которые можно было бы эффективно использовать в рамках биотехнологий для получения антител, пока получить не удалось.
В этой связи необходимо было искать новые технологии получения антител. Решением проблемы стали гибридные, гуманизированные и одноцепочечные антитела, производство которых подразумевало применение гибридомной технологии, кратко описанной выше, и технологии рекомбинантной ДНК.
Механизм действия моноклоналных антител
Моноклональные антитела широко используются в лечении заболеваний, у которых в патогенезе замешан иммунный компонент. С их помощью лечат псориаз, аутоиммунные заболевания, ревматоидный артрит, рассеянный склероз. Большие перспективы эти технологии получили и в онкологии в рамках таргетной терапии. При этом, их эффект основан на различных механизмах, которые рассмотрены ниже.

В качестве примера изменения клеточных сигналов можно привести рецепторы факторов роста. Некоторые злокачественные клетки имеют на своей поверхности большое количество рецепторов к факторам роста, активирующим каскад реакций, направленный на усиление размножения клетки. Чем больше таких рецепторов, тем активнее протекает этот процесс. Если блокировать рецептор с помощью моноклонального антитела, он не сможет связаться с лигандом (фактором роста), и соответственно каскад этих реакций не будет запущен. Клетка не будет так активно размножаться и в конце концов погибнет.
Этот механизм реализуется следующим образом. Антитело связывается с антигеном, находящимся на поверхности злокачественной клетки, что приводит к активации многоэтапной системы комплемента (механизма иммунного ответа). Конечным этапом этих реакций является образование особого белка С 9, который перфорирует клеточную мембрану раковой клетки, что в конечном итоге приводит к ее гибели.
Препараты с моноклональными антителами
Препараты на основе моноклональных антител уже два десятилетия входят в протоколы противоопухолевого лечения некоторых злокачественных новообразований. В 2008 году ВОЗ были приняты рекомендации относительно непатентованных названий таких препаратов:
- Их название должно заканчиваться на маб, от английского monoclonal antibody.
- Для указания источника получения моноклонального антитела должны использоваться следующие подосновы:
- -аксо — гибридное антитело.
- -о — мышиное антитело.
- -кси — химерное антитело.
- -у — человеческое антитело.
В настоящее время используется два вида противоопухолевых моноклональных антител:
- Неконъюгированные антитела — они оказывают непосредственное действие на процессы, которые приводят к гибели злокачественной клетки.
- Конъюгированные антитела — они связаны (конъюгированы) с токсинами или изотопами. Токсины и изотопы обладают уничтожающим действием на злокачественные клетки, а антитело обеспечивает их прицельную доставку к клеткам-мишеням.
Эти препараты используются чаще всего. Их целью является определенный рецептор на поверхности злокачественной клетки.
К этому типу препаратов относится ритуксимаб — первое моноклональное антитело, которое было одобрено для применения в клинической практике. Его используют для лечения CD20+ В-клеточных лимфом. Рецептор CD20 есть на В-лимфоцитах, как здоровых, так и опухолевых, но он отсутствует на других тканях и клетках, в том числе на стволовых. Поэтому при воздействии ритуксимаба хоть и погибает популяция В-лимфоцитов, но потом она восстанавливается за счет нетронутых стволовых клеток. Причем восстанавливаются именно здоровые клетки.
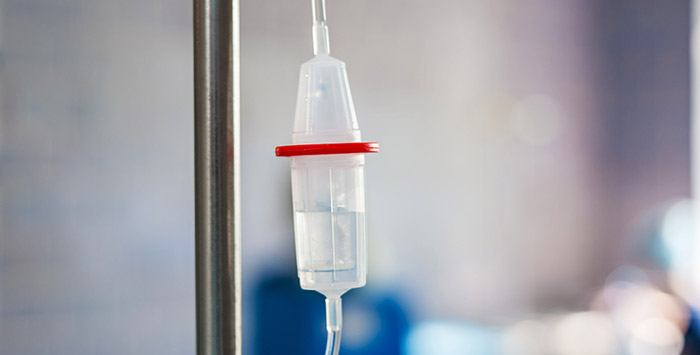
Неконъюгированные антитела могут помечать злокачественные клетки и делать их видимыми для иммунной системы. Таким способом работает алемтузумаб, который связывается с CD52+ лимфоцитами и привлекает к ним внимание иммунитета.
Также к неконъюгированным моноклональным антителам относятся ингибиторы рецепторов факторов роста. Факторы роста — это специальные молекулы, которые запускают деление клетки. Для того чтобы запустить этот процесс, фактор должен связаться со специальным рецептором, расположенным на мембране клетки, что приведет к каскаду соответствующих реакций. Такие рецепторы есть и у здоровых клеток, и у злокачественных, но у злокачественных их может быть очень много, что позволяет таким клеткам делиться быстрее. Блокирование рецепторов с помощью антител приводит к нарушению этого процесса деления и клетки уже не могут бесконтрольно размножаться. К таким препаратам относится трастузумаб, цетуксимаб и др.
К неконъюгированным антителам относятся и ингибиторы ангиогенеза — образования кровеносных сосудов. Ангиогенез очень важен для злокачественных опухолей, чтобы получать большее количество кислорода и питательных элементов, поэтому опухоли инциируют его образование с помощью специальных химических сигналов. Моноклональные антитела либо блокируют передачу этих сигналов, либо разрушают уже созданную внутри опухоли сосудистую сеть. Это приводит к нарушению ее питания и остановке роста. К группе этих препаратов относится рамуцирумаб, бевацизумаб и др.
Конъюгированные моноклональные антитела связывают с цитотоксическими или радиотоксическими веществами, что позволяет прицельно воздействовать разрушающим агентом на злокачественные клетки. В качестве примера такого препарата можно привести ибритумомаб (Зевалин), в котором моноклональное антитело против CD20 (как мы помним, это маркер В-лимфоцитов) соединено с радиоактивным изотопом — иттрием-90. Препарат применяется для лечения В-клеточных лимфом. В качестве другого препарата можно привести Кадсилу — препарат, в котором антитело трастузумаб конъюгировано с ингибитором микротрубочек DM1, оказывающим цитотоксический эффект. Применяют его для лечения рака молочной железы.
Проблемы при использовании моноклональных антител
Несмотря на, казалось бы, огромные перспективы в лечении онкологических больных, применение моноклональных антител не является панацеей и тоже имеет ряд проблем:
- Препараты на основе моноклональных антител биологически и биохимически нестабильны. Особенно это касается конъюгированных антител. Это требует особых условий производства, хранения и транспортировки.
- Антитела плохо проникают внутрь опухоли.
- Они могут вызывать иммунный ответ против себя, что блокирует их действие. У 75% пациентов, которым вводились мышиные антитела, наблюдалось образование нейтрализующих антител, что снижало эффективность лечения.
- Препараты на основе моноклональных антител оказывают токсическое действие. Конечно, оно не такое выраженное как у цитостатиков, но в ряде случаев токсичность настолько высокая, что требует отмены препарата.
- Наиболее важным моментом является высокая специфичность моноклональных антител и высокая гетерогенность опухолевых клеток. Не все раковые клетки имеют молекулы мишени, на которые направлено действие препарата. Соответственно, они ускользают от его действия и остаются нетронутыми. Постепенно масса этих клеток накапливается и опухоль становится резистентной к данному методу лечения.
Чтобы улучшить результаты лечения, разрабатываются новые виды моноклональных антител. Одним из вариантов являются биспецифические антитела, которые направлены сразу на две молекулярные мишени, например, блинатумомаб — препарат, направленный сразу на две клеточные мишени В-лимфоцита — CD 19 и CD22. Он повышает узнаваемость злокачественных клеток даже после их трансформации в другие виды лейкоза.
В любом случае моноклональные антитела — это новое и высокоперспективное направление в современной онкологии. Разработка современных, более совершенных технологий помогает решать имеющиеся проблемы и делает лечение пациентов эффективнее и безопаснее.
В составе комплексной терапии рака простаты отдельное место отводится лечению медицинскими препаратами. При своевременном применении в совокупности с лучевой терапией, хирургическим вмешательством в среднем способна продлить жизнь пациента на 10 лет, а также существенно улучшить качество жизни онкобольного.

- Сущность медикаментозного лечения
- Виды используемых препаратов
- Антиандрогены
- Противоопухолевые
- Иммунопрепараты
- Кортикостероиды
- Препараты на стадии экспериментов
Сущность медикаментозного лечения
Медикаментозная терапия рака простаты проводится комплексно, при лечении ставится много задач, каждую из которых решает отдельный медикамент. Так, одни лекарства уничтожают клетки рака, другие облегчают симптомы течения онкологии, устраняют причину болезни, снижают рост новообразования и т. д.
На ранних этапах онкологии предстательной железы используется гормональная терапия, по мере появления метастазов назначают химиотерапию. Медикаментозное лечение не применяется самостоятельно, его использование эффективно в комплексе с лучевой терапией и хирургическим вмешательством.
На крайних стадиях рака цель терапии – управлять онкологией, а не вылечить ее. Лечение позволяет максимально увеличить продолжительность жизни больного и предотвратить дальнейшее развитие метастазов. Кроме того, назначается прием симптоматических средств, чтобы облегчить состояние больного, снять болевой синдром, отечность.
Виды используемых препаратов
Выбор конкретного препарата при онкологии простаты проводится только лечащим врачом, учитывая следующие характеристики:
- возраст пациента;
- стадия рака;
- агрессивность новообразования;
- сопутствующие патологии.

Задайте вопрос врачу-урологу!

Выделяют следующие группы препаратов, используемых при онкологии:
- гормональные;
- патогенетические;
- симптоматические.
Гормональные препараты воздействуют на причину возникновения рака. Медикаменты этой группы предотвращают синтез тестостерона и ограничивают его влияние на простату.
Патогенетическая терапия направлена на восстановление прежнего функционирования организма больного. После химиотерапии и лучевого лечения онкобольной нуждается в повышении иммунитета и восстановлении первичного метаболизма. Симптоматическое лечение направлено на устранение болевого синдрома, облегчение опорожнения мочевого пузыря.
Применяя препараты, угнетающие выработку андрогенов, невозможно полностью устранить воздействие тестостерона на раковые клетки. В небольшом количестве гормон вырабатывается надпочечниками. Антиандрогенные препараты не воздействуют на работу внутренних желез, они предотвращают взаимодействие простаты с тестостероном.

Список лучших представителей группы:
- Абиратерон.
- Бикалутамид.
- Флутамид.
- Фирмагон.
- Нилутамид.
- Энзалутамид.
- Апалутамид.
Абиратерон является новейшим препаратом, может использоваться даже на запущенных стадиях онкологии. Таблетки обладают выраженным обезболивающим эффектом, благодаря чему используются у больных с метастатической формой рака. Подавляет выработку тестостерона в яичках, надпочечниках и самой опухоли. Препарат предназначен для мужчин с раком простаты, который перестал отвечать на гормональную терапию.

Бикалутамид относится к нестероидным медикаментам с противоопухолевыми свойствами. Воздействует на эндокринную систему, останавливает поступление андрогенов к клеткам рака. Препарат Касодекс является его аналогом, действующее вещество которого бикалутамид.
Флутамид применяется при метастатической форме патологии. Препарат подавляет активность тестостерона на клеточном уровне.
Фирмагон имеет действующее вещество дегареликс, способствует снижению продуцирования тестостерона в семенниках. Форма макропрепарата – инъекции.
Нилутамид применяют при паллиативном лечении рака с метастазами. Способствует нарушению деления раковых клеток железы. Назначают сразу после хирургической или медикаментозной кастрации. Энзалутамид блокирует андрогенные рецепторы и тормозит прогрессирование заболевания. Применяют при онкологии простаты завершающей стади. Апалутамид относится к классу нестероидных антиандрогенов (как и энзалутамид), однако имеет повышенную удельную активность и меньшее воздействие на нервную систему.
Это лекарства с цитостатическим эффектом. Препараты блокируют деление патологических клеток, их рост и развитие, способствуют гибели раковых клеток. Противоопухолевые медикаменты не используются на ранних этапах онкологии, они применяются на стадии появления метастазов, когда оперативным путем удалить новообразование не представляется возможным.

Препарат Эстрацит имеет действующее вещество эстрамустина фосфат. Действие заключается в понижении концентрация тестостерона в организме, как после хирургической кастрации. При этом Эстрацит при приёме умеренной дозы не допускает сильного кроветворного ингибирования.
Различают следующие разновидности иммунотерапии:
- моноклональные антитела (искусственный аналог иммунитета);
- ингибиторы контрольных точек (подавляют работу иммунитета, чтобы облегчить выявление и уничтожение раковых клеток);
- противораковые вакцины (способствуют формированию противоопухолевого иммунитета при помощи вакцины, содержащей иммуногенные антигены);
- иммуномодуляторы (активизируют силы иммунитета в целом).
Представители препаратов данной группы – бисфосфонаты. Используются для лечения костных метастазов, предотвращают костные осложнения и купируют болевой синдром. Золендроновая кислота относится к бисфосфонатам третьего поколения и в 100 эффективнее первого поколения.
Деносумаб – генно-инженерный препарат на основе моноклональных антител, применяется при костных метастазах рака простаты. Препарат способствует укреплению костных тканей, уменьшает вероятность компрессии спинного мозга. Лекарство воздействует на обмен веществ костной и хрящевой тканей.
Препараты снимают воспалительный процесс, используются при лечении онкологии с образованием метастазов при отсутствии улучшений после гормональной терапии. К кортикостероидам, используемым для лечения рака предстательной железы, относятся Преднизолон, Гидрокортизон и Дексаметазон.

Преднизолон улучшает самочувствие пациента, снижает показатель ПСА (простатспецифического антигена). Гидрокортизон, Дексаметазон и Преднизолон применяют в сочетании с противоопухолевыми препаратами. Небольшие дозы медикаментов способны подавлять надпочечниковые андрогены. Способствуют улучшению качества жизни больного, снимают воспаление.
Препараты на стадии экспериментов
Наиболее перспективным направлением в борьбе с онкологией простаты является вакцинирование от рака – разработка израильских врачей. За основу вакцины берется собственная кровь больного. После ее синтетической обработки и введения наблюдается активизация иммунитета.
Эксперты установили, что вакцина способна остановить метастазирование у 77% больных. Около 50% больных в ходе исследования отмечали уменьшение опухоли. Заявлено о способности продлить жизнь онкобольного на несколько лет. Апробирование методики происходит в Германии, США. Пока не обозначается дата, когда вакцина станет общедоступной, но обычно от момента клинических исследований до продажи препарата проходит 10–15 лет.
Если у вас остались вопросы, задайте их в комментариях (это абсолютно анонимно и бесплатно). По возможности, я или другие посетители сайта помогут вам.
Читайте также:


