Международная классификация рака желудка
Определение стадии развития рака имеет большое практическое значение. Оно позволяет выбрать наиболее адекватный метод лечения для каждого больного и оценить результаты различных хирургических операций.
Классификация по TNM была предложена Американским объединенным комитетом по изучению стадий рака и результатов его лечения (American Joint Comittee for Cancer Staging and Results Reporting of Cancer) в 1970 году и модифицирована в 1977.
Буква Т обозначает первичную опухоль:
Т1: опухоль ограничена слизистой оболочкой и подслизистой основой.
Т2: опухоль проникает в мышечную оболочку без поражения серозной оболочки.
Т3: опухоль прорастает серозную оболочку без инвазии в соседние структуры.
Т4: опухоль прорастает через серозную оболочку и распространяется на соседние структуры.
Буква N- наличие или отсутствие метастазов в регионарных лимфатических узлах:
Nx: недостаточно данных для оценки регионарных лимфоузлов.
N0: нет признаков метастатического поражения регионарных лимфатических узлов.
N1 имеются метастазы в лимфатических узлах не далее 3 см от края первичной опухоли.
N2: имеются метастазы в лимфатических узлах на расстоянии более 3 см от края первичной опухоли.
Буква R - наличие остаточного опухолевого поражения:
R0: после резекции желудка данных о наличии опухолевого поражения нет.
R1 после резекции желудка имеются микроскопические признаки опухоли.
R2: после резекции желудка имеются макроскопические признаки опухоли.
Буква М - наличие или отсутствие отдаленных метастазов:
М0: недостаточно данных для определения отдаленных метастазов.
М1 : имеются отдаленные метастазы.
Группировка рака по стадиям:
1 стадия рака желудка — T1-T2, N1,M0
2 стадия рака желудка — T1-T3, N1-N2,M0
3 стадия рака желудка — T2-T4, N2-N3, M0
4 стадия рака желудка — T1-T4, N1-N3,M0-M1
Различают следующие стадии рака желудка:
Стадия 0 (Внутриэпителиальный рак)
На нулевой стадии атипичные клетки находятся во внутреннем поверхностном слое слизистой оболочки стенки желудка. Эти атипичные клетки могут образовать раковую опухоль и распространиться на соседние нормальные ткани.
Стадия I
На первой стадии раковая опухоль уже сформировалась. Эту стадию делят на стадии IА и IВ, в зависимости от того, как распространился рак.
•Стадия IА: рак полностью распространился на слизистую оболочку стенки желудка.
•Стадия IВ: рак распространился
- полностью на слизистую оболочку стенки желудка и присутствует в 1 – 6 лимфатических узлах в области опухоли; или
- на мышечный (средний) слой стенки желудка без метастазов в лимфооузлы.
Стадия II
На второй стадии рак распространился:
•полностью на слизистую оболочку стенки желудка, и присутствует в 7 – 15 лимфатических узлах в области опухоли; или
•на мышечный (средний) слой стенки желудка, и присутствует в 1 – 6 лимфатических узлах в области опухоли; или
•на серозный (внешний) слой стенки желудка, но не в лимфатические узлы или другие органы.
Стадия III
Третью стадию рака желудка подразделяют на стадии IIIА и IIIВ, в зависимости от того, как распространился рак.
•Стадия IIIА: рак распространился на:
- мышечный (средний) слой стенки желудка и 7 – 15 лимфатических узлов в области опухоли; или
- серозный (внешний) слой стенки желудка и 1 – 6 лимфатических узлов в области опухоли; или
- органы, находящиеся рядом с желудком, но не лимфатические узлы или другие части организма.
•Стадия IIIВ: рак распространился на серозный (внешний) слой стенки желудка и 7 – 15 лимфатических узлов в области опухоли.
Стадия IV
На четвертой стадии рак распространился на:
•органы, находящиеся рядом с желудком, и хотя бы один лимфатический узел; или
•больше 15 лимфатических узлов; или
•другие части организма.
Принципы лечения
Выбор метода лечения зависит от многих факторов: месторасположение и стадия опухоли являются важными факторами. К другим факторам относится возраст, общее состояние и личные пожелания.
Основными методами лечения рака желудка являются: операция, химиотерапия и облучение. Часто наилучшим подходом к лечению может быть применение двух и более методов. Главной целью лечения является полное избавление от болезни. В том случае, когда полное излечение невозможно, терапия направлена на облегчение симптомов болезни, таких как нарушение приема пищи, боль или кровотечение. Перед началом лечения важно уточнить цель предполагаемой терапии.
Дата добавления: 2016-05-16 ; просмотров: 2008 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
ГЛАВА 8
РАК ЖЕЛУДКА (С16)
Наилучшие успехи отмечены при хирургическом лечении раннего рака желудка, когда опухоль ограничена слизистым и подслизистым слоями стенки желудка. Так, 5-летняя выживаемость составляет при поражении слизистой оболочки 85-92%, подслизистой — 68-78%.
К наиболее прогностически неблагоприятным факторам большинство авторов относят прорастание опухолью всей стенки желудка, метастатическое поражение регионарных лимфатических узлов, локализацию в проксимальном отделе желудка, инфильтративный тип роста и др.
Так, при отсутствии метастатического поражения регионарных лимфатических узлов 5-летняя выживаемость составляет 34-62%, а при их наличии — 8-36%; при прорастании опухолью серозной оболочки — 10-39%; при локализации опухоли в дистальных отделах желудка — 39-61%, в проксимальном — 23-42%, а при тотальном поражении — 15%.
В целом, после потенциально радикальных операций у 16-80% больных развиваются изолированные рецидивы или рецидивы в сочетании с отдаленными метастазами. По данным клинико-инструментального исследования, местно-регионарные рецидивы диагностируются у 16-25% больных, по данным повторных оперативных вмешательств — у 5-54%, по секционным находкам — до 68-80%.
В последние десять лет в Республике Беларусь наблюдалось постепенное снижение ежегодно регистрируемых случаев заболевания раком желудка с 3577 в 2001 году до 3147 в 2010 г. (в 1,1 раза).
Из вновь заболевших раком этой локализации в 2010 году, 1804 случая было зарегистрировано среди мужчин и 1343 — среди женщин. У 474 больных раком желудка (15,1%) установлена I стадия заболевания, у 757(24,1%) – II, у 806 (25,6%) – III стадия, у 957 (30,4%) – IV стадия заболевания.
Грубый интенсивный показатель заболеваемости раком желудка для всего населения республики составил 32,6 0 /0000, для мужчин – 40,0 0 /0000, для женщин – 26,0 0 /0000. Стандартизованные показатели заболеваемости — 19,0 0 /0000, 29,7 0 /0000, 12,4 0 /0000 соответственно.
На конец года в онкологических учреждениях республики состояло на учете 12 369 больных раком желудка (6 510 мужчин и 5 859 женщин). Болезненность в целом по республике составила 128,0 0 /0000, 144,4 0 /0000 — у мужчин и 113,6 0 /0000 — у женщин.
В 2010 году умерло 2233 больных раком желудка (1307 мужчин и
926 женщин). Грубый интенсивный показатель смертности составил в целом 23,1 0 /0000, 29,0 0 /0000 — у мужчин и 18,0 0 /0000 — у женщин, а стандартизованный — 13,5 0 /0000, 21,5 0 /0000, 8,5 0 /0000 соответственно.
Одногодичная летальность для всего населения была 50,7%, у мужчин –51,6%, у женщин – 49,3%.
Соотношение смертности и заболеваемости раком желудка выглядело следующим образом: 0,71 – среди всего населения, 0,72 – у мужчин, 0,69 – у женщин.
Международная гистологическая классификация рака желудка.
| Аденокарцинома |
| кишечный тип |
| диффузный тип |
| Папиллярная аденокарцинома |
| Тубулярная аденокарцинома |
| Муцинозная аденокарцинома |
| Перстневидно-клеточный рак |
| Аденоплоскоклеточный рак |
| Плоскоклеточный рак |
| Мелкоклеточный рак |
| Недифференцированный рак |
| Другие формы рака |
83.1. Макроскопическая классификация рака желудка по Borrmann
1 тип – грибовидный или полиповидный
2 тип – язвенный с четко очерченными краями
3 тип – язвенно-инфильтративный
4 тип – диффузно-инфильтративный (Linitis plastic)
5 тип – неклассифицируемые опухоли
83.2. Макроскопические типы раннего рака желудка
I тип – возвышенный (высота опухоли больше толщины слизистой оболочки)
II тип – поверхностный
III тип – изъязвленный (язвенный дефект слизистой оболочки)
84. Классификация TNM(7-е издание, 2009 г.)
84.1. Правила классификации
Классификация применима только для рака желудка. Должно быть гистологическое подтверждение диагноза. Опухоль, эпицентр которой находится в 5см от кардиоэзофагеального перехода и распространяется также на пищевод, классифицируется согласно классификации рака пищевода. Все другие опухоли с эпицентром в желудке, расположенном на расстоянии больше 5см от пищеводно-желудочного соединения, или те, что расположены в пределах 5см от пищеводно-желудочного соединения, без распространения на пищевод, классифицируются как рак желудка.
84.2. Процедурами оценки категорий T, N и M являются:
| Категории T | Физикальное обследование, методы визуализации, эндоскопия и/или интраоперационное исследование |
| Категории N | Физикальное обследование, методы визуализации и/или интраоперационное исследование |
| Категории M | Физикальное обследование, методы визуализации и/или интраоперационное исследование |
84.3. Анатомические части
Антральный (С16.3) и пилорический (С16.4) отделы
84.4. Регионарные лимфатические узлы (рисунок 2)
Регионарными лимфоузлами для рака желудка являются перигастральные узлы, расположенные вдоль малой (1, 3, 5) или большой (2, 4а, 4б, 6) кривизны, вдоль левой желудочной (7), общей печеночной (8), селезёночной (10, 11) и чревной (9) артерий, а также гепатодуоденальные узлы (12).

Рисунок 2. Регионарные лимфатические узлы
Поражение других внутрибрюшинных лимфоузлов, таких как ретропанкреатических и парааортальных, классифицируется как отдаленные метастазы.
84.4. Клиническая классификация TNM
84.4.1. Т – первичная опухоль
ТХ – недостаточно данных для оценки первичной опухоли
Т0 – первичная опухоль не определяется
Tis – карцинома in situ: внутриэпителиальная опухоль без инвазии собственной пластинки слизистой оболочки, дисплазия высокой степени
Т1 – опухоль поражает собственную пластинку слизистой оболочки, мышечную пластинку слизистой оболочки или подслизистый слой
Т1а – опухоль поражает собственную пластинку или мышечную пластинку слизистой оболочки
Т1b – опухоль поражает послизистый слой
Т2 – опухоль поражает мышечную оболочку
Т3 – опухоль поражает субсерозный слой
Т4 – опухоль перфорирует серозную оболочку или поражает прилегающие структуры 1,2,3
Т4а – опухоль прорастает серозную оболочку
Т4b – опухоль распространяется на соседние структуры 1,2,3
1 соседнимиструктурами желудка являются селезёнка, поперечно-ободочная кишка, печень, диафрагма, поджелудочная железа, брюшная стенка, надпочечник, почка, тонкая кишка забрюшинное пространство.
2 внутристеночное распространение на двенадцатиперстную кишку или пищевод классифицируется по глубине наибольшей инвазии в любую из этих областей, включая желудок.
3 опухоль, проникающая в желудочно-ободочную или желудочно-печеночную связки, либо большой или малый сальник без перфорации висцеральной брюшины, покрывающей эти структуры, классифицируется как Т3.
84.4.2. N – регионарные узлы
NХ – недостаточно данных для оценки регионарных лимфатических узлов
N0 – нет признаков метастатического поражения регионарных лимфатических узлов
N1 – метастазы в 1-2 регионарных лимфоузлах
N2 – метастазы в 3-6 регионарных лимфоузлах
N3 – метастазы в 7 или более регионарных лимфоузлах
N3а – метастазы в 7-15 регионарных лимфоузлах
N3b – метастазы в 16 или более регионарных лимфоузлах
84.4.3. М – отдаленные метастазы
М0 – нет признаков отдаленных метастазов.
М1 – имеются отдаленные метастазы.
Отдаленные метастазы включают диссеминацию по брюшине и диссеминаты в большом сальнике, подтвержденные цитологически, и не рассматриваются как распространение опухоли на прилегающие структуры.
84.4.4. Патогистологическая классификация pTNM
Категории pT и pN соответствуют категориям T и N.
pN0 – гистологическое заключение о состоянии регионарных лимфоузлов должно быть основано на исследовании 16 или более лимфатических узлов. Если в исследованных лимфатических узлах нет метастазов, но их количество менее 16 – случай классифицируется как pN0 (независимо от общего количества, удаленного и исследованного)
84.4.5. Гистопатологическая дифференцировка G
GХ – степень дифференцировки не может быть оценена
G1 – высокая степень дифференцировки
G2 – средняя степень дифференцировки
G3 – низкая степень дифференцировки
G4 – недифференцированный рак
84.4.6. Группировка по стадиям (таблица 22)
Похожие темы научных работ по клинической медицине , автор научной работы — Шмак А.И., Ревтович М.Ю., Котов А.А.
Международная классификация рака желудка по системе TNM в сравнительном историческом аспекте
ПРОБЛЕМНЫЕ СТАТЬИ И ОБЗОРЫ
д.м.н. Шмак А.И., к.м.н. Ревтович М.Ю., Котов А.А.
РНПЦ онкологии и медицинской радиологии им. Н.Н. Александрова
Рак желудка - одна из наиболее часто встречающихся злокачественных опухолей человека, несмотря на наметившуюся тенденцию к снижению заболеваемости. По статистике заболеваемости и смертности рак желудка занимает лидирующие позиции во многих странах мира, в частности в странах Юго-восточной Азии, странах СНК7 включая Республику Беларусь, Восточной Европы, Латинской Америки [26].
Отдаленные результаты лечения больных раком желудка остаются все еще неудовлетворительными, за исключением ранних стадий. Поэтому изучение прогностических факторов играет очень важную роль в выборе стратегии лечения больных [24]. Известными и независимыми прогностическими факторами являются глубина опухолевой инвазии стенки желудка (Т) и метастатическое поражение лимфатических узлов М [3, 14-16, 18, 19, 22, 27, 29].
В настоящее время большинство онкологов применяют классификацию международного противоракового союза (и1СС) и Американского объединительного комитета ^СС) - TNM. Система TNM классификации используется для определения стадии опухолевого процесса и имеет большое научно-практическое значение. Она помогает клиницисту в планировании лечения, определении прогноза заболевания, оценке результатов лечения и в облегчении обмена научной информацией между медицинскими центрами. Основная цель Международной классификации - разработка методики единообразного представления клинических данных [8, 20, 21, 24].
В настоящее время система TNM является золотым стандартом в стадирова-нии злокачественных опухолей вообще и рака желудка в частности.
В 2009 г была издана 7-я редакция классификации TNM злокачественных новообразований, которая была представлена на VIII Международном конгрессе по раку желудка.
водно-желудочного соединения и распространяющиеся на пищевод. Согласно новой классификации, такие опухоли стали относить к раку пищевода.
[пубина опухолевой инвазии стенки желудка (Т) и количество метастатических лимфатических узлов М, - самые важные прогностические факторы у больных раком желудка [3, 6, 7, 14, 18, 19]. По мнению ряда авторов, особенно важным и независимым прогностическим фактором является состояние регионарных лимфоузлов [5, 22].
Для стадирования рака желудка используются две классификации: Японская классификация рака желудка ^СвС) и классификация TNM. При этом классификация метастатически измененных лимфоузлов в каждой из этих классификаций производится по-разному. Так, классификация JCGC основана на изучении состояния лимфатических узлов в зависимости от их локализации по отношению к местоположению опухоли [10]. Аналогичный принцип был использован в 4-м издании TNM-классификации злокачественных опухолей. В частности, оценка критерия N была также основана на степени анатомического расположения регионарных лимфатических узлов (меньше или больше 3 см от первичной опухоли) [14]. Однако начиная с 5-го выпуска TNM-классификации, критерий N был основан на изучении только количества удаленных метастатических лимфатических узлов [23]. Предпосылкой к переходу на количественную оценку критерия N послужили данные ряда исследователей о превосходстве такого подхода в объективности и точности прогноза заболевания в сравнении с Японской классификацией рака желудка (JCGC) [1, 11].
В 5-м издании и|Сс классификации TNM критерий N0 указывал на отсутствие
метастатического поражения регионарных лимфоузлов; N1, N2, N3 соответствовали метастатическому поражению 1-6, 7-15 и более 15 регионарных лимфоузлов соответственно [23].
В 7-м выпуске и1СС TNM-классифи-кации рака желудка основные изменения касаются оценки критерия N N0 - нет метастатического поражения региональных лимфатических узлов; N1 - метастатическое поражение 1-2, N2 - 3-6, N3a - 7-15 и N3^ - больше чем 15 регионарных лимфоузлов [25].
Необходимость в пересмотре и модификации и1СС классификации широко обсуждалась в научной литературе еще задолго до принятия современной классификации [4, 9]. Ряд японских исследователей указывали, что прогноз для pN3 не был достоверно хуже по сравнению с pN2 в их исследованиях [13]. В другом исследовании [9], было показано что критерий N классификации и1СС 6-го издания не обладает истинной информативностью при раннем раке желудка.
¿. СИае с соавт. [2] провели сравнительный анализ 5-, 6- и 7-го изданий и1СС классификации. В исследование было включено 295 пациентов с раком желудка, которые были оперированы одним хирургом. При однофакторном анализе независимыми прогностическими факторами были размер, локализация опухоли, состояние регионарных лимфоузлов.
МЕДИЦИНСКИЕ НОВОСТИ |11
Проблемные статьи и обзоры |мн
Сравнительный многофакторный анализ показал, что критерии T и N в соответствии с 7-м по сравнению с 5-м и 6-м выпусками UICC классификации являлись достоверно независимыми прогностическими факторами. Показатели выживаемости в соответствии с 7-м изданием UICC классификации распределялись более равномерно. Так, в соответствии с 5-м и 6-м изданиями UICC классификации различия в 5-летней выживаемости в группах пациентов между N0 и N1 составили 23,5%, N1 и N2 - 43,1%, N2 и N3 -17,7%. Перерасчет аналогичных данных в соответствии с 7-м изданием UICC классификации показал, что различия в группах между N0 и N1 составили 16,1%, N1 и N2 - 18,7%, N2 и N3а - 31,8%, N3а и N3b - 17,7% [2]. Более равномерное распределение показателей выживаемости при расчете их в соответствии с 7-м изданием UICC было отмечено и другими авторами [3, 5, 17, 28]. Так, по данным Deng J. с соавт. [5], получены достоверные различия 5-летней выживаемости в группах больных N1 и N2 в соответствии с 7-м изданием UICC классификации и никаких различий между группами пациентов N2 и N3 при расчетах в 5-м и 6-м выпусках.
В 7-м издании UICC изменения коснулись и других критериев. Так, в современной трактовке категория T изменена по сравнению с предыдущим изданием. Критерий Т1 разделён на Т1а (инвазия lamina propria) и Т1 b (инвазия в подслизистый слой). Т2 (ранее Т2а) соответствует опухоли, прорастающей в мышечный слой, а Т3 (ранее Т2Ь) - в субсерозный слой стенки желудка. Т4 (ранее Т3-4) характеризует опухоль, прорастающую в серозный слой или в окружающие структуры.
Изменения коснулись и трактовки критерия М (отдаленные метастазы). Категории Мх (недостаточно данных для
определения отдаленных метастазов) в современной редакции UICC классификации нет. Если по данным клинического и инструментального исследований на дооперационном этапе не установлены отдаленные метастазы, то это соответствует критерию сМо. Диагностированные по данным УЗИ, КТ МРТ например, метастазы в печени, будут трактоваться как сМ1. В случаях морфологической верификации отдаленных метастазов (пункционная биопсия) устанавливается критерий рМ1. Наличие раковых клеток в смывах с брюшины трактуется как М1.
В соответствии с критериями T N, М существенно изменена группировка по стадиям. В последнем издании UICC классификации все стадии, кроме IV разделены на подразделы А и В. Все случаи с установленными отдаленными метастазами, относятся к IV стадии заболевания.
Таким образом, имеется ряд существенных различий в 7-й редакции UICC классификации по сравнению с предыдущим изданием. В основном современная классификация требует выполнения более точного предоперационного стадиро-вания опухолевого процесса. Введенные новые дополнительные прогностические факторы позволяют более точно определить долгосрочный прогноз, а также тактику лечения.
1. Celen O., Yildirim E, Gulben K, Beiberoglu U. // Eur. J. Surg. Suppl. -2003. - Vol. 588. - P. 33 -39.
2. Chae S, Lee A, Lee J. // Gastric Cancer. - 2011. -Vol. 14, № 1. - P. 89 -99.
3. Del Rio P., Dell'Abate P., Soliani P. et al. // J. Ga-strointest. Surg. - 2003. - Vol. 7. - P. 912 -916.
4. Deng JY, Liang H, Sun D. et al. // J. Surg. Oncol. -2008. - Vol. 98. - P. 343 -348.
5. Deng JY, Liang H, Sun D. et al. // Ann. Surg. Oncol. - 2010. - Vol. 17. - P. 1259 -1266.
6. D'Ugo D, Pacelli F, Persiani R. et al. // World J. Surg. - 2002. - Vol. 26. - P. 672 -677.
7. Hermanek P., Sobin L.H (eds) TNM Classification of Malignant Tumors (UICC). - 4th ed. - Berlin: Springe, 1987. - P. 43 -46.
8. Hermanek P. // Cancer. - 2000. - Vol. 88. -P.1763 -1765.
9. Huang B, ZhengX, WangZ. et al. // Ann. Surg. Oncol. - 2009. - Vol. 16. - P. 61 -67.
10. Japanese Gastric Cancer Association. Japanese classification of gastric carcinoma. - 2nd English edition // Gastric Cancer - 1998. - Vol. 1. - P. 10 -24.
11. Ichikura T., Tomimatsu S, Uefuji K. et al. // Cancer. - 1999. - Vol. 86. - P. 553 -558.
12. Inoue K, Nakane Y, liyama H. et al. // Ann. Surg. Oncol. - 2002. - Vol. 9. - P. 27 -34.
13. Katai H, Yoshimura K, Maruyama K. et al. // Cancer. - 2000. - Vol. 88. - P. 1796 -1800.
14. Kim J.P., Kim YW., Yang H.K., Noh DY// World J. Surg. - 1994. - Vol. 18. - P. 872 -877.
15. Kim J.P., Lee J.H., Kim S.J. et al. // Gastric Cancer. - 1998 - Vol. 1. - P. 125 -133.
16. Kooby D.A., Suiiawinata A, Klimstra D.S. et al. // Ann. Surg. - 2003. - Vol. 237. - P. 828 -835.
17. Klein K.E, Hermans J., van Krieken J.H., van de Velde C.J. // Br. J. Cancer. - 2001. - Vol. 84, № 1. -P. 64 -71.
18. Manfe A.Z, Segalina P., Maffei FaccioliA. // Minerva Chir. - 2000. - Vol. 55. - P. 299 -305.
19. Maruyama K., Sasako M., Kinoshita T // Gut. -
1999. - Vol. 45 (suppl. 5). - P. 66A.
20. Omejc M., Juvan R., Jelenc F, Repse S. // Int. Surg. - 2001 - Vol. 86. - P. 14 -19.
21. PersianiR., RauseiS., BiondiA. et al. // Eur. J. Surg. Oncol. - 2007. - Vol. 34. - P. 519 -524.
22. Siewert J.R., Bottecher K., Stein H.J., Roder J.D. // Ann. Surg. - 1998. - Vol. 228. - P. 449 -461.
23. Sobin L.H, Wittekind C.H. TNM classification of malignant tumors (UICC). - 5th ed. - New York: Wiley 1997. - P. 59 -62.
24. Sobin L.H. // Cancer. - 2001. - Vol. 91. -P. 1589 -1592.
25. Sobin L.H., Wtttekind C, Gospodaowicz M. (eds) TNM classification of malignant tumors (UICC). 7th edn. - New York: Wiley -Blackwell, 2009. - P. 73 -77.
26. Takeuchi H., Kttagawa Y. // Ann. Surg. Oncol. -2010. - Vol. 17. - P. 1257 -1258.
27. Yamamura Y, Nakajima T., Ohta K. et al. // Gastric Cancer. - 2002. - Vol. 5. - P. 201 -207.
28. Yang H., Ahn H., Yoon H. et al. // Abstracts 8th IGCC. - 2009. - Vol. 51. - P. 29.
29. Yokota T, Kunii Y, Teshima S. et al. // Int. Surg. -
2000. - Vol. 85. - P. 286 -290.
Поступила 11.04.2011 г.
НАУЧНО- П РАКТИ Ч ЕСЛИ Й ЖУРНАЛ ДЛЯ ВРАЧЕЙ
Продолжается подписка на IV квартал 2011 г.*
16 лет мы вместе с вами во имя здоровья людей!
Стоимость подписки на 1 и 3 месяца соответственно: по индексу 74954 (инд.) - 10120 руб. и 30360 руб., по индексу 749542 (вед.) - 21810 руб. (НДС: 3635 руб.) и 65 430 руб. (НДС: 10905 руб.)
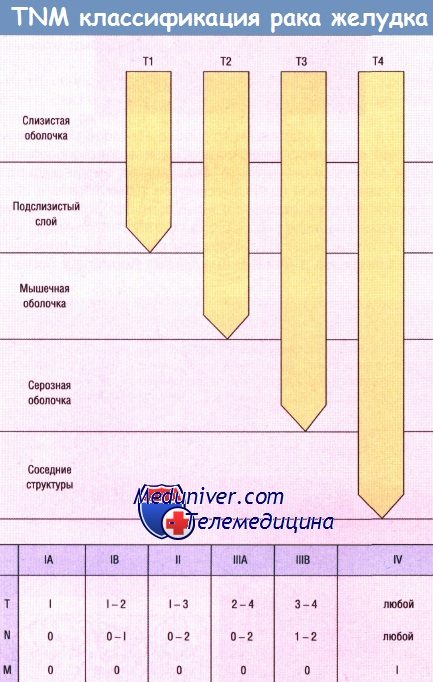
Установление классификации рака желудка и определение стадии его развития имеет большое практическое значение. Оно позволяет выбрать наиболее адекватный метод лечения для каждого больного и оценить результаты различных хирургических операций, сравнить статистические данные, полученные в различных хирургических центрах. Классификация по TNM была предложена Американским объединенным комитетом по изучению стадий рака и результатов его лечения (American Joint Comittee for Cancer Staging and Results Reporting of Cancer) в 1970 году и модифицирована в 1977. Буква Т обозначает первичную опухоль:
Т1: опухоль ограничена слизистой оболочкой и подслизистой основой.
Т2: опухоль проникает в мышечную оболочку без поражения серозной оболочки.
Т3: опухоль прорастает серозную оболочку без инвазии в соседние структуры.
Т4: опухоль прорастает через серозную оболочку и распространяется на соседние структуры.
Буква N обозначает наличие или отсутствие метастазов в регионарных лимфатических узлах:
Nx: недостаточно данных для оценки регионарных лимфоузлов.
N0: нет признаков метастатического поражения регионарных лимфатических узлов.
N1 имеются метастазы в лимфатических узлах не далее 3 см от края первичной опухоли, которые могут быть удалены при субтотальной резекции и гастрэктомии.
N2: имеются метастазы в лимфатических узлах на расстоянии более 3 см от края первичной опухоли, которые также удаляются при резекции и гастрэктомии, включая лимфатические узлы по ходу левой желудочной артерии, селезеночной артерии, чревного ствола и общей печеночной артерии. Буква R обозначает наличие остаточного опухолевого поражения:
R0: после резекции желудка данных о наличии опухолевого поражения нет.
R1 после резекции желудка имеются микроскопические признаки опухоли.
R2: после резекции желудка имеются макроскопические признаки опухоли.
Буква М обозначает наличие или отсутствие отдаленных метастазов:
М0: недостаточно данных для определения отдаленных метастазов.
М1 : имеются отдаленные метастазы.
Лимфатический отток от желудка описан был ранее. Расширению наших знаний о лимфогенном метастазировании рака желудка способствовали многочисленные исследования, многие из которых выполнены японскими учеными.
В желудке различают три лимфатических барьера: Первый лимфатический барьер образуется следующими группами лимфатических узлов: 1 — правые паракардиальные узлы; 2 — лимфатические узлы малой кривизны желудка, сопровождающие левую желудочную (венечную) артерию и правую желудочную (пилорическую) артерию; 3 — лимфатические узлы большой кривизны, сопровождающие левую желудочно-сальниковую артерию; 4 — лимфатические узлы, расположенные под привратником; 5 — лимфатические узлы, расположенные над привратником; 6 — лимфатические узлы, расположенные за привратником. Все эти лимфатические узлы удаляются при субтотальной резекции желудка или гастрэктомии. Второй лимфатический барьер образуется следующими лимфатическими узлами: 7 — передние, верхние передние и нижние панкреатодуоденальные лимфатические узлы; 8 — нижние диафрагмальные лимфатические узлы; 9 — лимфатические узлы, сопровождающие чревный ствол; 10 — лимфатические узлы, сопровождающие общую печеночную артерию; 11 — лимфатические узлы, расположенные вблизи желчного пузыря: 12 — лимфатические узлы, расположенные в области ворот селезенки; 13 — лимфатические узлы, расположенные над поджелудочной железой. Третий лимфатический барьер образуется следующими лимфатическими узлами: 14 — лимфатические узлы, расположенные под поджелудочной железой: 15 — лимфатические узлы, сопровождающие верхнюю брыжеечную артерию; 16 — лимфатические узлы, расположенные латерально от брюшной аорты; 17 — лимфатические узлы, расположенные спереди от брюшной аорты; 18 — лимфатические узлы, сопровождающие верхнюю полую вену. При выполнении и описании гистологического исследования различных групп лимфатических узлов их следует обозначать соответственно локализации, а не номеру, как делают некоторые авторы, гак как в этом случае хирургу приходится запоминать и номера, соответствующие локализации этих групп лимфатических узлов, что сложнее, чем просто запомнить их местонахождение. В классификации по TNM это означает: N0 лимфатические узлы не поражены. N1 поражен первый лимфатический барьер. N2 поражен второй лимфатический барьер. N3 поражен третий лимфатический барьер.
При резекциях желудка по поводу рака, по принятой в странах Запада методике, удаляют лимфатические узлы барьеров N. и N2, а иногда и некоторые группы лимфатических узлов барьера N3. Хирургическая резекция трех лимфатических барьеров желудка является трудной задачей и связана с высоким риском развития осложнений и летальности, хотя имеются и противоположные мнения. Расширенная лимфаденэктомия применяется только в исключительных случаях, так как не доказано, что она приводит к повышению выживаемости.
Онкологические заболевания нередко называют чумой XXI века. Действительно, распространенность этих патологий, к сожалению, растет, и врачи пока не нашли лекарства, которое действовало бы на все виды рака. Среди онкологических заболеваний рак желудка — один из самых распространенных: в год фиксируется около миллиона новых случаев, а смертность от рака желудка превышает 500 тысяч человек в год [1] . Россия входит в число стран, где пациенты сталкиваются с этой патологией достаточно часто. Какие симптомы могут выявить рак желудка и как его лечить, мы расскажем в этой статье.
Классификация рака желудка
Частота возникновения метастазов при этом заболевании превышает 80% [2] . Но на ранних стадиях проявления заболевания можно спутать с другими патологиями, поэтому пациенты нередко не обращают на тревожные симптомы внимания и начинают лечение несвоевременно.
Перечислим различные существующие сегодня классификации рака желудка.
- Международная классификация ВОЗ выделяет несколько разновидностей рака:
- Папиллярная аденокарцинома (опухоль из железистого эпителия);
- Тубулярная аденокарцинома (опухоль из клеток кубического и цилиндрического эпителия);
- Низкодифференцированная аденокарцинома (клетки, образующие опухоль, плохо различаются);
- Муцинозная аденокарцинома (опухоль состоит из эпителиальных клеток, которые могут продуцировать слизь);
- Перстневидный рак желудка (атипичные клетки быстро распространяются вглубь органа);
- Плоскоклеточный рак (развивается из клеток шиповатого слоя эпителия);
- Железисто-плоскоклеточный рак (сочетание аденокарциномы и плоскоклеточного рака);
- Карциносаркома (достаточно редко встречающаяся опухоль, состоящая из клеток разного вида);
- Хориокарцинома (редкая агрессивная форма заболевания, которая характеризуется ранним метастазированием);
- Недифференцированный рак (также агрессивная форма заболевания, для которого характерно раннее метастазирование);
- Другие формы рака.
- В рамках классификации по морфологическому признаку выделяются следующие виды рака желудка:
- Ограниченно растущий рак (экзофитная форма). Обычно для этой формы заболевания характерны кровотечения, симптомы интоксикации. Достаточно хорошо поддается излечению.
- Инфильтративно растущий рак (эндофитная, диффузная форма). Чаще связан с ростом метастазов, быстрым поражением желудка.
- Есть также переходные формы, объединяющие черты перечисленных двух.
- Классификацию рака желудка по гистологическому признаку называют также классификацией по Lauren. Фактически эта классификация описывает три формы рака желудка:
- Кишечный тип. Эта разновидность заболевания подобна раку кишечника. Опухоль напоминает железистую структуру.
- Диффузный тип. В опухоли дифференцируются одиночные клетки или небольшие группы клеток с большим содержанием муцина (слизи).
- Также выделяется смешанный тип, для которого характерны черты описанных выше двух.
- Нулевая. Начало процесса перерождения нормальных клеток эпителия в патологические. На этой стадии рак обычно не имеет проявлений, но если заболевание диагностируют, то пациенту рекомендуют оперативное лечение с высокими шансами на полное выздоровление.
- Первая. Врачи отмечают возникновение опухоли с четкими контурами, которая находится или в слизистом слое, или начинает проникать в мышечный. Симптомы: быстрая утомляемость, падение уровня гемоглобина в крови, вздутие живота после еды, отказ от еды, бледность.
- Вторая. На этой стадии опухоль начинает поражать не только оболочки желудка, но и лимфатические узлы. Рак на этой стадии вызывает болезненность желудка, жар, боль при глотании. Необходимо удалять опухоль, но если она находится в районе крупных сосудов, то операция сопряжена с очень большим риском.
- Третья. Опухоль разрастается, затрудняя движение желудка, начинается ее прорастание в соседние органы. Поражается мышечный слой стенки желудка и большое количество лимфоузлов. На этой стадии заболевания происходит резкое расстройство пищеварения, постоянная тошнота сочетается с запорами и диареей, пациент резко теряет вес.
- Четвертая. Опухоль прорастает в соседние, а также отдаленные органы (в том числе и в головной мозг), поражает большое количество лимфоузлов. На этой стадии рак желудка вызывает постоянные боли, частую рвоту с примесями крови, ощущение тяжести даже при небольших порциях съеденной пищи, накопление жидкости в брюшине. На этой стадии излечение рака невозможно, основная цель лечения — облегчение состояния пациента и предупреждение осложнений.
Мы уже упомянули о том, что рак желудка на начальной стадии явными симптомами не сопровождается. Тем не менее чем раньше обнаружена патология, тем выше шансы на успешное излечение. Именно поэтому важно знать о методах диагностики, с помощью которых можно достоверно выявить это опасное заболевание.
Ассоциация онкологов России разработала рекомендации, в соответствии с которыми основными методами диагностики рака желудка являются следующие:
- Осмотр, сбор анамнеза.
- Эндоскопия верхних отделов ЖКТ, биопсия тканей. В ходе обследования уточняются размеры опухоли, визуализируются ее границы.
- Рентген желудка. Врач может оценить протяженность опухоли, однако не при всех видах рака желудка этот вид диагностики показателен.
- УЗИ или КТ органов брюшной полости. УЗИ — неинвазивный метод диагностики, хорошо переносится пациентами. Позволяет оценить, есть ли метастазы и насколько они распространились.
- Клинический и биохимический анализы крови.
- ЭКГ и обследование грудной полости.
На сегодняшний день существует несколько методик лечения рака желудка, эффективность которых зависит от стадии заболевания, локализации опухоли, состояния пациента. Расскажем подробнее о каждом из видов лечения.
Оперативное лечение
Операция по удалению части желудка или желудка полностью является самым распространенным методом радикального лечения рака. При этом если операция проведена вовремя, на ранней стадии рака, выживаемость составляет более 90% в течение 5 лет. Во время операции удаляется не только часть органа или желудок полностью, но и лимфоузлы, в том числе и в большом количестве, если есть серьезный риск распространения опухоли.
Медикаментозное лечение
Медикаментозное лечение рака желудка проводится по нескольким направлениям. Во-первых, это обезболивающие препараты, причем на начальных стадиях заболевания не рекомендуется прописывать сильные анальгетики. В противном случае они не будут действовать на более поздних стадиях. В сочетании с анальгетиками могут быть назначены антидепрессанты и нейролептики для усиления эффекта.
Химиотерапия
На протяжении довольно длительного времени считалось, что при раке желудка химиотерапия неэффективна. Однако последние исследования показали, что трех- и пятилетняя выживаемость пациентов при применении химиотерапии вырастает на 10–15%.
Чаще всего для лечения рака желудка в рамках химиотерапии применяется 5-фторурацил, который блокирует деление клеток, а значит, и рост опухоли. В последние годы чаще стали использоваться препараты платины в составе комбинированной химиотерапии. Также химиотерапия применяется в сочетании с лучевым лечением.
Лучевая терапия
Как и при лечении других форм рака, при поражении желудка применяется лучевая терапия, которая в данном случае ограничена близким расположением других органов и вариабельным положением желудка. При облучении нужно, чтобы воздействию подвергался весь желудок, но в этом случае в зону облучения попадают, например, почки или сердце. Это осложняет проведение лечения.
Второй непростой момент при проведении лучевой терапии — питание больных. Рак желудка нередко приводит к серьезной потере массы тела, отсутствию аппетита, у больного может развиться анорексия. Лучевая терапия, ухудшающая самочувствие пациента, приводит к еще большему сокращению рациона, поэтому очень важно подобрать для пациента оптимальный режим питания и диету.
Лучевая терапия применяется в сочетании с другими методами. В частности, она может выполняться и во время операции, когда действие пучка частиц наиболее направлено. Такая методика помогает избежать лучевых осложнений.
Паллиативное лечение
Паллиативное лечение проводится на поздних стадиях рака желудка, чтобы облегчить состояние пациента. Удалить опухоль или избавиться от метастазов на этой стадии, как правило, невозможно, однако можно добиться облегчения состояния пациента. Для этого проводятся паллиативные операции, которые улучшают пищеварение, облегчают прохождение пищи по ЖКТ. Выполняется паллиативное удаление опухоли и метастазов. Это не приводит к излечению от рака, но улучшает качество жизни пациента. Также паллиативные операции по удалению очага опухоли уменьшают ее массу, снижают интоксикацию организма, позволяют провести курс химио- или лучевой терапии, которые оказываются более эффективными.
Врачи неизменно отмечают, что перспективы пациента с любым видом рака, в том числе раком желудка, зависят от того, на какой стадии заболевания началось лечение. На ранних стадиях возможность благоприятного исхода превышает 80% [5] . Однако многие пациенты обращаются к врачам тогда, когда заболевание уже серьезно сказывается на общем состоянии здоровья, когда пострадал не только желудок, но и лимфатическая система, а также близлежащие органы, что существенно затрудняет лечение. В частности, оперативное вмешательство не дает заметного результата, когда врачи вынуждены назначать симптоматическое, поддерживающее, лечение. Именно поэтому необходимо обращаться к специалистам при появлении первых тревожных симптомов, таких как потеря веса, расстройство аппетита, тошнота, наличие крови в кале и других.
Читайте также:

