Между хлором и калием в таблице менделеева
Отгадайте загадку:
Выше леса, выше гор Расстилается ковёр. Он всегда, всегда раскинут Над тобой и надо мной, То он серый, то он синий, То он ярко-голубой. Показать ответ>>
Выше человека, Ниже курицы. Показать ответ>>
Вышел месяц на балкон, там засеребрился. Кто остался на балконе, когда месяц скрылся? Показать ответ>>
Другие значения этого слова:
- "Ar" в периодической таблице
- "Недеятельный" среди газов
- "Сварочный" газ
- 18-й в менделеевском строю
- 18-й в химической таблице
- 18-я графа химической таблицы
- Ar, химический элемент, благородный газ
- в таблице он между хлором и калием
- в таблице он перед калием
- В таблице он после хлора.
- восемьнадцатый элемент
- вслед за хлором в таблице
- Газ в синеголубых лампах
- газ для заполнения ламп
- газ для сварки цветных металлов
- Газ из благородных
- Газ, дающий синеватое свечение в электрических лампах и осветительных трубках
- газ, соблюдающий нейтралитет
- двадцатая графа Менделеева
- двадцатый в таблице Менделеева
- двадцатый инертный газ
- его благородие газ
- идущий следом за хлором в таблице
- Инертный газ, используется при сварке алюминия
- Инертный газ, от которого "лампы горят синим пламенем
- какой газ замыкает третий период таблицы Менделеева?
- Какой химический элемент (атомный номер 18) обозначается символом Ar
- какой химический элемент можно получить, если к названию древнегреческого корабля добавить одну букву?
- между хлором и калием
- между хлором и калием в таблице
- менделеев его назначил двадцатым
- менделеев его назначил двадцатым в таблице
- Менделеев его определил двадцатым
- Мешанина из слова "онагр"
- Недеятельный" благородный газ
- один из инертных газов
- перед калием в таблице
- после хлора в таблице
- последователь хлора в таблице
- последыш хлора в таблице
- предтеча калия в таблице
- предшественник калия в таблице
- Преемник хлора в таблице
- Рекламный газ
- следом за хлором в таблице
- сосед хлора
- химический элемент с позывным Ar
- химический элемент, Ar
- Химический элемент, инертный газ без цвета и запаха, входящий в состав воздуха
- Химический элемент, являющийся благородным газом с атомной массой 40
- Элемент главной подгруппы восьмой группы, третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 18. Обозначается символом Ar. Третий по распространённости элемент в земной атмосфере
- Элемент, Ar
- этот инертный газ не вступает практически ни в какие химические реакции, за что и получил свое название
- №18 согласно Менделееву
Что за звёздочки сквозные На пальто и на платке, Все сквозные, вырезные, А возьмёшь — вода в руке.
Пеpвое лезвие бpеет чисто.
Втоpое -- еще чище.
. Двадцать четвеpтое полиpует челюсть.
В 1966 году на сигаретных пачках появляются предупреждения о вреде сигарет для здоровья.
Сканворды, кроссворды, судоку, кейворды онлайн
Хлор (лат. chlorum), cl, химический элемент vii группы периодической системы Менделеева, атомный номер 17, атомная масса 35,453; относится к семейству галогенов . При нормальных условиях (0°С, 0,1 Мн/м 2 или 1 кгс/см 2 ) жёлто-зелёный газ с резким раздражающим запахом. Природный Х. состоит из двух стабильных изотопов: 35 cl (75,77%) и 37 cl (24,23%). Искусственно получены радиоактивные изотопы с массовыми числами 32, 33, 34, 36, 38, 39, 40 и периодами полураспада ( t 1 /2 ) соответственно 0,31; 2,5; 1,56 сек ; 3 , 1 ? 10 5 лет; 37,3, 55,5 и 1,4 мин. 36 cl и 38 cl используются как изотопные индикаторы .
Историческая справка. Х. получен впервые в 1774 К. Шееле взаимодействием соляной кислоты с пиролюзитом mno 2 . Однако только в 1810 Г. Дэви установил, что хлор — элемент и назвал его chlorine (от греч. chlor o s — жёлто-зелёный). В 1813 Ж. Л. Гей-Люссак предложил для этого элемента название Х.
Распространение в природе. Х. встречается в природе только в виде соединений. Среднее содержание Х. в земной коре (кларк) 1,7 ? 10 -2 % по массе, в кислых изверженных породах — гранитах и др. 2,4 ? 10 -2 , в основных и ультраосновных 5 ? 10 -3 . Основную роль в истории Х. в земной коре играет водная миграция. В виде иона cl он содержится в Мировом океане (1,93%), подземных рассолах и соляных озёрах. Число собственных минералов (преимущественно хлоридов природных ) 97, главный из них галит naci. Известны также крупные месторождения хлоридов калия и магния и смешанных хлоридов: сильвин kcl, сильвинит (na, k) ci, карналлит kci ? mgcl 2 ? 6h 2 o, каинит kci ? mgso 4 ? 3h 2 o, бишофит mgci 2 ? 6h 2 o. В истории Земли большое значение имело поступление содержащегося в вулканических газах hcl в верхние части земной коры.
Физические и химические свойства. Х. имеет t kип —34,05°С, t nл — 101°С. Плотность газообразного Х. при нормальных условиях 3,214 г/л ; насыщенного пара при 0°С 12,21 г/л ; жидкого Х. при температуре кипения 1,557 г/см 3 ; твёрдого Х. при — 102°c 1,9 г/см 3 . Давление насыщенных паров Х. при 0°С 0,369; при 25°c 0,772; при 100°c 3,814 Мн/м 2 или соответственно 3,69; 7,72; 38,14 кгс/см 2 . Теплота плавления 90,3 кдж/кг (21,5 кал/г ); теплота испарения 288 кдж/кг (68,8 кал/г ); теплоёмкость газа при постоянном давлении 0,48 кдж/ ( кг ? К ) [0,11 кал/ ( г ? ° С)] . Критические константы Х.: температура 144°c, давление 7,72 Мн/м 2 (77,2 кгс/см 2 ) , плотность 573 г/л , удельный объём 1,745 ? 10 -3 л/г . Растворимость (в г/л ) Х. при парциальном давлении 0,1 Мн/м 2 , или 1 кгс/см 2 , в воде 14,8 (0°С), 5,8 (30°c), 2,8 (70°c); в растворе 300 г/л naci 1,42 (30°c), 0,64 (70°c). Ниже 9,6°С в водных растворах образуются гидраты Х. переменного состава cl ? n h 2 o (где n = 6 ? 8); это жёлтые кристаллы кубической сингонии, разлагающиеся при повышении температуры на Х. и воду. Х. хорошо растворяется в ticl 4 , sic1 4 , sncl 4 и некоторых органических растворителях (особенно в гексане c 6 h 14 и четырёххлористом углероде ccl 4 ). Молекула Х. двухатомна (cl 2 ). Степень термической диссоциации cl 2 + 243 кдж u 2cl при 1000 К равна 2,07 ? 10 -40 %, при 2500 К 0,909%. Внешняя электронная конфигурация атома cl 3 s 2 3 p 5 . В соответствии с этим Х. в соединениях проявляет степени окисления —1, +1, +3, +4, +5, +6 и +7. Ковалентный радиус атома 0,99 å, ионный радиус cl - 1,82 å, сродство атома Х. к электрону 3,65 эв, энергия ионизации 12,97 эв .
Химически Х. очень активен, непосредственно соединяется почти со всеми металлами (с некоторыми только в присутствии влаги или при нагревании) и с неметаллами (кроме углерода, азота, кислорода, инертных газов), образуя соответствующие хлориды , вступает в реакцию со многими соединениями, замещает водород в предельных углеводородах и присоединяется к ненасыщенным соединениям. Х. вытесняет бром и йод из их соединений с водородом и металлами; из соединений Х. с этими элементами он вытесняется фтором. Щелочные металлы в присутствии следов влаги взаимодействуют с Х. с воспламенением, большинство металлов реагирует с сухим Х. только при нагревании. Сталь, а также некоторые металлы стойки в атмосфере сухого Х. в условиях невысоких температур, поэтому их используют для изготовления аппаратуры и хранилищ для сухого Х. Фосфор воспламеняется в атмосфере Х., образуя pcl 3 , а при дальнейшем хлорировании — pcl 5 ; сера с Х. при нагревании даёт s 2 cl 2 , scl 2 и др. s n cl m . Мышьяк, сурьма, висмут, стронций, теллур энергично взаимодействуют с Х. Смесь Х. с водородом горит бесцветным или жёлто-зелёным пламенем с образованием хлористого водорода (это цепная реакция),
Максимальная температура водородно-хлорного пламени 2200°c. Смеси Х. с водородом, содержащие от 5,8 до 88,5% h 2 , взрывоопасны.
С кислородом Х. образует окислы: cl 2 o, clo 2 , cl 2 o 6 , cl 2 o 7 , cl 2 o 8, а также гипохлориты (соли хлорноватистой кислоты ) , хлориты , хлораты и перхлораты. Все кислородные соединения хлора образуют взрывоопасные смеси с легко окисляющимися веществами. Окислы Х. малостойки и могут самопроизвольно взрываться, гипохлориты при хранении медленно разлагаются, хлораты и перхлораты могут взрываться под влиянием инициаторов.
Х. в воде гидролизуется, образуя хлорноватистую и соляную кислоты: cl 2 + h 2 o u hclo + hcl. При хлорировании водных растворов щелочей на холоду образуются гипохлориты и хлориды: 2naoh + cl 2 = nacio + naci + h 2 o, а при нагревании — хлораты. Хлорированием сухой гидроокиси кальция получают хлорную известь .
При взаимодействии аммиака с Х. образуется трёххлористый азот. При хлорировании органических соединений Х. либо замещает водород: r—h + ci 2 = rcl + hci, либо присоединяется по кратным связям образуя различные хлорсодержащие органические соединения.
Х. образует с др. галогенами межгалогенные соединения . Фториды clf, clf 3 , clf 5 очень реакционноспособны; например, в атмосфере clp 3 стеклянная вата самовоспламеняется. Известны соединения хлора с кислородом и фтором — оксифториды Х.: clo 3 f, clo 2 f 3 , clof, clof 3 и перхлорат фтора fclo 4 .
Получение. Х. начали производить в промышленности в 1785 взаимодействием соляной кислоты с двуокисью марганца или пиролюзитом. В 1867 английский химик Г. Дикон разработал способ получения Х. окислением hcl кислородом воздуха в присутствии катализатора. С конца 19 — начала 20 вв. Х. получают электролизом водных растворов хлоридов щелочных металлов. По этим методам в 70-х гг. 20 в. производится 90—95% Х. в мире. Небольшие количества Х. получаются попутно при производстве магния, кальция, натрия и лития электролизом расплавленных хлоридов. В 1975 мировое производство Х. составляло около 25 млн. т. Применяются два основных метода электролиза водных растворов naci: 1) в электролизёрах с твёрдым катодом и пористой фильтрующей диафрагмой; 2) в электролизёрах с ртутным катодом. По обоим методам на графитовом или окисном титано-рутениевом аноде выделяется газообразный Х. По первому методу на катоде выделяется водород и образуется раствор naoh и nacl, из которого последующей переработкой выделяют товарную каустическую соду. По второму методу на катоде образуется амальгама натрия, при её разложении чистой водой в отдельном аппарате получаются раствор naoh, водород и чистая ртуть, которая вновь идёт в производство. Оба метода дают на 1 т Х. 1,125 т naoh.
Электролиз с диафрагмой требует меньших капиталовложений для организации производства Х., даёт более дешёвый naoh. Метод с ртутным катодом позволяет получать очень чистый naoh, но потери ртути загрязняют окружающую среду. В 1970 по методу с ртутным катодом производилось 62,2% мировой выработки Х., с твёрдым катодом 33,6% и пр. способами 4,2%. После 1970 начали применять электролиз с твёрдым катодом и ионообменной мембраной, позволяющий получать чистый naoh без использования ртути.
Применение. Одной из важных отраслей химической промышленности является хлорная промышленность. Основные количества Х. перерабатываются на месте его производства в хлорсодержащие соединения. Хранят и перевозят Х. в жидком виде в баллонах, бочках, ж.-д. цистернах или в специально оборудованных судах. Для индустриальных стран характерно следующее примерное потребление Х.: на производство хлорсодержащих органических соединений — 60—75%; неорганических соединений, содержащих Х., — 10—20%; на отбелку целлюлозы и тканей — 5—15%; на санитарные нужды и хлорирование воды — 2—6% от общей выработки.
Х. применяется также для хлорирования некоторых руд с целью извлечения титана, ниобия, циркония и др.
Х. в организме. Х. — один из биогенных элементов , постоянный компонент тканей растений и животных. Содержание Х. в растениях (много Х. в галофитах ) — от тысячных долей процента до целых процентов, у животных — десятые и сотые доли процента. Суточная потребность взрослого человека в Х. (2—4 г ) покрывается за счёт пищевых продуктов. С пищей Х. поступает обычно в избытке в виде хлорида натрия и хлорида калия. Особенно богаты Х. хлеб, мясные и молочные продукты. В организме животных Х. — основное осмотически активное вещество плазмы крови, лимфы, спинномозговой жидкости и некоторых тканей. Играет роль в водно-солевом обмене , способствуя удержанию тканями воды. Регуляция кислотно-щелочного равновесия в тканях осуществляется наряду с др. процессами путём изменения в распределении Х. между кровью и др. тканями. Х. участвует в энергетическом обмене у растений, активируя как окислительное фосфорилирование , так и фотофосфорилирование. Х. положительно влияет на поглощение корнями кислорода. Х. необходим для образования кислорода в процессе фотосинтеза изолированными хлоропластами . В состав большинства питательных сред для искусственного культивирования растений Х. не входит. Возможно, для развития растений достаточны весьма малые концентрации Х.
Отравления Х. возможны в химической, целлюлозно-бумажной, текстильной, фармацевтической промышленности и др. Х. раздражает слизистые оболочки глаз и дыхательных путей. К первичным воспалительным изменениям обычно присоединяется вторичная инфекция. Острое отравление развивается почти немедленно. При вдыхании средних и низких концентраций Х. отмечаются стеснение и боль в груди, сухой кашель, учащённое дыхание, резь в глазах, слезотечение, повышение содержания лейкоцитов в крови, температуры тела и т.п. Возможны бронхопневмония, токсический отёк лёгких, депрессивные состояния, судороги. В лёгких случаях выздоровление наступает через 3—7 сут. Как отдалённые последствия наблюдаются катары верхних дыхательных путей, рецидивирующий бронхит, пневмосклероз и др.; возможна активизация туберкулёза лёгких. При длительном вдыхании небольших концентраций Х. наблюдаются аналогичные, но медленно развивающиеся формы заболевания. Профилактика отравлений: герметизация производственного оборудования, эффективная вентиляция, при необходимости использование противогаза. Предельно допустимая концентрация Х. в воздухе производственных помещений 1 мг/м 3 . Производство Х., хлорной извести и др. хлорсодержащих соединений относится к производствам с вредными условиями труда, где по сов. законодательству ограничено применение труда женщин и несовершеннолетних.
Лит.: Якименко Л. М., Производство хлора, каустической соды и неорганических хлорпродуктов, М., 1974; Некрасов Б. В., Основы общей химии, 3 изд., [т.] 1, М., 1973; Вредные вещества в промышленности, под ред. Н. В, Лазарева, 6 изд., т. 2, Л., 1971; comprehensive inorganic chemistry, ed. j. c. bailar [a. o.], v. 1—5, oxf. — [a. o.], 1973.
Хлор в таблице менделеева занимает 17 место, в 3 периоде.
| Символ | Cl |
| Номер | 17 |
| Атомный вес | 35.4460000 |
| Латинское название | Chlorum |
| Русское название | Хлор |
Электронная схема хлора
Cl: 1s 2 2s 2 2p 6 3s 2 3p 5
Короткая запись:
Cl: [Ne]3s 2 3p 5
Одинаковую электронную конфигурацию имеют атом хлора и P -2 , S -1
Порядок заполнения оболочек атома хлора (Cl) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ - до 6, на ‘d’ - до 10 и на ‘f’ до 14
Хлор имеет 17 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
5 электронов на 3p-подуровне
Степень окисления хлора
Атомы хлора в соединениях имеют степени окисления 6, 5, 4, 3, 2, 1, 0, -1, -2.
Степень окисления - это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
Ионы хлора
Валентность Cl
Атомы хлора в соединениях проявляют валентность VI, V, IV, III, II, I.
Валентность хлора характеризует способность атома Cl к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа Cl
Квантовые числа определяются последним электроном в конфигурации, для атома Cl эти числа имеют значение N = 3, L = 1, Ml = 0, Ms = -½
Видео заполнения электронной конфигурации (gif):
Результат: 
Энергия ионизации
Чем ближе электрон к центру атома - тем больше энергии необходимо, что бы его оторвать. Энергия, затрачиваемая на отрыв электрона от атома называется энергией ионизации и обозначается Eo. Если не указано иное, то энергия ионизации - это энергия отрыва первого электрона, также существуют энергии ионизации для каждого последующего электрона.
Перейти к другим элементам таблицы менделеева
Серебристо-белый мягкий металл 
39,0983 а. е. м. (г/моль)
418,5 (4,34) кДж/моль (эВ)
| K | 19 |
| 39,0983 | |
| 4s 1 | |
| Калий | |
Калий — элемент главной подгруппы первой группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 19. Обозначается символом K (лат. Kalium). Простое вещество калий (CAS-номер: 7440-09-7) — мягкий щелочной металл серебристо-белого цвета. В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах. Он очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь. Во многих отношениях химические свойства калия очень близки к натрию, но с точки зрения биологической функции и использования их клетками живых организмов они все же отличаются. История и происхождение названия калий
Калий (точнее, его соединения) использовался с давних времён. Так, производство поташа (который применялся как моющее средство) существовало уже в XI веке. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор (щёлок) после фильтрования выпаривали. Сухой остаток, помимо карбоната калия, содержал сульфат калия K2SO4, соду и хлорид калия KCl.
Присутствие в природе калия
В свободном состоянии не встречается. Калий входит в состав сильвинита KCl·NaCl, карналлита KCl·MgCl2·6H2O, каинита KCl·MgSO4·6H2O, а также присутствует в золе некоторых растений в виде карбоната K2CO3 (поташ). Калий входит в состав всех клеток (см. ниже раздел Биологическая роль).
Калий — получение калия
Калий, как и другие щелочные металлы, получают электролизом расплавленных хлоридов или щелочей. Так как хлориды имеют более высокую температуру плавления (600—650 °C), то чаще проводят электролиз расправленных щелочей с добавкой к ним соды или поташа (до 12 %). При электролизе расплавленных хлоридов на катоде выделяется расплавленный калий, а на аноде — хлор:
K + + e − → K
2Cl − − 2e − → Cl2
При электролизе щелочей на катоде также выделяется расплавленный калий, а на аноде — кислород:
4OH − − 4e − → 2H2O + O2
Вода из расплава быстро испаряется. Чтобы калий не взаимодействовал с хлором или кислородом, катод изготовляют из меди и над ним помещают медный цилиндр. Образовавшийся калий в расплавленном виде собирается в цилиндре. Анод изготовляют также в виде цилиндра из никеля (при электролизе щелочей) либо из графита (при электролизе хлоридов).
Физические свойства калия
Калий — серебристое вещество с характерным блеском на свежеобразованной поверхности. Очень лёгок и легкоплавок. Относительно хорошо растворяется в ртути, образуя амальгамы. Будучи внесённым в пламя горелки калий (а также его соединения) окрашивает пламя в характерный розово-фиолетовый цвет.
Химические свойства калия
Калий, как и другие щелочные металлы, проявляет типичные металлические свойства и очень химически активен, легко отдаёт электроны.
Является сильным восстановителем. Он настолько активно соединяется с кислородом, что образуется не оксид, а супероксид калия KO2 (или K2O4). При нагревании в атмосфере водорода образуется гидрид калия KH. Хорошо взаимодействует со всеми неметаллами, образуя галогениды, сульфиды, нитриды, фосфиды и т. д., а также со сложными веществами, такими как вода (реакция проходит со взрывом), различные оксиды и соли. В этом случае они восстанавливают другие металлы до свободного состояния.
Калий хранят под слоем керосина.
При взаимодействии калия с кислородом воздуха образуется не оксид, а пероксид и супероксид:
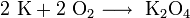
Оксид калия может быть получен при нагревании металла до температуры не выше 180 °C в среде, содержащей очень мало кислорода, или при нагревании смеси супероксида калия с металлическим калием:
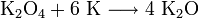
Оксиды калия обладают ярко выраженными основными свойствами, бурно реагируют с водой, кислотами и кислотными оксидами. Практического значения они не имеют. Пероксиды представляют собой желтовато-белые порошки, которые, хорошо растворяясь в воде, образуют щёлочи и пероксид водорода:
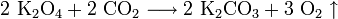
Свойство обменивать углекислый газ на кислород используется в изолирующих противогазах и на подводных лодках. В качестве поглотителя используют эквимолярную смесь супероксида калия и пероксида натрия. Если смесь не эквимолярна, то в случае избытка пероксида натрия поглотится больше газа, чем выделится (при поглощении двух объёмов CO2 выделяется один объём O2), и давление в замкнутом пространстве упадёт, а в случае избытка супероксида калия (при поглощении двух объёмов CO2 выделяется три объёма O2) выделяется больше газа, чем поглотится, и давление повысится.
В случае эквимолярной смеси (Na2O2:K2O4 = 1:1) объёмы поглощаемого и выделяемого газов будут равны (при поглощении четырёх объёмов CO2 выделяется четыре объёма O2).
Пероксиды являются сильными окислителями, поэтому их применяют для отбеливания тканей в текстильной промышленности.
Получают пероксиды прокаливанием металлов на воздухе, освобождённом от углекислого газа.
Гидроксид калия (или едкое кали) представляет собой твёрдые белые непрозрачные, очень гигроскопичные кристаллы, плавящиеся при температуре 360 °C. Гидроксид калия относится к щелочам. Он хорошо растворяется в воде с выделением большого количества тепла. Растворимость едкого калия при 20 °C в 100 г воды составляет 112 г.
Важным химическим продуктом с глубокой древности являлась зола. Мылкий раствор, образующийся при кипячении золы с водой (щёлок), был первым моющим средством, созданным человеком. В Средние века люди научились выделять из золы соединения, которые и делали ее раствор мылким, — соду и поташ (карбонаты натрия и калия). Долгое время названия этих двух солей означали лишь разные виды золы: поташом или кали называли золу, остающуюся после сгорания древесины, соломы, камыша и папоротника (эта зола богата калийными солями), а содой или натроном – золу других травянистых растений, в которых преобладали соли натрия.
На Руси производство поташа существовало уже в XI в. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор после фильтрования выпаривали. Сухой остаток кроме карбоната калия содержал также и другие примеси в виде калийных солей.
В отличие от поташа, сода встречается в природе, например в водах натронных озёр в Египте. Природную соду древние египтяне использовали для бальзамирования, отбеливания холста, при изготовлении красящих веществ и при варке пищи. Плиний Старший писал, что в дельте Нила соду выделяли из речной воды. Сода, получаемая из растительной золы, также содержала большое количество других солей. Она поступала в продажу в виде крупных кусков, из-за примеси угля окрашенных в серый или черный цвет.
Химическое различие между содой и поташом окончательно установил в 1758 г. немецкий химик А. С. Маргграф. А в 1807 г. Г. Дэви провёл электролиз расплавов щелочей – гидроксида натрия и гидроксида калия, выделив металлические натрий и калий.
Вследствие очень легкой окисляемости щелочные металлы встречаются в природе исключительно в виде соединений. Натрий и калий принадлежат к распространенным элементам: содержание каждого из них в земной коре равно приблизительно 2%. Оба металла входят в состав различных минералов и горных пород силикатного типа. Хлорид натрия содержится в морской воде, а также образует мощные отложения каменной соли во многих местах земного шара. В верхних слоях этих отложений иногда содержатся довольно значительные количества калия, преимущественно в виде хлорида или двойных солей с натрием и магнием. Однако большие скопления солей калия, имеющие промышленное значение встречаются редко. Наиболее важными из них являются соликамские месторождения Пермского края, стассфуртские в Германии и эльзасские – во Франции. Залежи натриевой селитры находятся в Чили. В воде многих озер содержится сода. Наконец, огромные количества сульфата натрия находятся в заливе Кара-Богаз-Гол Каспийского моря, где эта соль и в зимние месяцы осаждается толстым слоем на дне.

Добыча соли
Среди соединений натрия важная роль принадлежит карбонату, или соде. Безводный средний карбонат натрия Na2CO3 называют кальцинированной содой, десятиводный кристаллогидрат Na2CO3∙10H2O – стиральной содой, а гидрокарбонат NaHCO3 – питьевой или пищевой содой.
Растворы среднего карбоната имеют сильнощелочную реакцию среды, их используют при стирке белья и при обработке шерсти. Кроме того, кальцинированная сода находит широкое применение в производстве мыла, стекла, сульфита натрия, органических красителей. Растворы гидрокарбоната имеют слабощелочную реакцию среды, поэтому питьевую соду используют в медицине, а также при приготовлении пищи.
Значительно меньше, чем натрий и калий, распространены литий, рубидий и цезий. Чаще других встречается литий, но содержащие его минералы редко образуют большие скопления. Рубидий и цезий содержатся в небольших количествах в некоторых литиевых минералах.
Все известные изотопы франция радиоактивны и быстро распадаются (период полураспада изотопа 223 Fr составляет 21,8 мин.). Первым был открыт изотоп 223 Fr французской исследовательницей М.Пере в 1939 г.В честь своей родины она назвала его францием. Он образуется при распаде актиния и в ничтожном количестве встречается в природе. В настоящее время небольшие количества франция получают искусственно.
Во внешнем электронном слое атомы щелочных металлов имеют по одному электрону. Во втором внешнем электронном слое у атома лития содержатся два электрона, а у атомов остальных щелочных металлов – по восемь электронов. Имея во внешнем электронном слое только по одному электрону, находящемуся на сравнительно большом удалении от ядра, атомы этих элементов довольно легко отдают этот электрон. Легкость отдачи внешних электронов характеризует рассматриваемые элементы как наиболее типичные представители металлов: металлические свойства выражены у щелочных металлов особенно резко.
- Взаимодействие щелочных металлов с неметаллами
а) взаимодействие с кислородом
Обратите внимание, что только литий окисляется кислородом до нормального оксида:
Основным продуктом окисления натрия является пероксид:
а калий, рубидий и цезий сгорают в кислороде с образованием супероксидов (надпероксидов):
б) взаимодействие с галогенами (продукты взаимодействия галогениды):
в) взаимодействие с серой и фосфором (продукты взаимодействия сульфиды и фосфиды):
г) взаимодействие с водородом (продукты взаимодействия гидриды):
Гидриды щелочных металлов разлагаются водой с образованием щелочи и свободного водорода:
д) взаимодействие с азотом и углеродом
Эти реакции наиболее характерны для лития, который с азотом взаимодействует даже при обычной температуре:
- Взаимодействие щелочных металлов со сложными веществами
а) взаимодействие с водой
Возможность взаимодействия щелочных металлов с водой обусловлена тем, что они находятся в начале ряда напряжений металлов, т.е. обладают очень высокой восстановительной активностью и могут окисляться даже ионами водорода из воды.

Взаимодействие натрия с водой
В результате реакций образуются растворы щелочей и выделяется водород, который иногда самовоспламеняется:
б) взаимодействие с разбавленными кислотами
2Na + 2HCl = 2NaCl + H2↑
Концентрированную серную кислоту щелочные металлы восстанавливают до сероводорода:
Соли щелочных металлов окрашивают пламя горелки в различные цвета:
Это свойство используется для качественного анализа, т.е. для обнаружения этих катионов.

Цвет пламени ионов щелочных металлов
В промышленности натрий получают электролизом расплава смеси хлоридов натрия и кальция (она плавится при более низкой температуре, чем чистый хлорид натрия). Интересно, что первым из расплава выделяется не кальций, а более активный натрий, так как ион Na + в расплаве легче, чем Са 2+ , принимает электроны. Процесс проводят в стальных электролизёрах при 580 ̊ С. Образующийся жидкий натрий всплывает на поверхность расплава и собирается в специальный приёмник.

Схема электролиза для получения натрия
Ежегодно в мире производится около 200 тыс. тонн металлического натрия, который применяется на атомных электростанциях и в авиадвигателях в качестве теплоносителя, в металлургии – как восстановитель, в лабораторной практике – для абсолютирования (обезвоживания) растворителей.
Литий, как и натрий получают электролизом расплавов, а остальные щелочные металлы вытесняют из расплавленных солей металлическим натрием и кальцием. Например, натрий при 850 ̊ С легко вытесняет более активный калий из расплава его хлорида: KCl + Na → NaCl + K↑
Это объясняется тем, что калий (tкип = 762 ̊ С), более летучий, чем натрий (tкип = 883 ̊ С), испаряется, и в соответствии с принципом Ле-Шателье равновесие реакции смещается вправо. Аналогично из хлорида цезия можно получить цезий: Ca + 2CsCl = 2Cs↑ + CaCl2
Натрий представляет собой серебристо-белый металл. Он настолько мягок, что легко режется ножом. Вследствие легкой окисляемости на воздухе его хранят под слоем керосина.
В организме человека натрий в виде его растворимых солей, содержится в основном во внеклеточных жидкостях – плазме крови, лимфе, пищеварительных соках. Осмотическое давление плазмы крови поддерживается на необходимом уровне прежде всего за счет хлорида натрия.
Значительная потеря ионов натрия (они выводятся из организма с мочой и потом) неблагоприятно сказываются на здоровье человека. Поэтому врачи рекомендуют людям есть больше соленого. Однако и избыточное содержание их в пище вызывает негативную реакцию организма, например повышение артериального давления.
Гидроксиды щелочных металлов называют едкими щелочами. Они представляют собой белые кристаллические вещества, устойчивые к нагреванию, хорошо растворимые в воде (за исключением LiOH), а также в спирте.

Гидроксид калия
Другим способом получения едкого натра служило взаимодействие соды с известью Ca(OH)2 (каустификация соды): Ca(OH)2 + Na2CO3 ⇄ CaCO3 + 2NaOH.
В наше время едкие щелочи получают электролизом растворов солей, например хлоридов. При этом наряду с щелочью образуются другие важные вещества – водород и хлор.
Гидроксиды натрия и калия применяют для очистки нефти и масел, в производстве бумаги, моющих средств, искусственных волокон. Благодаря способности активно поглощать влагу из воздуха (гигроскопичности) NaOH и KOH используются в лабораториях как осушители.
Перекись(или пероксид) натрия образуется при сжигании натрия на воздухе или в кислороде. В заводских условиях перекись натрия готовят нагреванием расплавленного натрия в токе воздуха, освобожденного от СО2. Получающийся продукт имеет слабо-желтоватую окраску, обусловленную примесью соединения NaO2, называемого надперекисью натрия.
Перекись натрия – очень сильный окислитель. Многие органические вещества при соприкосновении с ней воспламеняются.
При осторожном растворении перекиси натрия в холодной воде получается раствор, содержащий гидроксид натрия и перекись водорода. Если нагревать полученный раствор, то вследствие разложения перекиси водорода из него выделяется кислород.
При действии на перекись натрия разбавленных кислот также получается перекись водорода, например: Na2O2 + H2SO4 = H2O2 + Na2SO4
Перекись натрия применяется для отбелки тканей, шерсти, шелка и т.п. Важное значение имеет реакция взаимодействия перекиси натрия с углекислым газом:
На этой реакции основано применение перекиси натрия для регенерации воздуха в изолированных помещениях.
Он может быть получен при пропускании над натрием, нагретым не выше 180̊ С, умеренного количества кислорода или нагреванием перекиси натрия с металлическим натрием: Na2O2 + 2Na = 2Na2O
Оксид натрия бурно реагирует с водой с образованием гидроксида натрия и выделением большого количества теплоты:
По внешнему виду, а также по физическим и химическим свойствам калий очень похож на натрий, но обладает еще большей активностью. Подобно натрию, он имеет серебристо- белый цвет, быстро окисляется на воздухе и бурно реагирует с водой с выделением водорода.
Соли калия очень сходны с солями натрия, но обычно выделяются из растворов без кристаллизационной воды.
Калий принадлежит к числу элементов, необходимых в значительном количестве для питания растений. Хотя в почве находится довольно много солей калия, но и уносится его с некоторыми культурными растениями также очень много. Особенно много калия уносят лен и табак.
Калий отлагается в растениях главным образом в стеблях, поэтому удобрение земли навозом, содержащим солому, отчасти пополняет убыль калия. Но так как стебли перечисленных выше растений используются для промышленных целей, то в конце концов большая часть калия уходит из почвы, и для пополнения его убыли необходимо вносить калийные удобрения.
Источником получения калийных удобрений служат естественные отложения калийных солей. В России такие отложения находятся в районе Соликамска. Пласты соли состоящие главным образом из минералов карналлита KCl∙MgCl2∙6H2O и сильвинита KCl∙NaCl, залегают на большой площади между верховьями Камы и предгорьями Урала.

Соликамская шахта по добыче соли
Как и натрий, калий содержится во всех тканях организма человека. Но, в отличие от натрия, калий в преобладающем количестве находится внутри клеток. Ион калия играет важную роль в некоторых физиологических и биохимических процессах. Определенная концентрация калия в крови необходима для нормальной работы сердца. В организм калий поступает главным образом с растительной пищей; суточная потребность человека в нем составляет 2-3 г.
В свободном состоянии литий – серебристо-белый металл, мягкий, хотя и жёстче остальных щелочных металлов, а также не такой легкоплавкий (tпл = 181̊ С). Литий настолько лёгок, что не тонет даже в керосине.

Литий
По сравнению с другими щелочными металлами литий обладает рядом особенностей. Так, при сгорании на воздухе он дает оксид Li2O, напрямую взаимодействует с азотом, образуя нитрид Li3N, и с углеродом, образуя карбид Li2C2. Некоторые соли лития (карбонат, фторид) малорастворимы в воде, а карбонат и гидроксид лития разлагаются при сильном нагреве с образованием оксида. Все эти свойства говорят о том, что химия лития близка химии магния.
Добро пожаловать на сайт! Здесь вы найдете самую полную информацию об истории химии и ее развитии как науки, а также интересные статьи о всех химических элементах известных на сегодняшний день и о соединениях, которые они образуют.
Читайте также:

