Метастазирование рака молочной железы диссертации
Аннотация научной статьи по клинической медицине, автор научной работы — Вишневская Я. В., Ермилова В. Д., Савелов Н. А., Нечушкин М. И., Триголосов А. В.
Lobular infiltrating carcinoma (LIC) is the second most common histological form of breast cancer. Metastases in the lymph nodes and distant organs are most important predictors. The purpose of the study was to investigate the specific features of LIC and the number of metastases into regional lymph nodes. Surgical tumor removal revealed 60% of metastasis into the regional lymph nodes. Distant metastases were observed in 1% on primary admission and in 10% at 5-year follow-up. There are extremely rare cases of secondary involvement of the uterus and its appendages, omentum, gastrointestinal tract, and exocrine glands; in this case, it is necessary to specify the presence of a primary breast tumor and its histogenesis by an immunohistological study.
Похожие темы научных работ по клинической медицине , автор научной работы — Вишневская Я. В., Ермилова В. Д., Савелов Н. А., Нечушкин М. И., Триголосов А. В.
LOBULAR INFILTRATING CARCINOMA OF THE BREAST: SPECIFIC FEATURES OF DISSEMINATION, HISTOLOGICAL AND IMMUNOHISTOCHEMICAL CHARACTERISTICS
Lobular infiltrating carcinoma (LIC) is the second most common histological form of breast cancer. Metastases in the lymph nodes and distant organs are most important predictors. The purpose of the study was to investigate the specific features of LIC and the number of metastases into regional lymph nodes. Surgical tumor removal revealed 60% of metastasis into the regional lymph nodes. Distant metastases were observed in 1% on primary admission and in 10% at 5-year follow-up. There are extremely rare cases of secondary involvement of the uterus and its appendages, omentum, gastrointestinal tract, and exocrine glands; in this case, it is necessary to specify the presence of a primary breast tumor and its histogenesis by an immunohistological study.
ОСОБЕННОСТИ МЕТАСТАЗИРОВАНИЯ ДОЛЬКОВОГО ИНФИЛЬТРАТИВНОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ, ГИСТОЛОГИЧЕСКАЯ И ИММУНОГИСТОХИМИЧЕСКАЯ ХАРАКТЕРИСТИКА
Я.В. Вишневская, В.Д. Ермилова, Н.А. Савелов, М.И. Нечушкин, А.В. Триголосов
РОНЦ им. Н.Н.Блохина РАМН
LOBULAR INFILTRATING CARCINOMA OF THE BREAST: SPECIFIC FEATURES OF DISSEMINATION, HISTOLOGICAL
AND IMMUNOHISTOCHEMICAL CHARACTERISTICS Ya.V. Vishnevskaya, V.D. Yermilova, N.A. Savelov, M.I. Nechushkin, A.V. Trigolosov N.N. Blokhin Russian Cancer Research Center, Russian Academy of Medical Sciences
Lobular infiltrating carcinoma (LIC) is the second most common histological form of breast cancer. Metastases in the lymph nodes and distant organs are most important predictors.
The purpose of the study was to investigate the specific features of LIC and the number of metastases into regional lymph nodes. Surgical tumor removal revealed 60% of metastasis into the regional lymph nodes. Distant metastases were observed in 1% on primary admission and in 10% at 5-yearfollow-up. There are extremely rare cases of secondary involvement of the uterus and its appendages, omentum, gastrointestinal tract, and exocrine glands; in this case, it is necessary to specify the presence of a primary breast tumor and its histogenesis by an immunohistological study.
Второй по частоте гистологической формой рака молочной железы (РМЖ) является дольковый инфильтративный рак (ДИР) [1, 2]; в последние годы количество зарегистрированных случаев ДИР значительно увеличилось. Иногда течение ДИР отличается от такового при других вариантах карцином молочной железы, и в первую очередь от протокового инфильтративного рака (ПИР). По данным J. Dixon и соавт. [9], ДИР при всех вариантах имеет более благоприятный прогноз, чем ПИР. В связи с этим представлялось интересным изучить факторы, влияющие на прогноз данного заболевания.
Один из наиболее важных признаков, определяющих стадию болезни и прогрессирование процесса, — наличие метастазов в лимфатических узлах (ЛУ) и отдаленных вторичных очагов во внутренних органах [15].
Метастазирует ДИР наиболее часто лимфогенным путем в регионарные подмышечные, подключичные и парастернальные ЛУ. Отдаленными гематогенными метастазами чаще поражены кости с возникновением патологического перелома, легкие и плевра, печень [4], костный мозг [6]. Вторичное поражение головного мозга расценивается как карци-номатозный менингит в виде диффузной лептоме-нингиальной инфильтрации [12, 19]. Встречаются метастазы в позвоночнике со сдавлением структур спинного мозга, развитием нижней параплегии и нарушением функции тазовых органов [17]. Интрааб-доминальные метастазы имеют склонность к вовлечению серозных оболочек [12], забрюшинного пространства и яичников [10]. Диффузный рост опухоли в матке и яичниках клинически и морфологически напоминает метастазы рака желудка и в ряде случаев неотличим от опухоли Крукенберга [12—14, 20]. Крайне редко при ДИР молочной железы встречается изолированное метастатическое поражение желу-
дочно-кишечного тракта (ЖКТ). В литературе описано 31 подобное наблюдение, в том числе случай метастатического поражения желудка через 30 лет после радикальной мастэктомии [16].
Сложности дифференциальной диагностики метастазов ДИР в костном мозге связаны с тем, что изолированные опухолевые клетки рака могут быть похожими на элементы гемопоэза и выявляются с помощью иммуноморфологического исследования [5, 6].
D. DiCostanzo и соавт. [7] не обнаружили различий в метастазировании при классическом ДИР и различных его вариантах (тубулолобулярном, альвеолярном, солидном, смешанном).
Целью нашего исследования были изучение особенностей метастазирования ДИР и частоты метастазов в ЛУ регионарных зон (в первую очередь менее изученных — парастернальных), а также определение органов, являющихся мишенями при отдаленных метастазах, и частоты их поражения, включая редкие случаи вторичного поражения некоторых органов ДИР. Иногда выявить метастазы ДИР оказывалось сложно и требовалось применение иммуноги-стохимического (ИГХ) исследования для верификации раковых клеток. Кроме того, нашей целью была разработка ИГХ-признаков в случаях необходимости дифференциальной диагностики между метастазами ДИР и первичной опухолью пораженного органа.
Особенности регионарного и отдаленного ме-тастазирования ДИР изучены нами на материале, полученном при оперативном лечении 257 больных в разных стадиях процесса. Выживаемость пациенток прослежена в течение 5 лет. Оперативное лечение проводилось в объеме мастэктомии или радикальной секторальной резекции с удалением регионарной клетчатки и одномоментно — парастернальных ЛУ из первого—четвертого межреберия с помощью видеоторакоскопической парастернальной
ИЗ ПРАКТИКИ МАММОЛОГИЯ ’2006
ИЗ ПРАКТИКИ МАММОЛОГИЯ ’2006
Учитывали возраст больных, размеры и локализацию опухолевого узла, стадию процесса (по Международной классификации TNM), сопоставляли поражение парастернального и подмышечного лимфатических коллекторов, а также прослеживали наличие прогрессирования заболевания за 5-летний период.
Морфологическому исследованию подвергался операционный материал, включавший молочную железу, блок аксиллярной клетчатки, материал из парастернального лимфатического коллектора, который был удален моноблочно из первого—четверного межреберия и интраоперационно маркирован по межреберьям с целью детализации гистологических изменений.
В исследование были также включены 3 пациентки, находившиеся в РОНЦ РАМН по поводу метастазов ДИР в матку и придатки, 2 больные с метастатическим поражением ЖКТ, 1 — с вовлечением в процесс околоушной слюнной железы и 1 — с карциномой simplex желудка при наличии в анамнезе ДИР (в последнем случае проводилась дифференциация между первичным раком желудка и вторичным поражением ДИР).
У ряда больных для выявления микрометастазов, уточнения диагноза и для дифференциальной диагностики ДИР и других нозологических форм проводилось ИГХ-исследование с использованием широкого спектра антител, из которых в ДИР экспрессировались панцитокератин, цитокератины 7 и 18, эпителиальный мембранный антиген (ЭМА), HER-2/neu, ER, PgR [5].
При метастазировании в ЛУ классического ДИР опухолевые клетки локализуются преимущественно в синусоидах, реже — в лимфоидных зонах. Поражение может быть минимальным, представленным единичными раковыми клетками, рассеянными среди лимфоидных элементов, или группами из нескольких клеток, локализующихся субкапсулярно, в толще узла или (и) эмбола в просветах сосудов капсулы. Чаще наблюдаются субтотальное или тотальное замещение лимфоидной ткани, в некоторых узлах — прорастание капсулы ЛУ и инфильтрация прилежащей клетчатки. Неблагоприятным прогностическим фактором является формирование конгломератов метастатических узлов. Клетки рака в метастазах чаще формируют солидно-альвеолярные структуры независимо от варианта ДИР и не повторяют структурных особенностей первичного узла в молочной железе.
стневидноклеточные гистиоциты могут давать слабоположительную реакцию с красителями, выявляющими муцин, — альциановым синим (PAS-реакция) и муцикармином. Перстневидные клетки доль-ковой карциномы не всегда окрашиваются на слизь по Крейбергу или другими красителями, что также затрудняет дифференциальную диагностику между метастатическими проявлениями рака и реактивными изменениями клеток синусов лимфатического узла. Такие данные приводят также P. Rosen [18], P. Allenby и соавт. [4], V. Gould и соавт. [11]. Дифференциация этих двух процессов возможна с помощью ИГХ-исследования, так как клетки рака молочной железы (в отличие от гистиоцитов) экспрессируют широкий спектр цитокератинов и ЭМА, гистиоциты же неиммунореактивны с этими антителами. ИГХ-окрашивание с применением антител к панцитокератину, цитокератинам 7, 18 и ЭМА часто выявляет намного больше клеток метастаза рака в ЛУ, чем рутинное гистологическое исследование, а также позволяет обнаружить микрометастазы, не видимые на световом уровне при окрашивании гематоксилином и эозином, по Ван-Гизону и т.д.
В ряде случаев дифференциально-диагностическим критерием метастазов ДИР служит сильное положительное ИГХ-окрашивание рецепторов стероидных гормонов. Выраженная экспрессия ЭР и (или) ПР (++/+++) в ядрах опухолевых клеток позволяет исключить метастаз из другого органа или новообразование другой гистогенетической принадлежности [8]. Прежде всего это актуально для определения первоисточника при опухоли Крукен-берга. Однако следует помнить, что слабая экспрессия ЭР(+) может быть выявлена в опухолевых клетках аденокарциномы желудка [10].
Частота регионарного метастазирования нами изучена в 257 случаях ДИР. При исследовании гистологических препаратов у больных с классическим или другими вариантами ДИР в 163 (63,42%) случаях выявлены метастазы в регионарных ЛУ, в 157 (61,08%) — в подмышечных и в 54 (21,01%) — в па-растернальных ЛУ. У 5 (1,95%) больных наблюдалось поражение парастернальных ЛУ при отсутствии метастатического поражения ЛУ подмышечной клетчатки. То есть в 108 (42,02%) случаях наблюдалось поражение только подмышечного (103 случая; 48,07%) или парастернального (5 случаев; 1,95%) лимфатического коллектора, в 49 (19,07%) — поражение обеих групп ЛУ (табл. 1).
У 133 (51,8%) больных первичный узел локализовался в левой молочной железе, у 124 (48,2%) — в правой. Данные о расположении первичного очага в молочной железе и частоте поражения квадрантов ДИР при наличии метастазов в парастерналь-ных ЛУ и клетчатке представлены в табл. 2.
Как видно из приведенных данных, наиболее частой неблагоприятной локализацией первичного узла явилась граница внутренних квадрантов (36,4%). При анализе расположения опухоли во внутренних и наружных квадрантах, а также при локализации пер-
Таблица 1. Частота метастатического поражения подмышечного и парастернального лимфатических коллекторов в зависимости от стадии ДИР
Стадия TNM* Количество Метастазы Метастазы
случаев в подмышечных ЛУ в парастернальных ЛУ
по TNM абс. % (от общего абс. % (от количества

Рак молочной железы (РМЖ) на протяжении многих лет в структуре онкологической заболеваемости и смертности среди женского населения Российской Федерации продолжает занимать лидирующую позицию [1]. На 2013 год абсолютное число заболевших злокачественными новообразованиями в мире 12,7 млн, и РМЖ занял второе место после рака легкого [2]. С 1980 по 2012 г. абсолютное число заболевших злокачественными новообразованиями на территории Российской Федерации составило 59,5 на 100 тыс. человек [3]. По мнению некоторых ученых, рост заболеваемости РМЖ связан с изменениями факторов репродуктивного риска, увеличением продолжительности жизни, пагубными привычками [4; 5]. В настоящее время диагностика и лечение РМЖ достигли высокого уровня, однако прогрессирование опухолевого процесса и отдаленное метастазирование свидетельствуют о неблагоприятном прогнозе для этих больных. Последние годы ознаменовались появлением новых современных методов, использование которых позволяет осуществлять раннюю диагностику этой патологии. Диагноз метастатического поражения зачастую устанавливается после появления симптоматики и подтверждается с помощью таких современных методов, как мультиспиральная компьютерная томография (МСКТ), магнитно-резонансная томография (МРТ), позитронно-эмиссионная томография (ПЭТ-КТ). Главной причиной летального исхода большинства онкологических больных является развитие рецидива и отдаленных метастазов, ежегодно выявляемых в 30-40% наблюдений, при этом метастатический РМЖ является наиболее частой причиной смертности среди женщин моложе 55 лет [6]. Особенностью РМЖ является достаточно высокий процент гематогенного и лимфогенного метастазирования. Частота метастазирования в значительной степени зависит от особенностей гистологического типа первичной опухоли. Так, частота гематогенного церебрального метастазирования рака молочной железы c гиперэкспрессией HER2/neu достигает 28-43%, при отрицательном статусе стероидных гормонов и без экспрессии белка HER2/neu - 55%, при гормон-позитивном типе опухоли - 11%, а легочные метастазы при РМЖ по частоте возникновения занимают второе место и обнаруживаются в 29,4% наблюдений [2].
Порог двухлетней выживаемости преодолевают лишь 8% больных с церебральными метастазами РМЖ, а пятилетняя выживаемость немногим превышает 2%. Значимую роль в прогнозе выживаемости носит характер метастазирования, определяющий эффективность химиотерапевтического лечения. Однако качество жизни данной категории пациентов в течение всего периода времени в существенной степени зависит от выбранной тактики лечения [7]. Методами локального лечения являются хирургическое удаление метастазов и лучевая терапия, а системным – химиотерапия. На сегодняшний день остается неопределенной роль хирургического компонента в лечении больных РМЖ с внутрилегочными метастазами и метастазами в головной мозг. Наиболее значимыми прогностическими факторами при лечении данной категории больных с использованием хирургического метода являются: количество метастазов, характер оперативного вмешательства, длительность безрецидивного периода, состояние внутригрудных лимфатических узлов и локализация вне жизненно важных зон головного мозга [8]. Целесообразность лечения метастазов РМЖ в головной мозг и легкие не подвергается никакому сомнению, несмотря на его паллиативный характер, так как удается продлить жизнь больных более чем на 6 месяцев [9]. Стандартное лечение метастазов рака молочной железы в головной мозг включает лучевую терапию, неи?рохирургическое лечение, химиотерапию и зависит от гистологического типа первичного источника метастазирования. Появление таких новейших методов лечения, как гамма-нож (облучение четко ограниченным сфокусированным пучком), существенно улучшает прогноз заболевания [10]. В настоящее время чередование различных схем цитотоксической, гормональной, таргетной терапии и применение новых хирургических технологий позволяют добиться улучшения непосредственных и отдаленных результатов лечения и сохранения удовлетворительного качества жизни [11]. Оптимальная продолжительность терапии у больных метастатическим РМЖ с объективными регрессиями или стабилизацией до сегодняшнего дня не определена. Считалось, что поддерживающая пролонгированная терапия может улучшить качество жизни и увеличить время до прогрессирования заболевания, однако не влияет на выживаемость [12].
Концепция неизлечимости метастатического РМЖ в наши дни определяет выбор тактики лечения этого заболевания, главной целью которого являются максимальное продление жизни пациентки и облегчение симптомов болезни.
Представляем клинический случай больной раком молочной железы с метастатическим поражением головного мозга, множественными метастазами обоих легких.
В октябре пациентка А., 46 лет обратилась в поликлинику по месту жительства с жалобами на новообразование в правой молочной железе, обнаруженное самостоятельно. Больная направлена на консультацию к онкологу. При осмотре: молочные железы симметричные; в левой молочной железе фиброзно-кистозные изменения; в верхнем наружном квадранте правой молочной железы по передней аксиллярной линии груднои? клетки определяется округлой формы, плотное, ограниченно смещаемое новообразование диаметром 2 см; симптомы площадки, умбиликации и Ке?нига – отрицательные. Регионарные лимфатические узлы не пальпируются.
При маммографии молочные железы полусферическои? формы, симметричные. Контуры кожи и соски желез не изменены. Ретромаммарное пространство не затемнено. В верхненаружном квадранте правой молочнои? железы лоцируется округлой формы без четких контуров образование размером 2,0 см - диагностическая категория BI-RADS (Breast Imaging Reporting and Data System): справа – 4; слева – 1. По данным ультразвукового исследования молочных желез, в правой молочнои? железе по переднеи? аксиллярнои? линии в проекции VII межреберья визуализируется очаговое образование сниженнои? эхогенности, неоднороднои? структуры, без четких контуров, с признаками инфильтративного роста, с вертикальнои? ориентациеи? максимальнои? оси размером 19,0х20,0 мм. Кровоток интранодулярныи?, визуализируется единичныи? питающии? сосуд (Ri (resistive index) – 0,63). В правой подмышечной области лоцируется группа измененных лимфатических узлов, максимальным размером 14 мм. При ультразвуковом исследовании органов брюшной полости и малого таза данные о метастазах не выявлены. Выполнена тонкоигольная аспирационная биопсия новообразования правой молочной железы. По данным цитологического исследования – инвазивный рак молочной железы. Установлен диагноз: рак правой молочной железы сT1cN1M0, IIa. Пациентке 1 ноября 2007 г. выполнена радикальная мастэктомия правой молочной железы по Madden с лимфодиссекцией D2. В послеоперационном периоде выполнено иммуногистохимическое исследование. Сформулирован окончательный диагноз: инвазивный дольковый солидно-альвеолярный рак правой молочной железы pT1cN1M0, IIa, умеренной степени злокачественности - 7 баллов, ER- (0), PR- (0), HER2/neu-(3+). Назначено комплексное лечение: системная терапия по схеме FAC 6 курсов (фторурацил 500 мг/м2, доксорубицин 50 мг/м2, циклофосфамид 500 мг/м2 1 раз в 21 день) и курс лучевой гамма-терапии на зоны регионарного метастазирования (СОД 49,5 Гр) и послеоперационный рубец (СОД 50 Гр). С декабря 2007 по январь 2013 года больная находилась под диспансерным динамическим наблюдением у онколога в поликлинике по месту жительства. При проведении очередного контрольного обследования в январе 2013 г. при МРТ головы отмечено прогрессирование заболевания в виде появления единичных метастатических поражений левой лобной доли головного мозга и нижней доли правого легкого (рис. 1, 2).
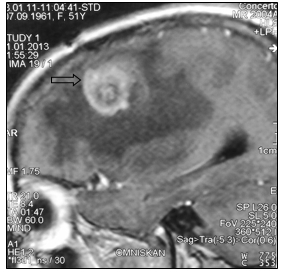
а
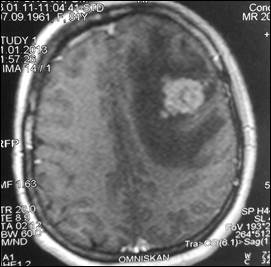
б
Рис. 1. МР-томограммы больной А., 51 год, с метастазом в левую лобную долю (стрелка):
а – сагиттальная плоскость; б – горизонтальная плоскость (объяснение в тексте)
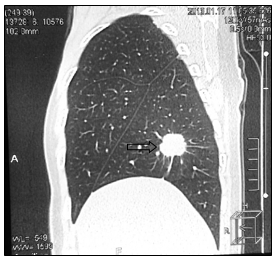
а
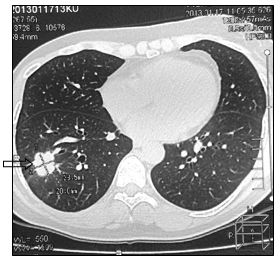
б
Рис. 2. КТ-картина метастаза в нижнюю долю правого легкого (стрелка):
а – сагиттальная плоскость; б – горизонтальная плоскость (объяснение в тексте)
Консилиумом врачей принято решение об оперативном лечении. 06.02.2013 г. выполнена костно-пластическая трепанация черепа, удаление опухоли левой лобной доли головного мозга. Гистологическое заключение удаленного препарата: метастаз низкодифференцированной аденокарциномы (рис. 3)
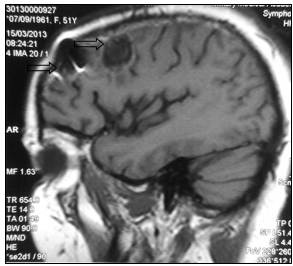
а
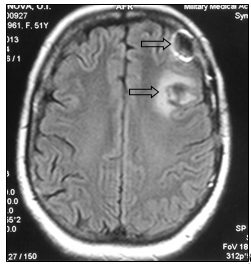
б
Рис. 3. МР-картина послеоперационных отечно-глиозных изменений в левой лобной доле (стрелка): а – сагиттальная плоскость; б – горизонтальная плоскость (объяснение в тексте)
Далее проведена системная химиотерапия доцетакселом (80 мг/м2). На фоне 2 циклов 2 линии в мае 2013 г. установлено прогрессирование заболевания в виде увеличения размеров существующего метастаза в нижней доле правого легкого с 20х24х21 до 22х28х25 мм и появления нового метастаза нижней доли левого легкого 7х11х8 мм (рис. 4).
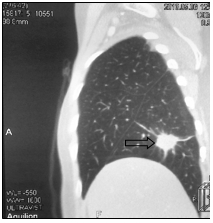
а
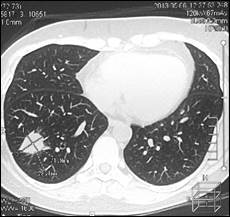
б
в
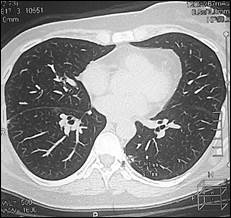
Рис. 4. Компьютерная томография от 05.06.2013 г., признаки прогрессирования в виде увеличения размеров метастазов в нижней доле правого легкого и нижней доле левого легкого: а – метастаз в нижнюю долю правого легкого (стрелка), сагиттальная плоскость; б – горизонтальная плоскость; в - метастаз в нижнюю долю левого легкого (объяснение в тексте)
В связи с неэффективностью проводимой системной терапии принято решение о назначении 3 линии ПХТ (капецитабин 1250 мг/м2+герцептин 2 мг/кг). На фоне 12 циклов 3 линии химиотерапии достигнута стабилизация процесса. Однако при контрольном обследовании спустя год отмечено прогрессирование в виде увеличения размеров метастазов в нижней доле правого легкого с 22х28 до 32х28 мм и нижней доле левого легкого с 7х11 до 11х11 мм (рис. 5).
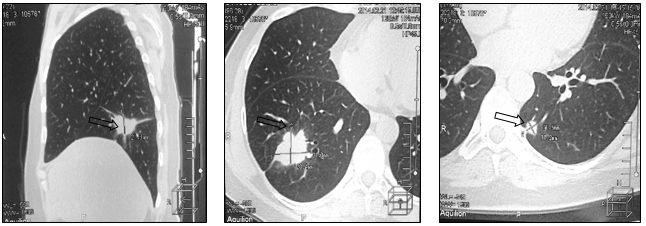
Рис. 5. Компьютерная томография больной А., 52 года, прогрессирование заболевания в виде увеличения размеров опухоли (стрелка): а – метастаз в нижнюю долю правого легкого, сагиттальная плоскость; б – горизонтальная плоскость; в - метастаз в нижнюю долю левого легкого (объяснение в тексте)
В связи с прогрессированием заболевания произведена смена системной химиотерапии на гемцитабин 1250 мг/м2. 4 линия ПХТ позволила стабилизировать онкологический процесс на протяжении 6 месяцев. При контрольном обследовании в июле 2014 г. выявлено новое метастатическое поражение верхней доли левого легкого, размеры других образований не изменились по сравнению с предыдущим исследованием (рис. 6).
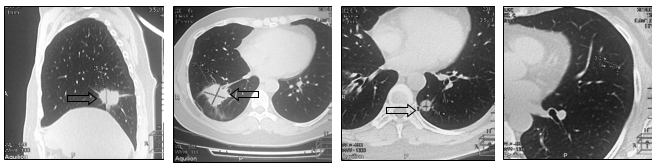
Рис. 6. Компьютерная томография (07.2014 г.), прогрессирование в виде метастатического поражения верхней доли левого легкого, размеры других образований не увеличились (стрелка): а – метастаз в нижнюю долю правого легкого, сагиттальная плоскость;
б – горизонтальная плоскость; в - метастаз в нижнюю долю левого легкого; г – метастаз в верхнюю долю левого легкого (объяснение в тексте)
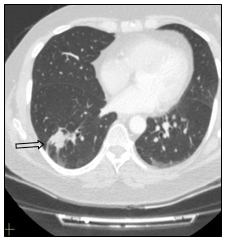
Произведена очередная смена системной химиотерапии. Назначена монохимиотерапия по схеме паклитаксел (260 мг/м2). Проведено 38 циклов с частичным регрессом заболевания - уменьшение размеров метастазов легких. В настоящее время пациентка продолжает получать назначенное лечение. Общая продолжительность жизни составляет 10 лет (рис. 7, 8).
а
б
в
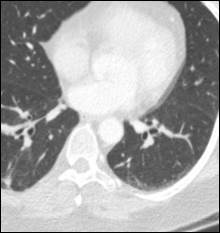
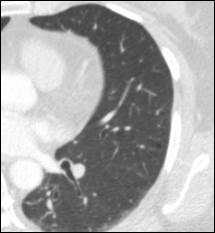
Рис. 7. Компьютерная томография больной А., 55 лет, с метастазами в легкие (стрелка): а – горизонтальная плоскость; б – очаговое уплотнение легочной ткани нижней доли левого легкого; в – уменьшение очагового уплотнения легочной ткани верхней доли левого легкого (объяснение в тексте)
а
б
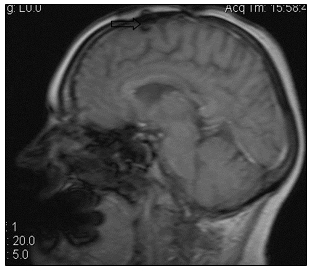
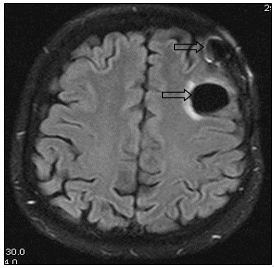
Рис. 8. МР-томограммы больной А., 55 лет, МР-картина послеоперационных кистозно-глиозных изменений в левой лобной доле (стрелка): а – сагиттальная плоскость; б – горизонтальная плоскость (объяснение в тексте)
Метастазирование злокачественных опухолей является одной из важнейших проблем современной онкологии. По данным литературы, пятилетняя выживаемость при метастатическом раке молочной железы составляет 0,6–5%, а десятилетняя 0,3–1,2%. Лекарственное лечение РМЖ является ключевым составляющим комплексной терапии. При раннем операбельном РМЖ применение адъювантной системной терапии позволяет улучшить результаты лечения, повышая при этом общую и безрецидивную выживаемость больных, а при метастатическом РМЖ является основным методом лечения, способствующим добиться выраженного клинического эффекта в виде полной или частичной ремиссии различной продолжительности у 40-70% больных. Но и при достижении полной клинической ремиссии в случае метастатического РМЖ остается риск рецидива заболевания и возникновения лекарственной персистентности. В свою очередь сложность лечения рецидивов и метастазов РМЖ осложняется результатами ранее проведенной терапии, включающей облучение, неоадъювантную и адъювантную терапию, что приводит к развитию резистентности опухолевых клеток к цитостатическим препаратам и к снижению функциональных резервов печени, сердечно-сосудистой системы, костномозгового кроветворения.
Данное наблюдение демонстрирует возможность комплексного лечения инвазивного долькового солидно-альвеолярного рака молочной железы с локализацией метастазов в головной мозг и легкие. В описанном клиническом случае создается одна из наиболее важных и трудных для врача проблема выбора терапии. Следует отметить, что значительным моментом является наличие большого числа противоопухолевых препаратов и различных схем полихимиотерапии, обладающих различной степенью активности.
Сегодня метастатический РМЖ продолжает оставаться неизлечимым заболеванием и рассматривается как хронический процесс, который требует достаточно длительного лечения с периодической сменой одного вида терапии на другой. У части больных появилась возможность увеличения длительности ремиссии, выживаемости и улучшения ее качества посредством комбинации методов противоопухолевого лечения. Характерной чертой современных исследовании? продолжает оставаться стремление к индивидуализации терапии, в истоках которой лежит более глубокое понимание молекулярно-биологических основ канцерогенеза и применение новейших достижении? науки, в том числе нанотехнологии?. Поэтому представляет интерес поиск критериев отбора больных распространенным раком молочной железы, чувствительным к проведению противоопухолевого лечения.
Материалы этого сайта размещены для ознакомления, все права принадлежат их авторам.
Если Вы не согласны с тем, что Ваш материал размещён на этом сайте, пожалуйста, напишите нам, мы в течении 1-2 рабочих дней удалим его.
На правах рукописи
Андреяшкина Ирина Ивановна
ОПТИМИЗАЦИЯ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ
С МЕТАСТАЗАМИ В ЛЕГКИЕ С УЧЕТОМ ФАКТОРОВ ПРОГНОЗА
диссертации на соискание ученой степени
доктора медицинских наук
Научный консультант –
Плохов Владимир Николаевич
Официальные оппоненты:
Владимирова Любовь Юрьевна
Огнерубов Николай Алексеевич
Вельшер Леонид Зиновьевич
Ведущая организация –
Ученый секретарь совета по защите докторских и кандидатских диссертаций, д.м.н., профессор
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Широкое внедрение комплексных методов лечения онкологических заболеваний способствует улучшению показателей выживаемости при различных локализациях злокачественных новообразований. Одним из факторов, резко ухудшающих прогноз после проведенного лечения, служит появление отдаленных метастазов (Чиссов В.И. и соавт., 2012).
Легкие – это орган, где наиболее часто появляются метастазы различных злокачественных опухолей. Метастатическое поражение легких чаще связано с гематогенным распространением процесса (Давыдов М.И.и соавт.,2011). Данные о частоте легочных метастазов при раке молочной железы в литературе противоречивы. Частота метастазирования в легкие при раке молочной железы составляет 29,4% (Аксель Е.М. и соавт.,2012).
Лечение больных диссеминированным раком молочной железы представляет одну из наиболее сложных проблем клинической онкологии. Совершенствование лекарственного лечения не сопровождается снижением смертности в популяции от этой патологии. Средняя продолжительность жизни пациенток с момента выявления метастазов по-прежнему не превышает 3 лет, при этом более 5 лет живет 25–30%, более 10 лет – 10% больных (Переводчикова Н.И., 2012). У больных раком молочной железы с метастазами в легкие особенно актуальным является определение гормональной и лекарственной чувствительности опухолей для индивидуального подбора схем терапии. План лечения пациентов метастатическим раком молочной железы представляется как оптимальное применение всех лечебных воздействий для достижения максимального паллиативного эффекта и отсрочки прогрессирования заболевания и смерти, по возможности с минимальным токсическим эффектом (Тюляндин С.А. 2011).
В данном исследовании предложена математическая модель прогнозирования метастазирования рака молочной железы в легкие и пятилетней выживаемости, основанный на многофакторном анализе влияния параметров опухоли и организма на процесс диссеминации в легкие, а также индивидуальный подбор методов лечения.
Цель исследования повышение эффективности лечения рака молочной железы с метастазами в легкие путем дифференцированного применения методов противоопухолевой терапии на основе создания математической модели прогнозирования метастазирования в легкие и пятилетней выживаемости.
Задачи исследования:
1. Определить комплекс факторов прогноза метастазирования рака молочной железы в легкие.
2. Оценить влияние параметров опухоли и организма на интервал времени до метастазирования рака молочной железы в легкие.
3. Изучить эффективность и обоснованность показания к применению различных схем химиотерапии и гормонотерапии у больных раком молочной железы с метастазами в легкие, с учетом факторов прогноза пятилетней выживаемости.
4. Оценить роль хирургического лечения солитарных метастазов в легкие в комплексном лечения у больных раком молочной железы.
5. Исследовать показатели гормонов гипоталямо-гипофизарной системы, опухолевых маркеров – СА 15-3, РЭА на различных этапах течения опухолевого процесса и их изменение под влиянием проводимой терапии.
6. Выявить прогностическую значимость ряда показателей гипоталямо-гипофизарной системы и возможность их применения в мониторинге больных раком молочной железы с метастазами в легкие.
7. Изучить иммунный статус и коагуляционный гемостаз больных раком молочной железы на различных этапах метастазирования в легкие.
8. Создать алгоритм прогнозирования метастазирования рака молочной железы в легкие и пятилетней выживаемости в данной группе больных по отличительным параметрам опухоли и организма.
Научная новизна работы состоит в том, что впервые проведена комплексная оценка клинических, морфологических, гормональных, иммунологических факторов у больных раком молочной железы с метастазами в легкие. Выявлены особо значимые факторы для определения прогноза метастазирования в легкие и пятилетней выживаемости в данной группе больных, основанные на отличительных биологических особенностях опухоли и организма. Дана количественная оценка степени выраженности каждого из данных факторов.
В работе на основании собственного клинического материала изучено влияние параметров опухоли и организма на интервал времени метастазирования рака молочной железы в легкие. Впервые предложена модель многоступенчатого алгоритма выбора оптимального лечения рака молочной железы с метастазами в легкие. Показаны возможности индивидуального подхода к планированию лечения больных раком молочной железы с метастазами в легкие по результатам пятилетней выживаемости.
Впервые при динамическом наблюдении и на фоне проводимого лечения выявлена прогностическая значимость уровня гормонов гипоталямо-гипофизарной системы и их взаимосвязи с маркерами опухолевого процесса, иммунологические показатели у больных раком молочной железы с метастазами в легкие.
В работе впервые предложен алгоритм прогнозирования метастазирования в легкие и пятилетней выживаемости при раке молочной железы с метастазами в легкие по биологическим параметрам опухоли и организма. Выявленные благоприятные и неблагоприятные факторы риска метастазирования рака молочной железы в легкие, позволяют обеспечить превентивность проводимого лечения у больных раком молочной железы.
Основные положения, выносимые на защиту.
1. Прогноз метастазирования рака молочной железы в легкие зависит от комплекса факторов, характеризующих биологические особенности опухоли и организма.
2. Предложенный метод математического анализа позволяет прогнозировать метастазирование рака молочной железы в легкие и пятилетнюю выживаемость в данной группе больных и является патогенетически обоснованным подходом к выбору плана лечения.
3. Рациональность применения параметров, характеризующих состояние гипоталямо-гипофизарно-надпочечниковой системы, показателей иммунного статуса в мониторинге больных раком молочной железы с метастазами в легкие.
Публикации. По теме диссертации опубликовано 78 научных работ, из них – 17 в рецензируемых журналах, рекомендованных ВАК РФ.
Структура и объем работы. Диссертационная работа изложена на 234 стр. машинописного текста, состоит из введения, 6 глав, заключения, выводов, практических рекомендаций и указателя литературы, включающего 158 источников отечественной и 109 зарубежной литературы. Работа иллюстрирована 61 таблицей и 52 рисунками.
СОДЕРЖАНИЕ РАБОТЫ
Характеристика материала, методов исследования и лечения
В зависимости от вышеперечисленных факторов и планировалось лечение, которое было комбинированным, комплексным или монолечением. Преимущественно проводилось комплексное лечение у 62% больных, комбинированное лечение – 36,2%. Монолечение было представлено во всех случаях хирургическим вмешательством (1,8%) с паллиативной целью.
С целью определения возможностей различных вариантов лечения больных раком молочной железы с метастазами в легкие из общего количества больных были выделены три основных подгруппы и подгруппы контроля.
Оценка эффективности проводимого лечения в каждой группе проводилась посредством оценки одногодичной и 5-летней выживаемости.
Первую основную подгруппу составили больные раком молочной железы с ранними метастазами в легкие, которым проводили полихимиотерапию с включением препарата группы таксанов, (n= 70).
Контрольную подгруппу для них составили пациентки, которым проводилась системная полихимиотерапия, включающая антрациклины, (n= 70).
Вторую основную подгруппу составили больные раком молочной железы с поздними метастазами в легкие (n=30), которым в качестве метода лечения применена гормонотерапия препаратом анастразол. Контрольную подгруппу составили больные, получавшие тамоксифен, (n=30).
Третью подгруппу составили больные раком молочной железы с поздними метастазами в легкие, которым при выявлении солитарного метастаза в легкие проводилось оперативное лечение, с последующей гормонотерапией (n=30).
Данный этап исследования представлен на рисунке 1.
Все больные, которым применялась системная ХТ и гормонотерапия по основным прогностическим факторам, влияющим на выживаемость, были сопоставимы.
Группа сравнения Основная группа
Рис. 1. Распределение больных РМЖ в зависимости от этапов исследования
Для оценки токсичности ХТ использовали критерии CTC-NCIC (Переводчикова Н.И., 2000).
Методы лечения
Системная химиотерапия проводилась по стандартным методикам. В первой основной подгруппе больных раком молочной железы с метастазами в легкие, схема лечения включалала препарат группы таксанов, химиотерапия проводилась в двух режимах.
1-й: пациенты, получавших 6 циклов AD (доксорубицин – 50 г/м2 в 1-й день, доцетаксел 75 мг/м2 инфузия 1 час в 1-й день, перерыв 3 недели).
2-й: пациенты, получавшие доцетаксел (таксотер – 100 мг/м2, через 3 недели) в монорежиме.
В контрольной подгруппе пациенты, получали 6 циклов АС (доксорубицин + циклофосфан). Каждый цикл включает внутривенную однократную инъекцию доксорубицина в дозе 60 мг/м2 и циклофосфана в дозе 600 мг/м2, каждый цикл повторялся через 21 день.
Вторая основная подгруппа: пациенты, получавшие анастрозол в дозе 1 мг в сутки в течение 1 года. Контрольную подгруппу составили пациенты, получавшие тамоксифен в дозе 20 мг в сутки в течение 1 года.
Третью подгруппу составили больные раком молочной железы с поздними метастазами в легкие, которым при выявлении солитарного метастаза в легкие проводилось оперативное лечение с последующей гормонотерапией: тамоксифен в дозе 20 мг в сутки.
Рентгенологическое исследование начинали с обзорной рентгенографии в двух проекциях (прямой и боковой), в последующем проводилась компьютерная диагностика, которую осуществляли с помощью компьютерного томографа Somaton CR фирмы Siemens.
Морфологическое исследование проводилось на амбулаторном и клинических этапах обследования. Для оценки динамики развития метастатического процесса, в работе применена система многоэтапной морфологической диагностики, разработанная в клинике.
Иммуногистохимическое исследование проводилось авидин-биотиновым методом.
В ходе исследования определяли рецепторный статус опухоли (РЭ и РП), HER 2neu, Ki 67, p 53.
Иммунологическое исследование проводилось с учетом степени выраженности показателей клеточного, гуморального звеньев иммунитета и общей неспецифической резистентности организма.
Лабораторная диагностика показателей гипоталамо-гипофизарно-надпочечниковой системы и показателей коагуляционного гемостаза и фибринолиза в сыворотке крови проводилось на автоматическом биохимическом анализаторе фирмы Olympus AU680.
Опухолевые маркеры определяли иммунохемилюминесцентным методом с помощью автоматического анализатора ADVIA-CENTAUR фирмы Bayer (Германия).
Статистическую обработку проводили путем анализа историй болезни, и результаты проведенных исследований были занесены в специально созданную автоматизированную базу данных.
Результаты исследования и их обсуждения
На основании многофакторного анализа определен комплекс факторов, влияющих на метастазирование рака молочной железы в легкие. У 111 (48,3%) больных наблюдалась инфильтративная форма роста, смешанная форма роста опухоли отмечалась у 92 (40%) больных, однако статистической разницы в данных группах не было отмечено. Узловая форма роста встречалась у 27 (11,7%) пациенток. Наибольший риск метастазирования в легкие имеют опухоли с инфильтративной и смешанной формой роста при корреляции с низкой степенью злокачественности, высокой степенью дифференцировки, положительной экспрессией HER-2neu и отрицательным рецепторным статусом. При смешанной и инфильтративной форме роста опухоли метастазирование в легкие имело множественный характер поражения легких, 89,1%–95,2%, соответственно (p
Читайте также:

