Лучевой патоморфоз рака прямой кишки
При светооптическом сравнительном исследовании плоскоклеточного рака гортани и аденокарциномы прямой кишки до и после лучевого воздействия отмечено сохранение в фиброзной строме на месте бывшей опухоли роговых масс (при раке гортани) и скоплений слизи (при аденокарциноме прямой кишки).
В зависимости от степени повреждения при плоскоклеточном раке гортани повышение дифференцировки опухолевых клеток было неодинаковым. При I степени лучевых повреждений структура опухоли обычно ие изменялась, выявлено лишь некоторое усиление ороговения в центре опухолевых компонентов II степень повреждений характеризовалась очаговым фиброзным замещением паренхимы опухоли, в ряде наблюдений обнаруживали ноля роговых масс с наличием но периферии их отдельных многоядерных гигантских клеток инородных тел. При III и IV степени повреждения в зоне опухоли находили грубоволокнистую соединительную ткань с остатками роговых масс, окруженных гигантскими клетками инородных тел.
При электронно-микроскопическом исследовании рака легкого накопление кератина после облучения наблюдали только в более дифференцированных опухолевых клетках, расположенных среди фиброзной ткани.
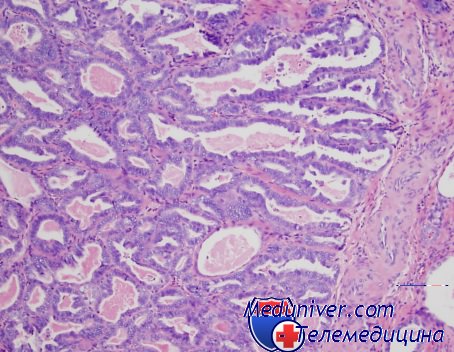
Избыточное образование кератогиалина в клетках дифференцированного плоскоклеточного рака легкого отмечено после облучения в дочах свыше 40 Гр. Оно приводит к гибели опухолевых клеток, а отложение роговых масс в строме вызывает усиленную пролиферацию гистиоцитариых элементов которые активно участвуют в резорбции опухоли. Показано, что гигантские многоядерные клетки типа гигантских клеток инородных тел имели отчетливые признаки макрофагальной диффереинировки, и они фагоцитировали не только распавшиеся, но и жизнеспособные опухолевые клетки.
При обзорной электронной микроскопии облученной аденокарциномы прямой кишки в ней обнаруживали клетки, недифференцированные и дифференцированные в направлении бокаловидных энтероцитов и кишечных энителиоцитов. Поскольку в облу ченных новообразованиях визуально преобладали клетки с той или иной степенью повреждения их органоидов, это затрудняло определение направления и степени их специализации. Однако сохранившиеся раковые клетки имели крупные ядра, небольшое число органоидов и по своей ультраструктуре были ближе всего к клеткам недифференцированного типа, которые в функциональном отношении являются, по-видимому, покоящимися клетками.
Морфологическая картина лечебного патоморфоза остеогенной саркомы характеризовалась изменением направленности дифференцировки с костной в хрящевую, а в гигантоклеточнои опухоли — с костной в фиброзную. Этим фактам дается следующее объяснение.
Направленность дифференцировки клеток в значительной мере определяется условиями микроокружения. При достаточной васкуляризации и интенсивной оксигенации дифференцнровка осуществляется в костном направлении с продукцией соответствующего промежуточного вещества различной степени зрелости. Наоборот, снижение уровня васкуляризации после лечебного воздействия создает брадитрофные условия метаболизма н диффереи-цировка осуществляется по хондроидному типу с появлением характерных клеточных форм и промежуточного вещества.
Описание патента на изобретение RU2349916C1
Предлагаемое изобретение относится к медицине, а именно к колопроктологии, онкологии, и может использоваться при лечении больных раком прямой кишки с целью повышения его эффективности.
Актуальность проблемы обусловлена высоким уровнем и темпами роста заболеваемости раком прямой кишки, которая по данным ВОЗ составляет 17 на 100000 населения. Частота рака прямой кишки в общей структуре злокачественных опухолей составляет до 10%, а ежегодный прирост заболеваемости раком данной нозологической формы в России - 3,46%. В лечении рака прямой кишки ведущим методом остается хирургический, однако неудовлетворительные отдаленные результаты лечения, высокий процент рецидивов побуждает к поискам различных комбинированных методов. Одним из компонентов комбинированного лечения рака прямой кишки является предоперационная лучевая терапия.
Эффективность проводимого лечения во многом зависит от радиочувствительности опухолевой ткани. Прогнозирование ее путем исследования лучевого патоморфоза в процессе лучевого лечения является одним из перспективных направлений в повышении эффективности лечения рака прямой кишки, улучшении непосредственных и отдаленных результатов.
В литературе имеется ряд работ, в которых проводится оценка лучевых изменений опухоли, однако не выявлено ни одного способа прогнозирования чувствительности опухоли к проводимой лучевой терапии у больных раком прямой кишки. В связи с этим выбрать прототип не представляется возможным.
Известен способ оценки реакции опухоли на лучевую терапию путем динамического наблюдения за больными. При этом изучаются размеры новообразования и его подвижность при пальцевом исследовании до начала и в процессе лечения. Полную реализацию эффекта лучевого воздействия оценивают через 3-4 недели после окончания курса проводимой терапии. Регресс опухоли менее 50% расценивается как ее относительная радиорезистентность. При уменьшении ткани опухоли более чем на 50% от первоначального размера констатируется чувствительность опухоли к лучевой терапии [Гарин A.M., Трапезников Н.Н. Новые предложения Всемирной организации здравоохранения по стандартизации оценки лечения онкологических больных. // Вопросы онкологии, 1978]. Данный способ является аналогом.
- данные критерии оценки относятся к ретроспективным (предназначены для суждения об эффективности уже проведенного лечения) и субъективным;
- оценить эффект можно только через 3-4 недели после завершения лечения в то время как изменения биологического объекта начинаются уже в момент первого лучевого воздействия (в случае радиорезистентности опухоли теряется время).
Кроме того, известен способ прогнозирования чувствительности опухоли к лучевой терапии у больных раком молочной железы. При этом анализируется динамика изменений показателей периферической крови в процессе лучевой терапии. При значении эозинофилов >=4%, лимфоцитов >=0.3% на 15-30 день от начала лучевой терапии прогнозируют высокую чувствительность опухоли к облучению (лучевой патоморфоз III-IV степени), а при меньших значениях данных показателей - слабую чувствительность (лучевой патоморфоз I-II степени) [Сеньчукова М.А.]. Описанный выше способ принят за аналог 2.
Недостатки второго аналога:
- изменения показателей периферической крови могут быть связаны с особенностями организма, его реактивностью, состоянием иммунной системы;
- большой срок обнаружения радиорезистентности (на 15-30 день от начала лечения).
Целью предлагаемого способа является прогнозирование чувствительности опухоли к лучевой терапии у больных раком прямой кишки в ранние сроки от начала лечения, а именно на 4-й день.
Поставленная цель достигается тем, что после 4-х сеансов лучевой терапии дробно-протяженным методом проводят гистологическое исследование биоптата, взятого из опухоли, и при наличии патоморфоза III-IV степени прогнозируют высокую чувствительность опухоли к лучевой терапии, а при наличии патоморфоза I-II степени - низкую чувствительность. Наличие патоморфоза III-IV степени определяют при значении площади некроза >43.8%, количества клеток с необратимыми формами дистрофий >52%, количества митотически делящихся клеток 48%, а I-II степени - при площади некроза и количества клеток с необратимыми формами дистрофий меньше приведенных значений, а количества митотически делящихся клеток больше таковых.
Основу исследования составил анализ гистологических препаратов больных раком прямой кишки, которым в предоперационном периоде проведен курс дробно-протяженной лучевой терапии тормозным излучением на изоцентрическом ротационном линейном ускорителе Philips с энергией 6 МэВ с разовой очаговой дозой 2 Гр и в суммарной очаговой дозе 40 Гр. Радикальная операция выполнялась через 3-4 недели после окончания лучевого лечения. Морфологические исследования включали изучение материала биопсий, проведенных до начала облучения, в процессе его (после 4-го, 8-го, 12-го, 16-го и 20 сеансов), и операционных препаратов удаленных опухолей.
Для этого использованы такие классические параметры, как площадь некроза ткани новообразования, количество некротизированных раковых элементов, клеток с необратимыми формами дистрофий, количество сохранившихся опухолевых клеток, митотический индекс с учетом форм патологических митозов, что позволило в последующем дать степенную оценку терапевтического патоморфоза непосредственно после проведенных воздействий на опухоль в рамках схем, предложенных Г.А.Лавниковой с соавторами (1973 г.). Изучалась динамика данных параметров, степень выраженности в зависимости от дозы лучевой терапии. При оценке биологического действия ионизирующего излучения на опухолевые ткани установлено время появления прогностических критериев (признаков), которые в последующем либо нарастали в случае, если опухоль оказывалась радиочувствительной и были максимально выражены после завершения лечения, либо оставались незначительными, если опухоль была радиорезистентной. О чувствительности опухоли можно было судить уже на 4-й день от начала лечения. При признаках патоморфоза III-IV степени, таких как площадь некроза (% от площади исследуемого материала) >43.8%, количество клеток с необратимыми формами дистрофий >52%, количество митотически делящихся клеток (% от общего количества клеток) 48%, - прогнозировалась высокая чувствительность, а при I-II степени: площадь некроза и количество клеток с необратимыми формами дистрофий меньше приведенных значений, а количество митотически делящихся клеток больше таковых - относительная радиорезистентность.
Преимущества по сравнению с аналогами:
- критерии оценки относятся к проспективным (прогностическим) и могут помочь наметить наилучший план лечения больного;
- оценка проводится на тканевом уровне (объективные критерии);
- оценить эффект проводимого лечения можно уже на 4-й день.
Через 3 недели после окончания лучевой терапии отмечен регресс опухоли на 50%. По данным трансректального УЗИ стенка кишки утолщена до 11 мм, признаков инвазии в соседние органы не выявлено. Субъективно пациент отметил улучшение состояния: стул стал регулярным, жалоб на тенезмы и выделение крови не предъявлял. Выполнена экстирпация прямой кишки.
Гистологическое исследование операционного материала: в опухоли имеются резкие проявления лучевого патоморфоза, больший объем новообразования полностью некротизирован (IV-III степень по Лавниковой), среди полей некроза встречаются небольшие редкие опухолевые комплексы с патоморфозом II ст.
Проведенные исследования впервые выявили, что прогнозировать радиочувствительность опухоли можно уже на 4-й день от начала лучевой терапии. Установлено, что для этого среди известных критериев оценки степени реакции опухоли на облучение необходимыми и достаточными для прогнозирования являются такие показатели, как площадь некроза (% от площади исследуемого материала), количество клеток с необратимыми формами дистрофий(%), количество митотически делящихся клеток (% от общего количества клеток), количество клеток с патологией деления.
Через 3 недели после окончания лучевого лечения отмечен регресс опухоли менее 50% (в нижнеампулярном отделе прямой кишки определяется опухоль, занимающая всю переднюю стенку). При трансректальном ультразвуковом исследовании передняя стенка кишки утолщена до 15 мм, слоистость ее нарушена, контур ровный, граница с окружающими тканями четкая. После проведенного лечения жалобы остались прежними. На операции выявлено, что опухоль врастает во влагалище, вдоль аорты имеются увеличенные до 3-4 см лимфатические узлы, лучевая инфильтрация тканей выражена значительно. Выполнена экстирпация прямой кишки с резекцией влагалища.
Гистологическое исследование операционного материала: патоморфоз носит очаговый характер: 1/3 участков с патоморфозом преимущественно III, местами IV степени, в остальных зонах патоморфоз 0-II степени. В сохранных участках количество клеток с необратимыми формами дистрофий - 27±7.6%, количество митотически делящихся клеток - 7±1.7%, из них клеток с патологией деления - 13.1±6.4%. В 2-х лимфоузлах имеются метастазы аденокарциномы.
Таким образом, в связи с радиорезистентностью опухоли констатирована потеря времени на облучение из-за отсрочки операции. Также это повлияло на технику операции.
Всего обследовано 20 больных, из них у семи пациентов после 4-го сеанса лучевого лечения прогнозировалась высокая чувствительность опухоли к проводимой терапии, а у тринадцати - низкая. Результаты прогноза подтвердились гистологическим исследованием операционного материала: у семи больных - наличие IV-III степени терапевтического патоморфоза, у остальных 13 - I-II степень патоморфоза.
1. Гарин A.M., Трапезников Н.Н. Новые предложения Всемирной организации здравоохранения по стандартизации оценки лечения онкологических больных. Вопросы онкологии 1978.
3. Мардынский Ю.С., Андреев В.Г. Прогностическое значение регрессии опухоли в процессе лучевой терапии. Современные методы оценки эффективности лучевой терапии. Обнинск, 1988 г.
4. Саенко А.С., Пелевина И.И. Прогнозирование реакции опухоли на облучение. XI Всесоюзный съезд рентгенологов и радиологов, Обнинск, 1984 г.
5. Сеньчукова М.А. Способ прогнозирования чувствительности рака молочной железы к лучевой терапии. Патент N 2099703.
Похожие патенты RU2349916C1
Реферат патента 2009 года СПОСОБ ПРОГНОЗИРОВАНИЯ ЧУВСТВИТЕЛЬНОСТИ ОПУХОЛИ К ЛУЧЕВОЙ ТЕРАПИИ У БОЛЬНЫХ РАКОМ ПРЯМОЙ КИШКИ
Изобретение относится к медицине, а именно к онкологии. Способ прогнозирования чувствительности опухоли к лучевой терапии у больных раком прямой кишки основан на гистологическом исследовании биоптата, взятого из опухоли после 4-го сеанса лучевой терапии, проводимой дробно-протяженным методом. При наличии патоморфоза III-IV степени прогнозируют высокую чувствительность опухоли к облучению, а при наличии патоморфоза I-II степени - низкую чувствительность. Использование способа позволяет прогнозировать чувствительность опухоли у больных раком прямой кишки к проводимой лучевой терапии в ранние сроки, что позволяет при выявлении радиорезистентности опухоли своевременно выполнять радикальную операцию - экстирпацию прямой кишки. 1 з.п. ф-лы.
Формула изобретения RU 2 349 916 C1
1. Способ прогнозирования чувствительности опухоли к лучевой терапии, проводимой дробно-протяженным методом, у больных раком прямой кишки, отличающийся тем, что после 4-х сеансов лучевой терапии проводят гистологическое исследование биоптата, взятого из опухоли, и при наличии патоморфоза III-IV степени прогнозируют высокую чувствительность опухоли к лучевой терапии, а при наличии патоморфоза I-II степени - низкую чувствительность. 2. Способ по п.1, отличающийся тем, что наличие патоморфоза III-IV степени определяют при значении площади некроза >43,8%, количества клеток с необратимыми формами дистрофий >52%, количества митотически делящихся клеток 48%, a I-II степени - по площади некроза и количества клеток с необратимыми формами дистрофий меньше приведенных значений, а количества митотически делящихся клеток больше таковых.
Рак прямой кишки – что это такое?
Это злокачественное онкологическое заболевание происходит из эпителия прямой кишки. Этой опухоли присущи характерные черты любого злокачественного образования – быстрый рост, прорастание в соседние ткани, метастазирование.
Подвержены болезни мужчины и женщины в равной степени. Рост числа заболевших отмечается с 45 лет, а пик заболеваемости приходится на 75-летних.
О заболевании
Слизистая оболочки конечного участка толстой кишки покрыта цилиндрическим эпителием с большим количеством желез. Их клетки продуцируют слизь. Под влиянием факторов риска появляются патологические клетки с бесконтрольным делением и утратой механизма апоптоза – запрограммированной гибели. Постепенно из них формируется опухоль прямой кишки.
Предположительно установлены причины рака прямой кишки:
- Неправильное питание.
Преобладание в рационе мясной пищи, животных жиров с одновременным дефицитом растительной клетчатки ухудшает прохождение кала, способствует запорам и развитию колоректальных опухолей. - Роль наследственности — замечена при возникновении некоторых форм новообразований.
- Предраковые патологии — полипы, болезнь Крона, неспецифический язвенный колит.
- Иммунодефицитные состояния, карцинома половых органов или молочной железы у женщин.
Виды рака прямой кишки
Тип опухоли определяется ее локализацией:
- Аноректальное расположение характерно для 5-8% случаев.
- Ампулярное встречается чаще других, до 80%. Это патология в самой широкой части кишки.
- Надампулярная локализация до 12% больных.
Характер роста опухоли может быть:
- экзофитный – растет в просвет кишечника;
- эндофитный – прорастает толщу стенки, инфильтрирует ее, может охватывать циркулярно;
- смешанный рост.
По гистологической картине новообразование бывает:
- железистый рак (аденокарцинома);
- солидный;
- перстневидно-клеточный;
- скирр;
- плоскоклеточный.
Симптомы рака прямой кишки, первые признаки
Обсуждение проблем прямой кишки для многих людей является чем-то постыдным. Поэтому первые признаки патологии часто остаются без должного внимания. Начальные симптомы рака прямой кишки – изменения характера стула. Появляется частая смена запора и диареи, меняется форма кала. Он становится значительно тоньше, чем раньше. Беспокоят чувство неполной дефекации, неприятные ощущения, повышенное образование газов.
Развитие опухолевого процесса вызывает отдаленные признаки рака прямой кишки:
- слизь и кровь в кале;
- гнойные выделения;
- чувство переполненного кишечника;
- вздутие живота;
- боль в области прямой кишки;
- хроническая усталость, утомляемость;
- анемия;
- потеря веса.
На начальных стадиях проявления болезни может не быть. При выявлении анемии неизвестного происхождения стоит искать причину скрытого кровотечения. Возможно, это рак.
Поздние стадии характеризуются поражением других органов:
- прорастание в соседние органы, образование межорганных свищей;
- гнойно-воспалительные процессы – парапроктит, флегмона малого таза;
- перфорация опухоли надампулярной локализации с развитием перитонита;
- кровотечение.
Как выглядит рак прямой кишки – фото
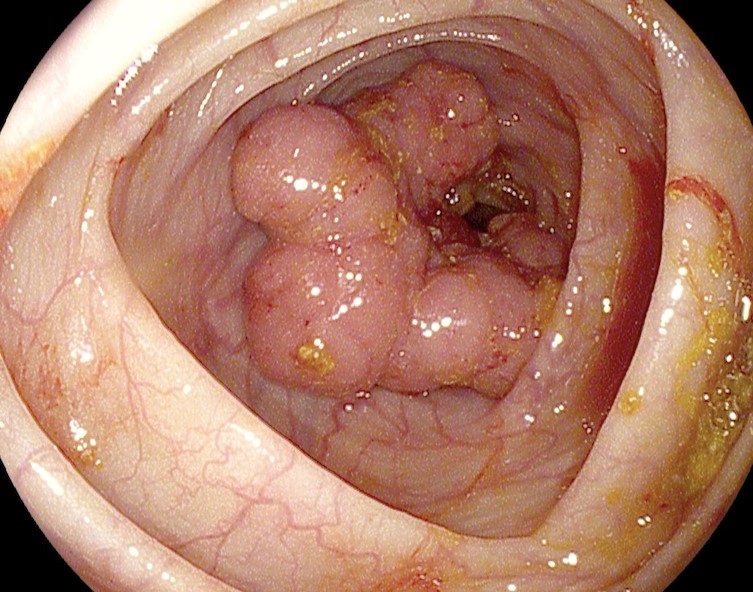
На фото рака прямой кишки можно заметить, что он значительно сужает просвет кишечника. Это является причиной запоров, переполненного живота, метеоризма.
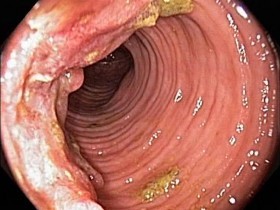
На этом фото карцинома растет инфильтративно, охватывая стенку.
Диагностика
После обращения к врачу, определяют симптомы, которые беспокоят пациента и позволяют предположить болезнь ректального отдела.
Стадии рака прямой кишки
Течение ракового процесса при отсутствии должного лечения прогрессирует. Стадия определяется по степени поражения самого кишечника, прорастанием ее через стенку, наличием метастазов в лимфоузлах, отдаленных поражениях других органов.
В связи с этим опухоли делят на 4 стадии. Такое распределение универсально для любых злокачественных опухолей.
1 стадия – опухоль небольших размеров, растет на слизистом слое, не поражает соседние органы и лимфоузлы.
2 стадия делится на А и Б. 2А – это поражение от трети до половины окружности кишечной трубки, но растет строго в стенке или просвете, метастазов нет. 2Б – размер очага такой же, но есть метастазы в околокишечных лимфоузлах.
3А – опухоль занимает более половины окружности кишки, прорастает через все слои и околокишечную клетчатку. Могут быть единичные метастазы в ближайших лимфоузлах.
3Б – любой размер опухоли, метастазы в отдаленных лимфоузлах, принимающих лимфу от ректальной области.
4 стадия – метастазы распространяются по внутренним органам и отдаленным лимфатическим узлам. Размер первичной опухоли может быть любой.
Методы лечения рака прямой кишки
Небольшой размер опухоли и ее прорастание только через слизистый и подслизистый слой прямой кишки, не затрагивая мышечный и серозный, позволяет выполнить хирургическое удаление самой опухоли. Иногда возможно проведение операции через кишку с помощью колоноскопа.
Если она проросла в мышечный слой, то показана резекция прямой кишки или экстирпация (полное удаление органа). Также удаляется параректальная клетчатка и лимфоузлы, в которых в 20% случаев уже обнаруживаются метастазы. Для проведения операции используют два доступа – лапаротомия (рассечение брюшной стенки) и лапароскопия (операция с помощью видеооборудования через несколько проколов на животе).
Тип операции выбирается исходя из локализации опухоли. Высокое расположение позволяет провести удаление новообразования и временно вывести конец кишки на брюшную стенку – сформировать колостому для дефекации. Такая манипуляция нужна, если пока сшить между собой концы кишки невозможно. Вторым этапом через некоторое время восстанавливают целостность кишечника.
При низком расположении опухолевого процесса, если ниже ее не осталось здоровых тканей, проводят удаление пораженного участка и анального отверстия, накладывают колостому на брюшную стенку.
Прогноз выживаемости
После проведения радикальной операции выживаемость в течение 5 лет колеблется в пределах 34-68%. На исход лечения влияет стадия, на которой была диагностировна опухоль, состояние самого пациента, его возраст, сопутствующие заболевания.
В зависимости от стадии опухолевого процесса, пятилетняя выживаемость определена следующими цифрами:
- 1 стадия – до 77%;
- 2 стадия – до 73%;
- 3 а стадия – 46%;
- 3 б стадия – 43%.
4 стадия не рассматривается в данной статистике. Радикальные операции зачастую провести невозможно, т.к. метастазы опухоли диссеминрованы по всему организму. Летальный исход зависит от общего состояния больного.
Противопоказания
Операция противопоказана при следующих условиях:
- тяжелые хронические заболевания пациента – артериальная гипертензия, ишемическая болезнь сердца, когда невозможно дать наркоз;
- преклонный возраст пациента;
- запущенные стадии рака.
При распространенном процессе с метастазированием во многие органы применяют паллиативные резекции, направленные на облегчение состояния больного. Симптоматические операции – наложение обходных анастомозов, чтобы разгрузить кишечник и избежать осложнений на последних стадиях рака.
Лечение до и после операции
Химиотерапия и лучевая терапия показаны для больных с опухолями 2 и выше стадиями.
Если до операции были выявлены метастазы в нескольких лимфоузлах, а опухоль проросла мышечный слой, то на этапе подготовки к операции проводят лучевую терапию коротким курсом в течение 5 дней. Это позволяет уничтожить ранние метастазы, уменьшить размер самого образования.
Лечение рака прямой кишки после хирургического вмешательства проводится после получения патоморфологических данных об удаленных тканях. Решается вопрос о проведении облучения или его сочетании с химиотерапией. Лучевая терапия после операции уничтожает оставшиеся клетки в зоне первичной опухоли и предупреждает ее рецидив. У неоперабельных больных она облегчает состояние.
Чувствительность к химиотерапии выявляется у 30% больных. Ее назначают с лечебной целью для уничтожения метастазов.
Также химиотерапию проводят адьювантно – для предупреждения распространения карциномы, если выявлялось поражение нескольких лимфоузлов. Этот способ терапии улучшает качество и продолжительность жизни пациентов с метастазами. Применяют препараты платины, 5-фторурацил, лейковарин, фолинат кальция. Лекарства вводятся внутривенно капельно, курсами по несколько дней. Также применяют химиотерапию в сочетании с лучевой до проведения операции при местнораспространенной форме рака. Такое комбинированное лечение проводят в течение 1-1,5 месяца, а после окончания облучения через 6 месяцев выполняют операцию.
Изобретение относится к медицине, а именно к онкологии, и касается способа лечения местнораспространенного рака прямой кишки.
Проблема лечения рака прямой кишки остается одной из самых актуальных и сложных в современной клинической онкологии и хирургии. Неуклонный рост заболеваемости раком прямой кишки сопровождается высоким уровнем смертности (J. Ferlay, Ε. Steliarova-Foucher, J. Lortet-Tieulent, S. Rosso, J.W.W. Coebergh, H. Comber, D. Forman, F. Bray, Cancer incidence and mortality patterns in Europe: Estimates for 40 countries in 2012, Eur J Cancer., 2013, 49, No 6, P. 1374-1403.). Заболеваемость раком прямой кишки в Российской Федерации за 10 лет возросла практически в 1,5 раза с 60,4 в 2001 году до 87,9 в 2011 году на 100 тыс.населения. Уровень летальности за этот период имеет тенденцию к снижению, хотя остается достаточно значительным - 35,1 и 27,7 на 100 тыс. населения соответственно [Давыдов М.И., Аксель Е.М. Статистика злокачественных новообразований в России и странах СНГ в 2009 г., Вестник РОНЦ им. Н.Н. Блохина РАМН, 2010, 23, №3].
Местнораспространенный рак прямой кишки характеризуется распространением за пределы мезоректального слоя (The Beyond ТМЕ Collaborative; Br J Surg. 2013 собр. 2 Jul; 100(8): 1009-14).
Лечение больных местнораспространенным раком прямой кишки осуществляется комбинированным способом с использованием предоперационной лучевой терапии, химиотерапии и последующим оперативным вмешательством (De Paoli Α., Chiara S., Luppi G. Capecitabine in combination with preoperative radiation therapy in locally advanced, resectable, rectal cancer: a multicentric phase II study. Ann. Oncol. 2006, Vol. 17, №2. p. 246-251; W Gollins, S Myint, S Susnerwala, В Haylock, M Wise, С Topham, L Samuel, R Swindell, J Morris, L Mason, and Ε Levine; Preoperative downstaging chemoradiation with concurrent irinotecan and capecitabine in MRI-defined locally advanced rectal cancer: a phase I trial (NWCOG-2) Br J Cancer. 2009 Sep 15; 101(6): 924-34).
Известен способ лечения местнораспространенного рака прямой кишки, включающий лучевую терапию СОД 60 Гр и химиотерапию терафуром и оксалиплатином. (Vestermark LW, Jensen НА, Pfeiffer P., High-dose radiotherapy (60 Gy) with oral UFT/folinic acid and escalating doses of oxaliplatin in patients with non-resectable locally advanced rectal cancer (LARC): a phase I trial, Acta Oncol. 2012 Mar; 51(3): 311-7).
Недостатки данного способа: наличие токсичности III и IV степени у 17% пациентов; радикальные операции выполнены у 83% пациентов, при этом полный лечебный патоморфоз выявлен у 33% пациентов.
Известен способ лечения местнораспространенного рака прямой кишки, включающий применение лучевой терапии СОД 50.4 Гр, фракциями по 2 Гр в сочетании с 5 фторурацилом и лейковорином. (Ferrigno, R., Р.Е. Novaes, et al. "Neoadjuvant radiochemotherapy in the treatment of fixed and semi-fixed rectal tumors. Analysis of results and prognostic factors." Radiat Oncol, 2006, 1: 5).
Наиболее близким к заявляемому способу (прототипом) является способ, включающий предоперационную дистанционную лучевую терапию: первые две фракции по 4 Гр, затем по 2 Гр пять дней в неделю до СОД 50 Гр, всего 24 сеанса и 3 курса химиотерапии оксалиплатином в дозе 130 мг/м 2 в первый день и капецитабином в дозе 1000 мг/м 2 два раза в день с 1 по 14 день. Первые два курса химиотерапии проводят одновременно с лучевой терапией, третий курс - после окончания лучевой терапии. Лечение проведено 36 пациентам, курс лечения занимает 8 недель. Оперативное вмешательство проводят через 5 недель после окончания предоперационной терапии (Gao YH1, Zhang X, An X, Cai MY, Zeng ZF, Chen G, Kong LH, Lin JZ, Wan DS, Pan ZZ, Ding PR., Oxaliplatin and capecitabine concomitant with neoadjuvant radiotherapy and extended to the resting period in high risk locally advanced rectal cancer; Strahlenther Onkol 2014, 190: 158-164).
Недостатки прототипа: наличие токсичности III и IV степени у 13,9% пациентов (радиодерматит, лейкопения и диарея); у 2 больных не проведен курс консолидирующей химиотерапии и хирургическое лечение отсрочено до 14 недель; полный лечебный патоморфоз у пациентов со стадией Т4 достигнут лишь у 1 (11,1%) из 9 пациентов, а со стадией Т3 у 12 (44,4%) из 27 пациентов.
Задачей заявляемого изобретения является создание эффективного способа лечения местнораспространенного рака прямой кишки с увеличением частоты полного лечебного патоморфоза и снижением степени токсичности.
Технический результат: заявляемый способ лечения местнораспространенного рака прямой кишки является более эффективным, позволяет добиться выраженного лечебного патоморфоза при Т3 и Т4 стадиях заболевания, обладает низкой степенью токсичности.
Поставленная задача решается тем, что предложен способ лечения местнораспространенного рака прямой кишки, включающий дистанционную конформную крупнофракционную лучевую терапию в сочетании с химиотерапией капецитабином и двух курсов консолидирующей химиотерапии оксалиплатином и капецитабином с последующим оперативным вмешательством.
Способ осуществляется следующим образом.
Проводят дистанционную конформную крупнофракционную лучевую терапию на область малого таза и зоны регионарного метастазирования течение 22 дней 3 раза в неделю РОД 4 Гр до СОД 40 Гр (в изодозе 56 Гр), всего 10 сеансов. Одновременно с лучевой терапией проводят курс химиотерапии капецитабином в дозе 850 мг/м 2 внутрь два раза в сутки с интервалом 12 часов. С интервалом в 7 дней проводят 2 курса консолидирующей химиотерапии оксалиплатином в дозе 130 мг/м 2 внутривенно капельно в первый день, капецитабином в суточной дозе 2000 мг/м 2 внутрь два раза в сутки с интервалом 12 часов, в течение 14 дней. Общая продолжительность лечения составляет 8 недель. Через 2 недели после окончания терапии проводят оперативное вмешательство.
Для оценки тяжести токсичности используют критерии CTC-NCIC и CTC-NCI version 2.0. В соответствии с данными критериями I (легкая) степень токсичности не влияет на качество жизни. II (умеренная) степень характеризуется функциональными нарушениями, не влияющими на активность больных. Токсичность III и IV (тяжелая и крайне тяжелая) степени характеризуются выраженными функциональными нарушениями, снижающими активность пациентов и ограничивающими своевременное проведение лечения (Gerard, J.P., D. Azria, et al. "Comparison of two neoadjuvant chemoradiotherapy regimens for locally advanced rectal cancer: results of the phase III trial ACCORD 12/0405-Prodige 2." J Clin Oncol; 2010, 28(10): 1638-1644.; Roh, M, G. Yothers, et al. "The impact of capecitabine and oxaliplatin in the preoperative multimodality treatment in patients with carcinoma of the rectum; 2011, NSABP R-04)
Изобретение иллюстрируется примерами 1 и 2
Пример 1. Пациент Π., 67 лет.
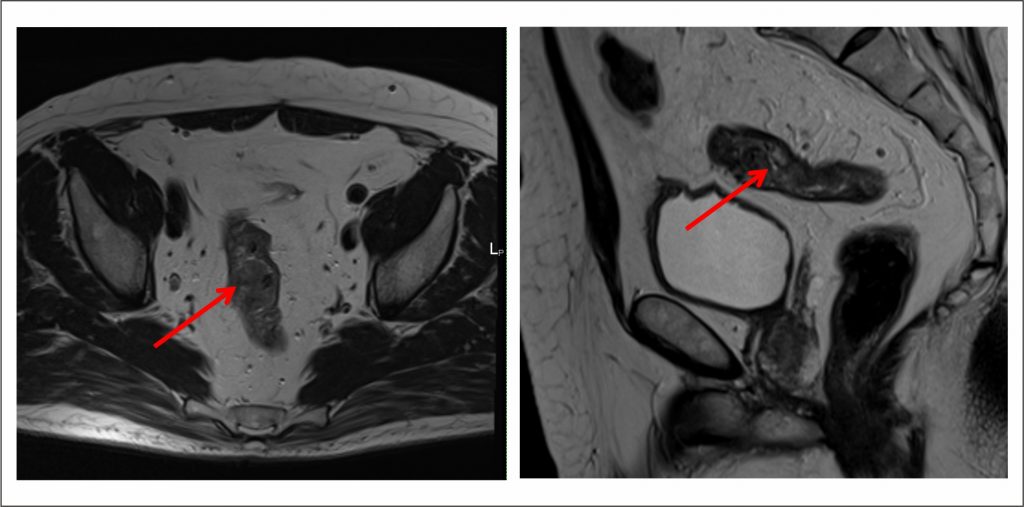
Клинический диагноз: Местнораспространенный рак прямой кишки верхнеампулярного отдела mrT4N2M0. Гистологический диагноз: умеренно дифференцированная аденокарцинома. При комплексном обследовании: определена опухоль на высоте 10 см от переходной анальной складки, циркулярно суживающая просвет кишки, подвижность ее ограничена. По данным МРТ: опухоль размерами 8,2×7,4 см, с инвазией тазовой брюшины, в параректальной клетчатке визуализированы множественные увеличенные лимфатические узлы до 0,8 см в диаметре.
В течение 22 дней 3 раза в неделю проведена лучевая терапия на область малого таза и зоны регионарного метастазирования РОД 4 Гр до СОД 40 Гр (изодоза 56 Гр). Одновременно с лучевой терапией пациент получал капецитабин внутрь в дозе 850 мг/м 2 с интервалом 12 часов, 2 раза в день. С интервалом 7 дней проведено 2 курса консолидирующей химиотерапии оксалиплатином в дозе 130 мг/м 2 внутривенно капельно в первый день и капецитабином в суточной дозе 2000 мг/м 2 внутрь два раза в сутки с интервалом 12 часов, в течение 14 дней.
Лечение проведено в планируемые сроки в полном объеме.
Общая продолжительность лечения составила 8 недель.
Токсичность II степени: диарея до 4 раз в сутки.
После завершения предоперационного этапа лечения проведено комплексное обследование.
По данным МРТ: фиброз в опухоли составлял более 50%, увеличилось расстояние до нижнего полюса опухоли с 10 см до 12 см без признаков инвазии тазовой брюшины, опухоль уменьшилась в размерах до 3,5×5,7 см, в параректальной клетчатке единичные лимфатические узлы до 0,5 см в диаметре.
Через 2 недели после окончания предоперационного лечения выполнено оперативное вмешательство - чрезбрюшная резекция прямой кишки.
При гистологическом исследовании операционного материала обнаружены участки выраженного фиброза без признаков опухолевого роста. Полная регрессия, IV стадия лечебного патоморфоза, в 2 лимфатических узлах параректальной клетчатки зарегистрирован полный лечебный патоморфоз IV стадии.
Пациент выписан из стационара через 12 суток после операции.
Пример 2. Пациентка М., 68 лет.
Клинический диагноз: Местнораспространенный рак прямой кишки нижнеампулярного отдела mrT3cN1M0.
Гистологический диагноз: Умереннодифференцированная аденокарцинома. При комплексном обследовании: определена опухоль на высоте 4 см от переходной анальной складки, циркулярно суживающая просвет кишки, подвижность ее ограничена. По данным МРТ: опухоль размерами 7,0×8,0 см, с инвазией мезоректальной фасции, в параректальной клетчатке единичные лимфатические узлы до 1 см в диаметре.
Проведена лучевая терапия на область малого таза и зоны регионарного метастазирования РОД 4 Гр до СОД 40 Гр течение 22 дней 3 раза в неделю. Одновременно с лучевой терапией пациент получал капецитабин внутрь в дозе 850 мг/м 2 с интервалом 12 часов, 2 раза в день. С интервалом в 7 дней проведено 2 курса консолидирующей химиотерапии оксалиплатином в дозе 130 мг/м 2 внутривенно капельно в первый день и капецитабином в суточной дозе 2000 мг/м 2 внутрь два раза в сутки с интервалом 12 часов в течение 14 дней.
Лечение проведено в планируемые сроки в полном объеме.
Суммарная очаговая доза предоперационного облучения составила 40 Гр, изодоза 56 Гр.
Общая продолжительность лечения составила 8 недель.
Токсичность II степени: диарея до 6 раз в сутки, купирована медикаментозно.
После завершения предоперационного этапа лечения проведено комплексное обследование.
По данным МРТ фиброз в опухоли составлял 50%, увеличилось расстояние до нижнего полюса опухоли с 4 см до 6 см без признаков инвазии мезоректальной фасции, опухоль уменьшилась в размерах до 4,0×5,0 см, в параректальной клетчатке единичные лимфатические узлы до 0,5 см в диаметре.
Через 2 недели после окончания предоперационного лечения выполнена брюшно-анальная резекция прямой кишки.
При гистологическом исследовании операционного материала: в прямой кишке на дне язвенного дефекта - разрастание фиброзной ткани без признаков опухолевого роста. Полная регрессия, IV стадия лечебного патоморфоза, в 10 лимфатических узлах параректальной клетчатки элементов опухоли не выявлено.
Пациентка выписана из стационара через 12 суток после операции.
Лечение по заявляемому способу проведено 18 пациентам с местнораспространенным раком прямой кишки. Полный лечебный патоморфоз опухоли при Т3 стадии достигнут у 37,5% и при Т4 стадии - у 40% пациентов. У 6 (33,3%) пациентов зарегистрирована токсичность II степени: диарея до 4-6 раз в сутки - у 22,2%, проктит - у 5,5% пациентов и сочетание диареи и проктита - у 5,5%. В течение последующих 12 месяцев не выявлено признаков прогрессирования заболевания.
Способ лечения местнораспространенного рака прямой кишки, включающий дистанционную лучевую терапию, химиотерапию капецитабином и оксалиплатином, консолидирующую химиотерапию с последующим оперативным вмешательством, отличающийся тем, что проводят конформную крупнофракционную дистанционную лучевую терапию в разовой очаговой дозе 4 Гр до суммарной очаговой дозы 40 Гр кратностью 3 раза в неделю, всего 10 сеансов; одновременно с курсом лучевой терапии проводят курс химиотерапии капецитабином в дозе 850 мг/м два раза в сутки внутрь с интервалом 12 часов; далее проводят 2 курса консолидирующей химиотерапии с интервалом 7 дней: оксалиплатином в дозе 130 мг/м внутривенно капельно в первый день каждого курса и капецитабином в суточной дозе 2000 мг/м внутрь два раза в сутки с интервалом 12 часов в течение 14 дней, с общей продолжительностью лечения 8 недель.
Читайте также:

