Лимфопролиферативные опухоли кожи вавилов pdf
В теле человека имеются не только кровеносные, но и так называемые "белые" сосуды. Известны они были довольно давно, а в середине 18 столетия знания о лимфатической системе стали более обширными. К сожалению, нередко встречаются лимфопролиферативные заболевания, а возникнуть они могут в любом органе.
Лимфатическая система
Она выполняет в функционировании человека довольно важную роль: благодаря лимфатической системе происходит транспортировка полезных веществ, удаляется лишняя межтканевая жидкость. Еще одна немаловажная способность – это обеспечение иммунитета. Жидкость, которая выполняет данные задания, называется лимфой. Она имеет прозрачный цвет, в составе преобладают лимфоциты. Самой небольшой структурной единицей системы являются капилляры. Они переходят в сосуды, которые бывают как внутриорганными, так и внеорганными. Их строение включает и клапаны, что предотвращают обратный ток жидкости. Самые большие лимфатические сосуды имеют название коллекторы. Именно в них накапливается жидкость от внутренних органов и других больших частей тела. Еще одна составляющая, которую имеет лимфатическая система (фото расположено внизу), – узлы. Это круглые образования, которые имеют разный диаметр (от полумиллиметра до 5 сантиметров). Расположены они группами на пути сосудов. Основная функция – фильтрация лимфы. Именно здесь она очищается от вредных микроорганизмов.
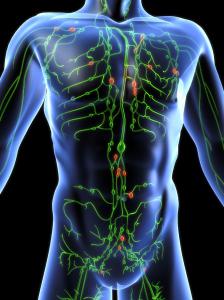
Лимфатические органы
Частью лимфатической системы человека являются также и следующие органы: миндалины, вилочковая железа (тимус), селезенка, костный мозг. Лимфоциты, которые формируются в тимусе, имеют название Т-клетки. Их особенностью является непрерывная циркуляция между лимфой и кровью. Частицы, которые образовываются в костном мозге, называются В-клетками. Оба типа после созревания разносятся по организму. В-клетки остаются в лимфоидных органах. На этом их миграция прекращается. В брюшной полости размещается еще один крупный орган, который является неотъемлемой частью лимфатической системы, – это селезенка. Состоит она из двух частей, одна из них (белая пульпа) генерирует антитела.
Лимфопролиферативное заболевание. Что это такое
Возможные причины возникновения
Среди причин, способных вызвать лимфоприлиферативные заболевания, выделяют определенную группу вирусов. Также не последнюю роль играет и фактор наследственности. Заболевания кожи, которые длятся значительное время (например, псориаз) могут спровоцировать рост злокачественных новообразований. Ну и, конечно, существенно влияет на данный процесс излучение. Радиация, некоторые аллергены, токсические вещества активизируют процесс разрастания клеток.
Лимфомы. Диагностика
Одна из разновидностей злокачественных новообразований лимфатической системы – это лимфома. Симптомы на начальных стадиях могут быть не сильно выражены.
Наблюдается увеличение лимфатических узлов, которые не являются болезненными. Еще один яркий признак – усталость, причем в довольно большой степени. Пациент может жаловаться на повышенную потливость в ночное время, значительную и резкую потерю массы тела. Возможен также и зуд, красные пятна. Температура тела иногда повышается, особенно по вечерам. Насторожить такие симптомы должны тогда, если они не исчезают спустя несколько недель. Для эффективного лечения очень важно определить тип лимфомы. При диагностике учитывают место расположения, внешний вид опухоли, вид белка, что находится на ее поверхности. Специалист назначает полное медицинское исследование, анализ крови на раковые клетки, проводится диагностика внутренних органов. Для большей информативности необходима биопсия. Под микроскопом пораженные клетки имеют специфический вид.
Лечение лимфомы
Методы лечения данного заболевания следующие. Для уничтожения новообразования используют химиотерапию или радиотерапию (с помощью рентгеновских лучей). Используется комбинация препаратов, они распространяются в организме и могут уничтожить также и те клетки, которые не удалось диагностировать. После проведения химиотерапии поражается и костный мозг, поэтому может понадобиться его пересадка. Осуществляют ее как из материала донора, так и непосредственно из собственного костного мозга пациента (предварительно его извлекают до начала процедур). Лимфопролиферативные заболевания поддаются и биологической терапии, но она носит преимущественно экспериментальный характер. Базируется на применении веществ, что синтезируются из клеток пациента. Для достижения хорошего результата необходимо тщательно следовать указаниям лечащего врача, вовремя принимать препараты, уделить должное внимание питанию.

Лейкоз. Клиническая картина
Заболевание характеризуется изменением кроветворных клеток, при котором происходит замещение здоровых элементов костного мозга на пораженные. В крови значительно повышается уровень лимфоцитов. В зависимости от того, какие клетки были перерождены, выделяют болезнь лимфолейкоз (изменения лимфоцитов), миелолейкоз (поражены миелоциты). Определить вид болезни можно под микроскопом и по анализу белка. Лимфопролиферативное заболевание (что это такое, было описано выше) имеет в данном случае две формы протекания: хроническую и острую. Последняя проходит довольно тяжело. В этом случае необходимо незамедлительное лечение, так как клетки незрелые и не способны выполнять свои функции. Хроническая форма может длиться немало лет.
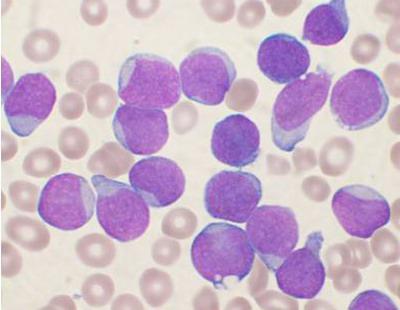
Хронические лимфопролиферативные заболевания
У людей старшего возраста нередко диагностируют хронический лимфолейкоз. Болезнь протекает довольно медленно, и только на поздних стадиях наблюдаются нарушения в процессе образования крови. К симптомам можно отнести увеличение лимфоузлов и селезенки, частые инфекционные заболевания, потерю веса, потливость. Нередко такие лимфопролиферативные заболевания обнаруживают случайно.
Актуальной и важной проблемой в дерматологии является своевременная нозологическая диагностика заболеваний кожи, что в условиях наблюдаемого патоморфоза хронических дерматозов, таких как псориаз, атопический дерматит, хроническая экзема, представляется сложной задачей для специалиста-дерматовенеролога [4, 18].
Особенно сложной и ответственной задачей представляется диагностика лимфопролиферативных заболеваний кожи, когда установление правильного диагноза злокачественной лимфомы определяет путь к назначению специфической терапии, предотвращает прогрессирование процесса, в том числе с развитием летальных стадий заболевания [7]. Определение локализации и биологической сущности неопластического процесса у пациентов с лимфомами кожи является ключевым моментом, так как в большинстве случаев первичные лимфомы кожи (ПЛК) и их системные аналоги имеют сходные гистологические, иммунологические и генетические признаки, но при этом характеризуются различным течением и требуют разных подходов в лечении [23, 29, 30].
ПЛК кожи составляют до 2,0 % от всех кожных заболеваний дерматологического профиля, по частоте встречаемости занимают второе место среди экстранодальных лимфом и представлены в подавляющем большинстве опухолевыми пролифератами в коже, состоящими из Т-лимфоцитов, то есть Т-клеточными лимфомами кожи (ТКЛК) [7, 8, 25].
Дифференцировать ТКЛК необходимо, в первую очередь, с тяжелыми формами атопического дерматита в его взрослой фазе развития, почесухой взрослых, хронической экземой, псориазом и парапсориазами, вторичными эритродермиями. Детальное изучение кожных поражений при ПЛК на различных этапах наблюдения за больными в процессе клинического мониторирования, выявление диагностически значимых симптомов, сопоставление их с таковыми при хронических доброкачественных дерматозах, позволяет разработать алгоритм дифференциальной диагностики между данными заболеваниями, что имеет значение в связи с существенными различиями в тактике ведения больных с лимфомами кожи и хроническими дерматозами [21].
Гистологические исследования биоптатов кожи выполняются в наиболее сложных случаях, в частности, при подозрении на наличие лимфопролиферативного процесса. Возможность установления диагноза ПЛК только клиническими методами не превышает 50,0 %, при использовании гисто- и цитоморфологических методов, при повторных в динамике заболевания гистологических исследованиях точность диагностики увеличивается лишь до 75,0 %. Изучение иммунологических характеристик клеток, составляющих субстрат болезни в коже, то есть иммунофенотипирование (ИФТ) клеточного пролиферата повышает возможность диагностики лимфом кожи до 90,0 %, является обязательным дополнением к клиническим и гистологическим данным, значительно расширяющим возможности ранней диагностики ПЛК [10, 14, 25].
Тарасенко Ю.Г. в диссертационном исследовании, выполненном в 2008 г. показала, что совпадение диагнозов, поставленных врачами при первичном осмотре и после полноценного обследования больных с подозрением на лимфопролиферативные заболевания кожи, имело место только в 1/3 случаев. Диагноз ТКЛК был подтвержден у 17,9 % больных. С другой стороны, ПЛК выявлены у 2/3 больных с предварительными диагнозами хронических доброкачественных дерматозов. Наиболее часто ТКЛК имитировали: эритродермическая форма псориаза (76,9 %), бляшечный парапсориаз (77,8 %), атопический дерматит в форме эритродермии Хилла (57,1 %), распространенная истинная экзема (50,0 %) и почесуха взрослых (50,0 %). Диагноз псевдолимфом кожи подтвержден у 2/3 больных. ТКЛК почти в половине случаев (46,4 %) диагностировались на поздних стадиях (III и IV). Преобладали больные с ГМ (87,8 %), при этом классическая форма лидировала и была диагностирована у 41,7 % пациентов. Наибольшая продолжительность диагностического периода наблюдалась при пойкилодермической форме ГМ (101,7 ± 25,9 мес.) и была в 2 раза короче при классической форме, в 3 раза – при эритродермической. Отмечается, что характерными для ТКЛК являются следующие иммунофенотипические маркеры: CD3+, CD4+, CD5+, CD8-, CD20-, CD25-; для В-клеточных лимфом кожи (ВКЛК) – CD20+, CD22+, CD37+, CD38+. Автор считает, что ИГХ-метод диагностики ПЛК наиболее информативен и позволяет поставить диагноз уже на ранней стадии заболевания, при этом его высокая стоимость оправдана, так как затраты на выполнение ИГХ-анализа кожи соизмеримы со стоимостью нерациональной терапии при неправильно поставленном диагнозе [21].
Учитывая необходимость комплексного подхода к постановке диагноза ПЛК, включающего использование клинического, пато- и иммуноморфологического методов, основанных на стандартизованных фактических данных, актуальным является внедрение в медицину математических методов анализа и создание компьютерных программ, позволяющих своевременно диагностировать данную группу заболеваний [1, 2].
В большинстве представленных в печати современных работ в той или иной мере используются количественые методы исследований. Так, для ранней диагностики лимфом кожи Тарасенко Ю.Г. (2008 г.) разработана математическая модель на основе нейронной сети. Применение ее на практике позволило сократить продолжительность диагностического периода при ТКЛК на 6,7 мес., при В-клеточных лимфомах – на 5,4 мес. Увеличилось в 1,4 раза количество больных ТКЛК (77,8 %), диагностированных на II стадии заболевания [21].
Белоусова И.Э. (2010) подчеркивает, что количественные оценки диагностической значимости клинических, гистологических, иммуногистохимических и молекулярно-биологических признаков отдельных форм лимфопролиферативных заболеваний кожи позволяют дифференцировать их в группах заболеваний сходной клинической картины и/или гистологического строения [3].
В работах Скрек С.В. (2011), Разнатовского К.И. и соавт. (2012) обозначены приоритеты в применяемых методах диагностики. Авторы считают, что морфологический (гистологический и ИГХ) метод исследования является наиболее информативным в лабораторной диагностике ПЛК и позволяет верифицировать диагноз у 69 % больных первичными ТКЛК и у 78 % больных первичными ВКЛК. Кроме того, авторы полагают, что ИГХ-метод диагностики может быть рекомендован для прогнозирования течения ГМ; о наличии опухолевой прогрессии и трансформации ГМ может свидетельствовать появление абберантного фенотипа Т-лимфоцитов. При этом диагностический алгоритм для выявления больных ПЛК на разных стадиях заболевания должен состоять из совокупной оценки данных клинического, гистологического и ИГХ исследований, лишь в некоторых случаях, (таких как подозрение на синдром Сезари) этот комплекс должен быть дополнен ПЦР [17, 19].
Остаются мало исследованными вопросы дифференциальной диагностики лимфом кожи и парапсориазов. До настоящего времени неясно, является ли мелкобляшечный парапсориаз воспалительным дерматозом, который имеет потенциал развития в ГМ, или представляет собой форму ГМ [22]. Дифференциальная диагностика между пятнистой стадией ГМ и крупнобляшечпым парапсориазом представляет объективные трудности, отличить заболевания по клиническим, гистологическим и ИГХ признакам практически невозможно. Отсутствуют критерии, позволяющие прогнозировать трансформацию крупнобляшечного парапсориаза в лимфому кожи [25].
Жуковым А.С., Белоусовой И.Э. и соавт. (2014) представлены результаты изучения пролиферативной активности лимфоцитов в коже больных ГМ и бляшечным парапсориазом. Установлено, что коэффициент эпидермо-дермального отношения пролиферативной активности клеток (Ki-67 +) кожи у больных ГМ всех стадий ниже, чем у здоровых людей и пациентов с парапсориазом. Индекс пролиферативной активности клеток при ГМ бляшечно-опухолевой стадии выше, чем у больных бляшечным парапсориазом. Количество CD3 + Ki-67 + клеток у больных ГМ пятнистой и бляшечно-опухолевой стадии выше, чем у здоровых и пациентов с бляшечным парапсориазом. Авторы считают, что на современном этапе остается актуальной проблема поиска новых ИГХ-маркеров и методов оценки их экспресии [22].
Известно, что уровень экспрессии Ki-67 увеличивается при прoгрессировании ГМ [28]. B статье Олисовой О.Ю., Грабовской О.В. и др. (2013 г.) приведено описание клинического наблюдения ТКЛК. Показана сложность диагностики в связи с полиморфизмом клинической картины, имитирующей различные хронические заболевания кожи: на протяжении 3 лет заболевание кожи у женщины 77 лет напоминало клиническую картину красной волчанки, саркоидоза, многоформной экссудативной эритемы, проявляясь различной пятнисто-бляшечной сыпью. Лишь при появлении узловых высыпаний была диагностирована ТКЛК, подтвержденная ИГХ-исследованиями с применением моноклональных антител CD3, CD4, CD5, CD8, CD20 и Ki-67. Индекс пролиферации в данном наблюдении составил 55,4 % [20].
Автоматизированная и стандартизированная оценка результатов ИГХ-анализа биоптатов кожи, основанная на прецизионной квантифицированной колорометрии, открывает широкие возможности перспективных научных исследований по данной тематике с расширением базы знаний в области своевременной диагностики редко встречающихся форм лимфом кожи, их онкогенного потенциала; изучения патогенеза развития ПЛК на основании количественных подходов в оценке выраженности, структуры и цитоархитектоники эпидермальной и дермальной лимфоидной инфильтрации, выявлении характера и выраженности активности пролиферативных и оппозитных процессов (готовность к апоптозу, свершившийся апоптоз, локальная клеточная цитотоксичность) и разработка на основании полученных данных прогностических критериев течения ПЛК, адекватности применяемой терапии.
Таким образом, к настоящему времени общепризнано, что наряду с клиническими наблюдениями ИГХ-метод является наиболее важной составляющей комплексных исследований при установлении диагноза лимфопролиферативных заболеваний кожи. Использование количественной оценки данных иммунофенотипирования клеток позволяет объективизировать диагностический процесс, что соотносится с современными критериями доказательной медицины и положительно влияет на своевременность и точность постановки диагноза, а также открывает новые возможности в изучении фундаментальных вопросов возникновения и прогрессирования злокачественной лимфопролиферации в коже.

Рекомендуемые книги

Готовим с Еленой Прохорчук

Тридцать миллионов слов. Развиваем мозг малыша, просто беседуя с ним
Дана Саскинд, Лесли Левинтер-Саскинд, Бет Саскинд

Человек уставший: Как победить хроническую усталость и вернуть себе силы, энергию и радость жизни

Завтрак у Тиффани


Скретч карта мира My Map Chocolate edition (eng)


Homo Sapiens. Преходящий феномен

Язык программирования C. Лекции и упражнения

Загальна психологія. Теоретичний курс. Навчальний поcібник

Мозг. Инструкция по применению. Как использовать свои возможности по максимуму и без перегрузок

Психология стимулирования персонала. Современные решения

Активное продвижение. Тренинг. Игры и упражнения


Дельфины капитализма. 10 историй о людях, которые сделали всё не так и добились успеха

Изучаем JavaScript: руководство по созданию современных веб-сайтов

Найбагатший чоловік у Вавилоні

Класична листівка Ти котик!

Культ домашней еды: Завтраки, обеды, ужины

Опис України Г.Л. де Боплан. Українські козаки; Богдан Хмельницький Проспер Меріме
Гійом Левассер де Боплан

Алгоритмы. Справочник с примерами на C, C++, Java и Python
Джордж Хайнеман, Гэри Поллис, Стэнли Селков

Торговые войны: Битва за успех на прилавках и онлайн
Ричард Бэндлер, Джон Гриндер

Введение в анализ алгоритмов

Творческий приступ. Автобиографическая драма-раскраска о счастье, вдохновении, взлетах и падениях, отчаянии и надежде (в 30 актах)

Исследование о природе и причинах богатства народов.Книги 1–3

Чудове чудовисько. Комплект з 3-х книг

Когда бог был кроликом

Аудит продажу. Дистрибуція
Олесь Піщак, Дмитро Горлін, Асан Бекіров, Іван Даніленко

Как зарабатывать деньги в интернете

Найкращі народні казки: книга 1: Колобок. Колосок. Лисиця і журавель. Їжак та заєць. Цап та баран. Солом’яний бичок. Казка про Івасика-Телесика

Крупномасштабное машинное обучение вместе с Python
Бастиан Шарден, Лука Массарон, Альберто Боскетти

101 совет как пройти собеседование


Жінки, що біжать з вовками. Архетип Дикої жінки у міфах та легендах
Кларисса Пинкола Эстес

Все на борт! Игра на развитие памяти для юных пиратов

Чорнобиль. Історія ядерної катастрофи


Міні листівка I LOVE YOU красное сердце

Як прокласти залізницю

Міні листівка Я дуже сильно тебе кохаю
Книги из категории "Медицинская литература"

Лекарственные средства в педиатрии (т)

Нейронауки для чайников


Что не так в здравоохранении? Мифы. Проблемы. Решения

Великие лекарства: В борьбе за жизнь

Криве дзеркало життя. Головні міфи про рак і що сучасна наука думає про них

40 феноменов Болотова




Основы дистанционного зондирования. Изд.2

Внутрішня історія. Серце - найважливіший орган нашого тіла
Йоганнес Гінріх фон Борстель

Пандемия: Всемирная история смертельных вирусов


Дэвид Леви, Джоэл Килпатрик

Жизнь взаймы: Рассказы врача-реаниматолога о людях, получивших второй шанс

Неестественные причины. Записки судмедэксперта: громкие убийства, ужасающие теракты и очень запутанные дела

Код диабета.Научные данные о том, как диабет 2 типа стал самой "внезапной" болезнью столетия и простая программа восстановления без инъекций и лекарст

Протокол лечения больных экстранодальной лимфомой из клеток маргинальной зоны
пей иммуноглобулинов, что свидетельствует о постфолликулярном про исхождении этих опухолей. При некоторых из них обнаруживается сдвиг изотипа. Наиболее часто соматические гипермутации затрагивают се мейства V H4 , V H3 и V H1 . Известно, что гены именно этих регионов заинте ресованы в аутоантителообразовании, в частности в синтезе холодовых агглютининов, ревматоидного фактора и антител к нативной ДНК, что может служить свидетельством происхождения экстранодальных лим фом из клеток маргинальной зоны из аутореактивных В клеток. В гер манском исследовании по изучению репертуара генов IgV H MALT лим фом орбиты соматические мутации были выявлены в 8 случаях из 8, 6 из них — с участием семейства V H3 , причем в половине случаев был задейст вован сегмент V H3 23 с признаками внутриклоновой гетерогенности [1]. Хотя антигенная специфичность сегмента V H3 23 в отношении MALT лимфомы орбиты неизвестна, V H3 23 часто вовлечен в процесс соматиче ской гипермутации аутореактивных В клеток при ревматоидном артрите и гранулематозе Вегенера. Внутриклоновая гетерогенность свидетельст вует о продолжающемся процессе гипермутации. Предполагают, что этот процесс идет в ходе рециркуляции В клеток в герминативных цен трах, аналогично происходящему при нормальных иммунологических реакциях. Этот факт рассматривается как косвенное доказательство уча стия антигенной стимуляции в развитии MALT лимфом.
Цитогенетические нарушения, характерные для экстранодальной лимфомы из клеток маргинальной зоны, включают как структурные, так и количественные хромосомные аберрации. В структурные перестройки чаще всего вовлекаются локусы генов MALT1, API2, BCL10, FOXP1, тя желых и легких цепей иммуноглобулинов. Результатом большинства та ких перестроек является активация NF κB — ядерного транскрипцион ного фактора, играющего центральную роль в реакциях иммунного отве та, клеточной пролиферации и дифференцировки. В физиологических условиях активация NF κB происходит после контакта с антигеном при непосредственном участии MALT1 и BCL10. Патогенетический меха низм транслокаций, выявляемых при экстранодальных ЛМЗ, таких как t(11;18), t(1;14), t(14;18), и, вероятно, трисомии по 18 й хромосоме свя зан с физиологической ролью BCL10 и MALT1 в антигензависимой ак тивации NF κB.
Транслокация t(11;18)(q21;q21)/ API2 MALT1 специфична для экст ранодальной MALT лимфомы и не обнаруживается при других видах лимфом из клеток маргинальной зоны — селезеночной и нодальной. Эта перестройка с высокой частотой выявляется при локализации опухоли в желудке (22%), легочной ткани (42%), кишечнике (15%), реже — при по ражении орбиты (до 10%) [2]. Прогностическое значение транслокации t(11;18)(q21;q21) при MALT лимфомах различных локализаций, несу щих эту хромосомную перестройку, точно не установлено, но в t(11;18) позитивных MALT лимфомах гораздо реже выявляются микро

сателлитные альтерации, часто встречающиеся в негативных по этой транслокации случаях. Отсутствие дополнительных хромосомных абер раций может отчасти объяснить тот факт, что t(11;18) позитивные MALT лимфомы характеризуются меньшей частотой крупноклеточной трансформации. Вместе с тем наличие транслокации ассоциируется с да леко зашедшими стадиями и неэффективностью антибактериальной те рапии.
Частота выявления транслокации t(14;18)(q32;q21)/ IGH MALT1 в экстранодальной ЛМЗ составляет от 3 до 40% [3]. Прогностическое зна чение не установлено.
Транслокация t(1;14)(p22;q32)/ BCL10 IGH и ее вариант t(1;2)(p22;p12)
встречаются в 1—2% MALT лимфом с локализацией преимущественно в желудке, легких, коже, слюнных железах, крайне редко — в орбите. В слу чаях с этой транслокацией нередко выявляются дополнительные хромо сомные аберрации, а стадия заболевания обычно более IE [4].
Трисомия по 18 й хромосоме при MALT лимфомах орбиты втречается в 37—56% случаев. Основным патогенетическим механизмом при этой аберрации считается гиперэкспрессия MALT1 за счет увеличения коли чества копий гена с последующей активацией NF κB. Косвенным под тверждением этому могут служить случаи выявления MALT лимфомы с двумя хромосомами 18, но тремя копиями локуса 18q21. Появление три сомии по 18 й хромосоме на более поздних этапах развития лимфомы согласуется с менее благоприятным прогнозом у этих больных и отража ет трансформацию опухоли, морфологически проявляющуюся увеличе нием количества крупных опухолевых клеток [5].
Трисомия по 3 й хромосоме — одна из самых частых хромосомных аберраций, выявляемых при экстранодальных лимфомах из клеток мар гинальной зоны. В частности, при первичном поражении орбиты трисо мия по 3 й хромосоме обнаруживается в 12—68% случаев [5]. На сего дняшний день существуют только теоретические предположения отно сительно участия в лимфомогенезе некоторых генов, расположенных на 3 й хромосоме и участвующих в активации лимфоцитов и реакциях им мунного ответа. Точные патогенетические механизмы онкогенеза при этой хромосомной аберрации пока неизвестны. Прогностическое значе ние трисомии по 3 й хромосоме также не определено.
Транслокация t(3;14)(p14.1;q32)/ FOXP1 IgH выявлена недавно Streu bel с соавт. в 20% MALT лимфом орбиты [6]. FOXP1 входит в семейство генов, кодирующих транскрипционные факторы, выполняющих в клет ках различные функции в зависимости от их тканевой принадлежности. В В лимфоцитах он регулирует экспрессию рекомбиназ Rag1 и Rag2, инициирующих рекомбинации V(D)J. Тем не менее его роль в лимфомо генезе пока точно не определена. Продукт этого гена, белок FOXP1 (fork head box protein P1), при иммуногистохимическом исследовании выяв ляется как при MALT лимфомах, так и при экстранодальных диффуз ных В крупноклеточных лимфомах с полисомией. Есть данные, свиде тельствующие о низкой выживаемости больных крупноклеточной лимфомой, гиперэкспрессирующей FOXP1 [7].

Протокол лечения больных экстранодальной лимфомой из клеток маргинальной зоны
Начальные стадии заболевания трудноотличимы от реактивной ги перплазии лимфоидной ткани, вызванной хронической антигенной сти муляцией. Дополнительным дифференциально диагностическим кри терием является эффективность эмпирической антибактериальной те рапии, назначаемой с учетом выделенного возбудителя или локализации процесса.
В случаях неэффективности антибактериальной терапии, а также при антигеннезависимых ЛМЗ унифицированного подхода к лечению в на стоящее время не существует. При локальных стадиях чаще всего ис пользуется лучевая терапия, а при мультифокальном поражении — раз личные программы химиотерапии.
Локальные методы воздействия
Хирургическое лечение. Хирургический метод при экстранодальных лимфомах редко используется с лечебной целью. Большинством авторов отмечается высокая частота рецидивов при отсутствии дополнительного лечения после иссечения опухоли. Поэтому оперативное вмешательство необходимо только для биопсии и не имеет целью радикальное удаление опухоли.
Локальная лучевая терапия может использоваться у пациентов с I ста дией заболевания. Эффективность этого вида терапии довольно высо кая — пятилетняя безрецидивная выживаемость достигает 80%. Однако при ее выборе необходимо учитывать вероятность развития постлучевых реакций и осложнений, а также вовлечение в зону облучения соседних органов с нарушением их функций. Так, при первичном локальном по ражении орбиты лучевая терапия (дистанционная гамма терапия) со провождается развитием различных видов постлучевых реакций и ос ложнений у 50—70% больных; некоторые из них значительно снижают качество жизни (катаракта, ксерофтальмия, постлучевая ретинопатия и др.). В то же время метод аппликационной бета терапии позволяет облу чать пораженные участки конъюнктивы с минимальной лучевой нагруз кой на соседние здоровые структуры глаза и орбиты: на глубине 3 мм суммарная доза составляет 25% от поверхностной, а на глубине 5 мм — только 1%. При проведении дистанционной гамма терапии в случаях ЛМЗ желудка в зону облучения попадает левая почка, что чревато разви тием радиационного нефрита или гипертонии почечной этиологии. Об лучение легких сопровождается возникновением лучевого пульмонита, головного мозга (при ЛМЗ мозговых оболочек) — отеком и лучевым нек розом ткани мозга, органов малого таза (при ЛМЗ кишечника, репродук тивных органов) — постлучевыми циститами, проктитами, формирова нием мочеточниково влагалищных и мочеточниково абдоминальных свищей и др. В то же время при ЛМЗ кожи или мягких тканей возникаю щие в процессе облучения реакции не приводят к формированию серьез ных осложнений, и локальное облучение очага в этих случаях может рас сматриваться в качестве терапии выбора.

Мультифокальная ЛМЗ или локальная ЛМЗ, при которой локальная лучевая терапия сопряжена с высоким риском постлучевых осложнений, требует проведения системной терапии.
Исследований, оценивающих эффективность химиотерапии при первичных экстранодальных лимфомах из клеток маргинальной зоны, крайне мало. Они преимущественно посвящены использованию алки лирующих агентов или аналогов пуриновых оснований в качестве моно терапии или в комбинации с другими препаратами. На монотерапии хло рамбуцилом общий ответ достигает 100%, частота полных ремиссий — 79% при пятилетней безрецидивной выживаемости 60% [8]. Похожие ре зультаты получены при использовании аналогов пуриновых оснований в терапии экстранодальных ЛМЗ различных локализаций — в частности, при лечении кладрибином частота полных ремиссий составляет 84% [9]. Ритуксимаб в монорежиме малоэффективен — получаемые ремиссии обычно неполные, а рецидивы возникают в короткие сроки.
Комбинированная терапия позволяет улучшить результаты, при этом эффективность программ химиотерапии, базирующихся на алкилирую щих препаратах, значительно уступает курсам ПХТ, включающим ана логи пуринов. В частности, использование хлорамбуцила совместно с ритуксимабом позволяет получить полные ремиссии у 8 из 9 пациентов [10]; комбинация циклофосфамида, винкристина и преднизолона (CVP) обеспечивает только 76,2% полных ремиссий [11]. В то же время Zinzani с соавт. показано преимущество флударабин содержащих курсов FM (флударабин + митоксантрон) перед химиотерапией по программе СVР
в лечении экстранодальных MALT лимфом [12].
В Гематологическом научном центре лечение пациентов с экстрано дальной лимфомой из клеток маргинальной зоны с 2004 г. проводится по программе FMC (с ритуксимабом или без него). Большинство случаев представлено ЛМЗ мягких тканей орбиты и конъюнктивы (52 пациента), 2 случая — ЛМЗ легких, 2 случая — сочетанным поражением мягких тка ней орбиты и легких, 1 случай — ЛМЗ молочной железы. Трем пациен там (двум с поражением кожи и одному с поражением мягких тканей) проведена локальная лучевая терапия. У большинства пациентов полу чен полный ответ и сохраняются ремиссии заболевания (сроки наблюде ния от 3 месяцев до 10 лет). У трех больных с ЛМЗ конъюнктивы после терапии по программе FMC (без ритуксимаба) отмечено развитие ло кального рецидива. В двух случаях получены повторные ремиссии на брахитерапии, в третьем — полный ответ на монотерапии ритуксимабом. Полученные данные свидетельствуют о необходимости особого подхода к лечению больных ЛМЗ конъюнктивы. Использование высокоэффек тивной и малотоксичной аппликационной бета терапии (брахитерапии) представляется наиболее разумной и рациональной терапией первой ли нии больных ЛМЗ этой локализации. Применение химиотерапии при ЛМЗ конъюнктивы оправдано при мультифокальном поражении и в случаях развития рецидива.

Протокол лечения больных экстранодальной лимфомой из клеток маргинальной зоны
Несмотря на высокую эффективность программы FMC, высокая вероятность развития вторичных миелодисплазий и острых лейкозов вследствие комбинированной терапии лейкозогенными цитостатиче скими препаратами ограничивает ее применение, особенно у молодых больных. В этой связи представляется необходимым дальнейший по иск высокоэффективной и малотоксичной терапии лимфом из клеток маргинальной зоны. Для реализации этой задачи работа может вес тись по двум направлениям. Первым является изучение возможности снижения токсичности лечения за счет уменьшения количества про тивоопухолевых препаратов (исключение митоксантрона из курса FMC) и длительная поддерживающая иммунотерапия моноклональ ными антителами к CD20 (ритуксимаб). Второе направление — ис пользование препаратов с принципиально новым механизмом дейст вия, обладающих низкой токсичностью. Среди таких препаратов рас сматривается бендамустин, представляющий собой гибрид пуриново го аналога и алкилирующих препаратов. Многими исследованиями продемонстрирован синергизм бендамустина и ритуксимаба в лече нии не только первичных, но и рефрактерных и рецидивных зрелокле точных лимфом [13, 14].
С целью повышения эффективности терапии и уменьшения ее мест ных и системных токсических эффектов предлагается протокол лечения больных экстранодальной лимфомой из клеток маргинальной зоны.
Протокол лечения больных экстранодальной лимфомой из клеток маргинальной зоны
Критерии диагноза экстранодальной лимфомы из клеток маргинальной зоны
1. Клинические данные: наличие опухолевого поражения любого не лимфоидного органа.
2. Гистологическое строение, характеризующееся инфильтратом из центроцитоподобных лимфоидных клеток и/или малых лимфоцитов без выраженных признаков клеточной атипии с наличием лимфоэпи телиальных повреждений, колонизацией реактивных фолликулов и плазматической дифференцировкой. Однако отсутствие среди гисто логических признаков опухоли лимфоэпителиальных повреждений и реактивных лимфоидных фолликулов не противоречит диагнозу MALT лимфомы.
3. Экспрессия В ассоциированных антигенов CD20, CD79а с отсутст вием экспрессии дифференциально диагностических маркеров CD5, CD10, CD23, CD43 в типичных случаях. Индекс пролиферативной активности не превышает 20%. Иногда может встречаться экспрессия CD5, СD10 или СD23, при этом проводится цитогенетическое иссле дование для исключения лимфомы из клеток мантийной зоны, фол ликулярной лимфомы и лимфомы из малых лимфоцитов.

4. Отсутствие генерализованной лимфаденопатии и спленомегалии, до пускается вовлечение регионарных лимфоузлов.
Критерии включения в протокол
1. Диагноз первичной экстранодальной лимфомы из клеток маргиналь ной зоны независимо от количества первичных очагов поражения и вовлечения костного мозга.
2. Возраст 18—70 лет.
Критерии исключения из протокола
1. Трансформация в диффузную В крупноклеточную лимфому.
2. Тяжелая сопутствующая патология, не связанная со специфическим поражением органов:
почечная недостаточность (уровень сывороточного креатинина более 200 мкмоль/л); печеночная недостаточность и острый гепатит (с признаками цито
лиза и белково синтетической недостаточности: уровень сывороточ ного билирубина более 1,5 нормы, активность аминотрансфераз бо лее 3 норм, протромбиновый индекс менее 70%, альбумин менее 30 г/л); легочная патология (ХОБЛ, пневмония), сопровождающаяся дыха
тельной недостаточностью (одышка более 26 в минуту, гипоксемия — P a O 2 менее 80 мм рт. ст.).
3. Тяжелые психические нарушения.
4. Декомпенсированный сахарный диабет.
Если в ходе симптоматической терапии удалось купировать указан
ные состояния, то пациент может быть включен в исследование по про токолу.
Дизайн протокола (рис. 1)
1. При локальных стадиях в случаях предполагаемого антигензависимо го механизма развития опухоли проводится курс эрадикационной ан тибактериальной терапии:
При ЛМЗ желудка — четырехкомпонентная схема эрадикации Helico
ингибитор протонного насоса 2 раза в сутки (омепразол, 40 мг/сут, или рабепразол, 20 мг/сут);
висмута трикалия дицитрат (Де Нол), по 1 таблетке (120 мг) за 30 ми нут до еды 4 раза в сутки;
кларитромицин, 500 мг 2 раза в сутки;
амоксициллин, 1000 мг 2 раза в сутки, или метронидазол, 500 мг 2 раза в сутки.
Продолжительность лечения 7—10 дней.

Протокол лечения больных экстранодальной лимфомой из клеток маргинальной зоны
Экстранодальная лимфома из клеток маргинальной зоны
Читайте также:

