Лекарство от рака нано

В современной медицине нет таблетки, которая действует напрямую на какое-либо заболевание. В идеале лекарство должно попадать только в больные клетки, не нанося вреда здоровью других, но на деле отличить больную клетку от здоровой очень сложно. Яркий пример — химиотерапия при раке. Чтобы облучить больные клетки, приходится жертвовать и здоровыми, поэтому лечение так тяжело дается.
Почему отличить сложно? Большинство лекарств замечает только одно несоответствие в сигналах клетки, однако оно может быть и в здоровом соединении.
С этой проблемой борется группа ученых из подмосковного МФТИ и Института общей физики РАН. Они смогли создать умный материал, который анализирует полностью всю клетку и ее окружение, причем обладают сверхчувствительностью.

Ведущий научный сотрудник лаборатории нанобиотехнологий МФТИ делает тестовые полоски для ДНК-теста. Источник фото: МФТИ
Нет, ученые не придумали лекарство, которое сразу выявляет проблему и лечит ее за считаные секунды. Они лишь приблизились к созданию такого препарата. Пройдут десятилетия, прежде чем на его основе можно будет выпускать лекарства.
Общепринятые способы доставки лекарств напоминают письмо с указанием города и улицы, но без номера дома и квартиры. Для эффективной доставки нужно уметь анализировать больше параметров

Аспирантка МФТИ готовит образцы для проверки. Источник фото: МФТИ
Вообще, ДНК-тест помогает узнать о заболеваниях, которые пока никак себя не проявили, но могут вдруг проснуться. Анализ показывает предрасположенность к каким-то болезням, помогает определить причину неясных симптомов, открывает глаза на непереносимость тех или иных препаратов. ДНК-тест рассказывает и о вероятности осложнений во время беременности у женщин, о склонности к алкоголизму и еще о многих интересных (или печальных) особенностях организма.
Даже в современном мире сделать ДНК-анализ — целая операция. Нужно дорогое оборудование, особые реактивы и лицензия. Всего этого нет у небольших клиник. Для пациента это тоже испытание: сначала нужно сдать материал для анализа (мазок с поверхности щеки, слюну, кровь, волосяные луковицы, ушную серу и так далее), потом это все едет в лабораторию и исследуется минимум неделю.
Разработанная российскими учеными технология делает ДНК-тест настолько простым, что его можно проводить чуть ли на дому. Причем пациент получит результаты быстрее, да и эффективность лечения серьезных заболеваний будет выше.
Удачные эксперименты провели и подмосковные ученые, но по другому направлению. Исследователи разработали сильнейший анальгетик.
Мы не показали лечение, мы показали наночастицу, которую дальше надо испытывать и в живых организмах. Пока их эффективность не показана на животных, но мы создали частицу, которая может узнавать раковую клетку по нескольким параметрам, причем анализировать параметры очень чувствительно
Никитин подчеркнул: его команда не создала лекарство от рака и других серьезных болезней. Однако ученые смогли разработать нанороботов, способных находить болячки, обнаружить которые раньше было либо очень трудно, либо вообще невозможно.
Пока слишком рано говорить, что конкретно мы можем диагностировать с помощью этой технологии. Она настолько нова, что позволяет детектировать те вещи, которые раньше было либо сверхсложно детектировать, либо невозможно. А мы можем это детектировать в очень быстром, легком формате

Схема работы умного материала. Источник фото: МФТИ
Если в течение пяти лет исследования покажут пользу малых молекул для диагностики рака, тогда ученые смогут быстро диагностировать болезнь. Если покажут связь с атеросклерозом, то появится тест, определяющий наличие этого вида заболевания.
Сила этой технологии — она открывает направление потенциальных тестов, но мы впереди фундаментальной науки, которая должна сказать нам, какую мишень детектировать для какого заболевания
Нобелевская премия за революционые открытия в области онкологии
В 2018 году ученые Джеймс Эллисон и Тасуку Хондзё получили Нобелевскую премию за открытия иммуннотерапии – новой вехи использования лекарств против рака.
Содержание:
В основе их подхода к лечению рака лежит наблюдение за так называемыми контрольными иммунными точками – молекулами, с помощью которых клетки рака подавляют иммунный ответ на рост онкологических опухолей.
Ведь иммунная система очень мощная, ее задачей как раз и является коррекция неправильных угрожающих жизни процессов в организме, например, неконтролируемого деления клеток, чем является раковая опухоль. Это природное средство от рака.
Ингибиторы иммунных контрольных точек произвели революцию в лечении раковых заболеваний. Есть случаи полного выздоровления, например, при меланоме (смертность обычно 100%).
Исследование показало, что новая терапия увеличила выживаемость пациентов с последней стадией меланомы до 34 процентов, рака легких – до 15 процентов и почечно-клеточного рака – до 27 процентов. Действие основано на активности молекулы PD-1, которая атакует раковую опухоль.
Новые лекарства против рака отличаются по направлениям лечения разных стадий и видов заболеваний.
Например, пембролизумаб зарегистрирован для лечения множества опухолей при условии наличия репарации ДНК (восстановлении) и повышенной склонностью к мутациям.
Сложнейший иммунотерапевтический препарат — это CAR-T, который тренирует иммунные клетки бороться с раковыми. Метод уже зарегистрирован для лечения острых лейкозов у детей, но до сих пор является очень дорогим.
Лекарство от рака анти PD 1, комментарий онколога
Распространенные препараты от рака
Лекарства от рака обычно включаются в комплекс химиотерапевтических и лучевых методов лечения.
Тем не менее, зарегистрированных средств используемых на разных стадиях заболевания насчитывается десятки наименований только для онкологии молочной железы, к примеру. Следует учесть, что формы рака постоянно мутируют.
- Ампулы для перорального использования
- Флаконы для инфузионного раствора
- Таблетки
Бортезомиб (Велкейд), Этопозид (Эпиподофиллотоксин), Фторафур (Фторурацил, Синофлурол, Тегафур), Метотрексат (Эветрекс);
Ифосфамид, Циклофосфан (Цитоксан, Циклофосфамид, Эндоскан), Гемцитабин (Цитогем, Гемзар), Гидроксикарбамид;
Ифосфамид, Стрептозоцин, Иматиниб (Гливек), Гемцитабин, Фторафур;
Доксорубицин (Синдроксоцин, Растоцин), Цисплатин (Платинотин), Эверолимус (Афинитор), Сорафениб (Нескавар), Фторафур;
Доксорубицин, Винкристин, Паклитаксел, Фторурацил, Иматиниб;
Фторурацил, Дакарбазин, Цисплатин, Сунитиниб, Иматиниб, Гемцитабин;
Капецитабин, Лейковорин, Оксалиплатин (Медакса, Карбоплатин, Цитоплатин), Бевацизумаб, Иринотекан, Цетуксимаб (Эрбитукс);
Циклофосфамид, Каброплатин, Дакарбазин, Цетуксимаб;
Этопозид, Цисплатин, Ифосфамид, Дакарбазин, Доксорубицин;
Паклитаксел, Пертузумаб (Пьеретта), Гозерелин, Тамоксифен, Тиотепа, Летромара, Метотрексат, Трастузумаб, Эпирубицин;
Циклофосфамид (Эндоксан), Хлорамбуцил, Метотрексат, Дакарбазин;
Ифосфамид, Циклофосфан, Кселода, Пертузумаб (Пьеретта);
Мелфалан, Цисплатин, Цитофорсфан, Фторурацил, Хлорамбуцил;
Цитарабин, Доксорубицин, Ибрутиниб, Флударабин, Идарубицин (Заведокс);
Каброплатин, Ифосфамид, Циклофосфамид;
Доксорубицин, Блеомицин, Циклофосфамид, Алемтузумаб, Этопозид, Ритуксимаб (Ритуксан, Реддитукс);
Бевацизумаб, Прокарбазин, Темозоломид (Темодал), Циклофосфан, Винкристин;
Демекольцин, Глиозомид, Фторурацил, Мелфалан;
Цисплатин, Циклофосфамид, Гемцитабин, Метотрексат, Карбоплатин;
Фторурацил, Бикалутамид (Касодекс), Лейпрорелин, Трипторелин (Диферелин), Флутамид, Дегареликс (Фирмагон).
Новые препараты постоянно появляются, поэтому указать все мы не можем, да и в этом нет смысла. Доктора всегда могут проинформировать вас о современных лекарственных средствах от рака.
Немецкие препараты
Выпуском противораковых лекарств (Алкеран, Гемзар, Кризотиниб, Оксалиплатин, Холоксан и т.д.) в Германии занимаются различные фармацевтические компании (самые известные – Merck и Bayer AG).
Препарат Nexavar от компании Bayer используется в лечении почечно-клеточной ли гепатоцеллюлярной карциномы (неоперабельной), опухоли щитовидной железы.
В том числе компания производит Stivagra (Регорафениб) – ингибитор протеинкиназ – для лечения опухоли кишечника и радиофармацевтическый препарат Xofigo для лечения онкологии костных тканей с метастазами.
Компания Merck создала экспериментальный препарат Zolinza или Vorinostat (Вориностат), который используется при прогрессирующей кожной Т-клеточной лимфоме, не поддающейся воздействию химиотерапии. Действующее вещество – субероиланилид-гидроксамовая кислота, ингибирующая гистондезацетилазы. Клинические испытания показали активность лекарства против немелкоклеточной карциномы легкого и мультиформной рецидивирующей глиобластомы (опухоли головного мозга).
Препараты в Израиле
Препарат Ниволумаб (Nivolumab) или Опдиво (Opdivo) – один из самых современных препаратов, используемых в таргетной терапии при прогрессировании меланомы, карциномы почек и немелкоклеточного рака легкого. Препарат разработан японской биофармацевтической компанией Ono Pharmaceutical и Medarex (США), выпускается американской Bristol-Myers Squibb.
Американские препараты
Более десятилетие назад в американской компании Bristol-Myers Squibb стартовала разработка экспериментального препарата Танеспимицин (Tanespimycin) – производного антибиотика Гелданамицина, чье применение изучалось против лейкемии, опухолей почек и множественной миеломы.
Когда компания отказалась от производства Танеспимицина, компания Co-D Therapeutics начала выпускать Triolimus – новое средство против онкологии карциномы легких, молочной железы и ангиосаркомы. Этот препарат содержит полимерные мицеллы, созданные с помощью нанотехнологий и позволяющие одновременно доставлять несколько агентов, таких как Паклитаксел, Танеспимицин и Рапамицин.
Кстати, в 2006 году компания Bristol-Myers Squibb также начала выпуск нано препарата Спрайсел (Дазатиниб), предназначенного для борьбы с метастазирующим раком кожи и лимфобластным лейкозом.
Наномолярные концентрации лекарства действуют целенаправленно, подавляя рост исключительно опухолевых клеток.
Российское лекарство
В комплексной терапии онкологических заболеваний молочной железы применяется российское средство от рака Рефнот.
Копания BIOCAD выпускает моноклональные противораковые антитела BCD-100, Бевацизумаб и Ацеллбия (Ритуксимаб), а также ингибитор протеасом Бортезомиб и антиметаболит Гемцитабин (Гемцитар).
Бортезомиб производится предприятием Ф-Синтез под названиями Борамилан-ФС и Амилан-ФС; Борамилан – от компании Натива; под названием Бортезол производится компаний Фармасинтез. Также Бортезомиб выпускается с названием Милатиб.
Весной 2017 появились новости о том, что изобретено и было испытано на крысах новейшее российское лекарство против любого вида рака. В его основе лежит белок теплового шока, оказывающий противоопухолевое воздействие.
Финские лекарства
Финляндия официально была признана лучшей страной в Европе в лечении онкологии области шеи и головы, молочной железы, третьей – рака простаты, четвертой – рака кишечника.
Орион Фарма выпускает антиэстрогенное лекарство Фарестон против онкозаболеваний молочной железы. Также она производит антигормональный препарат Флутамид против онкологических заболеваний предстательной железы.
Хельсинский университет и американская компания Pfizer совместно ведут работу над разработкой инновационных препаратов против лейкемии.
Индийское лекарство
Супрапол ЖКТ (от компании Glerma Pharmaceuticals) может применяться в лечении злокачественных образований.
Этот препарат состоит из гуминовой (фульвиновой) кислоты и антиметаболита фторурацила. Лекарство имеет ряд ингибирующих свойств, а также проявляет анаболические и адаптогенные свойства, ускоряет детоксикацию организма.
Китайские лекарства
У многих китайских препаратов растительное происхождение, этим же отличается и лекарственный препарат Канглайт, который производится с помощью зерен бусенника обыкновенного или жемчужного ячменя. Этот злак является азиатским родственником кукурузы – также он носит называние слез Иовы. Вместе с прочими травами он на протяжении столетий используется в народной китайской медицине в качестве спазмолитического, обезболивающего и мочегонного средства.
В середине XX века изучением этого растения занимались и японцы – на более тщательное исследование свойств злака ученых натолкнул тот факт, что среди людей, проживающих в районе, где растение постоянно присутствует в рационе, отмечаются самые низкие в стране показатели появления онкологических заболеваний.
Препарат Канглайт – это эмульсия липидов из зерен ячменя, смесь ненасыщенных и насыщенных жирных кислот. После всевозможных исследований лекарство прошло клинические испытания, доказав высокую эффективность лечения карциноме легких и опухолей желудка, печени и молочной железы.
Также отмечается способность данного препарата замедлять митоз клеток рака и образование в опухолях сосудов.
Метод лечения Джоанны Бадвиг
Джоанна Бадвиг была семь раз номинирована на Нобелевскую премию в области медицины, что уже само по себе вызывает уважение к ее работе. Она умерла в 2003 в возрасте 95 лет.
Первый этап состоит из комбинации натуральных продуктов: серного белка творога и омега-з из семян льна. Доктор Бадвиг обнаружила, что организм будет вычленять омега-3 из льняного масла ровно в том количестве, которое ему необходимо.
Она утверждала, что существует ряд жирных кислот, без которых дыхательные ферменты просто не работают. Человек не сможет дышать, даже если вокруг него будет воздух обогащенный кислородом. К тому же многие процессы в организме замедляются из-за отсутствия этих полезных жирных кислот.
Доктор Бадвиг говорила, что мы не можем существовать без них, ровно как без воздуха и еды.
Это лекарство, в основном принимается внутрь, но в большинстве сложных случаях доктор Бадвиг вводила льняное масло ректально.
Вторая часть метода Бадвиг включает в себя специальную диету. Пациентам рекомендуется следовать этой диете в течение, по крайней мере, 6 месяцев, независимо от симптомов.
- 1 чашка очищенного творога (убедитесь, что он сделан не из гомогенизированного молока)
- 2-5 столовых ложек льняного масла, которые содержатся в около 10 капсулах в виде пищевой добавки или 1-3 столовых ложках перемолотых семян льна (обратите внимание, что льняное масло или молотые семена должны быть использованы сразу же после контакта с воздухом)
- немного красного стручкового перца
- Все ингредиенты тщательно перемешиваются. Полученное лекарство принимают внутрь, по крайней мере, один раз в день. Его нужно наливать в деревянную ложку и никогда в металлическую.
- Избегайте животных жиров в чистом виде.
- Не используйте магазинные заправки для салатов и начинки.
- Откажитесь от использования магазинного майонеза.
- Воздержитесь от мяса, если вы не уверены в его натуральном происхождении или вы не знаете, чем кормили животное.
- Избегайте масла и маргарина.
- Пейте фреши из овощей: морковь, сельдерей и свекла.
- Пейте чашку теплого чая три раза в день. Чаи из мяты, лепестков роз и виноградный чай. Используйте мед, чтобы подсластить свой напиток.
- Отдавайте предпочтения продуктам без химических добавок.
- Избегайте всех продуктов, которые были предварительно обработаны.
- Сократите прием всех лекарств.
- Не употребляйте напитков с добавками.
- Откажитесь от воды из-под крана и воды из пластика, пища не должна содержать фториды.
- Готовить необходимо каждый день, чтобы любое блюдо было свежим.
Исследования российских ученых
Валерий Александрович Черешнев, академик РАМН, почти сорок лет назад на медицинской базе военно-промышленного комплекса Советского Союза сделал открытие еще давно в эволюционирующем человеческом организме постоянно присутствовали гемолитические стрептококки группы А, которые в процессе своей жизнедеятельности вырабатывали необходимые для его правильной работы ферменты. Некоторые из них оказывают губительное воздействие на клетки опухолей!
Основываясь на этом, Черешневу удалось создать противораковую вакцину – Пиротат, которую так же можно использовать для лечения сердечно-сосудистых заболеваний, лидирующих среди причин смертности человека!
При этом удалось научно обосновать механизм, по которому эта вакцина действует. Всё дело именно в работе ферментов.
Одни из них, не проникая в здоровые клетки, оказывают прямое губительно воздействие на раковые, вызывают их деградацию.
Другие устраняют непроходимость кровеносных сосудов, например, растворяя бляшки из холестерина на стенках сосудов, тем самым улучшая кровоток и обеспечивая беспрепятственный доступ кислорода в здоровые клетки и доставляя иммунные клетки к местам образования опухолевых.
Третьи способны растворять нуклеиновые кислоты в элементарных тельцах, тем самым препятствуя распространению метастазов, губя при этом и различные вирусы. Очень важными являются и ферменты, которые приводят раковые клетки к голоданию, растворяя в местах их скопления глюкозу, что ведёт к заметному торможению роста опухоли. Эти же ферменты играют важную роль при лечении диабета.
Витамин В17 от рака
Амигдалин, обладающий научным названием mandelonitrile beta-D-gentiobioside, считается нитрилозидом – природным цианидсодержащим веществом. Лаэтрил (экстракционная форма витамина B17) наиболее известен тем, что потенциально помогает предотвратить развитие рака путем производства цианистого водорода.
Это полезное соединение высвобождается в ткани тела и разрушает мутировавшие клетки. Вы можете прочитать отзывы пациентов и врачей, а также приобрести витамин В17 в нашем магазине.

Что такое нанодоставка лекарств?
Эта наука появилась в 80-е годы, работы по липосомальной нанодоставке были чуть раньше. Она потихоньку эволюционировала, двигалась в сторону понимания того, что полимерный носитель можно конструировать, чтобы он выполнял важные функции доставки лекарства. Эти системы доставки работают, как автомобиль, в который мы загружаем пассажира, привозим его туда, куда надо, и высаживаем в нужной точке. Оказалось, что эти полимерные системы очень маленькие: их размер от 10 до 100 нанометров (нм). Отсюда возник и термин наномедицина, нанотехнологии.
Мы используем полимеры, которые содержат растворимые и нерастворимые части. Нерастворимые части самособиратся вокруг нерастворимого лекарства в так называемые мицеллы, а на поверхности остаются растворимые группы, которые обеспечивают растворимость всей частицы, так называемой полимерной мицеллы. Одна из работ, благодаря которым я стал известен, выполненная еще в 1989 году, заключалась в том, что мы стали использовать такие полимерные мицеллы, чтобы доставлять лекарства.
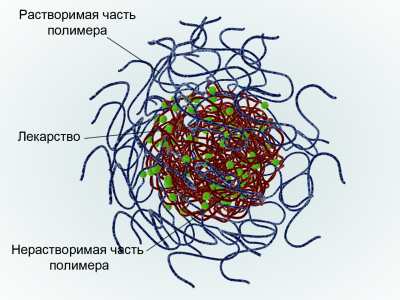
Схема мицеллы с лекарством//Дарья Алахова
Лекарства часто бывают нерастворимыми, тогда они включаются в эту полимерную мицеллу, как в маленький контейнер.
У этой мицеллы есть четко выраженное ядро и внешняя оболочка. В ядре располагается лекарство – оно спрятано от окружающей среды до тех пор, пока мицелла не рассыплется и не выделит лекарство. Оболочка играет роль маскирующего барьера, который не дает лекарству раньше времени взаимодействовать с организмом и обеспечивает необходимые для доставки свойства, например растворимость. Мицелла несколько похожа на орех с оболочкой и ядром, размер которого 20–30 нм. Это позволяет таким частицам эффективно проникать в клетки, а уже внутри они рассыпаются.
Нанолекарства сегодня и завтра
Уже сейчас на фармацевтическом рынке доступны нанолекарства. Пока это липосомальные препараты, но это действительно настоящие нанолекарства. Они имеют размер меньше 100 нм и оказываются более эффективными (либо менее токсичными – это очень важно) благодаря тому, что активный препарат неким образом упакован, в данном случае в липосому. Хороший пример липосомального лекарства – это доксил, липосомальная форма доксорубицина, которая сейчас используется для лечения метастазирующего рака яичников и СПИД-ассоциированной саркомы Капоши. Исходная идея доксила заключалась в том, что когда доксорубицин – очень токсичное лекарство – упаковывали в липосомальный контейнер, то оно становилось гораздо менее кардиотоксичным. Но потом оказалось, что доксил еще и повышает эффективность лечения ряда раков.
Сейчас на рынок (несколько лет назад) вышло другое нанолекарство, так называемый абраксан. Это лекарство паклитаксель (его лекарственная форма – таксол). Абраксан – наноформа паклитакселя, аналог таксола, только гораздо лучше сконструированный. В нем гораздо больше лекарственного препарата на единицу формуляции.
Сейчас разрабатывается масса нанопрепаратов. Эта область фактически взорвалась порядка пяти лет назад – ею стали заниматься и химики, и физики, и фармацевты. Было выделено и продолжает выделяться колоссальное финансирование.
В 2004 году в своем университете в Небраске мы основали Центр наномедицины и доставки лекарств. Как я понимаю, это был первый в Америке и в мире академический наномедицинский центр.
С тех пор мы работаем по двум главным направлением: одно связано с лечением рака, а другое – с доставкой веществ через гематоэнцефалический барьер. Обе задачи очень большие и серьезные.
В области лечения рака, пожалуй, дальше всего ушла работа, в которой
мы показали, что определенные полимеры драматически повышают эффективность лекарства против резистентных раков.
Эта работа привела к созданию клинического препарата, по нему мы уже завершили вторую фазу клинических испытаний. Мы показали, что такая полимерная мицелла, состоящая из лекарственного препарат доксирубицина и полимера, обладает высокой эффективностью лечения больных резистентными раками, у которых не оставалось терапевтических опций.
Более новая разработка касается повышения содержания лекарственного вещества в формуляции. Если вы хотите повысить эффективность препарата, его нужно сконструировать так, чтобы в нем было как можно больше того, что вы непосредственно доставляете, и как можно меньше балласта, вспомогательных веществ. Желательно, чтобы само действующее вещество составляло хотя бы 10% веса препарата. Редко кому удавалось сделать больше, используя контейнеры полимерных мицелл. Недавно мы обнаружили определенные полимерные материалы, которые позволяют на 1 г того же паклитакселя использовать всего 1 г полимерного носителя. За счет этого мы многократно снижаем нагрузку на организм. Дело в том, что у лекарственной формы – таксола – токсичность, ограничивающая дозу, определяется наличием того, что требуется, чтобы растворить такое нерастворимое вещество, как паклитаксель. А мы используем в 100 раз меньше полимера-балласта, чем в таксоле, необходимого для растворения (и в 10 раз меньше, чем в абраксане). Поэтому и токсичность у нас гораздо меньше, следовательно, мы можем повысить дозу и лечить рак лучше. В принципе в фармацевтических науках такие простые решения наиболее эффективны. Интересно, что эту работу мы делаем при поддержке Американского национального института рака совместно с коллегами из Технического университета Дрездена, Германия. Так что современная наука интернациональна и не знает границ: у нас общее дело – помочь людям во всех странах.
Есть два пути улучшения лекарства – снизить токсичность или повысить активность. В первом случае мы повысили активность – и можем убивать рак лучше. Во втором случае мы снизили токсичность, поэтому можем повысить дозу – и опять убивать рак лучше.
Около 20 лет назад мы с моим коллегой, ныне академиком РАМН, Владимиром Павловичем Чехониным начали конструировать различные полимерные системы, которые могли обмануть эти системы защиты гематоэнцефалического барьера и проникнуть в мозг. Эти работы очень прогрессировали, расширились в нашем центре. Сейчас таким образом мы уже умеем доставлять в мозг ферменты, которые уничтожают вредные окислительные частицы – свободные радикалы, которые вырабатываются в мозге в ответ на многие дегенеративные процессы. Дегенеративные процессы очень часто сопряжены с образованием свободных радикалов, воспалением, связанным с их образованием, и последующим разрушением нейронов – нервных клеток мозга, нейродегенерацией. Такова общая схема развития и болезни Паркинсона, и болезни Альцгеймера, и инсультов, и довольно широкого круга других дегенеративных процессов в мозге. Конечно, было бы идеально вводить в мозг так называемые антиоксиданты, но это сложно сделать из-за наличия гематоэнцефалического барьера.
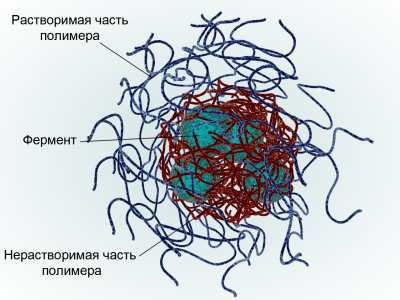
Схема нанозима//Дарья Алахова
Планы работ в России
Новое направление – магнитные наночастицы.
Базироваться она, скорее всего, будет на кафедре химической энзимологии, однако в работе будет участвовать и кафедра высокомолекулярных соединений (там есть хороший накопленный опыт работы), и другие сотрудники МГУ – химики, биологи, физики, которые могут внести важный вклад в эту работу. Мы планируем расширять сотрудничество с Государственным медицинским университетом (группа академика РАМН Владимира Павловича Чехонина), потому что конечная наша цель – лекарства. Нам мой взгляд, формируется хороший квалифицированный коллектив. В прошлом году наш медицинский центр Университета штата Небраски заключил соглашения о научном и образовательном обмене как с МГУ, так и с РГМУ. Вместе с тем у нас будет возможность пользоваться научными ресурсами и биологическими моделями заболеваний, приборной базой моего центра в Америке, что, безусловно, полезно.
Проблема внедрения медицинских разработок в США и России
Внедрение разработанных лекарств в медицинскую практику не такая простая задача. Механизм внедрения научных разработок не до конца отработан и в США, поэтому у России хорошие возможности в этой области.
Для того чтобы начать применять лекарство на практике, мало показать, что оно работает на некоторых моделях. Нужно показать, что оно работает на всех без исключения моделях, на которых оно должно работать. Кроме того, нужно показать полную безопасность препарата.
И как ее решить, мало кто понимает.
С этой же проблемой мы сталкиваемся в моем центре в США. Его общее финансирование из грантов около $34 млн (почти $8 млн в год). Это огромные деньги для фундаментальных исследований. Но мы не можем тратить эти деньги на развитие конечного продукта. Дело даже не в том, что это будет незаконно, так как деньги выделены на что-то другое. Допустим, я сумею убедить Национальный институт здоровья, что мне нужно выделить эти деньги. Как только я начну этим заниматься, у меня приостановятся новые разработки, я перестану делать то, что необходимо, чтобы эти деньги получить, – и я их потеряю.
Я говорю ребятам на самом первом этапе разработки, когда у нас появляется некая идея: представим себе, что мы уже создали продукт. Какими параметрами будет обладать этот продукт на основе этой идеи, чтобы эффективно лечить заболевание? И вообще какое это будет заболевание? Вот мы говорим: мы будем лечить рак. Но рак – это слишком общо, это огромный спектр разнообразных заболеваний, и подходы к лечению разных типов рака разные, поэтому нужно определиться, где у нас действительно может быть прорыв и где у нас может быть конкретное преимущество по сравнению с имеющимися и ныне разрабатываемыми методами лечения. Есть и другие важные вопросы: как мы будем проводить клинические испытания, как будет устроено производство продукта. Будучи фундаментальной группой, много достигшей в понимании процессов нанодоставки в клетках, мы одновременно начали думать о таких практических вещах. На наши переговоры мы стали приглашать бизнесменов, специалистов по клиническим исследованиям. И я надеюсь, что это позволяет нам в своих фундаментальных исследованиях очень рано сделать правильный выбор. Например, не работать с неким полимером, потому что он не биосовместимый, а работать с другим – биосовместимым. Иначе мы так всю жизнь и останемся на разработках по небиосовместимому полимеру, которые нельзя внедрить: чтобы получить новый грант, нам надо дать предыдущие результаты, а они уже зациклены на неправильном пути. Поэтому мне кажется, что такого рода деловые игры играют большую роль в судьбе разработок, в эффективности всего процесса.
Когда я был молодым, эта область науки была очень новой. Мы создавали новую науку, делали открытия – и этого было достаточно. Сейчас десятки групп занимаются полимерными мицеллами, опубликованы тысячи работ, это больше не выделяет нас. А вот то, что мы дошли до третьей стадии клинических испытаний, – это ценно и важно. Я сам несколько лет был председателем совета по распределению грантов Национального института здоровья США. И я смотрел, как люди приносят идеи – одну, другую; но это идеи, которые никогда не будут реализованы.
И я решил, что, работая в области здравоохранения, неправильно не ориентировать свою деятельность на создание реального лекарства. С тех пор мы изменили подход к своей работе и всегда ориентируемся на конечный продукт.
Не могу сказать, что мы совсем уж впереди планеты всей, но мы одна из самых сильных в Америке групп, которая этим занимается.
То есть ученые в России должны осознавать, что проблема внедрения фундаментальных научных разработок очень серьезна и она не решена ни в США, ни в Европе. Поэтому и у русских есть шанс серьезно поучаствовать в решении этих проблем. Мы сегодня ведем разговор с учеными-практиками и клиницистами здесь, в России, вполне серьезно, и я рассчитываю, что мы сможем вместе решать эти вопросы. Вместе мы можем создать хороший препарат и испробовать его на серьезной клинической базе.
Возрождение науки: опыт Китая
Нет ни малейших сомнений, что российская, советская наука пережила ужасный сокрушительный период перестройки, 90-х годов, но Китай действительно был в худшей ситуации.
Я специально изучал шаги, которые они предприняли для возрождения науки. У них тоже были и мегагранты – и более крупные, и более мелкие для временно приезжающих для чтения лекций профессоров. И сейчас у них и свои хорошие ученые, и студенты, которые хотят учиться, заниматься наукой, потому что есть компании, где можно применить свои знания. Если Россия пойдет по этому пути, то результат будет.
Это самый важный вопрос – куда пойдет Россия. И он гораздо более важен, чем вопрос, вернутся окончательно или нет получатели грантов.
Опыт Китая, которым я интересовался, показал, что самую большую пользу для возрождения науки сыграли крупные ученые китайского происхождения, которые не вернулись назад в КНР.
Читайте также:

