Клинические исследования по раку яичников
Эффективные методики и новые технологии
Ведущим методом остается хирургический (удаление рака яичника) и химиотерапия при раке яичников. Химиотерапия при раке яичников улучшает результаты лечения при локализованной форме болезни, занимает ведущее место при диссеминированном характере опухоли. Химиотерапия при раке яичников может быть применена также в предоперационном периоде с целью уменьшения проявлений болезни. Последовательность лечения определяется на междисциплинарной онкологической конференции с привлечением высококвалифицированных онкологов (с учетом всех данных обследования).
При IА стадии заболевания выполняют органосохраняющие операции у женщин, желающих сохранить детородную функцию, с последующим строгим контролем. При изначально распространенном раке проводится современное лечение метастазов рака яичников – лечение начинают с химиотерапии, позволяющей уменьшить размер опухоли или привести к полному ее исчезновению, с целью создания условий для проведения радикальной операции. Выполняется овариэктомия. Овариэктомия – это хирургическое удаление пораженного опухолью яичника. Стандартный объем операции включает в себя удаление матки с придатками, удаление большого сальника, удаление всех макроскопических очагов опухоли. В послеоперационном периоде продолжается химиотерапия. В связи с возможностью возврата (рецидива) рака яичников даже после достижения полного эффекта от лечения больная должна находиться под постоянным контролем. Для этого раз в три месяца проводится контроль маркера СА-125 (онкомаркер яичников), УЗИ органов брюшной полости и малого таза, осмотр онкогинеколога.
Ученые продолжают исследования в попытках обнаружить гены, которые отвечают за наследственные варианты рака яичников. Работы начинают приносить свои плоды: функция подобных генов в норме становится ясной, а также влияние ее нарушения на развитие рака. Полученные сведения пригодятся в разработке новых лекарств для профилактики и лечения семейных форм рака яичников.
Улучшить обнаружение генов, которые существенно увеличивают возможность развития болезни, смогли исследования в данной области. Это в каждом конкретном случае помогает оценить риск рака яичников. Ученые стремятся лучше понять взаимодействие гормональных и генетических факторов (таких как применение противозачаточных средств).
Огромное влияние на коэффициенты выживаемости могут оказать точные методы ранней диагностики рака яичников.
Исследователи изучают новые способы скрининга рака яичников.
Было создано государственные хранилище образцов крови и тканей, полученных от пациенток с раком, для содействия подобным изысканиям. Изучение особенностей белкового состава крови (сфера деятельности так называемойпротеомики) является одним из многообещающих методов выявления рака.
Для женщин с опухолями яичников предназначен тест под названием OVA1.
На 2 категории: высокого риска и низкого риска - позволяет разделить пациенток с опухолями совместное определение всех белков.
Опухоль, скорее всего, доброкачественная, если женщина входит в группу низкого риска. У женщин из группы высокого риска, вероятно, опухоль носит злокачественный характер, что должно быть подтверждено специалистом (онкогинекологом) хирургически. Этот тест предназначен лишь для применения у женщин с опухолями яичников.
У некоторых пациенток с эпителиальным раком яичников оказывается нормальным содержание в крови маркера CA125. Эффективность лечения в подобных случаях оценить (или выявить рецидив рака) позволяют только методики визуализации (такие как компьютерная томография или УЗИ).
У многих женщин с раком яичников увеличивается содержание белка HE4 в крови. Если содержание маркера CA125 оказывается нормальным, врач может исследовать при раке яичников уровень HE4. Белок HE4, при его высокой концентрации, может использоваться для определения эффективности лечения вместо маркера CA125.
Определение ценности используемых методов, а также разработку новых терапевтических подходов включают исследования в области лечения.
Новые сочетание химиопрепаратов, которые при устойчивости опухоли к существующим лекарствам могут помочь, изучаются постоянно. Также в исследованиях рассматривается применение средств прицельной терапии рака яичников.
Поли(АДФ-рибоза)-полимеразы (PARP) - это недавно обнаруженные ферменты. Они являются ключевыми регуляторами жизненного цикла клетки. С раком, вызванным мутациями генов BRCA1 и BRCA2, борются лекарства, которые подавляют фермент PARP-1. Увеличить чувствительность рака яичников без наличия мутации к радиотерапии и некоторых видами химиопрепаратов (метилирующим агентам и ингибиторам топоизомеразы I) позволяют данные препараты. Вопросам влияния данных препаратов на прогноз у женщин с раком яичников без мутаций BRCA посвящены проводимые клинические исследования. vРазработка вакцин, которые программируют иммунную систему на распознавание раковых клеток, может быть другим подходом к лечению.
Изучаются моноклональные антитела, которые специфически выявляют и атакуют клетки опухоли. Моноклональные антитела, которые направлены на поверхностный белок клеток рака яичников - это фарлетузумаб. При лечении рака на ранних стадиях выявлена его эффективность. Катумаксомаб является другими моноклональными антителами, применение которых изучается при раке яичников. С белком, находящимся в некоторых клетках иммунной системы и на некоторых раковых клетках, связывается препарат
Также в клинических исследованиях изучается консолидационная терапия: лечение, которое проводится для предупреждения рецидива рака после терапии первой линии. Для этих целей, в некоторых работах, используются химиопрепараты, моноклональные антитела и ингибиторы факторов роста.
Принять верные практические решения о профилактике женщинам помогут новые сведения о влиянии мутаций генов BRCA1 и BRCA2 на риск развития рака яичников. Например, были разработаны математические модели, помогающие рассчитать количество лет, которые при профилактическом удалении обоих яичников и маточных труб на фоне наличия мутации генов BRCA можно прибавить к жизни.
Рак маточной трубы у женщин при наличии мутации генов BRCA развивается намного чаще, чем ранее считали врачи, как показали недавние исследования. Тем не менее, важно не забывать, что сделать точный прогноз для жизни в каждом конкретном случае, несмотря на то, что средние исходы для группы из большого числа женщин врачи предугадывать научились, до сих пор невозможно.
Влияние новых препаратов на профилактику рака яичников изучается в других работах.
Такие факторы, как питание, образ жизни и лекарства, которые могут снизить риск развития опухоли, исследователи изучают постоянно.
Международное многоцентровое клиническое исследование III фазы MK7339
В рамках этого исследования у наших пациенток есть возможность получить самые современные препараты для лечения рака онкологических заболеваний – олапариб (ингибитор PARP) и пембролизумаб (иммунотерапия, моноклональное антитело к PD-1). Предполагается, что добавление этих препаратов к стандартной химиотерапии позволит значительно улучшить результаты лечения заболевания.
Основные критерии включения:
1. Гистологически подтвержденный диагноз рака яичников ИЛИ маточной трубы ИЛИ первичный рак брюшины (допускаются различные варианты опухоли (включая редкие варианты);
2. IIIC или IV стадия заболевания;
3. Если было проведено хирургическое лечение – не раньше 56 дней до включения в исследование;
4. Возраст старше 18 лет;
5. Нормальное общее состояние (статус по шкале Карновского ≥70%);
6. Отсутствие тяжелой сопутствующей патологии.
Основные критерии исключения:
1. Ранее проведенная химиотерапия;
2. Наличие подтвержденной мутации в генах BRCA1 или BRCA2;
3. Декомпенсированная сопутствующая патология.
Распределение в одну из трех групп:
· Пембролизумаб (Китруда) + паклитаксел + карбоплатин + олапариб (Линпарза);
· Пембролизумаб (Китруда) + паклитаксел + карбоплатин;
Тюляндина Александра Сергеевна
Румянцев Алексей Александрович
1. Многоцентровое рандомизированное исследование фазы 3 применения рукапариба по сравнению с химиотерапией для лечения пациенток с рецидивирующим, имеющим мутацию гена BRCA, высокой степени злокачественности эпителиальным раком яичников, маточных труб или первичным раком брюшины
Основные критерии включения для отбора в исследование
Наличие гистологически подтвержденного диагноза высокой степени злокачественности серозного или эндометриоидного стадии 2 или 3 эпителиального рака яичников, маточных труб или первичного рака брюшины.
Прохождение ? 2 предшествующих курсов химиотерапии с рецидивом или прогрессированием заболевания по данным рентгенографической оценки.
Наличие вредной мутации BRCA1/2
Должно быть достаточное количество фиксированной формалином и залитой парафином (ФФЗП) опухолевой ткани для планируемых анализов
Наличие адекватной функции органов: функция костного мозга, функция печени, функция почек.
Основные критерии невключения
Активное второе злокачественное заболевание
Предшествующая терапия любым ингибитором ПАРП, включая рукапариб
Предшествующая монотерапия паклитакселом
Заболевание, рефрактерное к препаратам платины: прогрессирование заболевания по данным рентгенографии в течение 4 недель после завершения наиболее последнего курса терапии на основе препаратов платины
Симптоматические и (или) нелеченые метастазы в центральную нервную систему (ЦНС)
Наличие дуоденального стента и (или) любых других нарушений или дефектов со стороны желудочно-кишечного тракта
Потребность в регулярных гемотрансфузиях, гранулоцитарном колониестимулирующем факторе или трансфузиях тромбоцитов

вместе создадим единую базу клинических исследований в онкологии
- Руководства ESMO
- Помощь пациентам в период пандемии COVID-19
- Руководства RUSSCO
- Школа жизни онкологического пациента во время коронавируса (интервью члена Правления RUSSCO, проф. Н.В. Жукова)
Клинические исследования, которые проходят в данный момент
Многоцентровое, рандомизированное, открытое клиническое исследование фазы 3 в трех группах применения препаратов энкорафениб, цетуксимаб совместно с биниметинибом или без него, по сравнению с применением препаратов иринотекан/цетуксимаб или инфузионной терапии с применением 5-фторурацила (5-ФУ)/ фолиновой кислоты (ФК)/ иринотекана (FOLFIRI)/ цетуксимаба с определением безопасной дозы введения комбинации препаратов энкорафениб, бениметиниб, цетуксимаб для лечения пациентов с метастатическим коларектальным раком с мутацией BRAF V600E
Рандомизированное двойное слепое плацебо-контролируемое исследование для сравнения двух гуманизированных моноклональных антител направленного специфического действия против фактора роста эндотелия сосудов, применяемых в сочетании с химиотерапией по модифицированной схеме FOLFOX6 у пациентов с нерезектабельной метастатической колоректальной опухолью
TASCO1
Открытое рандомизированное исследование II фазы по оценке эффективности комбинации препарата TAS-102 с бевацизумабом и комбинации капецитабина с бевацизумабом у пациентов с метастатическим колоректальным раком, ранее не получавших лечение по поводу распространенного опухолевого процесса и которым не показано проведение интенсивной химиотерапии
Двойное слепое рандомизированное плацебо-контролируемое исследование III фазы препарата нинтеданиб в комбинации с оптимальной поддерживающий терапией (ОПТ), по сравнению с плацебо в комбинации с ОПТ, у пациентов с колоректальным раком, устойчивым к стандартному лечению
Рандомизированное двойное слепое плацебо-контролируемое многоцентровое международное исследование III фазы дурвалумаба или комбинации дурвалумаба с тремелимумабом в качестве консолидирующей терапии у пациентов с локализованным мелкоклеточным раком легкого I-III стадии, у которых не произошло прогрессирование после одновременной химиолучевой терапии (ADRIATIC)
Рандомизированное двойное слепое плацебо-контролируемое многоцентровое международное исследование III фазы дурвалумаба или комбинации дурвалумаба с тремелимумабом в качестве консолидирующей терапии у пациентов с локализованным мелкоклеточным раком легкого I-III стадии, у которых не произошло прогрессирование после одновременной химиолучевой терапии (ADRIATIC)
База, на которой проводится исследование:
Международное, рандомизированное, открытое исследование 3 фазы препарата REGN2810 (анти-PD 1 антитело) по сравнению с химиотерапией препаратами платины в качестве первой линии терапии у пациентов с распространенным или метастатическим PD-L1-положительным немелкоклеточным раком легких
Рандомизированное, открытое исследование 3 фазы комбинации препарата REGN2810 (анти-PD 1 антитело), ипилимумаба и двухкомпонентной схемы химиотерапии производными платины в терапии первой линии пациентам с распространенным или метастатическим немелкоклеточным раком легкого и уровнем экспрессии в опухоли PD-L1 менее или равно 50%
Открытое многоцентровое исследование III фазы, проводимое для сравнения действия препарата авелумаб с действием двухкомпонентной химиотерапией препаратами платины при их применением в качестве первой линией терапии рецидивирующего или PD-L1-положительного немелкоклеточного рака легкого IV стадии
Протокол № EMR 100070-005
Многоцентровое исследование 2 фазы с целью изучения пероральной терапии ингибитором cMET, препаратом INC280 у взрослых пациентов с распространенным немелкоклеточным раком легкого при немутантном статусе EGFR (WT)
2) Аболмасов Александр Евгеньевич
+7 (925) 928-51-59
Открытое многоцентровое рандомизированное исследование 3 фазы по изучению эффективности и безопасности препарата BGB-A317 (анти-PD1 антитела) по сравнению с доцетакселом у пациентов с немелкоклеточным раком легкого и прогрессированием заболевания после курса платиносодержащей химиотерапии
Рандомизированное открытое исследование фазы 3 применения Бригатиниба (Алунбриг™) в сравнении с Алектинибом (Алеценса ® ) у пациентов с распространенным ALK-позитивным немелкоклеточным раком легких, у которых возникла прогрессия заболевания на фоне применения Кризотиниба (Ксалкори ® )
Многоцентровое рандомизированное, двойное слепое, плацебо-контролируемое исследование III фазы, проводимое с целью оценки эффективности и безопасности анаморелина гидрохлорида, применяемого для восполнения дефицита массы тела и лечения анорексии, развившихся на фоне распространенного немелкоклеточного рака легкого у взрослых пациентов
Двойное слепое, рандомизированное, проводимое в параллельных группах исследование 3-й фазы с использованием активного препарата в качестве контроля с целью сравнения эффективности и безопасности препарата CT-P16 и разрешенного в ЕС препарата Авастин, применяемых в качестве первой линии терапии метастатического или рецидивирующего неплоскоклеточного немелкоклеточного рака легкого
Протокол № CT-P16 3.1
Рандомизированное, двойное слепое, многоцентровое исследование III фазы для оценки эффективности, безопасности, фармакокинетики и иммуногенности исследуемого препарата SB8 (предлагаемого биоаналога бевацизумаба) в сравнении с препаратом Авастин ® у пациентов с метастатическим или рецидивирующим неплоскоклеточным немелкоклеточным раком легкого
2) Козлов Вадим Викторович
+7 (913) 463-828-6
2) Бабина Ксения Геннадьевна
+7 (968) 267-77-76
Открытое исследование препарата афатиниб у пациентов с местнораспространенным или метастатическим немелкоклеточным раком легкого с мутацией рецептора эпидермального фактора роста, ранее не получавших лечение или предварительно получавших химиотерапию
Рандомизированное, двойное-слепое, плацебо-контролируемое исследование III фазы по изучению ARQ 197 плюс эрлотиниб vs эрлотиниб у ранее леченых пациентов с местно-распространенным или метастатическим неплоскоклеточным немелкоклеточным раком легкого
Программа расширенного доступа к ИПИЛИМУМАБУ для больных глиобластомой и глиомой
Mногоцентровое, рандомизированное, открытое исследование III фазы Атезолизумаба (антитело к PD-L1) в комбинации с адъювантной химиотерапией на основе антрациклина/таксана в сравнении только с химиотерапией у пациентов с операбельным трижды негативным раком молочной железы
Двойное слепое рандомизированное исследование III фазы, проводимое в параллельных группах, по сравнению эффективности, безопасности и иммуногенности TX05 и препарата Герцептин ® у пациентов с ранней стадией HER2-положительного рака молочной железы
Двойное слепое продолженное исследование для проведения адъювантной монотерапии препаратом Герцептин ® или препаратом TX05 для продолжения оценки безопасности и иммуногенности у пациентов с ранней стадией HER2-положительного рака молочной железы после проведения неоадъювантной терапии и хирургической резекции в рамках протокола TX05-03
Рандомизированное открытое исследование 3 фазы по оценке препарата абемациклиб в комбинации со стандартной адъювантной эндокринной терапией по сравнению с применением только стандартной адъювантной эндокринной терапии у больных раком молочной железы на ранней стадии, с высоким риском развития рецидива, поражением регионарных лимфатических узлов, с положительным статусом гормональных рецепторов и отрицательным статусом рецептора эпидермального фактора роста человека 2-го типа
Рандомизированное, многоцентровое, открытое, III фазы исследование лапатиниба плюс капецитабин или трастузумаб плюс капецитабин упациенток с Her2/neu позитивным метастатическим раком молочной железы ранее получавших антрациклины и таксаны
Международное проспективное открытое многоцентровое неинтервенционное исследование OPTIMIS.
Изучение результатов лечения больных гепатоцеллюлярным раком, получавших или не получавших сорафениб после трансартериальной химиоэмболизации (ТАХЭ), и влияние времени начала терапии сорафенибом
Многоцентровое открытое исследование 1b фазы с эскалацией дозы по изучению безопасности и переносимости препарата квинакрин у пациентов с опухолевыми заболеваниями печени различного происхождения
Многоцентровое рандомизированное открытое исследование (3 фаза) эффективности и безопасности Ленватиниба (E7080) в сравнении с Сорафенибом в первой линии лечения больных неоперабельным печеночно-клеточным раком
Рандомизированное многоцентровое двойное слепое исследование III фазы препарата регорафениб у больных ГЦР, ранее получавших сорафениб
Рандомизированное, двойное-слепое исследование II фазы по сравнительной оценке режимов рамуцирумаба в комбинации с цисплатином и гемцитабином; мерестиниба в комбинации с цисплатином и гемцитабином или плацебо в комбинации с цисплатином и гемцитабином в качестве первой линии терапии у пациентов с распространенным или метастатическим раком желчевыводящих путей
JAVELIN BLADDER 100
Многоцентровое, международное, открытое, рандомизированное, проводимое в параллельных группах исследование 3-й фазы, в котором Авелумаб (MSB0010718C) в комбинации с наилучшей симптоматической терапией сравнивается с наилучшей симптоматической терапией в качестве поддерживающего лечения у пациентов с местно-распространённым или метастатическим уротелиальным раком, который не прогрессировал после завершения первой линии химиотерапии на основе препаратов платины
2) Аболмасов Александр Евгеньевич
+7 (925) 928-51-59
Многоцентровое, рандомизированное, двойное слепое исследование III фазы для оценки эффективности и безопасности препарата BIBIF 1120 в комбинации с карбоплатином и паклитакселом в сравнении сплацебо в комбинации с карбопалином и паклитакселом у пациентов с распространенным раком яичников
Многоцентровое, двойное слепое, плацебо-контролируемое, рандомизированное исследование II фазы по изучению омрабулина у больных с чувствительным к препаратом платины рецидивирующим раком яичников, получающих карбоплатин/паклитаксел
MK1775 в сочетании с карбоплатином и паклитакселом при платиночувствительном раке яичников
Эффективность и безопасность Пембролизумаба у пациентов с прогрессией распространенного рака яичников (KEYNOTE 100)
Рандомизированное двойное слепое плацебо-контролируемое исследование III фазы эффективности и безопасности копанлесиба в комбинации с ритуксимабом у пациентов с рецедивами индолетных В-клеточных лимфом (иНХЛ) – CHRONOS-3
Исследование II/III фазы по оценке продолжительности тяжелой нейтропении при лечении плинабулином в сравнении с пэгфилграстимом у пациентов с солидными опухолями, получающих миелосупрессивную химиотерапию доцетакселом
Мультинозологичное исследование: анализ предиктивных биомаркеров для применения пембролизумаба при распространенных солидных опухолях (KEYNOTE 158)
* Критерии включения и исключения представлены не в полном объёме
Большинство достижений в лечении злокачественных опухолей яичников за последние 20 лет — результат комплексного подхода, эффективность которого доказали в III фазе клинических исследований. Есть надежда, что сочетание индивидуального подхода, новых химиотерапевтических препаратов, лучшего понимания механизмов резистентности к лекарственным средствам и применение модификаторов биологических реакций позволит улучшить результаты лечения этих опухолей, характеризующихся неблагоприятным прогнозом.
Химиотерапия (XT) обладает высокой эффективностью при лечении поздних стадий некоторых гистологических типов рака яичника (РЯ) и, следовательно, служит полезным дополнением к хирургическому лечению и лучевой терапии (ЛТ). Успешная химиотерапия (ХТ) (90 %) возможна всего лишь при 10 % опухолей человека.
Возможно, эта сложная биологическая проблема связана со склонностью некоторых тканей вырабатывать специфическую и стойкую резистентность ко многим химиотерапевтическим препаратам. Обсуждение устойчивости опухолевых клеток к цитостатикам не входит в задачи этого раздела, однако можно дать несколько общих комментариев. В нормальных клетках устойчивость не развивается, это врожденное свойство злокачественных клеток, подобное инвазии и метастазированию.
В связи с этим возникает две клинические проблемы. Первая связана с первоначальной чувствительностью опухоли, по крайней мере, к некоторым цитостатикам, поскольку после регрессии заболевания возникает рецидив, несмотря на эффективное первичное лечение. Ситуацию легче всего объяснить феноменом отбора, когда после гибели чувствительных остается популяция устойчивых клеток, которая затем пролиферирует.
Вторая проблема состоит в так называемой природной устойчивости, когда опухоль de novo проявляет резистентность к лечению или, по крайней мере, показывает высокую устойчивость к широкому спектру химиотерапевтических препаратов.

Несмотря на огромную работу, которая выполнена по изучению и лечению злокачественных опухолей яичников, на самом деле это только вершина айсберга. С появлением новых генетических методик анализа и молекулярной биологии открываются новые горизонты исследования.
Молекулярная биология. Изучены многие аспекты молекулярной биологии рака яичника (РЯ). Это клональное заболевание, связанное с активацией рецепторов тирозинкиназы, цитоплазматических киназ и мономерных G-белков. Однако механизм влияния генов-супрессоров опухолевого роста на сигнальный каскад клеток до настоящего времени неизвестен. Возможно, важная роль принадлежит инвазии, адгезии и паракринным факторам.
Влияние трансформирующего фактора роста b на прогрессирование рака яичника (РЯ) находится в стадии изучения. В патогенезе важная роль может принадлежать эпителиально-стромальным взаимодействиям, активину и ингибину. Создание банка опухолей и сыворотки больных раком яичника (РЯ), предпринятое GOG, позволит продолжить изучение этих и многих других вопросов молекулярной биологии.
Экспериментальные методы лечения. Генетическая терапия весьма привлекательна, по крайней мере теоретически. Выявление генного дефекта позволяет провести его замену. Этот метод лечения только начинает развиваться. Существует множество видов генной терапии: иммуногенная; антионкогенная, влияющая на гены-супрессоры опухолевого роста; антиростовые факторы; гены, регулирующие апоптоз; цитокиновые гены лекарственной устойчивости. Начаты предварительные исследования по этому вопросу, причем особое внимание уделяют терапии, препятствующей ангиогенезу в опухолях.
Новые препараты. Основная проблема химиотерапии (XT) — резистентность, поэтому проводят исследования по поиску препаратов, не вызывающих перекрестной устойчивости, а также поиску новых мишеней для лекарственного воздействия. Многие препараты проходят II фазу клинических исследований. Есть надежда на скорое появление нового цитостатика на основе платины.
Качество жизни. Эта проблема представляет интерес при всех типах рака, в т. ч. и при раке яичника (РЯ). Разработаны достоверные методы измерения этого показателя. GOG и другие исследователи теперь вносят его во многие протоколы. Оценивают симптомы рака, токсичность лечения и психологический стресс. Проблемам лечения боли, нарушения сексуальной функции, поддержки семьи и способности трактовать новую генетическую информацию не уделяли должного внимания. Сейчас ситуация привлекла внимание специалистов и начинает понемногу улучшаться.
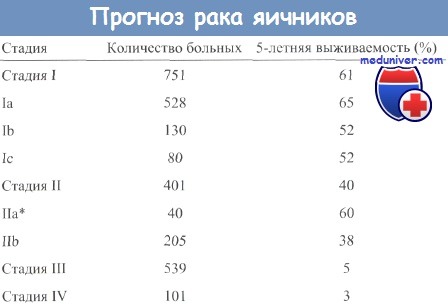
*Особенно важно различие между стадией IIа и IIb, поскольку 5-летняя выживаемость больных в стадии IIа близка к таковой для больных в стадии I.

У пациенток с раком яичников IV стадии (метастатическим раком) заболевание распространилось за пределы брюшной полости или в печень.
В настоящее время стандартным подходом к лечению метастатического рака яичников остается хирургическое вмешательство с последующей химиотерапией. К сожалению, длительная выживаемость после стандартного лечения отмечается менее, чем в 10% случаев. Дело в том, что рак яичников IV стадии сложно удалить полностью в ходе операции, а доступная в данный момент химиотерапия не способна уничтожить все оставшиеся злокачественные клетки. Пациенткам рекомендуется оптимальная циторедуктивная операция и химиотерапия на основе препаратов платины. Доказано, что эти методы позволяют отсрочить рецидив и повысить общую выживаемость.
Навигация по статье
Как пройти дистанционное лечение рака в Израиле во время эпидемии коронавируса?
- Циторедуктивная хирургия
- Химиотерапия при метастатическом раке яичников
- Стратегии совершенствования лечения
- Выбирая метод лечения, нужно задать врачу следующие вопросы:
- Стоимость диагностики и лечения рака яичников в Израиле
- Почему лечить рак яичников нужно в Израиле?
Циторедуктивная хирургия
Во время циторедуктивной операции врачи стараются удалить максимум злокачественных клеток. Циторедуктивное вмешательство способствует уменьшению общего количества раковых клеток и тем самым облегчает задачу для химиотерапевтических препаратов. Такой подход снижает вероятность развития у опухоли резистентности к химиотерапевтическим компонентам.
Первичная циторедуктивная операция считается стандартом лечения рака яичников. По итогам научных исследований можно увидеть, что оптимальная циторедуктивная хирургия повышает выживаемость пациенток и отсрочивает развитие рецидива. Субоптимальное циторедуктивное вмешательство не дает настолько перспективных результатов.
После операции всем пациенткам с раком яичников IV стадии предлагают дополнительное лечение. Дополнительная терапия действительно необходима: многие раковые опухоли яичников рецидивируют даже после полной хирургической резекции. Что касается метастатического рака яичников, у многих пациенток в организме остаются клетки, которые нельзя удалить традиционным хирургическим способом. Таким больным нужна эффективная терапия, состоящая в уничтожении оставшихся злокачественных клеток. Дополнительная терапия позволяет улучшить достигнутые результаты. В настоящее время таким способом лечения является химиотерапия.
Химиотерапия при метастатическом раке яичников
Результаты клинических испытаний демонстрируют, что применение комбинированной химиотерапии с содержанием препарата на основе платины (Платинол или Параплатин) продлевает выживаемость женщин, больных метастатическим раком яичников. Кроме того, такие схемы более эффективны в профилактике рецидивов рака, чем комбинации хирургического вмешательства с химиотерапией без препаратов платины. Традиционная схема химиотерапии состоит из паклитаксела и препарата платины, которые следует принимать один раз в три недели на протяжении 6-8 циклов.

Чаще всего врачи назначают химиотерапию после того, как пациентка перенесет операцию. В некоторых случаях химиотерапия применяется не только после, но и до операции. Предоперационное лечение противораковыми медикаментами уменьшает объем злокачественных тканей, то есть – облегчает удаление максимального количества раковых клеток в ходе хирургического вмешательства. Этот подход к лечению до сих пор вызывает вопросы у многих специалистов, однако в ряде случаев он показан избранным пациенткам с метастатическим раком яичников, которым по какой-либо причине нежелательно сразу ложиться на операцию.
К сожалению, 5-летняя выживаемость без признаков рецидива наблюдается менее, чем в 10% случаев, – даже несмотря на лечение паклитакселом и препаратом на основе платины. Так как у многих пациенток рак рецидивирует даже после стандартной терапии, врачам и больным следует задуматься об участии в клинических испытаниях. Во многих научных исследованиях изучаются инновационные методы первичной терапии метастатического рака.
Лечение в онкоцентре Ихилов не выходя из дома.
Как специалисты клиники лечат пациентов во время коронавируса.
Лікування в онкоцентрі Іхілов не виходячи з дому.
Як фахівці клініки лікують пацієнтів під час коронавируса.
Стратегии совершенствования лечения
Прогресс в лечении рака яичников стал достижимым благодаря совершенствованию методик лечения и тестированию новых стратегий и медикаментов в рамках клинических испытаний. В настоящее время ученые активно изучают несколько новых методик лечения этого заболевания.
- Препараты таргетной терапии

Препараты таргетной терапии – это противораковые медикаменты, которые нарушают особые сигнальные пути, участвующие в процессе роста и обеспечении выживаемости раковых клеток. Прием этих медикаментов можно сочетать с другими способами лечения рака, включая традиционную химиотерапию.
Ученые возлагают определенные надежды на новый таргетный препарат для лечения рака яичников – Авастин (бевацизумаб). Авастин замедляет или предотвращает рост новых кровеносных сосудов, ингибируя белок под названием VEGF. Тем самым он лишает раковые клетки кислорода и питательных веществ. Воздействуя на сосуды, препарат облегчает поступление химиотерапевтических средств к раковой опухоли.
- Консолидирующая терапия
Консолидирующая, или поддерживающая, терапия – это дополнительная химиотерапия, назначаемая по завершении стандартного курса. В настоящее время проводятся клинические исследования, в ходе которых ученые пытаются более подробно изучить особенности данной методики. Основной вопрос звучит следующим образом: повышает ли такая терапия выживаемость пациенток с метастатическим раком яичников – и если да, стоит ли ради этого подвергать больных потенциальным рискам, связанным с побочными эффектами в результате продолжительного лечения?
- Интраперитонеальная химиотерапия
Данная методика позволяет уничтожить множество раковых клеток за счет обработки всей брюшной полости химиотерапевтическими препаратами. Лекарства поступают через большой катетер , устанавливаемый внутрь брюшной полости во время операции по удалению опухоли. Наибольшая эффективность интраперитонеальной химиотерапии наблюдается после хирургического удаления всех островков раковых тканей, превышающих размером 1 см. (Такое хирургическое вмешательство называется оптимальной циторедукцией.)
В ходе клинического испытания третьей фазы ученые сравнили эффективность 2 подходов к лечению женщин с раком яичников III стадии, перенесших оптимальную циторедукцию:
- одна группа пациенток лечилась только химиотерапевтическими препаратами для внутривенного введения;
- в стратегию лечения второй группы женщин добавили интраперитонеальную химиотерапию.
- Химиотерапия с сокращенными интервалами
Применение нескольких разных однокомпонентных режимов химиотерапии с сокращенными интервалами и максимально возможными дозировками повышает действенность лечения и в некоторых случаях предотвращает развитие лекарственной устойчивости у раковых клеток.
Недавно ученые провели клиническое испытание с целью оценки режима химиотерапии, состоящего в применении 3 лекарств с сокращенными интервалами и показанного пациенткам с метастатическим раком яичников. Схема состояла из четырех курсов Платинола и Гикамтина с последующими четырьмя курсами Платинола и паклитаксела. (Пациентки перенесли хирургическую операцию либо до химиотерапии, либо между курсами.) На основе полученных данных ученые зафиксировали полное или частичное исчезновение признаков рака почти у 80% участниц исследования.
- Высокодозная химиотерапия и аутологичная трансплантация стволовых клеток

Химиотерапия атакует и уничтожает быстро делящиеся клетки – в том числе раковые. Высокодозная химиотерапия убивает больше злокачественных клеток, чем традиционная химиотерапия с низкими дозами.
К сожалению, высокодозная химиотерапия также уничтожает больше здоровых клеток, в особенности кроветворящих стволовых клеток в костном мозге. Стволовые клетки – это незрелые клетки, вырабатываемые костным мозгом – губчатым веществом внутри костей. Стволовые клетки рано или поздно превращаются либо в эритроциты, доставляющие кислород к тканям, либо в лейкоциты, борющиеся с инфекциями, либо в тромбоциты, способствующие свертыванию крови.
Высокодозная химиотерапия уничтожает и раковые, и здоровые стволовые клетки. Разрушение костного мозга приводит к уменьшению запасов стволовых клеток, а следовательно – и к снижению уровней циркулирующих кровяных телец. Когда уровни циркулирующих кровяных телец становятся критическими, развиваются осложнения:
- анемия
- инфекции
- кровоизлияния
Так как все эти осложнения могут привести к летальному исходу, необходимо как можно скорее восстановить уровни кровяных телец. Именно поэтому большинству пациенток, перенесших высокодозную химиотерапию, назначают трансплантацию стволовых клеток.
Исследователи, ведущие Регистр аутологичных трансплантатов крови и костного мозга, оценили результаты лечения более 400 женщин с метастатическим раком яичников, перенесших высокодозную химиотерапию и аутологичную трансплантацию стволовых клеток. Спустя 2 года после лечения в живых остались 35% участниц данного исследования.
Более того: ученые выделили подгруппу, в рамках которой двухлетняя выживаемость составила 55%. В эту подгруппу вошли более молодые женщины с раком определенного микроскопического типа (несветлоклеточным), не страдающие иными заболеваниями. Они перенесли высокодозную химиотерапию и аутологичную трансплантацию стволовых клеток во время первой ремиссии.
Результаты исследования указывают на потенциальное повышение показателей выживаемости благодаря высокодозной химиотерапии и аутологичной трансплантации стволовых клеток. Эта стратегия особенно эффективна при условии ее применения на начальных этапах курса лечения.
- Комбинированные подходы
Комбинирование двух и более стратегий лечения – это наиболее перспективное направление научной работы. Так, пациентка получает наибольший шанс на полную ремиссию, если курс ее лечения состоит из следующих процедур:
- индукционной химиотерапии с сокращенными интервалами,
- интервальной циторедукции и высокодозной химиотерапии,
- аутологичной трансплантации стволовых клеток.
Пациенткам, достигшим ремиссии, показано дополнительное лечение в виде поддерживающей химиотерапии или применения средств биологической терапии. Многие комбинированные подходы в настоящее время тестируются в клинических испытаниях.
Выбирая метод лечения, нужно задать врачу следующие вопросы:
- Доказано ли, что инновационная методика лучше традиционного подхода? Так как рецидив наблюдается более, чем у 50% пациенток с раком яичников IV стадии, не стоит сравнивать такие показатели, как ответная реакция на химиотерапию, средняя выживаемость или выживаемость без рецидивов.
- Если вы выбираете стратегию лечения, лучше сравнить число (процент) пациенток, проживших 3-5 лет после лечения – с рецидивами или без таковых. Это наилучший показатель эффективности того или иного подхода.
- Что известно о рисках или побочных эффектах нового метода? Важно понимать, что чем больше вы лечитесь, тем сильнее становятся побочные эффекты. Так как первичная терапия практически не помогает пациенткам с метастатическим раком яичников, не стоит надолго откладывать принятие решения о лечении новыми методами. В противном случае повышается риск тяжелых побочных эффектов при меньшей действенности терапии.

В сентябре 2015 года я почувствовала комок в левой груди. Я не паникер, но я знала, что это может значить. У меня была назначена встреча через месяц с моим акушером-гинекологом, поэтому сначала я подумала, что подожду и поговорю об этом со своим врачом.
У меня была маммография всего шесть месяцев назад. Но после изучения информации в интернете, я поняла, что для безопасности нужно встретиться с врачом раньше.

За пять лет до того, как мне поставили диагноз, я тренировалась четыре раза в неделю и была в отличной форме. Друзья заметили, что я сильно похудела, но я просто думала, что это связано с моим активным образом жизни. В это время у меня постоянно были проблемы с желудком. Мои врачи рекомендовали безрецептурные препараты.
В течение месяца у меня также была постоянная диарея. Мои врачи не нашли ничего плохого.

В начале 2016 года я воспользовалась советом врача и сделала колоноскопию. Я никогда этого не делала до этого. Мой доктор показал мужу, и мне изображение толстой кишки. На изображении были видны два полипа. Врач указал на первое место на моей толстой кишке, заверив нас, что беспокоиться не о чем. Затем он указал на другое место и сказал нам, что, по его мнению, есть подозрение на рак. Во время процедуры он сделал биопсию, и ткань была проанализирована.

В 2011 году у меня начался кислотный рефлюкс. Это было неудобно и тревожно, поэтому я пошел к нашему семейному врачу для обследования. Во время визита он спросил меня, когда я в последний раз проверял свой антиген пса, рутинный тест, который многие мужчины делают, чтобы проверить возможные признаки рака простаты. Прошло около трех лет с тех пор, как я делал этот тест, поэтому он добавил его к моему визиту в тот день.

Моя история начинается с онемения. Однажды в 2012 году три пальца на моей левой руке внезапно потеряли чувствительность. Я сразу же записался на прием к врачу. К тому времени, когда врач меня смог принять, уже все прошло, но жена убедила меня все-таки пойти на консультацию. У меня был рентген, чтобы увидеть, есть ли какие-либо признаки повреждения позвоночника, возможно, от вождения грузовика. Когда на пленке появились какие-то.

Зимой 2010 года, когда мне было 30 лет, я почувствовала внезапную боль в правом боку. Боль была резкой и началась без предупреждения. Я сразу же отправилась в ближайшую больницу.
Врач получил результаты моего анализа крови, и он увидел, что мой уровень лейкоцитов был чрезвычайно повышен. Врач и другие, кто видел эти результаты, были встревожены и попросили гинеколога по вызову приехать ко мне сразу же.

Около трех лет я боролся с прерывистым кашлем. Он появлялся зимой и исчезал к весне, а потом я забывал о нем. Но осенью 2014 года это произошло раньше. В октябре моя жена позвонила местному пульмонологу. Первая встреча нам назначили через три месяца.
. В онкоцентре Ихилов мы встретились с торакальным хирургом. Решили полностью удалить узелок.
Стоимость диагностики и лечения рака яичников в Израиле
Для удобства пациентов из-за рубежа приведем цены в долларах на некоторые диагностические и лечебные процедуры, которые назначаются в онкоцентре Ихилов при раке яичников.
Чтобы узнать точную стоимость лечения рака в Израиле, заполните заявку. В ближайшие 2 часа в сами свяжется врач онкоцентра. Он задаст вам необходимые вопросы и сообщит точную стоимость лечения. Получить информацию вы можете также по телефону: +972-3-376-03-58 в Израиле и +7-495-777-6953 в России.
Читайте также:

