Климов а в рак почки
Полный текст:
- Аннотация
- Об авторах
- Список литературы
- Cited By
Цель исследования – оценка роли паллиативной нефрэктомии у больных диссеминированным раком почки, которым планируется проведение таргетного антиангиогенного лечения.
Материалы и методы. В исследование включены данные 83 больных диссеминированным почечно-клеточным раком Т1 – Т4N0 / +M1, которые получили не менее 2 курсов анти-VEGF / VEGFR-терапии с 2009 по 2011 г. До начала лечения паллиативная нефрэктомия выполнена 48 (57,8 %) пациентам, в 35 (42,2 %) случаях первичную опухоль не удаляли. До начала таргетной терапии во всех случаях подтвержден диагноз светлоклеточного почечно-клеточного рака (с саркоматоидным компонентом – 7; 8,4 %). Медиана наблюдения за всеми пациентами составила 21 (12–36) мес.
Результаты. Медиана беспрогрессивной (БПВ) и общей выживаемости (ОВ) всех 83 больных на фоне 1-й линии антиангиогенной терапии составила 6,8 (5,3–8,5) и 23,4 (13,8–32,9) мес соответственно. Неудаленная пораженная почка у больных диссеминированным раком почки, получающих таргетную антиангиогенную терапию, – независимый фактор неблагоприятного прогноза БПВ (медиана 3,9 мес против 8,9 мес соответственно; отношения рисков (ОР) 2,4; 95 % доверительный интервал (ДИ) 1,2–4,7) и ОВ (медиана 12,5 мес против 29,1 мес соответственно; ОР 2,8; 95 % ДИ 1,3–6,3).
Выводы. Паллиативная нефрэктомия у отобранных больных диссеминированным раком почки, получающих таргетную антиангиогенную терапию, увеличивает БПВ и ОВ.
1. Coppin C., Porzsolt F., Autenrieth M. et al. Immunotherapy for advanced renal cell cancer. Cochrane Database Syst Rev 2005, p. CD001425.
2. Flanigan R.C., Salmon S.E., Blumenstein B.A. et al. Nephrectomy followed by interferon alfa- 2b compared with interferon alfa-2b alone for metastatic renal-cell cancer. N Engl J Med 2001;345:1655–9.
3. Mickisch G.H., Garin A., van Poppel H. et al. European Organisation for Research and Treatment of Cancer (EORTC) Genitourinary Group Radical nephrectomy plus nterferonalfa- based immunotherapy compared with interferon alfa alone in metastatic renal-cell carcinoma: a randomised trial. Lancet 2001;358:966–70.
4. Flanigan R.C., Mickisch G., Sylvester R. et al. Cytoreductive nephrectomy in patients with metastatic renal cancer: a combined analysis. J Urol 2004;171:1071–6.
5. Coppin C., Le L., Porzsolt F. et al. Targeted therapy for advanced renal cell carcinoma. Cochrane Database Syst Rev 2008;(2):CD006017.
6. Conti S.L., Thomas I.C., Hagedorn J.C. et al.Utilization of cytoreductive nephrectomy and patient survival in the targeted therapy era. Int J Cancer 2014;134:2245–52.
7. Escudier B., Bellmunt J., Negrie S. et al. Phase III trial of bevacizumab plus interferon alfa_2a in patients with metastatic renal cell carcinoma (AVOREN): Final analysis of overall survival. J Clin Oncol 2010;28:2144–50.
8. Rini B., Halabi S., Rosenberg J. et al. Phase III trial of bevacizumab plus interferon alfa versus interferon alfa monotherapy in patients with metastatic renal rell carcinoma: final results of CALGB 90206. J Clin Oncol 2010;28:2137–43.
9. Motzer R.J., Hutson T.E., Tomczak P. et al. Sunitinib versus interferon alfa in metastatic renal_cell carcinoma. N Engl J Med 2007;356:115–24.
10. Hudes G., Carducci M., Tomczak P. et al. Temsirolimus, interferon alfa, or both for advanced renal–cell carcinoma. N Engl J Med 2007;356:2271–81.
11. Escudier B., Eisen T., Stadler W.M. et al. Sorafenib for treatment of renal cell carcinoma: Final efficacy and safety results of the phase III treatment approaches in renal cancer global evaluation trial. J Clin Oncol 2009;27:3312–8.
12. Sternberg C., Davis I., Mardiak J. et al. Pazopanib in locally advanced or metastatic renal cell carcinoma: results of a randomized phase III trial. J Clin Oncol 2010;28:1061.
13. Motzer R.J., Escudier B., Oudard S. et al. Efficacy of everolimus in advanced renal cell carcinoma: a doubleblind, randomized, placebo_controlled phase III trial. Lancet 2008;372:449–56.
14. Abdollah F., Sun M., Thuret R. et al. Mortality and morbidity after cytoreductive ephrectomy for metastatic renal cell carcinoma: a populationbased study. Ann Surg Oncol 2011;18:2988–96.
15. Chapin B.F., Delacroix S.E., Culp S.H. et al. Post operative complications from cytoreductive nephrectomy after pre-surgical targeted therapy for metastatic renal cell carcinoma. AUA Annual Meeting, 2011.
16. Beck J., Procopio G., Bajetta E. et al. Final results of the European Advanced Renal Cell Carcinoma Sorafenib (EU-ARCCS) expandedaccess study: a large open-label study in diverse community settings. Ann Oncol 2011;22(8):1812–23.
17. Heng Daniel Y.C., Wells J. Connor, Rini Brian I. Cytoreductive nephrectomy in patients with synchronous metastases from renal cell carcinoma: Results from the International Metastatic Renal Cell Carcinoma Database Consortium. Eur Urol 2014;66:704–10.
18. Choueiri T.K., Xie W., Kollmannsberger C. et al.The impact of cytoreductive ephrectomy on survival of patients with metastatic renal cell carcinoma receiving vascular endothelial growth factor targeted therapy. J Urol 2011;185:60–6.
19. Warren M., Venner P.M., North S. et al. A population-based study examining the effect of tyrosine kinase inhibitors on survival in metastatic renal cell carcinoma in Alberta and the role of nephrectomy prior to treatment. Can Urol Assoc J 2009;3(4):281–9.
20. Heng M., Xie W., Regan M.M. et al. Prognostic factors for overall survival in patients with metastatic renal cell carcinoma treated with vascular endothelial growth factor-targeted agents: results from a large, multicenter study. J Clin Oncol 2009;27:5794–9.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.

- Опухоли почки
- Метастазы рака почки
- Как часто и у кого встречается рак почки?
- Диагностика опухолей почек
- Лечение рака почки на разных стадиях
- Цены в Европейской онкологической клинике на лечение рака почки
Опухоли почки
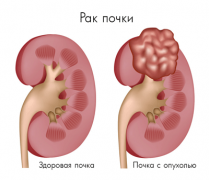
Второй характеристикой опухоли почки, как впрочем и большинства других опухолей, является потеря спецификации клетки – так как клетка быстро делится, она просто не успевает специализироваться. Таким образом, опухоль почки в первом приближении можно характеризовать, как массу клеток, бесконтрольно делящихся и потерявших способность к специализации. Чем меньше специализирована клетка опухоли для выполнения своей функции, чем быстрее она делится и чем больше его способность к распространению по кровеносным и лимфатическим сосудам, тем опухоль злокачественнее.
Почти 90 % опухолей почки злокачественны. Оставшиеся 10 процентов приходятся на ангиомиолипомы и другие, гораздо более редкие доброкачественные опухоли почки. Между тем, даже доброкачественные опухоли почки вполне могут быть опасны для здоровья. Например – ангиомиолипома может повредить сосуды почки, вызывая кровотечение. Что же касается злокачественных опухолей или рака почки, то тут мы сталкиваемся с повреждением функционирующей почечной ткани, ее сосудов и кровотечением, с метастазированием в кости, легкие, головной мозг и, соответственно, нестерпимыми болями.
Метастазы рака почки
Метастазирование — это распространение опухоли по кровеносным или лимфатическим сосудам. Опухоли, как и всему живому в организме, требуется питание, обеспечиваемое сосудами. Вот в эти сосуды и попадают 1-2 клетки из основной опухоли, которые распространяются на различные органы. Для рака почки характерно метастазирование в кости и легкие, а также в печень, надпочечники и головной мозг.
рака почки, как и основная опухоль, нарушает функцию органа, где развивается. Например, метастаз рака почки в легкие вызывает упорный кашель, метастаз в кости — страшные, изнуряющие боли, от которых помогают только сильнодействующие наркотические препараты. К сожалению, часть пациентов, обративших к врачу, уже имеют отдаленные метастазы в тех или иных органах. Это резко ухудшает прогноз течения заболевания, так как приходится бороться не с одной опухолью, а, по сути, с опухолями множеством опухолей в нескольких органах.
Как часто и у кого встречается рак почки?
Диагностика опухолей почек
При подозрении на рак почки пациенту назначают общий анализ мочи, общий и биохимический анализы крови.
Один из наиболее информативных методов диагностики рака почки – компьютерная томография. Она помогает оценить размер, форму и локализацию злокачественного новообразования, обнаружить очаги в лимфатических узлах и других анатомических структурах за пределами почек. Исследование нередко дополняют внутривенным контрастированием. Введение контраста противопоказано при нарушении функции почек.
Магнитно-резонансную томографию применяют реже, чем КТ. Она показана, когда пациенту нельзя проводить компьютерную томографию с контрастом, если имеется подозрение на прорастание опухоли в нижнюю полую вену или другие крупные сосуды, для обнаружения метастатических очагов в головном и спинном мозге.

Ангиография – рентгенография с контрастирование сосудов, почки. Она помогает в диагностике заболевания и планировании хирургического лечения.
Позитронно-эмиссионная томография помогает обнаружить вторичные очаги рака в различных частях тела. Суть метода в том, что в организм пациента вводят вещество, которое обладает слабой радиоактивностью и накапливается в опухолевых клетках. Затем выполняют снимки с помощью специального аппарата, и на них опухолевые очаги хорошо видны.
В отличие от других онкологических заболеваний, биопсия при раке почки проводится редко. Обычно результатов других исследований хватает для того, чтобы принять решение о необходимости хирургического вмешательства. Уже после операции удаленную опухоль направляют в лабораторию, чтобы подтвердить диагноз. Биопсию проводят, если другие исследования не позволяют разобраться, показана ли операция. В случаях, когда хирургическое вмешательство противопоказано, исследование опухолевой ткани помогает определиться с тактикой лечения.
В медицине нет категоричных, стопроцентных ответов. Какова цель операции по удалению рака почки? Удалить опухоль? Удалить почку с подлежащими структурами? Удалить только первичный очаг опухоли, а потом бороться с метастазами теми или иными способами? Перенесет ли пациент операцию, каково его общее состояние? Какую именно операцию выбрать для конкретного больного? На эти вопросы должен ответить онкоуролог, перед тем, как предложить хирургическое, консервативное или комбинированное лечение. В основном, это зависит от стадии рака почки, расположения опухоли, наличия метастазов в лимфатические узлы и общего состояния здоровья пациента.

Это зависит главным образом от стадии, на которой была диагностирована опухоль, и начато лечение. Пятилетняя выживаемость (процент пациентов, оставшихся в живых спустя 5 лет) наиболее высока для I стадии и составляет 81%. На II и III стадиях она, соответственно, составляет 74 и 53%. При IV стадии — 8%.
Стадия рака почки зависит от размеров и расположения опухоли. Так, рак почки первой стадии — это опухоль меньше 7 см, не выходящая за пределы почки. Рак почки второй стадии — это опухоль меньше 10 см, также не выходящая за пределы почки. А вот рак почки третьей стадии — это уже опухоль любых размеров, ограниченная почкой, либо повреждающая надпочечник, почечную вену, но имеющую метастаз в ближайших лимфатических узлах. Рак почки четвертой стадии может быть любых размеров, однако при этой стадии опухоль либо выходит за пределы почечной фасции, либо имеются больше одного метастаза в ближайших лимфатических узлах, либо имеются метастазы в легкие, кости, печень или головной мозг.
Стадию рака почки определяют в соответствии с международной классификацией TNM. Рядом с каждой из трех букв аббревиатуры указывают индекс, описывающий характеристики первичной опухоли (T), поражение регионарных лимфатических узлов (N), наличие отдаленных метастазов (M):
T1 – опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр не более 4 см (T1a) или 4–7 см (T1b).
T2 - опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр 7–10 см (T2a) или более 10 см (T1b).
T3 – злокачественное новообразование распространяется на почечную вену и ее ветви, на надпочечник на одноименной стороне, паранефральную клетчатку, не прорастая фасцию Героты (T3a), на нижнюю полую вену ниже (T3b) или выше (T3c) диафрагмы или врастает в стенку вены.
T4 – опухоль распространяется за пределы фасции Героты.
N0 – опухолевые очаги в регионарных лимфоузлах отсутствуют.
N1 – обнаруживается опухолевый очаг в одном лимфоузле.
N2 – обнаруживаются опухолевые очаги в двух и более регионарных лимфоузлах.
M0 – отдаленных метастазов нет.
M1 – отдаленные метастазы присутствуют.
В зависимости от значений T, N и M, выделяют четыре стадии рака почки:
- Стадия I: опухоль в почке не более 7 см (T1), лимфоузлы не поражены, отдаленных метастазов нет.
- Стадия II: первичная опухоль более 7 см (T2), отсутствуют очаги поражения в лимфатических узлах и отдаленные метастазы.
- Стадия III: злокачественная опухоль распространяется на соседние структуры (T3) и/или поражен один регионарный лимфатический узел (N1).
Стадия IV: опухоль распространяется на соседние структуры (T4), либо поражено 2 и более регионарных лимфоузла (N2), либо обнаружены отдаленные метастазы (M1).
Опухоль почки размером 2 см может быть расположена вблизи почечных сосудов и ее удаление технически может быть невозможным. Однако данные литературы указывают, что если нет метастазов в лимфатические узлы и отдаленные органы, то опухоль почки до 7 см можно удалять с сохранением почки, что, безусловно, лучше полного удаления почки и инвалидизации пациента.
Лечение рака почки на разных стадиях
Выбор тактики лечения при раке почки в первую очередь определяется стадией опухоли и состоянием здоровья пациента.
При стадиях I и II возможно хирургическое лечение. Стандартным вариантом считается нефрэктомия. К органосохраняющим операциям прибегают реже, в частности, при опухолях в единственной почке. Кроме того, на выбор объема операции влияет размер опухоли. Также удаляют близлежащие лимфатические сосуды, особенно если они увеличены, окружающую жировую клетчатку.
При III стадии рака почки основным методом лечения также является нефрэктомия, при этом должны быть удалены все регионарные метастазы. Если опухоль прорастает в почечную или нижнюю полую вену или мигрирует в их просвете в виде опухолевого тромба, пораженные ткани также нужно удалить, при этом может потребоваться подключение пациента к аппарату искусственного кровообращения.
При высоком риске рецидива после операции применяют адъювантную терапию таргетным препаратом сунитинибом. Пациенты получают его в течение года.
Если хирургическое вмешательство противопоказано, прибегают к радиочастотной аблации, эмболизации.
На IV стадии подходы к лечению могут быть разными, в зависимости от степени распространения рака в организме. В некоторых случаях возможно хирургическое лечение, в том числе циторедуктивные операции, во время которых хирурги не могут убрать опухоль полностью, но стараются удалить как можно больший ее объем. В редких случаев возможно удаление основной опухоли в почке и единичных вторичных очагов в других органах. После операции назначают курс таргетной терапии, иммунотерапии.
При неоперабельном раке почки основными методами лечения становятся иммунотерапия и таргетная терапия.

В некоторых случаях рак почки удается выявить на ранних стадиях, когда опухолевые клетки не распространяются за пределы органа. Но зачастую заболевание диагностируют на более поздних стадиях. Во-первых, это связано с тем, что рак почки может очень долго протекать бессимптомно. Во-вторых, для этого типа рака на данный момент не существует рекомендованных скрининговых исследований.
Все симптомы можно разделить на ренальные (связанные с поражением почек) и экстраренальные.
Среди ренальных проявлений рака почки наиболее характерны три:
- Гематурия (примесь крови в моче) – самый распространенный и зачастую первый симптом. Он возникает более чем у половины пациентов с раком почки. Моча приобретает красный цвет, при этом боль не беспокоит либо носит острый характер и возникает после гематурии. Этим злокачественная опухоль отличается от неопухолевых заболеваний почки, например, мочекаменной болезни, при которой обычно сначала возникает боль, а потом появляется примесь крови в моче. Гематурия периодически исчезает, но через некоторое время снова появляется, причем, промежутки между кровотечениями сокращаются. Количество крови в моче не зависит от размеров опухоли.
- Боли беспокоят около половины пациентов. Острая боль после гематурии возникает из-за того, что сгустки крови перекрывают просвет мочеточника. Тупые сильные боли зачастую говорят о плохом прогнозе.
- Пальпируемая опухоль – симптом, который выявляет врач во время осмотра примерно у трети пациентов.
Все три симптома одновременно встречаются у одного из десяти пациентов с раком почкеи. Обычно при этом выявляют запущенные опухоли.
Среди экстраренальных симптомов в первую очередь стоит отметить повышение температуры тела. У 5% больных лихорадка – единственное проявление заболевания. У некоторых пациентов повышается артериальное давление, отмечается покраснение лица из-за увеличения количества эритроцитов в крови, у мужчин – расширение вен мошонки (варикоцеле). На поздних стадиях снижается аппетит, пациент теряет вес без видимой причины, постоянно ощущает утомление, недомогание.
Распространенная патология
На современном этапе рак почки считается одним из часто встречаемых онкологических заболеваний. И за последние годы можно отметить значимый прирост в выявлении опухолей этой локализации. Связано это с тем, что, конечно же, улучшилась инструментальная диагностика. Если раньше выявлялись преимущественно метастатические формы патологии, то сегодня довольно много больных с первичными локализованными и местно-распространенными формами заболевания. А это значит, что большему числу пациентов возможно провести операцию на ранней стадии, тем самым гарантируя в большинстве случаев полное выздоровление.
Однако при этом, к сожалению, остается довольно высокий процент больных с метастатическими формами заболевания — приблизительно каждый четвёртый пациент с впервые выявленным раком почки уже имеет метастазы в лимфоузлы или другие органы. Это усложняет лечение, так как необходимо проводить не только операцию, но и различные варианты системной терапии.
Также есть и такой нюанс — у каждого третьего пациента, которому на ранних стадиях заболевания выполнялось только одно хирургическое вмешательство, в течение последующих 5 лет (срок, признанный усредненным для оценки состояния человека с онкологическим заболеванием) появляются отдаленные метастазы. И им все равно в итоге приходится проводить системное лечение.

Факторы риска
Конечно же, многих интересуют факторы, которые могут поспособствовать развитию данной проблемы. Итак, если говорить про пол, то мужчины болеют раком почки в два раза чаще, чем женщины.
Если рассматриваем возраст, то и тут есть зависимость. Чем старше человек, тем выше риски. Частота встречаемости рака почки у тридцатилетних в разы меньше, чем у пятидесятилетних.
Из числа провоцирующих факторов на первом месте стоит наследственность и генетическая предрасположенность. Так, триггером запуска онкопроцесса в почке может служить ген VHL. Кроме того, негативным фактором является и окружающая среда. Спровоцировать рак почки могут радиация, химические производства, коррозийные производства.
Не стоит злоупотреблять и приемом нестероидных противовоспалительных средств, которые большинству известны как обезболивающие препараты. Они также могут влиять на частоту возникновения рака почки.
Определенным образом может влиять и питание. Да, этот фактор не самый значимый, но все же.
При этом довольно часто мы встречаем пациентов с раком почки, у которых он диагностируется независимо от связи с этими перечисленными факторами. Триггерами для развития рака почки могут служить такие сопутствующие патологии, как сахарный диабет, гипертония или какое-либо имеющееся у больного системное заболевание. Также спровоцировать проблему может доброкачественное образование почки, например аденома, или длительное воспаление органа — тот самый пиелонефрит. Киста почки озлокачествляется достаточно редко, поэтому при постановке такого диагноза впадать в панику не стоит, главное, просто вовремя проводить контрольные обследования.
Если мы говорим про поражение органа, чаще всего рак почки бывает односторонним. Очень редко бывает, чтобы в процесс вовлекались одновременно обе почки.
Что касается рецидивов, они напрямую зависят от стадии заболевания и степени дифференцирования опухоли. Чем более злокачественная опухоль, тем чаще она приводит к рецидиву заболевания.
Симптомы
Раньше, когда опухоль почки обнаруживалась на поздних стадиях, симптомами заболевания были боль в животе, кровь в моче и пальпируемая опухоль. Сейчас эти признаки встречаются крайне редко. Чаще всего рак почки характеризуется бессимптомным течением и случайно выявляется при диспансеризации, как правило, при ультразвуковом исследовании.
Если же говорить о симптомах, на которые надо обратить внимание, то я бы назвал одним из наиболее частых признаков рака почки гипертонию. Тем, у кого отмечаются скачки давления, стоит выполнять ультразвуковое исследование для проверки состояния почек. Почему гипертония? Потому что опухолевые клетки вырабатывают белки, токсины, которые выбрасывают в кровоток, приводя к сужению сосудов. На этом фоне и начинается повышение давления.
Хирургическое лечение
Одним из основных методов лечения является операция. Раньше при обнаружении такой патологии удаляли орган сразу. Сегодня же перед хирургами стоит другая задача — сохранение органа. Тем более что большинству пациентов можно выполнять органосохраняющую операцию — частичное удаление почки с опухолью.
Однако пациентам не стоит переживать, если понадобится удалить одну почку целиком. В общей популяции 10% людей рождаются с одной почки и даже не знают об этом, пока не пройдут обследование по поводу другого заболевания. Можно сказать, у нас одна почка запасная — так природа распорядилась. Причем даже если у человека остается после операции лишь половина почки, этого будет вполне достаточно, чтобы она смогла осуществлять свою секреторно-выделительную функцию в полном объёме.
Систематическая терапия
Ранее при раке почки использовались различные препараты, которые имели низкую эффективность (химиотерапия, гормонотерапия и др.). С 2005 года началась эпоха таргетной терапии, к настоящему времени уже зарегистрировано 8 препаратов. А в последние годы активное распространение получила иммунотерапия. Она показывает высокую эффективность, в 2-3 раза превышающую таргетные препараты. Согласно проведённым исследованиям, каждый третий пациент с отдаленными метастазами, получающий иммунотерапию, может быть полностью излечен от метастатического рака почки. Еще лет 5-7 назад мы о таком мечтать не могли.

Профилактические мероприятия
Обследование после
Частота обследований после обнаружения и лечения рака почки напрямую зависит от стадии заболевания. Обычно после операции рекомендуется выполнять обследования 1 раз в три месяца в первый год, 1 раз в полгода во второй год, 1 раз в год с третьего года после хирургического лечения. Если же имеются метастазы, контроль должен проводиться чаще — компьютерную томографию необходимо выполнять не реже чем 1 раз в 12 недель. Это необходимо, чтобы отслеживать прогрессию или метастазирование.
Людям после операции и эффективного лечения можно вести обычный образ жизни. Единственное, чего стоит избегать — курения, так как оно негативно влияет на сосуды.
Серегин А.В., Шустицкий Н.А., Индароков Т.Р., Серегин А.А., Морозов А.Д., Мулабаев А.K.
Заболеваемость раком почки растет с каждым годом, в связи с этим данная патология в настоящее время является одной из основных проблем онкоурологии. На сегодняшний день рак почки занимает 10-е место по уровню заболеваемости среди злокачественных новообразований, а по уровню его прироста уступает только раку предстательной железы. Злокачественные новообразования почки (ЗНП) в 2013 году составили 3,9% всех злокачественных новообразований населения Российской Федерации, занимая 10-е ранговое место в структуре онкологической заболеваемости обоих полов [1]. По данным литературы каждый год в мире раком почки заболевает около 250 тысяч человек, а погибает от него 100 тысяч человек [2]. В Российской Федерации по данным статистики в 2013 году зарегистрировано 20 892 новых случаев заболевания почечно-клеточным раком (ПКР). По темпам прироста онкологической заболеваемости за последние 10 лет ПКР устойчиво занимает одно из ведущих мест (29,14%) [3].
Диагностика рака почки в последние годы претерпела существенные изменения, что связано главным образом с прогрессом методов лучевой диагностики [4]. Клинические признаки болезни в настоящее время перестали играть решающую роль в выявлении рака почки. В подавляющем большинстве наблюдений заболевание выявляется случайно на той стадии, когда клинических проявлений еще нет. Известная классическая триада симптомов (боль в пораженном органе, пальпируемое образование почки, макрогематурия) встречается в настоящее время редко и является свидетельством плохого прогноза заболевания. Развитие диагностической техники позволяет выявлять онкологический процесс на ранних стадиях, что дает возможность выполнять органосохраняющие операции.
В урологической клинике ГКБ им. С.П. Боткина разработана и внедрена методика протективной резекции почки с применением превентивных – гемостатических швов. Несомненным преимуществом данного метода является то, что данная методика позволяет выполнять операции без пережатия почечной ножки, в том числе и при центрально расположенных опухолях, что ведет к сохранению почечной функции и является основной задачей органосохраняющего лечения.
Цель исследования – демонстрация преимуществ применения превентивного – гемостатического шва при выполнении органосохраняющих операций.
МАТЕРИАЛЫ И МЕТОДЫ
В период с 2013 по 2015 гг. в урологической клинике ГКБ им. С.П. Боткина было выполнено 113 органосохраняющих операций у пациентов с опухолями почек. У 97% пациентов опухоль почки была выявлена случайно при выполнении ультразвукового исследования (УЗИ). Всем пациентам выполнена компьютерная томография (КТ) органов забрюшинного пространства с внутривенным контрастированием. У 100% пациентов выявлено накопление контрастного вещества в опухолях почек с увеличением плотности в артериальную фазу до 80±20 единиц HU.
Показания к выполнению органосохраняющего лечения разделяются на 3 группы: абсолютные, относительные и элективные. В настоящее время грань между относительными и элективными показаниями к органосохраняющим операциям на почке практически стерлась.
В нашем исследовании по абсолютным показаниям резекция почки выполнялась у 7,8% пациентов (наличие единственной функционирующей почки, пораженной опухолью, наследственные формы рака почки) и по относительным – у 91,2%.
Одним из основных показателей является расположение опухолевого узла в сегментах почки, так как именно центрально расположенные опухоли вызывают наибольшие затруднения при выполнении органосохраняющих операций. В нашем исследовании у большинства пациентов (47 больных) опухоль располагалась в центральном сегменте, что составило 41,6%. Опухоль верхнего сегмента выявлена у 36 (31,8%) пациентов, и у 30 (26,5%) пациентов опухоль располагалась в нижнем сегменте (рис. 1).
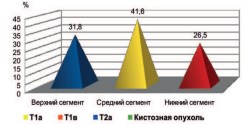
Рис. 1. Частота расположения опухолей в сегментах почки
Из 113 исследуемых пациентов 67 пациентов были мужчины, 46 пациентов – женщины. Средний диаметр опухоли равнялся 4,6 см. По стадиям опухолевого процесса пациенты распределялись следующим образом: стадия T1a установлена 57 пациентам, стадия T1b – 39 пациентам, стадия T2a – двум пациентам. Также в наше исследование вошли 15 пациентов с кистозными опухолями почек (IV стадия по Bosniak) (рис. 2).
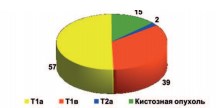
Рис. 2. Стадии опухолевого процесса
РЕЗУЛЬТАТЫ
Всем пациентам были выполнены органосохраняющие операции с применением превентивных швов.
Схематическоеизображение операции представлено на рисунке 3.
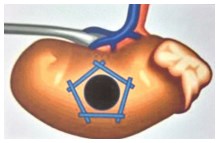
Рис. 3. Схематическое изображение методики с наложением превентивных швов
По всей окружности опухоли до проведения резекции почки производится наложение превентивных – гемостатических швов (рис. 4).
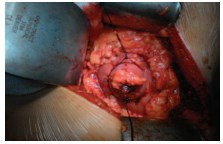
Рис. 4. Наложение превентивных швов по всей окружности опухоли
Следующим этапом является проведение резекции почки с опухолью с применением аргонового скальпеля в пределах заранее намеченной окружности (рис. 5).
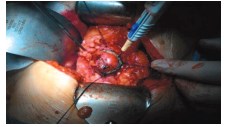
Рис. 5. Резекция почки с опухолью с применением аргонового скальпеля
После выполнения резекции и достижения гемостаза производится ушивание ложа опухоли чаще всего с применением прокладки. При ушивании паренхимы почки, наложенные превентивные швы позволяют избежать прорезывания нитей (рис. 6).
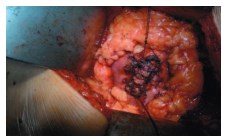
Рис. 6. Ушивание ложа опухоли
Основным ограничивающим фактором для выполнения органосохраняющих операций являются центрально расположенные опухоли, при которых существует риск значительной кровопотери, длительного пережатия почечной ножки и часто возникает необходимость реконструкции чашечно-лоханочной системы, что, соответственно, достаточно часто заставляет хирургов отказаться от выполнения органосохраняющих операций при центрально расположенных опухолях. При проведении оперативного лечения с применением превентивных гемостатических швов ни в одном случае мы не производили пережатия почечных артерии и вены, несмотря на то, что у большинства пациентов опухоль располагалась в центральном сегменте. Объем кровопотери в среднем при волнении непосредственно самой резекции составил 100 ± 20 мл.
В послеоперационном периоде всем пациентам проводилось полное клинико-лабораторное и инструментальное обследование. По данным ультразвукового исследования, проведенного на 3 и 5 сутки после операции, патологических и жидкостных образований в зоне резекции не выявлено. Уровень гемоглобина составил 114±10 г/л, средний уровень креатинина и мочевины – 86±15 ммоль/л и 5,4±2 ммоль/л, соответственно. Средний койко-день в послеоперационном периоде равнялся 7±2.
КЛИНИЧЕСКИЙ СЛУЧАЙ
В 41-е урологическое отделение ГКБ им. С.П. Боткина обратился пациент Б. По данным ультразвукового обследования от 06.03.2015 в паренхиме почки, между верхним и средним полюсом, частично экстраренально, диагностировано объемное солидное образование неправильной округлой формы, с четкими неровным контурами, с неоднородной гипоэхогенной структурой, размерами 42х50х45 мм (объем 50 см3 ), оттесняющее верхнюю группу чашечек. Признаков инвазии в почечный синус и почечную вену не выявлено (рис. 7).
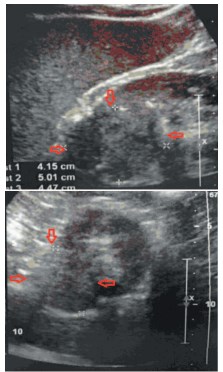
Рис. 7. Пациент Б. Ультразвуковое иследование: опухоли левой почки
Так же пациенту выполнена КТ с внутривенным контрастированием, по данным которой в верхнем полюсе левой почки определяется образование, исходящее из почечной паренхимы, с четкими наружными контурами, размером 41х45х52 мм, в нативную фазу средней плотностью 22 ед.Н., неоднородно накапливает контраст в артериальную фазу-до 56 ед.Н., в венозную-64 ед.Н., отсроченную фазу-45 ед.Н. (рис. 8.).
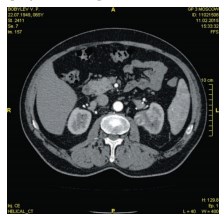
Рис. 8. Пациент Б. Компьютерная томография с внутривенным контрастированием. Опухоль верхнего полюса левой почки
После предоперационной подготовки пациенту выполнено оперативное лечение: резекция левой почки с опухолью с применением превентивных – гемостатических швов. Продолжительность операции составила 150 минут, время общей анестезии – 165 минут. Объем кровопотери при выполнении резекции – 50 мл. Почечная ножка при этом не пережималась. Интраоперационно осложнений не выявлено.
Послеоперационный период протекал без особенностей. Страховой дренаж удален на 2-е сутки после операции. По данным проведенного лабораторного обследования: гемоглобин – 120 г/л, уровень креатинина – 72 мкмоль/л, мочевина – 4,6 ммоль/л, по данным ультразвукового исследования, выполненного на 3-и и 7-е сутки после оперативного лечения, патологических образований в зоне резекции не выявлено. Пациент выписан из отделения на 7-е сутки после операции. Через год выполнена контрольная компьютерная томография: левая почка расположена в типичном месте, контуры ее ровные, четкие плотность паренхимы не изменена. ЧЛС не расширена. Данных за рецидив не выявлено (рис. 9).
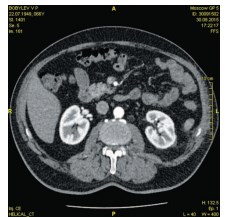
Рис. 9. Пациент Б. Компьютерная томография через один год после оперативного лечения. Данных за рецидив опухоли не выявлено
ЗАКЛЮЧЕНИЕ
Применение превентивных – гемостатических швов является эффективной и безопасной методикой органосохраняющего лечения ПКР, позволяющей избежать как интра -, так и послеоперационных осложнений. Проведение органосохраняющих операций у пациентов с центрально расположенными опухолями позволяет уменьшить количество радикальных нефрэктомий. Данная методика позволяет выполнять резекции почки почти при любом расположении опухоли, без пережатия почечной ножки, тем самым позволяя избежать негативное воздействие ишемии на почечную паренхиму, что ведет к сохранению максимального количества функционирующей паренхимы. Использование превентивных швов позволяет уменьшить количество местных рецидивов за счет лучшей визуализации операционного поля. Таким образом, мы рекомендуем технику применения превентивных-гемостатических швов для органосохраняющего лечения пациентов с ПКР.
ЛИТЕРАТУРА
1. Грицкевич А.А. Ильин С.А, Тимина И.Е., с соавт. Резекция почки ex vivo в условиях фармако – холодовой ишемии без пересечения мочеточника с ортотопической реплантацией сосудов при почечно-клеточномраке. Вестник урологии 2015; (3): 3 – 33.
2 Носов Д.А. Диссеминированный рак почки: современные возможности лекарственного лечения. Практическая онкология 2012; (3); 185-194.
3 Алексеев Б.Я., Нюшко К.М., Калпинский А.С. Неоадъювантная таргетная терапия у больных почечно-клеточным раком. Онкоурология 2015; (2): 23 – 33.
4. АляевЮ.Г.,АхвледианиН.Д.,ФиевД.Н., ПетровскийН.В. Возможностиметодов визуализации в диагностике имониторинге опухоли почки. Экспериментальная и клиническая урология 2011; (2-3): 96 – 97.
5 Capitanio U., Terrone C., Antonelli A., Minervini A., Volpe A., Furlan M. Nephronsparing techniques independently decrease the risk of cardiovascular events relative to radical nephrectomy in patients with a T1a-T1b renal mass and normal preoperative renal function. Eur Urol 2015 Apr; 67(4):683-689.
6 Huang W.C., Levey A.S, Serio A.M., Snyder M., Vickers A.J, Raj G.V., et al. Chronic kidney disease a?er nephrectomy in patientswith renal cortical tumours: a retrospective cohort study. Lancet Oncol 2006; 7(9):735-40.
7 Волкова М.И., Скворцов И.Я., Климов А.В., Комаров М.И., Черняев В.А., Матвеев В.Б. Функциональные результаты радикальной нефрэктомии при клинически локализованном раке почки. Экспериментальная и клиническая урология 2013; (4):16 – 20.
Читайте также:

