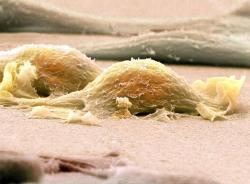
Клетки опухоли экспрессируют виментин
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Саркомы – это группа различных по клиническим и морфологическим признакам злокачественных новообразований, которые происходят из любых неэпителиальных тканей. В этом заключено основное отличие саркомы от рака, ростком которого являются эпителиальные клетки.
Риск возникновения данного заболевания повышается при некоторых генетических патологиях:
- синдром базальноклеточных невусов;
- синдром Вернера;
- синдром Гарднера;
- туберозный склероз;
- кишечный полипоз т.д.
А болезнь Реклингхаузена, или нейрофиброматоз 1 типа, является наиболее распространенным наследственным заболеванием, которое осложняется опухолевыми процессами. При этой патологии нейрофибросаркомы возникают примерно в 15% случаев. Описаны также случаи возникновения саркомы в зоне воздействия ионизированного излучения, как патологического, так и с лечебными целями.
Гистоморфологическая классификация сарком
Зачастую точно определить, из какой именно ткани возникла конкретная опухоль, довольно сложно. Кроме того, выделяется большая группа опухолей, которые имеют неясный гистогенез.
Наиболее часто диагностируются фибросаркомы, липосаркомы и рабдомиосаркомы. Вторыми по частоте встречаемости следует злокачественная гистиоцитарная саркома мягких тканей и саркомы неясного генеза. Ангиосаркомы, синовиальные саркомы, злокачественные шванномы, лейомиосаркомы и прочие типы наблюдаются редко.
Опухоли жировых тканей
Промежуточные (местно-агрессивные) формы:
- атипичный липоматоз;
- высокодифференцированные липосаркомы.
Злокачественные формы:
- недифференцированные липосаркомы;
- миксоидные липосаркомы;
- круглоклеточные липосаркомы;
- полиморфная липосаркома;
- липосаркомы смешанного типа;
- липосаркомы без признаков дифференцировки.
Миофибропластические и фибробластические опухоли
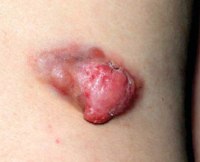
Промежуточные, или местно-агрессивные, формы:
- поверхностные подошвенные или ладонные фиброматозы;
- фиброматозы десмоидного типа;
- липофиброматозы.
Редко метастазирующие формы:
- солитарные фиброзные опухоли;
- гемангиоперицитомы, включая липоматозные гемангиоперицитомы;
- воспалительные миофибропластические опухоли;
- миофибропластические саркомы низкой степени дифференцировки;
- миксоидные фибропластические саркомы;
- инфантильные фибросаркомы.
Злокачественные формы:
- зрелые фибросаркомы;
- миксофибросаркомы;
- медленнорастущие фибромиксоидные саркомы;
- гиалинизирующие веретеноклеточные саркомы;
- склерозирующие эпителиоидные фибросаркомы.
Фиброгистиоцитарные опухоли
Промежуточные, или местно-агрессивные формы:
- плеоморфные фиброгистиоцитарные опухоли;
- гигантоклеточные саркомы мягких тканей.
Злокачественные формы:
- недифференцированные плеоморфные саркомы;
- недифференцированные плеоморфные саркомы с гигантскими клетками;
- недифференцированные плеоморфные саркомы с преобладанием воспаления.
Саркома мышечной ткани
Опухоли скелетных мышц:
- эмбриональные веретеноклеточные и анапластические рабдомиосаркомы;
- альвеолярные солидные и анапластические рабдомиосаркомы;
- плеоморфные рабдомиосаркомы.
Саркома гладких мышц: лейомиосаркома, включая и кожные формы.
Периваскулярные опухоли
- Злокачественные гломусные опухоли;
- миоперицитомы.
Сосудистые опухоли
Промежуточные, или местно-агрессивные формы: гемангиоэндотелиомы типа Капоши.
Редко метастазирующие формы:
- ретиформные гемангиоэндотелиомы;
- папиллярные внутрилимфатические ангиоэндотелиомы;
- смешанные гемангиоэндотелиомы;
- саркомы Капоши.
Злокачественные формы:
- эпителиоидные гемангиоэндотелиомы;
- гемангиосаркома мягких тканей.
Костно-хрящевые опухоли
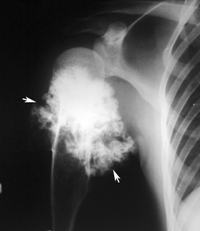
Опухоль костной ткани, или остеогенная саркома:
- обыкновенные: хондробластические, фибробластические, остеобластические;
- телеангиоэктатические;
- мелкоклеточные;
- центральные, имеющие низкую злокачественность;
- вторичные;
- параоссальные;
- периоссальные;
- поверхностные, имеющие высокую злокачественность.
Опухоли хрящевой ткани (хондросаркомы):
- центральные, первичные и вторичные;
- периферические;
- дедифференцированные;
- мезенхимальные;
- светлоклеточные.
Опухоли неясного происхождения
Редко метастазирующие формы:
- ангиоматоидные фиброзные гистиоцитомы;
- оссифицирующие фибромиксоидные опухоли;
- миоэпителиомы;
- парахондромы.
Злокачественные формы:
- синовиальная саркома;
- эпителиоидные саркомы;
- альвеолярная мягкотканная саркома;
- светлоклеточная саркома мягких тканей;
- внескелетные миксоидные хондросаркомы хордоидного типа;
- примитивные нейроэктодермальные опухоли (PNET);
- внескелетные саркомы Юинга;
- десмопластические мелко- и круглоклеточные опухоли;
- внепочечные рабдоидные опухоли;
- злокачественные мезенхимомы;
- миелоидная саркома;
- новообразования, имеющие периваскулярную эпителиоидно-клеточную дифференцировку (PEComa);
- светлоклеточные миомеланоцитарные опухоли;
- интимальные саркомы.
Каждый из названных гистологических типов отличается не только своими морфологическими признаками и гистогенезом, но также имеет определенное клиническое течение. Конечно, подобное многообразие морфологических форм сарком вызывает значительную трудность в их диагностике.
Еще больше гистологическое типирование сарком осложняется в детском возрасте. Обусловлено это тем, что у детей большая часть опухолей происходит из примитивных эмбриональных клеток (эмбриональная саркома) или клеток, которые еще не завершили свое гистогенетическое становление. Такие опухоли, имея большое разнообразие морфологических форм, зачастую не имеют четких признаков гистотиповой дифференцировки, характеризуются резкой анаплазией и вариабельностью клеточного состава. Вместе с тем часто наблюдается и обратная картина: новообразования различного происхождения часто имеют сходные признаки строения. Все это делает типирование опухолей значимой проблемой.
Распределение основных типов сарком по преобладанию в их составе
клеток определенной формы
Рутинная оценка сарком начинается с оценки общего строения опухоли, которая базируется, прежде всего, на ее "узнаваемости" при микроскопии. Описывается общая картина преобладания клеток определенной формы.
Опухоли, состоящие из округлых клеток:
- нейробластома;
- саркома Юинга/PNET;
- мезенхимальная хондросаркома;
- эмбриональная и альвеолярная рабдомиосаркома;
- десмопластичная круглоклеточная саркома;
- круглоклеточная липосаркома;
- малигнизированная рабдоидная опухоль.
Опухоли, состоящие из веретенообразных клеток:
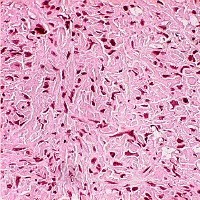
- фибросаркома;
- веретеноклеточная рабдомиосаркома;
- лейомиосаркома;
- злокачественные опухоли периферических нервных стволов;
- веретеноклеточная ангиосаркома;
- монофазная веретеноклеточная синовиальная саркома.
Опухоли, состоящие из эпителиоидных клеток:
- эпителиоидноклеточная синовиальная саркома;
- эпителиоидноклеточная ангиосаркома;
- эпителиоидноклеточные злокачественные опухоли нервного ствола;
- склерозирующая эпителиоидноклеточная фибросаркома;
- злокачественная фиброзная гистиоцитома;
- эпителиоидноклеточная лейомиосаркома.
Остальные гистоморфологические типы сарком, входящие в классификацию, имеют преимущественно смешанную форму клеток. Кроме того, иногда форма злокачественно перерожденных клеток не поддается описанию и определению. В таких случаях опухоль классифицируется как плеоморфная саркома.
Типирование сарком по степени дифференцировки клеток
После определения гистологического типа саркомы оценивается степень ее дифференцировки (G). При этом учитываются такие критерии, как клеточный полиморфизм, митотическая активность и др.
Степени дифференцировки сарком:
- GX – степень дифференцировки клеток определить невозможно;
- G1 – саркома высокодифференцирована;
- G2 – саркома дифференцирована умеренно;
- G3 – саркома низкодифференцирована;
- G4 – недифференцированая саркома.
Дифференциация клеток определяется возможностью установить, к какому именно виду ткани относится конкретная клетка. Чем ниже степень дифференциации клеток, составляющих опухоль, тем более выраженную злокачественность имеет данная саркома. Это напрямую связано с шансами раннего метастазирования в другие органы и ткани. Кроме этого, чем выше злокачественность саркомы, тем быстрее она увеличивается в размерах, тем большую инфильтративность имеет ее рост и тем стремительнее прогрессирует заболевание.
Иммуногистохимическое (ИГХ) типирование сарком
Иммуногистохимическое исследование позволяет:
- провести гистогенетическое типирование опухоли и определить нозологический вариант новообразования;
- определить органопринадлежность первичной опухоли при метастазах неизвестного происхождения;
- определить степень злокачественной трансформации клеток опухоли;
- прогнозировать течение опухолевого заболевания;
- прогнозировать чувствительность и резистентность опухолевых клеток к химиотерапевтическим препаратам и лучевой терапии;
- определить возможность проведения узконаправленной терапии.
Сегодня при верификации сарком используется несколько десятков основных ИГХ-маркеров. Поскольку практически нет ИГХ-маркеров, которые были бы специфичными только для какого-то конкретного типа опухоли, для типирования новообразования должен использоваться набор из нескольких антител.
1. В группу опухолей, состоящих из мелких округлых клеток, относятся новообразования, наиболее часто встречающихся в детском возрасте. Они обычно имеют низкую дифференцировку и высокую степень злокачественности.
- Бластная нейрогенная саркома. Все ее разновидности экспрессируют нейрональные маркеры, такие как нейронспецифическая энолаза (NSE), синаптофизин, хромогранины (CgA), СD56, СD57.
- Рабдомиосаркома. Все ее виды экспрессируют виментин, десмин и мышечный специфический актин (MA), а также СD99. Основными же ее специфическими маркерами является миогенные ядерные регуляторные протеины – миогенин и МуоD1.
- Основными диагностическими маркерами для саркомы Юинга и примитивной нейроэктодермальной опухоли являются СD99 (продукт гена MIC2) и Fli-1. Также клетки этих опухолей экспрессируют виментин, сравнительно часто - синаптофизин, в редких случаях - цитокератины (CK), CD57.
- Клетки мезенхимальной хондросаркомы экспрессируют виментин, S-100 протеин и, реже, СD57.
- Мелкоклеточная остеосаркома характеризуется экспрессией виментина, остеокальцина, может наблюдаться экспрессия СD57 и СD99.
- Мелкоклеточная низкодиференцированная синовиальная саркома мягких тканей, как и другие типы синовиальных сарком (монофазная веретеноклеточная синовиальная саркома, эпителиоидная синовиальная саркома, дедиференцированная полиморфноклеточная саркома), экспрессируют CK, эпителиальный мембранный антиген (EMA), виментин, коллаген IV типа.
- Десмопластическая мелкокруглоклеточная опухоль - очень редкий вид чрезвычайно агрессивного новообразования. Обычно клетки этой опухоли экспрессируют эпителиальные (СК и ЕМА), мезенхимальные (виментин), миогенные (десмин) и нейральные (СD56, NSE) маркеры.
2. К опухолям, состоящим из веретенообразных клеток, прежде всего относятся новообразования, развивающиеся из производных мезенхимы.
- Фибросаркома и инфантильная фибросаркома не имеют специфического иммунопрофиля, но всегда положительны к виментину, а иногда – и к SMA.
- Клетки лейомиосаркомы, как правило, экспрессируют виментин, десмин, МА, SMA, кальдесмон.
- Злокачественная опухоль оболочки периферического нервного ствола экспрессирует виментин, коллаген IV типа и СD57.
- Сосудистая эпителиоидно- и веретеноклеточная саркома, а также саркома Капоши экспрессируют Fli-1, CD31, CD34 и фактор фон Виллебранта (фактор VIII связывающий протеин).
- Гемангиоперицитома и солитарная фиброзная мягкотканая саркома относятся к новообразованиям, пограничным по своему потенциалу злокачественности. Их клетки обычно экспрессируют CD34, CD99, а также bcl-2.
3. Опухоли, состоящие из эпителиоидных клеток, характеризуются признаками, присущими специализированным клеточным элементам соединительной ткани (миофибробластам, эпителиоидным клеткам сосудов, миоэпителиальным клеткам).
- Злокачественная воспалительная миофибробластическая опухоль (воспалительная фибросаркома) демонстрирует иммунореактивность с кальпонином, SMA и десмином.
- Злокачественная фиброзная гистиоцитарная саркома характеризуется коэкспрессией виментина, EMA и CD68, в некоторых случаях наблюдается экспрессия MA, однако не экспрессируются миогенин и МиоD1.
- Периваскулярные эпителиоидноклеточные опухоли (PEC-омы) – это группа опухолей, к которым относятся: ангиомиолипома почек (и других локализаций), светлоклеточная саркома легких ("сахарная" опухоль), лимфангиолейомиоматоз и др. Клетки этих опухолей демонстрируют меланоцитарный иммунофенотип (положительны к: Мелан-А, НМВ45, тирозиназе) с коэкспрессией SMA.
- Эпителиоидная саркома коэкспрессирует виментин и СК.
Помимо гистогенетического типирования опухолей, принципиально важной задачей ИГХ является определение степени злокачественности опухоли и выявление прогностических маркеров. Это позволяет намного более обоснованно и достоверно прогнозировать течение болезни, а также чувствительность опухоли к лечебным средствам.
Медицинский эксперт статьи


Сегодня многие задаются вопросом, что представляют собой опухолевые клетки, какова их роль, представляют ли они опасность и приносят ли пользу, или исключительно направлены на уничтожение макроорганизма? Давайте разберемся в этом вопросе.
Трансформированные клетки, которые образуют злокачественную опухоль. Клетки претерпевают многочисленные изменения. Эти изменения ощутимы на морфологическом, химическом, биохимическом уровне. Некоторые видны даже невооруженным глазом. Обнаружение других же требует специального оборудования. Все зависит от типа и локализации.
Отличительной чертой является способность беспредельно увеличивать свою биомассу, что обусловлено нарушением апоптоза (обеспечивает программированную гибель). Заканчивается такой рост только вместе с гибелью человека.
Отличие опухолевой клетки от нормальной
Существует система клеточного апоптоза, который представляет собой запрограммированную гибель клеточного звена. Обычно клетка, прошедшая свой жизненный цикл, погибает. На ее месте со временем развивается новая субпопуляция клеточного цикла. Но при раковой трансформации такой естественный механизм нарушается, в результате чего эта клетка не погибает, а продолжает расти и функционировать в организме.
Именно такой внутренний механизм и является базовой основой формирования опухоли, обладающей тенденцией к бесконтрольному и неограниченному росту. То есть, по сути, подобного рода клеточная структура представляет собой клетку, не способную к гибели, и обладающую неограниченным ростом.

[1], [2], [3], [4], [5], [6], [7], [8]
Клеточный атипизм и атипичные клетки
Под атипичными клетками подразумевают клетки, подверженные мутации. Чаще всего атипичные клетки образуются под действием различных внешних факторов, или наследственности путем их трансформации из стволовых клеток. Чаще всего пусковым фактором развития опухолевой клетки является специфический ген, который кодирует гибель клетки. Некоторые потенциально онкогенные вирусы, например ретровирусы, герпесвирусы, способны вызывать трансформацию стволовых клеток в раковые.
Клеточный атипизм представляет собой собственно процесс трансформации, которому подвергаются здоровые клетки. Этот процесс включает в себя комплекс химических и биохимических процессов. Мутация осуществляется при условии нарушений иммунной системы, в особенности при аутоиммунных заболеваниях, при которых функция иммунной системы трансформируется таким образом, что он начинает вырабатывать антитела, направленные против клеток и тканей собственного организма. Развитию клеточного атипизма способствует ухудшение естественных защитных способностей организма, в частности, при нарушении активности Т-лимфоцитов (киллеров), нарушаются процессы гибели клеток, что приводит к их злокачественному перерождению.

[9], [10], [11], [12], [13], [14], [15], [16], [17], [18], [19], [20], [21]
Канцерогенез
Процесс потенциального разрастания тканей, что никаким образом не ассоциировано с нормальным состоянием организма. Канцерогенез подразумевает процесс перерождения нормальной клетки в опухолевую, которая есть локальным образованием, однако вовлекается весь организм. Характеристика - опухоли могут давать метастазы, бесконечно разрастаться.

[22], [23], [24], [25], [26], [27], [28], [29]
Раковая клетка под микроскопом
В основе развития раковой клетки лежит резкое увеличение ядра. Раковую клетку легко обнаружить под микроскопом, поскольку ядро в ней может занимать большую часть цитоплазмы. Также ярко выражен митотический аппарат, причем заметны его нарушения. В первую очередь обращает на себя внимание наличие хромосомных аббераций, нерасхождения хромосом. Это приводит к образованию многоядерных клеток, увеличению и утолщению ядра, переходу их в фазу митотического деления.
Также под микроскопом можно обнаружить глубокие инвагинации ядерной мембраны. При электронной микроскопии видны внутриядерные структуры (гранулы). Также в ходе световой микроскопии можно обнаружить потерю четкости контуров ядра. Ядрышки могут сохранять нормальную конфигурацию, могут увеличиваться к количественном и качественном отношении.
Происходит набухание митохондрий. При этом происходит уменьшение количества митохондрий, нарушаются митохондральные структуры. Также наблюдается диффузное расположение рибосом относительно эндоплазматической сети. В некоторых случаях возможно полное исчезновение аппарата Гольджи, но в некоторых случаях возможно и его гипертрофия. Происходит также изменение субклеточных структур, например меняется структура, внешний вид лизосом, рибосом. При этом происходит неодинаковая степень дифференциации клеточных структур.
В ходе микроскопии можно выявить низкодифференцированные и высокодифференцированные опухоли. Низкодифференцированные опухоли представляют собой бледные клетки, в состав которых входит минимальное количество органелл. Большую часть клеточного пространства занимает клеточное ядро. При этом все субклеточные структуры имеют различную степень зрелости и дифференциации. Для высокодифференцированных опухолей характерно сохранение исходной тканевой структуры.

[30], [31], [32], [33], [34], [35], [36]
Свойства и особенности опухолевых клеток
Если клетка становится опухолевой, нарушает ее генетическая структура. Это влечет за собой репрессионные процессы. В результате дерепрессии других генов происходит появление модифицированных протеинов, изоферментов, а также происходит клеточное деление. Это может изменить интенсивность генного и ферментного функционирования. Часто наблюдается репрессия белковых компонентов. Ранее они отвечали за специализацию клетки, активировались депрессией.
Элементы, выступающие в качестве триггеров, инициирующих патологический процесс. Есть предположение относительно того, что внедрение химических веществ осуществляется непосредственно в ДНК и РНК клеток. Это способствует нарушению созревания, развивается увеличение клеточной проницаемости, в результате чего потенциально онкогенные вирусы способны проникать в клетку.
Также пусковыми механизмами могут стать и некоторые физические факторы, такие как повышенный уровень радиации, облучение, механические факторы. В результате их воздействия происходит повреждение генетического аппарата, нарушение клеточного цикла, мутации.
Резко увеличивается потребление аминокислот, увеличивается анаболизм, тогда как катаболические процессы снижаются. Резко увеличивается гликолиз. Также происходит резкое снижение числа дыхательных ферментов. Наблюдается также изменение антигенной структуры опухолевой клетки. В частности, она начинает продуцировать белок альфа-фетопротеин.
Наиболее простым способом диагностики онкологического заболевания является сдача анализа крови на выявление онкомаркеров. Исследование проводится довольно быстро: 2-3 дня, в случае экстренной необходимости может выполниться за 3-4 часа. В ходе анализа выявляют специфические маркеры, которые указывают на протекание в организме онкологических процессов. По виду выявленного маркера можно говорить о том, какой вид рака протекает в организме, и даже определить его стадию.
Следует понимать, что клетка не способна к гибели. Она также может давать патологические метастазы. Также характеризуется нарушением синтетических процессов, интенсивно поглощает глюкозу, быстро расщепляет белки и углеводы, изменяет действие ферментов.

[37], [38]
Сама суть трансформационных изменений – активация синтеза нуклеиновых кислот. Стандартный комплекс претерпевает существенные изменения. Редуцируется синтез ДНК-полимеразы-3, которая отвечает за синтез новой ДНК на базе нативной структуры. Вместо этого увеличивается синтез аналогичных структур 2 типа, которая способна восстанавливать ДНК даже на основании денатурированной ДНК. Именно это и обеспечивает специфику рассматриваемых элементов.
Наиболее известным является рецептор эпидермального фактора роста, который представляет собой трансмембранный рецептор. Происходит активное взаимодействие его с эпидермальными факторами роста.
Любая трансформация влечет за собой изменение генотипа. Наглядно это выражается в изменениях, которые отражены на фенотипическом уровне. Любое изменение подобного рода является чужеродным для организма. Это подразумевает чрезмерную агрессивность иммунной системы человека, которая сопровождается атакой и разрушением собственных тканей организма.
Экспрессия опухолевых клеток
Экспрессия объясняется несколькими причинами. В первичный канцерогенез вовлекается всего одна клетка, но иногда может наблюдаться и одновременное вовлечение в этот процесс нескольких клеток. Затем развивается опухоль, происходит ее рост и размножение. Часто процесс сопровождается спонтанными мутациями. Опухоли приобретают новые свойства.
Отличительной чертой является способность к экспрессии генов, которые выступают в качестве факторов роста для опухоли. Они полностью изменяют обменные процессы исходной клетки, подчиняя ее своим потребностям, выступая своеобразным паразитом.

[39], [40], [41], [42], [43], [44], [45], [46], [47]
Для активного клеточного деления, требуется присутствие в крови, постоянная экспрессия фактора, подавляющего (репрессирующего) активность гена.

[48], [49], [50], [51], [52], [53], [54], [55], [56], [57], [58]
В ходе дифференциации мутированной ткани, она утрачивает способность к экспрессии редуцирующего гена, который отвечает за программированный аппоптоз. Утрата этой способности, лишает соответствующую структуру возможности прекратить свое существование. Соответственно, она непрерывно растет и размножается.

[59], [60], [61], [62], [63]
Пролиферация опухолевых клеток
Пролиферация - показатель разрастания, определяет тяжесть и стадию. Наблюдается функциональная анаплазия. У быстроастущих опухолей полностью утрачиваются все исходные свойства ткани.
Показатель зависит от места локализации. Определяется по экспрессии Ки – 67. Выражается в процентах путем определения соотношения между количеством нормальных клеток и количеством опухолевых клеток. Выражается в процентах, где 1 % - минимальное количество, ранняя стадия опухолевого процесса. 100% - максимальная стадия, как правило, обнаруживается при летальном исходе.
Представляют собой трансформированные клетки, которые подверглись мутационным процессам. Также в этих клетках ярко выражена способность к трансформации основных свойств исходной клетки. Отличительной чертой является неспособность к гибели и способность к неограниченному росту.
Прежде всего, необходимо знать, что этот феномен являет собой не что иное, как перерожденная клетка человеческого организма, которая в силу различных причин подверглась злокачественной трансформации. Этому процессу потенциально может подлежать практически любая здоровая клетка человеческого организма. Главное – наличие триггерного фактора, который запустит механизм трансформации (канцерогенез). В качестве таких факторов может выступать вирус, повреждение клеточной или тканевой структуры, наличие специального гена, кодирующего раковое перерождение.
Циркулирующие опухолевые клетки
Основная особенность такой клетки состоит в изменении ее биохимического цикла. Происходит изменение ферментативной активности. Также стоит отметить тенденцию к уменьшению количества ДНК – полимеразы 3, которая использует все компоненты нативной ДНК клетки. Также существенно меняется синтез. Резко увеличивается синтез белков, как в качественном, так и в количественном отношении. Также представляет определенный интерес наличие в раковых клетках крупноядерного белка веретена. В норме содержание этого белка не должно превышать 11%, при опухолях число возрастает до 30%. Происходит изменение метаболической активности.

[64], [65], [66], [67], [68], [69], [70], [71], [72], [73]
Стволовые опухолевые клетки
Можно сказать, что это первичные, не дифференцированные структуры, которые в дальнейшем будут подвергаться дифференциации функций. Если же такая клетка подвергается мутации, и превращается в раковую, она становится источников метастаз, поскольку свободно перемещается с током крови, и способна дифференцироваться в любую ткань. Живет долго и медленно пролиферируется. При пересадке имеющему низкий иммунитет (иммунодефицит), способна вызвать развитие злокачественного новоообразования
Апоптоз опухолевых клеток
Основная проблема опухолевой клетки - в ней нарушены процессы апоптоза (запрограммированной гибели, не способна к гибели, и продолжает постоянно расти и размножаться). Существует ген, который инактивирует ген, придающий клетке бессмертность. Это позволяет запустить вновь процессы апоптоза, в результате чего можно наладить нормальные клеточные процессы, и вернуть клетку в нормальное состояние, вызвать ее гибель.

[74], [75], [76], [77], [78], [79], [80], [81]
Дифференцировка опухолевых клеток
Опухолевые клетки дифференцируются в зависимости от того, в состав каких тканей она входит. Названия опухолей также зависят от названий ткани, в состав которой они входят, а также от того органа, который подвергся опухолевому превращению: миома, фибромиома, эпителиальная, соединительнотканная опухоль.

[82], [83], [84], [85], [86], [87], [88], [89], [90]
Читайте также:

