Кисты пвл что это
1. Причины и факторы риска 2. Патогенез 3. Клиническая картина 4. Терапевтические мероприятия
Изменения головного мозга проявляются кистами и полостями, которые формируются в течение примерно одного месяца. Именно поэтому в конце первого месяца жизни для всех новорожденных детей должна быть проведена нейросонография (НСГ).

Поражение носит необратимый характер. Это значит, что лечение, которое применяется после постановки этого диагноза, не может помочь избавиться от патологии.
У недоношенных новорожденных детей часто могут возникать другие поражения головного мозга, которые необходимо дифференцировать от ПВЛ. К некоторым из них относятся церебральная лейкомаляция, телэнцефальный глиоз, псевдокисты, мультикистозная энцефаломаляция, субкортикальная
лейкомаляция и т. д.
Причины и факторы риска
Возможность появления этой патологии повышается у недоношенных детей: при этом чем меньше вес при рождении, тем вероятнее развитие патологического процесса. К другим факторам риска относят пол ребенка: мальчикам диагностируют это заболевание чаще, чем девочкам.
Помимо гипоксии мозга на появление очагов ПВЛ может влиять избыточное количество углекислого газа (гиперкапния) в крови, а также кислородное отравление (гипероксия), которое иногда возникает при искусственной вентиляции легких во время реанимационных мероприятий. Опасной является ситуация резкой смены гипоксии гипероксией, что может случиться без контроля содержания и соотношения кислорода и углекислоты в крови во время ИВЛ. Кроме того, усугублять положение может развившаяся инфекция.

Отмечено также, что риск появления ПВЛ повышается, в зависимости от времени года: чаще всего она диагностируется у тех детей, последние два – три месяца которых приходятся на зиму или раннюю весну. Специалисты связывают это с влиянием метеорологических перепадов, которые влияют на беременность. Также может играть роль гиповитаминоз.
Патогенез
В результате названных причин возникает некроз белого вещества головного мозга, после чего к патологическому процессу добавляется дегенерация астроцитов (звездчатых нейроглиальных клеток с отростками), разрастание микроглии (специфических глиальных клеток ЦНС) и скопление липидосодержащих макрофагов в некротизированных тканях. После этого начинается фагоцитоз поврежденных участков – примерно через 5–7 дней, а через неделю происходит формирование кист (это занимает две недели, а иногда – больше). На завершающих стадиях возникают глиозные рубцы или псевдокисты. В некротизированных областях появляются вторичные геморрагические инфаркты. В течение 2–4 месяцев происходит атрофия ткани.
ПВЛ развивается в первые часы, но также может возникнуть и позднее – вплоть до 10 дней после рождения. Лейкомаляция также может поражать внутриутробно – если течение беременности отличается патологическим характером (гестоз, обострение хронического пиелонефрита, гепатита, фетоплацентарная недостаточность).
Уже в роддоме у детей отмечается синдром угнетения центральной нервной системы. Он выражается снижением:
- тонуса мышц;
- специфических рефлексов;
- двигательной активности;
Примерно у четверти новорожденных младенцев присутствует судороги. Почти половина детей страдает от синдрома гипервозбудимости. У некоторых младенцев могут отмечаться стволовые симптомы (нарушения сердечно-сосудистой, дыхательной деятельности). В некоторых случаях какие-либо аномалии в периоде новорожденности могут отсутствовать, а в отдельных вариантах ПВЛ приводит к летальному исходу, независимо от лечения.

Перивентрикулярная лейкомаляция становится почти в 90% случаев причиной детского церебрального паралича (ДЦП), в 60% - сходящегося косоглазия.
Степень тяжести церебральных расстройств зависит от многочисленности и площади лейкомаляционных полостей. Однако в тех случаях, когда очаги распределены тонко вокруг желудочков, прогноз имеет более благоприятный характер.
Процент практически здоровых младенцев с ПВЛ составляет примерно 4%. Последствия поражения для них могут быть незначительны.
Изменения головного мозга носят необратимый характер – по этой причине радикальное лечение, позволяющее избавиться от патологии, не существует. Терапия направлена на устранение негативных симптомов и улучшение мозговых процессов. Стандартно используются ноотропы, корректоры мозгового кровообращения, а также препараты, позволяющие справляться с двигательными нарушениями.
Поскольку ПВЛ в большинстве случаев встречается у недоношенных новорожденных детей, главной мерой профилактики патологии является продление срока беременности, предупреждение преждевременных родов.
Частота осложнений после получения кровоизлияний может снижаться, если адекватно использовать в лечении препараты сурфаканта, уменьшающего проявление дыхательных нарушений. Кроме того, оснащение реанимации новорожденных современной аппаратурой для проведения автономной искусственной вентиляции легких снижает возможность тяжелого последствия для детей.
Поддерживающее лечение ребенка с данным диагнозом должно происходить в течение всего периода детства.
Итак, перивентрикулярная лейкомаляция – это тяжелое поражение головного мозга, которое встречается у новорожденных (преимущественно, недоношенных) детей вследствие тяжелых родов, осложненной беременности. Заболевание следует отличать от других патологий (среди которых псевдокисты, церебральная лейкомаляция, телэнцефальный глиоз и т. д.), по той причине, что лечение этих болезней может отличаться друг от друга.

Прохождение родовых путей таит для младенца немало опасностей. Одна из них – лейкомаляция головного мозга, формирование патологического очага в перивентрикулярной зоне головного мозга ребенка. Он развивается из-за дефицита кислорода, поступающего к тканям мозга. Располагается очаг поражения в верхних отделах боковых желудочков. Его дальнейшее развитие грозит перерождением в кистообразные новообразования, в образование пустотных полостей. Как результат – тяжелое осложнение в функциях ЦНС у ребенка.
Причины
Гинекологи напоминают будущим мамам, насколько важен период 2-х–3-х месяцев от зачатия ребенка, когда закладывается нервная система будущего человека. Во внутриутробном развитии фактически нет неважных для развития малютки этапов. Последний триместр важен для полноценного формирования мозговых отделов и их функций. Здоровье мамы – залог того, что у ее ребенка не сформируется лейкопатия головного мозга, что он родится доношенным и полноценно развитым.
Статистика показывает, что особую группу риска по образованию лейкомаляции в головном мозге новорожденных составляют дети, родившиеся раньше срока, с фактором недоношенности.
Формированию патологии в перивентрикулярной области мозга подвержены дети, рождающиеся ранней весной.
Перивентрикулярная лейкомаляция представляет собой очаг с некрозом клеток тканей боковых желудочков. Клетки отмирают из-за резкого кислородного голодания, такой же дефицит кислорода ощущает и беременная женщина с повышенной чувствительностью к изменениям метеорологических условий. У будущей мамы болит голова, болезненность спровоцирована спазмами сосудов, как ответ на смену погоды.
Причинами неврологической патологии могут стать:
- диабет у будущей мамы; другие нарушения эндокринной системы;
- анемия и авитаминоз у беременной;
- внутриутробная инфекция во время беременности;
- сильное кровотечение в ходе родов;
- изменение АД новорожденного;
- острый дефицит дыхательной деятельности новорожденного.
И все же главная причина появления лейкомаляций – недоношенность плода. Гинекологи и перинатологи обращают внимание на предупреждение ранних родов, профилактическими мерами пытаются не допустить нарушений внутриутробного кислородного обеспечения.
Механизм развития
Провоцирующие факторы, вызывающие кислородное голодание, приводят к отмиранию белого вещества нервных клеток в первые часы после рождения ребенка. Нейроциты с полноценными функциями перерождаются в патологическую ткань. На 7-14 сутки эти ткани превращаются в кисты перивентрикулярного типа, пустотные или наполненные жидкостью. Завершающий этап формирования патологии – образование рубцовой ткани на нервных волокнах. Пораженная зона атрофируется.

Перивентрикулярная лейкомаляция у недоношенных детей поражает боковые желудочки мозга плода внутриутробно, если беременность осложняется пиелонефритом, гепатитом. Избежать церебрального поражения плода можно, если женщина постоянно наблюдается у врача, при появлении признаков ухудшения своего состояния принимает соответствующие меры для защиты ребенка.
Поражение мозга необратимо, любое лечение этой патологии не избавляет от заболевания, оно остается с человеком на всю его жизнь.
Симптомы
Родителям трудно увидеть симптомы ПВЛ у своего недоношенного ребенка. Патология проявляется разнообразными и невыразительными признаками, которые следует дифференцировать от других нервных заболеваний. Дефицит кислорода для нервных клеток может вызвать и другие болезни.
Для перивентрикулярной лейкомаляции характерна особая клиническая картина, которую видит у грудничка детский врач:
- повышенная возбудимость, выражающаяся в частых криках, лишних движениях;
- появление судорог;
- вялые мышечные рефлексы.
У недоношенных детей ПВЛ проявляется более выраженными симптомами:
- температурными перепадами без видимых причин;
- непреходящей вялостью, сонливостью;
- нарушениями сосательного и глотательного рефлексов;
- расстройствами сна, дыхания;
- парезами конечностей;
- зрительными нарушениями в заметном косоглазии.
Внешние проявления патологии в раннем возрасте сами по себе стихают, взрослым кажется, что лейкомаляция была либо ошибочным диагнозом, либо прошла. Но к году она показывает свои симптомы в явном дефиците ЦНС, видимом отставании в развитии.
МКБ-10 классифицирует несколько видов поражения мозга, которые врачам важно дифференцировать от ПВЛ: церебральная лейкомаляция, глиоз, поликистозная энцефаломаляция, субкортикальная лейкомаляция. Их симптомы схожи, разницу клинической картины показывает своевременно сделанная МРТ.
МРТ детям делают под наркозом, потому что они не в состоянии без движения вылежать необходимое время обследования.
Диагностика
В современных перинатальных центрах детям в первые дни после рождения неонатолог назначает проведение НСГ – нейросонографии, если у врача есть подозрения на развитие патологии в головном мозге. Это обследование показывает сформировавшиеся во внутриутробном развитии кисты и полости, локализующиеся в боковых долях полушарий.
Информативным методом обследования состояния головного мозга является УЗИ, которое специалисты могут сделать ребенку, пока еще не закрыт родничок. Аккуратными движениями врач двигает и поворачивает датчик на месте родничка, просматривая все ткани мозга.
Ранняя диагностика позволяет выявить степени церебрального поражения тканей мозга у новорожденных: легкую, среднюю, тяжелую; повышает вероятность установления правильного диагноза, назначение направленного лечения.

Легкая степень ПВЛ показывает симптомы кислородного голодания в течение 1 недели после рождения малютки. К 7 дням состояние малыша стабилизируется, приходит в соответствие возрастным нормам. При средней степени ПВЛ патогномоничные признаки сохраняются до 2-х недель, могут проявиться судорожные приступы, угасание рефлексов. Такое состояние для малыша опасно дальнейшими последствиями, нарушением вегетатики, нервной проводимости, нарушением речи, поэтому обязательно требуется наблюдение и лечение у детского невропатолога.
Тяжелая степень ПВЛ проявляется в длительном угнетении ЦНС вплоть до комы. Состояние угрожает жизни ребенка, его лечат в условиях реанимации. Если врачам удается вывести малютку из коматозного состояния, то ему на всю жизнь грозит инвалидность.
Лечение
Новорожденным с нарушенными функциями дыхания дают Сурфаксин, Альвеофакт, позволяющие со временем перейти с искусственной вентиляции легких на естественное дыхание. При признаках ослабленного дыхания ребенка возвращают в кювез и вновь дают препараты, поддерживающие дыхательные функции.
В годовалом возрасте лечебные рекомендации направлены на снижение последствий острой ПВЛ, проводится симптоматическая терапия. При среднем и тяжелом течении болезни врачи предупреждают, что от приема лекарства будет только временное улучшение. Киста не рассосется, основные симптомы патологии останутся. Прогноз болезни на тяжелой стадии – только инвалидность человека.

Лечат ПВЛ у детей после года:
- Мексидолом, Мексипримом, Армадином – они улучшают кислородное насыщение крови.
- Актовегином, Церебролизином – это ангиопротекторы, они укрепляют стенки сосудов.
- Нейромультивитом – отлично зарекомендовавшим себя витаминным препаратом.
- Дибазолом, Тропацином – это спазмолитики, они улучшают нервную проводимость.
- Пироцетамом, Ницерголином – ноотропами, улучшающими артериальное кровоснабжение и функции мозга.
- Карбамазепином, Зептолом, Конвулексом – противосудорожными и противоэпилептическими средствами.
- Диакарбом – для снижения внутричерепного давления; с ним вместе обязателен прием кальцийсодержащих препаратов.
- Мелиссой, Валерианой, Пионом – мягкими седативными средствами, допустимыми с раннего возраста.
Разовые и суточные дозы приема препарата рассчитывает невропатолог по возрасту, весу, состоянию ребенка. Родителям запрещается менять или нарушать режим приема препаратов, это влечет необратимые последствия.


![]()
![]()

Комментарии пользователей
- 1
- 2

![]()
У нас была угроза пвл, не знаю реализовалась или нет, так как после месяца угрозу сняли. Но у сына гемипарез в лёгкой форме (ходьба, мелкая моторика и равновесие). Это вижу я и знающие врачи. Последствие пвл Зависит от количества кист и их размера. Обычно спастика нарастает после 6 мес. До этого может казаться все ок. Самое главное вам не стимулировать эпи. Выбирайте реа… Но не гонитесь чтобы успеть все до года. если доча в год будет ползать на четвереньках, это будет замечательно. К сожалению я знаю только плохие случаи с пвл. Но исключительно по интернету, в частности с форума дети ангелы. Вы его, наверное, знаете. Там большая тема про пвл. Но и пишут туда те, у которых дети все же имеют трудности в движении. У кого все ок — обычно не пишут. Желаю здоровья, и чтобы тяжёлое прошлое мимо!

![]()
![]()
У моей по мрт пвл (именно лейкомаляция, не лейкоэнцефалопатия). Интеллект ттт не затронут, двигательно умеренный левосторонний гемипарез, у сына начальницы тоже пвл, вообще изменений никаких нет ни умственно, ни двигательно, обычный ребенок. А по мрт одни повреждения
![]()
![]()
Не знаю что такое пвл. У нас асфиксия, энцефалопатия по мрт. Так вот на мрт затронуто белое вещество и никто мне не сказал на что это повлияет на двигательную, речевую или ещё какую функцию. А знаете почему никто не сказал? Потому что никто не знает. Один невролог так и сказал никто вам не скажет за что оно отвечает. Во! Мрт делали. А что может вообще кт знать.


![]()
![]()

![]()
Да знаешь и дцп такое бывает, что поймет только очень хороший невролог, что у человека дцп. Я сама лично видела на реабилитации таких детей. Так что просто работать надо, а там все в руках Божьих. Не дожидаясь проблем занимайтесь уже массажами, лфк, иглоукалыванием и т.д.

![]()
![]()
![]()
![]()
![]()
еще про ПВЛ. дочка доношенная в 40недель. сложные роды-экс. только после рождение 32 нед двойни, когда обнаружила в их 2,5мес в выписке пвл, полезла в карту дочери( там тоже море диагнозов было), у нее тоже пвл написано, но без кист. Мы до школы пахали и пахали, двигательно тоже все ок было, но вот с интеллектом и с речью-понималкой работали до школы, садик лого был, плюс психоневролог лечение медикаментозное. Сейчас окончила 3 класс, умничка, на 4 и 5.
работала я конечно с ними много, на сколько хватило сил
в основном реабилитации бесплатные. Челябинск отличный центр есть, там же есть Войта терапия и мануальный и очень сильное лфк
Москва НИИ ИМ.Вельтищева. Тоже бесплатно ездили туда на обследование, там нам делали расширенное нсг, почти 40минут 4мя датчиками смотрели, сказали, что мозг после вжк хорошо скомпенсировался, хотя писали гидроц синдром

![]()
![]()
![]()
![]()
![]()
у нас у двоих пвл писали на нсг до месяца. но у нас без кистозная форма. мрт и кт не делали. мы 32 недельные. и плюс у одного вжк 2-3ст
но повторяюсь, без кист
по двигательному-все ок, бегают, ходят, залазят везде и тп и тдп
но нет речи пока вообще. нам 2г6мес
про пвл в группе недоношенных много пишут. и это не лечится! как выше пишут. это отмирание клеток мозга-а мозг новый не восстановить
но много положительных историй в недоношенных пишут.
Наиболее распространенным гипоксически-ишемическим повреждением у недоношенных новорожденных является перивентрикулярная лейкомаляция (ПВЛ). Miller et al. (2000) сообщали об этом состоянии у доношенных детей. Термин ввели Banker и Larroche в 1962 г. в отношении размягчения (malacia) белого (leicos) вещества. Большинство детей в их исследовании были рождены после 28 недели гестации и на момент смерти были в возрасте нескольких недель. Аноксические эпизоды были зарегистрированы во всех случаях.
При патологоанатомическом исследовании встречались двусторонние, хотя необязательно симметричные, коагуляционные некрозы, примыкающие к наружному углу боковых желудочков. В последние годы классическая картина распознается реже и в работе Paneth et al. (1990) только 3 из 15 новорожденных с некрозами белого вещества имели классические изменения при ПВЛ. В настоящее время (Volpe, 2008) принято различать преимущественно очаговый тип повреждения белого вещества — с кистозными образованиями, ограниченными областью угла и затылочным рогом, вовлекающими в процесс зрительную лучистость, иногда распространяясь кпереди в область лобно-теменного белого вещества, и более диффузный тип, который сейчас чаще называют лейкоэнцефалопатией или повреждением перивентрикулярного белого вещества (periventricular white matter injury — PWMI), реже — ПВЛ (Leviton и Gilles, 1984, Back, 2006).
В то время как эволюция в кисты, хорошо различимые при ультразвуковом сканировании черепа, является отличительным признаком очагового типа, более диффузные изменения интенсивности сигнала МРТ являются информативным показателем для диагностики диффузных патологических изменений белого вещества (Counsell et al, 2003).
Кистозная перивентрикулярная лейкомаляция (к-ПВЛ) была впервые диагностирована с использованием краниальной ультрасонографии в 1982 г. (Hill et al., 1982а). По данным прежних патологических исследований, примерно 25% повреждений носили геморрагический характер (Levene et al., 1983). Как было отмечено, заболеваемость к-ПВЛ за последнее десятилетие снизилась (Hamrick et al., 2004) с 5-10% до менее 1% в некоторых центрах.
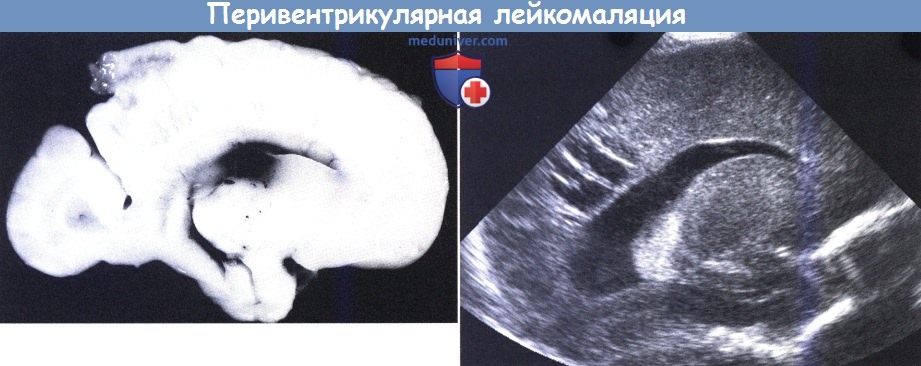
Перивентрикулярная лейкомаляция.
Новорожденный с гестационным сроком 28 недель (масса при рождении 945 г),
умерший в возрасте двух недель: многочисленные мелкие полости в перивентрикулярной области (с разрешения J-C Larroche, Maternite Port Royal, Paris).
Ультразвуковое сканирование другого ребенка, сагиттальная проекция: множественные полости около полостей желудочков. 
Несколько исследований с применением МРТ показали, что имеется невыраженная корреляция между перивентрикулярной эхогенности (ПВЭ) и изменениями интенсивности сигнала в белом веществе (Maalouf et al., 2001, Debillon et al., 2003, Miller et al., 2003, Inder et al, 2003a). Раннюю ПВЭ можно было бы соотнести с диффузным сигналом сверхвысокой интенсивности (Diffuse excessive high signal intensity—DEHSI), который выявляется на Т2-взвешенных спин-эхо последовательностях у 70% недоношенных детей в приблизительном эквиваленте зрелого возраста. Измерение коэффициента диффузии (the apparent diffusion coefficient — ADC) подтвердило, что этот показатель действительно отражает повреждение белого вещества (Counsell et al., 2003).
У небольшого количества младенцев очаги перивентрикулярной эхогенности (ПВЭ) постепенно превратились в локализованные или более обширные кисты. Чем меньше и чем более ограниченна киста, тем больше времени требуется для ее развития. Мелкие кисты могут остаться не выявленными. Более 50% небольших кист впервые выявляли при еженедельном ультразвуковом исследовании после 28 дней (Pierrat et al., 2001, de Vries et al., 2004). Более чем у половины детей маленькие кисты разрешались к 40 неделям постконцептуального возраста, приводя к легкому расширению желудочков (вентрикуломегалии) в некоторых, но не во всех случаях. С уменьшением длительности вентиляции новорожденных и возрастанием числа пациентов большинство младенцев переводят в районные стационары до развития кистозных изменений и возвращают для наблюдения в клинику в 40 и более недель постконцептуального возраста.
Если ультразвуковое исследование не проводится в местных больницах, кисты могут оставаться не диагностированными, что, вероятно, является основной причиной плохой репутации краниального УЗИ как предиктора церебрального паралича (de Vries et al., 2004). В улучшении наблюдения за детьми группы риска по развитию кист МРТ, как было показано, может быть перспективным. Inder et al. (1999b) впервые продемонстрировали обширные изменения на ДВ-МРТ, предшествовавшие развитию кист. Получены немногисленные данные об очень ограниченном количестве детей с ПВЭ, обследованных на ранней стадии этого тяжелого расстройства (Bozzao et al., 2003).
Кисты, даже обширные, могут разрешаться от нескольких недель до месяцев, и МРТ играет главную роль в определении распространенности повреждений белого вещества на этапе позднего неонатального периода. Классическая картина в периоде младенчества может быть представлена в виде неравномерного расширения боковых желудочков, различной степени утраты белого вещества, извилин, прилегающих к желудочковым стенкам, задержки миелинизации и перивентрикулярного глиоза (Byrne et al., 1990, Truwit et al., 1992).
de Vries et al. (1993) обнаружили хорошую степень корреляции между тяжестью патологии при ультразвуковом исследовании новорожденных и глиозными изменениями на МРТ, в период младенчества. Современные технологии, использующие диффузионо-тензорное изображение (ДТИ), позволяют выполнить диффузионнотензорную трактографию (ДТТ) и таким образом отображать и подсчитывать белое вещество пирамидального тракта недоношенных новорожденных (Miller et al., 2002, Berman et al., 2005, Partridge et al., 2005). Counsell et al. (2006) указали на существенно повышенный радиальный коэффициент диффузии в задней части внутренней капсулы и утолщении мозолистого тела, а также значительно повышенный радиальный и аксиальный коэффициент диффузии в белом веществе семиовального центра, в белом веществе лобной, перивентрикулярной и затылочной областей. Эти данные, полученные Counsell et al. (2006), позволяют предположить, что DEHSI при стандартном МРТ отражает патологические изменения олигодендроцитов и/или аксонов белого вещества.
б) Патогенез. Патогенез ПВЛ многофакторный и менее понятен, чем при кровоизлиянии в герминативный матрикс и внутрижелудочковом кровоизлиянии (КГМ-ВЖК). Первоначально это состояние связывали с гипоперфузией пограничных зон в белом веществе, но исследования с использованием непрерывного измерения кровяного давления до сих пор не в состоянии определить гипотензию как независимый фактор риска для повреждения белого вещества (Trounce et al., 1988, Watkins et al., 1989, Dammann et al., 2002). Тяжелая гипокапния, которая приводит к снижению мозгового кровотока, в нескольких исследованиях была выделена в качестве самостоятельного фактора риска для развития ПВЛ (Calvert et al., 1987, Greisen et al., 1987, Graziani et al., 1992, Fujimoto et al., 1994, Wiswell et al., 1996, Okumura et al., 2001, Shankaran et al., 2006). У детей с развитием ПВЛ было обнаружено заметное снижение как мозгового кровотока, так и доставки кислорода к мозгу (Pryds, 1994).
Результаты ближней инфракрасной спектроскопии (БИС), Tsuji et al. (2000) подтвердили дисфункцию церебральной ауторегуляции у 17 из 32 недоношенных детей; у 9 из них развились тяжелые внутричерепные повреждения по сравнению только с 2 из 15 с неизмененной ауторегуляцией.
В нескольких интересных исследованиях была обнаружена связь между восходящей внутриматочной инфекцией, продукцией воспалительных цитокинов и повреждением белого вещества (Leviton и Gilles, 1984, Bejar et al., 1988, Murphy etal., 1995, Perlman et al., 1996, Verma et al., 1997, Yoon et al., 1997, Minagawa et al., 2002). В недавнем обзоре (Leviton et al., 2005) выдвинута гипотеза, что поражение белого вещества возникает в результате взаимного усиления врожденной и приобретенной иммунных систем. При мета-анализе была установлена связь между хориоамнионитом и церебральным параличом, и хориоамнионит был выделен в качестве фактора риска как для церебрального паралича (КР 1,9; 95% ДИ 1,5-2,5), так и для ПВЛ (КР 2,6; 95% ДИ 1,7-3,9) (Wu и Colford, 2000). Yanowitz et al. (2002) смогли показать взаимосвязь между хориоамнионитом, повышенным уровнем ИЛ-1 р и ИЛ-6, а также снижением среднего и диастолического давления крови после рождения.
Редактор: Искандер Милевски. Дата публикации: 25.11.2018
Читайте также:

