Карцинома с высоким ядерным полиморфизмом

В гистологическом заключении содержится подробная информация об опухоли. Одним из важных параметров опухоли, который можно найти в вашем гистологическом заключение, — это степень ее злокачественности. По сути, это описание того, как клетки злокачественной опухоли выглядят под микроскопом, насколько они отличаются от нормальных клеток (уровень клеточной дифференцировки).
Гистологическая степень злокачественности (Grade, G) рака молочной железы определяет агрессивность опухоли, её потенциал к прогрессированию и метастазированию. Этот критерий порой играет ключевую роль в определении оптимального варианта лечения.
Ноттингемская модификация системы Скарфа-Блума-Ричардсона используется в настоящее время для определения гистологической степени злокачественности рака молочной железы. Ноттингемская градирующая система рекомендована различными профессиональными организациями на международном уровне (ВОЗ, AJCC, EU).
Зачем необходимо гистологическое градирование рака молочной железы?
Выполнена биопсия, у вас подтвердился диагноз — карцинома молочной железы. И теперь вам интересно знать, какое лечение лучше всего для вас подходит и каков прогноз.
Прежде всего, чтобы это узнать, необходимо определить стадию онкологического заболевание. Многие ошибочно думают, что степень злокачественности и стадия рака молочной железы это одно и тоже.
Стадия рака (карциномы) указывает на размер первичной опухоли и ее распространённость (уровень поражения регионарных лимфатических узлах, наличие или отсутствие отдалённых метастазов). Кроме того, учитываются и другие критерии. Стадия определяет насколько серьезен ваш рак, и какое лечение лучше всего вам подходит.
Степень злокачественности карциномы — это одним из критериев, которые используются при стадировании рака молочной железы. Это показатель оценивает характеристики раковых клеток, с его помощью можно предсказать дальнейшее поведение онкологического заболевания.
Степень злокачественности является лишь одним из параметров, которые используются для определения стадии опухоли молочной железы. Другими являются размер и местоположение опухоли, инвазия в сосуды и нервы, количество пораженных лимфатических узлов и степень отдалённого метастазирования.
Как определяется степень злокачественности рака молочной железы?
Ноттингемская градирующая система является обновлением предыдущей системы Скарфа-БлумаРичардсона. Последняя была впервые принята в 1957 году. Ноттингемская градирующая система основана на полуколичественной оценке морфологических характеристик опухоли. С ее помощью можно определить, насколько агрессивным будет злокачественное новообразование.
Опухоли низкой степени злокачественности, у которых злокачественные клетки практически ничем не отличаются от нормальных, имеют тенденцию к медленному росту. В свою очередь, опухоли с высокой степени злокачественности быстро растут и рано дают метастазы. Их клетки сильно отличаются от нормальных.
Градирование рака молочной железы (определение степени злокачественности) подразумевает оценку 3 компонентов, каждый из которых оценивается от 1 до 3 баллов: железистая дифференцировка (соотношение тубулярных/ацинарных/железистых структур), ядерная атипия/полиморфизм и количество митозов.
Этот компонент оценивается соотношения нормальной ткани молочной железы и изменённой. Это так называемая железистая дифференцировка, которая гарантируется следующим образом:
Количество делящихся (митотических) клеток, видимых под микроскопом при увеличении в 400 раз, градируется следующим образом:
| 1 балл | менее 10 митотических клеток |
| 2 балла | от 10 до 19 клеток |
| 3 балла | более 20 клеток |
Оценивается размер и форма ядра в злокачественных клетках.
| 1 балл | ядра маленькие, немного увеличены по сравнению с эпителием нормальных структур, с правильными очертаниями, моноформным ядерным хроматином, небольшой вариацией в размерах |
| 2 балла | клетки больше, чем нормальные эпителиальные клетки, с везикулярными ядрами, заметными ядрышками, умеренными различиями в размерах и форме |
| 3 балла | везикулярные ядра, часто с заметными ядрышками, выраженные различия по форме и размеру, иногда с очень крупными и причудливыми формами |
Три выше перечисленных компонента объединяются для определения степени злокачественности опухолии. Чем выше степень злокачественности, тем рак молочной железы более агрессивен, обладает большим потенциалом к метастазированию.
| Общая градация | Степени злокачественности | Внешний вид клеток |
| От 3 до 5 | G1, I степень злокачественности | Хорошо дифференцированы (выглядят нормально, медленно делятся, не агрессивны) |
| От 6 до 7 | G2, II степень злокачественности | Умеренно дифференцированы (полунормальные) |
| От 8 до 9 | G3, III степень злокачественности | Плохо дифференцированы (ненормально, агрессивны) |
Статья по теме: Как быстро растет и распространяется рак молочной железы?
Степень злокачественности и стадия опухоли
Степень рака будет использоваться для постановки вашего рака, то есть, насколько прогрессировал ваш рак.
Постановка поможет вашему врачу решить, какое лечение может полностью искоренить злокачественную опухоль с наименьшим количеством вреда. Например, рак на ранней стадии может потребовать хирургического вмешательства или облучения, в то время как рак на поздней стадии может нуждаться в лечении химиотерапией.
Постановка диагноза рака молочной железы подразумевает методологии:
- Клиническая стадия основана на всей доступной информации, полученной до операции, включая результаты ваших физических обследований и визуальных исследований (таких как рентген и компьютерная томография или компьютерная томография).
- Патологическая стадия использует те же тесты, но также включает оценку патологом опухолевой ткани и лимфатических узлов, удаленных в ходе операции.
Патологическая стадия считается более точной, поскольку она включает в себя прямое исследование опухоли. Тем не менее, клиническая стадия может быть целесообразной в некоторых ситуациях, учитывая, что не все виды рака требуют хирургического вмешательства.
TNM классификация
Что касается рака молочной железы, классификация злокачественных опухолей (TNM) TNM является системой, наиболее часто используемой для постановки. Он широко используется для постановки многих видов рака (за исключением случаев рака крови или злокачественных новообразований центральной нервной системы). Наиболее распространенные опухоли имеют собственную систему классификации TNM.
TNM обозначает опухоль, узлы и метастазы, в частности, размер опухоли (T), количество лимфатических узлов, пораженных раком (N), и степень метастазирования (M).
Узнайте больше: Система TNM для классификации рака молочной железы
Когда ваш врач получит отчет о патологии, будут учтены как степень, так и стадия рака — по шкале от 0 (неинвазивный) до 4 (метастатический).
В отчете о патологии также будет подробно:
- Есть ли у вас одна или несколько опухолей в пораженной груди
- В какой степени злокачественная опухоль ограничивается грудью
- Обнаружен ли рак в лимфатических узлах под рукой
- Если рак распространился на сосок и кожу
- При наличии свободных от рака полей вокруг удаленной опухоли
- Если рак является эстроген-позитивным или эстроген-негативным (показатель того, может ли гормон влиять на рост опухоли)
Основываясь на этих выводах и особенностях, ваш врач разработает план лечения, который вы сможете рассмотреть и обсудить. Если есть что-то, что вы не понимаете, спросите своего врача об этом и как это влияет на решение о лечении.
Список использованных источников:
Прогноз и прогностические факторы
При лобулярной карциноме частота метастазирования в подмышечные лимфатические узлы меньше чем при протоковой карциноме; разница от 3 до 10% метастатического увеличения лимфатических узлов из-за рассеивания отдельных клеток может быть сходно с синусоидальными гистиоцитами, что требует иммуногистохимического исследования.
Метастатическое поражение при лобулярной карциноме отличается от таковых при протоковой. Большая частота распространения опухоли на костную ткань, ЖКТ, матку, яичники, висцеральные серозные оболочки, мозговые оболочки наблюдается при лобулярной карциноме. В то время как поражение легких более часто встречается при протоковой карциноме. Иммуногистохимия с использованием антител против GCDFP-15, цитокератина 7, эстрогенновых рецепторов и Е-кадхерина может помочь установлению источника лобулярной карциномы.
Некоторые исследования сообщают о более благоприятном прогнозе лобулярной карциноме, нежели чем протоковой, в то время как другие исследования не выявили существенных различий, или же выявили худший прогноз при лобулярной карциноме.
При раздельном анализе гистологических субтипов лобулярной карциномы более благоприятный исход сообщается для классического типа, нежели для вариантов лобулярной карциномы. Как бы там ни было альвеолярный вариант лобулярной карциномы рассматривается как низкогрейдная опухоль. В то время как при плеоморфной лобулярной карциноме в некоторых исследованиях сообщается о неблагоприятном прогнозе. Другие исследования не сообщают о благоприятном исходе для разных типов лобулярной карциноме.
К тому же значительное вовлечение лимфатических узлов не увеличивает риск местного рецидива. Так же сообщается о связи низких значений экспрессий Е-кадхерина и неблагоприятного исхода.
Лечение лобулярной карциномы зависит от стадии развития опухоли. Для лобулярной карциномы подходит консервативное лечение.
Тубулярная карцинома
Определение.
Специфический тип карциномы молочной железы с особенно благоприятным прогнозом, состоящей из высоко дифференцированных тубулярных структур с однослойной эпителиальной выстилкой.
Эпидемиология.
В большинстве исследований на долю тубулярной карциномы приходится менее 2% инвазивных опухолей молочной железы. Более высокая частота встречаемости до 7% прослеживается в исследованиях малых Т1 раков молочной железы.
Тубулярная карцинома часто легко диагностируется при маммографии. По сравнению с инвазивной протоковой карциномой она чаще возникает у возрастных группе пациентов, меньше в размерах и реже метастазирует в лимфатические узлы. Эти опухоли возникаю в ассоциации с некоторой эпителиальной пролиферацией, включая высокодифференцированную низкогрейдную протоковую карциному In situ ,лобулярную неоплазию и плоскоклеточную эпителиальную атипию.
Макроскопия.
Специфических макроскопических признаков у данной опухоли нет. Единственным отличием от более частой протоковой карциномы или смешанных типов является малые размеры опухоли. Тубулярная карцинома обычно составляет от 0,2 до 2 см в диаметре; в большинстве случаев 1см и менее.
В большинстве случаях протоковая карцинома In situ осоциированна с тубулярной карциномой. В этих случаях она представлена низкогрейдными крибрифорбными или папиллярными участками. В некоторых случаях компонент, расположенный In situ имеет тубулярный тип. В недавнее время описано ассоциация эпителиальной плоскоклеточной атипии и микропапилярной протоковая карцинома In situ. На сегодняшний день не существует единого мнения относительно количества тубулярных структур необходимых для постановки диагноза тубулярная карциномаIn situ.
В предыдущей классификации ВОЗ и определенных публикациях нет указаний на четкие критерии, однако существует предположения, что для диагноза вся опухоль должна состоять из тубулярных структур. Некоторые авторы требуют для постановки диагноза строгой тубулярной структуры. Другие настаивают на 70% тубулярных структур, некоторые на 90%. Практическое решение данной проблеме нам представляется 90% тубулярных структур. Опухоль, в которой 50-90% тубулярных структур должна рассматриваться как карцинома смешенного типа.
К тому же при микрограндулярном аденозе кольцом базальной мембраны окружены тубулы. Комплексное склерозирующее поражение имеет типичную архитектонику с центральным фиброзам и эластозом и содержит несколько маленьких часто искаженных структур, в которых обнаруживаются миоэпителиальные клетки. Окружающие их грандулярные структуры отражают различную степень протоковой эпителиальной гиперплазии.
Принято считать, это следует подчеркнуть, что чем более резко выражен клеточный полиморфизм, тем злокачественнее опухоль и хуже прогноз. Однако полного соответствия между этими признаками нет, н нередко как раз наиболее злокачественные новообразования отличаются мономорфностью.
Для новообразований также характерно значительное варьирование формы, размеров и плотности ядер опухолевых клеток, высокое ядерно-цитоплазматическое отношение. Нередко ядра бывают крупные, резко полиморфные, гиперхромные. Они могут содержать несколько ядрышек, иногда гипертрофированных.
Изменения хроматина в опухолевых клетках могут характеризоваться нарастанием процесса его гетерохроматизации, при этом интенсивно окрашивающийся гетерохроматин имеет мелко- или круиноглыбчатое строение, занимает периферические или центральные участки ядра или распределяется диффузно по нему. Соответственно варьируют светлоокрашенные участки, содержащие эухроматин. Следует сказать, что соотношение в ядрах гетерохроматина, являющегося более инертной (конденсированной) частью хроматина, и эухроматяна, содержащего основную массу активно функционирующих генов, значительно варьирует от опухоли к опухоли н от одной клетки к другой в одном и том же новообразовании, отражая степень дифференцнровки ядра. На гистологических препаратах, окрашенных гематоксилином и эозином, степень гиперхромиости ядер обусловлена выраженностью в них гетерохроматизации.
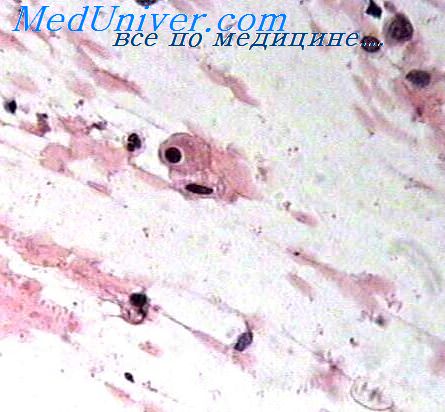
Каждая конкретная опухоль обычно представляет собой популяцию клеток с изменчивым числом хромосом, т. е. неравномерным содержанием ДНК. Однако в опухоли при этом можно обычно выделить одну, две или несколько модальных линий со стабильно повышенным содержанием ДНК, соответствующим определенной плоидности числа хромосом. Гистограммы, построенные на основании цитоспектрометрни, цитоспектрофлуориметрии, импульсной цитофотометрии или иных способов, отражают модальную линию или линии и все варианты содержания ДНК в данной опухоли. Их анализ может иметь важное практическое значение для дифференциальной диагностики предопухолевых и опухолевых процессов, так как при последних количество ДНК увеличено.
Морфологическая катаплазия опухолевых клеток значительно варьирует от новообразования к новообразованию, в связи с чем делались многочисленные попытки найти корреляцию между ее выраженностью и степенью злокачественности опухоли.
Распространение получило исследование степени злокачественности плоскоклеточного рака гортани на основании определения различных сторон клеточной катаплазии (расположения клеток, степени их кератинизации, ядерного полиморфизма, митозов и др. ).
Разбирая значение клеточной катаплазии в определении степени злокачественности опухоли с точки зрения ее прогноза, следует подчеркнуть два обстоятельства. Во-первых, использование электронной микроскопии в диагностике опухолей человека позволяет, как никогда раньше, объективно оценивать степень дифференцировки опухолевых клеток и их гистогенетическую (точнее цитогенетическую) принадлежность, о чем подробнее будет изложено в следующем разделе. Во-вторых, важным является определение не одного, а суммы факторов (признаков), определяющих в своей совокупности степень злокачественности и прогноз для конкретного вида опухоли, в связи с чем наибольшие перспективы имеет многофакторный анализ с использованием электронно-вычислительной техники.
В определении степени злокачественности опухоли и ее прогноза важное значение имеют не только признаки клеточной катаплазни, но и другие факторы, как, например, состояние стромы, лимфоидная инфильтрация, глубина инвазии и многие иные клинико-анатомические проявления опухолевого роста, которых мы в рамках данной статьи не касаемся, но учитывать которые необходимо.
Гистологическая дифференцировка рака молочной железы
Гистологическую градацию рака молочной железы (РМЖ) впервые ввел R.B. Greenough из Бостона, который в 1925 г. опубликовал анализ 73 случаев РМЖ.
Несмотря на то что прошло много времени и опубликовано большое количество работ о применении гистологической градации рака молочной железы, ничего существенного не добавлено в перечень морфологических критериев, которые определяют группы РМЖ, имеющие клиническое значение.
Работа R.B. Greenough актуальна и сегодня, он сформулировал прогностически значимые категории инвазивного рака молочной железы низкой, средней и высокой степени злокачественности.
Это деление базируется на 5 признаках:
1) тканевой (гистологической) организации опухоли, то есть способности образовывать дольки, протоки и железистоподобные структуры;
2) степени секреторной активности, которая подтверждается цитоплазматическими вакуолями, капельками муцина в просвете желез;
3) клеточной атипии, то есть единообразии или вариации размеров и формы клеток, соотношении размеров ядра и цитоплазмы;
4) наличии гиперхромных ядер;
5) наличии ядерной атипии и количества митотических фигур.
В соответствии с градациями по Greenough типы рака высокой степени злокачественности имеют клетки и ядра неправильной формы и различного размера, без секреторной функции, клетки расположены столбцами, отмечают гиперхроматоз ядер и большое количество атипичных митозов.
И наоборот, опухоли, состоящие из желез, построенных из единообразных по размеру и строению клеток без гиперхроматоза, с малым количеством митозов, следует относить к РМЖ низкой степени злокачественности.
По данным R.B. Greenough, после радикальной мастэктомии пациентки с раком низкой степени злокачественности были излечены в 68%, умеренной — в 33% случаев и нулевым был результат при высокой.
В 1928 г. Patey и Scarff из Лондона опубликовали анализ 50 случаев рака молочной железы. Они изучили корреляцию между гистологической градацией по Greenough, статусом лимфатических узлов и выживаемостью пациенток. Выявлено, что пациентки с раком низкой степени злокачественности после радикальной мастэктомии излечивались в 85%, средней степени — в 45% и высокой — в 23% случаев.
Кроме того, авторы отметили, что прогноз течения заболевания всегда хороший при отсутствии метастазов в лимфатических узлах, изъязвления опухоли и распространения ее на фасции независимо от гистологической степени злокачественности по Greenough.
Они также сделали заключение, что в случаях нераспространенного РМЖ более продолжительный период ремиссии, то есть период до появления метастазов или рецидивов после радикальной мастэктомии, у пациенток с опухолью низкой степени злокачественности по Greenough, а в случаях распространенного рака — более эффективна паллиативная терапия.
Последующая работа H.J.C. Bloom из Лондона, опубликованная в 1950 г., подтвердила выводы Patey и Scarff. В классическом труде Bloom-Richardson, опубликованном в 1957 г., окончательно сформулированы критерии гистологической градации РМЖ. В своей работе они проанализировали течение болезни 1409 пациенток, из которых 359 прожили более 15 лет.
Подобно R.B. Greenough, исследователи разделили рак молочной железы (РМЖ) на 3 категории, базируясь на трех показателях:
1) относительном количестве тубулярных структур;
2) наличии вариаций размеров клеток рака;
3) количестве гиперхромных ядер и фигур митоза.
Каждый из этих показателей авторы оценили в баллах (1, 2 или 3 балла). Суммируя количество баллов, получим возможные комбинации от 3 до 9. Наименьшее количество баллов соответствует наиболее низкой степени злокачественности рака молочной железы.
Авторы разделили шкалу злокачественности на три части: 3, 4 или 5 суммарных баллов — низкая степень злокачественности (grade 1); 6 или 7 суммарных баллов — средняя (grade 2); 8 или 9 — высокая (grade 3). Эта схема стала наиболее популярной в мире и называется схема градации РМЖ по Bloom-Richardson или технология Scarff-Bloom-Richardson, хотя должна была называться техникой градации по Greenough, в честь человека, впервые опубликовавшего эту градацию в 1925 г.
Bloom и Richardson установили, что 26% из 1409 исследованных случаев РМЖ имели 1-ю степень гистологической злокачественности, 45% — 2-ю, 29% — 3-ю. Результаты сравнения гистологических степеней злокачественности первичной опухоли и метастазов в аксиллярных лимфатических узлах показали, что в 82% степени совпадали.
В 12% случаев степень злокачественности была выше, а в 6% — ниже в метастазе, чем в первичной опухоли. Авторы выявили, что степень гистологической злокачественности, как и статус регионарных лимфатических узлов, дает независимую прогностическую информацию (табл. 2).
Таблица 2. Выживаемость пациенток с РМЖ в соответствии с градационной схемой Bloom-Richardson (исследованы 1409 пациенток). 
Bloom и Richardson пришли к выводу, что степень гистологической злокачественности рака молочной железы отражает предполагаемое клиническое течение заболевания и вероятность развития метастазов в дальнейшем, что стало в свое время очень прогрессивным учением.
Очевидно, что степень гистологической дифференцировки имеет корреляцию с темпами роста опухоли и соответственно показателями S-фазы митотического цикла (ЗН-тимидина, Ki67), показателями анеуплоидии, экспрессией С-егВ-2, рецепторов эстрогена и прогестерона.
Важность этого показателя очевидна, однако в ряде публикаций гистологическое стадирование подвергается жесткой критике из-за трудности, возникающей при его воспроизводимости. Отмечают, что процент расхождения в оценке гистологической дифференцировки иногда составляет 50-60%.
Однако когда критерии оценки гистологической степени злокачественности оценивают профессионально и тщательно, совпадение результатов этой оценки составляет 90%.
H.F. Frierson и соавторы прорецензировали патологоанатомические заключения 7 патологоанатомов, проводивших исследование 75 случаев инвазивного протокового РМЖ. Совпадение при оценке гистологической структуры составило 71%, тубулярных структур — 81%, полиморфизма ядер — 64%, митозов — 67%.
C.W. Elston рекомендует проводить двойное исслeдoвание. Это возможно при проведении исследования двумя патологами или одним патологом дважды на разных образцах.
Следующим недостатком предложенной Bloom и Richardson системы градаций РМЖ стало то, что большая часть пациентов относится к 2-й и 3-й степени градации. С .W. Elston, используя модифицированную систему гистологической градации Bloom и Richardson, исследовал рак молочной железы у 1831 пациентки с периодом наблюдения 16 лет и диагностировал 1-ю степень гистологической дифференцировки рака в 18%, 2-ю — в 34%, 3-ю — в 47% случаев.
Автором отмечена очень выраженная корреляция с клиническим прогнозом. У пациенток с раком 1-й степени злокачественности значительно лучшая выживаемость, чем со 2-й и 3-й степенью (р
План лечения составляют с учётом стадии опухолевого процесса, морфологической структуры опухоли, возраста больной, сопутствующих заболеваний, общего состояния пациентки. Применяют следующие методы лечения: хирургический, комбинированный (сочетание операции с лучевой или лекарственной терапией) и ком.
По данным многочисленных публикаций, этиология и патогенез РМЖ сложны и определяются сочетанием многих факторов. Гормональная регуляция функции молочных желез значительно сложнее, чем эндометрия. Помимо эстрогенов и прогесторона, развитие молочных желез в пубертатном периоде, их функция во время бер.
Гистологическую градацию рака молочной железы впервые ввел R.B. Greenough из Бостона, который в 1925 г. опубликовал анализ 73 случаев рака молочной железы. Несмотря на то что прошло много времени и опубликовано большое количество работ о применении гистологической градации рака молочной железы, ниче.
При анализе данных, получаемых с помощью ультразвукового исследования, целесообразно выделить ряд диагностических задач, решение которых позволит получить полный комплекс эхографических признаков рака молочной железы и метастатических лимфатических узлов, по которым в дальнейшем будет производиться .
Патологические процессы в молочной железе отличаются многообразными клиническими проявлениями, что норой создает серьезные дифференциально-диагностические трудности. Для гипеколога важнее всего заметить (не пропустить!) патологию молочных желез, что приведет в движение систему методов уточня.
Доброкачественные изменения молочных желез относятся к наиболее распространенным заболеваниям и включают различные по клиническим, морфологическим и этиологическим признакам процессы. Отличительной особенностью молочной железы является сложность четкой дифференцировки физиологических и патологически.
Рак молочной железы развивается из эпителия млечных протоков и альвеол. Патоморофологическая характеристика рака молочной железы включает такие параметры, как размер первичного очага, его локализацию в молочной железе, тип роста, морфологическое строение, степень дифференцировки, наличие регионарных.
Злокачественные опухоли молочной железы, как причина смертности от онкологических заболеваний среди женщин, занимают первое место как в России, так и в мире. Это также основная причина смерти среди женщин старше 40 лет. Примерно у 8% женщин (одной из 13) в течение жизни развивается злокачественная опухоль молочной железы. К сожалению, отмечается тенденция к росту заболеваемости и смертности от рака молочной железы, особенно выраженная в странах с высоким уровнем жизни. Так, в странах Северной Европы, Северной Америки и Австралии заболеваемость составляет 70-90 вновь выявленных случаев злокачественных опухолей на 100 000 населения в год (ВОЗ, 2003). Около 90% злокачественных опухолей молочной железы составляет рак, реже встречаются неэпителиальные опухоли.
Факторы риска рака молочной железы
— Возраст: чаще диагностируется у женщин старше 40 лет.
— Генетические особенности: наиболее часто предрасположенность передается по материнской линии, имеет значение мутация генов BRCA и BRCA 2.
— Диагностированный ранее рак, особенно дольковый, в одной молочной железе.
— Избыточная жировая клетчатка, особенно при быстром наборе веса, в сочетании с гиперплазией эпителия протоков.
— Раннее начало менструаций (ранее 12 лет) и позднее их окончание (после 50 лет).
— Чаще рак развивается у женщин без детей или не кормивших детей. В норме инволюция молочной железы происходит только после вскармливания ребенка грудью; если женщина не кормила грудью, чаще развиваются гиперпластические и диспластические процессы.
— Пролиферативная форма фиброзно-кистоз-ной болезни.
— Нарушение гормонального баланса: длительное лечение гормонами, особенно эстрогенами, активные опухоли яичника, эндометрия и щитовидной железы, гормональная контрацепция при неправильном применении и гормональная заместительная терапия в климактерическом периоде.
— Рентгеновское облучение: ткань молочной железы в 30-9 лет наиболее подвержена действию рентгеновских лучей.
Клинические проявления
Клинические признаки могут отсутствовать, или имеется лишь один из признаков, или их различное сочетание:
• Уплотнение в молочной железе.
• Болезненность в молочной железе или в подмышечной области.
• Опухолевидные образования в подмышечной области.
Факторы, влияющие на прогноз заболевания
• Распространенность процесса. Лучшим прогнозом отличается ранний рак (неинфильт-ративный дольковый или протоковый, рак Педжета или инвазивный, рак размером до 1 см и без метастазов в регионарных лимфатических узлах). Наличие опухоли больших размеров в момент установления диагноза является признаком неблагоприятным. При установлении диагноза на стадии распространенного рака с поражением лимфатических узлов (особенно если имеется более четырех пораженных лимфатических узлов) и других органов отмечен плохой прогноз. Висцеральные метастазы наиболее часто встречаются в легком, печени, костях и головном мозге, могут поражаться и другие органы.
• Гистологические особенности. Медуллярный, папиллярный и слизистый рак отличается лучшим прогнозом по сравнению с другими формами рака: реже поражаются лимфатические узлы, больше продолжительность жизни. При дольковом раке прогноз хуже, чем при протоковом. Увеличенное число гистиоцитов в лимфатических узлах, наличие плазматических клеток и лимфоцитов в ткани, окружающей опухоль, сочетается с более благоприятным прогнозом.
• Возраст при установлении диагноза. Прогноз у женщин пожилого возраста лучше, чем у молодых с аналогичной опухолью и стадией процесса.
• Особенности организма. Рост и развитие рака напрямую зависят от взаимоотношения организма и клеток рака (иммунного статуса, гормонального фона и проч.).
Врач, устанавливающий морфологический диагноз рака, должен отдавать себе отчет в том, что этот диагноз может служить основанием к началу, как правило, тяжелого лечения (хирургического, лучевого, химиотерапевтического и проч.).
Рак молочной железы: общие цитологические признаки
Клеточный и ядерный полиморфизм:
• разные размеры и форма клеток и ядер;
• неровные контуры ядерной мембраны;
• неравномерное распределение хроматина;
• глыбчатая и грубоглыбчатая структура хроматина;
• ядрышки разных размеров и формы. Разрозненное (рыхлое) расположение клеток (что обеспечивает их попадание в лимфоот-ток, кровь):
• обильный клеточный состав;
• отсутствие упорядоченности расположения клеток в структурах (комплексах);
• разрозненное расположение клеток с сохранившейся цитоплазмой.
Дегенеративные изменения клеток и ядер. Нарушение ядерно-цитоплазматического соотношения.
Клеточный и ядерный полиморфизм
Для рака характерны разные размеры и форма опухолевых клеток (клеточный полиморфизм) и ядер (ядерный полиморфизм). Наиболее достоверным критерием рака является увеличение размера ядер и ядерный полиморфизм:
• Увеличение размера ядер до 12-40 мкм, что в 1,5-5 раз больше диаметра эритроцита (рис. 59). Однако существуют варианты рака молочной железы с мелкими ядрами (тубу-лярный, дольковый, некоторые формы про-токового); при этих вариантах, в отличие от доброкачественных состояний, отмечается умеренный полиморфизм и рыхлое расположение клеток.
• Разная степень увеличения ядер.
• Неровные контуры ядерной мембраны.
• Неравномерное распределение хроматина: хроматин распределяется глыбками, зернами,

Рис. 59. Рак (описание в тексте). Окрашивание по Паппенгейму. х1000


Рис. 60. Рак. Клеточный и ядерный полиморфизм (описание в тексте). Окрашивание по Лейшману. а — х400, б — х1000
чередующимися с неравномерно распределенными светлыми участками. • Грубый хроматин характерен для большинства опухолевых клеток. Структура хроматина часто бывает глыбчатой и грубоглыбча-той (рис. 59, 60).
• Атипическая форма ядер.
Ядра могут иметь неправильную форму, с выростами, неровными контурами (рис. 61). В связи с выраженной митотической активностью опухолевые клетки могут быть многоядерными, содержать как хорошо сохранившиеся ядра, так и ядерные фрагменты разных размеров. Нарушение деления клетки может привести к формированию ги
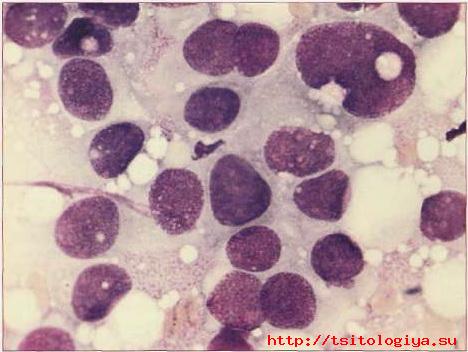
Рис. 61. Рак. Атипическая форма ядер (описание в тексте). Окрашивание по Паппенгейму. х1000
гантских опухолевых клеток, значительно более крупных, чем обычные опухолевые клетки, 50 мкм и более в диаметре. После облучения нередко появляются ядра причудливой формы, многодольчатые, с выраженной вакуолизацией. Реже обнаруживают перстневидные клетки, с уплощенным ядром, оттесненным к периферии клетки. Они встречаются практически при всех видах рака, но чаще при при дольковом и слизистом раке.
При большом увеличении (х1000) (рис. 62) четко видна неровность ядерной мембраны, ее утолщения, вдавления, зазубренность контуров.
Могут быть увеличенными или множественными, при окраске по Романовскому -нежно-голубыми или фиолетовыми (рис. 62-65). При окрашивании по Папаниколау ядрышки выглядят темными и хорошо просматриваются на фоне светлого хроматина. Укрупненные ядрышки могут быть и при доброкачественных пролиферативных состояниях, но очень крупные встречаются только при злокачественных процессах. Отсутствие ядрышек не исключает злокачественного поражения: особенно часто они не видны при раке у женщин пожилого возраста.
На малом увеличении примерно у 15% опухолевых клеток ядра выглядят сравнительно мономорфными, что особенно хорошо проявляется при высокодифференцированном раке.
Разрозненное (рыхлое) расположение клеток
Связано с нарушением межклеточных связей, поэтому клетки перестают выстраиваться в привычном для данной ткани порядке, а также отрываются от структур и располагаются разрозненно. В связи с этим отмечается:
• Обильный клеточный состав.
В связи с тем, что нарушаются межклеточные связи, клетки легче отторгаются от ткани и при аспирации за счет отрицательного давления большое их число попадает в мазки.
Исключением из этого правила являются некоторые формы рака, в частности небольшое число клеток при аспирации встречается иногда при скиррозном типе протокового рака, в связи с плотной фиброзной стромой, а также при доль-ковом раке. Но и при других формах рака, особенно при высокой дифференцировке опухоли, нередко в пунктате обнаруживается необильный клеточный состав. Число клеток зависит также от того, насколько правильно выполнена пункция. При необильном клеточном составе желательно
повторить пункцию, при повторных неудачах -использовать иглы большего диаметра.
• Отсутствие упорядоченности расположения клеток в комплексах.
При раке в цитологических препаратах вместо структур, свойственных доброкачественным процессам, обнаруживают комплексы, для которых характерны:
— потеря полярности расположения ядер (ядра ориентированы в разных направлениях);
— неодинаковое расстояние между клетками. Однако при некоторых формах рака, например при слизистом, может сохраняться плотное
расположение клеток в скоплениях. Такие скопления нужно рассматривать очень внимательно, чтобы оценить характер клеток, детали которых увидеть трудно из-за наложения ядер.
• Разрозненное расположение клеток с сохранившейся цитоплазмой.
Дегенеративные изменения клеток и ядер
Наличие слизи или эритроцитов в аспирате не является признаком доброкачественности или злокачественности.
Нарушение ядерно-цитоплазматического соотношения
Для рака характерны разные размеры и форма опухолевых клеток. Однако некоторые классические для большинства локализаций критерии злокачественности не могут быть оценены по пун-ктатам из молочной железы. Так, например, увеличение ядерно-цитоплазменного соотношения в пунктатах молочной железы удается отметить не всегда.
Ядерно-цитоплазменное соотношение в клетках протокового эпителия, как правило, сдвинуто в сторону ядер. В злокачественных опухолях нередко увеличивается размер и ядер и цитоплазмы, кроме того, цитоплазма клеток бывает нежной, клеточная мембрана недостаточно плотной, границы ее видны нечетко, оценить ядерно-цитоплазменное соотношение достаточно сложно, поэтому при установлении диагноза рака большое значение имеют изменения ядер.
Читайте также:

