Какая связь образуется между водородом и хлором
Химические свойства водорода
Атом водорода имеет электронную формулу внешнего (и единственного) электронного уровня 1s 1 . С одной стороны, по наличию одного электрона на внешнем электронном уровне атом водорода похож на атомы щелочных металлов. Однако, ему, так же как и галогенам не хватает до заполнения внешнего электронного уровня всего одного электрона, поскольку на первом электронном уровне может располагаться не более 2-х электронов. Выходит, что водород можно поместить одновременно как в первую, так и в предпоследнюю (седьмую) группу таблицы Менделеева, что иногда и делается в различных вариантах периодической системы:
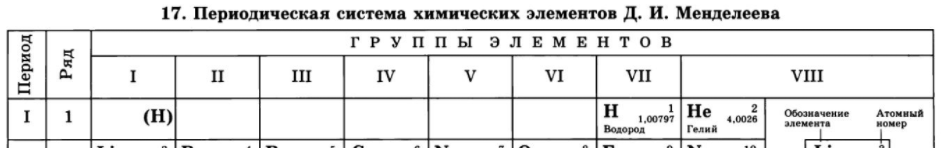
С точки зрения свойств водорода как простого вещества, он, все-таки, имеет больше общего с галогенами. Водород, также как и галогены, является неметаллом и образует аналогично им двухатомные молекулы (H2).
В обычных условиях водород представляет собой газообразное, малоактивное вещество. Невысокая активность водорода объясняется высокой прочностью связи между атомами водорода в молекуле, для разрыва которой требуется либо сильное нагревание, либо применение катализаторов, либо и то и другое одновременно.
Из металлов водород реагирует только с щелочными и щелочноземельными! К щелочным металлам относятся металлы главной подгруппы I-й группы (Li, Na, K, Rb, Cs, Fr), а к щелочно-земельным — металлы главной подгруппы II-й группы, кроме бериллия и магния (Ca, Sr, Ba, Ra)
При взаимодействии с активными металлами водород проявляет окислительные свойства, т.е. понижает свою степень окисления. При этом образуются гидриды щелочных и щелочноземельных металлов, которые имеют ионное строение. Реакция протекает при нагревании:
Следует отметить, что взаимодействие с активными металлами является единственным случаем, когда молекулярный водород Н2 является окислителем.
Из неметаллов водород реагирует только c углеродом, азотом, кислородом, серой, селеном и галогенами!
Под углеродом следует понимать графит или аморфный углерод, поскольку алмаз — крайне инертная аллотропная модификация углерода.
При взаимодействии с неметаллами водород может выполнять только функцию восстановителя, то есть только повышать свою степень окисления:
Водород не реагирует с оксидами металлов, находящихся в ряду активности металлов до алюминия (включительно), однако, способен восстанавливать многие оксиды металлов правее алюминия при нагревании:
Из оксидов неметаллов водород реагирует при нагревании с оксидами азота, галогенов и углерода. Из всех взаимодействий водорода с оксидами неметаллов особенно следует отметить его реакцию с угарным газом CO.
С неорганическими кислотами водород не реагирует!
Из органических кислот водород реагирует только с непредельными, а также с кислотами, содержащими функциональные группы способные к восстановлению водородом, в частности альдегидные, кето- или нитрогруппы.
В случае водных растворов солей их взаимодействие с водородом не протекает. Однако при пропускании водорода над твердыми солями некоторых металлов средней и низкой активности возможно их частичное или полное восстановление, например:
Химические свойства галогенов
Галогенами называют химические элементы VIIA группы (F, Cl, Br, I, At), а также образуемые ими простые вещества. Здесь и далее по тексту, если не сказано иное, под галогенами будут пониматься именно простые вещества.
Все галогены имеют молекулярное строение, что обусловливает низкие температуры плавления и кипения данных веществ. Молекулы галогенов двухатомны, т.е. их формулу можно записать в общем виде как Hal2.
Следует отметить такое специфическое физическое свойство йода, как его способность к сублимации или, иначе говоря, возгонке. Возгонкой, называют явление, при котором вещество, находящееся в твердом состоянии, при нагревании не плавится, а, минуя жидкую фазу, сразу же переходит в газообразное состояние.
Электронное строение внешнего энергетического уровня атома любого галогена имеет вид ns 2 np 5 , где n – номер периода таблицы Менделеева, в котором расположен галоген. Как можно заметить, до восьмиэлектронной внешней оболочки атомам галогенов не хватает всего одного электрона. Из этого логично предположить преимущественно окисляющие свойства свободных галогенов, что подтверждается и на практике. Как известно, электроотрицательность неметаллов при движении вниз по подгруппе снижается, в связи с чем активность галогенов уменьшается в ряду:
Все галогены являются высокоактивными веществами и реагируют с большинством простых веществ. Однако, следует отметить, что фтор из-за своей чрезвычайно высокой реакционной способности может реагировать даже с теми простыми веществами, с которыми не могут реагировать остальные галогены. К таким простым веществам относятся кислород, углерод (алмаз), азот, платина, золото и некоторые благородные газы (ксенон и криптон). Т.е. фактически, фтор не реагирует лишь с некоторыми благородными газами.
Остальные галогены, т.е. хлор, бром и йод, также являются активными веществами, однако менее активными, чем фтор. Они реагируют практически со всеми простыми веществами, кроме кислорода, азота, углерода в виде алмаза, платины, золота и благородных газов.
При взаимодействии всех галогенов с водородом образуются галогеноводороды с общей формулой HHal. При этом, реакция фтора с водородом начинается самопроизвольно даже в темноте и протекает со взрывом в соответствии с уравнением:
Реакция хлора с водородом может быть инициирована интенсивным ультрафиолетовым облучением или нагреванием. Также протекает со взрывом:
Бром и йод реагируют с водородом только при нагревании и при этом, реакция с йодом является обратимой:
Взаимодействие фтора с фосфором приводит к окислению фосфора до высшей степени окисления (+5). При этом происходит образование пентафторида фосфора:
При взаимодействии хлора и брома с фосфором возможно получение галогенидов фосфора как в степени окисления + 3, так и в степени окисления +5, что зависит от пропорций реагирующих веществ:
При этом в случае белого фосфора в атмосфере фтора, хлора или жидком броме реакция начинается самопроизвольно.
Взаимодействие же фосфора с йодом может привести к образованию только триодида фосфора из-за существенно меньшей, чем у остальных галогенов окисляющей способности:
Фтор окисляет серу до высшей степени окисления +6, образуя гексафторид серы:
Хлор и бром реагируют с серой, образуя соединения, содержащие серу в крайне не свойственных ей степенях окисления +1 и +2. Данные взаимодействия являются весьма специфичными, и для сдачи ЕГЭ по химии умение записывать уравнения этих взаимодействий не обязательно. Поэтому три нижеследующих уравнения даны скорее для ознакомления:
Как уже было сказано выше, фтор способен реагировать со всеми металлами, даже такими малоактивными как платина и золото:
Остальные галогены реагируют со всеми металлами кроме платины и золота:
Более активные галогены, т.е. химические элементы которых расположены выше в таблице Менделеева, способны вытеснять менее активные галогены из образуемых ими галогеноводородных кислот и галогенидов металлов:
Аналогичным образом, бром вытесняет серу из растворов сульфидов и сероводорода:
Хлор является более сильным окислителем и окисляет сероводород в его водном растворе не до серы, а до серной кислоты:
Вода горит во фторе синим пламенем в соответствии с уравнением реакции:
Бром и хлор реагируют с водой иначе, чем фтор. Если фтор выступал в роли окислителя, то хлор и бром диспропорционируют в воде, образуя смесь кислот. При этом реакции обратимы:
Взаимодействие йода с водой протекает в настолько ничтожно малой степени, что им можно пренебречь и считать, что реакция не протекает вовсе.
Фтор при взаимодействии с водным раствором щелочи опять же выступает в роли окислителя:
Умение записывать данное уравнение не требуется для сдачи ЕГЭ. Достаточно знать факт о возможности такого взаимодействия и окислительной роли фтора в этой реакции.
а при нагревании:
Йод реагирует с щелочами исключительно по второму варианту, т.е. с образованием йодата, т.к. гипоиодит не устойчив не только при нагревании, но также при обычной температуре и даже на холоду:

Рассмотрим взаимодействия, возникающие между отдельными молекулами в веществе — межмолекулярные взаимодействия . Межмолекулярные взаимодействия — это такой вид взаимодействия между нейтральными атомами, при котором не образуются новые ковалентные связи. Силы взаимодействия между молекулами обнаружены Ван-дер Ваальсом в 1869 году, и названы в честь него Ван-дар-Ваальсовыми силами . Силы Ван-дер-Ваальса делятся на ориентационные, индукционные и дисперсионные . Энергия межмолекулярных взаимодействий намного меньше энергии химической связи.
Ориентационные силы притяжения возникают между полярными молекулами (диполь-диполь взаимодействие). Эти силы возникают между полярными молекулами. Индукционные взаимодействия — это взаимодействие между полярной молекулой и неполярной. Неполярная молекула поляризуется из-за действия полярной, что и порождает дополнительное электростатическое притяжение.
Особый вид межмолекулярного взаимодействия — водородные связи.
Водородные связи — это межмолекулярные (или внутримолекулярные) химические связи, возникающие между молекулами, в которых есть сильно полярные ковалентные связи — H-F, H-O или H-N. Если в молекуле есть такие связи, то между молекулами будут возникать дополнительные силы притяжения.
Механизм образования водородной связи частично электростатический, а частично — донорно–акцепторный. При этом донором электронной пары выступают атом сильно электроотрицательного элемента (F, O, N), а акцептором — атомы водорода, соединенные с этими атомами. Для водородной связи характерны направленность в пространстве и насыщаемость.
Водородную связь можно обозначать точками: Н ··· O. Чем больше электроотрицательность атома, соединенного с водородом, и чем меньше его размеры, тем крепче водородная связь . Она характерна прежде всего для соединений фтора с водородом, а также кислорода с водородом, в меньшей степени азота с водородом.

Водородные связи возникают между следующими веществами:
- фтороводород HF (газ, раствор фтороводорода в воде — плавиковая кислота),
- вода H2O (пар, лед, жидкая вода):
- раствор аммиака и органических аминов — между молекулами аммиака и воды;
- органические соединения, в которых есть связи O-H или N-H : спирты, карбоновые кислоты, амины, аминокислоты, фенолы, анилин и его производные, белки, растворы углеводов — моносахаридов и дисахаридов.
Водородная связь оказывает влияние на физические и химические свойства веществ. Так, дополнительное притяжение между молекулами затрудняет кипение веществ. У веществ с водородными связями наблюдается аномальное повышение тепературы кипения.
Например , как правило, при повышении молекулярной массы наблюдается повышение температуры кипения веществ. Однако в ряду веществ H2O-H2S-H2Se-H2Te мы не наблюдаем линейное изменение температур кипения.

А именно, у воды температура кипения аномально высокая — не меньше -61 о С, как показывает нам прямая линия, а намного больше, +100 о С. Эта аномалия объясняется наличием водородных связей между молекулами воды. Следовательно, при обычных условиях (0-20 о С) вода является жидкостью.
Кемеровский государственый университет
- Главная
- О факультете
- Абитуриенту
- Учебный процесс
- Студенту
- Научная работа
- Студенческая жизнь
- Поздравления
- КемГУ
- Наши выпускники
Материалы
Тема 3. Химическая связь. Задания
1.Валентность хрома в соединениях CrO, Cr2O3, CrO3 равна соответственно:
- II, III, VI
- I, II, III
- во всех соединениях II
- во всех соединениях I
2. Степень окисления -3 азот проявляет в соединении:
3. В соединении HClO3 степень окисления хлора равна:
- -1
- +5
- +3
- +7
4. Свою максимальную степень окисления бром проявляет в соединении:
- NaBr
- HBrO
- BrF5
- KBrO4
5. В каком соединении углерод проявляет низшую степень окисления:
6. Высшая положительная степень окисления марганца равна:
- +2
- +4
- +7
- +8
7. Вещество с ионной связью имеет формулу:
- HCl
- CF4
- SO2
- KBr;
8. Только ковалентная связь имеет место в соединении с формулой:
9. Ковалентная неполярная связь наблюдается в следующем веществе:
- аммиак
- алмаз
- углекислый газ
- хлороформ;
10. Ковалентная связь отличается от ионной:
- большей длиной
- меньшей энергией
- общими электронными парами между атомами
- меньшей длиной;
11. Только ионные связи имеют место в веществе:
- пероксид натрия
- гашеная известь
- медный купорос
- сильвинит.
12. Химическая связь наиболее прочна в молекуле:
- йодоводорода
- кислорода
- хлора
- азота;
13. Наиболее выражен характер ионной связи в соединении:
- хлорид кальция
- фторид калия
- фторид алюминия
- хлорид натрия;
14. Длина связи увеличивается в ряду веществ, имеющих формулы:
15. Длина связи увеличивается в ряду:
- H2O – H2S – H2Se,
- HBr – HCl – HI,
- NH3 – H2O – HF,
- H2Se – H2S – HCl;
16. Вещество, имеющее молекулу с кратной связью, - это:
- углекислый газ
- хлор
- аммиак
- этанол;
17. Число π – связей в молекуле пропеновой кислоты равно:
- одной
- двум
- трем
- четырем;
18. Образование водородной связи между молекулами веществ не оказывает влияния на физическое свойство:
- электропроводность
- плотность
- температура кипения
- температура плавления;
19. Наиболее прочные водородные связи образуются между атомом водорода и атомом:
- азота
- кислорода
- хлора
- серы;
20. Прочность водородной связи зависит:
- от величины избыточного положительного заряда на атоме водорода,
- от электроотрицательности атома элемента, образующего такую связь с атомом водорода,
- от величины поляризации связи водород – гетероатом,
- все выше перечисленные ответы верны;
21. В молекуле этилена атомы углерода находится в состоянии:
- sp-гибридизации
- sp 2 -гибридизации
- sp 3 -гибридизации
- не гибридизованы
22. Вещество, в молекуле которого все атомы углерода находится в sp 3 -гибридном состоянии:
- ацетон
- пропаналь
- фенол
- этанол;
23. Неполярная молекула с ковалентной полярной связью – это молекула:
- аммиака
- диэтилового эфира
- тетрахлорметана
- оксида серы (IV)
24. Число σ - связей в молекуле уксусной кислоты равно:
- четырем
- пяти
- шести
- семи;
25. Линейное строение имеет молекула:
- аммиака
- воды
- метанола
- хлорида бериллия
26. В ряду NH3 → PH3 происходит увеличение:
- основных свойств
- прочности связи
- длины связи
- полярности связи;
27. Установите соответствие между формулой вещества и степенью окисления хрома в нем.
| Формула вещества: | Степень окисления Cr: |
| 1) CrO3 | A) +2 |
| 2) KCrO2 | Б) +3 |
| 3) K2Cr2O7 | В) +4 |
| 4) K3[Cr(OH)6] | Г) +5 |
| Д) +6 | |
| Е) +7; |
28. Установите соответствие между формулой вещества и степенью окисления марганца в нем.
| Формула вещества: | Степень окисления Mn: |
| 1)K2MnO4 | A) +1 |
| 2) Mn(OH)4 | Б) +2 |
| 3) MnO2 | В) +4 |
| 4) MnS | Г) +5 |
| Д) +6 | |
| Е) +7 | |
| Ж) +8; |
29. Установите соответствие между названием химического элемента и возможными значениями его степеней окисления.
| Название элемента: | Степени окисления: |
| 1) хлор | A) -2, -1, 0, +2 |
| 2) фтор | Б) -2, 0, +4, +6 |
| 3) фосфор | В) -3, 0, +3, +5 |
| 4) сера | Г) -1, 0 |
| Д) -1, 0, +1, +3, +5, +7 | |
| Е) -4, -2, 0, +2, +4 |

Общее описание
Электроотрицательность – способность атома удерживать валентные электроны на внешнем энергетическом уровне или количественная характеристика, показывающая, с какой силой притягиваются электроны к ядру атома. Наиболее электроотрицательными элементами являются фтор, азот и кислород.

Рис. 1. Ряд электроотрицательности.
Сильное электростатическое взаимодействие между атомом водорода и электроотрицательными атомами обуславливается небольшими размерами атома водорода и силой притяжения атомов элементов. В результате возникает частный случай ковалентной полярной связи. Примерами водородной химической связи являются:
- плавиковая кислота (HF);
- вода (H2O);
- аммиак (NH3);
- соляная кислота (HCl);
- сероводород (H2S).
Наличие водородной связи обуславливает физические и химические свойства вещества. В частности определяет температуру плавления, кипения, растворимость, кислотность.
Особенностью связи является её невысокая прочность и распространённость, особенно в органических веществах.
Водородная связь бывают двух типов:
- межмолекулярная, возникающая между несколькими однотипными молекулами;
- внутримолекулярная, возникающая внутри одной молекулы.
Например, молекула воды образована одним атомом кислорода и двумя атомами водорода. За счёт высокой электроотрицательности кислород, на внешнем энергетическом уровне которого шесть электронов, притягивает единственные электроны двух атомов водорода. Две пары электронов кислорода остаются свободными. При этом у водорода освобождается орбиталь. Другая аналогичная молекула может присоединиться в месте свободных электронных пар атома кислорода, заполнив освободившуюся орбиталь водорода. Возникает межмолекулярная водородная связь.

Рис. 2. Строение молекулы воды.
Аналогичным образом соединяются молекулы плавиковой кислоты и аммиака. Однако связь между азотом и водородом будет слабее, чем между водородом и кислородом. Также молекулы плавиковой кислоты сильнее притягиваются друг к другу, чем молекулы воды. Это объясняется величиной электроотрицательности.
Внутримолекулярная водородная связь чаще всего возникает внутри сложных молекул органических веществ – белков, ДНК, аренов. Например, водородная связь образуется в молекуле салициловой кислоты между атомом водорода гидроксильной группы и кислорода, входящего в функциональную группу -СООН.

Рис. 3. Водородная связь в салициловой кислоте.
Водородные связи графически изображаются точками.
Что мы узнали?
Между атомами водорода и атомами неметаллов возникает водородная связь, основанная на электростатическом взаимодействии атомов. Это частный случай ковалентной полярной связи, характеризующийся взаимодействием водорода и атомов с высокой электроотрицательностью. Связь бывает двух типов: межмолекулярная, возникающая между молекулами вещества, и внутримолекулярная, возникающая между водородом и атомом другого элемента в одной молекуле. Водородная связь присуща неорганическим и органическим веществам.
При взаимодействии двух атомов одного и того же элемента-неметалла между ними образуется ковалентная химическая связь с помощью общих электронных пар. Эту ковалентную связь называют неполярной, так как общие электронные пары принадлежат обоим атомам в одинаковой степени и ни на одном из них не будет избытка или недостатка отрицательного заряда, который несут электроны.
Однако если ковалентная связь образуется между атомами разных элементов-неметаллов, то картина будет несколько иной. Рассмотрим, например, образование молекулы хлороводорода НС1 из атомов водорода и хлора.
1. Атом водорода имеет на единственном уровне один электрон, и до его завершения ему не хватает ещё одного электрона. У атома хлора на внешнем уровне — семь электронов, и ему также недостает до завершения одного электрона.
2. Атомы водорода и хлора объединяют свои непарные электроны и образуют одну общую электронную пару, т. е. возникает ковалентная связь:

Структурная формула молекулы хлороводорода Н-С1.
3. Так как ковалентная связь образуется между атомами различных элементов-неметаллов, то общая электронная пара будет принадлежать взаимодействующим атомам уже не в равной степени. Для того чтобы качественно определить, какому из этих атомов общая электронная пара будет принадлежать в большей мере, используют понятие электроотрицательностъ.
| Электроотрицательность (ЭО) — это способность атомов химического элемента смещать к себе общие электронные пары, участвующие в образовании химической связи. |
ЭО можно охарактеризовать как меру неметалличности химических элементов. В порядке уменьшения ЭО химические элементы располагаются в следующий ряд:

Величина ЭО элемента зависит от его положения в таблице Д. И. Менделеева: в каждом периоде она обычно возрастает с увеличением порядкового номера элемента, а в каждой подгруппе — уменьшается.
Пользуясь рядом ЭО, можно определить, куда смещаются общие электронные пары. Они всегда смещены к атомам элемента с большей ЭО. Например, в молекуле хлороводорода НС1 общая электронная пара смещена к атому хлора, так как его ЭО больше, чем у водорода. В результате на атомах образуются частичные заряды 
, в молекуле возникают два полюса — положительный и отрицательный. Поэтому такую ковалентную связь называют полярной.
В формулах соединений химический знак менее электроотрицательного элемента пишут первым. Так как ковалентная полярная связь является разновидностью ковалентной связи, то алгоритм рассуждений для её схематического изображения такой же, как и для ковалентной неполярной связи (см. § 11), только в этом случае добавится ещё один шаг — четвёртый: по ряду ЭО определим более электроотрицательный элемент и отразим полярность связи в структурной формуле стрелкой и обозначением частичных зарядов.
Например, рассмотрим алгоритм схематического изображения образования связи для соединения OF2 — фторида кислорода.
1. Кислород — это элемент главной подгруппы VI группы (VIA группы) Периодической системы Д. И. Менделеева. Его атомы имеют по шесть электронов на внешнем электронном слое. Непарных электронов будет: 8-6 = 2.
Фтор — элемент главной подгруппы VII группы (VIIA группы) Периодической системы Д. И. Менделеева. Его атомы содержат по семь электронов на внешнем электронном слое. Непарным является один электрон.
2. Запишем знаки химических элементов с обозначением внешних электронов:

3. Запишем электронную и структурную формулы образовавшихся молекул:

4. По ряду ЭО определим, что общие электронные пары будут смещены от кислорода к фтору, как к более электроотрицательному элементу, т. е. связь будет ковалентной полярной: 
.
Аналогично образуются молекулы воды:

В действительности молекула воды имеет не линейную, а угловую форму (∠HOH = 104°27'). Строение молекулы воды можно изобразить различными способами (рис. 40).

Рис. 40.
Различные модели молекулы воды
| Число ковалентных связей, которыми атом одного химического элемента связан с атомами этого же или других элементов, называется валентностью. |
Атом водорода образует только одну ковалентную связь с другими атомами. Поэтому говорят, что водород одновалентен. Атом кислорода связан с другими атомами двумя химическими связями — он двухвалентен. При образовании молекул атомы соединяются таким образом, чтобы все их валентности были задействованы. Понятно, что двухвалентный кислород должен соединиться с двумя атомами одновалентного водорода. Если обозначить валентность чёрточкой, то схему образования молекулы воды можно представить так:

Аналогично трёхвалентный азот соединяется с тремя атомами одновалентного водорода в молекулу аммиака

Формулы, в которых валентности элементов обозначены чёрточками, как вы знаете, называют структурными.
Структурная формула метана СН4 — соединение четырёхвалентного углерода с водородом — будет следующей:
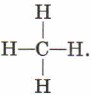
А каким образом соединяются в молекулу углекислого газа С02 атомы четырёхвалентного углерода и двухвалентного кислорода? Очевидно, этот способ может отразить только следующая структурная формула:

Является ли валентность постоянной величиной? Оказывается для водорода и кислорода это утверждение верно, а вот для азота и углерода нет, так как эти элементы могут проявлять и другие значения валентности. Например, азот может быть одно-, двух-, трёх-, четырёхвалентен. Его соединения с кислородом будут иметь разный состав. Следовательно, различают:
- элементы с постоянной валентностью (например, одновалентные: Н, F; двухвалентные: О, Be; трёхвалентные: В, А1);
- элементы с переменной валентностью (например, S проявляет валентности II, IV, VI; С1 — валентности I, III, V и VII).
Давайте научимся выводить формулы двухэлементных соединений по валентности.
Для вывода формулы соединения фосфора с кислородом, в котором фосфор пятивалентен, порядок действий следующий:
-
запишем рядом знаки элементов:

над знаками римскими цифрами обозначим валентности элементов:

найдём наименьшее общее кратное между валентностями элементов:

разделим наименьшее общее кратное на валентность каждого элемента — определим индексы, т. е. число атомов каждого элемента в формуле данного вещества (для фосфора индекс равен 2, а для кислорода — 5):

Аналогично выведем формулу соединения азота с кислородом, в котором азот четырёхвалентен.

Индекс 1 в формулах не записывается.
Знание валентности химических элементов необходимо для того, чтобы верно записать формулу вещества. Однако справедливо и обратное: по формуле вещества можно определить валентность одного из элементов, если известна валентность другого. Например, определим валентность серы в соединении, формула которого SО3:
-
над знаком кислорода в формуле обозначим его валентность, так как она постоянна, а потому известна:
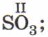
определим общее число валентностей всех атомов кислорода:

разделим полученное число на число атомов серы — это и будет значение её валентности:
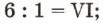
запишем валентность серы над её знаком в формуле:

Используя шаростержневые наборы, соберите модели молекул следующих веществ:
- вариант 1 — хлороводорода НС1, четырёххлористого углерода СС14;
- вариант 2 — сернистого газа SО2, хлорида алюминия AlCl3.
Ключевые слова и словосочетания
- Ковалентная неполярная и ковалентная полярная химические связи.
- Электроотрицательность.
- Частичный заряд.
- Валентность.
- Составление формул ковалентных соединений по валентности.
- Определение валентности по формулам.
Работа с компьютером
- Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
- Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
Читайте также:

