Иммунотерапия при плоскоклеточном раке легкого
Последние мои публикации были посвящены результатам применения ингибиторов контрольных точек иммунного ответа в первой линии системной терапии немелкоклеточного рака легкого (НМРЛ). Результаты исследований, доложенные на прошедших конгрессах AACR и ASCO в этом году, полностью изменили наше представление о характере ее проведения.
Уместно вспомнить, что еще в декабре 2016 года схема лечения метастатического НМРЛ была предельна проста. Больные аденокарциномой с активирующими мутациями были кандидатами для получения таргетных препаратов. В случае прогрессирования после ингибиторов тирозинкиназы больным было показано назначение химиотерапии. Остальные больные НМРЛ были кандидатами для получения химиотерапии. У больных аденокарциномой в качестве химиотерапии первой линии преимущественно назначали комбинации цисплатина и пеметрекседа или карбоплатина и паклитаксела. У больных плоскоклеточным раком в качестве химиотерапии первой линии назначали комбинацию цисплатина и гемцитабина или цисплатина и паклитаксела. В случае прогрессирования больным назначали вторую линию препаратами пеметрексед или доцетаксел.
Все изменилось в декабре 2016 года, когда стали доступны результаты исследования KEYNOTE 024, в котором проводили сравнение между ингибитором PD-1 пембролизумабом и химиотерапией в качестве первой линии у больных НМРЛ с экспрессией PD-L1 более 50%. Столь высокая экспрессия PD-L1 диагностируется у 25-30% больных НМРЛ независимо от гистологии опухоли. Назначение пембролизумаба в первой линии достоверно снизило относительный риск прогрессирования на 50% и риск смерти на 37% по сравнению с химиотерапией [1]. Медиана продолжительности жизни в группе пембролизумаба достигла 30,0 мес. по сравнению с 14,2 мес. в группе химиотерапии при одновременной лучшей переносимости лечения [2]. В связи с этим пембролизумаб был рекомендован в качестве предпочтительной первой линии системной терапии у больных как аденокарциномой, так и плоскоклеточным раком с высокой экспрессией PD-L1. Ни ниволумаб, ни атезолизумаб в монотерапии не смогли продемонстрировать преимущество перед химиотерапией у больных НМРЛ.
В исследовании KEYNOTE 189 у больных аденокарциномой независимо от экспрессии PD-L1 проведено сравнение химиотерапии и комбинации химиотерапии и пембролизумаба. Комбинация пембролизумаба и химиотерапии продемонстрировала лучшие отдаленные результаты по сравнению с химиотерапией только, достоверно уменьшив относительный риск прогрессирования и смерти на 48% и 51% соответственно [3]. Преимущество комбинации отмечено во всех изученных подгруппах, в том числе и у больных с различной экспрессией PD-L1. Относительный риск смерти при добавлении пембролизумаба был снижен на 41% в группе с отсутствием экспрессии PD-L1, на 45% – в группе с экспрессией PD-L1 1-49% и на 58% – в группе с экспрессией более 50%. Остается неясным, есть ли выигрыш от использования комбинации химиотерапии и пембролизумаба в сравнении с пембролизумабом только, который в монотерапии показал прекрасные результаты у больных с высокой экспрессией PD-L1. При этом большинство специалистов рекомендуют монотерапию пембролизумабом у больных с высокой экспрессией, резервируя использование комбинации с химиотерапией для больных аденокарциномой с низкой экспрессией (менее 50%) или ее отсутствием.
В исследовании iMPower 150 у больных с аденокарциномой независимо от экспрессии PD-L1 оценена целесообразность добавления атезолизумаба к комбинации химиотерапии и бевацизумаба. При медиане наблюдения 9,5 мес. добавление атезолизумаба достоверно уменьшило относительный риск прогрессирования на 38% и риск смерти на 22% по сравнению с комбинацией химиотерапии и только бевацизумаба [4]. Улучшение результатов лечения при добавлении атезолизумаба было отмечено у всех больных, независимо от уровня экспрессии PD-L1. Интерес представляет наблюдение о высокой активности комбинации атезолизумаба, бевацизумаба и химиотерапии у больных с активирующими мутациями при прогрессировании на фоне ингибиторов тирозинкиназы.
Оставалась еще одна группа больных, для которой требовалось определить эффективность иммунотерапии в первой линии. Это больные с плоскоклеточным раком и экспрессией PD-L1 менее 50%. В исследовании KEYNOTE-407 проведено сравнение химиотерапии и комбинации химиотерапии и пембролизумаба у больных IIIb-IV стадией плоскоклеточного рака независимо от уровня экспрессии PD-L1. При медиане наблюдения 8 месяцев назначение комбинации привело к снижению относительного риска смерти на 36% и прогрессирования на 44% по сравнению с химиотерапией [5]. Увеличение продолжительности жизни при добавлении пембролизумаба наблюдалось во всех анализируемых подгруппах, в том числе и при различной экспрессии PD-L1. Сделан предварительный вывод, что добавление пембролизумаба к химиотерапии достоверно и существенно улучшает отдаленные результаты лечения больных плоскоклеточным раком легкого независимо от уровня экспрессии PD-L1. Полученные результаты являются серьезным аргументом для регистрации комбинации пембролизумаба и химиотерапии в качестве предпочтительной первой линии системной терапии у больных плоскоклеточным раком с низкой экспрессией PD-L1.
Для больных плоскоклеточным раком независимо от уровня экспрессии PD-L1 в исследовании iMpower 131 проведено сравнение химиотерапии и комбинации химиотерапии и атезолизумаба. При медиане наблюдения 17 мес. добавление атезолизумаба к химиотерапии уменьшило относительный риск прогрессирования на 29% по сравнению с только химиотерапией, не оказав влияния на показатели общей выживаемости [6].
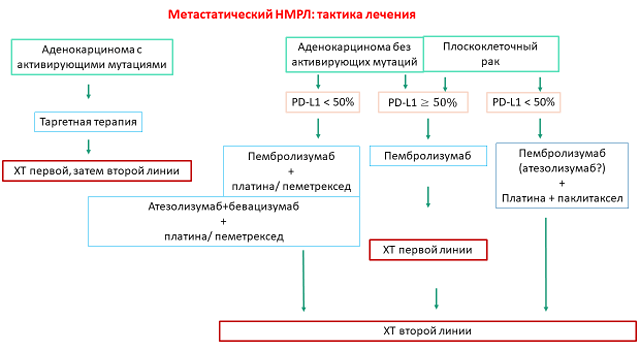
Рисунок 1. Тактика лечения больных метастатическим НМРЛ (по результатам проведенных исследований).
Таким образом, проведенные исследования изменили рекомендации по выбору первой линии системной терапии у больных НМРЛ (рис. 1). Химиотерапия, которая была до недавнего времени основным методом лечения этих больных, потеряла свое самостоятельное значение. У больных с высокой экспрессией PD-L1, вероятно, достаточно назначения одного пембролизумаба. У больных с аденокарциномой и низкой экспрессией PD-L1 показано назначение пембролизумаба и химиотерапии или комбинации атезолизумаба, бевацизумаба и химиотерапии. У больных с плоскоклеточным раком и низкой экспрессией PD-L1 рекомендовано назначения комбинации пембролизумаба и химиотерапии. Возможно, для этой группы больных будет рекомендована комбинация атезолизумаба и химиотерапии.
Теперь для определения тактики лечения нам необходимо кроме гистологии и наличия активирующих мутаций в опухоли знать уровень экспрессии PD-L1. Российское общество клинической онкологии в рамках программы молекулярно-генетической диагностики (www.cancergenome.ru) начало определение экспрессии PD-L1 в опухоли. Хочется надеяться, что использование моноклональных антител ингибиторов контрольных точек иммунного ответа отдельно или совместно с химиотерапией станут доступны и российским онкологам, что непременно приведет к существенному улучшению отдаленных результатов лечения больных метастатическим НМРЛ.
Ключевые слова: немелкоклеточный рак легкого, пембролизумаб, атезолизумаб, химиотерапия.
- Reck M, Rodríguez-Abreu D, Robinson AG, et al. Pembrolizumab versus chemotherapy for PD-L1-positive non-small-cell lung cancer. N. Engl. J. Med. 2016; 375 (19): 1823-1833.
- Brahmer JR, Rodríguez-Abreu D, Robinson AG, et al. Health-related quality-of-life results for pembrolizumab versus chemotherapy in advanced, PD-L1-positive NSCLC (KEYNOTE-024): a multicentre, international, randomized, open-label phase 3 trial. Lancet Oncol. 2017 Dec; 18(12): 1600-1609.
- Gandhi L, Rodriguez-Abreu D, Gadgeel S, et al. KEYNOTE-189: randomized double-blind, phase 3 study of pembrolizumab or placebo plus pemetrexed and platinum as first-line therapy for metastatic NSCLC. AACR 2018.
- Socinsky M.A., Jotte R.M., Cappuzzo F, et al. Atezolizumab for first-line treatment of metastatic nonsquamous NSCLC. N. Engl. J.Med 2018, published online June 4.
- Paz-Ares L, Luft A, Tafreshi A, et al. KEYNOTE-407: phase 3 study of carboplatin-paclitaxel/nab-paclitaxel with or without pembrolizumab for metastatic squamous NSCLC. ASCO 2018.
- Jotte RM, Cappuzzo F, Vynnychenko I, et al. IMpower131: Primary PFS and safety analysis of a randomized phase III study of atezolizumab + carboplatin + paclitaxel or nab-paclitaxel vs carboplatin + nab-paclitaxel as 1L therapy in advanced squamous NSCLC. ASCO 2018; abstract LBA9000.
Активная иммунотерапия рака легкого
В настоящее время рак легкого является наиболее распространенной формой опухоли у мужчин и остается одной из важнейших медицинских и социально-экономических проблем.
Различают два гистологических типа опухоли: немелкоклеточный и мелкоклеточный. По локализации различают центральный и периферический рак легкого.
Хирургический метод лечения рака легкого на ранних стадиях болезни до сих пор является единственно радикальным.
Радиохимиотерапия распространенных форм заболевания решает в основном паллиативные задачи и не оказывает существенного влияния на показатели выживаемости пациентов. Поэтому, иммунотерапия рассматривается как наиболее перспективный метод системного лечения рака легкого.
Наш опыт свидетельствует о том, что клинический эффект разной степени выраженности (полный, частичный ответ, стабилизация болезни) продолжительностью не менее 6 месяцев может быть достигнут у значительной части вакцинированных пациентов с IV стадией рака легкого.
Пациент Д, 50 лет с диагнозом: центральный плоскоклеточный рак левого нижнедолевого бронха, MTS в верхней доли правого легкого и региональных лимфоузлах (T2 N3M1), ателектаз 6 сегмента слева, начал получать иммунотерапевтическое лечение, находясь в состоянии средней степени тяжести. Имелись жалобы на одышку, слабость, утомляемость, кашель со скудным отделяемым, периодическое кровохарканье, а также на боли в области поясницы. СОЭ – 60 мм/ч. В ответ на первую вакцинацию отмечен подъем температуры тела до 38.5ºС. Далее было отмечено ухудшение состояния: усилилась одышка и кровохарканье. Из-за слабости и быстрой утомляемости пациент большую часть времени проводил в постели. В связи с этим была расширена симптоматическая терапия. Однако, в течение 2 месяцев состояние стабилизировалось, симптомы сгладились. Через год после начала иммунотерапии показатели крови пришли в норму. Рентгенологическая картина была без отрицательной динамики. По данным УЗИ было обнаружено образование в правой почке размером 56х54 мм. Появилась периодически возникающая макрогематурия. Назначено симптоматическое (гемостатики и уросептики) лечение.
Через 3 года после начала иммунотерапии было проведено очередное обследование. Рентгенологическая картина: трахея и органы средостения резко смещены влево; легочной рисунок деформирован, грубый ячеистый пневмосклероз; корень неструктурен, костальная плевра утолщена на всем протяжении; cправа в верхней доле, апикально, неинтенсивного характера мелкоочаговые тени. Изменения в левом легком можно было трактовать как последствия хронического диффузного бронхолегочного процесса. По данным КТ выявлены признаки очагового образования правой почки (49,5 х 56,4 х 6,0 мм.), в области тела подвздошной кости определялся участок деструкции неправильной формы размерами 27,9 х 61,2 х 70 мм. Была удалена правая почка (гистология – MTS) и продолжена вакцинотерапия в усиленном режиме. Состояние через 4,5 года после начала вакцинотерапии стабильное, данных за прогрессию заболевания отмечено не было.
Пациент Е, 75 лет с дагнозом: центральный плоскоклеточный рак правого лёгкого (Т3N1Mх) на момент начала вакцинотерапии предъявлял жалобы на кашель с умеренным количеством белой, тягучей мокроты, одышку в покое, слабость. Индекс Карновского 70%. Ренгенологически был выявлен участок уплотнения линейной формы в S3 слева и II межреберье справа. В анализах крови и мочи без патологии. Лечение переносил хорошо. В дни вакцинации отмечалась субфебрильная температура, местно в месте инъекции развивалось покраснение, болезненное при пальпации, исчезающее в течение нескольких часов.
Рак легких - одна из самых распространенных злокачественных опухолей. Врачи ежегодно выявляют около 1,8 миллионов новых случаев. Заболевание встречается одинаково часто среди мужчин и женщин. Ежегодно 1,6 миллионов человек погибают от рака легких, и это ведущая причина смертности от онкологических заболеваний.
Каждый пятый онкологический больной погибает от рака легких
Чаще всего опухоль выявляют на поздних стадиях — IIIB и IV. Химиотерапия, лучевая терапия и хирургические вмешательства могут продлить жизнь таких пациентов, но вероятность полного излечения крайне низкая. Несмотря на появление новых, более эффективных, химиопрепаратов, прогноз для многих больных по-прежнему остается неблагоприятным — нередко после лечения происходят рецидивы. Поиск новых методов лечения, которые помогли бы более эффективно бороться с раком легких — очень актуальная задача, стоящая перед современной онкологией. Многие ученые видят большие перспективы в применении иммунотерапии.
Рак легких всегда относили к опухолям, имеющим низкую иммуногенность — в опухолевых клетках очень мало антигенов, которые могли бы стать мишенями для иммунопрепаратов. Тем не менее, исследования показали, что иммунотерапия при раке легких может быть эффективна.
Какие виды иммунотерапии применяются при раке легких?
Существует две основные разновидности рака легких: мелкоклеточный (МРЛ) и немелкоклеточный (НМРЛ). Также встречается мезотелиома — злокачественная опухоль плевры. На данный момент дальше всего удалось продвинуться в применении иммунопрепаратов для лечения немелкоклеточного рака, который встречается в 85% случаев. Но ученые также активно занимаются разработкой новых методов иммунотерапии, которые были бы эффективны против мелкоклеточного рака легких и мезотелиомы.
Существует 4 направления иммунотерапии в лечении рака легких:
Моноклональные антитела
Моноклональные антитела — это молекулы, которые прицельно связываются с определенными антигенами опухолевых клеток. Сегодня многие из них применяются для лечения онкологических заболеваний.
Например, Американским управлением по надзору за качеством пищевых продуктов и медикаментов (FDA) утвержден для лечения немелкоклеточного рака легких препарат Бевацизумаб (Авастин). Его мишенью является фактор роста эндотелия сосудов (ФРЭТ, VEGF).
Ипилимумаб (Ipilimumab, Ервой, Yervoy). В 2011 году этот препарат был одобрен для лечения пациентов с метастатической меланомой. В настоящее время Ипилимумаб проходит испытания при НМРЛ и МРЛ.
Ниволумаб (Nivolumab, Опдиво, Opdivo). В марте 2015 года одобрен для лечения пациентов с плоскоклеточным НМРЛ, устойчивым к химиотерапии.
Пемброзилумаб (Pembrolizumab, Кейтруда, Keytruda). Препарат был одобрен FDA для лечения меланомы в сентябре 2014 года, а для лечения немелкоклеточного рака легкого — в октябре 2014 года.
Лечебные вакцины
Задача лечебных вакцин — активировать B- и T-лимфоциты, чтобы они могли атаковать определенные типы раковых клеток. Для этого в организм пациента вводят соответствующий антиген. Мишенью для лечебных вакцин являются общие или опухоль-специфические антигены, такие как:
- MAGE-3 — экспрессируется в 42% случаев рака легких;
- NY-ESO-1 — экспрессируется в 30% случаев рака легких;
- р53 — мутирует в 50% случаев рака легких.
Адаптивный перенос Т-лимфоцитов
Лечение рака легких в Европейской онкологической клинике
Ученые, которые занимаются исследованиями в области иммунотерапии рака легкого и других злокачественных опухолей, сталкиваются с рядом сложностей. Далеко не все попытки увенчиваются успехом, не все предположения оказываются верны при проверке на практике. Исследования занимают много времени, требуют больших затрат и задействования многих ресурсов. Самые мощные препараты зачастую имеют серьезные побочные эффекты и могут применяться не у всех пациентов.
Несмотря на это, наука постоянно движется вперед. Иммунотерапия имеет большие перспективы. Многие препараты уже одобрены и успешно применяются в онкологических клиниках — они помогают улучшить прогнозы, продлить жизнь пациентов.
Европейская онкологическая клиника старается постоянно находиться на острие последних достижений онкологии. Мы сотрудничаем с крупнейшими зарубежными клиниками для того, чтобы наши пациенты могли получить наиболее качественную медицинскую помощь, наилучший результат из возможных.

Иммунотерапия, также известная как биологическая терапия, может принести неоценимую пользу людям, борющимся с определенными видами рака легких.
Этот метод лечения основан на применении высокоселективных препаратов, которые стимулируют иммунную систему для эффективной борьбы с раком.
За пару десятилетий иммунотерапия смогла изменить взгляды на лечение многих видов рака, включая рак легких, молочной железы, колоректальный рак.
В этой статье мы рассмотрим, как работает иммунотерапия, как биологические препараты помогают людям с раком легких и какими могут быть побочные эффекты.
Что такое иммунотерапия рака легких
Существует несколько типов иммунотерапии для борьбы с опухолями легких:
• адаптивная Т-клеточная иммунотерапия
• ингибиторы иммунных контрольных точек
• терапевтические вакцины
Каждый вид иммунотерапии обладает своими преимуществами, недостатками и особенностями применения. По-прежнему существует потребность в дополнительных исследованиях, потому что медицина только начинает открывать это направление и управлять удивительными возможностями иммунной клетки.
Как работает иммунотерапия
Метод достаточно сложный и дорогостоящий. Адаптивная Т-клеточная терапия требует современного лабораторного оборудования и специально подготовленных специалистов, поэтому доступна далеко не во всех онкологических центрах.
Этот метод демонстрирует многообещающие результаты, однако он нуждается в дополнительных исследованиях, чтобы широко использоваться для лечения рака легких.
Иммунная система человека постоянно обследует организм на присутствие чужеродных частиц и мутировавших клеток, немедленно распознавая и устраняя их. Иммунные клетки несут определенные контрольные молекулы, которые мешают иммунной системе повреждать нормальные ткани. Однако раковые клетки используют эти же контрольные точки, чтобы избежать атаки со стороны иммунной системы.
Ингибиторы иммунных контрольных точек не позволяют злокачественным клеткам прикрываться этими молекулами. Подавляя контрольные точки, эти препараты помогают лимфоцитам нацеливаться на опухоль и разрушать ее.
Администрация по контролю за продуктами и лекарствами США (FDA) одобрила уже несколько ингибиторов иммунных контрольных точек для лечения рака легких.
Эти препараты подразделяются на две категории:
Примеры ингибиторов PD1 и PD-L1 (международные непатетнованные названия):
• nivolumab (ниволумаб)
• durvalumab (дурвалумаб)
• atezolizumab (атезолизумаб)
• pembrolizumab (пемброзулимаб)
• avelumab (авелумаб)
Кому нужна иммунотерапия
Типичными кандидатами для иммунотерапии являются пациенты с определенными подтипами немелкоклеточного рака легкого (НМРЛ). Часто иммунотерапия рекомендуется пациентам, чей рак вернулся после проведенного ранее лечения. Иногда иммунопрепараты являются первой и основной терапевтической опцией, обычно в комбинации с химиотерапевтическими средствами.
К сожалению, врачи еще не в состоянии использовать возможности иммунотерапии на полную. Необходимо провести дополнительные исследования, чтобы определить, почему некоторые пациенты очень хорошо реагируют, а другие вообще не реагируют. В этом исследователям помогут знания о клеточных рецепторах рака.
Преимущества, риски и побочные эффекты
Люди, которые хорошо реагируют на иммунотерапию, испытывают меньше побочных эффектов, чем от стандартной химиотерапии цитостатиками. Если ответ на иммунотерапию хороший, она может остановить развитие болезни, предотвратить образование метастазов и существенно продлить жизнь больных даже на поздних стадиях рака легких.
Среди наиболее частых и легких побочных эффектов: суставная боль, утомляемость, снижение аппетита, кашель, диарея и запоры, тошнота, кожная сыпь и зуд.
К сожалению, некоторые пациенты на иммунопрепаратах рискуют чрезмерно активировать свою иммунную систему. В этих редких случаях лимфоциты начинают атаковать здоровую ткань и внутренние органы, развивается аутоиммунный процесс.
Тогда лечение приходится остановить, чтобы не нанести больному организму еще больше вреда. Пациентам остается возлагать надежды на альтернативные методы лечения рака легких — хирургическое удаление опухоли, химиотерапию, облучение.
Исследования и будущее иммунотерапии
Зарубежные ученые с оптимизмом относятся к иммунотерапии и ее будущему в лечении рака легких, но признают достаточное число пробелов в современных знаниях. Количество завершенных клинических испытаний иммунопрепаратов и вакцин невелико, но фармацевтические компании активно работают в этом направлении.
Имеющиеся результаты показывают, что иммунопрепараты могут дать огромные возможности в лечении рака легких и других онкозаболеваний.
Внедрив новые лабораторные анализы, можно было бы предсказывать ответ на иммунотерапию и более точно прогнозировать развитие заболевания.
Константин Моканов: магистр фармации и профессиональный медицинский переводчик
Лечение рака легких в Израиле эффективно благодаря современным методам лечения. К таким методам относится иммунотерапия. В развитых западных странах этот вид лечения рака постепенно заменяет химиотерапию.
Навигация по статье
Как пройти дистанционное лечение рака в Израиле во время эпидемии коронавируса?
- Как работает иммунотерапия
- Иммунные препараты для лечения рака легких
- CAR-T-клеточная терапия
- Иммунотерапия мелкоклеточного рака легких
Иммунотерапия помогает иммунной системе обнаруживать и уничтожать раковые клетки. В израильском онкоцентре Ихилов такая терапия применяется в рамках индивидуальных комплексных программ лечения рака легких вместе с хирургией, радиотерапией и химиотерапией. Иммунотерапия при раке легких 4 стадии позволяет израильским специалистам примерно в 1,5 раза повысить выживаемость пациентов по сравнению со странами постсоветского пространства.

Как работает иммунотерапия
В норме иммунная система запрограммирована на уничтожение любых чужеродных клеток, например бактерий, вызывающие различные заболевания. Однако иммунная система не может распознавать клетки раковых опухолей. Дело в том, что рак развивается постепенно: здоровые клетки со временем приобретают ряд мутаций ДНК, что позволяет им уклоняться от иммунной системы.
Лечение рака легких иммунотерапией позволяет добиться более высоких результатов, чем химиотерапия, и избежать тяжелых побочных эффектов химиопрепаратов.
Иммунные препараты для лечения рака легких
Для терапии рака легких используют целый ряд иммунных препаратов. В их число входят:
- ипилимумаб
- бевацизумаб
- рамуцирумаб
- ниволумаб
- пембролизумаб
- атезолизумаб
- дурвалумаб
- кейтруда
Многие из этих препаратов применяются и для лечения других онкологических заболеваний.
Иммунотерапия при раке легких подбирается индивидуально, в соответствии с видом опухоли. В онкоцентре Ихилов планирование такого лечения проводится на медицинском консилиуме. Чтобы определить, какой из препаратов лучше всего подходит для конкретного пациента, команда врачей — онкологов, патологов и других специалистов – должна обсудить результаты обследования больного.
Лечение в онкоцентре Ихилов не выходя из дома.
Как специалисты клиники лечат пациентов во время коронавируса.
Лікування в онкоцентрі Іхілов не виходячи з дому.
Як фахівці клініки лікують пацієнтів під час коронавируса.
CAR-T-клеточная терапия
Еще одним видом иммунной терапии являются инфузии химерных антигенных рецепторов Т-клеток (CAR-T). Пока что такое лечение доступно только в рамках клинических испытаний. Сначала пациенту проводят специальный анализ, чтобы определить, содержит ли его опухоль определенный белок. После этого у пациента проводят забор крови для получения Т-клеток. Затем полученные Т-клетки генетически изменяются для выработки химерного антигенного рецептора, уникального для конкретной опухоли. Наконец, пациент получает индивидуально изготовленный иммунный препарат, который используется для лечения.
В разработке CAR-T-клеточной терапии принимают активное участие ученые Израиля.
Иммунотерапия мелкоклеточного рака легких
Злокачественные опухоли легких делят на 2 большие группы – мелкоклеточный и немелкоклеточный рак. Мелкоклеточный рак диагностируется в 15% случаев. Он отличается быстрым прогрессированием, ранним образованием метастазов и частыми поражениями головного мозга. Лишь 20-40% пациентов с локализованными стадиями мелкоклеточного рака легких и менее 5% с обширными опухолями живут дольше 2 лет.
В то время как для лечения немелкоклеточного рака легких в последние 20 лет были разработаны новые протоколы, основывающиеся на генетических мутациях опухоли, лечение мелкоклеточного рака не менялось. Лишь в последние 2-3 года в развитых западных странах, включая Израиль, были проведены эффективные клинические испытания новых схем лечения мелкоклеточного рака легких, включающих иммунные препараты. К таким схемам относятся:
- ниволумаб+ипилимумаб;
- карбоплатин/этопозид/атезолизумаб;
- пембролизумаб (Кейтруда).
Инновационное иммунное лечение мелкоклеточного рака легких можно пройти и в онкоцентре Ихилов.

В сентябре 2015 года я почувствовала комок в левой груди. Я не паникер, но я знала, что это может значить. У меня была назначена встреча через месяц с моим акушером-гинекологом, поэтому сначала я подумала, что подожду и поговорю об этом со своим врачом.
У меня была маммография всего шесть месяцев назад. Но после изучения информации в интернете, я поняла, что для безопасности нужно встретиться с врачом раньше.

За пять лет до того, как мне поставили диагноз, я тренировалась четыре раза в неделю и была в отличной форме. Друзья заметили, что я сильно похудела, но я просто думала, что это связано с моим активным образом жизни. В это время у меня постоянно были проблемы с желудком. Мои врачи рекомендовали безрецептурные препараты.
В течение месяца у меня также была постоянная диарея. Мои врачи не нашли ничего плохого.

В начале 2016 года я воспользовалась советом врача и сделала колоноскопию. Я никогда этого не делала до этого. Мой доктор показал мужу, и мне изображение толстой кишки. На изображении были видны два полипа. Врач указал на первое место на моей толстой кишке, заверив нас, что беспокоиться не о чем. Затем он указал на другое место и сказал нам, что, по его мнению, есть подозрение на рак. Во время процедуры он сделал биопсию, и ткань была проанализирована.

В 2011 году у меня начался кислотный рефлюкс. Это было неудобно и тревожно, поэтому я пошел к нашему семейному врачу для обследования. Во время визита он спросил меня, когда я в последний раз проверял свой антиген пса, рутинный тест, который многие мужчины делают, чтобы проверить возможные признаки рака простаты. Прошло около трех лет с тех пор, как я делал этот тест, поэтому он добавил его к моему визиту в тот день.

Моя история начинается с онемения. Однажды в 2012 году три пальца на моей левой руке внезапно потеряли чувствительность. Я сразу же записался на прием к врачу. К тому времени, когда врач меня смог принять, уже все прошло, но жена убедила меня все-таки пойти на консультацию. У меня был рентген, чтобы увидеть, есть ли какие-либо признаки повреждения позвоночника, возможно, от вождения грузовика. Когда на пленке появились какие-то.

Зимой 2010 года, когда мне было 30 лет, я почувствовала внезапную боль в правом боку. Боль была резкой и началась без предупреждения. Я сразу же отправилась в ближайшую больницу.
Врач получил результаты моего анализа крови, и он увидел, что мой уровень лейкоцитов был чрезвычайно повышен. Врач и другие, кто видел эти результаты, были встревожены и попросили гинеколога по вызову приехать ко мне сразу же.

Около трех лет я боролся с прерывистым кашлем. Он появлялся зимой и исчезал к весне, а потом я забывал о нем. Но осенью 2014 года это произошло раньше. В октябре моя жена позвонила местному пульмонологу. Первая встреча нам назначили через три месяца.
. В онкоцентре Ихилов мы встретились с торакальным хирургом. Решили полностью удалить узелок.
Читайте также:

