Гранулоциты убивают раковую клетку
Д-р Чжэн Цуй из Медицинской школы при Университете Wake Forest показал в ходе лабораторных экспериментов, что иммуноциты у одних людей могут быть почти в 50 раз эффективнее в борьбе с раком, чем у других. (Иммуноциты – клетки организма, осуществляющие иммунный ответ. К иммуноцитам относятся иммунокомпетентные (Т- и В-лимфоциты) и фагоцитирующие клетки (мононуклеарные фагоциты, полиморфно-ядерные гранулоциты и мелкие клетки центральной нервной системы – микроглия).
Д-р Цуй, чья работа была опубликована на этой неделе в журнале New Scientist, ранее доказал, что клетки иммунной системы – гранулоциты – мышей, которые неуязвимы для рака, могут быть использованы при лечении новообразований у других мышей. Эта работа делает возможным использование гранулоцитов, полученных от доноров с устойчивой к раку иммунной системой, для многократного усиления иммунитета пациента и потенциального излечения.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов Соединенных Штатов (FDA) выдало д-ру Цую на прошлой неделе разрешение на инъекцию сверхмощных гранулоцитов 22 пациентам.
Д-р Цуй уверен, что пациенты могут уже в скором времени воспользоваться плодами нового метода, поскольку технология получения гранулоцитов идентична той, которая уже применяется в клиниках для получения других компонентов, входящих в состав крови, таких как плазма или тромбоциты.
Д-р Цуй, который на прошлой неделе представил свои последние разработки на конференции по геронтологии в Кембридже, получил гранулоциты из организма 100 человек, включая больных раком. Когда иммунноциты были смешаны с клетками, пораженными раком шейки матки, полученными от разных людей, их способность убивать раковые образования резко возросла.
Д-р Цуй отметил, что способность иммунной системы к подавлению раковых клеток может зависеть также от уровня стресса и времени года.
Предварительные эксперименты указывают также на возможность пересадки гранулоцитов с большим антираковым потенциалом в организм тех, кто уже болен раком.
В 1999 году профессор Цуй и его коллеги обнаружили самца мыши, который оказался абсолютно устойчивым к смертельно опасным раковым клеткам различных видов.
Далее было установлено, что 2000 мышей в 15 поколениях, которые произошли от этой устойчивой к раку мыши, и 40% потомства унаследовали этот иммунитет.
Ученые, работающие над вакциной от рака, пытаются стимулировать реакцию клеток иммунной системы, что требует некоторого предварительного воздействия на эти клетки.
В прошлом году д-р Цуй произвел сенсацию в сообществе ученых-онкологов, когда обнаружил, что гранулоциты являются клетками, ответственными за противораковый иммунитет мышей – поскольку они относятся к клеткам, которые действуют автоматически.
Еще более впечатляющим результатом явилось то, что благодаря этой процедуре заболевание перешло в стадию ремиссии, а затем животное было полностью излечено в течение нескольких недель. Похоже на то, что однократное введение таких клеток делает организм большинства мышей устойчивым к раку на всю последующую жизнь.
Гранулоциты ранее использовались для борьбы с инфекционными заболеваниями больных раком, поскольку их иммунная система была ослаблена вследствие химиотерапии. Однако их эффективность оставалась невыясненной, так как процедуре подвергались пациенты на поздней стадии болезни.
Ник Флеминг (Nic Fleming), Telegraph, 21.09.2007
Рак остается одним из самых сложных для лечения заболеваний, от которого не существует одного эффективного лекарства. При этом в многочисленных исследованиях, посвященных поиску эффективных средств от недуга, не раз упоминаются определенные продукты питания, которые разными исследователями считаются эффективными для уничтожения раковых стволовых клеток.

Это очень важно, потому что именно тот факт, что химиотерапия не уничтожает раковые стволовые клетки, считается причиной того, что у онкологических пациентов случаются рецидивы и появляются метастазы. Эти клетки, иногда называемые "материнскими клетками", составляют лишь небольшую часть всех клеток опухоли, но они имеют способность самовосстанавливаться и сопротивляются химиотерапии. Они также могут отделяться и создавать новые колонии опухолей, поэтому их уничтожение является ключом к эффективному лечению рака в долгосрочной перспективе.
Лекарств, нацеленных конкретно на эти клетки, нет, но исследователи обнаружили множество природных веществ, способных бороться с этими клетками. Naturalnews. com перечислил продукты, которые являются лучшими "убийцами" раковых клеток.
Зеленый чай
Зеленый чай уже давно используется в китайской медицине для лечения множества недугов, но только недавно исследователи раскрыли его невероятный потенциал для лечения рака. Исследователи из медицинского центра Бэйлорского университета обнаружили, что активный ингредиент зеленого чая, EGCG (epigallocatechin-3-gallate), убивает раковые стволовые клетки и, следовательно, может помочь в случаях, когда образование не поддается химиотерапии. Хотя EGCG присутствует также в черном чае, в зеленом чае его концентрация выше.
Имбирь
Доклиническое исследование показывает, что один из компонентов имбиря дает в 10 000 раз большую эффективность в борьбе со стволовыми клетками при раке молочной железы, чем популярный препарат Таксол. Компонент, который известен как 6-Shogaol, выделяется, когда корень имбиря сварен или высушен, и его концентрация, необходимая для умерщвления раковых клеток, для клеток здоровых не опасна, в отличие от традиционных препаратов, применяемых в таких случаях.
Куркума
Куркумин, компонент древней индийской специи куркума, может выборочно влиять на стволовые раковые клетки без риска воздействия на здоровые стволовые клетки, необходимые для регенерации ткани. Это вещество эффективно при раке молочной железы, раке поджелудочной железы, колоректальном раке и раке головного мозга.
Ягоды винограда
Вещество resveratrol, которое находится в коже и семенах ягод винограда, наносит "смертельный" удар по стволовым клеткам рака толстой кишки. Таковы выводы ученых из Пенсильванского университета. Они верят, что в будущем это открытие поможет научиться предотвращать рак толстой кишки, который является одним из самых распространенных ныне типов рака. Когда во время эксперимента resveratrol и выдержка из семени винограда принимались одновременно, их воздействие было чрезвычайно мощно, и при этом они не повредили здоровым клеткам.
Другие продукты, которые убивают раковые стволовые клетки
Хотя вышеозначенные продукты — одни из самых мощных противораковых природных лекарств, есть и много других со сходным эффектом. Среди них — черника, морковь, кофе, грейпфрут, мята, вишня, лук, черный перец и тимьян.
Обилие продуктов, которые могут иметь большое влияние на рак, напоминает нам, насколько эффективно и безопасно природа может помочь справиться с серьезными недугами нашего времени. Многие врачи не очень хорошо разбираются в теме, у иных же есть финансовые мотивы, чтобы продолжать настаивать на дорогих и часто опасных лекарствах. По этой причине есть большой смысл расширять свой кругозор и узнавать, что, помимо лекарственной помощи, доступно нам в борьбе с серьезными заболеваниями.

- Образование и жизненный цикл
- Виды
- Функции
- Норма
- Причины отклонения от нормы
- Проведение анализа
Гранулоциты (зернистые лейкоциты) – группа белых кровяных клеток, которые в своей цитоплазме содержат гранулы. Пониженное или повышенное количество данного компонента в крови является признаком развития определенного патологического процесса, но установить это можно только путем проведения диагностических мероприятий.
Лейкоциты, то есть белые клетки, в крови разделяются на два типа – гранулоциты и агранулоциты. К первой группе относятся компоненты, которые включают в себя цитоплазму с гранулами. Сегментоядерные гранулоциты очень важны для организма, так как относятся к первой линии защиты от микробов: при образовании очага воспаления именно гранулоциты начинают реакцию иммунного ответа организма.
Причины того, что гранулоциты повышены или понижены, могут быть не только в патологических процессах, но и в факторах внешней среды. Так, спровоцировать отклонение от нормы может прием препаратов или частые стрессы. Контролировать данные показатели в крови у детей или у взрослых очень важно, так нарушение баланса может привести к довольно серьезным осложнениям.
Образование и жизненный цикл
Гранулоциты образуются в костном мозге: клетки делятся в течение четырех дней, после чего происходит их морфологическое дозревание. Данный этап длится не более пяти дней. После того как клетки выходят в кровяное русло, происходит их деление на два вида: пристеночные, которые временно крепятся к стенкам сосудов, и активно циркулирующие. По кровеносной системе они циркулируют около недели, затем выходят в ткань. Здесь клетки живут около двух суток, после чего происходит завершение их жизненного цикла.
Количество гранулоцитов в крови составляет около 60% от общего количества белых клеток. Данные компоненты, в свою очередь, делятся на подвиды.
Таким образом, к гранулоцитам относятся следующие клетки:
Если те или иные гранулоциты понижены или повышены, это может негативно сказаться на работе организма, например, при попадании патогенных организмов иммунная реакция может быть слишком слабой, что приведет к серьезным осложнениям.

Функции
Основные функции гранулоцитов заключаются в формировании иммунной реакции при попадании в организм вируса, паразита, аллергена или любого другого патогенного тела.
Кроме этого, некоторые подвиды белых телец отвечают за ускорение кровообращения при ранении, что помогает предотвратить большую кровопотерю. В целом данный компонент отвечает за полноценное функционирование внутренних органов.
Норма
Норма гранулоцитов будет зависеть от возраста и половой принадлежности человека.
Оптимальными показателями являются следующие:
- у ребенка до месяца гранулоциты норма – 5,5-12,5 10 9 клеток/л
- у ребенка до 12 лет – 4,5-10,0 10 9 клеток/л;
- у ребенка в пубертатный период – 4,3-9,5 10 9 клеток/л;
- в крови у женщин и у мужчин – 1,2-6,8 10 9 клеток/л.
Следует отметить, что повышение гранулоцитов при беременности – это нормальный физиологический процесс и патологией не является. Однако, если показатели существенно выше предельной границы, то обязательно следует пройти полное обследование, на основании которого врач поставит диагноз и назначит корректное лечение.
Возможные причины отклонения от нормы
Причины повышения количества белых телец в крови могут быть следующие:
- паразитарные инфекции;
- острые воспалительные процессы;
- инфекционные заболевания;
- патологические процессы, которые сопровождаются некротизацией тканей;
- аллергические реакции;
- интоксикация организма;
- острые геморрагии;
- болезни кроветворной системы;
- онкологические заболевания;
- воспалительные процессы в желудочно-кишечном тракте;
- синдром Ходжкина;
- нарушения эндокринного характера;
- заболевания сердечно-сосудистой системы;
- гемолитическая анемия;
- инфекционные процессы непаразитарной природы.
Привести к тому, что гранулоциты в крови будут выше нормы, может и прием некоторых медикаментозных препаратов. Как правило, после отмены медикаментов показатели приходят в норму.
Причины того, что гранулоциты в крови ниже нормы, следующие:
- аллергические реакции;
- гастроэнтерологические заболевания;
- системные или аутоиммунные заболевания;
- различные виды анемии;
- скарлатина;
- ревматизм;
- саркоидоз.
Следует учитывать и то, что при расшифровке анализа принимаются во внимание и другие показатели крови, поэтому самостоятельно трактовать данные не рекомендуется: правильно это может сделать только врач.
Проведение анализа
Для того чтобы определить количество белых телец в крови, проводится общий клинический анализ биологической жидкости путем пункции из пальца. Следует отметить, что на результаты могут повлиять и внешние факторы: неправильное проведение процедуры забора жидкости, нарушение техники проведения анализа, неподготовленный пациент. Поэтому, если результаты будут показывать существенное отклонение от нормы, врач может назначить повторное проведение лабораторного исследования.
Контролировать показатели гранулоцитов в крови очень важно, так как от них зависит состояние иммунной системы. Поскольку симптоматически заметить отклонение от нормы не всегда представляется возможным, в целях профилактики необходимо периодически проходить медицинский осмотр со сдачей лабораторных анализов. Любое заболевание гораздо легче предотвратить, чем устранять его последствия.
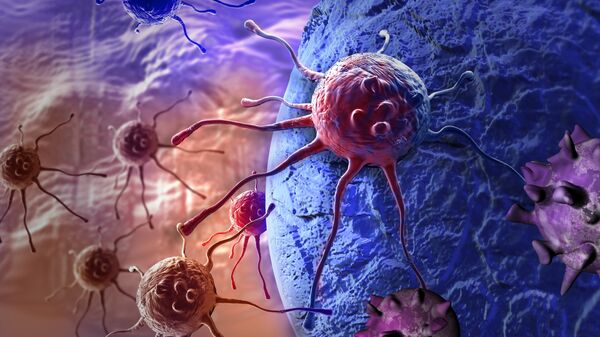
МОСКВА, 30 ноя — РИА Новости. Биологи из МГУ и их шведские коллеги выяснили, что раковые клетки можно заставить самоуничтожаться при делении, если ввести в них вещества, связанные с так называемой митотической катастрофой. Об этом говорится в статье, опубликованной в журнале Scientific Reports.
Значительная часть раковых опухолей возникает из-за поломки в гене p53. Он отвечает за синтез белка, который обеспечивает целостность генетической информации, а при серьезных повреждениях ДНК включает механизм самоуничтожения — апоптоз. Поэтому культуры клеток с поврежденным геном p53 крайне сложно уничтожить — в их геноме просто нет программы самоуничтожения.
Существуют и другие механизмы самоуничтожения клеток, например энтоз и митотическая катастрофа. Под последней биологи понимают сложный процесс, который приводит к резкому увеличению размеров клетки, появлению в ней лишних ядер и гибели в тот момент, когда она начинает делиться и при этом имеет серьезные повреждения в ДНК.
Ученые считают митотическую катастрофу одним из защитных механизмов организма, который убивает клетки до того, как они превращаются в раковые новообразования и становятся угрозой для жизни.
Животовский и его коллеги решили выяснить, какую роль играют в этом процессе митохондрии — своеобразные "энергостанции" клетки. Они не только вырабатывают молекулы "энерговалюты" АТФ, но и участвуют в запуске апоптоза. Это натолкнуло биологов на мысль, что митохондрии могут быть задействованы и в митотической катастрофе.
Для проверки этой идеи ученые вырастили культуру раковых клеток прямой кишки и попытались вызвать митотическую катастрофу при помощи двух противораковых лекарств — антибиотика доксирубицина, который продуцируют микробы-стрептомицеты, и алкалоида колцемида, получаемого из цветов-осенников. Оба препарата нарушают работу двух ключевых этапов цикла деления клетки.
Как показали опыты, комбинация этих веществ заставляет примерно 80% раковых клеток самоуничтожиться во время деления. Это позволило биологам детально изучить роль митохондрий в данном процессе, а также то, какие изменения в работе клеток запускают его.
Во-первых, ученые обнаружили, что наступление митотической катастрофы само по себе не приводит к смерти клетки — она самоуничтожается потому, что в ней активируются цепочки генов, связанные с двумя другими типами клеточной смерти, — апоптозом и аутофагией.

Во-вторых, оказалось, что для запуска митотической катастрофы необходимо лишь прекратить доступ кислорода к митохондриям и заставить их выделять два "белка смерти" — Mcl-1 и Bcl-xL. Сейчас Животовский и его команда проверяют несколько соединений, способных вызывать подобную реакцию в раковых клетках и не затрагивать их здоровых соседей.
Если эти эксперименты закончатся удачно, то ученым, вероятно, удастся создать новый класс противораковых препаратов с куда более щадящим эффектом, чем радиация или химиотерапия.
В мартовском Трансфюжне опубликовано исследование, посвященное возможным отдаленным последствиям гранулоцитафереза со стимуляцией гранулоцитарным колониестимулирующим фактором (G-KSF, нейопоген) и дексаметазоном для доноров. Это уникальное в своем роде исследование, потому что прежде отдаленные последствоя гранулоцитафереза не изучались. Известен быстрый эффект стимуляции G-KSF (ломота в костях, головная боль, миалгия). Было исследование здоровья доноров через два и четыре года после донации (никакого эффекта донация не оказала). Но вот данные исследования отдаленных последствий публикуются впервые.
Мало кто из доноров читает Трансфьюжн, но всем интересно, чем же чревато донорство гранулоцитов. Поэтому творчески переосмысливаю содержание статьи здесь. Надеюсь, авторы статьи на меня не очень обидятся.
Quillen K., Ph. Byrne, Y.Yau, S.F.Leitman. Ten-year follow-up of unrelated volunteer granylocyte donors who have received multiple cycles of granulocyte-colony-stimulating factor and dexametasone. Transfusion, vol. 49, pp513-518
В исследовании участвовали доноры, сдававшие гранулоциты в период с 1994 по 2002 год. Средний срок, прошедший после последнего гранулоцитафереза составил 10 лет. Всего в Клиническом центре Уоррена Магнусона (Мэрилэнд, США) в этот период было 92 донора, которые сдавали гранулоциты 3 раза и более. Связаться удалось только с 83. Про остальных известно только, что они живы…
В качестве контрольной группы использовали доноров тромбоцитов, подобранных по возрасту и полу так, чтобы выборка по этим параметрам совпала с выборкой доноров гранулоцитов. Среднее количество тромбоцитаферезов на донора – 87,5 раз (!).
Исследовали результаты общего анализа крови, с-реактивный белок, наличие сердечно-сосудистых и онкологических заболеваний, тромбозы.
Из интересного, про доноров гранулоцитов. Схема мобилизации (стимуляции выхода гранулоцитов в периферическое русло) у них такая же, как и у нас в больнице. Сдавать гранулоциты в Омереке можно раз в месяц. Если донор совпадает с реципиентом по показателям тканевой совместимости, то чаще. В среднем, доноры в исследованной выборке сдавали гранулоциты 2-3 раза в год. Среднее число гранулоцитаферезов на донора – 13,5 (!). В исследовании участвовали 54 мужчины и 29 женщин, возраст доноров колебался от 30 до 77 лет.
Разницы по показателям анализа крови и уровню с-реактивного белка между донорами тромбоцитов и гранулоцитов не обнаружено. В обоих группах (тромбоцитной и гранулоцитной) было обнаружено по 2 случая сердечно сосудистых заболеваний. В гранулоцитной группе зарегистрирован один случай тромбоза глубоких вен, в тромбоцитной – ни одного. В обоих группах не случилось ни одного инсульта. Теперь по онкологическим заболеваниям. В группе гранулоцитных доноров нашли 2 лимфомы и две солидные опухоли (рак легких и меланома). В группе тромбоцитных – три солидные опухоли (рак кишечника, простаты и груди). Таким образом, не выявлено тенденции к возникновению случаев какого-то специфического вида рака.
Авторы делают вывод, что статистически значимых различий по исследованным показателям между исследованными выборками нет. Авторы полагают, что полученные данные позволяют считать стимуляцию донора дексаметазоном и G-CSF безопасной. Авторы сетуют на ограниченный объям выборок и считают, что подобные исследования следует продолжать.
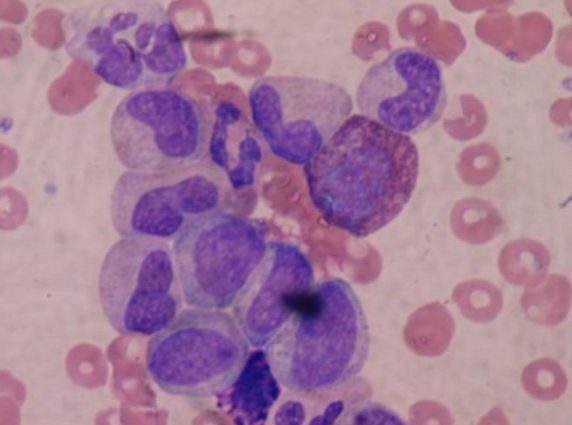
Гранулоцитопения – это снижение, ниже принятой нормы, числа гранулоцитов при общем уменьшении количества лейкоцитов в крови. Иногда бывает так, что общее количество лейкоцитов в крови остается в норме, а количество гранулоцитов снижается.
Недостаток белых кровяных клеток, чаще всего связан с бактериальной инфекции, но может появиться также и в ходе лейкемии. Лечение заключается в приеме средств, повышающих выработку гранулоцитов в костном мозге.
Характеристика гранулоцитов
Гранулоциты – это тип белых кровяных клеток, которые заполнены микрогранулами, содержащими ферменты, которые уничтожают микроорганизмы.
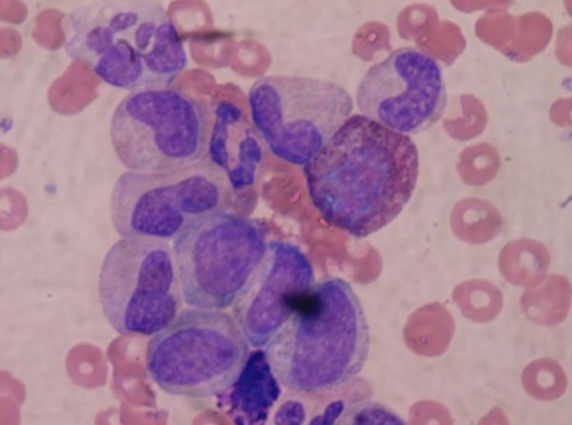
Они являются частью врожденной, неспецифической иммунной системы потому , что реагируют на все антигены, попадающие в организм.
Белые кровяные клетки защищают организм от вторжения патогенных микроорганизмов и тем самым выполняют функцию защиты организма от инфекции.
Гранулоциты можно разделить на:
Исходя из этих типов гранулоцитопении подразделяют на:
- нейтропения (дефицит нейтрофилов);
- эозинопения (дефицит эозинофилов);
- базопения (дефицит базофилов).
Причины гранулоцитопении
Гранулоцитопения является результатом частых хронических бактериальных инфекций кожи, легких, горла и т.д. Болезнь может быть также унаследована генетически или вызвана появлением лейкемии у больного.
- синдром Рихтера (редким врожденным заболеванием, которое характеризуется отсутствием пигментации кожи и глаз, нарушениями иммунной системы, болезнями крови и другими аномалиями);
- отравление Подофиллом щитовидным (маленькое цветущее растение, имеющее одиночные цветки и плоды напоминающие яблоки, которые желтеют при созревании);
- патологии ретикулоцитов (аномальная пролиферация ретикулярных клеток (гистиоцитов), которые проникают в органы. В результате макрофаги уничтожают клетки крови)
Гранулоцитопения возникает из-за сокращения производства гранулоцитов в костном мозге, повышенного их уничтожения или активного использования. Тормозящее действие на производство гранулоцитов в костном мозге оказывают наркотики и лучевая терапия.
Гранулоцитопения – это побочный эффект применения многих лекарственных средств. Негативное влияние имеют антиметаболиты, некоторые антибиотики и антиаритмические препараты.
Лечение гранулоцитопении
Гранулоцитопению не нужно лечить, но человек должен сознательно предотвращать её появление.
Это осуществляется, в основном, через:
- избегание контакта с источниками инфекций;
- избегание контакта с веществами, такими как бензол, ксилол, толуол и другими органическими растворителями;
- избегание ионизирующего излучения;
- отказ от употребления продуктов, которые обрабатывали пестицидами, а также от маринованных, копченых и с плесенью;
- ограничение принимаемых лекарств;
- ликвидацию в зародыше любых инфекций.
Снижение уровня гранулоцитов обнаруживают при выполнении исследований в лаборатории (общий анализ крови). Затем врач принимает решение о возможном лечении, состоящем из курса антибиотиков или некоторых противогрибковых лекарств. Применяют препараты, стимулирующие производство нейтрофилов в костном мозге.
Лейкоциты, или белые клетки крови, являются компонентами, которые защищают организм от инфекционных агентов. Они играют важную роль, защищая иммунную систему путем выявления, уничтожения и удаления патогенов, поврежденных клеток (например, раковых) и других посторонних веществ из организма. Лейкоциты образуются из стволовых клеток костного мозга и циркулируют в крови и лимфатической жидкости. Как они образуются и как протекает их жизненный цикл? Какова продолжительность жизни лейкоцитов?
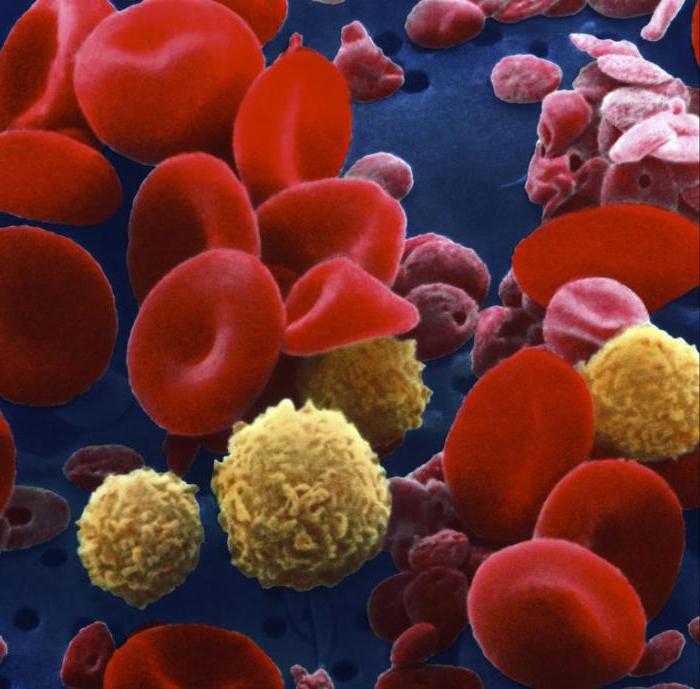
Белые клетки крови
Лимфоциты являются наиболее распространенным типом белых кровяных клеток, которые имеют сферическую форму с крупными ядрами и небольшим количеством цитоплазмы. Существуют три основных типа: Т-клетки, В-клетки и естественные клетки-киллеры. Первые два типа являются критическими для специфических иммунных реакций. Природные клетки-киллеры обеспечивают неспецифический иммунитет.
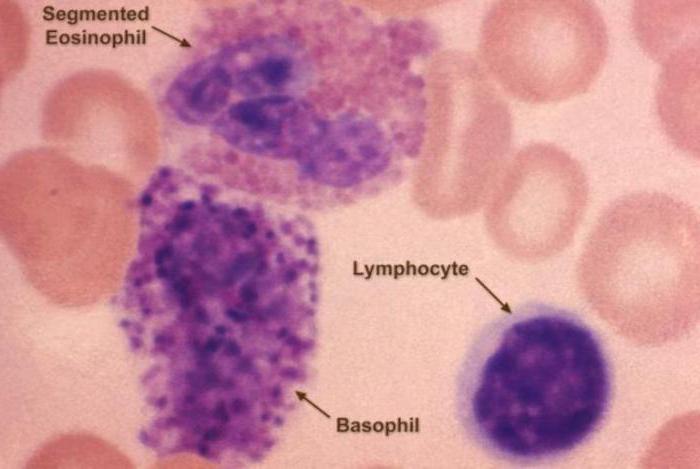
Образование лейкоцитов
В основном белые клетки крови образуются в костном мозге, некоторые из них созревают в лимфатических узлах, селезенке и вилочковой железе. Продолжительность жизни лейкоцитов колеблется примерно от нескольких часов до нескольких дней. Производство клеток крови часто регулируются такими структурами организма, как лимфатические узлы, селезенка, печень и почки. Низкий уровень лейкоцитов может быть связанным с заболеванием, воздействием радиации или повреждениями костного мозга. Высокий может указывать на наличие инфекционного или воспалительного заболевания, анемии, лейкемии, стресса или обширного повреждения тканей организма.
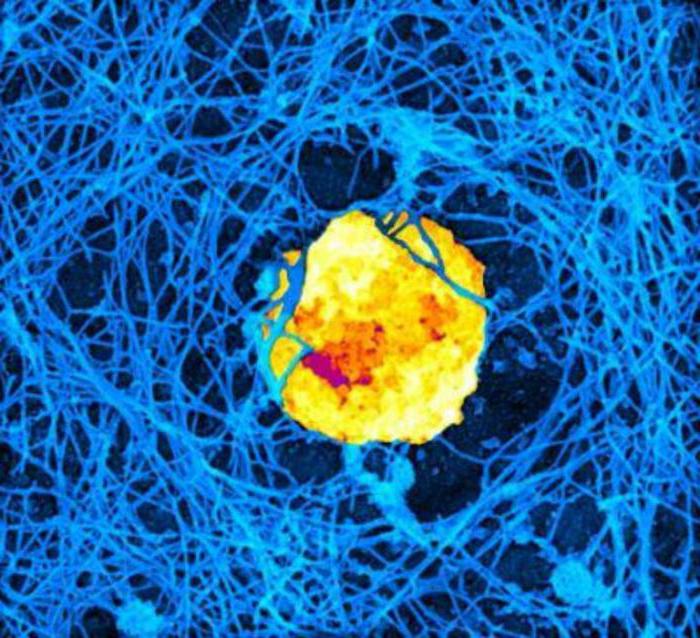
Какие еще существуют типы клеток крови?
Помимо белых кровяных телец, существуют красные, которые называются тромбоцитами. Эти клетки имеют двояковогнутую форму и заняты транспортировкой кислорода к клеткам и тканям тела посредством кровообращения. Они также транспортируют углекислый газ в легкие. Тромбоциты имеют жизненно важное значение для процесса свертывания крови и являются необходимыми для предотвращения ее потери.
Продолжительность жизни белых клеток крови
Какова продолжительность жизни лейкоцитов в крови? Можно сказать, что белые кровяные клетки живут быстро и умирают молодыми. Они имеют относительно короткий жизненный цикл - от нескольких дней до нескольких недель. Но это вовсе не означает их хрупкость и ненадежность. Вся сила заключается в цифрах: одна капля крови может содержать от 7 до 25 тысяч белых кровяных телец одновременно. Это число может увеличиться, если присутствует заражающая инфекция.
Жизнь гранулоцитов после выхода из костного мозга, как правило, составляет от 4 до 8 часов, если они циркулируют в крови, и от 4 до 5 дней - если движутся по тканям. Во время тяжелой инфекции общая продолжительность жизни лейкоцитов часто сокращается до всего лишь нескольких часов. Лимфоциты входят в кровеносную систему постоянно, наряду с дренажем лимфы из лимфатических узлов и другой лимфоидной ткани. Через несколько часов они поступают из крови обратно в ткань, затем возвращаются в лимфу и, таким образом, циркулируют. Продолжительность жизни лейкоцитов может варьироваться от нескольких недель до нескольких месяцев, все зависит от потребности организма в этих клетках.
Защита от инфекций
Кровь состоит из нескольких компонентов, в том числе красных кровяных клеток, лейкоцитов, тромбоцитов и плазмы. Здоровый взрослый человек имеет от 4500 до 11 000 белых кровяных клеток на кубический миллиметр крови. Лейкоциты, также называемые лейкоцитарными или белыми корпускулами, являются клеточным компонентом крови, который защищает организм от инфекций и болезней путем проглатывания инородных материалов и разрушения инфекционных агентов, в том числе раковых клеток, а также путем получения антител.
Аномальное увеличение числа белых клеток известно как лейкоцитоз, в то время как ненормальное уменьшение их числа носит название лейкопении. Количество лейкоцитов может расти в ответ на интенсивные физические нагрузки, судороги, острые эмоциональные реакции, боли, беременность, роды и некоторые другие болезненные состояния, такие как инфекции и интоксикации. Их количество может снижаться в ответ на определенные типы инфекций или препаратов либо в сочетании с определенными условиями, такими как хроническая анемия, недоедание или анафилаксия.

Сложный химический состав
Химические пути, используемые лейкоцитами, являются более сложными, чем у тех же эритроцитов. Белые клетки содержат ядро и способны производить рибонуклеиновую кислоту, а также синтезировать белок. В то же время они не претерпевают деление клеток (митоз) в крови, хотя некоторые из них сохраняют эту способность. Белые клетки сгруппированы в три основных класса: лимфоциты, гранулоциты и моноциты, каждый из которых имеет свои особенности и выполняет несколько иные функции.
Важный компонент системы крови
Лейкоциты являются важным компонентом системы крови, которая также состоит из красных кровяных клеток, тромбоцитов и плазмы. Хотя они составляют всего около 1 % от всей крови, их воздействие значительно: они необходимы для хорошего здоровья и защиты от болезней. Можно сказать, что это клетки иммунитета. В каком-то смысле они постоянно находятся в состоянии войны с вирусами, бактериями и другими "иностранными захватчиками", которые угрожают вашему здоровью.
Когда конкретная область подвергается атакам, белые кровяные клетки стремятся уничтожить вредное вещество и предотвратить болезнь. Лейкоциты производятся внутри костного мозга и хранятся в крови и лимфатических тканях. Поскольку продолжительность жизни лейкоцитов человека невелика, некоторые их типы имеют и вовсе короткий срок существования - от одного до трех дней. Поэтому костный мозг занимается их постоянным воспроизводством.
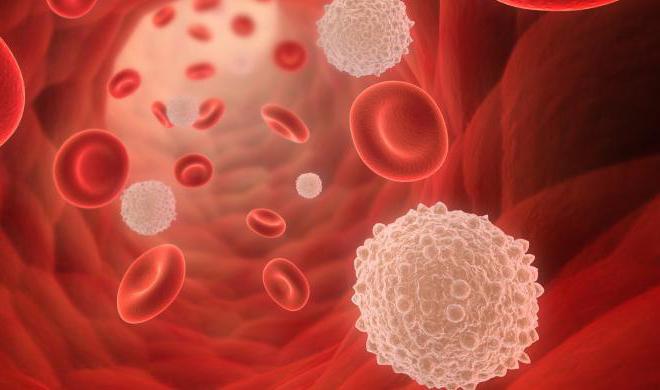
Типы лейкоцитов
Моноциты. Они имеют более длительный срок службы, чем многие белые кровяные клетки, и помогают разрушать бактерии.
Лимфоциты. Они продуцируют антитела для защиты от бактерий, вирусов и других потенциально вредоносных захватчиков.
Нейтрофилы. Они убивают и переваривают бактерии и грибки. Являются наиболее многочисленным типом белых кровяных клеток и первой линией защиты при поражении инфекциями.
Базофилы. Эти маленькие клетки выделяют такие химикаты, как гистамин и маркер аллергической болезни, которые помогают контролировать иммунный ответ организма.
Эозинофилы. Они атакуют и убивают паразитов, уничтожают раковые клетки и помогают при аллергических реакциях.
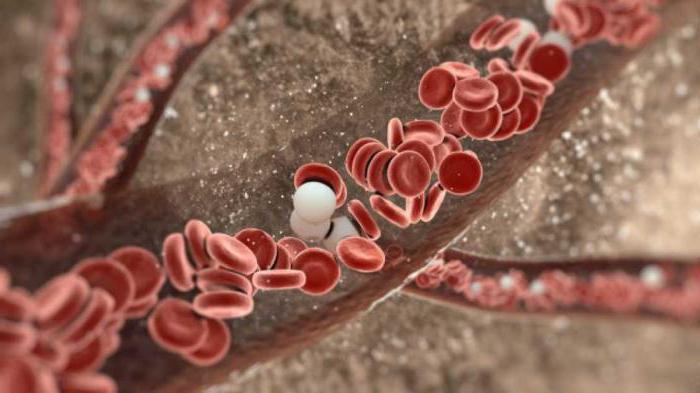
Чем больше - тем лучше?
Даже при всей их способности бороться с болезнями, слишком большое количество белых кровяных клеток может быть плохим признаком. Например, человек, страдающий лейкемией, раком крови, может иметь до 50 000 лейкоцитов в одной капле крови. Все её элементы (эритроциты, лейкоциты и тромбоциты) происходят из гемопоэтических стволовых клеток и костного мозга, а также пуповины новорожденных детей. В среднем в теле взрослого человека содержится около 5 литров крови, которая в основном состоит из плазмы (55-60 %) и клеток крови (40-45 %). Продолжительность жизни эритроцитов, лейкоцитов и тромбоцитов, а также их структура и состав различаются, но все они играют важную роль в функционировании организма.
Число эритроцитов и лейкоцитов в крови может служить индикатором некоторых заболеваний. Лейкопения может быть вызвана факторами, которые могут нарушать функции костного мозга. Состояние, для которого характерно низкое количество эритроцитов, обычно называют анемией, она бывает в том числе железодефицитной и вызванной дефицитом витамина B12. Это заболевание может нарушить способность крови к переносу кислорода, что может проявляться в повышенной усталости, одышке и бледности. Продолжительность жизни лейкоцитов, тромбоцитов и эритроцитов, их внешний вид, состав и функции кардинально различаются, но все они играют важную роль. Таким образом, сокращение или значительное увеличение их числа может привести к различным проблемам со здоровьем.
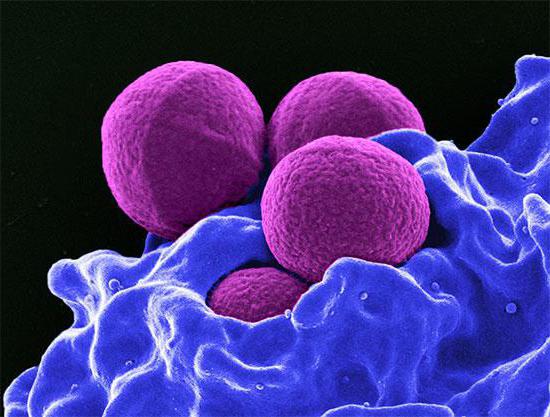
Жизненный период эритроцитов и лейкоцитов
Продолжительность жизни эритроцитов, лейкоцитов, тромбоцитов, как мы уже неоднократно упоминали, разная. Первые являются самыми устойчивыми. Эритроциты живут около 120 дней, в то время как продолжительность жизни лейкоцитов в крови человека может составлять в среднем от 3 до 4 дней. И это количество может в значительной степени снижаться в случае тяжелой инфекции.
Количество лейкоцитов должно быть под контролем
Врачи рекомендуют периодически проверять уровень ваших белых кровяных клеток. Если их количество продолжительное время остается высоким или низким, это может свидетельствовать об ухудшении состояния здоровья. Что касается эритроцитов, то их продолжительность жизни - три-четыре месяца. Лейкоциты в этом плане значительно уступают. И все же это важная часть защиты организма от инфекционных и чужеродных веществ. Проверить количество и состояние крови можно при помощи проведения специальных лабораторных тестов.
Расстройства лейкоцитов
Основные расстройства лейкоцитов включают в себя следующие патологические состояния:
Нейтропения (аномально низкое количество нейтрофилов).
Лейкоцитоз нейтрофилов (аномально высокое количество нейтрофилов).
Лимфоцитопения (аномально низкое количество лимфоцитов).
Лимфоцитарный лейкоцитоз (аномально высокое количество лимфоцитов).
Наиболее распространенными являются расстройства нейтрофилов и лимфоцитов. Менее распространены отклонения, связанные с моноцитами и эозинофилами, реже встречаются проблемы, связанные с базофилами.
Разрушение лейкоцитов
Продолжительность жизни лейкоцитов, тромбоцитов и эритроцитов изучены достаточным образом, чего не скажешь о процессах их разрушения. Известно, что все виды белых клеток после некоторого периода циркуляции в крови попадают в ткани. Обратной дороги уже нет. В тканях они выполняют свою фагоцитарную функцию и гибнут. Важный вклад в изучение белых клеток крови и их свойств внесли Илья Мечников и Пауль Эрлих. Первый обнаружил и исследовал явление фагоцитоза, а второй вывел различные типы лейкоцитов. В 1908 году за эти достижения ученые вместе были удостоены Нобелевской премии.
Читайте также:

